Method Article
Propiedades Electroactivos Polymer Nanopartículas Exponer fototérmica
En este artículo
Resumen
A protocol is presented for the synthesis and preparation of nanoparticles consisting of electroactive polymers.
Resumen
A method for the synthesis of electroactive polymers is demonstrated, starting with the synthesis of extended conjugation monomers using a three-step process that finishes with Negishi coupling. Negishi coupling is a cross-coupling process in which a chemical precursor is first lithiated, followed by transmetallation with ZnCl2. The resultant organozinc compound can be coupled to a dibrominated aromatic precursor to give the conjugated monomer. Polymer films can be prepared via electropolymerization of the monomer and characterized using cyclic voltammetry and ultraviolet-visible-near infrared (UV-Vis-NIR) spectroscopy. Nanoparticles (NPs) are prepared via emulsion polymerization of the monomer using a two-surfactant system to yield an aqueous dispersion of the polymer NPs. The NPs are characterized using dynamic light scattering, electron microscopy, and UV-Vis-NIR-spectroscopy. Cytocompatibility of NPs is investigated using the cell viability assay. Finally, the NP suspensions are irradiated with a NIR laser to determine their effectiveness as potential materials for photothermal therapy (PTT).
Introducción
Polímeros electroactivos cambian sus propiedades (color, conductividad, reactividad, volumen, etc.) en presencia de un campo eléctrico. Los tiempos de conmutación rápidos, tunability, la durabilidad, y las características de peso ligero de polímeros electroactivos han dado lugar a muchas aplicaciones propuestas, incluida la energía alternativa, sensores, Electrochromics, y dispositivos biomédicos. Polímeros electroactivos son potencialmente útiles como, baterías y condensadores electrodos ligeros flexibles. 1 Aplicaciones de polímeros electroactivos en dispositivos electrocrómicos incluyen sistemas de reducción de deslumbramiento para edificios y automóviles, gafas de sol, gafas de protección, dispositivos de almacenamiento ópticos y textiles inteligentes. 2.5 ventanas inteligentes pueden reducir los requerimientos de energía mediante el bloqueo de determinadas longitudes de onda de la luz a la carta y la protección de los interiores de las casas y automóviles. Textiles inteligentes pueden ser utilizados en la ropa para ayudar a proteger contra la radiación UV. 6 polímeros electroactivos tienen als,o comenzado a ser utilizado en dispositivos médicos. Entre los polímeros electroactivos utilizados en dispositivos biomédicos, polipirrol (PPy), polianilina (PANI), y poli (3,4-etilenodioxitiofeno) (PEDOT) se encuentran entre los más comunes. Por ejemplo, estos tipos de polímeros se utilizan comúnmente como transductores en dispositivos biosensores 7 Aplicaciones en la entrega terapéutico también se han mostrado prometedores.; estudios han demostrado la liberación de los fármacos y proteínas terapéuticas de los dispositivos preparados a partir de polímeros electroactivos 8-12. Más recientemente, polímeros electroactivos se han utilizado como agentes terapéuticos en la terapia fototérmica 13-15. En la terapia fototérmica, agentes fototérmicos deben absorber la luz en el Cercano infrarrojo de (NIR) región (~ de 700-900 nm), también conocida como la ventana terapéutica, donde la luz tiene la profundidad máxima de penetración en el tejido, típicamente de hasta 1 cm. 16,17 En este rango, cromóforos biológicos tales como la hemoglobina , la hemoglobina oxigenada, lípidos y agua tienen poco que-noabsorbancia, que permite que la luz penetre fácilmente. Cuando los agentes fototérmicos absorben la luz en esta ventana terapéutica, la foto energético se convierte en energía fototérmica.
Irvin y colaboradores han informado anteriormente alcoxi-monómeros sustituidos de benceno bis-Edot que se sintetizaron usando un acoplamiento de Negishi. 18 de acoplamiento de Negishi es un método preferido para la formación de enlaces carbono-carbono. Este proceso tiene muchas ventajas, incluyendo el uso de productos intermedios organometálicos de cinc, que son menos tóxicos y tienden a tener mayor reactividad que otros compuestos organometálicos utilizados. 19,20 compuestos orgánico de zinc también son compatibles con una amplia gama de grupos funcionales en los organohaluros. 20 En el reacción de acoplamiento de Negishi, un organohaluro y organometálico están acoplados mediante el uso de un catalizador de paladio (0) catalizador. 20 En el trabajo presentado en el presente documento, este método de acoplamiento cruzado se utiliza en la síntesis de 1,4-dialcoxi-2,5-bis ( 3,4-ethylenedioxythienyl) benzemonómeros ne (2 Bedot-B (OR)). Estos monómeros pueden ser fácilmente polimerizan electroquímicamente o químicamente para producir polímeros que son candidatos prometedores para su uso en aplicaciones biomédicas.
Los métodos convencionales para la preparación de suspensiones poliméricas coloidales en soluciones acuosas para aplicaciones biomédicas implican típicamente la disolución de polímeros a granel seguido por nanoprecipitation o emulsión técnicas de evaporación de disolvente. 21,22 A fin de producir NPs de poli (Bedot-B (OR) 2) , un enfoque de abajo hacia arriba se demuestra aquí, donde los PN se sintetizan a través de polimerización en emulsión situ. La polimerización en emulsión es un proceso que es fácilmente escalable y es un método relativamente rápido para la preparación de NP. 22 Los estudios que utilizan la polimerización en emulsión para producir NPs de otros polímeros electroactivos se han reportado para PPy y PEDOT. 15,23,24 PEDOT NPs, por ejemplo, se han preparado utilizando emulsión de aerosol polymerization. 24 Este método es difícil de reproducir, y por lo general produce, partículas de tamaño micrométrico más grandes. El protocolo se describe en este artículo explora el uso de un método de la gota-sonicación para preparar de forma reproducible 100 nm PN polímero.
En este protocolo, los polímeros electroactivos adaptados para absorber la luz en la región NIR similar al poli informó anteriormente (Bedot-B (OR) 2) se sintetizan y caracterizado para demostrar su potencial en dispositivos electrocrómicos y como agentes de PTT. En primer lugar, se describe el protocolo para la síntesis de los monómeros a través de acoplamiento de Negishi. Los monómeros se caracterizan usando espectroscopía de RMN y UV-Vis-NIR. También se describe la preparación de suspensiones coloidales NP a través de polimerización en emulsión oxidativo en medios acuosos. El procedimiento se basa en un proceso de polimerización en emulsión de dos etapas descrito previamente por Han et al. Que se aplica a los diferentes monómeros. Un sistema de dos tensioactivo esutilizado para controlar el monodispersidad NP. Un ensayo de viabilidad celular se utiliza para evaluar citocompatibilidad de los NPs. Por último, el potencial de estas NPs para actuar como transductores de PTT se demuestra por la irradiación con un láser NIR.
Protocolo
Precaución: Por favor consulte todas las hojas de seguridad pertinentes (SDS) antes de su uso. Varios de los reactivos usados en estas síntesis son potencialmente peligrosos. Utilice todas las prácticas de seguridad apropiadas, incluyendo el equipo de protección personal (gafas de seguridad, guantes, bata de laboratorio, pantalones largos y zapatos cerrados), y realizar síntesis en campanas de extracción. Litiación es particularmente peligroso y sólo debe ser realizada por personas debidamente capacitado con supervisión.
1. Síntesis del monómero
Nota: La figura 1 muestra la ruta química para la preparación de precursores y monómeros cuya síntesis se describe en las secciones 1.2 - 1.5.
- Materiales
- Purificar EDOT como se describió anteriormente. 25
- Se recristaliza tetrabutil perclorato de amonio (TBAP) en acetato de etilo y se seca bajo vacío durante 24 hr. Valorar n-butil-litio (nBuLi, 2,5 M en hexanos) como se describe por Hoye et al. 26 dentro de 48 horas antes de su uso para determinar la concentración real.
- Sulfato de magnesio seco y carbonato de potasio a 100 ° C durante 24 hr antes de su uso. Use todos los demás productos químicos utilizados en este protocolo que se recibió.
- Síntesis de 1,4-Dialkoxybenzenes
Nota: La figura 1A muestra la preparación de 1,4-dihexyloxybenzene usando 1-bromohexano.- Equipar un matraz de tres bocas de fondo redondo secado al horno con un septo, un adaptador de entrada de argón y un condensador equipado con un adaptador de salida de gas conectado a un burbujeador. Añadir una barra de agitación al matraz antes de sellar.
- Conectar el adaptador de entrada a una línea Schlenk utilizando poli (cloruro de vinilo) (PVC) tubo y purgar el matraz de fondo redondo con argón.
- Añadir 12,5 g (113,5 mmol) de hidroquinona al matraz de fondo redondo y se disuelven en 20 ml de tetrahidrofurano anhidro (THF) con agitación.
- Por separado, se disuelven 14 g (250 mmol) de KOH en 30 ml de etanol en un solo cuellomatraz de fondo redondo y revuelva hasta que se disuelva.
- Una vez disuelto, añadir lentamente la solución de KOH a la de tres bocas matraz de fondo redondo usando una jeringa. Dejar que la mezcla se agita durante 1 hora.
- Después de 1 h, añadir 250 mmol de 1-bromoalcano a la mezcla de reacción.
- Se calienta la mezcla de reacción a reflujo durante 24 h con agitación bajo argón.
- Después de 24 h, se deja que la mezcla de reacción se enfriara a temperatura ambiente y añadir 15 ml de agua DI y 10 ml de diclorometano.
- Transferir la mezcla a un embudo de separación. Aislar la capa orgánica y se lava tres veces con 10 ml de agua DI.
- Se seca la capa orgánica sobre 15 g de MgSO 4 durante 15 min.
- Retire la MgSO4 mediante filtración al vacío a través de papel de filtro.
- Eliminar el disolvente de la solución filtrada usando un evaporador rotatorio a 50 ° C y 21 kPa para producir 1,4-dialcoxibenceno como un sólido blanco bruto.
- Se recristaliza el producto en bruto mediante la adición de suficiente etanol caliente paradisolver el producto. Una vez disuelto, colocar en un baño de hielo para inducir la cristalización.
- Recoger los cristales a través de filtración al vacío a través de papel de filtro y se lava con etanol frío.
- Se secan los cristales a vacío durante 24 horas a RT y almacenarlos bajo argón hasta su uso posterior. Este procedimiento produce 1,4-dihexyloxybenzene.
- Caracterizar el producto con punto de fusión y 1 H y 13 C espectroscopía de RMN. 27
- Síntesis de restos de éster 1,4-Dialkoxybenzenes que contienen
Nota: La Figura 1B muestra la ruta química para la preparación de una 1,4-dialcoxibenceno usando acetato-4-bromobutanoato.- Equipar un matraz de tres bocas de fondo redondo secado al horno con un septo, un adaptador de entrada de argón y un condensador equipado con un adaptador de salida de vidrio conectado a un burbujeador. Añadir una barra de agitación al matraz antes de sellar.
- Conecte el adaptador de entrada a la línea de Schlenk utilizando tubería de PVC y purgar con argón.
- Pesar 1,88 g (93,5 mmol) de KI y 15,69 g (93,3 mmol) de K 2 CO 3 y añadir al matraz de fondo redondo.
- Añadir 25 ml de N anhidro, N-dimetilformamida (DMF) y se agita hasta que las sales se disuelven.
- Una vez disuelto, añadir 2,5 g (18,7 mmol) de hidroquinona a la mezcla de reacción y permitir que la reacción para agitar hasta que se disuelva.
- Cuando se disolvieron todos los sólidos, añadir 46,8 mmol de bromoalkanoate alquilo; calentar la mezcla de reacción a reflujo durante 24 h bajo argón con agitación continua.
- Retire la mezcla de reacción del fuego y deje que se enfríe a temperatura ambiente.
- Transferir la mezcla de reacción a un embudo de separación y se añade agua (20 ml) y acetato de etilo (20 ml) para extraer la capa orgánica. Aislar la capa orgánica y se lava tres veces con agua (20 ml porciones).
- Se seca la capa orgánica sobre 15 g de MgSO 4 durante 15 min. Una vez seco, retire MgSO4 de la mezcla mediante filtración al vacío a través de filpapel ter.
- Se elimina el disolvente usando un evaporador rotatorio a 100 ° C y 21 kPa. Se seca el producto crudo al vacío a RT O / N.
- Se recristaliza el producto mediante la adición de etanol caliente sólo lo suficiente para disolver todo el sólido. Una vez disuelto, enfriar el matraz en hielo y permiten que se formen cristales. Recoger el producto mediante filtración al vacío y se lava con etanol frío.
- Seque los cristales al vacío a temperatura ambiente durante 24 horas y almacenar bajo argón hasta su uso posterior. Este procedimiento produce 1,4-bis (butanoiloxi etil) benceno.
- Caracterizar el producto con punto de fusión y 1 H y 13 C espectroscopía de RMN. 28
- Síntesis de 1,4-dialcoxi-2,5-dibromobencenos
Nota: La ruta química para la preparación de 1,4-dialcoxi-2,5-dibromobencenos se muestra en la Figura 1A y 1B.- Montar un matraz de tres bocas de fondo redondo seco con una entrada de argón, un embudo de adición de presión constante capsulado con unatapón de vidrio o tabique, y una salida conectada a un tubo de plástico provisto de un embudo de vidrio invertido suspendido sobre una solución 1 M de NaOH.
- En este matraz de fondo redondo, se disuelven 218 mmol de 1,4-dialcoxibenceno en diclorometano (15 ml).
- Por separado, añadir 12 ml (598 mmol) de Br 2 a un matraz de 250 ml y diluir con diclorometano (12 ml).
- Transferir la solución 2 / diclorometano Br al embudo de adición de presión constante. Añadir la solución gota a gota Br 2 en el matraz de fondo redondo de tres bocas, con agitación, en atmósfera de argón en un lapso de 2 hr.
- Después de completar la adición, dejar que la reacción se agite O / N bajo flujo de argón continua.
- Se detiene la reacción por adición de agua DI (20 ml), y se vierte la mezcla en un embudo de separación.
- Aislar la capa orgánica y se lava tres veces con agua DI (porciones de 20 ml). Se seca la capa orgánica sobre 15 g de MgSO 4 durante 15 min.
- Retire la MgSO4 porfiltración a vacío a través de papel de filtro, y eliminar el disolvente utilizando un evaporador rotatorio a 75 ° C y 21 kPa.
- Purificar crudo 1,4-dialcoxi-2,5-dibromobenceno añadiendo suficiente etanol caliente para disolver todo el sólido. Una vez disuelto, enfriar el matraz en hielo y permiten que se formen cristales. Recoger el producto mediante filtración al vacío y se lava con etanol frío.
- Se seca el producto purificado al vacío a RT O / N; almacenar en atmósfera de argón.
- Caracterizar el producto con punto de fusión y 1 H y 13 C espectroscopía de RMN. 27,28
- El acoplamiento de Negishi con 3,4-etilenodioxitiofeno 2,5-dibromobencenos 1,4-dialcoxi-(EDOT)
Nota: La Figura 1C muestra el acoplamiento de Negishi de 1,4-dialcoxi-2,5-dibromobencenos con EDOT para formar monómeros M1 y M2.- Montar un matraz de fondo redondo de tres cuellos limpio con un septo, un condensador equipado con un adaptador de control de flujo de entrada conectado a argón, y un flujo de salida de gas conadaptador de control conectado a un burbujeador.
- Conecte el adaptador de entrada a la línea de Schlenk utilizando tubería de PVC de paredes gruesas. Comenzará a fluir argón en el matraz de reacción durante varios minutos.
- El uso de un mechero Bunsen, llama seque el aparato al vacío y purgar con argón tres veces con el fin de garantizar un ambiente sin aire.
- Pesar 1,07 g (10 mmol) de EDOT purificada y añadir al matraz de reacción usando una jeringa insertada a través del septo. Diluir la EDOT con THF anhidro (20 ml) y se agita en atmósfera de argón.
- Enfríe el frasco que contiene la solución EDOT usando un baño de hielo seco / acetona durante 15 minutos a -78 ° C.
- Después de 15 min, añadir lentamente 11 mmol nBuLi en solución de hexanos gota a gota mientras se mantiene la temperatura a -78 ° C. Agitar la reacción a -78 ° C durante 1 hr.
Nota: La concentración exacta de la nBuLi debe determinarse por titulación antes de su uso según la Sección 1.1. - Después de 1 hora de agitación, retire el hielo / ba acetona secaXX.
- Inmediatamente después de la retirada del baño, añadir 14,13 ml de 1,0 M ZnCl 2 solución gota a gota. Permitir que la reacción transcurra durante 1 hora mientras se agitaba a RT.
- Después de 1 h de agitación, añadir 4 mmol de 1,4-dialcoxi-2,5-dibromobenceno y 0,08 mmol de tetraquis (trifenilfosfina) paladio (0) a la mezcla de reacción.
- Se calienta la mezcla de reacción a reflujo (70 ° C) en un baño de aceite.
- Seguimiento de progreso de la reacción mediante cromatografía en capa fina (TLC): Tome pequeñas (0,2 ml) alícuotas de la mezcla de reacción a diario utilizando una jeringa y precipitar en 2 ml de HCl 1 M. Se extrae con 2 ml de CHCl3 y detectar el extracto en una placa de TLC de sílice junto con manchas de soluciones de EDOT y la appropriate1,4 dialcoxi-2,5-dibromobenceno. Se eluye con 60:40 de acetato de etilo: hexano.
- Cuando la reacción es completa, permitir que la mezcla de reacción se enfríe a temperatura ambiente. Se detiene la reacción por adición de 10 ml de HCl 1 M seguido de la adición de diclorometano (20 ml).
- Transfer a un embudo de separación y aislar la capa orgánica.
- Se lava la capa orgánica con agua DI hasta que el agua de lavado ya no es ácido. Prueba de la acidez del agua de lavado con papel pH.
- Se seca la capa orgánica sobre 15 g de MgSO 4, filtrar y eliminar el disolvente utilizando un evaporador rotatorio a 50 ° C y 21 kPa para producir el monómero crudo extendido conjugación (M1 o M2) como un sólido amarillo-naranja.
- Se recristaliza el producto crudo usando una solución caliente de 3: 1 etanol: solución de benceno para M1 o 7: 2 de hexano: benceno para M2. Agregue la mezcla de disolvente caliente lo suficiente como para disolver el sólido. Una vez disuelto, enfriar el matraz en hielo y permiten que se formen cristales. Recoger el producto mediante filtración al vacío y se lava con etanol frío.
- Se seca el producto a vacío durante 24 horas a RT. Almacenar en la oscuridad bajo argón.
- Caracterizar el producto con punto de fusión y 1 H y 13 C espectroscopía de RMN. 18
2. Electroquímica
- Electropolimerización
- En un matraz aforado de 50 ml preparar una solución de electrolito 100 mM de tetrabutilamonio perclorato (TBAP) en acetonitrilo anhidro (CH 3 CN).
- En un matraz aforado de 10 ml preparar un monómero de 10 mM (M1 o M2) solución utilizando la solución mM TBAP 100 / CH 3 CN como diluyente.
- Añadir un alambre de plata (electrodo de pseudo-referencia) y una bandera de platino (contraelectrodo) a una célula electroquímica secado en horno.
- Insertar un botón de platino recién pulido (2 mm de diámetro 2) para su uso como el electrodo de trabajo. Asegúrese de que la parte inferior del electrodo de platino botón no está tocando el fondo de la celda electroquímica.
- Llenar la celda electroquímica con suficiente solución de electrolito monómero para asegurar que las puntas de los tres electrodos se sumergen en la solución.
- De-airear la solución durante 5 minutos por burbujeo de argón suavemente a través de una aguja sumergida en THsolución de correo.
- Levante la aguja 2 mm por encima de la solución y continuar flujo de argón durante todo el experimento para mantener un manto de argón sobre la solución.
- Conectar los electrodos al potenciostato y comenzar la polimerización en bicicleta a los potenciales aplicados cinco veces a una velocidad de barrido de 100 mV / sec y una gama de potencial entre -1,5 V y 1,0 V.
- Registre la salida de corriente durante este proceso para generar voltamogramas cíclicos.
- Electroquímica de Polímeros
- Después de la película de polímero se deposita sobre el electrodo de trabajo de platino botón, eliminar todos los electrodos de la solución de electrolito monómero y enjuagar suavemente con solución de electrolito-monómero libre (3 ml).
- Añadir los electrodos a una célula electroquímica limpia y añadir suficiente solución de electrolito-monómero libre para asegurar que las puntas de los tres electrodos se sumergen en la solución.
- Conectar los electrodos al potenciostato. Ciclo del tw potencial aplicadoveces o a una velocidad de barrido de 50 mV / seg y una gama de potencial entre -1,5 V y 1,0 V.
- Repetir el experimento en 100, 200, 300, y 400 mV / seg. Registre la salida de corriente en cada experimento para generar voltamogramas cíclicos.
- Preparación de electroquímicamente Películas de UV-Vis-NIR Espectroscopia y fototérmica Estudios
- Preparar películas de polímero como se describe en el apartado 2.1 anterior, esta vez utilizando un óxido de indio y estaño (ITO) portaobjetos de vidrio recubierta como el electrodo de trabajo. Crecer las películas de polímero más de 5 ciclos a una velocidad de barrido de 100 mV / s.
- Después de la deposición de polímero, retire los electrodos de la solución de monómero y enjuague con acetonitrilo (5 ml).
- Guarde la película de polímero en acetonitrilo antes de espectroscópico estudios.
3. Preparación NP
La Figura 2 muestra un esquema del proceso utilizado para la preparación NP a través de polimerización en emulsión.
- Prepare una solución 1 ml de 2% (w / v) de poli (ácido 4-estirenosulfónico ácido-co-maleico) (PSS-co-MA) en agua en un vial de vidrio. Agregue una pequeña barra de agitación magnética al vial. Esta es la fase acuosa.
- Preparar 100 l de 16 mg / solución de monómero ml en cloroformo en un tubo de microcentrífuga.
- Preparar la solución orgánica disolviendo 0,03 g de ácido dodecilbenceno sulfónico (DBSA) en la solución de monómero 100 l. Mezclar la solución orgánica usando un mezclador de vórtice automática durante 30-60 min con el fin de asegurar la homogeneidad de la solución.
- Añadir la fase orgánica a la fase acuosa gota a gota en 10 l porciones mientras se agitaba con una barra de agitación magnética hasta que se utiliza el volumen completo de la solución orgánica. Permitir agitación durante 60 seg entre adiciones.
- Añadir 2 ml de agua para diluir la mezcla. Retire la barra de agitación del vial.
- Sonicar la emulsión usando un sonicador de sonda para un total de 20 segundos en intervalos de 10 segundos a una amplitud de 30%, mientras que la inmersión de lavial en un baño de hielo.
- Retire el vial de la muestra del baño de hielo, reemplace la barra de agitación, y continuar agitando la emulsión.
- Añadir 3,8 l de solución de 100 mg / ml de FeCl 3 en agua a la emulsión de monómeros. Permita que la polimerización ocurra durante 1 hora mientras se agitaba continuamente. Esto produce protocolo NPs de polímero estabilizadas con PSS-co-MA.
- Retire la suspensión NP de la placa de agitación y transferir a 7 ml tubos de centrífuga. Centrifugar la suspensión a 75.600 g durante 3 min; recuperar el sobrenadante y desechar pellet.
- Dializar el sobrenadante durante 24 horas con 100 kDa tubos de diálisis molecular de corte de peso (MWCO).
4. Polymer Films y NP Caracterización
Nota: Caracterizar las películas de polímero y PN mediante espectroscopia UV-Vis-NIR y los PN utilizando dispersión dinámica de la luz, el análisis de potencial zeta, y microscopía electrónica.
- Determinación de polímero de absorción en el UV-Vis-NEspectro IR 29
- Suspensiones de NP: Transferencia de la suspensión a una cubeta de cuarzo y adquieren un espectro de 300 - 1000 nm en un intervalo de exploración de 5 nm.
- Películas de polímero oxidadas: Transferir el portaobjetos de vidrio ITO revestido de polímero a una cubeta de cuarzo y llenar la cubeta con acetonitrilo anhidro. Añadir 2 gotas de una solución / ml 100 mg de FeCl 3 en CHCl 3 a la acetonitrilo y mezclar para asegurar la película de polímero está completamente oxidado. Adquirir un espectro de 300 - 1000 nm en un intervalo de exploración de 5 nm.
- Películas de polímero reducidos: Transferir el portaobjetos de vidrio ITO revestido de polímero a una cubeta y llenar la cubeta con acetonitrilo anhidro. Añadir una gota de hidrazina para el líquido y mezclar para asegurar la película de polímero está completamente reducido. Adquirir un espectro de 300 - 1000 nm en un intervalo de exploración de 5 nm.
- Determinación de NP Tamaño Usando dinámica de dispersión de luz (DLS) 30
- Encienda el instrumento DLS y permitirque se caliente durante 15 minutos.
- Diluir la suspensión NP en agua a una concentración de 0,01 mg / ml y el lugar en una cubeta de poliestireno desechable.
- Colocar la cubeta en el lector y comenzar la medición.
- Determinación de NP Potencial Zeta 31
- Encienda el instrumento potencial zeta y deje que se caliente durante 30 minutos.
- Preparar la muestra por dilución de 200 l de NP suspensión en 800 l de solución de 10 mM KCl.
- Llenar una cubeta de poliestireno desechable con 700 l de la muestra.
- Inserte la celda de electrodo de potencial zeta en la muestra asegurando que no queden burbujas atrapadas entre los electrodos o en la trayectoria de la luz láser.
- Insertar la cubeta en el instrumento y siga las instrucciones de software para el funcionamiento de la medición.
- Determinación de NP Tamaño Usando microscopía electrónica de barrido (SEM) 32
- Drop-fundido 10 l de las suspensiones de NP en obleas de Si ydejar secar.
- Pulverización catódica abrigo de los PN secos con 2 nm de iridio.
- Image las muestras a una distancia de trabajo de 5 mm y en 5 kV.
5. Investigar la citocompatibilidad del PN
Nota: Todas las manipulaciones celulares deben llevarse a cabo en una cabina de bioseguridad (campana de flujo laminar) para evitar la contaminación de las células con bacterias, levaduras, hongos o desde el medio ambiente, y para proteger al usuario de enfermedades potencialmente infecciosas. Todas las soluciones y materiales de construcción utilizados con las células deben ser estériles. Utilice técnicas de cultivo celular de asepsia adecuadas.
- Cultivar las células SKOV-3 de cáncer de ovario en matraces T75 a 37 ° C en un incubador de CO2 (5% de CO 2) utilizando medio Eagle modificado de Dulbecco (DMEM) suplementado con 10% de suero bovino fetal como medio de crecimiento.
- Sembrar las células a una densidad celular de 5.000 células / pocillo en una placa de 96 pocillos y se incuba durante 24 horas a 37 ° C en un CO 2 incubadora.
- Inmediatamente antes de su uso, diluir NP suspensión en medio de crecimiento completo a una concentración de 1 mg / ml.
- Filtrar las suspensiones de NP mediante el paso a través de un filtro de 0,2 micras-estéril y diluir a las concentraciones deseadas de exposición (2-500 mg / ml) con medio de crecimiento completo suplementado con 1% de penicilina / estreptomicina.
- Retire el papel de cada uno de los pozos de la placa de 96 pocillos pipeteando suavemente y reemplazar con 100 l de suspensiones de NP en las diversas concentraciones de exposición, o con 100 l de los medios de comunicación NP-libre para ambos controles citocompatibilidad positivos y negativos. Utilizar 6 pocillos replicados por condición.
- Inmediatamente antes del siguiente paso, preparar una solución de 0,5 mg / ml de 3- (4,5-dimetiltiazol-2-il) -2,5-difeniltetrazolio (MTT) en fenol DMEM libre de rojo. Filtro estéril la solución de MTT a través de un filtro de 0,2 micras-estéril.
- Después de permitir que los NPs incubar con las células durante el período de tiempo deseado (tyPically 24 o 48 horas), retire las suspensiones de NP con la pipeta cuidadosamente.
- Reemplace inmediatamente los medios de comunicación con los siguientes dependiendo de la condición:
- Para el control citocompatibilidad negativo, añadir 100 l de metanol a cada uno de 6 pozos y deje reposar durante al menos 5 minutos. Después del tratamiento metanol, sustituir el metanol con 100 l de ml de solución filtrada de forma estéril 0,5 mg / MTT en fenol DMEM libre de rojo.
- Para el control positivo y muestras tratadas con NP, sustituir el medio con 100 l de ml de solución filtrada de forma estéril 0,5 mg / MTT en fenol DMEM libre de rojo.
- Se incuban las células durante 2 a 4 horas en la incubadora. Después de la incubación, examinar las células bajo el microscopio para verificar si la formación de cristales de formazán.
- Retire con cuidado la solución MTT con la pipeta y reemplazarlo con 100 l de dimetilsulfóxido (DMSO).
- Coloque la placa de 96 pocillos en un agitador y se mezcla durante varios minutos para fomentar la disolución de la decristales Mazan.
- Medir la absorbancia de cada pocillo a 590 nm (pico de absorbancia del producto de formazán) y 700 nm (línea de base).
- Restar la absorbancia de la muestra a 700 nm (línea de base) a partir de que a 590 nm para cada pocillo.
- Normalizar la absorbancia corregida dividiéndolo por la media del control positivo y convertir a un porcentaje multiplicando por 100.
- Determinar la viabilidad ciento promedio y la desviación estándar para cada condición.
6. fototérmica Estudios Transducción
Nota:. En este trabajo un sistema láser descrito previamente por Pattani y Tunell se utiliza 33
- Fototérmica Transducción de NP Suspensiones
- Diluir PN en agua DI a la concentración de interés.
- Añadir 100 l de NP suspensión a un pocillo de una placa de 96 pocillos. Coloque la placa de bien en una placa caliente mantenida a 25 ° C.
- Encienda el suministro de energía al láser y deje que to calentar durante varios minutos. En este estudio se utiliza un 808-nm diodo láser de fibra acoplado nominal de hasta 1 W de potencia.
- Ruta el rayo láser hacia la etapa de la muestra a través de una fibra óptica. Utilice una lente convexa a divergir el haz de láser para el tamaño del punto deseado.
- Medir la potencia de salida utilizando un medidor de potencia estándar y ajustar a una potencia de 1 W / cm 2.
- Encienda la cámara de infrarrojos (cámara infrarroja InSb (FLIR Systems SC4000)) y ajuste la región de interés (ROI) lugar para leer la temperatura del punto de 6 mm, donde se concentra el láser.
- Coloque el bien de interés en el punto focal del haz de láser. Registre la temperatura basal de la muestra. Encienda el láser y irradiar el bien de forma continua durante 5 minutos, mientras que el registro de la temperatura.
- Después de 5 minutos, apague el láser y continuar registrando la temperatura del pozo hasta que se enfría de nuevo a la temperatura de la línea de base de partida.
Nota: El calor y refrescarse cada suspensión tres veces y calcular elel cambio de la temperatura media en el tiempo. Use agua DI a 25 ° C en lugar de una suspensión NP como un control negativo para la conversión fototérmica.
- Fototérmica Transducción de Polymer Films
- Transferir el portaobjetos de vidrio ITO recubierto de polímero a una placa caliente mantenida a 25 ° C.
- Encienda el suministro de energía al láser y deje que se caliente durante varios minutos. En este estudio se utiliza un 808-nm diodo láser de fibra acoplado nominal de hasta 1 W de potencia.
- Ruta el rayo láser hacia la etapa de la muestra a través de una fibra óptica. Utilice una lente convexa a divergir el haz de láser para el tamaño del punto deseado.
- Medir la potencia de salida utilizando un medidor de potencia estándar y ajustar a una potencia de 1 W / cm 2.
- Encienda la cámara de infrarrojos (cámara infrarroja InSb (FLIR Systems SC4000)) y ajuste la región de interés (ROI) lugar para leer la temperatura del punto de 6 mm, donde se concentra el láser.
- Coloque la película en el punto focal del haz de láser. Registre la baseline temperatura de la muestra. Encienda el láser e irradiar la muestra continuamente durante 5 minutos, mientras que el registro de la temperatura.
- Después de 5 min, apagar el láser y continuar la grabación de la temperatura de la muestra hasta que se enfría de nuevo a la temperatura de línea base de partida.
Nota: El calor y refrescarse cada película tres veces y calcular el cambio de la temperatura media en el tiempo. Utilice una diapositiva ITO desnudo a 25 ° C como un control negativo para la conversión fototérmica.
Resultados
El protocolo de reacción produciendo M1 y M2 se muestra en la Figura 1. Los monómeros se pueden caracterizar por 1 H y 13 C RMN espectroscopía, punto de fusión, y análisis elemental. El espectro de RMN 1H proporciona información sobre la conectividad de los átomos y sus entornos electrónicos; por lo tanto, se utiliza de manera rutinaria para verificar que las reacciones se han completado con éxito. Reacciones de acoplamiento Negishi implican acoplamiento del anillo de fenilo a la EDOT, haciendo que el pico de protones de fenilo al pasar de 7,1 ppm a 7,8 ppm. El protón tienilo también se desplazará fuera del campo a 6,5 ppm. Los cuatro protones en los carbonos puente etilendioxi se dividirán en dos grupos de multipletes a 4,3 ppm. Los protones en carbonos alifáticos no cambiarán significativamente. El espectro de RMN 13 C exhibirá picos a 170, 145, 140, y 113 para los carbonos tienilo, y 150, 120, y 112 para los carbonos fenileno. Posiciones de alicarbonos fáticos no cambiarán significativamente. La estructura química, 1 H NMR y 13 C NMR de M2 se muestran en la Figura 3.
Electropolymerizations de M2 rendimiento de polímero (P2) y voltametría cíclica de P2 se muestran en la Figura 4 en la figura 4A, en un principio, no hay respuesta de corriente.; a medida que aumenta potenciales, el inicio de la oxidación del monómero M1 (E, M) se puede ver en el + 0,25 V, con la oxidación pico del monómero (E p, m) en + 0,61 V. Durante la primera exploración, la pico inicial observado es indicativa de la oxidación de monómero irreversible, lo que resulta en la formación de P2 en la superficie del electrodo de trabajo. Durante la segunda exploración se observan dos procesos de oxidación: la oxidación monómero todavía se considera en 0,25 V, y la oxidación de polímero se ve en 0 V. voltametría cíclica de P2 (Figura 4B) se llevó a cabo a velocidades de escaneo varían 50-400 mV / seg. La película de polímero es de color azul oscuro en el estado oxidado y rojo en el estado neutral. Ciclismo polímero en una variedad de velocidades de exploración revela una relación lineal entre la velocidad de barrido y corriente de pico, lo que indica que el polímero es electroactivo y adherido al electrodo. 18 Polymer oxidación (E a, p) se observa a -0,02 V para P2, y se observa la reducción de polímero (E c, p) a -0.3 V cuando ciclado a 100 mV / s.
Los NPs se sintetizaron como se muestra en la Figura 2 y caracterizado usando-Vis-NIR UV espectroscopia, microscopía electrónica, y DLS. La radiación UV-Vis-NIR espectros de películas oxidada y reducida P2 y de P2 oxidado PN, se muestran en la Figura 5. Las películas de polímeros oxidados y PN muestran un pico de absorbancia λ max a 1,56 eV (795 nm). Cuando se reduce en hidrazina, la absorbancia pico película se desplaza a un máximo λ de 2,3 eV (540 nm). La banda de polímero gap (E g) se determina a partir del inicio de la π- π * de transición en el polímero neutro, como se indica por la flecha en la Figura 5 negro.
La imagen SEM de P2 NPs en la Figura 6A muestra que los NPs son esféricas y sub-100 nm de diámetro. DLS datos de la Figura 6B muestra una Z-media de las suspensiones a ser 104 nm de diámetro con un índice de polidispersidad (PDI) de 0,13, lo que indica que la muestra se monodispersas moderadamente. El potencial zeta de la NPs P2 se encontró que era -30,5 mV. Cambio en la temperatura cuando PN están expuestos a la radiación NIR demuestra conversión fototérmica. En comparación con los controles de agua, que se someten a menos de un 1 ° C de aumento en la temperatura, suspensiones de NP en el agua son capaces de convertir la energía láser absorbida en calor tal como se demuestra por el aumento de 30 ° C en la temperatura de las suspensiones de NP (figura6C). Se observa un aumento de la temperatura similar (28 ° C) cuando las películas de polímero sobre vidrio ITO se irradiaron a 808 nm (Figura 6C).
El citocompatibilidad del PN de polímero se determina mediante ensayos de viabilidad celular MTT. Los resultados de estudios citocompatibilidad para PEDOT:. PSS-co-MA NPs se muestran en la Figura 7 Como se muestra, dentro de la gama de concentración NP de 0,23 a 56 g / ml, los NPs no disminuyen la viabilidad celular a menos del 90% de control. Típicamente, una reducción en la viabilidad celular de menos del 20% (es decir, hasta 80% de viabilidad) se considera aceptable para la determinación de NP citocompatibilidad.

Figura 1. síntesis de monómero general a partir de la síntesis de precursores. (A) Síntesis de 1,4-dialcoxi-2,5-dibromobenceno. (B) Síntesis de 1,4-dialcoxi-2,5-dibromobenceno resto que contiene éster. (C) reacción de acoplamiento cruzado de 1,4-dialcoxi-2,5-dibromobenceno con EDOT, produciendo monómeros M1 y M2. Haga clic aquí para ver una versión más grande de esta figura.

En el que se añade la solución orgánica Figura 2. Proceso de polimerización gota a gota a una solución acuosa creando una emulsión. El monómero y el disolvente orgánico puede variar. Polimerización oxidativa se produce cuando se añade FeCl 3 a la emulsión. Después de la purificación de la suspensión coloidal, los PN se suspenden en el medio acuoso. Haga clic aquí para ver una versión más grande de estacifra.
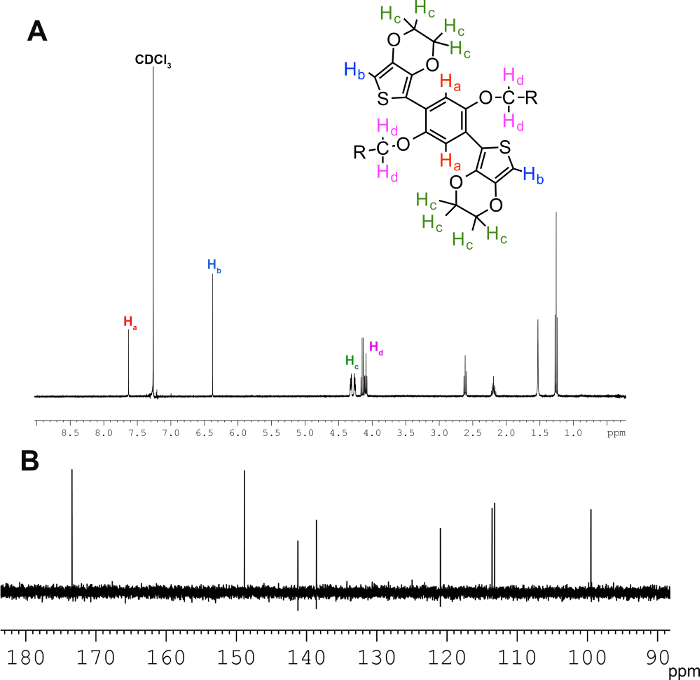
Figura 3. Los espectros de RMN de monómero M2. (A) 1 H RMN espectroscopía de M2 en el que el desdoblamiento de los protones etilendioxi a 4,32 ppm, el desplazamiento fuera del campo de los protones tienilo, y el desplazamiento campo arriba de los protones de fenilo son indicativos de acoplamiento exitoso . (B) 13 C RMN espectroscopía de M2 muestra los picos tienilo y carbono fenil. Haga clic aquí para ver una versión más grande de esta figura.
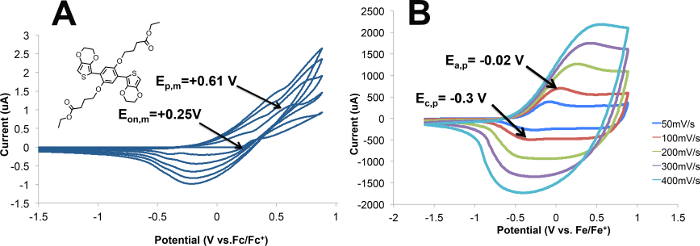
Figura 4. (A) polimerización electroquímica de M2 a P2; cinco ciclos a 100 mV / s de 0,01 M M2 en 0,1 M TBAP / CH 3 CN. (B) voltametría cíclica de la película de polímero en 0,1 M TBAP / CH 3 CN en bicicleta en 50, 100, 200, 300 y 400 mV / s. Haga clic aquí para ver una versión más grande de esta figura.

Figura 5. UV-Vis-NIR espectros de P2 tanto como una película y como una suspensión de PN. El espectro de la película oxidada se muestra en azul, el espectro de la película reducida se muestra en rojo, y el espectro de la oxidada NP suspensión se muestra en verde. La flecha negro corresponde a la línea tangente utilizado para la determinación de la banda prohibida polímero. Longitudes de onda de absorción máxima de los polímeros se proporcionan. Haga clic aquí para ver una versión más grande de estacifra.
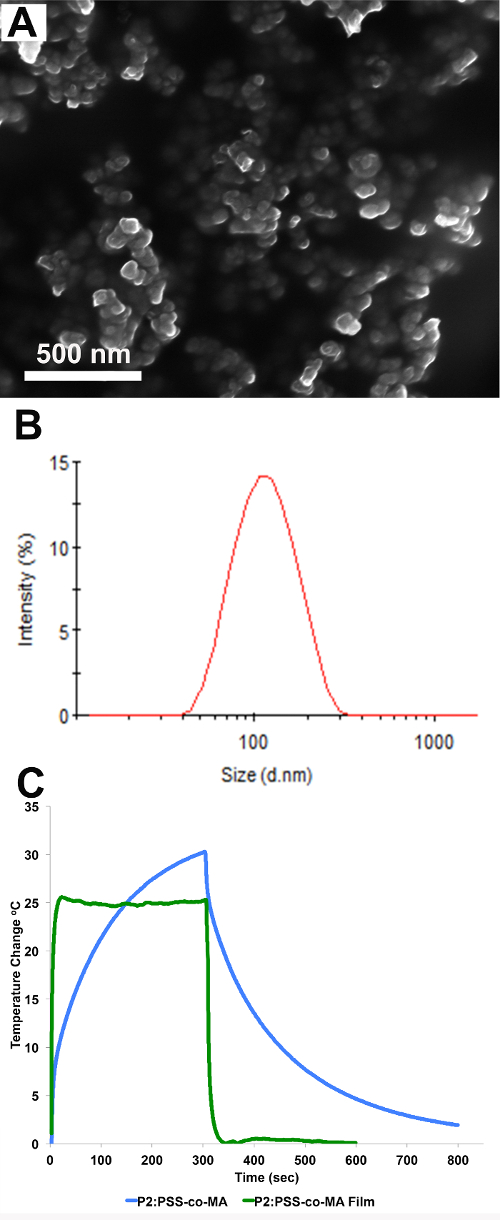
Figura 6. Imagen (A) SEM que muestra la morfología y el tamaño de P2 NPs. (B) Distribución de Tamaño de P2: PSS-co-MA NP suspensión donde el valor promedio Z es de 104 nm y el PDI es 0,13. (C) El cambio de temperatura de un P2:. PSS-co-MA NP suspensión a 1 mg / ml (azul) y el cine (verde) cuando se irradia con luz NIR de 300 seg, seguido de enfriamiento pasivo al término de la irradiación láser Por favor haga clic aquí para ver una versión más grande de esta figura.
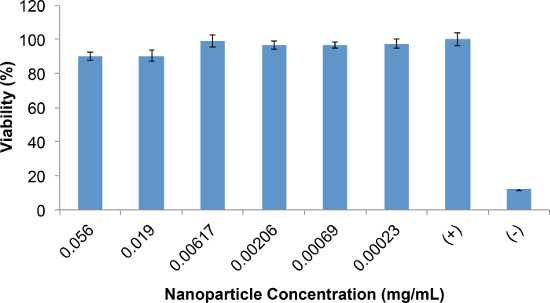
Figura 7. citocompatibilidad de PEDOT: PSS suspensiones-co-MA NP según lo determinado por el ensayo MTT Viabilidad es.se muestra para las células expuestas a concentraciones variables de NPS como el porcentaje promedio respecto a la de las células incubadas con medios NP-libre (control positivo). El control negativo se compone de células muertas por la exposición a metanol antes del ensayo MTT. Las barras de error representan la desviación estándar entre repeticiones (n = 6). Por favor, haga clic aquí para ver una versión más grande de esta figura.
Discusión
En este trabajo, los PN de polímeros electroactivos se han sintetizado como agentes potenciales de PTT para el tratamiento del cáncer. La preparación de los NPs se describe, a partir de la síntesis de los monómeros seguido por polimerización en emulsión. Mientras que la preparación de NPs utilizando polímeros electroactivos tales como EDOT y pirrol se ha descrito antes, este documento describe la preparación de NPs poliméricos a partir de monómeros de conjugación extendidos únicos, lo que demuestra que este proceso puede extenderse a más grandes, monómeros más complejas.
Dos rutas diferentes son necesarias para sintetizar los monómeros dialcoxibenceno. Mientras que el 1,4-dihexyloxybenzene se puede sintetizar usando KOH / EtOH, ese enfoque no tiene éxito en la síntesis de 1,4-bis (butanoiloxi etil) benceno, muy probablemente debido a la hidrólisis del éster promovida por una base. Cuando se utiliza un KI / K mezcla de 2 CO 3, se evita la hidrólisis, y el producto se obtiene con éxito. La bromación de both dialkoxybenzenes se logra utilizando Br 2. Es necesario llevar a cabo este experimento bajo un flujo de argón para desplazar HBr formado durante la reacción. La salida de gas debe ventilar a través de una solución de NaOH neutralizante para evitar HBr corroa accesorios campana; HBr en cuenta que puede causar un tubo de plástico se endurezca con el tiempo.
Bedot-B (OR) 2 monómeros M1 y M2 se sintetizaron utilizando acoplamiento de Negishi. Este es un método eficaz para el acoplamiento carbono-carbono de EDOT con 1,4-dialcoxi-2,5-dibromobencenos para producir Bedot-B (OR) 2 monómeros. Es crucial para enfriar el EDOT a -78 ° C antes de la adición del nBuLi, con el fin de minimizar las reacciones secundarias indeseables. Cuando todo el 1,4-dialcoxi-2,5-dibromobenceno se agota de la mezcla de reacción (determinado mediante TLC; esto lleva típicamente 3-5 días), la reacción es completa. La reacción es extremadamente sensible al aire, y cualquier exposición al aire afectará el rendimiento de la reacción. Así, cuando introducing compuestos sólidos (tales como el catalizador) en el matraz sellado, la exposición al aire debe ser minimizada mediante el aumento de flujo de argón.
Monómeros electroactivos y polímeros se caracterizan de manera rutinaria utilizando voltametría cíclica para determinar de monómero y de la oxidación de polímero potenciales y potenciales de reducción de polímero, y las películas preparadas mediante polimerización electroquímica se utilizan para determinar la absorción de polímero en el espectro UV-Vis-NIR tanto en los estados oxidado y reducido. En este trabajo, películas de polímero se depositan en tanto un botón de platino y ITO vidrio recubierto por electropolimerización. Algunas de las ventajas de electropolimerización son reproducibilidad y la capacidad de controlar el espesor de la película mediante el control de la corriente de la película polimerizada y detener el electropolimerización cuando se logra una respuesta específica 34 experimentos electroquímicos deben llevarse a cabo bajo una atmósfera inerte tal como argón.; el flujo de argón debe ser tan lento como para no perturbar la superficie de la solución para asegurar un proceso de difusión controlada. Alternativamente, los experimentos electroquímicos se pueden realizar en una caja seca atmósfera inerte equipada con pasamuros electroquímicos. Es importante que ninguno de los tres electrodos están tocando entre sí durante electropolimerización. Antes de polímero estudios de voltametría cíclica, las películas de polímero depositado deben ser lavados con solución electrolítica-monómero libre para eliminar cualquier monómero sin reaccionar de las películas. Para todos los estudios electroquímicos el rango potencial necesaria dependerá de la estructura del monómero / polímero; por lo que esta gama puede variar con monómeros y polímeros alternativos. Dependiendo de la estructura de los sustituyentes alcoxi, el disolvente utilizado para preparar las soluciones de electrolitos monómero también puede disolver el polímero. En ese caso, la deposición de polímero sobre el electrodo durante la electropolimerización será lenta o inexistente, y el disolvente utilizado para la polimerización debe ser cambiado.
e_content "> La polimerización en emulsión para la preparación de NPs compuesta de polímeros electroactivos es un método eficaz que produce NPs con una morfología uniforme En este trabajo, el proceso de polimerización en emulsión utiliza el mismo mecanismo de polimerización oxidativa utilizado durante la polimerización electroquímica;. La principal diferencia es que un oxidante químico (cloruro férrico) se utiliza en lugar de un potencial electroquímico aplicado. Esta polimerización en emulsión, por lo tanto, produce NPs idénticos en composición química a las películas preparadas mediante polimerización electroquímica. Mientras que la polimerización electroquímica proporciona un medio fácil de caracterizar las propiedades redox de la monómeros y polímeros, polimerización en emulsión es un proceso rápido, económico y reproducible, que es fácilmente escalable y potencialmente se puede utilizar con un número de diferentes polímeros electroactivos. La polimerización en emulsión también permite la preparación de NPs a partir de polímeros que tienen baja solubilidad en orgánicay disoluciones acuosas que no podían ser emulsionados con eficacia desde el estado polimérico. En nuestros polimerizaciones en emulsión, la fase orgánica se compone de monómero, disolvente orgánico (hexano), y ácido dodecilbencenosulfónico (tensioactivo). La fase acuosa se compone de agua, cloruro férrico (oxidante), y PSS-co-MA (tensioactivo). El proceso de polimerización en emulsión es precedida por una etapa de sonicación para asegurar la fase orgánica se dispersa bien en la fase acuosa. Durante la sonicación, es necesario sumergir la emulsión en un baño de hielo para evitar un calentamiento mayor. Los tensioactivos PSS-co-MA y DBSA permiten la dispersión de la NPs sintetizado en soluciones acuosas a través de inter-partículas electrostáticas fuerzas de repulsión. Estos tensioactivos también actúan dopantes de equilibrio de carga como adicionales y se ha demostrado para producir la geometría esférica NP 24 Los NPs poliméricas permanecen en el estado oxidado, (como se evidencia por el pico de absorción a 795 nm; Figura 4)., Que es críticoal para aplicaciones biomédicas en las que es necesaria la absorción en el rango NIR. 24Análisis del potencial Zeta se realiza comúnmente para evaluar la estabilidad de suspensiones de NP. El potencial zeta es el potencial en el límite entre la capa de Stern, donde los iones están fuertemente asociados con la superficie de NP, y la capa difusa donde los iones ya no interactúan con la superficie de NP. 31 Zeta mediciones de potencial se basan en el movimiento de NPs cargadas cuando una eléctrica campo se aplica a la suspensión. Específicamente, NPs cargados negativamente son atraídos hacia el electrodo positivo, y viceversa. Suspensiones coloidales pueden ser estabilizados mediante repulsiones electrostáticas. Específicamente, las suspensiones se consideran estables cuando su potencial zeta es mayor que +/- 30 mV. En nuestras formulaciones NP, la presencia de grupos sulfonato y carboxilato de DBSA y PSS-co-MA produce una carga superficial negativa sobre los NPs.
Purificación de THe NPs es un paso crucial con el fin de eliminar cualquier exceso de agente tensioactivo y cualquier material de partida sin reaccionar antes de los estudios de células in vitro. Eliminación surfactante ineficaz puede llevar a la muerte celular significativa. En cuanto a cualquier otro en el ensayo de células in vitro, es vital para trabajar en una campana de flujo laminar y trabajar en condiciones estériles. PN también deben ser esterilizados antes de su uso haciendo pasar la suspensión a través de un filtro de 0,2 micras estéril. También es importante para verificar la concentración de suspensiones de NP después de la filtración estéril. Para este propósito, una fracción de la suspensión NP filtrada de volumen conocido se puede liofilizar para obtener la masa seca. El ensayo de viabilidad celular MTT se utiliza típicamente para estudiar el efecto de biomateriales, incluyendo NPs, en células cultivadas. Este sencillo ensayo se puede adaptar a la investigación de la citocompatibilidad de suspensiones de NP con cualquier línea celular de mamífero. El ensayo colorimétrico MTT se basa en la conversión de un tetrazolio amarilla teñir en púrpura, INSOLcristales de formazán üble que luego se puede disolver en DMSO o soluciones ácidas alcohol 35,36. Cuando se realiza en ensayos celulares in vitro como el ensayo de viabilidad celular MTT en placas de múltiples pocillos, consistencia en la siembra de células y la manipulación es crítica para lograr diferencias mínimas entre replicar muestras. Antes y durante el experimento, las células sembradas deben ser examinadas bajo un microscopio para asegurar la siembra y el crecimiento constante, y también para descartar cualquier contaminación. Por último, la microscopía también puede ser utilizado para confirmar la completa disolución de cristales de formazán después de la adición de DMSO.
Se realizaron estudios de fototérmica utilizando un láser continuo a 808-nm. El uso de láseres pulsados vs. continuas puede calentar materiales de manera diferente. Estudios previos han comparado conversión fototérmica y la ablación fototérmica con nanoestructuras de oro como agentes de PTT, se necesita 37 pero más investigación para investigar la conversión fototérmica de polymeric PN como los descritos en el presente documento. En este trabajo, el láser se separaron en una lente convexa y se centró en un tamaño de punto 6 mm. Es importante tener cuidado de no perturbar el sistema óptico al ejecutar experimentos para prevenir cambios accidentales en el plano focal que podrían causar diferencias en los resultados de conversión fototérmica. Una placa caliente se utiliza para calentar y mantener una temperatura constante de línea de base para el estudio.
En conclusión, se describe un protocolo para la preparación de NP de polímeros electroactivos en suspensión en medio acuoso. Acoplamiento de Negishi es un método eficaz para el acoplamiento de 1,4-dialcoxi-2,5-dibromobencenos con 3,4-etilendioxitiofeno (EDOT). Electropolimerización de los monómeros se detalla en este protocolo. Esto demuestra ser una forma eficaz de producir rápidamente películas de polímero y estudiar sus propiedades electrónicas. Las películas de polímeros se caracterizan además utilizando espectroscopia UV-Vis-NIR para determinar los intervalos de banda de los polímeros neutros. Electrochrendimientos de polimerización en emulsión emical sub-100 nm PN con morfologías esféricas uniformes. Además de la terapia de ablación fototérmica, estos NPs tienen muchas aplicaciones potenciales en los dispositivos electroactivos, incluyendo almacenamiento de energía y sensores. Los estudios térmicos y citocompatibilidad realizados indican que estos PN podrían ser candidatos potenciales en aplicaciones biomédicas como agentes fototérmicos.
Divulgaciones
The authors have nothing to disclose.
Agradecimientos
Este trabajo fue financiado en parte por el Fondo de Texas Emerging Technology (inicio a la tuberculosis), el Programa de Mejora de Texas State University Research, el Texas State University Doctorado Becas de Investigación (al TC), la Asociación de la NSF para la Investigación y Educación en Materiales (PREM, DMR-1205670), la Fundación Welch (AI-0045), y los Institutos Nacionales de Salud (R01CA032132).
Materiales
| Name | Company | Catalog Number | Comments |
| 2 mm diameter platinum working electrode | CH Instruments | CH102 | Polished using very fine sandpaper |
| 3,4-ethylenedioxythiophene | Sigma-Aldrich | 483028 | Purified by vacuum distillation |
| 3-(4,5-Dimethylthiazol-2-yl)-2,5-Diphenyltetrazolium Bromide (MTT) 98% | Alfa Aesar | L11939 | |
| 505 Sonic Dismembrator | Fisher Scientific™ | FB505110 | 1/8“ tip and rated at 500 watts |
| 808 nm laser diode | ThorLabs | L808P1WJ | Rated at 1 W |
| Acetonitrile anhydrous 99% | Acros | 61022-0010 | |
| Avanti J-26 XPI | Beckman Coulter | 393127 | |
| Bromohexane 98% | MP Biomedicals | 202323 | |
| Dialysis (100,000) MWCO | SpectrumLabs | G235071 | |
| Dimethyl sulfoxide 99% (DMSO) | BDH | BDH1115 | |
| Dimethylformamide anhydrous (DMF) 99% | Acros | 326870010 | |
| Dodecyl benzenesulfonate (DBSA) | TCI | D0989 | |
| Dulbecco’s modified eagle medium (DMEM) | Corning | 10-013 CV | |
| EMS 150 TES sputter coater | Electron Microscopy Sciences | ||
| Ethanol (EtOH) 100% | BDH | BDH1156 | |
| ethyl 4-bromobutyrate (98%) | Acros | 173551000 | |
| Ethyl acetate 99% | Fisher | UN1173 | |
| Fetal bovine serum (FBS) | Corning | 35-010-CV | |
| Helios NanoLab 400 | FEI | ||
| Hexane | Fisher | H306-4 | |
| Hydrochloric acid (HCl) | Fisher | A142-212 | |
| Hydroquinone 99.5% | Acros | 120915000 | |
| Hydrozine anhydrous 98% | Sigma-Aldrich | 215155 | |
| Indium tin oxide (ITO) coated galss | Delta Technologies | CG-41IN-CUV | 4-8 Ω/sq |
| Iron chloride 97% FeCl3 | Sigma-Aldrich | 157740 | |
| Magnesium sulfate (MgSO4) | Fisher | 593295 | Dried at 100 °C |
| SKOV-3 | ATCC | HTB-26 | |
| Methanol | BDH | BHD1135 | |
| n-Butlithium (2.5 M) | Sigma-Aldrich | 230707 | Pyrophoric |
| Poly(styrenesulfonate-co-malic acid) (PSS-co-MA) 20,000 MW | Sigma-Aldrich | 434566 | |
| Potassium carbonate | Sigma-Aldrich | 209619 | Dried at 100 °C |
| Potassium hydroxide | Alfa Aesar | A18854 | |
| Potassium iodide | Fisher | P410-100 | |
| RO-5 stirplate | IKA-Werke | ||
| SC4000 IR camera | FLIR | ||
| Synergy H4 Hybrid Reader | Biotek | ||
| Tetrabutylammonium perchlorate (TBAP) 99% | Sigma-Aldrich | 3579274 | Purified by recrystallization in ethyl acetate |
| Tetrahydrofuran anhydrous (THF) 99% | Sigma-Aldrich | 401757 | |
| tetrakis(triphenylphosphine) palladium(0) | Sigma-Aldrich | 216666 | Moisture sensitive |
| Thermomixer | Eppendorf | ||
| USB potentiostat/galvanostat | WaveNow | AFTP1 | |
| Zetasizer Nano Zs | Malvern | Optical Arrangment 175° | |
| Zinc chloride (1 M) ZnCl2 | Acros | 370057000 |
Referencias
- Irvin, J., Irvin, D., Stenger-Smith, J. Electrically active polymers for use in batteries and supercapacitors. Handbook of Conducting Polymers. , (2007).
- Amb, C. M., Dyer, A. L., Reynolds, J. R. Navigating the color palette of solution-processable electrochromic polymers. Chemistry of Materials. 23 (3), 397-415 (2011).
- Beaujuge, P. M., Reynolds, J. R. Color control in pi-conjugated organic polymers for use in electrochromic devices. Chemical Reviews. 110 (1), 268-320 (2010).
- Ananthakrishnan, N., Padmanaban, G., Ramakrishnan, S., Reynolds, J. R. Tuning polymer light-emitting device emission colors in ternary blends composed of conjugated and nonconjugated polymers. Macromolecules. 38 (18), 7660-7669 (2005).
- Zhu, Y., Otley, M. T., et al. Neutral color tuning of polymer electrochromic devices using an organic dye. Chemical Communications, Cambridge, England. 50 (60), 8167-8170 (2014).
- Kline, W. M., Lorenzini, R. G., Sotzing, G. A. A review of organic electrochromic fabric devices. Coloration Technology. 130 (2), 73-80 (2014).
- Gerard, M., Chaubey, A., Malhotra, B. D. Application of conducting polymer to biosensors. Biosensors & Bioeletronics. 17, 345-359 (2002).
- Abidian, M. R., Kim, D. -H., Martin, D. C. Conducting-polymer nanotubes for controlled drug release. Advanced materials. 18 (4), 405-409 (2006).
- Ge, D., Qi, R., et al. A self-powered and thermally-responsive drug delivery system based on conducting polymers. Electrochemistry Communications. 12 (8), 1087-1090 (2010).
- George, P. M., LaVan, D. A., Burdick, J. A., Chen, C. -Y., Liang, E., Langer, R. Electrically controlled drug delivery from biotin-doped conductive polypyrrole. Advanced Materials. 18 (5), 577-581 (2006).
- Li, Y., Neoh, K. G., Kang, E. T. Controlled release of heparin from polypyrrole-poly(vinyl alcohol) assembly by electrical stimulation. Journal of biomedical materials research. Part A. 73 (2), 171-181 (2005).
- Svirskis, D., Travas-Sejdic, J., Rodgers, A., Garg, S. Electrochemically controlled drug delivery based on intrinsically conducting polymers. Journal of controlled release: official journal of the Controlled Release Society. 146 (1), 6-15 (2010).
- Cheng, L., Yang, K., Chen, Q., Liu, Z. Organic stealth nanoparticles for highly effective in vivo near-infrared photothermal therapy of cancer. ACS Nano. 6 (6), 5605-5613 (2012).
- Chougule, M. A. Synthesis and characterization of polypyrrole (PPy) thin films. Soft Nanoscience Letters. 01 (01), 6-10 (2011).
- Yang, K., Xu, H., Cheng, L., Sun, C., Wang, J., Liu, Z. In vitro and in vivo near-infrared photothermal therapy of cancer using polypyrrole organic nanoparticles. Advanced materials. 24 (41), 5586-5592 (2012).
- Diniz, S. N., Sosnik, A., Mu, H., Valduga, C. J. Nanobiotechnology. BioMed research international. 2013, (2013).
- Weissleder, R. A Clearer Vision for in vivo Imaging. Nature Biotechnology. , (2001).
- Irvin, J., Reynolds, J. Low-oxidation-potential conducting polymer: alternating substituted para-phenylene and 3,4-ethylenedioxythiophene repeat units. Polymer. 39 (11), 2339-2347 (1998).
- Yang, Y., Oldenhius, N., Buchwald, S. Mild and general condition for Negishi cross-coupling enabled by the use of palladacycle percatalysts. Angew Chem. 29 (6), 997-1003 (2012).
- Negishi, E., Hu, Q., Huang, Z., Qian, M., Wang, G. The Negishi Coupling: an update: Enantiopure sulfoxides and sulfinamides. New products from Aldrich R & D. Aldrichchimica Acta. 38 (3), (2005).
- Bilati, U., Allémann, E., Doelker, E. Development of a nanoprecipitation method intended for the entrapment of hydrophilic drugs into nanoparticles. European Journal of Pharmaceutical Sciences. 24 (1), 67-75 (2005).
- Nagavarma, B. V. N., Yadav, H. K. S., Ayaz, A., Vasudha, L. S., Shivakumar, H. G. Different techniques for preparation of polymeric nanopaticles-A review. Asian Journal of Pharaceutical and Clinical Research. 5 (3), 16-23 (2012).
- Vaitkuviene, A., Kaseta, V., et al. Evaluation of cytotoxicity of polypyrrole nanoparticles synthesized by oxidative polymerization. Journal of Hazardous Materials. 250-251, 167-174 (2013).
- Han, Y. K., Yih, J. N., et al. Facile synthesis of aqueous-dispersible nano-PEDOT:PSS-co-MA core/shell colloids through spray emulsion polymerization. Macromolecular Chemistry and Physics. 212 (4), 361-366 (2011).
- Winkel, K. L., Carberry, J. R., Irvin, J. A. Synthesis and electropolymerization of 3,5-bis-(3,4-ethylenedioxythien-2-yl)-4,4-dimethyl isopyrazole: A donor-acceptor-donor monomer. Journal of the Electrochemical Society. 160 (8), G111-G116 (2013).
- Hoye, T., Eklov, B., Voloshin, M. No-D NMR spectroscopy as a convenient method for titering. Organic Letters. 6 (15), 2567-2570 (2004).
- Umezawa, K., Oshima, T., Yoshizawa-Fujita, M., Takeoka, Y., Rikukawa, M. Synthesis of hydrophilic-hydrophobic block copolymer ionomers based on polyphenylenes. ACS Macro Letters. 1 (8), 969-972 (2012).
- Tao, Z., Fan, H., Zhou, J., Jin, Q. Conjugated polyelectrolyte with pendant caboxylate groups: synthesis, photophysics, and pH responses in the presence of surfactants. Journal of Polymer Science Part A-Polymer Chemistry. 46 (3), 830-843 (2008).
- Winkel, K. L., Carberry, J. R., et al. Donor-acceptor-donor polymers utilizing pyrimidine-based acceptors. Reactive & Functional Polymers. 83, 113-122 (2014).
- Kròl, E., Scheffers, D. -J. FtsZ polymerization assays: simple protocols and considerations. Journal of Visualized Experiments : JoVE. (81), e50844(2013).
- Zolnik, B., Potter, T. M., Stern, S. T. Zeta potential measurement. Methods in Molecular Biology. 697, 173-179 (2011).
- Nogi, K., Naito, M., Yokoyama, T. Nanoparticle technology handbook. , Elsevier. (2012).
- Pattani, V. P., Tunnell, J. W. Nanoparticle-mediated photothermal therapy: A comparative study of heating for different particle types. Lasers in Surgery and Medicine. 44 (8), 675-684 (2012).
- Subianto, S., Will, G. D., Kokot, S. Templated electropolymerization of pyrrole in a capillary. Journal of Polymer Science, Part A: Polymer Chemistry. 41 (12), 1867-1869 (2003).
- Sgouras, D., Duncan, R. Methods for the evaluation of biocompatibility of soluble synthetic polymers which have potential for biomedical use: use of the tetrazolium-based colorimetric assay (MTT) as a preliminary screen for evaluation of in vitro cytotoxicity. Journal of Materials Science: Materials in Medicine. 1 (2), 61-68 (1990).
- Ahmadian, S., Barar, J., Saei, A. A., Fakhree, M. A. A., Omidi, Y. Cellular toxicity of nanogenomedicine in MCF-7 cell line: MTT assay. Journal of Visualized Experiments : JoVE. (26), (2009).
- Huang, X., Kang, B., et al. Comparative study of photothermolysis of cancer cells with nuclear-targeted or cytoplasm-targeted gold nanospheres: continuous wave or pulsed lasers. Journal of Biomedical Optics. 15 (5), 058002(2015).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados