Kernspinresonanzspektroskopie (NMR-Spektroskopie)
Überblick
Quelle: Labor von Dr. Henrik Sundén-Chalmers University of Technology
Kernresonanzspektroskopie (NMR) ist eine wichtige Analysetechnik für organische Chemiker. Mit Hilfe der NMR wurde die Arbeit im biologischen Labor enorm erleichtert. Nicht nur kann es Auskunft über die Struktur eines Moleküls sondern auch bestimmen den Inhalt und die Reinheit einer Probe. Im Vergleich mit anderen häufig auftretenden Techniken für organische Chemiker — wie thermische Analyse und Massenspektrometrie (MS) – NMR ist eine zerstörungsfreie Methode, die wertvoll ist, wenn die Wiederherstellung der Probe wichtig ist.
Eines der am häufigsten verwendeten NMR-Techniken für organischer Chemiker ist Proton (1H) NMR. Die Protonen vorhanden in einem Molekül verhält sich anders abhängig von der chemischen Umgebung, macht es möglich, seine Struktur aufzuklären. Darüber hinaus ist es möglich, den Abschluss einer Reaktion durch den Vergleich der NMR-Spektren des Ausgangsmaterials, des Endprodukts zu überwachen.
Dieses Video veranschaulicht, wie NMR-Spektroskopie in der täglichen Arbeit von organischer Chemiker verwendet werden kann. Die folgenden angezeigt werden: ich) Vorbereitung einer NMR-Probe. (II) Verwendung von 1H NMR, um eine Reaktion zu überwachen. (III) Identifizierung des Erzeugnisses aus einer Reaktion mit 1H NMR gewonnen. Die Reaktion, die angezeigt wird, ist die Synthese aus einer E- Chalcone (3) ein Aldehyd (1) und ein Keton (2) (Schema 1). 1
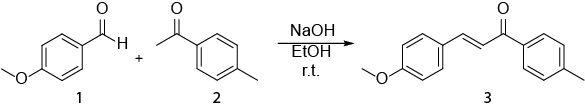
Schema 1. Synthese von (2E)-3-(4-methoxyphenyl)-1-(4-methylphenyl)-2-propen-1-one.
Grundsätze
Atomkerne mit einer ungeraden Masse oder Ordnungszahl haben eine Eigenschaft namens Spin, die es ermöglichen, NMR verwenden, um Elemente wie Wasserstoff (1H), Kohlenstoff (13C) und Phosphor (31P) zu erkennen. Die Spins sind zufällig und in zufällige Richtungen dreht; Allerdings werden durch die Anwendung eines äußeren Magnetfeldes diese Kerne selbst mit oder gegen die angelegten Magnetfeldes ausgerichtet. Diese beiden Staaten haben unterschiedlichen Energieniveaus: ein niedrig-Energie-Zustand und einen energiereichen Zustand. Bestrahlung mit elektromagnetischen Strahlung bewirkt den niedrigen Energiezustand um die energiereichen Zustand umzudrehen. Wenn die Strahlung nicht mehr ist, die Kerne werden Entspannung und ein kostenlosen induktive Zerfall (FID) erzielt wird. Die FID ist Fourier umgewandelt, um die Gipfel des NMR-Spektrum geben. Verschiedene Elemente haben unterschiedliche Frequenzen, was zu verschiedenen chemischen Verschiebungen (Tabelle 1). Die NMR-Spektren können verschiedene Arten von Informationen über eine Verbindung zur Verfügung stellen; Das Integral eines Peaks liefert die Anzahl der Protonen, vertreten die Kupplung konstant (J-Kupplung) gibt die Korrelation der Protonen und der Spaltung Muster eines Peaks erzählt, wie viele andere NMR-aktive Kerne in der Nähe sind (oft als "Nachbarn").
Seit 1H NMR Maßnahmen 1H Kerne ist es wichtig, deuterierte Lösungsmittel zu verwenden; sonst wird das Signal von Interesse in der Lärm des Lösungsmittels Signals verloren gehen.
| Art von proton | Verschiebung (δ, ppm) | Typ des Kohlenstoffs | Verschiebung (δ, ppm) |
| 1° Alkyl, RCH3 | 0,8-1,2 | 1° Alkyl, RCH3 | 0 – 40 |
| 2° Alkyl, R2CH2R | 1.2-1.5 | 2° Alkyl, R2CH2R | 10 – 50 |
| 3° Alkyl, RCHR2 | 1,4-1,8 | 3° Alkyl, RCHR2 | 15 – 50 |
| Allylic, R2C = CRCH3 | 1,6 – 1,9 | Alken, C=C | 100-170 |
| Keton, RC(=O) CH3 | 2.1-2.6 | Aryl, C im aromatischen ring | 100-170 |
| Äther, ROCH2R | 3.3 – 3,9 | Alkohol oder Äther, R3COR | 50 – 90 |
| Alkohol, HOCH2R | 3.3 – 4.0 | Carbonsäure oder Ester, R-C(= O) oder |
160-185 |
| Vinylic, R2C = CH2 | 4,6 – 5,0 | Aldehyd oder Keton, R-C(= O) R |
182 – 215 |
| Vinylic, R2C = CRH | 5.2-5.7 | ||
| Aromatisch, ArH | 6,0-8,5 | ||
| Aldehyd RC(=O)H | 9,5-10,5 | ||
| Alkohol Hydroxyl, ROH | 0,5-6,0 | ||
| Carboxylic, RC(=O) OH | 10 – 13 |
Tabelle 1. Gemeinsamen Protonen und Kohlenstoff NMR chemische Verschiebungen. 2
Verfahren
1. Vorbereitung der NMR Ausgangsmaterial
- Fügen Sie ~ 10 mg Ausgangsmaterial für ein sauberes NMR-Röhrchen.
- Lösen Sie das Ausgangsmaterial in ~0.7 mL deuterierter Lösungsmittel (Beispiel CDCl-3). Eine passende Höhe des Lösungsmittels für ein gutes Spektrum beträgt 4,5-5 cm.
- Röhrchen Sie die NMR vorsichtig und schreiben Sie den Probennamen auf der Kappe.
- Schütteln Sie die Probe vorsichtig, um sicherzustellen, dass alles Material aufgelöst hatte. Achten Sie darauf, vermeiden Sie den Kontakt zwischen dem Lösungsmittel und die Kappe, die zu möglichen Kontamination der Probe führen könnten.
- Die NMR-Röhrchen vorsichtig in ein Spinner einführen. Der Spinner dreht sich nach dem Einlegen in den Magneten um sicherzustellen, dass die gesamte Probe ein homogenes Magnetfeld erfährt. Reinigen Sie die Außenseite der NMR-Röhrchen und Spinner mit 2-Propanol und Labor Gewebe, um Fingerabdrücke und Schmutz entfernen.
- Ort der Spinner in einer Probe Tiefe messen um sicherzustellen, dass unten die NMR-Röhrchen nicht zu weit in der NMR-Sonde eingefügt wird, da, dass das Spektrometer möglicherweise beschädigen könnte. Verschiedene Sonden haben unterschiedlichen Tiefen und der Benutzer muss die spezifischen Tiefenmesser beachten.
- Legen Sie die Probe in der NMR-Spektrometer. Hier wurde ein Varian 400 MHz-Spektrometer, ausgestattet mit einem Autosampler verwendet.
- Verarbeiten Sie nach Beendigung der NMR-Messung das Spektrum zu und weisen Sie die Peaks im Spektrum.
2. Vorbereitung des 3 M NaOH und Chalcone Synthese
- 60 mg NaOH hinzu kommt eine volumetrische 50 mL-Flasche.
- Auflösen der NaOH durch Zugabe von entionisiertem Wasser auf die Hälfte des Kolbens. Verdünnen Sie die Lösung durch Zugabe von mehr Wasser, bis die Markierung erreicht ist.
- Fügen Sie 10 mL Ethanol in einer 50 mL Rundboden-Kolben ausgestattet mit einer magnetischen Stir Bar.
- Danach fügen Sie 680,5 mg 4-Methoxybenzaldehyde und 5 mL NaOH-Lösung, die in Schritt 2.1 in den gleichen Kolben vorbereitet.
- 671 mg 4-Methylacetophenone Folge der gerührten Lösung und den Kolben Mütze und rühren bei Raumtemperatur.
- Überwachen Sie den Fortschritt der Reaktion von 1H NMR in 30 min Abständen (siehe Schritt 3) bis zum vollständigen Verbrauch der Ausgangsstoffe.
- Fügen Sie 5 mL Wasser hinzu, wenn die Reaktion Abschluss (~ 3 h) erreicht hat. Filtern Sie den entstehenden Niederschlag zu und waschen Sie es mit 20 mL Ethanol/Wasser 1:2. Lassen Sie der Niederschlag der Luft trocknen.
- Berechnen Sie die Rendite des erworbenen Produkts. Eine NMR-Probe gemäß Schritt 1.2.2.7 vorbereiten. Überprüfen Sie die Reinheit mit 1H NMR. Wenn nicht rein, reinigen Sie das Produkt über Rekristallisation mit Ethanol.
- Ein NMR-Röhrchen mit einer Pasteurpipette ca. 3 Tropfen des Reaktionsgemisches hinzu und spülen Sie die Pipette mit deuterierte Lösungsmittel.
- Wiederholen Sie die Schritte 1,2 – 1,8.
3. kurze Interpretation von NMR-Spektrum
- Das Spektrum mit einem geeigneten Programm (Beispiel MestReNova) zu verarbeiten.
- Die verschiedenen Gipfeln der NMR Verschiebungen in der Tabelle 1zu korrelieren. Die chemischen Verschiebungen verleiht einen Hauch von welche Art von Umgebung, die die Protonen existiert in.
- Integrieren Sie die Spitzen um die Anzahl der Wasserstoffatome entspricht jede Spitze zu geben. Integration aller Peaks gibt eine relative Anzahl der gesamten Protonen.
- Die Aufspaltung der Proton-Gipfel, die die Anzahl der Nachbarn zu bewerten.
- Messen Sie die J-Kupplung um zu sehen, wie die Protonen miteinander verbunden sind.
Ergebnisse
Durch den Vergleich der Spektren der Ausgangsstoffe (Abbildungen 1 und 2), dass das Endprodukt (Abbildung 5) einen deutlichen Unterschied zwischen den Spektren kann beobachtet werden, Bildung von die Chalcone angibt. Der Endpunkt der Reaktion kann sein bestimmt durch die Entnahme von NMR-Proben in verschiedenen Zeitabständen; zum Beispiel den Aldehyd Proton Gipfel (C(=O)H) (1) sehen Sie in Abbildung 3 , aber nicht in Abbildung 4, bedeutet der Abschluss der Reaktion nach 3 h. Mit Blick auf die integrale, splitting Muster und J-Kupplungen der Gipfel, ist es möglich, die Struktur der die Chalcone zu validieren. Die integrale der Gipfel (Nummern unter dem Gipfel, Abbildung 5) zeigen die relative Höhe der Wasserstoffatome vorhanden, die auf die Höhe der Wasserstoffatome im Produkt gefunden entsprechen sollte. Darüber hinaus gibt das splitting Muster Aufschluss über die Anzahl der Nachbarn; z. B. Peak (5) und (1) — beide Unterhemden — bzw. keine Nachbarn in der Nähe mit integrale der 3 korreliert mit der MeO- und mir-Gruppe angeben. Durch den Vergleich der chemischen Verschiebungen in den Spektren mit Tabelle 1 lässt sich verdeutlichen, dass die MeO-Gruppe das Singulett bei 3,80 ppm und mir-Gruppe auf 2,45 ppm entspricht. Darüber hinaus kann man als zwei Dubletten (Abbildung 5), Bildung der Doppelbindung 7,80 und 7,44 ppm. Blick auf die J-Kopplung von 16 Hz zeigt Bildung eines E-Alken; die Z-Alken hat in der Regel einen kleineren Wert von 10 – 12 Hz.3 Zuordnung von den aromatischen Gipfeln überprüft die Struktur (Abbildung 5). 4
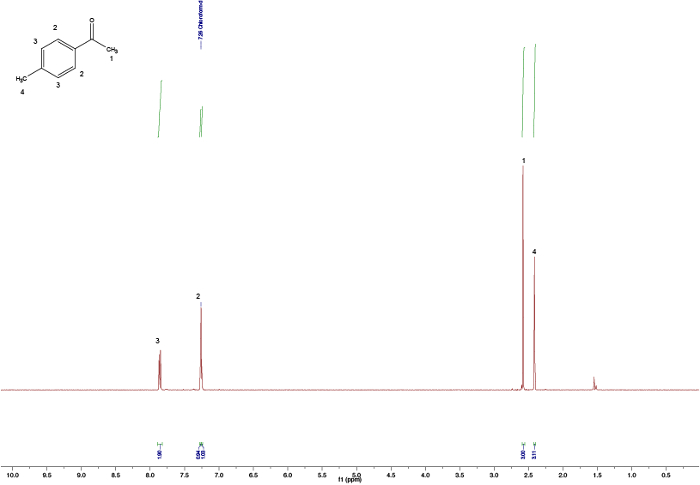
Abbildung 1: Zugewiesene 1H NMR-Spektren von 4-Methylacetophenone Klicken Sie bitte hier, um eine größere Version dieser Figur.
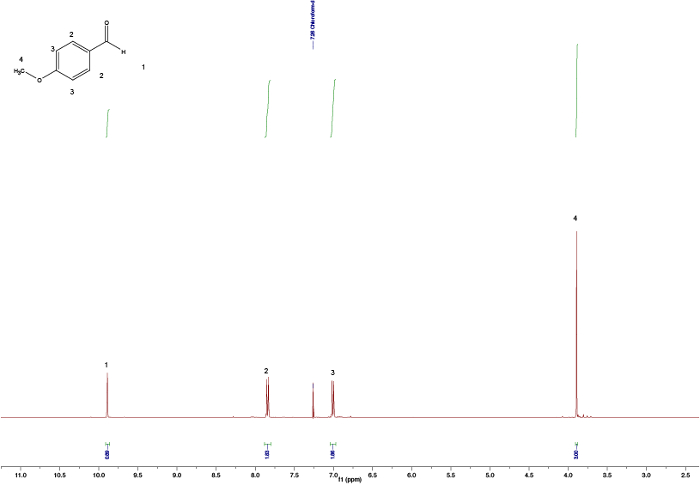
Abbildung 2: Zugewiesene 1H NMR-Spektren von 4-Methoxybenzaldehyde. Bitte klicken Sie hier für eine größere Version dieser Figur.
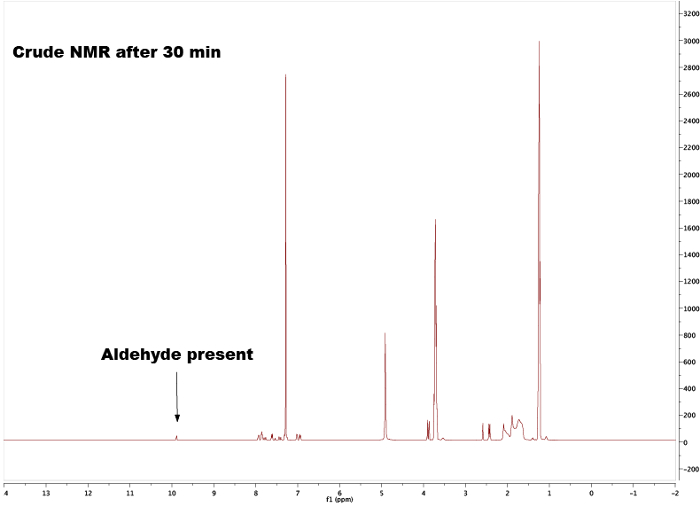
Abbildung 3. Rohe 1H NMR-Spektren nach 30 min zeigt die verbleibende Aldehyd-Spitze. Bitte klicken Sie hier für eine größere Version dieser Figur.
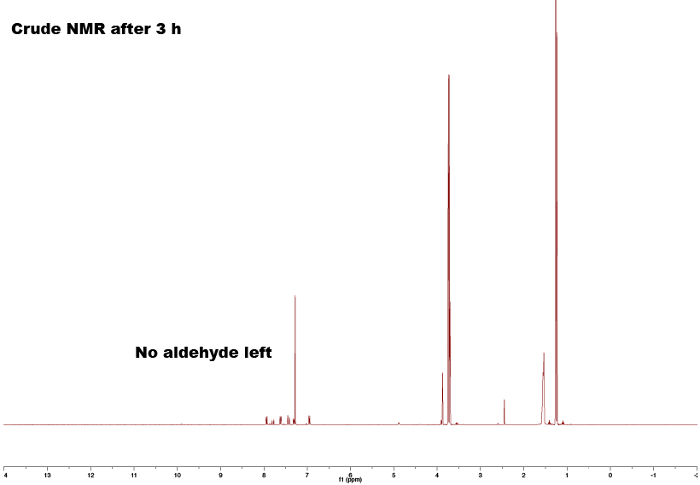
Abbildung 4. Rohe 1H NMR-Spektren nach 3 h zeigt keine Aldehyd Rest Spitze. Bitte klicken Sie hier für eine größere Version dieser Figur.
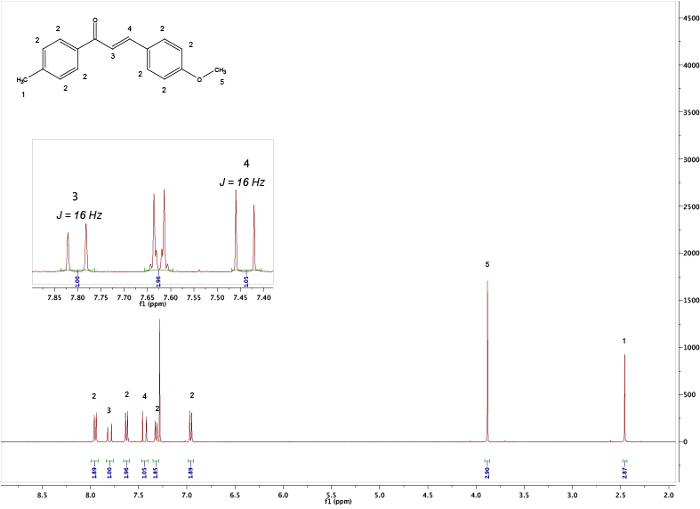
Abbildung 5. 1 H-NMR-Spektren des erhaltenen Produkts nach Aufarbeitung. Das eingefügte Bild zeigt die J -Kupplungen die Alken. Bitte klicken Sie hier für eine größere Version dieser Figur.
Anwendung und Zusammenfassung
NMR, beispielsweise lässt sich erkennen Reaktion Zwischenprodukte, erleichtern die Arbeit in der Aufklärung einen Reaktionsmechanismus. Mit Hilfe der NMR ist es auch möglich, molekularen Bewegungen und Interaktionen wichtig für die Entwicklung von Medikamenten zu beobachten. Darüber hinaus kann NMR Strukturinformationen über solide Materialien geben; zum Beispiel, eine Begründung für die beobachteten Materialeigenschaften bieten. Andere Anwendungen der NMR finden Sie im Bereich der Medizin, wo die Magnetresonanz-Tomographie (MRT) zur medizinischen Diagnostik häufig verwendet wird. NMR hat auch in Metabolomics verwendet worden, um verschiedene Metaboliten ausgeschieden durch den Organismus, wodurch einen metabolischen Fingerabdruck zu erkennen. Die Verwendung von NMR sind breit; aus der Bestimmung der Struktur eines einzelnen Moleküls zu Bildgebung des menschlichen Gehirns.
Tags
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Kernspinresonanzspektroskopie (NMR-Spektroskopie)
Organic Chemistry
249.2K Ansichten

Einführung in die Katalyse
Organic Chemistry
34.7K Ansichten

Montage eines Reflux-Systems für beheizte chemische Reaktionen
Organic Chemistry
168.6K Ansichten

Durchführung von Reaktionen unterhalb der Raumtemperatur
Organic Chemistry
70.8K Ansichten

Übertragen von Lösungmitteln mit der Schlenk-Technik
Organic Chemistry
41.7K Ansichten

Entgasung von Flüssigkeiten mittels Freeze-Pump-Thaw Cycling
Organic Chemistry
56.4K Ansichten

Vorbereiten von wasserfreien Reagenzien und Geräten
Organic Chemistry
79.5K Ansichten

Reinigen von Verbindungen durch Umkristallisation
Organic Chemistry
711.0K Ansichten

Trennen von Gemischen durch Ausfällung
Organic Chemistry
158.2K Ansichten

Fest-Flüssig-Extraktion
Organic Chemistry
238.4K Ansichten

Entfernung von Lösungsmitteln mit dem Rotationsverdampfer
Organic Chemistry
213.1K Ansichten

Fraktionierte Destillation
Organic Chemistry
335.1K Ansichten

Züchten von Kristallen für die Röntgenbeugungsanalyse
Organic Chemistry
32.9K Ansichten

Performing 1D Thin Layer Chromatography
Organic Chemistry
290.3K Ansichten

Säulenchromatographie
Organic Chemistry
361.6K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten