Bestimmung von NOX in Autoabgasen mittels UV/Vis-Spektroskopie
Überblick
Quelle: Labors von Margaret Workman und Kimberly Frye - Depaul University
In der Troposphäre wird Ozon natürlich gebildet, wenn Sonnenlicht spaltet sich Stickstoffdioxid (Nr.2):
NO2 + Sonnenlicht → NO + O
O + O2 → O3
Ozon (O3) kann weitergehen, um mit Stickstoffmonoxid (NO), Stickstoffdioxid (Nr.2) und Sauerstoff bilden zu reagieren:
NO + O3 → NO2 + O2
Dadurch NO Netto-Gewinn von Ozon (O3). Jedoch wurden mit der anthropogenen Produktion von Ozon bilden Vorstufen (NO, NO2und flüchtige organische Verbindungen) durch die Verbrennung fossiler Brennstoffe, erhöhte Werte von Ozon in der Troposphäre gefunden. Kfz-Auspuff ist eine bedeutende Quelle für diese Ozon bilden Vorstufen: NO, NO2und flüchtige organische Verbindungen (VOC). Zum Beispiel bilden mobile Quellen fast 60 % NO + NO2 -Emissionen.
Bei den hohen Temperaturen im Brennraum ein Auto gefunden reagieren Stickstoff und Sauerstoff aus der Luft zu Stickstoffmonoxid (NO) und Stickstoffdioxid (Nr.2):
N2(g) + O2 (g)→ 2 NO(g)
2 NO(g) + O2(g)→ 2 NO2(g)
Stickstoffmonoxid (NO) emittiert in den Autoabgasen ist allmählich zu Stickstoffdioxid (Nr.2) in der Luft oxidiert. Diese Mischung aus NO und NO2 wird oft als NOXbezeichnet. Wenn NOX mit flüchtigen organischen Verbindungen in der Atmosphäre in Gegenwart von Sonnenlicht reagiert, vereinfacht troposphärisches Ozon Formen, wie in diesem gesehen chemische Reaktion:
NOX + VOC + Sonnenlicht → O3 andere Produkte
Diese giftige Mischung der Luftverschmutzung, die Aldehyde, Peroxyacetyl Nitrat, Ozon, VOC und NOXenthalten kann, nennt man photochemischer Smog. Ozon ist der größte Bestandteil von photochemischer Smog. Diese Smog findet sich in allen modernen Städten, aber es findet sich vor allem in Städten mit sonnigen, warmen, trockenen Klima und eine große Zahl von Kraftfahrzeugen. Die gelb-braune Farbe der Smog in der Luft liegt teilweise an der Stickstoffdioxid vorhanden, da dieses Gas sichtbares Licht in der Nähe von 400 absorbiert nm (Abbildung 1).
Kurzfristig NO2 -Exposition (30 min bis 1 Tag), respiratorische Nebenwirkungen bei gesunden Menschen und erhöhte respiratorische Symptome bei Menschen mit Asthma führt. NOX reagiert mit Ammoniak und andere Verbindungen zur Form Partikel. Diese kleinen Partikel können in die Lunge eindringen und Atembeschwerden, einschließlich Emphysem und Bronchitis verursachen. Personen, die verbringen viel Zeit auf der Straße oder Leben in der Nähe einer Straße, erleben deutlich höhere Exposition gegenüber Nr.2.
Aufgrund der Auswirkungen auf menschliche Gesundheit und die Umwelt, die US Environmental Protection Agency (EPA) hat NO2 als Schadstoff Kriterien klassifiziert und setzt das Primärnormal bei 100 ppb (98. Perzentil der täglichen Höchstkonzentrationen 1-h, gemittelt über 3 Jahre) und 53 ppb (Jahresmittel). Wenn man bedenkt, dass etwa 1/3 der NOx -Emissionen in den USA on-Road Fahrzeuge entfallen, sind Automobile-Emissionen daher durch den Clean Air Act geregelt. Die amerikanische Umweltbehörde EPA gegründet Abgasnormen, die Automobilhersteller befolgen müssen, wenn Autos zu produzieren. Stufe 2-Abgasnormen sind zurzeit so eingestellt, dass Hersteller Flotte Durchschnitt NOx -Emissionen von nicht mehr als 0,07 g/Meile haben müssen.
One way Hersteller erfüllen diese Norm ist die Verwendung von Katalysatoren auf ihre Autos. Dieses Gerät befindet sich zwischen dem Motor und dem Endrohr. Der Abgasstrom des Katalysators durchläuft und Katalysator ausgesetzt ist. Ein Reduktionskatalysator Platin und Rhodium wird verwendet, um die NO-X -Konzentration im Abgas zu reduzieren. Wenn einer NO oder NO2 -Molekül im Abgas Katalysator wendet, ist das Stickstoffatom schnappte sich das Molekül und hielt sich an durch den Katalysator. Der Sauerstoff wird freigegeben und O2bildet. Das Stickstoffatom am Katalysator bindet mit einem anderen Stickstoffatom statt auf dem Katalysator, Form N2.
Katalysatoren haben stark die NOx aus Autoabgasen – bis zu 80 % Rabatt, Emissionen beim ordnungsgemäß durchführen. Sie funktioniert jedoch nur, wenn sie eine relativ hohe Temperatur erreicht haben. Daher ist bei einem Kaltstart eines Autos des Katalysators praktisch NOXentfernen. Es ist nicht bis der Katalysator erreicht höheren Temperaturen, dass sie effektiv die NO-X aus dem Abgasstrom entfernt. Katalysatoren funktionieren nicht für Diesel-Pkw aufgrund der mageren Bedingungen, unter denen sie arbeiten. Darüber hinaus wird der Schwefel im Dieselkraftstoff auch den Katalysator deaktiviert. Nr.X in Diesel-Motoren werden vor allem durch das Gas Abgasrückführung (AGR) Auslassventil, das kühlt die Temperatur der Verbrennungsgase reduziert. Diesel-Pkw emittieren demzufolge in der Regel mehr NOX als Benzinautos.

Abbildung 1: Charakteristische Färbung für Smog in Kalifornien in der Beige Cloud bank hinter der Golden Gate Brücke. Die braune Färbung resultiert aus der NOX in photochemischem Smog.
Grundsätze
In diesem Experiment werden die Konzentration von NOX in den Abgasstrom der verschiedenen Marken der automobilen zweimal gemessen (nach dem Einschalten und nach 10 min), die Möglichkeit der Auto-Katalysator, NOX aus dem Auspuff entfernen zu studieren. Der Katalysator erfordert eine hohe Temperatur um wirksam zu sein. Die Messung der Abgase beim Start des Autos stellt daher, die Menge an NOx in den Auspuff ohne Katalysator arbeiten. Es ist die Messung des Abgases nach 10 min den NOX im Abgas nach dem Katalysator darstellt.
NO-X -Konzentration wird durch Diazotierung von Sulfanilic Säure farbmetrisch bestimmt und anschließende Reaktion mit N-(1-naphthyl)-Ethylenediamine und Messung der Farbintensität der daraus resultierenden Azo Dye-Molekül mit einem UV-VIS Spektralphotometer eingestellt auf 550 nm.
In Lösung durchlaufen NO und NO2 die folgenden Reaktionen auf Nr.2–bilden:
2 NO3–(Aq) + H2O(l) → 2 H+(Aq) + NO2(g) und NO2–(Aq)
4NO(g) + O2(g) + 2 H2O(l) → 4 Nr2–(Aq) + 4 H+(Aq)
Zwar die erwartete Verhältnis zwischen Nr.2 und Nr.2– 2:1 bezogen auf die erste Gleichung, die zuvor aufgeführten, wurde es empirisch zu bestimmen, zu 1.39:1.
Wenn die Lösung Sulfanilic Säure und N-(1-naphthyl)-Ethylenediamine hinzugefügt werden, entwickelt sich ein pinkfarbenes Molekül (Abbildung 2).
Die Konzentration dieses rosafarbenen Moleküls ist direkt proportional zur Konzentration des NO-X in der Lösung. Die Konzentration des Moleküls Azo Farbstoff wird gemessen mit einer UV-VIS Spektralphotometer setzen bei 550 nm.
UV-VIS-Spektroskopie beruht auf der Messung der Absorption (A) von Lösungen, die in einem durchsichtigen Behälter der Breite b (in cm) statt. Die Konzentration der absorbierenden Spezies ist direkt proportional zu der Extinktion, wie in der folgenden Gleichung:
A =  b c
b c
wo  ist die molare Aufnahmefähigkeit. Diese Gleichung ist bekannt als Gesetz des Bieres. Die molare Aufnahmefähigkeit ist ein Maß dafür wie stark ein Stoff absorbiert Licht bei einer bestimmten Wellenlänge und ist eine Konstante für einen bestimmten Stoff.
ist die molare Aufnahmefähigkeit. Diese Gleichung ist bekannt als Gesetz des Bieres. Die molare Aufnahmefähigkeit ist ein Maß dafür wie stark ein Stoff absorbiert Licht bei einer bestimmten Wellenlänge und ist eine Konstante für einen bestimmten Stoff.
Um die Extinktion einer Lösung zu messen, ein Strahl von Licht mit Intensität Io richtet sich an die Lösung in einer Küvette (Abbildung 3). Die Intensität des Strahls eingeben (icho) und der aufstrebenden Strahl (I) werden gemessen, und die Extinktion wird berechnet, indem:


Abbildung 2. Ein Rosé-farbene-Molekül, das entsteht, wenn die Lösung Sulfanilic Säure und N-(1-naphthyl)-Ethylenediamine hinzugefügt werden.

Abbildung 3. Ein Lichtstrahl mit Intensität Io darauf abzielen, die Lösung in einer Küvette.
Verfahren
1. Vorbereitung der Stammlösung Nitrit (Nr.2–)
- 1,500 g NaNO2 wiegen Sie ab und verleihen Sie eine volumetrische 1-L-Flasche.
- Bis zur Markierung mit Nanopure Wasser verdünnen. (Überprüfen Sie das destillierte Wasser aus dem Wasserhahn – es kann genügend Nitrit um die Messungen stören.) Dadurch entsteht ein 1.000 µg NO2–-/mL-Stammlösung.
- Um 5,0 µg NO2–-/mL-Lösung, NO2 -/mL-Lösung 1 mL von 1.000 µg einnehmen und auf 200 mL in einem volumetrischen Kolben verdünnen.
2. Vorbereitung des NOX -Indikator-Lösung
- Wasserfreie Sulfanilic Säure 5,0 g wiegen Sie ab und in eine volumetrische 1-L-Flasche.
- 500 mL Nanopure Wasser hinzugeben.
- 140 mL Eisessig hinzugeben.
- Rühren Sie die Lösung mit einer rühren, bis die Sulfanilic Säure auflöst. Dies dauert ca. 30 Minuten.
- N-(1-naphthyl)-Ethylenediamine Dihydrochloride 0,020 g wiegen Sie ab und fügen Sie in den volumetrischen Kolben.
- Bis zur Markierung mit Nanopure Wasser verdünnen.
- Übertragen auf eine dunkle Flasche (um Photodecomposition zu verhindern) und Stöpsel fest (um Reaktion mit Luft zu vermeiden).
3. Vorbereitung des Kalibrierstandards
- 1,0 mL 5,0 µg NO2–-/mL-Lösung in eine volumetrische 25 mL-Fläschchen und mit der Nr.X Indikatorlösung bis zur Markierung verdünnen. Dies macht eine 0,2 µg NO2–-/mL-standard-Lösung.
- 2,0 mL 5,0 µg NO2–-/mL-Lösung in eine volumetrische 25 mL-Fläschchen und mit der Nr.X Indikatorlösung bis zur Markierung verdünnen. Dies macht eine 0,4 µg NO2–-/mL-standard-Lösung.
- 3,0 mL 5,0 µg NO2–-/mL-Lösung in eine volumetrische 25 mL-Fläschchen und mit der Nr.X Indikatorlösung bis zur Markierung verdünnen. Dies macht eine 0,6 µg NO2–-/mL-standard-Lösung.
- 4,0 mL 5,0 µg NO2–-/mL-Lösung in eine volumetrische 25 mL-Fläschchen und mit der Nr.X Indikatorlösung bis zur Markierung verdünnen. Dies macht eine 0,8 µg NO2–-/mL-standard-Lösung.
- 5,0 mL 5,0 µg NO2–-/mL-Lösung in eine volumetrische 25 mL-Fläschchen und mit der Nr.X Indikatorlösung bis zur Markierung verdünnen. Dies macht eine 1,0 µg NO2–-/mL-standard-Lösung.
4. Erstellung der Standardkurve
- Mit einem UV-VIS Spektralphotometer, setzen Sie das Instrument Extinktion zu lesen.
- Legen Sie die Wellenlänge auf 550 nm auf das Spektrophotometer.
- Verwenden die NO-X -Indikatorlösung, Null Spektralphotometer.
- Messen Sie die Absorption von 5 standard-Lösungen. Rekordwerte für die Datentabelle (Tabelle 1).
5. Auto Auspuff Probenmessung
- Starten Sie die dieselbetriebene Automobile.
- Mit einer 60 mL gasdichte Spritze, fügen Sie es ein paar Zoll in das Endrohr. Vermeiden Sie Verbrennungen und Dämpfe atmen Sie nicht ein. Ansaugen und Auspuff zweimal, um die Spritze Zustand zu vertreiben.
- Ziehen Sie die Indikatorlösung NOX 25 mL in die Spritze. Alle Luft aus der Spritze ohne Verschütten die Indikatorlösung zu vertreiben.
- Ziehen Sie 35 mL Auspuff in die Spritze, ziehen den Kolben, um die 60 mL-Markierung.
- Kappe der Spritze. Schütteln Sie die Lösung in der Spritze für 2 min. Abdeckung der Spritze mit Alu-Folie.
- Die Lufttemperatur in den Auspuff zu messen, wenn die Proben zu sammeln.
- Wiederholen Sie die Schritte 5.1-5.6 mit einem Benzin-Automobil. Diese Schritte können so oft wie gewünscht, mit verschiedenen Modellen von Automobilen wiederholt werden.
- Wiederholen Sie die Schritte 5.1-5.6 Nachdem die Automobile gelaufen haben mindestens 10 Minuten.
- Warten Sie 45 min um die Farbe vor der Messung der Extinktion der Lösung zu entwickeln, zu ermöglichen.
- Nach 45 min sind, das Gas aus der Spritze zu vertreiben, setzen Sie die Lösung in einer Küvette und messen die Extinktion mit dem Spektralphotometer setzen bei 550 nm. Rekordwerte für die Datentabelle (Tabelle 1).
| Probe | Extinktion |
| 0,2 µg NO2–/mL standard | |
| 0,4 µg NO2–/mL standard | |
| 0,6 µg NO2–/mL standard | |
| 0,8 µg NO2–/mL standard | |
| 1,0 µg NO2–/mL standard | |
| Diesel Auto Auspuff (beim Start) | |
| Diesel Auto Auspuff (nach 10 min laufen) | |
| Benzin Auto Auspuff (beim Start) | |
| Benzin Auto Auspuff (nach 10 min laufen) |
Tabelle 1. Leere Datentabelle auf Rekordwerte der Absorption.
Ergebnisse
Tabelle 2 enthält ein Beispiel für richtige Ergebnisse. Mit Hilfe der Extinktion Messungen von standard-Lösungen, werden ein Grundstück von Extinktion vs. Konzentration von2– vorgenommen (Abbildung 4). Dann kann die am besten passende Linie der Daten ermittelt werden. Mit der Best-fit Linie der Standardkurve, kann die Konzentration von NO2– in jeder unbekannten Lösung (µg/mL) berechnet werden. Dieser Wert kann die Konzentration von Nr.2 in der Auspuff gasförmigen Probe unter Verwendung der folgenden Gleichung konvertiert werden:
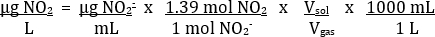
Basierend auf die ausgeglichene Gleichung NO2 H2O zuvor gesehen 2 Mol NO21 Mol, die NO2– -Verhältnis zu erwarten ist. In empirischen Experimenten wurde festgestellt näher ein 1.39:1 Verhältnis sein. Das Volumen der Lösung verwendet wurde 25 mL. Das Volumen der Gasprobe war 35 mL.
Die Konzentration von NO2 berechnet repräsentiert tatsächlich alle NO-X in der Abgas-Probe (Tabelle 3). Die Formel für die Umrechnung zwischen PpmV und µg/L hängt von der Temperatur und Druck, bei denen die Proben entnommen wurden. Die Umwandlung Gleichung lautet:

Wo R = allgemeine Gaskonstante = 0.08206 atm· L/Mol· K, P = atmosphärischer Druck in atm, T = Temperatur in K und MW = Molekulargewicht von NOX (als Nr.2) = 46.01 g/Mol. Daher
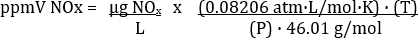
Es ist wichtig, Eingang T in K und P in atm.
| Probe | Extinktion |
| 0,2 µg NO2–/mL standard | 0,22 |
| 0,4 µg NO2–/mL standard | 0,43 |
| 0,6 µg NO2–/mL standard | 0,60 |
| 0,8 µg NO2–/mL standard | 0.79 |
| 1,0 µg NO2–/mL standard | 1.05 |
| Diesel Auto Auspuff (beim Start) | 1.03 |
| Diesel Auto Auspuff (nach 10 min laufen) | 1.03 |
| Benzin Auto Auspuff (beim Start) | 0.10 |
| Benzin Auto Auspuff (nach 10 min laufen) | 0,04 |
Tabelle 2. Datentabelle mit repräsentativen Ergebnisse der Absorption.

Abbildung 4. Eine Standardkurve Grundstück der Extinktion vs. Konzentration von NO2–.
| Fahrzeug | NOX -Konzentration (ppm) |
| Diesel-Pkw (beim Start) | 500 |
| Diesel-Pkw (nach 10 Minuten laufen) | 500 |
| Benziner (beim Start) | 48 |
| Benzinauto (nach 10 Minuten laufen) | 21 |
Tabelle 3. NOX -Konzentration (ppm) pro Fahrzeug.
Anwendung und Zusammenfassung
Die Messung von Nitrit mit der modifizierten Saltzman Reaktion ist sehr üblich und nützlich in vielen verschiedenen Bereichen. Wie beschrieben, kann die Methode verwendet werden, um NOX -Konzentrationen in Luftproben – Autoauspuff, Laborräume, Luftqualität in Städten usw. zu messen. Darüber hinaus kann diese Methode verwendet werden, um NOX im Zigarettenrauch zu überwachen. Das Verfahren wäre dieses Experiment sehr ähnlich, außer statt Autoabgasen in die Spritze, Zigarettenrauch angesaugt werden würde. Oft gibt es eine höhere Konzentration an NOx Zigarette Rauch als er aus dem Auspuff von Automobilen, die dazu neigt, die viele überraschen. Typische Werte für NOX in Zigarettenrauch reichen von 500-800 ppm.
Diese Methode kann auch verwendet werden, testen Sie die Ebenen von Nitrat in Anwesenheit von Nitrifikation Bakterien produziert. Nitrifikation Bakterien befinden sich in Boden und Wasser und spielen eine wichtige Rolle im Stickstoffkreislauf – Oxidation von Ammoniak zu Nitrit und dann Nitrat. Das Nitrat in der Probe wird zunächst durch das Enzym-Nitrat-Reduktase zu Nitrit umgewandelt. Dann wird das Nitrit mit der modifizierten Saltzman Reaktion gemessen. Zu guter Letzt kann diese Methode zur Bestimmung der Konzentration von Nitraten und Nitriten in Lebensmitteln verwendet werden. Nitrite und Nitrate werden hauptsächlich zu Fleisch und Fleischerzeugnissen zu bewahren Lebensmitteln zugesetzt. Ein typischer Wert für Nitrit in Wurstwaren ist etwa 125 µg/mL.
pringen zu...
Videos aus dieser Sammlung:

Now Playing
Bestimmung von NOX in Autoabgasen mittels UV/Vis-Spektroskopie
Environmental Science
30.1K Ansichten

Identifikation von Bäumen: Wie man einen dichotomen Bestimmungsschlüssel verwendet
Environmental Science
81.3K Ansichten

Analyse der Baumzusammensetzung eines Waldes
Environmental Science
49.4K Ansichten

Verwendung von GIS zur Untersuchung urbaner Forstwirstschaft
Environmental Science
12.6K Ansichten

Polymerelektrolytbrennstoffzelle
Environmental Science
22.1K Ansichten

Biokraftstoffe: Herstellung von Ethanol aus Zellulose-Material
Environmental Science
53.3K Ansichten

Tests für gentechnisch veränderte Lebensmittel
Environmental Science
89.8K Ansichten

Trübung und Trockenmasse in Oberflächengewässern
Environmental Science
35.9K Ansichten

Gelöster Sauerstoff im Wasser
Environmental Science
55.8K Ansichten

Nährstoffe in aquatischen Ökosystemen
Environmental Science
38.9K Ansichten

Messung von bodennahem Ozon
Environmental Science
26.5K Ansichten

Bleianalyse von Böden mittels Atomabsorptionsspektroskopie
Environmental Science
125.5K Ansichten

Kohlenstoff und Stickstoff-Analyse von Umweltproben
Environmental Science
29.5K Ansichten

Nährstoffanalyse des Bodens: Stickstoff, Phosphor und Kalium
Environmental Science
216.0K Ansichten

Analyse der Regenwurm-Populationen im Boden
Environmental Science
16.5K Ansichten
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten