Method Article
Überwachung des Ubiquitin-Proteasom-Aktivität in lebenden Zellen unter Verwendung eines Degron (DGN)-destabilisiert Green Fluorescent Protein (GFP)-basierte Reporter Protein
In diesem Artikel
Zusammenfassung
Eine Methode, um Ubiquitin-Proteasom-Aktivität in lebenden Zellen zu überwachen beschrieben. A Degron-destabilisierten GFP-(GFP-DGN) und eine stabile GFP-dgnFS Fusionsprotein erzeugt und transduziert in die Zelle mit einem lentiviralen Expressionsvektor. Diese Technik ermöglicht eine stabile GFP-dgn/GFP-dgnFS exprimierenden Zelllinie, in dem Ubiquitin-Proteasom-Aktivität leicht beurteilt werden kann, mit Epifluoreszenz oder Durchflusszytometrie generieren.
Zusammenfassung
Proteasome ist der wichtigste intrazelluläre Organellen in den proteolytischen Abbau von abnormal, fehlgefalteten, beschädigte oder oxidierte Proteine 1, 2 beteiligt. Wartung der Proteasom-Aktivität wurde in vielen wichtigen zellulären Prozessen beteiligt, wie Zelle Stressantwort 3, Regulation des Zellzyklus und Zelldifferenzierung 4 oder Reaktion des Immunsystems 5. Die Dysfunktion des Ubiquitin-Proteasom-System hat zu der Entwicklung von Tumoren und neurodegenerativen Krankheiten 4, 6 in Verbindung gebracht. Zusätzlich wurde eine Abnahme der Proteasom-Aktivität als Funktion der zellulären Seneszenz und organismal Alterung 7, 8, 9, 10 gefunden. Hier präsentieren wir eine Methode, um Ubiquitin-Proteasom-Aktivität in lebenden Zellen mit einem GFP-dgn Fusionsprotein zu messen. Um Ubiquitin-Proteasom-Aktivität in lebenden primären Zellen zu überwachen, konstruiert komplementäre DNA, die für ein grün fluoreszierendes Protein (GFP)-dgn Fusionsprotein (GFP-dgn, instabil) und eine Variante Tragen einer Frameshift-Mutation (GFP-dgnFS, stabil 11) werden in lentiviralen Expressionsvektoren insertiert. Wir bevorzugen diese Technik gegenüber herkömmlichen Transfektionstechniken weil es eine sehr hohe Transfektionseffizienz garantiert unabhängig von dem Zelltyp oder dem Alter des Spenders. Der Unterschied zwischen der Fluoreszenz, die von GFP-dgnFS (stabilen) Protein und dem destabilisierten Protein (GFP-dgn) in Abwesenheit oder Gegenwart von Proteasom-Inhibitor angezeigt kann zum Ubiquitin-Proteasom-Aktivität in jeder bestimmten Zellstamm abzuschätzen. Diese Unterschiede können durch Epifluoreszenzmikroskopie überwacht werden können oder mittels Durchflusszytometrie gemessen werden.
Protokoll
Ein. Plasmidkonstruktion
- Um individuelle Oligonucleotide Codierung für dgn (ACKNWFSSLSHFVIHL 11) und zum dgnFS (HARTGSLACPTSSSICE) und ligieren es in den pEGFP-C1-Vektor, um die Fusion des GFP mit dgn / dgnFS (Abbildung 1) zu erhalten.
- Amplify die kodierende Sequenz für GFP-DGN-und GFP-dgnFS mittels PCR nach dem Protokoll des pENTR Directional TOPO Cloning Kit und fahren mit dem pLenti6/V5 Directional TOPO Cloning Kit (Abbildung 6).
2. Virusproduktion
- Am Tag vor der Transfektion (Tag 1) Samen aus HEK 293FT Zellen in einem T75-Flaschen, so daß sie 90-95% konfluent auf dem Tag der Transfektion sein wird.
- Am Tag der Transfektion zu verdünnen 36 ul Lipofectamin 2000 Reagent in 1,5 ml DMEM ohne Serum und Antibiotika in einem 15 ml Falcon. Verwenden Sie einen anderen 15 ml Falcon und verdünnen 3 ug pLenti6/V5 Durchführung der komplementäre DNA-Konstrukt entweder für GFP -DGN-oder GFP-dgnFS, 2,5 ug Umschlag kodierenden Plasmid pMD2.G und 7,5 ug Vektor-Rückgrat psPAX2 in 1,5 ml DMEM ohne Serum und Antibiotika. Nach 5 min die verdünnte DNA wird mit der verdünnten Lipofectamin 2000 Reagenz kombiniert.
- Inkubieren des Gemisches für 20 min bei Raumtemperatur, um die DNA-Lipofectamin-Komplexe zu bilden ermöglichen.
- Entfernen Sie das Medium HEK 293FT Zellen, ersetzen Sie es sorgfältig von 7 ml Medium (ohne Antibiotika) und fügen Sie die DNA-Lipofectamin Mischung in den Kolben und Rock hin und her für das Mischen (Tag 2). Inkubieren Sie die Kolben über Nacht bei 37 ° C in einer befeuchteten 5% CO 2-Inkubator.
- Ändern Medium am nächsten Tag (10 ml Medium ohne Antibiotika-Tag 3).
- Nach 48 Stunden (Tag 5) Ernte Überstand Zentrifuge bei 300 xg für 5 min bei Raumtemperatur und filtern den Überstand durch einen 0,45 um PVDF-Filter.
Kulturmedium - DMEM (HEK 293FT)
Zelt "> DMEM10% FBS
0,1 mM MEM NEAA
6 mM L-Glutamin
1 mM MEM Natriumpyruvat
1% Pen-Strep (optional)
500 ug / ml Geneticin (optional)
3. Viruskonzentration durch Polyethylenglykol (PEG) Niederschlag
- Hinzufügen einem Volumen Polyethylenglykol-Lösung (50 mM Polyethylenglycol, 41 mM NaCl, Autoklaven, pH = 7,2; PEG) bis vier Volumina des Überstandes und inkubiere während 2 Stunden bei 4 ° C. Vorsichtig mischen Sie es alle 20-30 min durch Invertieren.
- Abzentrifugieren bei 1500 × g für 30 min bei 4 ° C. Ein weißes Pellet sichtbar sein soll.
- Überstand und zentrifugieren bei 1500 × g für 5 min bei 4 ° C. Saugen Sie den verbleibenden PEG-Lösung.
- Das Pellet in Medium oder phosphatgepufferter Salzlösung (PBS) durch Auf-und Abpipettieren und kräftig Vortex für 20 bis 30 Sekunden. Als Richtwert verwenden 500 ul für eine T75-Flasche und Aliquot auf 100 ul. Bewahren Sie das Virus bei -80 ° C.
4. Titrierung von Virus
- Saatgut aus 5 × 10 4 U2-OS-Zellen in jede Vertiefung einer Platte mit 6 Vertiefungen am Tag vor der Transfektion.
- Am Tag der Transfektion entfernen Kulturmedium und ersetzen Sie sie durch 1 ml DMEM mit 8 ug / ml Polybren (Hexadimethrinbromid). Verdünnen der konzentrierten Virusüberstand 1:10 und 1:100 und fügen Sie 1 ul jeweils ein gut. Für höhere Viruskonzentrationen verwenden 1 ul, 5 ul und 10 ul konzentrierter Virusüberstand für die restlichen Brunnen. Eine Vertiefung wird als positive Kontrolle gelassen.
- Am folgenden Tag ersetzt das Medium durch 2 ml DMEM.
- Beginnen Sie mit der Auswahl des nächsten Tages. Übernehmen 10 ug / ml Blasticidin auf jedem gut. Ersetzen Sie das Antibiotikum enthaltenden Medium jeden zweiten Tag.
- Etwa 6-7 Tage nach Beginn der Selektion werden die transduzierten Zellen tot sind. Für die Färbung Waschen Sie die Zellen dreimal mit PBS und decken die Zellen mit Kristallviolett (10 mg / l Kristallviolettin 20% Ethanol) und Inkubation für 5 bis 10 min bei Raumtemperatur. Aspirate Kristallviolett (kann ein paar Mal wiederverwendet werden) und spülen Sie die Vertiefungen zweimal mit ddH 2 O und trocknen Sie die Platte.
- Zählen Sie die Kolonien und mehrfach mit 1.000 und der entsprechenden Verdünnung (Abbildung 7). Dieses Verfahren ermöglicht die Transfektion Einheiten (TU) des Virus / ml zu berechnen.
Kulturmedium - DMEM (HFF-2/U2-OS)
DMEM
10% FBS
6 mM L-Glutamin
1% Pen-Strep
5. Transduktion von humanen diploiden Fibroblasten (Diese Prozedur kann für jeden Zelltyp verwendet werden.)
- Seed von 5 × 10 4 menschliche diploide Fibroblasten (HDF) bis 6-Well-Platten am Tag vor Transduktion.
- Verwenden eine Multiplizität der Infektion von zwei zusammen mit 8 ug / ml Polybren als Transduktion Enhancer in einer Gesamtmenge von einem Milliliter.
- Ändern Medium am nächsten Tag.
- WennDie Zellen werden bei 70-80% der Konfluenz Beginn die Auswahl mit 10 ug / ml Blasticidin. Nach der Auswahl abgeschlossen ist (nicht mehr transfizierten Zellen sterben) die Expansion der Zellen beginnen kann und die Zellen sind bereit für Experimente. Chronische Auswahl mit Blasticidin ermöglicht, eine stabile Zelllinie überexprimierenden GFP-dgn oder GFP-dgnFS Fusionsproteine bereit Proteasomenaktivität messen erzeugen. Dieses Verfahren garantiert einen sehr hohen Transfektionseffizienz unabhängig vom Zelltyp.
6. Messung durch Durchflusszytometrie
- Seed von 1 × 10 5 Zellen (Buchwert entweder GFP-DGN-oder GFP-dgnFS) am Tag vor dem Experiment.
- Saures Kontrollzellen 3 Stunden vor der Messung mit der Proteasom-Inhibitor, z. B. 100 g / ml LLnL.
- Zweimal mit PBS waschen und Ernte der Zellen mit 0,5 ml Trypsin. So stoppen Sie die Trypsinierung verwenden 4,5 ml Kulturmedium und übertragen die Zellen in ein 15 ml Falcon.
- Spin ter Zellen bei 300 xg für 5 Minuten bei Raumtemperatur.
- Absaugen Medium, werden die Zellen in PBS und drehen sich wieder bei 300 × g für 5 min bei 37 ° C.
- Absaugen PBS, in 400 ul FACS-Puffer (10 mM Hepes, 140 mM NaCl, 2,5 mM CaCl 2, pH = 7,4) resuspendiert und übertragen die Zellen in FACS-Röhrchen.
- Halten Sie die Zellen auf Eis und messen Proben mittels Durchflusszytometrie. Die Zellen sollten nicht mehr als 30 min bei 4 ° C gelagert werden
7. Repräsentative Ergebnisse
Das GFP-Fusionsprotein dgn trägt eine Sequenz, die das Proteasom und damit das Protein sofort abgebaut abzielt, sie entspricht der Abnahme der GFP-Fluoreszenz-Signal. Die Frameshift Mutante (GFP-dgnFS) eine mutierte Version dieser Sequenz und nicht abgebaut wird durch Proteasom, sie führt die höhere grünen Fluoreszenz. Aus diesen Gründen transduzierten junge HDFs mit erwarteten hohen Proteasom-Aktivität und mit GFP-dgn zeigen eine gering (6% positive Zellen) Fluoreszenzsignal sowohl Durchflusszytometrie Messung und in Epifluoreszenz (2A und B, Abbildung 3). Das gleiche HDFs transduziert mit GFP-dgnFS anzuzeigen 39,7% der positiven Zellen. Die Behandlung der Zellen mit Proteasom-Inhibitor LLnL (N-Acetyl-L-leucyl-L-leucyl-L-norleucinal) angehoben das Signal zu maximal 62,9% in beiden, GFP-dgn und GFP-dgnFS Zellen (2A und B ).
Um mögliche Rückgang der Proteasom-Aktivität bei älteren menschlichen Hautproben zu bestimmen, wurden Fibroblasten von jungen, mittleren Alters und alte Spendern isoliert mit GFP-DGN-und GFP-dgnFS infiziert, wie oben beschrieben und kultiviert auf die gleiche Passage-Nummer vor der Analyse mittels Durchflusszytometrie Zytometrie. In diesen Experimenten Spender eine klare Zunahme der GFP-Signal zwischen jungen Menschen (11,2 ± 0,88% GFP-positive Zellen) und mittleren Alters (20,4 ± 2,27% GFP-positiven Zellen, P = 0,003) beobachtet wurde, was auf eine Abnahme proteasome Aktivität in Proben aus alten Spendern 7 (Abbildung 4). Keine weitere Abnahme der Proteasom-Aktivität wurde in Fibroblasten von ältesten Individuen (Abbildung 4) getrennt beobachtet. Fluoreszenzintensität für GFP-dgnFS betrug in allen Fällen ca. 90% (Daten nicht gezeigt), zeigt einen hohen Transfektionseffizienz für die drei verschiedenen Altersgruppen.

Abbildung 1. Die GFP-DGN-und GFP-dgnFS Sequenz. Angezeigt wird das 3'-Ende des GFP (grün) die multiple Klonierungsstelle des pEGFP-CL1 Vektor (grau) und der DGN / dgnFS Sequenz (rot).
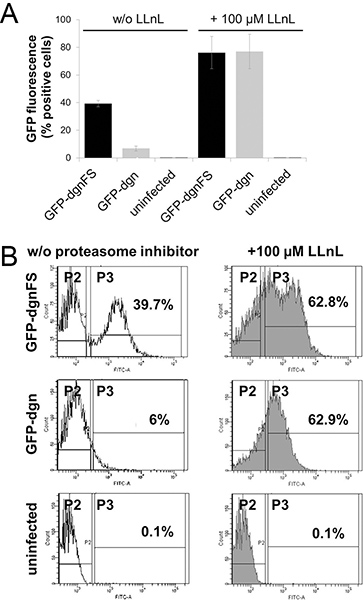
Abbildung 2. Durchflusszytometrie-Analyse der GFP-DGN-und GFP-dgnFS menschliche diploide Fibroblasten. A. Young humane Vorhautfibroblasten (HFF-2) wurden mit lentivirale Vektoren, die ein grün fluoreszierendes Protein infiziert (GFP)-Gen oder ein dgn GFP-dgnFS (Frameshift) zu konstruieren, wie angegeben und analysiert GFP-Fluoreszenz unter Verwendung von Durchflusszytometrie (FACS Canto II, Becton Dickinson) analysiert. Wo angegeben, wurden die Zellen auch für 3h mit Proteasom-Inhibitor N-Acetyl-L-leucyl-L-leucyl-L-norleucinal (LLnL) behandelt. Nichtinfizierten Zellen wurden als Kontrolle verwendet. Experimente wurden in dreifacher Ausführung durchgeführt. B. Daten sind repräsentativ für drei unabhängige Experimente. Die Zahlen spiegeln die Menge an GFP-positiven Zellen. Klicken Sie hier für eine größere Abbildung zu sehen .
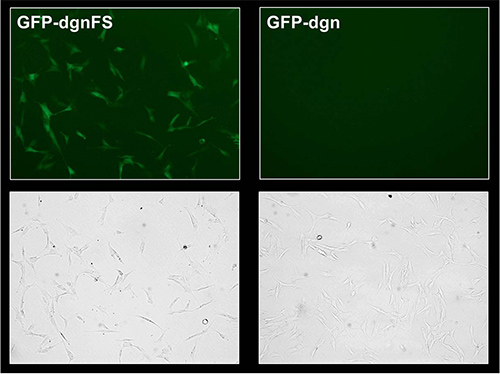
Abbildung 3. Fluoreszenzmikroskopie Analyse von GFP-dgn und GFP-dgnFS HFF-2-Zellen. Junge HFF-2 wurden wie in Abbildung 2 behandelt. Um 9 Tage nach der Infektion wurden die Zellen visualized durch Fluoreszenz und Phasenkontrast-Mikroskopie.
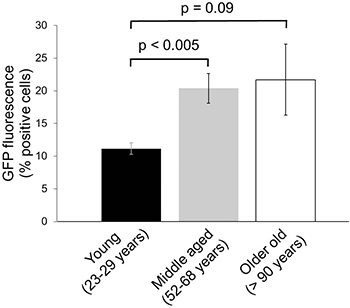
Abbildung 4. Änderungen im Proteasom-Aktivität in menschlichen Hautalterung. Die menschlichen Vorhautfibroblasten aus neun verschiedenen Spendern in den angegebenen Altersgruppen wurden minimal erweitert und infiziert mit lentiviralen Konstrukte Codierung für GFP-dgn. Um 9 Tage nach der Infektion wurden die Zellen durchflusszytometrisch analysiert. Die Daten wurden auf drei Proben pro Altersgruppe in Duplikaten (± SE) erhalten.
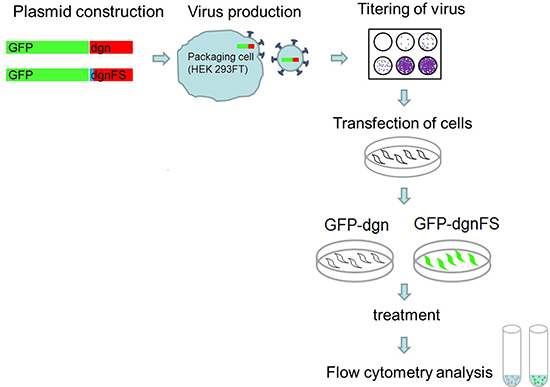
Abbildung 5. Experimentellen Ansatz. Custom-Oligonukleotide für die DGN und dgnFS in den pEGFP-C1-Vektor kloniert und Viren werden für jedes Konstrukt mit HEK 293FT Zellen produziert. Der Titer der Viren bestimmt. Zellen mit dem Virus transduziert und erweitert. Nach der bevorzugte Behandlung die Zellen werden analysiertfür Fluoreszenzsignal durch Durchflusszytometrie.
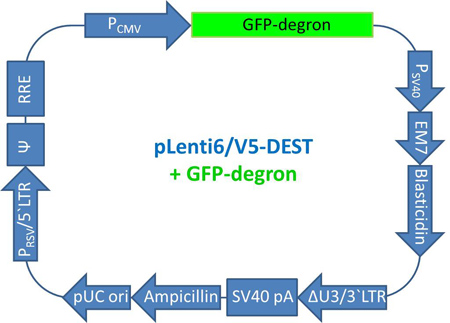
Abbildung 6. Karte von Plenti GFP-dgn. Die Karte des pLenti6/V5-DEST Vektor, der GFP-dgn Sequenz angezeigt wird. Abkürzungen: PCMV (CMV-Promotor), GFP-dgn (Sequenz von GFP-DGN), P SV40 (SV40 early Promotor), EM7 (EM7 Promotor), Blasticidin (Blasticidin Resistenzgen), ΔU3 / 3'LTR (3'LTR mit deletierte U3-Region), SV40 pA (SV40 Polyadenylierungssignal), Ampicillin (Ampicillin-Resistenz-Gen), pUC ori (pUC), PRSV / 5'LTR (RSV / 5'LTR Hybrid-Promotor), Ψ (HIV-1 Ψ Verpackungssignal ), RRE (HIV-1-Rev-Response-Element).
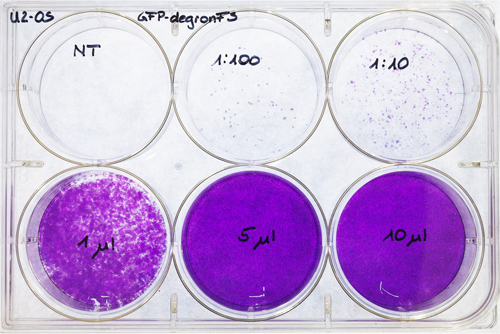
Abbildung 7. U2-OS Titerung Platte. U2-OS wurden auf einer 6-well-Platte ausgesät und transfiziert mit verschiedenen Virus-Konzentrationen (Verdünnung von 1/100 und 1/10, 1, 5 und 10 ul der Zusammenarbeitncentrated viralen Überstand). Ein gut als transfizierten Kontrolle (NT) eingesetzt. Nach 6-7 Tagen wurden die Zellen mit Kristallviolett angefärbt und luftgetrocknet.
Diskussion
Die erste Veröffentlichung mit grün fluoreszierendem Protein (GFP) als Reporter Substrat für Ubiquitin-Proteasom-Aktivität wurde in 2000 12 veröffentlicht. Seitdem hat GFP zu einem gemeinsamen Instrument zur zellulären Aktivitäten, insbesondere das Ubiquitin-Proteasom-Prozess zu visualisieren. Um Ubiquitin-Proteasom-Aktivität in vivo zu überwachen ein transgenes Mausmodell mit einem GFP-basierte Reporter wurde 13 eingeführt. Zusätzliche in vivo Forschung etabliert anderes transgenes Mausmodell mit einer ähnlichen Degron-destabilisierten GFP-Reporter in dieser Publikation 14 verwendet.
Leider hat GFP als Reporter einige Unvollkommenheit der durch Dantuma et al gezeigt wurde. Und Bowman et al. 12,15. Erstens kann destabilisierten GFP ohne die Hemmung der Proteasom aus unbekannten Gründen akkumulieren. Da das Ubiquitin-Proteasom-Maschinen ist ein System, dessen Funktion ist abhängig von mehreren Schritten, adisturbance vor dem Abbau kann zur Anreicherung des Reportersubstrats und führen zu falsch-positiven Auswirkungen 12 führen. Zweitens sind GFP-basierte Reporter Substrate aufgrund ihrer kurzen Halbwertszeiten empfindlich auf Änderungen in der Transkription und Übersetzung. Jede Änderung in GFP-Fluoreszenz kann somit ein Ergebnis verringert oder erhöht Synthese und Übersetzung 15 sein. Diese Probleme wurden in anderen Studien durch Modifikationen GFP angesprochen wie folgt:
Proteasomenaktivität erwies sich bei der zellulären Seneszenz und organismal Alterung 7, 8, 9, 10 verringert werden. Auf dem Gebiet der Alternsforschung, liegt der Fokus vor allem auf die Beseitigung von oxidierten Proteinen, wo das Proteasom spielt eine wichtige Rolle, und es gibt keine schlüssigen Beweise dafür, dass Protein Ubiquitin Abbau vorangeht in diesem Fall 2. Frühere Arbeiten haben gezeigt, dass die Verwendung von GFP mit einem mutierten nichtspaltbare Ubiquitin-Teil geeignet ist, den komplexen Vorgang der p studierenrotein Abbau 16. Dieses GFP-Konstrukt die Möglichkeit gibt Proteasomenaktivität ohne die potentiellen Einfluss auf seine Aktivität über Störungen im Ubiquitin Maschinen überwachen.
In dieser Arbeit verwendeten wir eine Degron-destabilisierten GFP-basierte Reporter Protein (GFP-dgn) an Ubiquitin-Proteasom-Aktivität in lebenden menschlichen diploiden Fibroblasten zu überwachen. Um einen Überblick über die Transfektionseffizienz, die Funktionalität und die Transkription / Translation Ebenen des GFP-dgn Reporter haben, wurden mehrere geeignete Kontrollen eingeschlossen. Wir haben junge unbehandelten GFP-dgn transfizierten Fibroblasten zu zeigen, dass es fast keine grüne Fluoreszenz sichtbar und Proteasom-Funktion wird nicht beeinflusst. Um zu bestätigen, dass die Signalleitungen steigt mit der Inhibition des Proteasoms, wir GFP-transfizierten Fibroblasten dgn behandelt mit einem Proteasom-Inhibitor, um die Ansammlung von GPF nach Hemmung sehen. Als dritte Kontrolle übernehmen wir verwendet GFP-dgnFS. Mit diesem Konstrukt können wir die overall Transfektionseffizienz, die von der Zelle Stamm Zellstamm und mit allen drei Kontrollen haben wir einen Überblick über die Syntheserate der Konstrukte innerhalb der Zelle unterscheiden können.
Die hier vorgestellte Methode ermöglicht dem Anwender, schnell und einfach messen die Ubiquitin-Proteasom-Aktivität in lebenden Zellen. Eine stabile Überexpression des GFP-Reporter Substrat kann mit verschiedenen Techniken 17 erreicht werden. In dieser Veröffentlichung wird die Transfektion des GFP-dgn cDNA in die Zellen durch lentiviralen welches eine stabile Expression erzielt bietet. Darüber hinaus ermöglicht die Verwendung dieses Systems hohe Transfektionseffizienz unabhängig von der Zelltyp, Zell-Stoffwechsel-Zustand oder Alter des Spenders 7. Wir haben erfolgreich diese Protokoll verwendet, um DNA zu den Endothelzellen, in denen andere Verfahren der Transfektion fehlgeschlagen 18 einzuführen. Dennoch zeigte früheren Experimenten, dass die Zellen, die länger in Kultur expandiert eine geringere Fluoreszenz-DisplaySignal als frisch transfizierte Zellen möglicherweise aufgrund der längeren Selektionsdruck.
Die PEG-Fällung wird der Titer der Transformieren Einheiten pro ml (TU / ml) zu erhöhen. Wenn gute Titer erreicht werden (über 5 × 10 5 TU / ml) kann der PEG-Fällung verzichtet. Ein wichtiger Schritt bei der PEG-Fällung ist kräftigem Aussetzung oder Pipettieren erzeugt Luftblasen zu vermeiden. Es kann inaktivieren die Viruspartikel und deutlich verringern Transfektionseffizienz.
Bei Verwendung Proteasom-Inhibitoren a priori Experimente durchgeführt werden. Die Endkonzentration verwendet und Inkubationszeit sind Zelltyp abhängig und muss experimentell ermittelt werden. Frühere Beobachtungen auf HFF-2-Zellen zeigte, dass 3h Inkubation mit nicht LLnL sollte wegen 1 überschritten werden), die toxischen Auswirkungen der Inhibitor 2) zu hoch GFP-Signal, die erreicht werden kann, oder 3) Nebenwirkungen des Proteasomenhemmung über längere time Perioden.
Offenlegungen
Keine Interessenskonflikte erklärt.
Danksagungen
Diese Studie wurde gefördert durch: National Research Network on Aging (NFN S93) von der österreichischen Science Foundation (FWF), Europäische Kommission Integrierte Projekte MiMAGE und PROTEOMAGE, Niederlande Genomics Initiative / Niederländische Organisation für wissenschaftliche Forschung (NGI / NWO, 05040202 und 050 - 060-810 NHG), das EU Network of Excellence Lebensdauer (FP6 036.894) finanziert und Innovation Oriented Research Program am Genomics (SenterNovem; IGE01014 und IGE5007).
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes | Firma | Katalog-Nummer | |
| pEGFP-C1 Vektor | BD Bioscience Clontech | 6084-1 | |
| pENTR Directional TOPO Cloning Kit | Invitrogen | K2400-20 | |
| pLenti6/V5 Directional TOPO Cloning Kit | Invitrogen | V496-10 | |
| Lipofectamine 2000 Reagent | Invitrogen | 11668019 | |
| DMEM | Sigma | D5546 | |
| PVDF-Filter (Rotilabo-Spritzenfilter) | Roth | P667.1 | |
| Polyethylenglykol | Sigma | P2139 | |
| NaCl | Merck | 1.06404.1000 | |
| Dulbeccos Phosphat-gepufferte Saline 1x (PBS) | Invitrogen | 14190 | |
| Hexadimethrinbromid | Sigma | 10,768-9 | |
| Blasticidin | Invitrogen | R21001 | |
| Kristallviolett | Sigma | C3886 | |
| FACS-Röhrchen | BD Biosciences | ||
| Penicillin Streptomycin (Pen-Strep) | Invitrogen | 15140130 | |
| L-Glutamin 200 mM | Invitrogen | 25030024 | |
| Fötales Rinderserum (FBS) | Biochrom AG | S0115 | |
| MEM Non-Essential Amino Acids (NEAA) 100x | Invitrogen | 11140035 | |
| MEM Natriumpyruvat 100 mM | Invitrogen | 11360039 | |
| D-(+)-Glucose (45%) | Sigma | G8769 | |
| Geneticin | Invitrogen | 11811023 | |
| CaCl2 | Merck | C5080 | |
| Hepes | Sigma | H3375 | |
| Trypsin-EDTA (0,05%) | Invitrogen | 25300054 |
Referenzen
- Coux, O., Tanaka, K., Goldberg, A. L. Structure and functions of the 20S and 26S proteasomes. Annu. Rev. Biochem. 65, 801-847 (1996).
- Davies, K. J. Degradation of oxidized proteins by the 20S proteasome. Biochimi. 83, 301-310 (2001).
- Stangl, K., Stangl, V. The ubiquitin-proteasome pathway and endothelial (dys)function. Cardiovasc. Res. 85, 281-290 (2009).
- Tuoc, T. C., Stoykova, A. Roles of the ubiquitin-proteosome system in neurogenesis. Cell Cycle. 9, 3174-3180 (2010).
- Rock, K. L., et al. Inhibitors of the proteasome block the degradation of most cell proteins and the generation of peptides presented on MHC class I molecules. Cell. 78, 761-771 (1994).
- Lehman, N. L. The ubiquitin proteasome system in neuropathology. Acta Neuropathol. 118, 329-347 (2009).
- Koziel, R., Greussing, R., Maier, A. B., Declercq, L., Jansen-Durr, P. Functional Interplay between mitochondrial and proteasome activity in skin aging. J. Invest. Dermatol. 131, 594-603 (2010).
- Grillari, J., Grillari-Voglauer, R., Jansen-Durr, P. Post-translational modification of cellular proteins by ubiquitin and ubiquitin-like molecules: role in cellular senescence and aging. Adv. Exp. Med. Biol. 694, 172-196 (2010).
- Bulteau, A. L., Szweda, L. I., Friguet, B. Age-dependent declines in proteasome activity in the heart. Arch. Biochem. Biophys. 397, 298-304 (2002).
- Strucksberg, K. H., Tangavelou, K., Schroder, R., Clemen, C. S. Proteasomal activity in skeletal muscle: A matter of assay design, muscle type, and age. Anal. Biochem. , (2009).
- Bence, N. F., Sampat, R. M., Kopito, R. R. Impairment of the ubiquitin-proteasome system by protein aggregation. Science. 292, 1552-1555 (2001).
- Dantuma, N. P., Lindsten, K., Glas, R., Jellne, M., Masucci, M. G. Short-lived green fluorescent proteins for quantifying ubiquitin/proteasome-dependent proteolysis in living cells. Nat. Biotechnol. 18, 538-543 (2000).
- Lindsten, K., Menendez-Benito, V., Masucci, M. G., Dantuma, N. P. A transgenic mouse model of the ubiquitin/proteasome system. Nat. Biotechnol. 21, 897-902 (2003).
- Liu, J., et al. Impairment of the ubiquitin-proteasome system in desminopathy mouse hearts. FASEB J. 20, 362-364 (2006).
- Bowman, A. B., Yoo, S. Y., Dantuma, N. P., Zoghbi, H. Y. Neuronal dysfunction in a polyglutamine disease model occurs in the absence of ubiquitin-proteasome system impairment and inversely correlates with the degree of nuclear inclusion formation. Hum. Mol. Genet. 14, 679-691 (2005).
- Myung, J., Kim, K. B., Lindsten, K., Dantuma, N. P., Crews, C. M. Lack of proteasome active site allostery as revealed by subunit-specific inhibitors. Mol. Cell. 7, 411-420 (2001).
- Menendez-Benito, V., Heessen, S., Dantuma, N. P. Monitoring of ubiquitin-dependent proteolysis with green fluorescent protein substrates. Methods Enzymol. 399, 490-511 (2005).
- Lener, B., et al. The NADPH oxidase Nox4 restricts the replicative lifespan of human endothelial cells. Biochem. J. 423, 363-374 (2009).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten