Method Article
制备,纯化和磁共振成像造影剂的使用稀土配合物的表征
摘要
我们展示metalation,净化,稀土配合物的特性。这里所描述的复合物,可以结合大分子,使这些分子利用磁共振成像进行跟踪。
摘要
常用Polyaminopolycarboxylate基于配体螯合稀土离子,并由此产生的复合物作为磁共振成像(MRI)造影剂。许多市售的配体是特别有用,因为它们包含的功能组别,允许快速,高纯度和高产通过胺反应活性酯和异硫氰酸团体或巯基反应马来酰亚胺的大分子和生物分子共轭。虽然这些配体metalation bioconjugation化学细微的差别,在metalation程序方面的常识,必须考虑选择金属起始原料时。此外,纯化及鉴定的存在,并选择最有效的程序的多个选项部分取决于起始材料的选择。这些细微的差别往往被忽视发布的协议。在这里,我们的目标是展示metalation,纯化和特性,可作为MRI(图1)造影剂使用的稀土配合物的常用方法。我们期望本出版物将使生物医学科学家将其纳入自己的常用反应剧目稀土络合反应,由宽松的起始材料和净化方法的选择。
研究方案
1。 Metalation使用LnCl 3盐
- 溶解在水中的配体产生30-265 mM的解决方案。在这个视频配体2 - (4 - isothiocyanatobenzyl)-二乙三胺五乙酸(P - SCN - BN - DTPA的)浓度在73毫米。
- 通过添加1个M NH 4 OH解决配体的pH值调整到5.5和7.0之间。在这段视频中,1米的NH 4 OH溶液0.2毫升。
- 溶解于水1-2 LnCl 3等值5-1000 mM的浓度与生产的解决方案。在这个视频,EuCl 3和GdCl 3分别用浓度为111毫米。过量的金属经常被用来驱动metalation来完成,从而简化了净化。
- 边搅拌边添加LnCl 3配体的解决方案解决方案。
- 此外LnCl 3后,调整所产生的反应混合物的pH值在5.5和7.0之间,加入0.2 M NH 4 OH。共0.5毫升0.2 M NH 4 OH溶液中使用这个视频。如果您的配体中含有酸敏感的官能团,在这一步调整pH值多次。注意 - 如果的解决方案就显得太基本,任何敏感的基地功能组别,如异硫氰酸盐,将被渲染为共轭无法使用。
- 监视器通过pH值测量的反应。反应完成后,当pH值保持不变。
2。提高pH值workup(不包括在这个视频,但无基敏感官能团配体的良好)
- 加浓氨水反应混合物中,调整pH值≥11 。这一步将不溶于水的氢氧化物沉淀为任何不拔的金属。
- 通过0.2微米的过滤器的过滤上清。如果反应混合物堵塞过滤器,离心过滤前调迁建议。
- 如果将不会被执行透析,除去溶剂,减少压力(旋转蒸发或建议冷冻干燥)下。
- 如果仍然免费稀土,可重复步骤2.1-2.3。
3。透析workup
- 透析管切割到适当的长度(按照制造商的指引)举行的样本量,同时留出额外的长度(约10%的样本量)。在这段视频中,一个100-500道尔顿分子量(MWCO)切断膜,但如果接合之前,执行metalation较大的截留分子量管,可酌情使用。此外,透析磁带可用于透析管的替代品,如果需要的话。
- 如果合适的基础上制造商的指引,在水中浸泡切透析管,在环境温度为15分钟。
- 装满水(透析液)透析水库(1升烧杯中,在本视频中使用)。透析液量应约100倍的样品。
- 折叠一端油管两次透析封钳油管安全的折叠部分。包装用橡皮筋封,以确保它仍然是封闭的透析过程中结束。
- 反应混合物通过0.2微米的过滤器过滤,滤液装入小心不要撕破管材管的开口端。一定要留下足够的头部空间,关闭油管。
- 油管剩余的开口端折两次,安全与封闭,封闭包装与步骤3.4橡皮筋。
- 安装一个玻璃小瓶,含有空气透析管,使用橡皮筋的一端钳。将一小瓶含沙的其他钳。这些小瓶确保管子留在透析液中浸泡。
- 将包含透析液透析水库管。
- 搅拌透析液中,用磁力搅拌盘速度缓慢,在环境温度(无震荡)。
- 变化的透析超过一天的课程(在此视频中,透析液改变为2.5,6.5,11.5 h)的3倍,然后让透析继续隔夜(20-28 h透析)。
- 从透析液中取出的透析管,小心地打开一个封闭取出样品。洗净透析管水3倍,并与样品相结合的洗涤。
- 卸下减压下的水。冷冻干燥是在这个视频。
4。评估自由金属的存在
- 金属配合物溶解在醋酸缓冲液(缓冲液配制:溶解在400毫升的水1.4毫升醋酸,调节pH至5.8,用1 M NH 4 OH,并加水产生总量为500 mL),并添加二甲酚橙指示剂在pH 5.8的缓冲(16微米)。在这个视频,0.3毫克复杂是0.3缓冲液溶解,并加入3毫升指示剂。
- 检测自由金属通过观察一个指标的颜色从黄色紫色变化。
- 如果需要,可用金属量可量化的创建校准曲线1。另外,染料偶氮胂III可以用来代替二甲酚橙2。如果免费的金属仍然存在,样品应进一步纯化,使用前透析,脱盐柱,高效液相色谱(HPLC)来表征。
5。测定水协调的数量(Q )
- 准备一个解决方案,欧盟三复杂的含H 2 O(〜1毫米),另一个在D 2 O的浓度相同的解决方案分析之前,必须在D 2 O解决方案蒸干,溶解在D 2 O 3次,以去除残留的H 2 O
- 水溶液加入到一个干净的比色皿,试管放入一个分光光度计。
- 执行的激发和发射扫描,以确定每个(〜395 nm和〜595纳米,分别)千里马。
- 执行一个磷光时间衰变实验,使用下列参数:激发和发射波长从初始延迟(0.01毫秒),步骤5.3中,激发和发射狭缝宽度(5纳米),闪光次数(100),最大延迟时间(13毫秒),确定和延迟增量(0.1毫秒)。这些条件是合适的,但最络合物的最大延迟和增量值可以增加或极长或极短的衰减时间下降的物种。
- 重复步骤5.4步骤5.1准备与D 2 O解决方案。
- 从5.4和5.5获得的发光衰减数据,情节强度随时间变化的的自然对数。这些线的斜率衰减率(τ- 1)(图2) 。在这段视频中,Microsoft Excel 2007中使用生成的原始数据的自然对数图。霍罗克斯和他的同事(EQ)3开发的公式中使用的衰变率。如果您的配体中含有OH或NH组协调,以金属,则方程必须修改使用前3。
公式1: 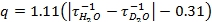
6。弛豫测量
- 选择弛豫时间分析仪所需的应用模式 :T 1(纵向弛豫时间) 或 T 2(横向弛豫时间)。
- 准备了一系列的样品含有不同浓度的含钆三 ,在水溶剂的复杂。在这段视频中,水被用作溶剂和解决方案为10.0,5.00,2.50,1.25,0.625,0毫米准备。其他水溶剂或缓冲区可以使用,但重要的是要使用的溶剂为空白。样品的最终体积是针对正在使用的仪器。
- 样品放置在仪器,让它坐5分钟,以平衡仪器的温度(37℃,在此视频)。
- 通过调整软件的参数,以获得平滑指数曲线为 T 1 或 T 2(代 表为 T 1 和 T 2曲线如图3所示),确定弛豫时间(s为单位) 。
- 所有样本包括空白,重复步骤6.3和6.4。
- 计算测 T 1 或 T 2值,单位为s - 1时的倒数。
- 绘制T 1 -1 或 T 2 -1与GD 第三浓度值(单位为mm)。由于III含钆复合物的吸湿性质, 确认第三钆的浓度,用原子吸收光谱法或电感耦合等离子体质谱。拟合直线的情节。代表图如图4所示。
- 拟合直线的斜率是弛豫(T 1 和 T 2分别为R 1 或 R 2)和MM -1 s - 1时的单位。
7。代表性的成果
已包括在这个协议的步骤有代表性的数据表和数字部分。除了在协议中所描述的情况下,协调水的数量和弛豫特性,重要的是要使用标准的化学技术的最终产品的特点。该化合物的身份可以得到使用,和有代表性的质谱质谱显示钆三同位素诊断模式- 欧盟III -含有复合物,如图5所示。此外,非钆三 含稀土配合物,核磁共振光谱可用于产品标识。为了描述复杂的纯度,高效液相色谱,元素分析,或两者都可以使用。
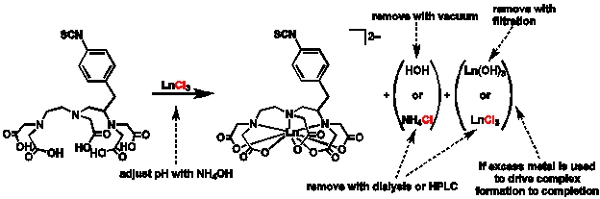
图1总体方案metalation和净化:计划描绘的一般程序metalation和用于选择不同的净化路线的原因。

图2发光强度的情节:代表的强度与时间从第5的自然对数的情节。用于生成水和D 2 O解决方案获得类似的曲线线条的斜坡式1来表征水配位数的欧盟III含络合物。
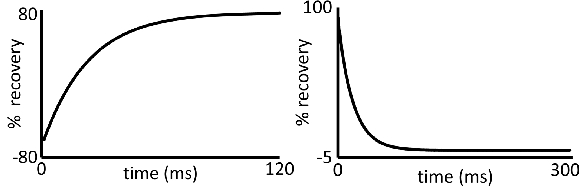
图3:松弛的衰减时间曲线:(左)T 1和(右)T 2采集有代表性的数据。从这些曲线形状的偏差,会产生不可靠的数据。
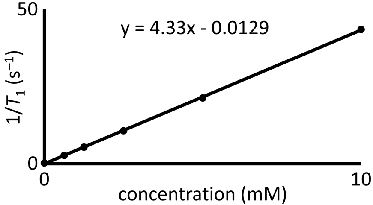
图4弛豫决心:一个有代表性的情节与浓度钆三 :1 / T 1。拟合直线的斜率是弛豫和MM -1 s - 1时的单位。
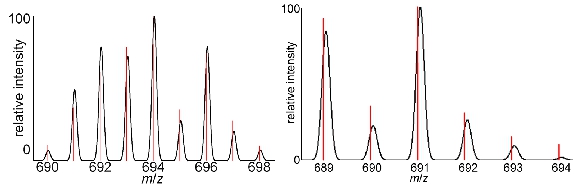
图5质谱:代表质谱诊断同位素模式(左)钆三含复合物和(右)欧盟III含有复合物。黑色的高斯峰代表理论同位素分布,红色线是实际的数据。
讨论
鉴于越来越多的出版物,包括镧系元素的造影剂4-14,这是重要的准备,净化和表征产品,以确保重现性好,比较的结果,采取照顾。这些复合物通常被认为是具有挑战性的净化和表征有机分子由于其顺磁性质和任何可以使用bioconjugation的功能组别的敏感性相对。我们已经描述了稀土配合物的合成,纯化,并表征的常用方法。然而,选择其中一种方法时,重要的是要考虑的具体制度,正在研究。
络合反应,可使用各种市售的金属盐类,盐的选择取决于研究的目的。例如,使用氯(或三氟或硝酸盐)盐的优点是比较温和的条件下对温度的要求。然而,这些方法都需要仔细监测的pH值,作为副产品生产的盐。如果所研究的系统是特别敏感,pH值的变化,然后仔细的监测和控制pH值,必须执行。此外,如果盐的副产品会损害正在研究的系统,他们必须被删除或替代合成应使用。随着稀土氧化钾(或氧化物)起始原料,必须在更高的温度下使用,因为这些物种的溶解度低,但metalation唯一的副产品是水。此方法是理想的反应,将很难淡化,但它不会对温度敏感的系统工作。还值得一提的是,这些metalation反应金属和配体的浓度是非常强大的。浓度范围列在第一部分中跨度浓度范围内,我们可以在文献中找到。
此外周到的金属起始原料的选择,重要的是要强调,无论是金属和配体可能有密切关联的水和溶剂分子,即使他们出现干燥。这些额外的分子往往不够,极大地扭曲反应的化学计量。因此,它是有帮助的特点起始原料(元素分析),因此,在反应中使用这些材料的准确金额。
在这篇文章中,我们强调保持反应混合物的pH值的重要性。这个pH值控制是关键的,因为多个方面的反应可能会失败,如果pH值允许近中性偏离。配体羧酸metalation反应发生,必须去质子(近中性或较高的pH值),而稀土离子必须留可溶性(近中性或较低的pH值)。如果pH值过高,稀土离子的不溶性的氢氧化复合物会沉淀,并停止反应。另外,如果pH值太低,羧酸仍将质子和配体不会协调的金属。此外,在极端的pH值,反应性官能团分解,呈现复杂的走向后续bioconjugation反应的惰性。为了进一步使问题复杂化,作为metalation发生反应,反应混合物的pH值降低羧酸去质子化。虽然metalation的pH值的平衡可能会出现复杂的,它可以很容易地控制基地仔细此外。
有许多细微的差别metalation战略。在这篇文章中,我们选择来形容使用多余的金属。这也是可以接受的超额配体或配体和金属(起始材料元素分析的基础上)的等值金额。每条路线的优点和局限性。主要优点是使用多余的金属,配体往往是最昂贵的起始原料,这种方法可以节省资金。然而,当金属过量使用,去除多余的金属是至关重要的,因为任何一个自由的金属,可以显着地影响重要的属性,包括弛豫和毒性。如果对水透析是不够的,以去除多余的金属,对柠檬酸缓冲液透析,可以执行删除柠檬酸缓冲液与水的透析其次。另外,一个脱盐柱或HPLC可以被用来只要小心,以确保流动相的pH中立用于。当配体过量使用,不再是迫切需要删除多余的金属和超额配体可能不会影响弛豫;然而,自由配体将继续。对于后续bioconjugation反应,这多余的配体可以是有问题的,结果是难以分开的不均匀的共轭。要解决此问题,金属比赛LEXES可以无水乙醚或高效液相色谱法可用于单独的超额配体的金属配合物沉淀。理想的情况下,配体和金属将被用来以1:1的比例在没有金属或基于配体的副产品。然而,元素分析为起始原料是前所需的每一个反应,如果有一个1:1的配体对金属的比例稍有偏差,那么反应会陷入要么配体过量或金属过量的类,在需要净化。
我们已经证明metalation产生复杂的准备bioconjugation 15-17。这一战略的另一种方法是首先由metalation 18,19配体和生物分子的共轭。这个共轭然后metalate战略,相同的因素在metalation路线(pH敏感性和温度敏感性的生物分子,以及从盐净化产品的能力)作出决定时需要考虑的。
披露声明
致谢
我们非常感谢来自韦恩州立大学(MJA),从美国的老龄化研究(SMV)基金会的赠款,并以独立职业过渡奖(R00EB007129)来自国家生物医学成像研究所和国家研究院生物的途径启动资金卫生(MJA)。
材料
| Name | Company | Catalog Number | Comments |
| 试剂和仪器 | 公司 | 目录编号 | |
|---|---|---|---|
| EuCl 3•6H 2 O | Sigma - Aldrich公司 | 203254 - 5G | |
| P - SCN - BN - DTPA | Macrocyclics | B - 305 | |
| 氢氧化铵 | 电解二氧化锰 | AX1303 - 3 | |
| 光谱/ POR生物纤维素酯(CE)的透析膜 - 500 ð截留分子量 | Fisher Scientific则 | 68-671-24 | |
| Millipore公司IC Millex - LG过滤单元 | Fisher Scientific则 | SLLG C13 NL | |
| 二甲酚橙四钠盐 | 阿法埃莎 | 41379 | |
| 乙酸 | Fluka公司 | 49199 | |
| D 2 O | 剑桥同位素实验室公司 | DLM - 4 - 25 | |
| 净水器 | ELGA | Purelab超 | |
| 高效液相色谱法和质谱 | 日本岛津 | LCMS - 2010EV | |
| 弛豫时间分析仪 | 布鲁克 | mq60 minispec | |
| 紫外可见分光光度计 | Fisher Scientific则 | 20-624-00092 | |
| 冷冻干燥机 | Fisher Scientific则 | 10-030-133 | |
| 酸度计 | HANNA INSTRUMENTS | 您好221 | |
| 分光光度计 | HORIBA Jobin Yvon公司 | Fluoromax - 4 | |
| 分子量计算器马修梦露6.46版本,下载2009年10月17日,日 | http://ncrr.pnl.gov/software/ | 分子量计算器 |
参考文献
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Med. Mol. Imaging. 1, 184-188 (2006).
- Nagaraja, T. N., Croxen, R. L., Panda, S., Knight, R. A., Keenan, K. A., Brown, S. L., Fenstermacher, J. D., Ewing, J. R. Application of arsenazo III in the preparation and characterization of an albumin-linked, gadolinium-based macromolecular magnetic resonance contrast agent. J. Neurosci. Methods. 157, 238-245 (2006).
- Supkowski, R. M., Horrocks, W. D. On the determination of the number of water molecules, q, coordinated to europium(III) ions in solution from luminescence decay lifetimes. Inorg. Chim. Acta. 340, 44-48 (2002).
- Menjoge, A. R., Kannan, R. M., Tomalia, D. A. Dendrimer-based drug and imaging conjugates: design considerations for nanomedical applications. Drug Discovery Today. 15, 171-185 (2010).
- Que, E. L., Chang, C. J. Responsive magnetic resonance imaging contrast agents as chemical sensors for metals in biology and medicine. Chem. Soc. Rev. 39, 51-60 (2010).
- Uppal, R., Caravan, P. Targeted probes for cardiovascular MR imaging. Future Med. Chem. 2, 451-470 (2010).
- Major, J. L., Meade, T. J. Bioresponsive, cell-penetrating, and multimeric MR contrast agents. Acc. Chem. Res. 42, 893-903 (2009).
- Datta, A., Raymond, K. N. Gd-hydroxypyridinone (HOPO)-based high-relaxivity magnetic resonance imaging (MRI) contrast agents. Acc. Chem. Res. 42, 938-947 (2009).
- León-Rodríguez, L. M. D., Lubag, A. J. M., Malloy, C. R., Martinez, G. V., Gillies, R. J., Sherry, A. D. Responsive MRI agents for sensing metabolism in vivo. Acc. Chem. Res. 42, 948-957 (2009).
- Castelli, D. D., Gianolio, E., Crich, S. G., Terreno, E., Aime, S. Metal containing nanosized systems for MR-molecular imaging applications. Coord. Chem. Rev. 252, 2424-2443 (2008).
- Caravan, P., Ellison, J. J., McMurry, T. J., Lauffer, R. B. Gadolinium(III) chelates as MRI contrast agents: structure, dynamics, and applications. Chem. Rev. 99, 2293-2352 (1999).
- Lauffer, R. B. Paramagnetic metal complexes as water proton relaxation agents for NMR imaging: theory and design. Chem. Rev. 87, 901-927 (1987).
- Yoo, B., Pagel, An overview of responsive MRI contrast agents for molecular imaging. Front. Biosci. 13, 1733-1752 (2008).
- Pandya, S., Yu, J., Parker, D. Engineering emissive europium and terbium complexes for molecular imaging and sensing. Dalton Trans. 23, 2757-2766 (2006).
- Nwe, K., Xu, H., Regino, C. A. S., Bernardo, M., Ileva, L., Riffle, L., Wong, K. J., Brechbiel, M. W. A new approach in the preparation of dendrimer-based bifunctional diethylenetriaminepentaacetic acid MR contrast agent derivatives. Bioconjugate Chem. 20, 1412-1418 (2009).
- Nwe, K., Bernardo, M., Regino, C. A. S., Williams, M., Brechbiel, M. W. Comparison of MRI properties between derivatized DTPA and DOTA gadolinium-dendrimer conjugates. Bioorg. Med. Chem. 18, 5925-5931 (2010).
- Caravan, P., Das, B., Deng, Q., Dumas, S., Jacques, V., Koerner, S. K., Kolodziej, A., Looby, R. J., Sun, W. -C., Zhang, Z. A lysine walk to high relaxivity collagen-targeted MRI contrast agents. Chem. Commun. , 430-432 (2009).
- León-Rodríguez, L. M. D., Kovacs, Z. The synthesis and chelation chemistry of DOTA-peptide conjugates. Bioconjugate Chem. 19, 391-402 (2008).
- Boswell, C. A., Eck, P. K., Regino, C. A. S., Bernardo, M., Wong, K. J., Milenic, D. E., Choyke, P. L., Brechbiel, M. W. Synthesis, characterization, and biological evaluation of integrin αVβ3-targeted PAMAM dendrimers. Mol. Pharm. 5, 527-539 (2008).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。