Method Article
Tükenme Yöntemi Kullanılarak Çözelti Dağılmış İnorganik Nano partiküller üzerine Kısa Peptit Adsorpsiyon Çalışması
Bu Makalede
Özet
Biyomolekül-inorganik solid faz etkileşimini kavramanın ilk adımı, adsorpsiyon izamları oluşturularak değerlendirilebilecek temel fizikokimyasal sabitleri ortaya çıkarmaktır. Sıvı fazdan adsorpsiyon kinetik, yüzey kapasitesi, pH ve rekabetçi adsorpsiyon ile sınırlıdır, hepsi bir adsorpsiyon deneyi ayarlamadan önce dikkatli bir şekilde dikkate alınmalıdır.
Özet
İnorganik-organik etkileşimlerin temelleri, biyoteknoloji ve tıpta kullanıma uygun yeni biyoarayüzlerin keşfi ve geliştirilmesinde kritik öneme sahiptir. Son çalışmalar proteinlerin sınırlı adsorpsiyon siteleri aracılığıyla yüzeylerle etkileşime girdiğini göstermektedir. Amino asitler ve peptidler gibi protein parçaları karmaşık biyolojik makromoleküller ve inorganik yüzeyler arasındaki etkileşim modellemeiçin kullanılabilir. Son otuz yılda, bu etkileşimlerin fiziksel kimya temellerini ölçmek için birçok geçerli ve hassas yöntem geliştirilmiştir: izoversal titrasyon kalorimetresi (ITC), yüzey plazmon rezonansı (SPR), kuvars kristal mikrodengesi (QCM), total iç yansıma floresansı (TIRF) ve zayıflatılmış toplam yansıma spektroskopisi (ATR).
Adsorpsiyon ölçümü için en basit ve en uygun teknik, çözelti dağılmış sorbent ile temas tan sonra sorbat konsantrasyonundaki (tükenme) değişimin hesaplandığı ve adsorbe edildiği varsayıldığı tükenme yöntemidir. Tükenme verilerine dayalı adsorpsiyon istermmleri tüm temel fizikokimyasal verileri sağlar. Ancak, çözümlerden elde edilen adsorpsiyon, yüksek spesifik yüzey alanına sahip kinetik kısıtlamalar ve sorbentler nedeniyle daha uzun denge süreleri gerektirir ve bu da onu makroskopik sabit düzlem yüzeylere neredeyse uygulanamaz hale getirir. Ayrıca, sols istikrarsızlığı gibi faktörler, nanopartikül agregalar, sorbent kristallik, nanopartikül boyutu dağılımı, çözeltinin pH, ve adsorpsiyon için rekabet, adsorbing peptidler çalışırken dikkate alınmalıdır. Tükenme verileri isotherm inşaat kelimenin tam anlamıyla her çözünür sorbat için kapsamlı fiziksel kimya verileri sağlar ama pahalı kurulumları gerektirmez gibi, en erişilebilir metodoloji kalır. Bu makalede, inorganik oksit üzerinde peptit adsorpsiyon deneysel çalışma için temel bir protokol açıklar ve süreci etkileyen tüm kritik noktaları kapsar.
Giriş
Son 50 yıldır inorganik yüzeyler ve peptidler arasındaki etkileşim, malzeme bilimi ve tıptaki yüksek önemi nedeniyle büyük ilgi çekmiştir. Biyomedikal araştırma uyumluluk ve biyoinorganik yüzeylerin stabilitesi üzerinde durulmuş, hangi rejeneratif tıp için doğrudan etkileri var, doku mühendisliği1,2,3, ve implantasyon4,5,6,7. Sensörler ve aktüatörler gibi çağdaş biyoduyarlı cihazlar, oksit yarı iletken yüzeyler8 ,89,,10,11,12,13üzerinde hareketsiz fonksiyonel proteinler dayanmaktadır. Protein üretimi için modern arıtma uygulamaları genellikle aşağı saflaştırma ve ayırma biyomolekül etkileşim özelliklerine dayanır14.
Birden fazla inorganik oksitler arasında, titanyum dioksit biyolojik olarak ilgili substratlar 15 ,,16ile birlikte en çok kullanılan kalır.15 TiO2tabanlı biyoarayüzler alanında yapılan araştırmalar, biyolojik ve yapısal özelliklerini değiştirmeden protein ve peptidlerin güçlü ve spesifik bağlanmasını oluşturmaya odaklanmıştir. Sonuçta, ana hedefi titanyum tabanlı biyoteknolojik ve tıbbi uygulamaların oluşturulmasını ilerletecek yüksek stabilite ve artan işlevsellik ile biyomoleküllerin yüksek yüzey yoğunluğu tabakası17.
Titanyum ve alaşımları birkaç nanometre kalınlığında bir yüzey TiO2 tabakası korozyona dayanıklı ve birçok in vivo uygulamalarda biyouyumluluk yüksek düzeyde sergiler çünkü en az altı yıldır bir cerrahi implant malzemesi olarak yaygın olarak kullanılmaktadır18,19,20. Titanyum dioksit de yaygın olarak biyomineralizasyon üretilen bir inorganik substrat olarak kabul edilir, burada çekirdekleşme ve inorganik faz büyüme proteinler ve peptidler ile birlikte umut verici katalitik ve optik özellikleri ile malzeme sağlayabilir21,22,23,24.
Genel olarak inorganik maddeler ve biyomoleküller arasındaki etkileşimin yüksek önemi ve özellikle protein-TiO2 etkileşimleri göz önüne alındığında, TiO2'dekiproteinlerin adsorpsiyonunun manipülasyonu ve kontrolüne yönelik birçok araştırma yapılmıştır. Bu çalışmalar nedeniyle, bu etkileşimin bazı temel özellikleri ortaya çıkmıştır, adsorpsiyon kinetik gibi, yüzey kapsama, ve biyomolekül konformasyonu, biyoarayüzler daha fazla gelişmeler için önemli destek veren5,13.
Ancak, protein karmaşıklığı tam belirlenmesi ve inorganik yüzeyler ile bir proteinmoleküler düzeyde etkileşimin anlaşılması önemli kısıtlamalar ekler. Biyomoleküllerin sınırlı bölgeler aracılığıyla inorganik yüzeylerle etkileşime girdiği varsayılmaktadır, bilinen yapıları ve amino asit dizileri ile bazı proteinler bileşenlerine-peptidlere ve ayrı ayrı incelenen amino asitlere indirgenmiştir. Bu peptidlerin bazıları önemli aktivite göstermiştir, onları önceki protein ayırma 25 gerek kalmadan adsorpsiyon çalışmaları benzersiz bir konu yapma25,26,27,28,29,30.
TiO2 veya diğer inorganik yüzeylerde peptid adsorpsiyonunun nicel karakterizasyonu, son birkaç on yıldır biyomoleküller için özel olarak uyarlanmış fiziksel yöntemlerle gerçekleştirilebilir. Bu yöntemler arasında izoversmal titrasyon kaloriferi (ITC), yüzey plazmon rezonansı (SPR), kuvars kristal mikrodengesi (QCM), toplam iç yansıma floresansı (TIRF) ve zayıflatılmış total yansıma spektroskopisi (ATR), bunların hepsi de anahtar termodinamik veriler sağlayarak adsorpsiyon mukavemetinin saptanmasına olanak sağlar: Bağlama sabiti, Gibbs serbest enerji, entalpi ve entropi31.
Biyomoleküllerin inorganik maddeye adsorpsiyonu iki şekilde gerçekleştirilebilir: 1) ITC ve tükenme yöntemi sabit makroskopik yüzeylere bağlanan bir çözeltiiçinde dağılmış parçacıklar kullanır; 2) SPR, QCM, TIRF ve ATR, sırasıyla altın kaplı cam veya metal yongaları, kuvars kristalleri, çinko sülfür kristalleri ve PMMA yongaları gibi inorganik madde ile modifiye edilmiş makroskopik yüzeyler kullanır.
İzotermit titrasyon kaloriferi (ITC), çözeltilerin veya heterojen karışımların titrasyonu nda üretilen veya tüketilen ısıyı ölçen etiketsiz fiziksel bir yöntemdir. Hassas kalorimetrik hücreler 100 nanojoule kadar küçük ısı etkilerini algılar, nanopartikül yüzeylerde adsorpsiyon ısıölçümü mümkün hale. Sürekli ek-titrasyon sırasında sorbattermal davranış, etkileşim intalpi ortaya tam bir termodinamik profil sağlar, bağlama sabiti, ve belirli bir sıcaklıkta entropi32,33,34,35,36.
Yüzey plazmon rezonans (SPR) spektroskopisi, çalışılan yüzeye yakın bir ortamda ortamın kırılma indisi ölçümüne dayanan yüzeye duyarlı bir optik tekniktir. Geri dönüşümlü adsorpsiyon ve adsordi tabaka kalınlığını izlemek için gerçek zamanlı ve etiketsiz bir yöntemdir. Bağlama sabiti ilişkilendirme ve ayrışma oranlarından hesaplanabilir. Farklı sıcaklıklarda yapılan adsorpsiyon deneyleri aktivasyon enerjisinin sıcaklık bağımlılığı ve sırayla diğer termodinamik parametreler hakkında bilgi sağlayabilir37,38,39.
Kuvars kristal mikrodengesi (QCM) yöntemi, adsorpsiyon ve desorpsiyon işlemleri sırasında piezoelektrik kristallerin salınım sıklığındaki değişimi ölçer. Bağlama sabiti adsorpsiyon ve desorpsiyon oranı sabitlerinin oranından değerlendirilebilir. QCM göreli kütle ölçümleri için kullanılır ve bu nedenle, hiçbir kalibrasyon25,,27,,40ihtiyacı . QCM hem gaz hem de sıvı dan adsorpsiyon için kullanılır. Sıvı tekniği QCM çeşitli modifiye yüzeylerde birikimi tanımlamak için bir analiz aracı olarak kullanılmasını sağlar41.
Toplam iç yansıma floresansı (TIRF), dahili olarak yansıyan evanescent dalgaları ile heyecanlanan adsoresan floresanlarının ölçümüne dayanan hassas bir optik interfasiyal tekniktir. Bu yöntem, yüzeyi kaplayan floresan moleküllerin onlarca nanometre sırasına göre kalınlıklarla algılanmasını sağlar, bu nedenle çeşitli yüzeylerde makromoleküler adsorpsiyon çalışmasında kullanılır42,43. Adsorpsiyon ve desorpsiyon üzerine floresan dinamikleri yerinde izleme adsorpsiyon kinetik ve dolayısıyla termodinamik veri42,43sağlar.
Zayıflatılmış toplam yansıma (ATR) Roddick-Lanzilotta tarafından lizin adsorpsiyon izomları 1.600 ve 1.525 cm-1lizin spektral bantları dayalı kurmak için kullanılmıştır. Bu TiO2 bir peptid için bağlayıcı sabit in situ kızılötesi yöntemi44kullanılarak tespit edildi ilk kez. Bu teknik polilizin peptidler45 ve asidik amino asitler için adsorpsiyon izamlarının oluşturulmasında etkili olmuştur46.
Adsorpsiyon parametresi yerinde ölçüldüğü yukarıda belirtilen yöntemlerin aksine, geleneksel bir deneyde adsorbe biyomoleküllerin miktarı, yüzey çözeltiyle temas ettikten sonra konsantrasyon değişimi ile ölçülür. Bir sorbat konsantrasyonu adsorpsiyon vakalarının büyük bir çoğunluğunda çürür çünkü, bu yöntem tükenme yöntemi olarak adlandırılır. Konsantrasyon ölçümleri, sorbate içsel bir analitik özelliğine veya 47 ,48,,49,48,50 veya türevleştirme51,52 bunların içsel bir analitik özelliğine dayalı olabilir doğrulanmış bir analitik test gerektirir.
QCM, SPR, TIRF veya ATR kullanılarak yapılan adsorpsiyon deneyleri, adsorpsiyon çalışmaları için kullanılan çiplerin ve sensörlerin özel yüzey hazırlanmasını gerektirir. Hazırlanan yüzeyler bir kez kullanılmalı ve oksit yüzeyinin kaçınılmaz hidrasyonu veya bir sorbat olası chemisorption nedeniyle adsorbat değiştirilince değişiklik gerektirir. ITC, QCM, SPR, TIRF veya ATR kullanılarak aynı anda yalnızca bir örnek çalıştırılabilirken, tükenme yönteminde miktar sadece termostat kapasitesi ve sorbent kullanılabilirliği ile sınırlı olan düzinelerce numune çalıştırılabilir. Bu özellikle büyük örnek toplu işveya biyoaktif moleküllerin kütüphaneleri işlenirken önemlidir. Daha da önemlisi, tükenme yöntemi pahalı ekipman gerektirmez, sadece bir termostat gerektirir.
Ancak, bariz avantajlarına rağmen tükenme yöntemi hantal görünebilir karmaşık prosedür özellikleri gerektirir. Bu makalede, tükenen tükenme yöntemini kullanarak TiO2'de dipeptit adsorpsiyonunun kapsamlı bir fizikokimyasal çalışmasının nasıl yapılacağını sunar ve araştırmacıların ilgili deneyler icra ederken karşılaşabilecekleri sorunları ele alın.
Protokol
1. Dipeptit stok çözeltilerinin ve seyreltmelerinin hazırlanması
- 16 mM dipeptid çözeltisinin hazırlanması
- Steril polimerik test tüpüne 0,183 g dipeptid (Ile-His) (Bkz. Malzeme Tablosu)yerleştirin, çift distile su (DDW) ile 35 mL'ye seyreltin ve oda sıcaklığında (RT) kuvvetli karıştırma altında çözünün.
NOT: Dipeptit karıştırırken DDW'de çözünmezse, dipeptit çözeltisini ultrasonik banyoya yerleştirin ve birkaç dakika sonicate verin. - Steril test tüpünde 50 mL DDW'de 0,533 g kuru2-(N-morolino)etanesülfonik asiterolarak 2-(N -morolino)etanesülfonik asit eriterek 2-(N -morolino)etanesulfonik asit inşite 2-(N -morolino)etanesulfonik asfere 50 mM çözeltisi hazırlayın.N DDW'nin 100 mL'inde 200 mg sodyum hidroksit eriterek 50 mM sodyum hidroksit çözeltisi hazırlayın.
- Önceden çözülmüş dipeptid çözeltisinin pH'ını, 50 mM MES veya 50 mM sodyum hidroksiti 16 mM dipeptid çözeltisine dikkatlice ekleyerek 7,4'e ayarlayın, RT'de karıştırın ve pH metre ile pH'ı izleyin. pH'ı ayarladıktan sonra çözeltiyi bir ölçüm silindirine dökün, test tüpünü durulayın ve ölçüm silindirini DDW ile 40 mL'ye doldurarak 16 mM'lik son konsantrasyonu yapın.
- Steril polimerik test tüpüne 0,183 g dipeptid (Ile-His) (Bkz. Malzeme Tablosu)yerleştirin, çift distile su (DDW) ile 35 mL'ye seyreltin ve oda sıcaklığında (RT) kuvvetli karıştırma altında çözünün.
- 16 mM stok çözeltisinden dipeptit seyreltmelerinin hazırlanması
- 16 mM dipeptid çözeltisini DDW ile seyrelterek 0,4 ile 12,0 mM arasında konsantrasyonlarda peptid seyreltmeleri hazırlayın. Örneğin, 8 mM dipeptit çözeltisi hazırlamak için 16 mM dipeptid çözeltisinin 10 mL'sine 7 mL DDW ddw ekleyin. Seyreltmeden sonra pH'ı 50 mM MES veya 50 mM NaOH damla damladılarak dipeptit çözeltisine ekleyerek 7,4'e ayarlayın (bkz. adım 1.1.3). pH'ı ayarladıktan sonra çözeltiyi bir ölçüm silindirine dökün, test tüpünü durulayın ve dipeptit konsantrasyonu 8 mM yapmak için ölçüm silindirini DDW ile 20 mL'ye kadar doldurun.
NOT: 16 mM dipeptit stok çözeltisinin 0.4, 0.8, 1.2, 1.6, 2.0, 3.0, 4.0, 8.0 ve 12.0 mM konsantrasyonları ile diğer seyreltmeleri Şekil 1'egöre hazırlanır. Her dipeptit çözeltisinin pH'ın 7.4'e ayarlanması adım 1.1.3'te açıklanmıştır.
- 16 mM dipeptid çözeltisini DDW ile seyrelterek 0,4 ile 12,0 mM arasında konsantrasyonlarda peptid seyreltmeleri hazırlayın. Örneğin, 8 mM dipeptit çözeltisi hazırlamak için 16 mM dipeptid çözeltisinin 10 mL'sine 7 mL DDW ddw ekleyin. Seyreltmeden sonra pH'ı 50 mM MES veya 50 mM NaOH damla damladılarak dipeptit çözeltisine ekleyerek 7,4'e ayarlayın (bkz. adım 1.1.3). pH'ı ayarladıktan sonra çözeltiyi bir ölçüm silindirine dökün, test tüpünü durulayın ve dipeptit konsantrasyonu 8 mM yapmak için ölçüm silindirini DDW ile 20 mL'ye kadar doldurun.
2. Titania sol hazırlanması
- DDW'nin 500 mL'inde 1.066 g MES'i eriterek 10 mM'lik MES tampon çözeltisini hazırlayın. PH metre ile pH'ı karıştırıp izlettikten sonra kuru sodyum hidroksit ile pH'ı 7,4'e ayarlayın.
- Grind 200 nanokristalin TiOmg 2 en az 5 dk için bir harç (Malzeme Tablosubakınız).
- Bir laboratuvar şişesi içine zemin titanyum dioksit nano tanecikleri 40 mg ağırlığında. Şişeyi laboratuvar standını kullanarak sonication bath'a koyun (Bkz. Malzeme Tablosu).
- 20 dakika boyunca TiO2 ve ultrasonik banyoda sonicate (5 L, 40 kHz, 120 W) ile şişe içine 10 mM MES tampon 20 mL ekleyin.
3. Karıştırma ve termostating
- Termostatı (bkz. Malzemeler Tablosu)istenilen sıcaklıklara (örn. 0.00, 10.00, 20.00, 30.00 veya 40.00 °C) ayarlayın.
- Işaretli adsorpsiyon şişelerine TiO2'nin sonicated sol'unun 1 mL'sini ekleyin. Ekstrüzyon polistiren köpükten yapılmış derme çatma bir yüzdürme cihazına ilgili dipeptit seyreltme karşı işaretli adsorpsiyon şişeleri yerleştirin. Yüzdürme cihazını işaretli şişeler ve ilgili dipeptit seyreltmeleri ile en az 5 dakika termostatiçine yerleştirin.
- Tüm karıştırma çözümlerinin aynı sıcaklığa sahip olmasını sağlayarak, ilgili işaretli adsorpsiyon şişesine her dipeptit seyreltmesinin 1 mL'sini ekleyin. Elde edilen adsorpsiyon numuneserilerini termostatta 0.00, 10.00, 20.00, 30.00 veya 40.00 °C'de 24 saat boyunca saklayın.
NOT: Elde edilen tüm dispersiyon örneklerini termostata koymadan önce dikkatlice sallayın. - Termostating sırasında el ile sallayarak Bazen TiO2 dispersiyonları karıştırın.
4. Termobelirtilmiş numunelerin filtrasyonu
- Sıcaklık kaynaklı titreşmeden kaçınmak için termostattan filtreleme için her seferinde bir numune alın.
- Bir şırınga iğnesi ile, bir şırınga ile her cam şişedipeptit çözeltisi bir örnek alın. İğneyi şırıngadan çıkarın ve dipeptit çözeltisini cam şişeye filtrelemek için şırınga filtresine (Bkz. Malzemeler Tablosu)tonuyla tonur. Filtrasyonu diğer numunelerle tekrarlayın.
- 5. bölüme uygun olarak filtratanaliz.
NOT: Birkaç dakika süreceği ve konsantrasyon dengesinde bir değişikliğe neden olabileceğinden, numuneleri santrifüj etmeyin.
5. Türevleştirme ve HPLC analizi
- Asetonitril trifloroasetik asit (TFA) bir 50 mL çözeltisi olun. Ölçüm silindirine 0,34 mL TFA ekleyin ve çözeltinin hacmini RT'de asetonnitril ile 50 mL'ye ayarlayın.
DİkKAT: Egzoz havalandırması olan bir duman kaputu altında TFA ile çalışın, çünkü trifloroasetik asit solunduğunda zararlıdır, ciddi deri yanıklarına neden olur ve düşük konsantrasyonlarda bile sucul organizmalar için toksiktir53. - Türevleştirme çözeltisini (yani Edman reaktifi54)mezun olmuş bir silindire 299°L fenil izotiyosiyanat ve 347 μL triethylamin yerleştirerek ve çözelti hacmini RT'de asetonitrile 50 mL'ye ayarlayarak hazırlayın.
- Yüksek performanslı sıvı kromatografi (HPLC) analizinden önce, numuneleri kromatografi şişelerinde Edman reaktifi ile türemiş olarak türetin. 400 μL'lik numuneyi Edman reaktifinin 400 μL'si ile karıştırın. Numuneyi 60 °C'de 15 dk ısıtın. Isıtmadan sonra numuneyi TFA çözeltisinin 225 l'si ile nötralize edin ve numuneyi RT'ye soğutmak için birkaç dakika bekleyin.
- Adsorpsiyon öncesi ve sonrası dipeptit çözeltisinin konsantrasyonunun belirlenmesi için HPLC analizini (Bkz. Malzemeler Tablosu)kullanın. Analiz edilen çözümlerle kromatografi şişelerini HPLC autosampler'ına yerleştirin ve yazılım tarafından belirlenen gerekli koşullarla numuneleri analiz etmeye başlayın (Bkz. Malzeme Tablosu).
NOT: Mobil faz, deiyonize suve saf asetonitril%0,1 TFA'dan oluşur, asetonitril gradyanları 286 nm'de %20-90'dan 13 dk. Her numuneyi üç kat analiz eder. Dipeptit çözeltisi konsantrasyonunu önceden belirlenmiş kalibrasyon eğrisini kullanarak ölçün(Şekil 2). Kromatografi özellikleri için shchelokov ve ark.55'e bakınız.
Sonuçlar
Nanokristalin titanyum dioksit üzerinde bir dipeptid adsorpsiyonu 0−40 °C sıcaklık aralığında biyouyumlu koşullarda incelendi. Titanyum dioksit yüzeyinde deneysel dipeptit adsorpsiyonu (A, mmol/g)

C0 ve Ce'nin sırasıyla milimollerde dipeptit başlangıç ve denge konsantrasyonları olduğu durumlarda; V litre bir dipeptit çözeltisi hacmidir; ve m gram olarak sorbent ağırlığıdır.
Dipeptit adsorpsiyon ölçümleri Henry modeli kullanılarak işlenmiştir. Bu isotherm modeli, sorbent yüzeyinde birbirinden izole edilmiş sorbat molekülleri ile nispeten düşük konsantrasyonlarda adsorpsiyon varsayar ve deneysel verileri tanımlamak için uygundur(Şekil 3). Ancak, bu modelin yalnızca geri döndürülebilir adsorpsiyon durumunda da doğrulanabilir şekilde uygulanabileceğini unutmayın. Birden fazla kez durulanan malzemenin IR-spektroskopisi bu amaçla uygundur. TiO2 ve çözeltide elde edilen denge peptid miktarları doğrusal denkleme uygun olarak ilişkilidir:

KH Henry'nin adsorpsiyon sabitidir.
Denge bağlama sabiti KH dipeptit adsorpsiyon(A)bağımlılığı nın eğiminden elde edildi dipeptit denge konsantrasyonu(Ce). Her sıcaklık için standart Gibbs serbest enerji(ΔG, kJ /mol) Van't Hoff denklemi ile belirlenmiştir:

R'nin J/mol*K'dakiideal gaz sabiti olduğu ve T'nin Kelvin'deki adsorpsiyon işleminin sıcaklığı olduğu yer.
Dipeptit Gibbs serbest enerjileri her sıcaklıkta belirlenen(Şekil 4) eksen ile doğrusal regresyon bir durdurma olarak entalpi (ΔH)açıkladı. Regresyon değişkeni, sürecin entropisi(ΔS),temel denklemden türetilmiştir:
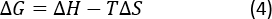
Denge bağlayıcı sabitin hesaplanan değerleri(KH),standart Gibbs enerjisi(ΔG), entalpi (ΔH), ile-His için entropi(ΔS) Tablo 1'desunulmuştur.

Şekil 1: 16 mM dipeptit stok çözeltisinin seyreltilmesi. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 2: Farklı dipeptit konsantrasyonunda kalibrasyon eğrisi. Dipeptit konsantrasyonları 0.4-16.0 mM arasında ydı. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 3: Henry modeli tarafından her sıcaklık için hesaplanan dipeptit adsorpsiyon izoformları. Dipeptit adsorpsiyon isothermleri (A) 0 °C (B) 10 °C (C) 20 °C (D) 30 °C ve (E) 40 °C, sırasıyla. Hesaplanan korelasyon katsayıları (R2),elde edilen tüm Henry modeli izamları için 0.96−0.99 aralığına düştü. Hata çubukları, üç aylık olarak ölçülen her numune konsantrasyonu için %95 güven aralığını temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.

Şekil 4: Dipeptit adsorpsiyonunun standart Gibbs serbest enerjisinin ısıya bağımlılığı. Hata çubukları, Gibbs serbest enerjisi için %95'lik güven aralığını Henry Model'e dayalı dolaylı ölçüm olarak temsil eder. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
| T, K | KH | ΔG0, kJ/mol | ΔH0, kJ/mol | ΔS0, kJ/mol K |
| 273.15 | 0,32 ± 0,01 | 2.6 ± 0.0 | - 41 ± 9 | - 0,16 ± 0,03 |
| 283.15 | 0,25 ± 0,01 | 3.2 ± 0,1 | ||
| 293.15 | 0,17 ± 0,06 | 4.3 ± 0.9 | ||
| 303.15 | 0,050 ± 0,002 | 7.6 ± 0.1 | ||
| 313.15 | 0,037 ± 0,002 | 8.3 ± 0.1 |
Tablo 1: Dipeptit adsorpsiyonunun termodinamik parametreleri.
Tartışmalar
Isotherm yapı çözümlerinin adsorpsiyonu, yüksek spesifik yüzey alanına sahip kinetik kısıtlamalar ve sorbentler nedeniyle daha uzun bir denge gerektirir. Ayrıca, sols istikrarsızlığı, nanopartikül agregalar, kristallik, nanopartikül boyutu dağılımı, çözeltinin pH, ve adsorpsiyon için rekabet amino asitler adsorbing sırasında dikkate alınmalıdır. Ancak, tükenme yöntemini kullanarak adsorpsiyon isotherm inşaat pahalı kurulumları gerektirmez, çünkü en kullanılabilir metodoloji kalır, ve henüz kelimenin tam anlamıyla her çözünür sorbatiçin ayrıntılı fiziksel kimya verileri sağlar.
Bir kristal malzeme sorbent olarak kullanıldığında adsorpsiyon modları (yani, çözelti dağılmış parçacıklar veya sabit bir yüzey) arasında bir ayrım yapılmalıdır. Makroskopik düz yüzeylerde ve parçacıklar üzerinde kristal yüzlerin dağılımında önemli bir fark beklenmelidir. Peptidlerin nano partiküller üzerindeki adsorpsiyonundan elde edilen termodinamik parametreler, peptit adsorpsiyonunun makroskopik düz yüzeylere kadar olan termodinamik parametrelerine karşılık olmayabilir.
İnorganik yüzeylerde adsorbe peptidlerin ortalama miktarı son derece düşüktür. Oda sıcaklığında, bu değer metrekare28başına mikrogram yaklaşık birkaç yüz. Bu küçük miktarda adsorbat, doğru ölçüm yöntemleri ve iyi gelişmiş yüzeylere sahip katı maddeler gerektirir. Bu nedenle, büyük bir özel yüzeye sahip küçük partikül maddeler (yüzlerce metrekare) adsorpsiyon deneyleri için kullanılmalıdır43,56,57,58,59,60.
Peptidler, proteinler gibi, kararsız, ve koşullar dar bir dizi işlevselliğini korumak. Adsorpsiyon deneyleri 0 °C-40 °C (273.15 K-313.15 K) ile uyumlu olan ve normal, işleyen, canlı bir organizmanınkine benzer şekilde nanokristalin titanyum dioksit üzerinde yapılmıştır. Daha yüksek veya daha düşük sıcaklıklarda adsorpsiyon alakasızdır ve deney için dikkate alınmamalıdır.
Çok fonksiyonlu biyolojik olarak aktif bileşikler de medya nın pH yüksek duyarlılık sergiler, yüzey yükü ve bu nedenle yüklü fonksiyonel gruplar arasında Coulomb etkileşimleri etkilergibi 61,62,63. Oksit malzemelerin sorbent yükü de sulu yüzeyde aktif proton değişimi nedeniyle pH'ya bağlıdır64. Bir tampon adsorpsiyon dengesi kullanımı için pH kararlı koşullar kurmak için gereklidir. Bu çalışmada, MES tampon onun koordinasyonsuz özelliği için kullanılır65, bu yüzden metal oksit yüzeyinde adsorpsiyon için peptid ile rekabet olmaz, fosfat tamponlar aksine66.
Amino asit adsorpsiyon bu son test nanopartikül üzerinde büyük bağlayıcı site yüzey defekti olduğunu gösterir55. Yüzeydeki kusur dağılımı nanokristalin yüzeylerin en az kontrol edilebilir özelliklerinden biridir, bu nedenle adsorpsiyon çalışmalarında tutarlılığı korumak için aynı partiden sorbent kullanmalıdır.
QCM, plazmon rezonans, ve ITC spektroskopik yöntemlerin bir arada yüzey ile etkileşim sırasında adsorbat yapısal özelliklerini ortaya ince hassasiyetile gerçek yöntemlerdir. Ancak, kinetik kısıtlamaların üstesinden gelmezler ve hala adsorpsiyon dengesini sağlamak için önemli bir zamana ihtiyaç duyarlar. Ayrıca, aynı anda yalnızca bir örnek işlenebilir, bu da toplu numune analizini zorlaştırabilir. Diğer taraftan, sunulan tükenme yöntemi basittir ve sadece termostat kapasitesiyle sınırlıdır, bu da çok sayıda numunenin işlenmesini mümkün kılar.
Isıya bağlı reelibration önlemek için termostat çıkarılır çıkarılmaz termosesinin süzülmesi gerekir. Yeni bir sıcaklıkta denge birkaç saat kadar sürebilir, ancak adsorpsiyon örneklerinin farklı bir sıcaklıkta tutulması en aza indirilmelidir. Birkaç dakika kadar sürer ve konsantrasyon dengesinde bir değişikliğe neden olabilir, çünkü supernatant ayırma için örneklerin santrifüj de tavsiye edilmez. Filtre malzemesinin seçimi sorbat yapısına bağlıdır ve maksimum geri kazanım için olası filtre bağlamayı azaltmalıdır. Belirli filtreleri seçerken satıcı yönergelerini ve önerilerini izlemek en iyisidir.
Ayrıca, bir adsorpsiyon çalışmalarında konsantrasyon değişikliği kütle spektrometresi, radyo-spektroskopi veya UV görünür spektroskopi kullanılarak doğrulanmış nicelik yöntemi kullanılarak izlenmesi gerektiğini akılda tutmak gerekir. Adsorbat spektroskopik olarak aktifse analiz kolaydır, aksi takdirde ek etiketleme veya adsorbat türevi gereklidir.
Açıklamalar
Yazarların açıklayacak bir şeyi yok.
Teşekkürler
Bu çalışma Rusya Temel Araştırma Vakfı (Grant No. 15-03-07834-a) tarafından mali olarak desteklenmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 2-(N-Morpholino)ethanesulfonic acid | TCI Chemicals | 4432-31-9 | MES, >98% |
| Acetonitrile | Panreac AppliChem | HPLC grade | |
| Chromatography vials | glass | ||
| Dipeptide Ile-His | Bachem | 4000894 | |
| Double-distilled water | DDW was obtained on spot | ||
| Heating cleaning bath "Ultrasons-HD" | J.P. Selecta | 3000865 | 5 L, 40 kHz, 120 Watts |
| High-performance liquid chromatograph system equipped with a UV−vis detector | Shimadzu, LC-20 Prominence | HPLC | |
| Isopropanol | Sigma-Aldrich (Merck) | 67-63-0 | 99.70% |
| LabSolutions Lite | Shimadzu | 223-60410 | Software for high-performance liquid chromatography system |
| Nanocrystalline TiO2 | Pure anatase with at least 99% crystallinity. Average particle size 10.62 ± 3.31 nm. Specific surface 131.9 m2/g (BET). See Langmuir 2019, 35, 538−550, for details. | ||
| Phenyl isothiocyanate | Acros Organics | 103-72-0 | PITC, 98% |
| Reversed-phase Zorbax column | ZORBAX LC | 150×2.5 mm i.d. with a mean particle size of 5 μm | |
| Syringe filter | Vladfilter | 25 mm, 0.2 μm pore, cellulose acetate | |
| Test sterile polymeric tube | polypropylene | ||
| Thermostat TC-502 | Brookfield | Refrigerating/heating circulating bath with the programmable controller for the sample derivatization | |
| Triethylamine | Sigma-Aldrich (Merck) | 121-44-8 | TEA; 99% |
| Trifluoroacetic acid | Panreac AppliChem | 163317 | TFA, 99% |
Referanslar
- Garcia, A. J. Interfaces to Control Cell-Biomaterial Adhesive Interactions. Polymers for Regenerative Medicine. 203, Chapter 71 171-190 (2006).
- Mahmood, T. A., et al. Modulation of chondrocyte phenotype for tissue engineering by designing the biologic-polymer carrier interface. Biomacromolecules. 7 (11), 3012-3018 (2006).
- Gandavarapu, N. R., Mariner, P. D., Schwartz, M. P., Anseth, K. S. Extracellular matrix protein adsorption to phosphate-functionalized gels from serum promotes osteogenic differentiation of human mesenchymal stem cells. Acta Biomaterialia. 9 (1), 4525-4534 (2013).
- Horbett, T. Biological Activity of Adsorbed Proteins. Surfactant Science Series. 110, 393-413 (2010).
- Ratner, B. D., Hoffman, A. S., Schoen, F. J., Lemons, J. E. Biomaterials Science: An Introduction to Materials in Medicine. , Elsevier Academic Press/Academic Press. San Diego. (2004).
- Jahangir, A. R., et al. Fluorinated surface-modifying macromolecules: Modulating adhesive protein and platelet interactions on a polyether-urethane. Journal of Biomedical Materials Research. 60 (1), 135-147 (2002).
- Shen, M., et al. PEO-like plasma polymerized tetraglyme surface interactions with leukocytes and proteins: In vitro and in vivo studies. Journal of Biomaterials Science, Polymer Edition. 13 (4), 367-390 (2002).
- Wisniewski, N., Moussy, F., Reichert, W. M. Characterization of implantable biosensor membrane biofouling. Fresenius' Journal of Analytical Chemistry. 366 (6-7), 611-621 (2000).
- Geelhood, S. J., et al. Passivating Protein Coatings for Implantable Glucose Sensors: Evaluation of Protein Retention. Journal of Biomedical Materials Research. Part B, Applied Biomaterials. 81, 251-260 (2007).
- Knowles, J. R. Enzyme catalysis: not different, just better. Nature. 350 (6314), 121-124 (1991).
- Blankschien, M. D., et al. Light-triggered biocatalysis using thermophilic enzyme - Gold nanoparticle complexes. ACS Nano. 7 (1), 654-663 (2013).
- Wu, H., et al. Catechol modification and covalent immobilization of catalase on titania submicrospheres. Journal of Molecular Catalysis B: Enzymatic. 92, 44-50 (2013).
- Gray, J. J. The interaction of proteins with solid surfaces. Current Opinion in Structural Biology. 14 (1), 110-115 (2004).
- Hlady, V., Buijs, J. Protein adsorption on solid surfaces. Current Opinion in Biotechnology. 7 (1), 72-77 (1996).
- Kulkarni, M., et al. Titanium nanostructures for biomedical applications. Nanotechnology. 26 (6), 062002(2015).
- Yin, F. Z., Wu, L., Gui Yang, H., Su, H. Y. Recent progress in biomedical applications of titanium dioxide. Physical Chemistry Chemical Physics. 15 (14), 4844-4858 (2013).
- Rezania, A., Johnson, R., Lefkow, A. R., Healy, K. E. Bioactivation of metal oxide surfaces. 1. Surface characterization and cell response. Langmuir. 15 (20), 6931-6939 (1999).
- Schenk, R. The Corrosion Properties of Titanium and Titanium Alloys. Titanium in Medicine. Brunette, D. M., et al. , Springer-Verlag. Berlin, Germany. 145-170 (2001).
- Bozzini, B., et al. An electrochemical impedance investigation of the behaviour of anodically oxidised titanium in human plasma and cognate fluids, relevant to dental applications. Journal of Materials Science: Materials in Medicine. 19 (11), 3443-3453 (2008).
- Popa, M. V., et al. Long-term assessment of the implant titanium material - Artificial saliva interface. Journal of Materials Science: Materials in Medicine. 19 (1), 1-9 (2008).
- Kim, J. K., et al. Lysozyme-mediated biomineralization of titanium-tungsten oxide hybrid nanoparticles with high photocatalytic activity. Chemical Communications. 50, 12392-12395 (2014).
- Suriyaraj, S. P., Selvakumar, R. Room temperature biosynthesis of crystalline TiO2 nanoparticles using Bacillus licheniformis and studies on the effect of calcination on phase structure and optical properties. RSC Advances. 4, 39619-39624 (2014).
- Inoue, I., et al. Thermo-stable carbon nanotube-TiO2 nanocompsite as electron highways in dye-sensitized solar cell produced by bio-nano-process. Nanotechnology. 26 (28), 285601(2015).
- Gardères, J., et al. Self-assembly and photocatalytic activity of branched silicatein/silintaphin filaments decorated with silicatein-synthesized TiO2 nanoparticles. Bioprocess and Biosystems Engineering. 39 (9), 1477-1486 (2016).
- Chen, H., Su, X., Neoh, K. G., Choe, W. S. QCM-D analysis of binding mechanism of phage particles displaying a constrained heptapeptide with specific affinity to SiO2 and TiO2. Analytical Chemistry. 78 (14), 4872-4879 (2006).
- Iucci, G., et al. Peptides adsorption on TiO2 and Au: Molecular organization investigated by NEXAFS, XPS and IR. Surface Science. 601 (18), 3843-3849 (2007).
- Gronewold, T. M. A., Baumgartner, A., Weckmann, A., Knekties, J., Egler, C. Selection process generating peptide aptamers and analysis of their binding to the TiO2 surface of a surface acoustic wave sensor. Acta Biomaterialia. 5 (2), 794-800 (2009).
- Gitelman, A., Rapaport, H. Bifunctional designed peptides induce mineralization and binding to TiO2. Langmuir. 30 (16), 4716-4724 (2014).
- Tada, S., Timucin, E., Kitajima, T., Sezerman, O. U., Ito, Y. Direct in vitro selection of titanium-binding epidermal growth factor. Biomaterials. 35 (11), 3497-3503 (2014).
- Micksch, T., Liebelt, N., Scharnweber, D., Schwenzer, B. Investigation of the peptide adsorption on ZrO2, TiZr, and TiO2 surfaces as a method for surface modification. ACS Applied Materials and Interfaces. 6 (10), 7408-7416 (2014).
- Limo, M. J., Perry, C. C., Thyparambil, A. A., Wei, Y., Latour, R. A. Experimental Characterization of Peptide-Surface Interactions. Bio-Inspired Nanotechnology: From Surface Analysis to Applications. , 37-94 (2013).
- Draczkowski, P., Matosiuk, D., Jozwiak, K. Isothermal titration calorimetry in membrane protein research. Journal of Pharmaceutical and Biomedical Analysis. 87, 313-325 (2014).
- Omanovic-Miklicanin, E., Manfield, I., Wilkins, T. Application of isothermal titration calorimetry in evaluation of protein-nanoparticle interactions. Journal of Thermal Analysis and Calorimetry. 127, 605-613 (2017).
- Jing, X., et al. Interaction of peptidomimetics with bilayer membranes: Biophysical characterization and cellular uptake. Langmuir. 28 (11), 5167-5175 (2012).
- Mizuguchi, C., et al. Effect of phosphatidylserine and cholesterol on membrane-mediated fibril formation by the N-terminal amyloidogenic fragment of apolipoprotein A-I. Scientific Reports. 8 (1), 5497(2018).
- Bisker, G., et al. Insulin Detection Using a Corona Phase Molecular Recognition Site on Single-Walled Carbon Nanotubes. ACS Sensors. 3 (2), 367-377 (2018).
- Singh, N., Husson, S. M. Adsorption thermodynamics of short-chain peptides on charged and uncharged nanothin polymer films. Langmuir. 22 (20), 8443-8451 (2006).
- Seker, U. O. S., et al. Thermodynamics of engineered gold binding peptides: Establishing the structure-activity relationships. Biomacromolecules. 15 (7), 2369-2377 (2014).
- Beutner, R., Michael, J., Schwenzer, B., Scharnweber, D. Biological nano-functionalization of titanium-based biomaterial surfaces: A flexible toolbox. Journal of the Royal Society Interface. 7 (Suppl 1), S93-S105 (2010).
- Sultan, A. M., et al. Aqueous Peptide-TiO2 Interfaces: Isoenergetic Binding via Either Entropically or Enthalpically Driven Mechanisms. ACS Applied Materials and Interfaces. 8 (28), 18620-18630 (2016).
- Teichroeb, J. H., Forrest, J. A., Jones, L. W., Chan, J., Dalton, K. Quartz crystal microbalance study of protein adsorption kinetics on poly(2-hydroxyethyl methacrylate). Journal of Colloid and Interface Science. 325 (1), 157-164 (2008).
- Lok, B. K., Cheng, Y. L., Robertson, C. R. Protein adsorption on crosslinked polydimethylsiloxane using total internal reflection fluorescence. Journal of Colloid And Interface Science. 91 (1), 104-116 (1983).
- Nakanishi, K., Sakiyama, T., Imamura, K. On the Adsorption of Proteins on Solid Surfaces, a Common but Very Complicated Phenomenon. Journal of Bioscience and Bioengineering. 91 (3), 233-244 (2001).
- Roddick-Lanzilotta, A. D., Connor, P. A., McQuillan, A. J. An In Situ Infrared Spectroscopic Study of the Adsorption of Lysine to TiO2 from an Aqueous Solution. Langmuir. 14, 6479-6484 (1998).
- Roddick-Lanzilotta, A. D., McQuillan, A. J. An in situ infrared spectroscopic investigation of lysine peptide and polylysine adsorption to TiO2 from aqueous solutions. Journal of Colloid and Interface Science. 217 (1), 194-202 (1999).
- Roddick-Lanzilotta, A., McQuillan, A. An in situ infrared spectroscopic study of glutamic acid and of aspartic acid adsorbed on TiO2: implications for the biocompatibility of titanium. Journal of Colloid and Interface Science. 227 (1), 48-54 (2000).
- Chan, B. M. C., Brash, J. L. Adsorption of fibrinogen on glass: reversibility aspects. Journal of Colloid And Interface Science. 82 (1), 217-225 (1981).
- van Enckevort, H. J., Dass, D. V., Langdon, A. G. The adsorption of bovine serum albumin at the stainless-steel/aqueous solution interface. Journal of Colloid And Interface Science. 98 (1), 138-143 (1984).
- Arnebrant, T., Nylander, T. Sequential and competitive adsorption of β-lactoglobulin and κ-casein on metal surfaces. Journal of Colloid And Interface Science. 111 (2), 529-533 (1986).
- Van Dulm, P., Norde, W. The adsorption of human plasma albumin on solid surfaces, with special attention to the kinetic aspects. Journal of Colloid And Interface Science. 91 (1), 248-255 (1983).
- Gonçalves, T. Fluorescent labeling of biomolecules with organic probes. Chemical Reviews. 109 (1), 190-212 (2009).
- Roth, K. D. W., Huang, Z. H., Sadagopan, N., Watson, J. T. Charge derivatization of peptides for analysis by mass spectrometry. Mass Spectrometry Reviews. 17 (4), 255-274 (1998).
- AppliChem, P. Safety Data Sheet According to Regulation (EU) 830/2015 3317 Trifluoroacetic Acid. , http://pub.panreac.com/msds/ing/3317.htm 112(2018).
- Heinrikson, R. L., Meredith, S. C. Amino acid analysis by reverse-phase high-performance liquid chromatography: Precolumn derivatization with phenylisothiocyanate. Analytical Biochemistry. 136 (1), 65-74 (1984).
- Shchelokov, A., et al. Adsorption of Native Amino Acids on Nanocrystalline TiO2: Physical Chemistry, QSPR, and Theoretical Modeling. Langmuir. 35 (2), 538-550 (2019).
- Fair, B. D., Jamieson, A. M. Studies of Protein Adsorption on Polystyrene Latex Surfaces. Journal of Colloid and Interface Science. 77 (2), 525-534 (1980).
- Kim, J. C., Lund, D. B. Adsorption behavior of p-lactoglobulin onto stainless steel surfaces. Journal of Food Processing and Preservation. 21 (607), 303-317 (1997).
- Kondo, A., Oku, S., Murakami, F., Higashitani, K. Conformational changes in protein molecules upon adsorption on ultrafine particles. Colloids and Surfaces B: Biointerfaces. 1, 197-201 (1993).
- Itoh, H., Nagai, T., Saeki, T., Sakiyama, T., Nakanishi, K. Adsorption of Protein onto Stainless Steel Particle Surface and its Desorption Behavior. Developments in Food Engineering. , 811-813 (1994).
- Itoh, H., Nagata, A., Toyomasu, T., Sakiyama, T., Nagai, T. Adsorption of β-Lactoglobulin onto the Surface of Stainless Steel Particles. Bioscience, Biotechnology, and Biochemistry. 59 (9), 1648-1651 (1995).
- Mudunkotuwa, I. A., Grassian, V. H. Histidine adsorption on TiO2 nanoparticles: An integrated spectroscopic, thermodynamic, and molecular-based approach toward understanding nano-bio interactions. Langmuir. 30, 8751-8760 (2014).
- Pászti, Z., Guczi, L. Amino acid adsorption on hydrophilic TiO2: A sum frequency generation vibrational spectroscopy study. Vibrational Spectroscopy. 50 (1), 48-56 (2009).
- Costa, D., Savio, L., Pradier, C. M. Adsorption of Amino Acids and Peptides on Metal and Oxide Surfaces in Water Environment: A Synthetic and Prospective Review. Journal of Physical Chemistry B. 120 (29), 7039-7052 (2016).
- Kosmulski, M. The significance of the difference in the point of zero charge between rutile and anatase. Advances in Colloid and Interface Science. 99 (3), 255-264 (2002).
- Kandegedara, A., Rorabacher, D. B. Noncomplexing tertiary amines as "better" buffers covering the range of pH 3-11. Temperature dependence of their acid dissociation constants. Analytical Chemistry. 71 (15), 3140-3144 (1999).
- Susumu, O., Teruaki, A., Koichi, T. The Adsorption of Basic a-Amino Acids in an Aqeous Solution by Titanium(IV) Oxide. Bulletin of the Chemical Society of Japan. 54, 1595-1599 (1981).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır