Method Article
המחקר של פפטיד קצר ספיחה על פתרון מפוזרים חלקיקים אורגניים באמצעות שיטת המחסור
In This Article
Summary
הצעד הראשון בתוך ההבנה של ביואוכאל-אורגני אינטראקציה שלב מוצק הוא חושף קבועים פיזיקליים הבסיסיים שניתן להעריך על ידי הקמת is, מערכת הספיחה. ספיחה מן השלב הנוזלי מוגבל על ידי קינטיקה, קיבולת פני השטח, pH, ו ספיחה תחרותי, אשר כל צריך להיחשב בזהירות לפני הגדרת ניסוי ספיחה.
Abstract
היסודות של אינטראקציות אורגניים-אורגני הם חשובים באופן ביקורתי בגילוי ופיתוח של הביוממשקים הרומן הקלה לניצול ביוטכנולוגיה ורפואה. מחקרים שנעשו לאחרונה עולה כי חלבונים אינטראקציה עם משטחים באמצעות אתרי ספיחה מוגבלת. שברי חלבונים כגון חומצות אמינו ופפטידים ניתן להשתמש עבור מידול אינטראקציה בין משטחים ביולוגיים מורכבים קרו ו אורגניים. במהלך שלושת העשורים האחרונים פותחו שיטות חוקיות ורגישות רבות כדי למדוד את יסודות הכימיה הפיזית של האינטראקציות האלה: איזותרמי טיטור calorimetry (התקשורת החשמלית), משטח התהודה של המשטח (spr), קוורץ מיקרו איזון גביש (qcm), השתקפות פנימית מוחלטת (טיטור), ומחליש השתקפות
הטכניקה הפשוטה והזולה ביותר למדידת הספיחה היא שיטת המחסור, שם השינוי בריכוז sorbate (דלדול) לאחר מגע עם הפתרון-מפוזר sorכופפים מחושב והניחו להיות ספיחה. מבוסס על נתוני מחסור לספק את כל הנתונים פיזיקליים בסיסיים. עם זאת, ספיחה מתוך פתרונות דורש שעות ארוכות יותר בגלל הגבלות קינטי ו סורבנטים עם שטח מסוים גבוה המשטח, מה שהופך אותו כמעט בלתי ישימה משטחי המטוס קבוע מאקרוסקופי. יתר על כן, גורמים כגון חוסר יציבות של sols, ננו-חלקיק אגרגטים, אחרים-סורבנטים crystallinity, התפלגות ננו-חלקיק גודל, pH של הפתרון, ותחרות עבור adsorption צריך להיחשב תוך לימוד פפטידים adsorption. מחסור בנתונים הבנייה מספק נתונים כימיה פיזיים מקיפה עבור פשוטו כמשמעו כל sorbate מסיסים עדיין נשאר המתודולוגיה הנגישה ביותר, כפי שהוא אינו דורש הגדרות יקרות. מאמר זה מתאר פרוטוקול בסיסי למחקר ניסיוני של פפטיד ספיחה על תחמוצת אורגנית מכסה את כל הנקודות הקריטיות המשפיעות על התהליך.
Introduction
במשך 50 השנים האחרונות האינטראקציה בין משטחים אורגניים ופפטידים משכו הרבה תשומת לב בשל חשיבותו הגבוהה במדעי החומר ורפואה. מחקר ביו-רפואי מתמקד בתאימות וביציבות של משטחים ביו-אורגניים, שיש להם השלכות ישירות לרפואה משובי, הנדסת רקמות1,2,3, והשרשה4,5,6,7. מכשירים ביומטריים עכשוויים, כגון חיישנים ומפעילים, מבוססים על חלבונים פונקציונליים מקיבוע על תחמוצת וליכים משטחים8,9,10,11,12,13. שיטות טיהור מודרניות לייצור חלבונים מסתמכות לעתים קרובות על תכונות של אינטראקציה ביואלוכאל בתוך הזרם לטיהור והפרדה14.
בין תחמוצות אורגניים מרובות, תחמוצת טיטניום נשאר מנוצל ביותר בשילוב עם מצעים רלוונטיים ביולוגית15,16. מחקר באזור של ממשקי ביולוגי מבוססי TiO2התמקדה בהקמת מחייב חזק וספציפי של חלבונים ופפטידים מבלי לשנות את המאפיינים הביולוגיים שלהם מבנית. בסופו של דבר, המטרה העיקרית היא שכבת צפיפות גבוהה של פני השטח של biomolecules עם יציבות גבוהה ופונקציונליות מוגברת אשר יקדם את היצירה של יישומים מבוססי טיטניום ביו ורפואיים17.
טיטניום וסגסוגות שלה כבר נעשה שימוש נרחב כמו חומר השתל כירורגי עבור לפחות שישה עשורים משום משטח TiO2 שכבה עם עובי של כמה ננומטר הוא עמיד בפני קורוזיה ומציג רמה גבוהה של תאימות רבים ב vivo יישומים18,19,20. טיטניום דו-חמצני נחשב גם למצע אי-אורגנית המופק ביומינרליזציה, שם הנוקלאוציה וצמיחה בפאזה אורגנית המלווה בחלבונים ופפטידים עשויים לספק חומרים עם תכונות קטליטיים ואופטיות מבטיחות21,22,23,24.
לאור הרלוונטיות הגבוהה של האינטראקציה בין חומרים אורגניים וbiomolecules באופן כללי, חלבון-TiO2 אינטראקציות בפרט, יש כבר הרבה מחקר כדי לטפל מניפולציה ושליטה של הספיחה של חלבונים על TiO2. בשל מחקרים אלה, נחשפו כמה מאפיינים בסיסיים של האינטראקציה הזאת, כגון קינטיקה של ספיחה, כיסוי פני השטח, ומערך ביולוגי, המעניק תמיכה ניכרת להתקדמות נוספת בביו-ממשקים5,13.
עם זאת, מורכבות החלבון מוסיפה הגבלות משמעותיות על נחישות והבנה מלאה של האינטראקציה ברמה המולקולרית של חלבון עם משטחים אורגניים. בהנחה כי biomolecules אינטראקציה עם משטחים אורגניים באמצעות אתרים מוגבלים, כמה חלבונים עם מבנים ידועים רצפי חומצות אמינו הופחת הרכיבים שלהם-פפטידים וחומצות אמינו-אשר נחקרו בנפרד. כמה פפטידים אלה הפגינו פעילות משמעותית, מה שהופך אותם נושא ייחודי של לימודי ספיחה ללא צורך הפרדת חלבון הקודם25,26,27,28,29,30.
אפיון כמותי של פפטיד ספיחה על TiO2 או משטחים אורגניים אחרים ניתן להשיג באמצעות שיטות פיזיות כי הותאמו במיוחד עבור biomolecules בעשורים האחרונים. שיטות אלה כוללות איזותרמי טיטור קלורימטריה, (spr), גביש קוורץ מיקרו-מאזן (qcm), השתקפות פנימית מלאה (טיטור), ומחליש את ההשתקפות הכוללת השתקפות (atr), שכולם מאפשרים זיהוי של חוזק הספיחה על-ידי מתן נתוני מפתח תרמודינמיים: הקבוע המחייב, אנרגיה חופשית של גיבס, אנתלפיה ואנטרופיה31.
הספיחה של biomolecules אל החומר האורגני עשוי להתבצע בשתי דרכים: 1) באופן מושלם, כמו גם שיטת דלדול להשתמש חלקיקים התפזרו בכריכה הפתרון למשטחים מאקרוסקופי קבוע; 2) SPR, QCM, TIRF, ו ATR להשתמש משטחים מאקרוסקופיים שונה עם חומר לא אורגני, כגון זכוכית מצופה זהב או שבבי מתכת, קריסטלים קוורץ, קריסטלים גופרתי אבץ, ו PMMA אסימונים, בהתאמה.
איזותרמי טיטור קלורימטריה היא שיטה פיזית נטולת תוויות המודד את החום המופק או נצרך על-ידי טיטור של פתרונות או תערובות הטרוגניות. תאים קלוריטריים רגישים לזהות אפקטי חום קטנים כמו 100 ננוג'לס, מה שהופך את המדידה של חום ספיחה על משטחים ננו-חלקיק אפשרי. התנהגות תרמית של sorbate במהלך תוספת רציפה-titration, מספק פרופיל תרמודינמי מלא של האינטראקציה חשיפת enthalpy, מחייב קבוע, ואנטרופיה בטמפרטורה נתונה32,33,34,35,36.
ספקטרוסקופית משטח (SPR) ספקטרוסקופיה היא טכניקה אופטית תלויית-שטח המבוססת על מדידת מדד השבירה של התקשורת בקרבת משטח למדה. זוהי שיטה בזמן אמת, ללא תווית עבור ניטור ספיחה הפיך ועובי שכבת ספיחה. ניתן לחשב את הקבוע המחייב מהשיוך וקצבי הדיסוציאציה. ניסויים adsorption שבוצעו בטמפרטורות שונות עשויים לספק מידע על התלות בטמפרטורה של אנרגיית ההפעלה ברציפות פרמטרים תרמודינמיים אחרים37,38,39.
גביש הקוורץ מיקרומאזן (QCM) מודד את השינוי בתדירות הנדנוד של גבישים פיזואלקטריים במהלך תהליכי הספיחה והספיחה. ניתן להעריך את קבוע האיגוד מיחס הקבועים של שיעור הספיחה והדסורזיה. Qcm משמש מדידות המסה יחסית ולכן, אין צורך כיול25,27,40. QCM משמש לספיחה משני הגזים והנוזלים. הטכניקה הנוזלית מאפשרת QCM לשמש ככלי ניתוח לתיאור התצהיר על משטחים ששונו באופן שונה41.
השתקפות פנימית מלאה (TIRF) היא טכניקה אופטית הפנים אופטי המבוסס על המדידה של הזריחה של האדסוורההואנפלאז מתרגש עם גלי אוונסי ביטוי פנימי. השיטה מאפשרת זיהוי של מולקולות פלורסנט המכסים את פני השטח עם עוביים על סדר של עשרות nanometers, ולכן הוא משמש במחקר של macromolecular ספיחה על משטחים שונים42,43. במעקב באתרו של הדינמיקה של הקרינה הפלואורסצנטית על ספיחה ו desorption לספק את קינטיקה ספיחה ומכאן נתונים תרמודינמיים42,43.
השתקפות כוללת של מחליש (ATR) שימש את השימוש על ידי רודפין-לנגיוטה כדי ליצור שיטת ליזין מבוסס על הלהקות ליזין ספקטרל ב 1,600 ו 1,525 ס"מ-1. זוהי הפעם הראשונה כי קבוע הכריכה עבור פפטיד ב-TiO2 נקבע באמצעות שיטה באתרו אינפרא אדום44. טכניקה זו הייתה יעילה ביצירת ספיחה איזוטרציאמים עבור פפטידים רב ליזין45 ו חומצות אמינו חומצה חומצי46.
שלא כמו השיטות הנ ל, שבו הפרמטר ספיחה נמדד באתרו, בניסוי קונבנציונאלי את כמות הספיחה biomolecules נמדד על ידי שינוי הריכוז לאחר פני השטח יצרה קשר עם הפתרון. בגלל הריכוז של sorbate נרקב ברוב המכריע של המקרים ספיחה, שיטה זו נקראת שיטת דלדול. מדידות הריכוז דורשות שיטת ניתוח אנליטית מאומתת, שעשויה להתבסס על המאפיין האנליטי הפנימי של sorbate או מבוסס על התיוג47,48,49,50 או לדבטיזציה51,52 ממנו.
ניסויים ספיחה באמצעות qcm, spr, tirf, או atr דורשים הכנת פני השטח המיוחד של שבבים וחיישנים המשמשים למחקרים ספיחה. משטחים מוכנים צריך לשמש פעם ולדרוש שינוי על ידי החלפת adsorbate, בשל הידרציה בלתי נמנעת של משטח תחמוצת או כימוזיה אפשרי של sorbate. רק מדגם אחד בכל פעם יכול להיות מופעל באמצעות החום, qcm, spr, tirf, או atr, ואילו בשיטת דלדול אחד יכול להפעיל עשרות דגימות, שעבורן הכמות מוגבלת רק על ידי קיבולת התרמוסטט ואת הזמינות אחרים-סורבנטים. דבר זה חשוב במיוחד בעת עיבוד אצוות או ספריות של מולקולות ביו-אקטיביות גדולות. חשוב מכך, שיטת המחסור אינה דורשת ציוד יקר אלא תרמוסטט בלבד.
עם זאת, למרות היתרונות הבולטים שלו שיטת הדלדול דורש תכונות פרוצדורליים מורכבים שעלולים להיראות מסורבלת. מאמר זה מציג כיצד לבצע מחקר מקיף כימי פיסיוכימיה של dipeptide ספיחה על TiO2 באמצעות שיטת דלדול וכתובות בעיות שחוקרים יכולים להתמודד בעת ביצוע ניסויים רלוונטיים.
Protocol
1. הכנת פתרונות מניות דיפפטיד ודילול
- הכנת תמיסת דיפפטיד 16 מ"מ
- מקום 0.183 g של דיפפטיד (Ile-שלו) (ראה טבלת חומרים) במבחנה סטרילי בדיקה פולימריים, לדלל ל 35 mL עם מים כפולים מזוקקים (ddw), ומתמוסס בטמפרטורת החדר (RT) תחת ערבוב נמרץ.
הערה: אם הדיפפטיד אינו מתמוסס ב-DDW תוך כדי ערבוב, הניחו את התמיסה הדיפפטיד לתוך אמבט קולי וsonicate לכמה דקות. - הכנת פתרון 50 mM של 2-(N-מורגולינו) מאגר חומצה ethanesulfonic על ידי המסת 0.533 g של יבש 2-(N-מורגוולסטינו) חומצה ethanesulfonic ב 50 מ ל של ddw במבחנה סטרילי. להכין 50 mM נתרן הידרוקסיד הפתרון על ידי המסת 200 mg של נתרן הידרוקסיד ב 100 mL של DDW.
- להתאים את ה-pH של הפתרון dipeptide מראש כדי 7.4 על ידי הוספה בזהירות (titration microliter מיקרוליטר) 50 mM MES, או 50 mM נתרן הידרוקסידי ל 16 הפתרון dipeptide, ערבוב ב RT וניטור ה-pH עם מד pH. לאחר התאמת ה-pH, יוצקים את הפתרון לתוך גליל מדידה, לשטוף את צינור הבדיקה, ולמלא את גליל מדידה עם DDW ל 40 mL לעשות ריכוז סופי של 16 מ"מ.
- מקום 0.183 g של דיפפטיד (Ile-שלו) (ראה טבלת חומרים) במבחנה סטרילי בדיקה פולימריים, לדלל ל 35 mL עם מים כפולים מזוקקים (ddw), ומתמוסס בטמפרטורת החדר (RT) תחת ערבוב נמרץ.
- הכנת דיפפטיד מתמיסה של 16 מ"מ במניה
- הכינו מדיקות פפטיד עם ריכוזים בין 0.4 ו 12.0 mM על ידי דילול 16 הפתרון dipeptide m עם DDW. לדוגמה, כדי להכין פתרון מסוג dipeptide בעובי 8 מ"מ, הוסף 7 מ ל עד 10 מ ל של הפתרון הדיפפטיד של 16 מ"מ. לאחר דילול, להתאים את ה-pH כדי 7.4 על ידי הוספת 50 mM MES או 50 מילימטר NaOH ירידה על ידי ירידה לפתרון dipeptide (ראה שלב 1.1.3). לאחר התאמת ה-pH, יוצקים את הפתרון לתוך גליל מדידה, לשטוף את צינור הבדיקה, ולמלא את גליל מדידה עד 20 מ ל עם DDW כדי להפוך את הריכוז dipeptide 8 מ"מ.
הערה: מדלל אחרים 16 פתרון מניות dipeptide מילימטר עם ריכוזים של 0.4, 0.8, 1.2, 1.6, 2.0, 3.0, 4.0, 8.0, ו 12.0 מ"מ, מוכנים בהתאם לאיור 1. ההתאמה של כל התמיסה dipeptide pH כדי 7.4 מתואר בשלב 1.1.3.
- הכינו מדיקות פפטיד עם ריכוזים בין 0.4 ו 12.0 mM על ידי דילול 16 הפתרון dipeptide m עם DDW. לדוגמה, כדי להכין פתרון מסוג dipeptide בעובי 8 מ"מ, הוסף 7 מ ל עד 10 מ ל של הפתרון הדיפפטיד של 16 מ"מ. לאחר דילול, להתאים את ה-pH כדי 7.4 על ידי הוספת 50 mM MES או 50 מילימטר NaOH ירידה על ידי ירידה לפתרון dipeptide (ראה שלב 1.1.3). לאחר התאמת ה-pH, יוצקים את הפתרון לתוך גליל מדידה, לשטוף את צינור הבדיקה, ולמלא את גליל מדידה עד 20 מ ל עם DDW כדי להפוך את הריכוז dipeptide 8 מ"מ.
2. הכנת טיטניה סול
- להכין פתרון 10 מ"מ של מאגר MES על ידי המסת 1.066 g של MES ב 500 mL של DDW. להתאים את ה-pH כדי 7.4 עם הידרוקסיד נתרן יבש על ערבוב וניטור ה-pH עם מד pH.
- טוחנים 200 מ"ג של nanocryסטולמן TiO2 בחומר מליטה לפחות 5 דקות (ראה טבלת חומרים).
- שוקלים 40 מ"ג של חלקיקים טיטניום דו תחמוצת הקרקע לתוך בקבוקון מעבדה. הכניסו את הבקבוקון לאמבט הsonication (ראו טבלת חומרים) באמצעות דוכן המעבדה.
- הוסף 20 מ מ של 10 מ"מ מאגר MES לתוך הבקבוקון עם TiO2 ו sonicate באמבטיה אולטראסוניות (5 L, 40 kHz, 120 W) עבור 20 דקות.
3. ערבוב וחום
- הגדר את התרמוסטט (ראה טבלת חומרים) לטמפרטורות הרצויות (כלומר, 0.00, 10.00, 20.00, 30.00, או 40.00 ° c).
- הוסף 1 מ ל של sonicated sol של TiO2 לתוך בבקבוקונים מסומנים ספיחה. מניחים את מבחנות ספיחה מסומנים נגד דילול דיפפטיד המקביל במכשיר ציפה מאולתר עשוי פוליסטירן מוקצף הבלטת קצף. מניחים את המכשיר ציפה עם הבקבוקונים מסומנים ודיפפטיד המקביל לתוך התרמוסטט לפחות 5 דקות.
- הוסף 1 מ ל של כל דילול dipeptide כדי בקבוקון ספיחה מסומן המקביל, וודא כי כל הפתרונות ערבוב יש את אותה טמפרטורה. שמור את הסדרה של דגימות ספיחה המתקבלים על התרמוסטט ב 0.00, 10.00, 20.00, 30.00, או 40.00 ° צ' עבור 24 שעות כדי להשיג את שיווי משקל ספיחה.
הערה: ללחוץ בזהירות את כל הדגימות של הדיבולים שהתקבלו לפני הכנסתו לתרמוסטט. - מדי פעם לערבב את TiO 2 דיספרסיות על ידי באופן ידני לטלטל אותם במהלךהתרמותיים .
4. סינון הדגימות התרמוד,
- כדי למנוע הפחתת משקל הטמפרטורה הנגרמת לקחת דגימה אחת בכל פעם מתרמוסטט לסינון.
- קח דגימה של פתרון dipeptide מכל בקבוקון זכוכית עם מזרק, דרך מחט מזרק. הסר את המחט מן המזרק ולשים על מסנן מזרק (ראה טבלת חומרים) כדי לסנן את הפתרון dipeptide לתוך בקבוקון זכוכית. חזור על הסינון עם הדגימות האחרות.
- לנתח את הפילטרט לפי סעיף 5.
הערה: אל צנטריפוגה את הדגימות, כי זה לוקח כמה דקות ועלול לגרום לשינוי בשיווי משקל הריכוז.
5. ניתוח הוראות לדריפיקציה ואנליזה
- להפוך פתרון 50 mL של חומצה trifluoroacetic (TFA) ב acetonitrile. הוסף 0.34 mL של TFA בצילינדר מדידה ולהתאים את נפח הפתרון ל 50 mL עם acetonitrile ב RT.
התראה: עבודה עם TFA תחת מכסה המנוע עם אוורור פליטה, כי חומצה trifluoroacetic מזיקה כאשר שאפה, גורם כוויות עור חמורות, והוא רעיל אורגניזמים ימיים גם בריכוזים נמוכים53. - הכינו את פתרון הדריבטיזציה (כלומר, אידמן מגיב54) על ידי הצבת 299 μl של פניאיל isothiocyanate ו 347 μl של triethylamine בצילינדר הדרגתי וכוונון נפח הפתרון 50 mL עם acetonitrile ב RT.
- לפני ניתוח האבחון הגבוה של הכרומטוגרפיה הנוזלית, למעשה הדגימות מהמגיב הכימית של אדמן בדגימות הכרומטוגרפיה. מערבבים 400 μL של המדגם עם 400 μL של מגיב הכימית של דמן. לחמם את המדגם ב 60 ° c עבור 15 דקות. לאחר החימום, לנטרל את המדגם עם 225 μL של הפתרון TFA ולחכות כמה דקות כדי לצנן את המדגם כדי RT.
- השתמש בניתוח האבחון (ראה טבלת חומרים) כדי לקבוע את ריכוז הפתרון הדיפפטיד לפני ואחרי ספיחה. הניחו את מבחנות הכרומטוגרפיה בעזרת הפתרונות שנותחו לתוך האבחון האוטומטי והתחילו לנתח את הדגימות בתנאים הנחוצים, הנקבעו על-ידי התוכנה (ראו טבלת חומרים).
הערה: השלב הנייד מורכב מ-0.1% TFA במים מפוהים ובאספניטריל טהור, עם מעברי הצבע של acetonitrile מ 20-90% ב 286 nm עבור 13 דקות.. לנתח כל מדגם בטרילקאט למדוד את הריכוז פתרון דיפפטיד באמצעות עקומת כיול שהוקמה בעבר (איור 2). למפרטי כרומטוגרפיה ר' שכלקוב ואח '55.
תוצאות
ספיחה של דיפפטיד על nanocryסטולמן טיטניום דו-חמצני נחקר בתנאים הביוגרפים בטווח טמפרטורות של 0-40 ° c. ספיחה ניסיונית דיאטנית (A, mmol/g) על פני השטח של תחמוצת טיטניום הוערך כמו

כאשר c0 ו- ce הם הריכוזים המתחילים והשיווי משקל של הדיפפטיד, בהתאמה; V הוא נפח של פתרון דיפפטיד בליטר; ו- m הוא המשקל של הסורפוף בגרמים.
המידות של ספיחה דיפפטיד היו נתונים שעובדו באמצעות מודל הנרי. זה המודל השני מניח ספיחה בריכוזים נמוכים יחסית עם מולקולות sorbate מבודדים זה מזה על פני משטח sorכופפים והוא מתאים לתיאור הנתונים ניסיוני (איור 3). עם זאת, שים לב כי מודל זה ניתן להחיל רק במקרה של adsorption הפיך, אשר יש לאשר גם. IR-ספקטרוסקופיה של החומר שוטפים מספר פעמים מתאים למטרה זו. פפטיד שיווי משקל שהושג כמויות על TiO2 ופתרון קשורים בהתאם למשוואה הליניארית:

כאשר KH הוא קבוע הספיחה של הנרי.
כריכת שיווי משקל קבוע KH התקבל משיפוע של התלות של דיפפטיד ספיחה (א) על הריכוז שיווי משקל dipeptide (Ce). אנרגיה חופשית של גיבס (ΔG, kJ/מול) עבור כל טמפרטורה T נקבע באמצעות משוואת וואן הוף:

כאשר R הוא קבוע הגז האידיאלי J/מול *K, ו T הוא הטמפרטורה של תהליך ספיחה ב קלווין.
דיפפטיד מאנרגיות חופשיות שנקבעו בכל טמפרטורה (איור 4), אנתלפיה (ΔH) כיירוט של הרגרסיה הלינארית עם הציר. משתנה הרגרסיה, האנטרופיה של התהליך (ΔS), נגזר מהמשוואה הבסיסית:
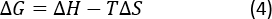
הערכים המחושבים של קבוע האיגוד לשיווי משקל (KH), אנרגיית גיבס סטנדרטית (ΔG), אנתלפיה (ΔH) ואנטרופיה (ΔS) עבור Ile-שלו מוצגים בטבלה 1.

איור 1: דילול של 16 מניות dipeptide פתרון המניה. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 2: עקומת כיול בריכוז דיפפטיד שונה. ריכוזי דיפפטיד היו בין 0.4-16.0 מ"מ. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 3: המודל הדיפפטיד האיזושני מחושב על ידי מודל הנרי עבור כל טמפרטורה. דיפפטיד ספיחה at (A) 0 ° צ' (ב) 10 ° צ' (ג) 20 ° צ' (ד) 30 ° צ' ו (ה) 40 ° c, בהתאמה. מקדמי המתאם המחושבים (R2) נפלו לטווח 0.96-0.99 עבור כל המתקבלים הנרי מודל isotherms. קווי שגיאה מייצגים את מרווח הביטחון של 95% עבור כל ריכוז לדוגמה הנמדד בטרילקאט. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.

איור 4: התלות של האנרגיה הסטנדרטית של גיבס ללא התקן הדיפפטיד בטמפרטורה. קווי שגיאה מייצגים את מרווח הביטחון של 95% עבור אנרגיה חופשית של גיבס כמדידה עקיפה המבוססת על הנרי מודל. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
| טי, קיי | KH | ΔG0, kJ/מול | ΔH0, kJ/מול | ΔS0, kJ/מול K |
| 273.15 | 0.32 ± 0.01 | 2.6 ± 0.0 | -41 ± 9 | -0.16 ± 0.03 |
| 283.15 | 0.25 ± 0.01 | 3.2 ± 0.1 | ||
| 293.15 | 0.17 ± 0.06 | 4.3 ± 0.9 | ||
| 303.15 | 0.050 ± 0.002 | 7.6 ± 0.1 | ||
| 313.15 | 0.037 ± 0.002 | 8.3 ± 0.1 |
שולחן 1: פרמטרים תרמודינמיים של דיפפטיד ספיחה.
Discussion
ספיחה מתוך פתרונות עבור בנייה is, דורש זמן רב יותר עבור הרמה עקב הגבלות הקינטי ומסורבי עם שטח מסוים גבוה הקרקע. יתר על כן, חוסר יציבות של sols, ננו-חלקיק אגרגטים, crystallinity, התפלגות ננו-חלקיק גודל, pH של הפתרון, ואת התחרות עבור ספיחה צריך להיחשב בזמן ספיחה חומצות אמינו. עם זאת, הבנייה is, ספיחה באמצעות שיטת דלדול נשאר המתודולוגיה הזמינה ביותר, כי זה לא דורש כיוונונים יקרים, ובכל זאת הוא מספק נתונים כימיה פיזיים ממצה עבור פשוטו כמשמעו כל sorbate מסיסים.
הבחנה יש לעשות בין מצבי ספיחה (כלומר, הפתרון חלקיקים מפוזרים או על משטח קבוע) כאשר חומר גבישי משמש כפוף. יש לצפות להבדל משמעותי בהפצת פרצופים גביתיים על משטחים שטוחים מקרוסקותיים ועל חלקיקים. הפרמטרים התרמודינמיים שנקבעו מתוך ספיחה של פפטידים על חלקיקי חלקיקים לא יכול להתאים את הפרמטרים תרמודינמיים של פפטיד ספיחה כדי משטחים שטוחים מעין
הכמות הממוצעת של מיטות פפטידים על משטחים אורגניים הוא נמוך מאוד. בטמפרטורת החדר, ערך זה הוא כמספר מאות מיקרוגרמות למטר רבוע28. זו כמות קטנה של adsorbate דורש שיטות מדידה מדויקת ומוצקים עם משטחים מפותחים היטב. לכן, חומרים חלקיקים קטנים עם משטח ספציפי גדול (מאות מטרים רבועים) יש להשתמש עבור ניסויים ספיחה43,56,57,58,59,60.
פפטידים הם, כמו חלבונים, לא יציב, ולשמור על הפונקציונליות שלהם בטווח צר של תנאים. ניסויים adsorption בוצעו על nanocryסטולמן טיטניום דו-חמצני בטמפרטורה ביולוגית של 0 ° צ'-40 ° צ' (273.15 K-313.15 K), אשר דומים לאלה של נורמלי, תפקוד, אורגניזם חי. ספיחה בטמפרטורות גבוהות או נמוכות יותר אינן רלוונטיות ואין לקחת בחשבון את הניסוי.
תרכובות פעילים ביולוגית משולבים גם מפגין רגישות גבוהה ל-pH של המדיה, כפי שהוא משפיע על הטעינה על פני השטח ולכן אינטראקציות קולון בין מחויב קבוצות פונקציונליות61,62,63. המטען אחרים-סורבנטים של חומרי תחמוצת הוא גם התלוי ב-pH עקב חילופי פרוטונים פעיל במשטח המים הרטוב64. כדי ליצור תנאים יציבים pH לשימוש שיווי משקל ספיחה של מאגר נדרש. במחקר זה, מאגר MES משמש עבור המאפיין הלא מתאם שלה65, כך הוא לא להתחרות עם פפטיד עבור ספיחה על משטח תחמוצת המתכת, בניגוד מאגרי פוספט66.
הבדיקה האחרונה של ספיחה חומצות אמינו מראה כי אתר האיגוד העיקרי על ננו-חלקיק הוא פגם פני השטח55. התפלגות פגמים על פני השטח היא אחת התכונות הפחות לשליטה של מצעים nanocry, ומכאן צריך להשתמש אחרים-סורבנטים מאותה אצווה על מנת לשמור על עקביות במחקרים ספיחה.
QCM, התהודה פלסמה, ו ה, ה, ה, והאינט, ה, והאינטגרפיות הם שיטות אמיתיות עם רגישות עדינה כי בשילוב של שיטות ספקטרוסקופיות לחשוף המוזרויות מבניים של adsorbate במהלך הגומלין עם פני השטח. עם זאת, הם לא להתגבר על הגבלות קינטי עדיין דורשים זמן רב כדי להשיג שיווציה ספיחה. יתר על כן, רק מדגם אחד בכל פעם יכול להיות מעובד, מה שהופך ניתוח לדוגמה אצווה מאתגרת. מצד שני, שיטת המחסור המוצגת היא פשוטה ומוגבלת רק לקיבולת התרמוסטט, מה שהופך את העיבוד של מספר רב של דגימות אפשריות.
יש לסנן את הדגימות התרמוסיביות ברגע שהן מוסרות מהתרמוסטט כדי למנוע הפחתת שיווציה של טמפרטורה. למרות שequiציה בטמפרטורה חדשה עשויה להימשך עד כמה שעות, שמירה על דגימות ספיחה בטמפרטורה שונה צריך להיות ממוזער. לא מומלץ לצנטריפוגה דוגמאות להפרדה בין-חושית, משום שהיא אורכת דקות ספורות ועלולה לגרום לשינוי בשיווי האיזון בריכוז. הבחירה של חומר הסינון תלוי בטבע sorbate וצריך להפחית את כריכת הסינון האפשרי להתאוששות מקסימלית. מומלץ לעקוב אחר הוראות הספק וההמלצות בעת בחירת מסננים ספציפיים.
בנוסף, יש לזכור ששינוי הריכוז במחקרים על הספיחה צריך להיות מנוטר באמצעות שיטת קוונפיקציה מאומתת באמצעות ספקטרומטר מסה, ספקטרוסקופיית רדיו, או ספקטרוסקופיית מעין UV. הניתוח קל אם adsorbate הוא פעיל ספקטרוסקואני, אחרת תיוג נוסף או ללעג של adsorbate נדרש.
Disclosures
. למחברים אין מה לגלות
Acknowledgements
עבודה זו הייתה נתמכת כספית על ידי הקרן הרוסית למחקר בסיסי (גרנט No. 15-03-07834-a).
Materials
| Name | Company | Catalog Number | Comments |
| 2-(N-Morpholino)ethanesulfonic acid | TCI Chemicals | 4432-31-9 | MES, >98% |
| Acetonitrile | Panreac AppliChem | HPLC grade | |
| Chromatography vials | glass | ||
| Dipeptide Ile-His | Bachem | 4000894 | |
| Double-distilled water | DDW was obtained on spot | ||
| Heating cleaning bath "Ultrasons-HD" | J.P. Selecta | 3000865 | 5 L, 40 kHz, 120 Watts |
| High-performance liquid chromatograph system equipped with a UV−vis detector | Shimadzu, LC-20 Prominence | HPLC | |
| Isopropanol | Sigma-Aldrich (Merck) | 67-63-0 | 99.70% |
| LabSolutions Lite | Shimadzu | 223-60410 | Software for high-performance liquid chromatography system |
| Nanocrystalline TiO2 | Pure anatase with at least 99% crystallinity. Average particle size 10.62 ± 3.31 nm. Specific surface 131.9 m2/g (BET). See Langmuir 2019, 35, 538−550, for details. | ||
| Phenyl isothiocyanate | Acros Organics | 103-72-0 | PITC, 98% |
| Reversed-phase Zorbax column | ZORBAX LC | 150×2.5 mm i.d. with a mean particle size of 5 μm | |
| Syringe filter | Vladfilter | 25 mm, 0.2 μm pore, cellulose acetate | |
| Test sterile polymeric tube | polypropylene | ||
| Thermostat TC-502 | Brookfield | Refrigerating/heating circulating bath with the programmable controller for the sample derivatization | |
| Triethylamine | Sigma-Aldrich (Merck) | 121-44-8 | TEA; 99% |
| Trifluoroacetic acid | Panreac AppliChem | 163317 | TFA, 99% |
References
- Garcia, A. J. Interfaces to Control Cell-Biomaterial Adhesive Interactions. Polymers for Regenerative Medicine. 203, Chapter 71 171-190 (2006).
- Mahmood, T. A., et al. Modulation of chondrocyte phenotype for tissue engineering by designing the biologic-polymer carrier interface. Biomacromolecules. 7 (11), 3012-3018 (2006).
- Gandavarapu, N. R., Mariner, P. D., Schwartz, M. P., Anseth, K. S. Extracellular matrix protein adsorption to phosphate-functionalized gels from serum promotes osteogenic differentiation of human mesenchymal stem cells. Acta Biomaterialia. 9 (1), 4525-4534 (2013).
- Horbett, T. Biological Activity of Adsorbed Proteins. Surfactant Science Series. 110, 393-413 (2010).
- Ratner, B. D., Hoffman, A. S., Schoen, F. J., Lemons, J. E. Biomaterials Science: An Introduction to Materials in Medicine. , Elsevier Academic Press/Academic Press. San Diego. (2004).
- Jahangir, A. R., et al. Fluorinated surface-modifying macromolecules: Modulating adhesive protein and platelet interactions on a polyether-urethane. Journal of Biomedical Materials Research. 60 (1), 135-147 (2002).
- Shen, M., et al. PEO-like plasma polymerized tetraglyme surface interactions with leukocytes and proteins: In vitro and in vivo studies. Journal of Biomaterials Science, Polymer Edition. 13 (4), 367-390 (2002).
- Wisniewski, N., Moussy, F., Reichert, W. M. Characterization of implantable biosensor membrane biofouling. Fresenius' Journal of Analytical Chemistry. 366 (6-7), 611-621 (2000).
- Geelhood, S. J., et al. Passivating Protein Coatings for Implantable Glucose Sensors: Evaluation of Protein Retention. Journal of Biomedical Materials Research. Part B, Applied Biomaterials. 81, 251-260 (2007).
- Knowles, J. R. Enzyme catalysis: not different, just better. Nature. 350 (6314), 121-124 (1991).
- Blankschien, M. D., et al. Light-triggered biocatalysis using thermophilic enzyme - Gold nanoparticle complexes. ACS Nano. 7 (1), 654-663 (2013).
- Wu, H., et al. Catechol modification and covalent immobilization of catalase on titania submicrospheres. Journal of Molecular Catalysis B: Enzymatic. 92, 44-50 (2013).
- Gray, J. J. The interaction of proteins with solid surfaces. Current Opinion in Structural Biology. 14 (1), 110-115 (2004).
- Hlady, V., Buijs, J. Protein adsorption on solid surfaces. Current Opinion in Biotechnology. 7 (1), 72-77 (1996).
- Kulkarni, M., et al. Titanium nanostructures for biomedical applications. Nanotechnology. 26 (6), 062002(2015).
- Yin, F. Z., Wu, L., Gui Yang, H., Su, H. Y. Recent progress in biomedical applications of titanium dioxide. Physical Chemistry Chemical Physics. 15 (14), 4844-4858 (2013).
- Rezania, A., Johnson, R., Lefkow, A. R., Healy, K. E. Bioactivation of metal oxide surfaces. 1. Surface characterization and cell response. Langmuir. 15 (20), 6931-6939 (1999).
- Schenk, R. The Corrosion Properties of Titanium and Titanium Alloys. Titanium in Medicine. Brunette, D. M., et al. , Springer-Verlag. Berlin, Germany. 145-170 (2001).
- Bozzini, B., et al. An electrochemical impedance investigation of the behaviour of anodically oxidised titanium in human plasma and cognate fluids, relevant to dental applications. Journal of Materials Science: Materials in Medicine. 19 (11), 3443-3453 (2008).
- Popa, M. V., et al. Long-term assessment of the implant titanium material - Artificial saliva interface. Journal of Materials Science: Materials in Medicine. 19 (1), 1-9 (2008).
- Kim, J. K., et al. Lysozyme-mediated biomineralization of titanium-tungsten oxide hybrid nanoparticles with high photocatalytic activity. Chemical Communications. 50, 12392-12395 (2014).
- Suriyaraj, S. P., Selvakumar, R. Room temperature biosynthesis of crystalline TiO2 nanoparticles using Bacillus licheniformis and studies on the effect of calcination on phase structure and optical properties. RSC Advances. 4, 39619-39624 (2014).
- Inoue, I., et al. Thermo-stable carbon nanotube-TiO2 nanocompsite as electron highways in dye-sensitized solar cell produced by bio-nano-process. Nanotechnology. 26 (28), 285601(2015).
- Gardères, J., et al. Self-assembly and photocatalytic activity of branched silicatein/silintaphin filaments decorated with silicatein-synthesized TiO2 nanoparticles. Bioprocess and Biosystems Engineering. 39 (9), 1477-1486 (2016).
- Chen, H., Su, X., Neoh, K. G., Choe, W. S. QCM-D analysis of binding mechanism of phage particles displaying a constrained heptapeptide with specific affinity to SiO2 and TiO2. Analytical Chemistry. 78 (14), 4872-4879 (2006).
- Iucci, G., et al. Peptides adsorption on TiO2 and Au: Molecular organization investigated by NEXAFS, XPS and IR. Surface Science. 601 (18), 3843-3849 (2007).
- Gronewold, T. M. A., Baumgartner, A., Weckmann, A., Knekties, J., Egler, C. Selection process generating peptide aptamers and analysis of their binding to the TiO2 surface of a surface acoustic wave sensor. Acta Biomaterialia. 5 (2), 794-800 (2009).
- Gitelman, A., Rapaport, H. Bifunctional designed peptides induce mineralization and binding to TiO2. Langmuir. 30 (16), 4716-4724 (2014).
- Tada, S., Timucin, E., Kitajima, T., Sezerman, O. U., Ito, Y. Direct in vitro selection of titanium-binding epidermal growth factor. Biomaterials. 35 (11), 3497-3503 (2014).
- Micksch, T., Liebelt, N., Scharnweber, D., Schwenzer, B. Investigation of the peptide adsorption on ZrO2, TiZr, and TiO2 surfaces as a method for surface modification. ACS Applied Materials and Interfaces. 6 (10), 7408-7416 (2014).
- Limo, M. J., Perry, C. C., Thyparambil, A. A., Wei, Y., Latour, R. A. Experimental Characterization of Peptide-Surface Interactions. Bio-Inspired Nanotechnology: From Surface Analysis to Applications. , 37-94 (2013).
- Draczkowski, P., Matosiuk, D., Jozwiak, K. Isothermal titration calorimetry in membrane protein research. Journal of Pharmaceutical and Biomedical Analysis. 87, 313-325 (2014).
- Omanovic-Miklicanin, E., Manfield, I., Wilkins, T. Application of isothermal titration calorimetry in evaluation of protein-nanoparticle interactions. Journal of Thermal Analysis and Calorimetry. 127, 605-613 (2017).
- Jing, X., et al. Interaction of peptidomimetics with bilayer membranes: Biophysical characterization and cellular uptake. Langmuir. 28 (11), 5167-5175 (2012).
- Mizuguchi, C., et al. Effect of phosphatidylserine and cholesterol on membrane-mediated fibril formation by the N-terminal amyloidogenic fragment of apolipoprotein A-I. Scientific Reports. 8 (1), 5497(2018).
- Bisker, G., et al. Insulin Detection Using a Corona Phase Molecular Recognition Site on Single-Walled Carbon Nanotubes. ACS Sensors. 3 (2), 367-377 (2018).
- Singh, N., Husson, S. M. Adsorption thermodynamics of short-chain peptides on charged and uncharged nanothin polymer films. Langmuir. 22 (20), 8443-8451 (2006).
- Seker, U. O. S., et al. Thermodynamics of engineered gold binding peptides: Establishing the structure-activity relationships. Biomacromolecules. 15 (7), 2369-2377 (2014).
- Beutner, R., Michael, J., Schwenzer, B., Scharnweber, D. Biological nano-functionalization of titanium-based biomaterial surfaces: A flexible toolbox. Journal of the Royal Society Interface. 7 (Suppl 1), S93-S105 (2010).
- Sultan, A. M., et al. Aqueous Peptide-TiO2 Interfaces: Isoenergetic Binding via Either Entropically or Enthalpically Driven Mechanisms. ACS Applied Materials and Interfaces. 8 (28), 18620-18630 (2016).
- Teichroeb, J. H., Forrest, J. A., Jones, L. W., Chan, J., Dalton, K. Quartz crystal microbalance study of protein adsorption kinetics on poly(2-hydroxyethyl methacrylate). Journal of Colloid and Interface Science. 325 (1), 157-164 (2008).
- Lok, B. K., Cheng, Y. L., Robertson, C. R. Protein adsorption on crosslinked polydimethylsiloxane using total internal reflection fluorescence. Journal of Colloid And Interface Science. 91 (1), 104-116 (1983).
- Nakanishi, K., Sakiyama, T., Imamura, K. On the Adsorption of Proteins on Solid Surfaces, a Common but Very Complicated Phenomenon. Journal of Bioscience and Bioengineering. 91 (3), 233-244 (2001).
- Roddick-Lanzilotta, A. D., Connor, P. A., McQuillan, A. J. An In Situ Infrared Spectroscopic Study of the Adsorption of Lysine to TiO2 from an Aqueous Solution. Langmuir. 14, 6479-6484 (1998).
- Roddick-Lanzilotta, A. D., McQuillan, A. J. An in situ infrared spectroscopic investigation of lysine peptide and polylysine adsorption to TiO2 from aqueous solutions. Journal of Colloid and Interface Science. 217 (1), 194-202 (1999).
- Roddick-Lanzilotta, A., McQuillan, A. An in situ infrared spectroscopic study of glutamic acid and of aspartic acid adsorbed on TiO2: implications for the biocompatibility of titanium. Journal of Colloid and Interface Science. 227 (1), 48-54 (2000).
- Chan, B. M. C., Brash, J. L. Adsorption of fibrinogen on glass: reversibility aspects. Journal of Colloid And Interface Science. 82 (1), 217-225 (1981).
- van Enckevort, H. J., Dass, D. V., Langdon, A. G. The adsorption of bovine serum albumin at the stainless-steel/aqueous solution interface. Journal of Colloid And Interface Science. 98 (1), 138-143 (1984).
- Arnebrant, T., Nylander, T. Sequential and competitive adsorption of β-lactoglobulin and κ-casein on metal surfaces. Journal of Colloid And Interface Science. 111 (2), 529-533 (1986).
- Van Dulm, P., Norde, W. The adsorption of human plasma albumin on solid surfaces, with special attention to the kinetic aspects. Journal of Colloid And Interface Science. 91 (1), 248-255 (1983).
- Gonçalves, T. Fluorescent labeling of biomolecules with organic probes. Chemical Reviews. 109 (1), 190-212 (2009).
- Roth, K. D. W., Huang, Z. H., Sadagopan, N., Watson, J. T. Charge derivatization of peptides for analysis by mass spectrometry. Mass Spectrometry Reviews. 17 (4), 255-274 (1998).
- AppliChem, P. Safety Data Sheet According to Regulation (EU) 830/2015 3317 Trifluoroacetic Acid. , http://pub.panreac.com/msds/ing/3317.htm 112(2018).
- Heinrikson, R. L., Meredith, S. C. Amino acid analysis by reverse-phase high-performance liquid chromatography: Precolumn derivatization with phenylisothiocyanate. Analytical Biochemistry. 136 (1), 65-74 (1984).
- Shchelokov, A., et al. Adsorption of Native Amino Acids on Nanocrystalline TiO2: Physical Chemistry, QSPR, and Theoretical Modeling. Langmuir. 35 (2), 538-550 (2019).
- Fair, B. D., Jamieson, A. M. Studies of Protein Adsorption on Polystyrene Latex Surfaces. Journal of Colloid and Interface Science. 77 (2), 525-534 (1980).
- Kim, J. C., Lund, D. B. Adsorption behavior of p-lactoglobulin onto stainless steel surfaces. Journal of Food Processing and Preservation. 21 (607), 303-317 (1997).
- Kondo, A., Oku, S., Murakami, F., Higashitani, K. Conformational changes in protein molecules upon adsorption on ultrafine particles. Colloids and Surfaces B: Biointerfaces. 1, 197-201 (1993).
- Itoh, H., Nagai, T., Saeki, T., Sakiyama, T., Nakanishi, K. Adsorption of Protein onto Stainless Steel Particle Surface and its Desorption Behavior. Developments in Food Engineering. , 811-813 (1994).
- Itoh, H., Nagata, A., Toyomasu, T., Sakiyama, T., Nagai, T. Adsorption of β-Lactoglobulin onto the Surface of Stainless Steel Particles. Bioscience, Biotechnology, and Biochemistry. 59 (9), 1648-1651 (1995).
- Mudunkotuwa, I. A., Grassian, V. H. Histidine adsorption on TiO2 nanoparticles: An integrated spectroscopic, thermodynamic, and molecular-based approach toward understanding nano-bio interactions. Langmuir. 30, 8751-8760 (2014).
- Pászti, Z., Guczi, L. Amino acid adsorption on hydrophilic TiO2: A sum frequency generation vibrational spectroscopy study. Vibrational Spectroscopy. 50 (1), 48-56 (2009).
- Costa, D., Savio, L., Pradier, C. M. Adsorption of Amino Acids and Peptides on Metal and Oxide Surfaces in Water Environment: A Synthetic and Prospective Review. Journal of Physical Chemistry B. 120 (29), 7039-7052 (2016).
- Kosmulski, M. The significance of the difference in the point of zero charge between rutile and anatase. Advances in Colloid and Interface Science. 99 (3), 255-264 (2002).
- Kandegedara, A., Rorabacher, D. B. Noncomplexing tertiary amines as "better" buffers covering the range of pH 3-11. Temperature dependence of their acid dissociation constants. Analytical Chemistry. 71 (15), 3140-3144 (1999).
- Susumu, O., Teruaki, A., Koichi, T. The Adsorption of Basic a-Amino Acids in an Aqeous Solution by Titanium(IV) Oxide. Bulletin of the Chemical Society of Japan. 54, 1595-1599 (1981).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved