Method Article
Повторная транскраниальная магнитная стимуляция в сочетании с тренировкой по наблюдению за действием у детей со спастическим церебральным параличом
В этой статье
Резюме
У детей со спастическим церебральным параличом (ПКП) наблюдается спастичность конечностей, двигательные расстройства и ненормальная осанка из-за травмы моторной области коры головного мозга, что приводит к неспособности нормально стоять и ходить. Таким образом, облегчение спастичности конечностей и улучшение крупной моторной функции у детей с УПП стали важными терапевтическими целями.
Аннотация
В этом исследовании представлены результаты рандомизированного контролируемого исследования с использованием факторного дизайна 2 x 2, в котором сравнивались эффекты повторной транскраниальной магнитной стимуляции (рТМС) и методов обучения наблюдению за действием (АОТ) на спастичность, функцию равновесия и моторную функцию у детей со спастическим церебральным параличом (ПКП). Исследование было направлено на то, чтобы выяснить, приводит ли комбинация этих двух вмешательств к большему улучшению, чем лечение по отдельности или традиционное лечение.
Испытуемые дети в данном исследовании, в соответствии с таблицей случайных чисел, были случайным образом разделены на четыре группы: конвенциональная группа, группа рТМС, группа АОТ и группа комбинированного вмешательства. Все дети четырех групп получали традиционное восстановительное лечение, на основании которого им были назначены различные терапевтические программы реабилитационных мероприятий. Традиционная группа не получала другого лечения, в то время как группа рТМС получала рТМС, группа АОТ получала АОТ, а группа комбинированного вмешательства получала комбинированное вмешательство в виде рТМС и АОТ. Их обучали пять дней в неделю в течение 12 недель. Изменения в показателях спастичности, функции равновесия, способности ходить и крупной моторной функции оценивались в начале программы тренировок и по завершении 12-недельного лечения.
В исследовании приняли участие 64 ребенка с УПП, результаты которых были проанализированы. Общая эффективность валовой моторной функции в 87,50% в экспериментальной группе была значительно выше, чем 25,00% в обычной группе, 62,50% в группе рТМС и 68,75% в группе АОТ. Предварительные результаты показали, что комбинированное вмешательство рТМС и АОТ может эффективно улучшить функцию равновесия и моторную функцию детей, а терапевтический эффект комбинированного вмешательства был лучше, чем у традиционного лечения, рТМС или только АОТ. Наконец, уточнена клиническая эффективность и оптимальные параметры лечения комбинированного вмешательства с целью обеспечения клинической основы для проведения терапевтами реабилитации функции нижних конечностей у детей с УПП.
Введение
Церебральный паралич1 (ДЦП) является одним из наиболее распространенных инвалидизирующих расстройств у детей и представляет собой группу стойких синдромов, вызванных непрогрессирующим повреждением головного мозга у развивающихся плодов и младенцев, включая центральную дискинезию, аномальную осанку и ограниченную подвижность. В настоящее время во всем мире насчитывается около 17 миллионов детей, страдающих церебральным параличом2, из них более 5 миллионов случаев в Китае. Среди различных форм детского церебрального паралича спастический церебральный паралич (ПКП) составляет примерно 80%3. Дети с SCP страдают от повреждения головного мозга, приводящего к мышечным спазмам, снижению сенсорных функций, нарушению мышечной координации и снижению способности к равновесию, что препятствует самостоятельной ходьбе и повседневной деятельности. Современные реабилитационные мероприятия для улучшения крупной моторной функции у детей с УПП включают в себя такие виды деятельности, как тренировка стабильности ядра4, ориентированная на задачу тренировка5, двигательная терапия, вызванная ограничениями6 и терапия зеркальной визуальной обратнойсвязью 7. Эти меры могут улучшить клинические симптомы у детей за счет регуляции и изменения центральной нервной системы снизу вверх за счет улучшения функций периферических органов.
Транскраниальная магнитная стимуляция (ТМС)8,9 является безболезненным, неинвазивным и безопасным терапевтическим методом. рТМС относится к непрерывному высвобождению стимулов через равные промежутки времени после одной команды, что является одним из регулярных повторяющихся паттернов стимуляции. Основанный на принципе электромагнитной индукции и электромагнитного преобразования, он применяет переходные токи через стимулирующие катушки для формирования импульсного магнитного поля, проникающего в череп, генерирующего индукционный ток для стимуляции нейронов и запускающего ряд физиологических и биохимических реакций. ТМС применяется для мониторинга, оценки и лечения неврологических заболеваний, обеспечивая новый подход к изучению структуры и функции мозга10. Существующие исследования11,12 показали, что рТМС оказывает различное терапевтическое воздействие на спазмы конечностей и двигательную функцию у детей с ДЦП. Более того, эффект от лечения рТМС в сочетании с другими реабилитационными методиками более заметен.
АОТ — это метод реабилитации, в котором используется система зеркальных нейронов (MNS) для формирования моторного обучения и памяти13,14. Суть АОТ заключается в том, чтобы наблюдатель внимательно наблюдал за действиями на видео и впоследствии старался изо всех сил имитировать то, что он увидел. Процесс наблюдения может вызвать активацию в нейронной сети, известной как MNS, сродни активации, которая происходит, когда человек лично участвует в выполненииэтих действий, что обеспечивает нейрофизиологическую основу для АОТ. АОТ показала успех в улучшении двигательных навыков у пациентов с двигательными нарушениями, что дает положительные результаты в восстановлении после инсульта и реабилитации двигательной функции верхних конечностей у пациентов с церебральным параличом16,17.
Наши предыдущие исследования показали, что АОТ на основе системы зеркальных нейронов может эффективно улучшить равновесие и способность ходить у детей с церебральнымпараличом. Кроме того, исследования19 показали, что рТМС может улучшать мышечную спастичность, движение и походку у детей с УПП, но стандарты лечения рТМС, применяемые к детям с ДЦП, не были унифицированы, и актуальной проблемой является изучение влияния различных параметров рТМС на детей с ДЦП, чтобы обеспечить персонализированный и точный стандарт лечения. Мы считаем, что сочетание рТМС с АОТ может стать ценной стратегией физиотерапии для неврологической реабилитации при церебральном параличе. Как рТМС, так и АОТ стимулировали кору головного мозга у детей с SCP20, тем самым способствуя развитию крупной моторной функции. Это исследование было направлено на то, чтобы выяснить, может ли комбинация рТМС и АОТ достичь большего синергетического эффекта, чем традиционное лечение или только рТМС или АОТ.
протокол
Это исследование было проведено в строгом соответствии с национальными стандартами экспериментов на людях, а клиническое исследование было одобрено Этической ассоциацией реабилитационной больницы Сянъя Боай (номер этического одобрения: 20211223). Опекуны детей дали согласие на участие в данной обучающей программе и подписали формы информированного согласия. Дети с УПП были набраны в реабилитационной больнице Сянъя Боай и больнице Сянъя Центрального южного университета с февраля 2022 года по декабрь 2022 года.
1. Подготовка перед экспериментом
- Чтобы обеспечить точность результатов исследования, проведите соответствующее обучение реабилитологов и заранее оцените их навыки, чтобы убедиться, что они могут направлять детей в обучении.
ПРИМЕЧАНИЕ: Технические специалисты rTMS должны быть обучены и квалифицированы для обеспечения безопасности детей. - Проведите скрининг безопасности ТМС с родителями перед экспериментом, в том числе опросите их о признаках судорог и принимаемых лекарствах.
ПРИМЕЧАНИЕ: Лекарства могут снизить порог судорог.
2. Подбор персонала
- Набирать детей с УПП, клинический диагноз и классификация которых соответствуют критериям Китайского руководства по реабилитационному лечению церебрального паралича (2022)21.
- Убедитесь, что детям от 3 до 6 лет.
- Убедитесь, что коэффициент развития адаптивной поведенческой зоны (DQ) > 55 у детей по шкале Гезелла Developmental Diagnostic Scale (GDDS), чтобы они могли активно участвовать в тренировках.
- Убедитесь, что у детей есть классификация крупной моторной функции (GMFCS) I-III.
- Убедитесь, что дети могут пройти более 10 м самостоятельно или с ходунками.
- Исключить: детей с другими видами ДЦП; детям, которым была назначена медицинская реабилитация или хирургическое вмешательство в период обучения; дети с эпилепсией, тяжелыми интеллектуальными нарушениями, нарушениями зрения или дефицитом внимания; Дети с кохлеарными имплантатами или внутричерепными имплантатами.
- Перед началом тренинга получите формы информированного согласия от опекунов детей на добровольное участие в данной обучающей программе 1 раз в день, 5 дней в неделю в течение 12 недель.
3. Оценка перед обработкой
- Проанализируйте исходные данные, собранные у отобранных детей с УПП, включая имя, пол, возраст, тип спастичности церебрального паралича, GMFCS, когнитивный уровень, ношение ортеза голеностопного сустава, предыдущее или текущее медицинское лечение и хирургический анамнез.
- Оценка реабилитации
ПРИМЕЧАНИЕ: Исследования показали, что Комплексная шкала спастичности (CSS), используемая для оценки степени спазма нижних конечностей у детей с SCP, обладает хорошей надежностью и валидностью22.- Определить степень спазма можно с помощью обследования ахиллова сухожильного рефлекса нижней конечности, мышечного напряжения группы подошвенных сгибателей голеностопного сустава и клонуса голеностопного сустава. Используйте следующие критерии оценки: отсутствие спазма, <7; слабый спазм, 7-9; умеренный спазм, 10-12; и сильный спазм, 13-16.
- Оцените функцию равновесия в соответствии с Педиатрической шкалой равновесия (PBS)23, которая включает 14 протестированных пунктов. Каждый предмет разделен на пять уровней по 0-4 балла за каждый предмет и 56 баллов в сумме. Чем выше балл, тем лучше функция баланса.
ПРИМЕЧАНИЕ: PBS основан на BBS Children's Revision, в основном корректируя порядок тестируемых элементов, сокращая время на поддержание осанки и уточняя инструкции к тесту. - Оцените способность детей к ходьбе на основе скорости ходьбы 10 м (10MWS)24.
- Попросите детей как можно быстрее ходить по взлетно-посадочной полосе с параметрами ширина x длина = 20 см x 15 м, самостоятельно или в ортопедическом стельке для голеностопного сустава или с использованием приспособления для ходьбы для детей с GMFCS класса III.
- Попросите детей начать ходить с отметки 15 м; Начните отсчет времени с 12 м, и остановитесь на 2 м, чтобы измерить время, затраченное на средние 10 м. Попросите детей выполнить три последовательных теста 10MWT и рассчитать скорость ходьбы (м/с).
ПРИМЕЧАНИЕ: Функциональный уровень детей был оценен как I-III в соответствии с GMFCS, что означает, что у них есть определенная способность стоять и ходить. - Оцените уровень крупной моторики детей, выбрав положение стоя в области D (13 предметов) и ходьбу, бег и прыжки в зоне E (24 пункта) в измерении крупной моторной функции (GMFM). Рассчитайте балл в соответствии со степенью выполнения каждого элемента (0-3 балла) и получите общий балл зон D и E. Чем выше балл, тем лучше крупная моторная функция.
- Рассчитайте уровень эффективности с помощью уравнений (1) и (2) и оцените клиническую эффективность вмешательств по развитию крупной моторной функции путем измерения разницы в баллах от секции GMFM-88E до и после лечения.
Коэффициент эффективности (%) =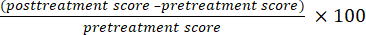 (1)
(1)
Коэффициент эффективности = значимый эффективный коэффициент + эффективный коэффициент (2)- Считайте, что результат является значительно эффективным, если уровень эффективности составляет >50%.
- Считайте, что результат эффективен, если уровень эффективности составляет от 20% до 50%.
- Считайте результат неэффективным, если уровень эффективности составляет <20%.
4. Терапевтический метод
ПРИМЕЧАНИЕ: Объясните опекунам детей принципы и цели программы обучения, а также возможные неблагоприятные последствия и проблемы безопасности во время тренировочного процесса.
- Случайным образом разделите детей с УПП на четыре различные группы: обычную группу, группу рТМС, группу АОТ и группу комбинированного вмешательства в соответствии с методом числовой таблицы (по 16 случаев в каждой группе в этом исследовании).
- Обеспечить, чтобы все дети получали традиционное реабилитационное лечение, на основании которого им будут назначены различные реабилитационные лечебные мероприятия. Традиционная группа не получает никакого другого реабилитационного лечения; группа rTMS получает rTMS; группа АОТ получает АОТ; и исследуемая группа получает рТМС в сочетании с АОТ.
- Подробно разъясните семьям испытуемых детей возможности их участия в обучающих программах традиционной реабилитации, рТМС, АОТ, а также комбинированных вмешательств. Убедитесь, что исследователи не обращают внимания на распределение предметов и не участвуют в оценке.
- В соответствии с порядком поступления этих детей сформируйте числовой список в виде таблицы. Рандомизируйте в группы следующим образом: числа 1, 5, 9... для обычной группы; номера 2, 6, 10... для группы rTMS; номера 3, 7, 11... для группы АОТ; и номера 4, 8, 12... для группы комбинированного вмешательства. Чтобы обеспечить уединение, используйте занавеску, чтобы предоставить каждому ребенку отдельное пространство во время каждого сеанса лечения.
- Традиционная реабилитация
- Лечебная физкультура
- Разъясните опекунам детей принцип и цель лечебной физкультуры и предупредите их, что продолжительность процедуры составляет 30 минут.
- В соответствии с их рейтингом мышечной силы проинструктируйте детей выполнять упражнения на мышечную силу для тренировки мышц отвода бедра, мышц заднего разгибателя бедра и мышц тыльного разгибания голеностопного сустава 10 раз в подход и три подхода в день.
- В соответствии с уровнем функции равновесия проинструктируйте детей проводить тренировку равновесия, например, стоять без поддержки, стоять с ногами вместе и стоять на одной ноге, продолжительностью 10 минут каждый раз.
- В зависимости от их способности ходить проинструктируйте детей о выполнении упражнений по ходьбе, таких как удержание на руках, самостоятельное хождение и преодоление препятствий, продолжительностью каждый раз 10 минут.
- Гидротерапия
- Разъясните опекунам детей принцип, процесс и цель гидротерапии и предупредите их, что продолжительность процедуры составляет 20 минут.
- При использовании специального аппарата для гидротерапии для детей отрегулируйте температуру воды до соответствующей температуры 37-38 °C.
- Попросите родителей помочь детям снять одежду, надеть водонепроницаемые плавки и ошейники для гидротерапии, а затем посадить их в аппарат для гидротерапии.
- Нажмите на кнопку с пеной для ванны, чтобы начать лечение, и попросите детей встать, повернуться и делать шаги поочередно, стоя обеими ногами в воде.
- Массажная процедура
- Сначала поставьте детям диагноз.
- Объясните опекунам детей эффект от массажа и сообщите им, что продолжительность процедуры составляет 30 минут.
- Поместите детей в положение лежа и применяйте чередующиеся техники сжатия и надавливания 5-10 раз вдоль обеих сторон коронарной артерии и меридиана мочевого пузыря.
- Поместите детей в положение лежа и нажмите, используя кончик большого пальца, на акупунктурные точки Футу, Лянцю, Цзусанли, Цзеси, Хуаньяо, Чэнфу и Уйчжун сверху вниз.
- Поместите детей в положение лежа на спине или лежа и применяйте ритмичные подъемы и сжатия 10-20 раз большим пальцем и другими четырьмя пальцами поочередно на квадрицепсы, подколенные сухожилия и икроножную мышцу трицепса одновременно.
- Лечебная физкультура
- рТМС
ПРИМЕЧАНИЕ: Физиотерапевт, занимающийся выполнением рТМС, сначала принял участие в тренинге, организованном производителем. Для безопасности участников терапевт или другие обученные медицинские работники должны контролировать весь процесс лечения и заранее информировать опекунов о том, что пульс, генерируемый рТМС, может вызвать временную и легкую боль и легкое подергивание лица и конечностей при попадании на кожу головы.- рТМС подготовка пациента
- При первом посещении сообщите физиотерапевту основную информацию и историю болезни испытуемых детей.
- Объясните процесс лечения рТМС и возможные ответы опекунам детей и сообщите им, что продолжительность лечения составляет примерно 30 минут.
- Положите детей в положение лежа на спине или сидя, обезжирьте их руки медицинским спиртом и выберите подходящую шапочку для позиционирования для каждого из них в соответствии с окружностью головы. Поместите носо-затылочную линию на позиционирующий колпачок на срединную линию участвующих детей, а точку пересечения носо-затылочной линии и височной теменной линии — в середине линии между бровью и затылочным задним килем.
ПРИМЕЧАНИЕ: Подходящий размер должен быть выбран в соответствии с окружностью головы. - Прикрепите регистрирующий электрод к мышце живота отводящего большого отведения у участвующих детей, электрод сравнения — к сухожилию отводящей большой мышцы, а нижний электрод — к запястью.
- Подготовка к работе rTMS
- Запустите компьютерное приложение на приборе rTMS, введите основную информацию и диагнозы участвующих детей, а также определите план лечения.
- Катушка стимуляции представляет собой круглую катушку с воздушным охлаждением, центр которой совпадает с контралатеральной областью М1, соответствующей идентифицированному abductor pollicis brevis. Поместите спираль под углом 45° к коже головы.
ПРИМЕЧАНИЕ: Позиционирующий колпачок был разработан в соответствии с системой расположения электродов электроэнцефалографии (ЭЭГ) 10-20, которая могла быстро локализовать область M1. - Выберите интенсивность стимуляции 30% и стимулируйте область М1, соответствующую контралатеральной абдукторной мышце pollicis brevis, с помощью мануального моноимпульса.
ПРИМЕЧАНИЕ: Во время лечения участвующие дети должны оставаться в своем положении, чтобы избежать отклонения от цели стимуляции. - Наблюдайте за графиком интерфейса моторных вызванных потенциалов и постепенно снижайте интенсивность стимуляции. Определите РМТ как минимальную интенсивность стимула, которая вызовет эту реакцию, если по крайней мере 5 из 10 последовательных стимуляций первичной моторной коры головного мозга ребенка (М1) вызывают силу двигательного потенциала более 50 мВ в контралатеральной абдукторной мышце hallucis brevis (рис. 1А).
- Нажмите на кнопку подтверждения , сохраните запись RMT, а затем войдите на страницу настройки параметров лечения .
- Лечение рТМС
- Для выполнения низкочастотной стимуляции в области М1 неповрежденной коры головного мозга используются следующие настройки: частота стимуляции 1 Гц, интенсивность стимуляции 80% RMT, число стимуляции 10, время стимуляции 10 с, количество повторений 80, общее количество импульсов 80025,26 (см. рисунок 1Б).
- Для выполнения высокочастотной стимуляции области М1 поврежденной коры головного мозга используйте следующие настройки: частота стимуляции 5 Гц, интенсивность стимуляции 100% RMT, число стимуляции 15, время стимуляции 3 с, повторение 80 раз, общее количество импульсов 120010 (см. рисунок 1C).
- Понаблюдайте за реакцией участвующих детей. Например, если дети начинают плакать из-за биения кожи головы, у них наблюдаются чрезмерные подергивания лица или появляются признаки судорог и других побочных реакций, немедленно прекратите лечение.
Примечание: У детей со спастической диплегией/квадриплегией высокочастотная стимуляция области М1 поврежденной коры головного мозга проводилась поочередно с обеих сторон поврежденного мозга. У пациентов со спастической гемиплегией область М1 неповрежденной коры головного мозга стимулировалась с низкой частотой, в то время как поврежденная кора головного мозга области М1 стимулировалась с высокой частотой.
- рТМС подготовка пациента
- АОТ
ПРИМЕЧАНИЕ: АОТ требует, чтобы физиотерапевты заранее снимали на видео движения тела испытуемых и контролировали безопасность и точность тренировки всего процесса лечения.- Объясните опекунам детей принцип, процесс и меры предосторожности при лечении АОТ и сообщите им, что продолжительность лечения составляет 30 минут.
- Попросите двух профессиональных физиотерапевтов снять на видео движения тела с трех разных углов: спереди, сбоку и сзади, и разработают шесть движений тела с целью улучшения баланса нижних конечностей и функции ходьбы.
- Первое движение идет из сидячего положения в стоячее: переместите корпус вперед из вертикального положения сидя, поднимая таз и разгибая коленный сустав, постепенно переходя в положение стоя, а затем садитесь. Выполните это 3 раза подряд (рисунок 2A).
- Второе движение – упражнение стоя: переместите вес тела влево или вправо как можно дальше, а затем вернитесь в нейтральное положение. Выполните его 3 раза по очереди (Рисунок 2B).
- Третье движение также является упражнением стоя: переместите вес тела вперед или назад как можно дальше и затем вернитесь в нейтральное положение. Выполните его 3 раза по очереди (рисунок 2C).
- Четвертое движение также является упражнением стоя: поверните корпус влево или вправо как можно дальше и затем вернитесь в нейтральное положение. Выполните его 3 раза по очереди (Рисунок 2D).
- Пятое движение представляет собой упражнение стоя: пройдитесь боком влево или вправо и затем вернитесь в нейтральное положение. Выполните его 3 раза по очереди (рисунок 2E).
- Шестое движение – упражнение стоя: поочередно шагайте вверх или вниз по ступеньке высотой 10 см левой и правой ногой. Выполните его 3 раза по очереди (Рисунок 2F).
- Соберите детей в тихой комнате и сядьте в 5 м от 86-дюймового телевизора в удобных положениях.
- Пусть физиотерапевт сначала объяснит движения тела, чтобы дети могли сосредоточиться на просмотре видео.
- После просмотра видео попросите детей повторить эти движения.
5. Оценка после лечения
ПРИМЕЧАНИЕ: Предварительное лечение и оценка в течение 12 недель после лечения для каждого пациента будут проводиться одним и тем же педиатрическим врачом-реабилитологом.
- После 12 недель различных реабилитационных мероприятий для четырех групп детей один и тот же детский врач-реабилитолог повторно оценит клиническую эффективность CSS, PBS, 10 MWS, GMFM и крупной моторной функции.
- Записывайте удовлетворенность опекунов и отзывы о плане лечения, в том числе степень удовольствия от лечения и улучшение самосознания, а также их пожелания и предложения по продолжению лечения.
6. Статистический анализ
- Введите демографические данные, CSS, PBS, скорость ходьбы 10 м (10MWS), GMFM и оценку эффективной скорости (%) в программное обеспечение для статистического анализа.
- Анализируйте данные подсчета с помощью теста χ2 или вероятностного метода Фишера.
- Определите, соответствуют ли данные нормальному распределению, и выразите нормально распределенные данные в виде среднего значения ± SD.
- Используйте анализ отклонения повторяющихся измерений для сравнения между четырьмя группами и выполните анализ дисперсии повторных измерений в рамках смешанной модели, чтобы проверить, согласуются ли результаты и оценки вариации каждой группы с приблизительно нормальным распределением.
- Рассматривайте время как внутригрупповой фактор, а вмешательство – как межгрупповой фактор. Если между этими двумя факторами существует какое-либо взаимодействие, проверьте межгрупповую разницу в каждой временной точке при a= 0,05. Если эффекта взаимодействия нет, протестируйте основной эффект. Рассматривайте различия как статистически значимые при P < 0,05.
Результаты
В данной работе представлены результаты обследования 64 детей с УПП (Дополнительная таблица S1 и Дополнительный файл 1), которые были случайным образом разделены на четыре группы по методу числовой таблицы и получили различные реабилитационные мероприятия в течение 12 недель. В течение всего процесса у участвующих детей не было никаких побочных реакций, таких как головные боли, головокружение и судороги.
Демографические данные по четырем группам детей приведены в таблице 1. До начала лечения не было существенных различий в соотношении полов, возрасте, спастической категории церебрального паралича, GMFCS, коэффициенте развития GDDS (GDDS DQ) и использовании вспомогательных устройств (голеностопного ортеза или ходунков) (все P > 0,05).
Баллы CSS четырех групп детей до и после 12-недельного лечения были сравнены в таблице 2. После 12 недель тренировок показатели CCS во всех четырех группах значительно снизились, при этом группа комбинированного вмешательства показала значительно большие изменения, чем другие три группы. Эффект времени и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами не был значимым (P > 0,05).
Баллы PBS, 10MWS и GMFM до и после 12-недельного обучения четырех групп показаны в таблицах 3, 4 и 5. По сравнению с предтренировочными показателями, баллы PBS, 10MWS и GMFM всех четырех групп значительно увеличились после лечения, при этом показатели группы комбинированного вмешательства улучшились больше всего. Эффект времени и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами не был значимым (P > 0,05).
Клиническое влияние на крупную моторику во всех четырех группах детей представлено в таблице 6. Общая эффективность валовой моторной функции в группе комбинированного вмешательства составила 87,50%, что было достоверно выше, чем в остальных трех группах (группа рТМС 62,50%, группа АОТ 68,75%, традиционная группа 25,00%) (χ2 = 13,850, P = 0,003).
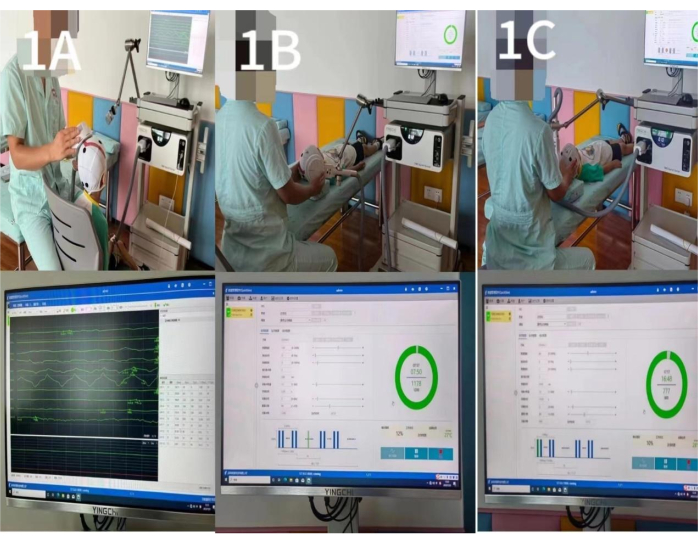
Рисунок 1: Стимуляция области M1. (A) Определение порога: Значение RMT измерялось, когда контралатеральная область M1, соответствующая отводящей мышце, стимулировалась одним импульсом для создания потенциала, вызванного движением. (Б) Низкочастотная стимуляция в области М1 неповрежденной коры головного мозга: частота стимуляции составила 1 Гц, интенсивность стимуляции составила 80% RMT, число стимуляции – 10, время стимуляции – 10 с, количество повторений – 80 раз, общее количество импульсов – 800. (В) Высокочастотная стимуляция области М1 поврежденной коры головного мозга: частота стимуляции составила 5 Гц, интенсивность стимуляции составила 100% РМТ, число стимуляции – 15, время стимуляции – 3 с, повторение – 80 раз, общее количество импульсов – 1200. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 2: Тренировка наблюдения за действием. (A) Первое движение: Преобразование из сидячего положения в стоп. (Б) Второе движение: смещение веса влево/вправо. (В) Третье движение: перемещение веса тела вперед/назад. (D) Четвертое движение: вращение влево/вправо. (Д) Пятое движение: ходьба влево/вправо. (F) Шестое движение: шаг вверх/вниз поочередно. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
| (n=64, x±с) | |||||||||
| Пункт | Традиционная группа | Группа rTMS | Группа АОТ | Группа комбинированного вмешательства | χ2 /F | P | |||
| Номер (n) | 16 | 16 | 16 | 16 | |||||
| Соотношение полов (мужской/женский) | 10/6 | 10/6 | 13/3 | 9/7 | 2.494 | 0.476 | |||
| Возраст (год) | 4,44±0,80 | 4,74±0,68 | 4,71±0,54 | 4,63±0,68 | 0.654 | 0.683 | |||
| Классификация спастического детского церебрального паралича (спастическая hemip legia/спастическая дип-легия/спастическая квадриплегия) | 02-07-2007 | 5/10/1 | 6/9/1 | 5/10/1 | 2.105 | 0.945 | |||
| GMFCS (n) (Уровень I/II/III) | 7/3/6 | 6/5/5 | 8/5/3 | 8/5/3 | 2.750 | 0.868 | |||
| GDDS DQ | 70.06±10.25 | 70.13±9.44 | 71.56±12.58 | 69.25±6.89 | 0.148 | 0.931 | |||
| Использование вспомогательных устройств (n) Да/Нет | 5/11 | 3/13 | 3/13 | 4/12 | 1.780 | 0.699 | |||
Таблица 1: Сравнение исходной информации четырех групп детей (n = 64, x ± с). * Односторонний дисперсионный анализ. До тренинга не было выявлено достоверных различий в соотношении полов, возрасте, спастической категории ДЦП, GMFCS, коэффициенте развития GDDS (GDDS DQ) и использовании вспомогательных приспособлений (голеностопного ортеза стопы или ходунков), что указывает на сопоставимость. Сокращения: GMFCS = Классификация крупной моторной функции; GDDS DQ = График диагностики развития по шкале Гезелла.
| Группа | Номер (n) | ПЕРЕД | ПОСЛЕ | F | P | ||
| Традиционная группа | 16 | 10.63±1.67 | 10.19±1.76 | ||||
| Группа rTMS | 16 | 10.88±1.41 | 9.75±1.13 | ||||
| Группа АОТ | 16 | 10.75±1.13 | 9.75±1.00 | ||||
| Группа комбинированного вмешательства | 16 | 10.69±1.01 | 8.88±1.02 | ||||
| Групповой фактор | 0.774 | 0.513 | |||||
| Фактор времени | 228.261 | <0,001 | |||||
| Групповой фактор * Временной фактор | 15.217 | <0,001 | |||||
Таблица 2: Сравнение баллов по CSS в четырех группах детей (n = 64, x ± s). После лечения результаты повторного измерения ANOVA показали, что эффект времени и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами был незначимым (P > 0,05). Сокращения: CSS = комплексная шкала спастичности; rTMS = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием.
| Группа | Номер (n) | ПЕРЕД | ПОСЛЕ | F | P | ||
| Традиционная группа | 16 | 28.25±9.38 | 31.13±9.22 | ||||
| Группа rTMS | 16 | 29.44±10.05 | 35.56±9.82 | ||||
| Группа АОТ | 16 | 29.25±9.84 | 35.94±8.62 | ||||
| Группа комбинированного вмешательства | 16 | 29.81±11.59 Стандарты | 41.88±8.03 | ||||
| Групповой фактор | 1.12 | 0.348 | |||||
| Фактор времени | 371.208 | <0,001 | |||||
| Групповой фактор * Временной фактор | 27.954 | <0,001 | |||||
Таблица 3: Сравнение баллов PBS в четырех группах детей (n = 64, x ± с). После лечения результаты повторного измерения ANOVA показали, что эффект времени и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами был незначимым (P > 0,05). Сокращения: PBS = педиатрическая шкала равновесия; rTMS = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием.
| Группа | Номер (n) | ПЕРЕД | ПОСЛЕ | F | P | ||
| Группа компаний «Конвенция» | 16 | 1,02±0,14 | 1,10±0,16 | ||||
| Группа rTMS | 16 | 0,98±0,18 | 1,15±0,16 | ||||
| Группа АОТ | 16 | 0,99±0,12 | 1,15±0,09 | ||||
| Группа комбинированного вмешательства | 16 | 1,02±0,15 | 1,24±0,11 | ||||
| Групповой фактор | 0.946 | 0.424 | |||||
| Фактор времени | 501.551 | <0,001 | |||||
| Групповой фактор * Временной фактор | 19.275 | <0,001 | |||||
Таблица 4: Сравнение баллов 10MWS в четырех группах детей (n = 64, x ± с). После лечения результаты повторного измерения ANOVA показали, что эффект времени и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами был незначимым (P > 0,05). Сокращения: 10MWS = скорость ходьбы 10 м; rTMS = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием.
| Группа | Номер (n) | ПЕРЕД | ПОСЛЕ | F | P | ||
| Группа компаний «Конвенция» | 16 | 46.63±20.05 | 54.00±22.19 | ||||
| Группа rTMS | 16 | 48.94±19.96 | 61.94±20.61 | ||||
| Группа АОТ | 16 | 50.25±15.25 | 63.63±16.40 | ||||
| Группа комбинированного вмешательства | 16 | 50.94±18.43 | 75.69±17.86 | ||||
| Групповой фактор | 1.300 | 0.283 | |||||
| Фактор времени | 502.502 | <0,001 | |||||
| Групповой фактор * Временной фактор | 31.184 | <0,001 | |||||
Таблица 5: Сравнение баллов GMFM в четырех группах детей (n = 64, x ± с). После лечения результаты повторных измерений ANOVA показали, что результаты повторных измерений ANOVA показали, что временной эффект и эффект взаимодействия между группами и временем были значимыми (P < 0,05), в то время как эффект между группами был незначимым (P > 0,05). Сокращения: GMFM = мера крупной моторной функции; rTMS = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием.
| Группа | Число | очевидная эффективность | Эффективный | Неэффективный | Эффективная ставка | ||
| Традиционная группа | 16 | 1 | 3 | 12 | 25.00% | ||
| Группа rTMS | 16 | 3 | 7 | 6 | 62.50% | ||
| Группа АОТ | 16 | 2 | 9 | 5 | 68.75% | ||
| Группа комбинированного вмешательства | 16 | 7 | 7 | 2 | 87.50% | ||
| χ2 | 13.850 | ||||||
| P | 0.003 | ||||||
| Сокращения: рТМС = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием. | |||||||
Таблица 6: Сравнение крупной моторной функции всех четырех групп детей (n [%]). Сокращения: рТМС = повторная транскраниальная магнитная стимуляция; AOT = тренировка по наблюдению за действием.
Дополнительный файл 1: Информация о пациенте. Пациенту проводилась терапия рТМС в сочетании с АОТ. Через 12 недель лечения сравнивали данные различных оценочных показателей до и после лечения с целью определения клинического влияния комбинированного вмешательства на крупную моторную функцию пациента. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Дополнительная таблица S1: Данные о пациенте. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Обсуждение
У детей с УПП повышенная активность γ и α нейронов приводит к ингибированию входа кортикоспинального тракта, что приводит к увеличению мышечного напряжения, известному как спазм. Поскольку спазмы конечностей существенно влияют на развитие моторной функции нижних конечностей у детей с УПП, одной из важнейших целей тренировки является снижение спастичности. В настоящее время для облегчения спастичности используются поэтапные стратегии лечения, включая реабилитационный уход, физиотерапию, применение ортопедических корсетов, инъекции ботулотоксина27, медикаментозное лечение и хирургические вмешательства28. В этом исследовании для снятия спазмов у детей с УПП использовались такие методы реабилитации, как лечебная физкультура, гидротерапия, массажная терапия и рТМС. Таблица 2 показывает, что показатели CSS в группе комбинированного вмешательства показали большее улучшение, чем в других трех группах, что позволяет предположить, что комбинированное вмешательство рТМС и АОТ более эффективно в облегчении спастичности у детей с УПП. Rajak et al.12 предположили, что увеличение частоты лечения рТМС может помочь уменьшить мышечные спазмы у детей с ДЦП и способствовать развитию двигательной функции. Gupta et al.29 лечили 20 пациентов с церебральным параличом с помощью рТМС с частотой 5 Гц и 10 Гц в течение 20 дней, стимулируя моторную кору головного мозга, и результаты показали, что мышечное напряжение при лечении рТМС было значительно ниже, чем в обычной группе. Этот вывод согласуется с результатами настоящего исследования, в котором показатели CSS экспериментальной группы были значительно выше, чем у других трех групп детей.
Перед началом лечения рТМС необходимо было сначала измерить двигательный порог детей, чтобы определить интенсивность лечения. У детей со спастической гемиплегией сначала оценивалась здоровая сторона, затем пораженная. Для определения интенсивности лечения использовали двигательный порог здоровой стороны. Во время лечения рТМС следует правильно носить позиционирующие колпачки, центр стимуляции катушки должен совпадать с фиксированной точкой, определенной катушкой, а катушка должна располагаться под углом 45° к коже головы. В этом исследовании область M1 была выбрана в качестве места стимуляции для улучшения двигательных нарушений нижних конечностей. Низкочастотная стимуляция с частотой 1 Гц позволяет снизить мозговой кровоток и возбудимость стимулируемой стороны и повысить возбудимость контралатеральной стороны. Высокочастотная стимуляция с частотой 5 Гц может напрямую улучшить корковую возбудимость стимулируемой стороны. Цель состоит в том, чтобы добиться лучшего межполушарного торможения, а чередование низко- и высокочастотной стимуляции способствует восстановлению двигательной функции.
АОТ представляет собой многообещающий подход к лечению церебрального паралича, восстанавливая поврежденные сети мозга для восстановления двигательной функции в качестве дополнения к физиотерапии15,30. В соответствии с этим механизмом ученые исследовали синергию АОТс терапией, вызванной ограничениями6, тренировкой вибрации всего тела31 и системами интерфейса мозг-компьютер32 в реабилитации церебрального паралича. АОТ должна представлять наблюдателям осмысленные действия и требует от детей определенных когнитивных способностей для имитации действий на видео. Ключевым моментом АОТ было наблюдение, а не выполнение действий. Поскольку нарушения равновесия могут влиять на самостоятельную ходьбу и повседневную деятельность детей с УПП, повышение их способности контролировать равновесие было особенно важным. Это исследование включало в себя программы АОТ, включающие функциональные движения для улучшения равновесия нижних конечностей и способности ходить. Дети внимательно смотрели видео, а физиотерапевты информировали их о более подробно о действиях, представленных в видео, и направляли и контролировали детей для правильного выполнения действий. Во время обучения физиотерапевты должны разъяснять детям детали движений и принимать стимулы для обеспечения спонтанного участия. АОТ обладает хорошими терапевтическими эффектами в условиях дистанционной реабилитации детей с ДЦП благодаря простоте эксплуатации33. Поэтому родителям рекомендуется проводить интенсивное обучение на дому для повышения эффективности обучения. Между тем, эффективность тренировки тесно связана с программой тренировок, которой придерживаются пациенты во время наблюдения и/или выполнения движений. Различные результаты обучения и результативности будут определяться на основе различий в уровнях внимания, уделяемого соблюдению учебных ресурсов34. Kim et al.35 не обнаружили существенных различий при сравнении результатов краткосрочных и долгосрочных вмешательств по лечению АОТ.
В этом исследовании, на основе традиционной реабилитации, были изучены эффекты четырех различных способов вмешательства, а именно только традиционных реабилитационных мероприятий, рТМС, АОТ и комбинированного вмешательства рТМС и АОТ, на крупную моторную функцию детей с УПП, соответственно, чтобы выяснить, имеет ли комбинированное вмешательство синергетический эффект. Таблицы 3, 4 и 5 показывают, что после 12 недель лечения показатели PBS, 10MWS и GMFM улучшились во всех группах. Тем не менее, комбинированная группа вмешательства продемонстрировала наиболее существенное улучшение показателей PBS, 10MWS и GMFM по сравнению с группами традиционной, рТМС и АОТ. Более того, его общая моторная функция также была значительно выше. Из таблицы 6 видно, что эффективный показатель валовой моторной функции в группе комбинированного вмешательства составил 87,50%, превысив показатели обычной группы (25,00%), группы рТМС (62,50%) и группы АОТ (68,75%) (χ2=13,850, P=0,003), что позволяет предположить, что комбинированное вмешательство рТМС и АОТ более эффективно в улучшении моторной функции детей с УПП. Механизмы регуляции могут быть следующими: во-первых, сайт рТМС — это М1-область моторной области нижних конечностей коры головного мозга, которая находится близко к области, где АОТ активирует МНС. Наблюдение за движением и его выполнение укрепляют связь между моторной корой и областью M1 через MNS36. Во-вторых, Sun et al.37подтвердили, что рТМС регулирует возбудимость целевой коры головного мозга, прикладывая магнитное поле к целевой мозговой области для генерации индуктивного тока, который может распространяться вдоль кортикоспинального тракта и периферических двигательных нервов, приводя к мышечным реакциям, способствующим восстановлению двигательной функции конечностей. АОТ может предоставить детям ожидаемый опыт и подготовку к действию путем предварительного просмотра видео, а также способствовать активности нейронной сети, зависящей от задачи, при выполнении одной и той же задачи38. В-третьих, стимуляция рТМС латеральных моторных областей коры головного мозга индуцирует транссинаптическую активацию подкорковых цепей с помощью индуцированных токов, вызывая снижение моторной и мышечной спастической активности для установления правильныхдвигательных паттернов. Видеоролики с действиями по программе АОТ можно наблюдать многократно и одновременно, улучшая моторную память и способствуя ремоделированию коры головного мозга за счет многократного выполнения программы40. Комбинированное вмешательство может синергетически регулировать активность коры головного мозга, повышать возбудимость моторной коры и рекрутирование двигательных единиц, уменьшать спастичность и мышечную гиперрефлексию, усиливать эффект взаимного взаимодействия. По этим причинам рТМС в сочетании с АОТ может иметь синергетический эффект для оптимизации нейропластических изменений и улучшения восстановления двигательных функций.
Комбинация рТМС и АОТ является эффективной стратегией индивидуализированной реабилитации при дисфункции нижних конечностей у детей с УПП, улучшая равновесие и двигательную функцию. В этом исследовании также есть недостатки: эффект плацебо может присутствовать при проведении рТМС, поскольку не использовалось фиктивное условие рТМС. Большинство методов оценки, использованных в исследовании, представляли собой шкалы оценки реабилитации, и объективная оценка с помощью визуализации, такая как нейрофизиология, электроэнцефалография или функциональная МРТ, не применялась. Кроме того, необходимы крупномасштабные долгосрочные клинические исследования и рандомизированные контролируемые исследования с объективной нейрофизиологической или визуализационной оценкой для получения стандартизированных параметров лечения рТМС-терапией и АОТ или для определения терапевтического эффекта.
Раскрытие информации
У авторов нет конфликта интересов, о котором можно было бы заявить.
Благодарности
Это исследование было поддержано при финансовой поддержке реабилитационной больницы Сянъя Боай.
Материалы
| Name | Company | Catalog Number | Comments |
| K6 multimedia scene interactive training system | Hunan Le Jiekang technology Co., LTD | Program implementation | |
| KLW-SLL type spa machine for children | Nanjing Kanglongwei Technology Industrial Co., LTD | Conventional therapy | |
| Pulse magnetic field stimulator model YRD CCY-II | Shenzhen Yingzhi technology Co., LTD | Program implementation | |
| SPSS26 software | IBM | Statistic analysis |
Ссылки
- Sadowska, M., Sarecka-Hujar, B., Kopyta, I. Cerebral palsy: current opinions on definition, epidemiology, risk factors, classification and treatment options. Neuropsychiatric Dis Treat. 16, 1505-1518 (2020).
- Alpay, S. Z., Kim, S. K., Oh, K. J., Graham, S. F. Advances in cerebral palsy biomarkers. Adv Clin Chem. 100, 139-169 (2016).
- Paul, S., Nahar, A., Bhagawati, M., Kunwar, A. J. A review on recent advances of cerebral palsy. Oxid Med Cell Longev. 2022, 2622310 (2022).
- Huang, C., et al. Efficacy and safety of core stability training on gait of children with cerebral palsy: A protocol for a systematic review and meta-analysis. Medicine. 99 (2), e18609 (2020).
- Kwon, H. Y., Ahn, S. Y. Effect of task-oriented training and high-variability practice on gross motor performance and activities of daily living in children with spastic diplegia. J Phys Ther Sci. 28 (10), 2843-2848 (2016).
- Jamali, A. R., Amini, M. The effects of constraint-induced movement therapy on functions of cerebral palsy children. Iran J Child Neurol. 12 (4), 16-27 (2018).
- Park, E. J., Baek, S. H., Park, S. Systematic review of the effects of mirror therapy in children with cerebral palsy. J Phys Ther Sci. 28 (11), 3227-3231 (2016).
- Fan, J., et al. The effectiveness and safety of repetitive transcranial magnetic stimulation on spasticity after upper motor neuron injury: A systematic review and meta-analysis. Front Neural Circuits. 16, 973561 (2022).
- Zewdie, E., et al. Safety and tolerability of transcranial magnetic and direct current stimulation in children: Prospective single center evidence from 3.5 million stimulations. Brain Stimul. 13 (3), 565-575 (2020).
- Dadashi, F., et al. The effects of repetitive transcranial magnetic stimulation (rTMS) on balance control in children with cerebral palsy. Annu Int Conf IEEE Eng Med Biol Soc. 2019, 5241-5244 (2019).
- Feng, J. Y., et al. Effect of infra-low-frequency transcranial magnetic stimulation on motor function in children with spastic cerebral palsy. Chinese Journal of Contemporary Pediatrics. 15 (3), 187-191 (2013).
- Rajak, B. L., Gupta, M., Bhatia, D., Mukherjee, A. Increasing number of therapy sessions of repetitive transcranial magnetic stimulation improves motor development by reducing muscle spasticity in cerebral palsy children. Ann Indian Acad Neurol. 22 (3), 302-307 (2019).
- Novak, I., et al. State of the evidence traffic lights 2019: systematic review of interventions for preventing and treating children with cerebral palsy. Curr Neurol Neurosci Rep. 20 (2), 3 (2020).
- Buchignani, B., et al. Action observation training for rehabilitation in brain injuries: a systematic review and meta-analysis. BMC Neurol. 19 (1), 344 (2019).
- Buccino, G. Action observation treatment: a novel tool in neurorehabilitation. Philos Trans R Soc Lond B Biol Sci. 369 (1644), 20130185 (2014).
- Lee, H. J., Kim, Y. M., Lee, D. K. The effects of action observation training and mirror therapy on gait and balance in stroke patients. J Phys Ther Sci. 29 (3), 523-526 (2017).
- Peng, T. H., et al. Action observation therapy for improving arm function, walking ability, and daily activity performance after stroke: a systematic review and meta-analysis. Clin Rehabil. 33 (8), 1277-1285 (2019).
- Fan, T. L., et al. Effects of action observation therapy based on mirror neuron theoryon the balance and walking ability of children with cerebral palsy. Chin J Child Health Care. 31 (2), 220-224 (2023).
- Noh, J. S., Lim, J. H., Choi, T. W., Jang, S. G., Pyun, S. B. Effects and safety of combined rTMS and action observation for recovery of function in the upper extremities in stroke patients: A randomized controlled trial. Restor Neurol Neurosci. 37 (3), 219-230 (2019).
- Parvin, S., et al. Therapeutic effects of repetitive transcranial magnetic stimulation on corticospinal tract activities and neuromuscular properties in children with cerebral palsy. Annu Int Conf IEEE Eng Med Biol Soc. 2018, 2218-2221 (2018).
- Children Rehabilitation Committee of China Rehabilitation Medical Association, China Rehabilitation Association for Disabled Children Cerebral Palsy Rehabilitation Committee, Chinese medical doctor association pediatric rehabilitation committee. & Chinese rehabilitation Guidelines for Cerebral Palsy (2022) Editorial board. Chinese Rehabilitation Guidelines for Cerebral Palsy (2022) Chapter 1: Generality. Chin J Appl Clin Pediatr. 37 (12), 887-892 (2022).
- Subspecialty Group of Rehabilitation, t. S. o. P.C. M. A. Rehabilitation strategy and recommendation for motor dysfunction in children with cerebral palsy. Zhonghua Er Ke Za Zhi. 58 (2), 91-95 (2020).
- Alimi, L., Kalantari, M., Nazeri, A. R., Akbarzade, B. A. Test-retest & inter-rater reliability of Persian version of Pediatric Balance Scale in children with spastic cerebral palsy. Iran J Child Neurol. 13 (4), 163-171 (2019).
- Thompson, P., et al. Test-retest reliability of the 10-metre fast walk test and 6-minute walk test in ambulatory school-aged children with cerebral palsy. Dev Med Child Neurol. 50 (5), 370-376 (2008).
- Yang, Z., Qiao, L., He, J., Zhao, X., Zhang, M. Effects of repetitive transcranial magnetic stimulation combined with functional electrical stimulation on hand function of stroke: A randomized controlled trial. NeuroRehabilitation. 51 (2), 283-289 (2022).
- Li, X., et al. Effect of virtual reality combined with repetitive transcranial magnetic stimulation on musculoskeletal pain and motor development in children with spastic cerebral palsy: a protocol for a randomized controlled clinical trial. BMC Neurology. 23 (1), 339 (2023).
- Multani, I., Manji, J., Hastings-Ison, T., Khot, A., Graham, K. Botulinum toxin in the management of children with cerebral palsy. Paediatr Drugs. 21 (4), 261-281 (2019).
- Volpon Santos, M., Carneiro, V. M., Oliveira, P., Caldas, C. A. T., Machado, H. R. Surgical results of selective dorsal rhizotomy for the treatment of spastic cerebral palsy. J Pediatr Neurosci. 16 (1), 24-29 (2021).
- Gupta, M., Rajak, B. L., Bhatia, D., Mukherjee, A. Neuromodulatory effect of repetitive transcranial magnetic stimulation pulses on functional motor performances of spastic cerebral palsy children. J Med Eng Technol. 42 (5), 352-358 (2018).
- Abdelhaleem, N., et al. Effect of action observation therapy on motor function in children with cerebral palsy: a systematic review of randomized controlled trials with meta-analysis. Clin Rehabil. 35 (1), 51-63 (2021).
- Jung, Y., Chung, E. J., Chun, H. L., Lee, B. H. Effects of whole-body vibration combined with action observation on gross motor function, balance, and gait in children with spastic cerebral palsy: a preliminary study. J Exerc Rehabil. 16 (3), 249-257 (2020).
- Rossi, F., et al. Combining action observation treatment with a brain-computer interface system: perspectives on neurorehabilitation. Sensors (Basel). 21 (24), 8504 (2021).
- Beani, E., Menici, V., Ferrari, A., Cioni, G., Sgandurra, G. Feasibility of a home-based action observation training for children with unilateral cerebral palsy: an explorative atudy. Front Neurol. 11, 16 (2020).
- Carson, H. J., Collins, D. J. Commentary: Motor imagery during action observation: a brief review of evidence, theory and future research opportunities. Front Hum Neurosci. 11, 25 (2017).
- Kim, D. H., An, D. H., Yoo, W. G. Effects of live and video form action observation training on upper limb function in children with hemiparetic cerebral palsy. Technol Health Care. 26 (3), 437-443 (2018).
- Qi, F., Nitsche, M. A., Ren, X., Wang, D., Wang, L. Top-down and bottom-up stimulation techniques combined with action observation treatment in stroke rehabilitation: a perspective. Front Neurol. 14, 1156987 (2023).
- Sun, Y. Y., et al. Effects of repetitive transcranial magnetic stimulation on motor function and language ability in cerebral palsy: A systematic review and meta-analysis. Front Pediatr. 11, 835472 (2023).
- Jeong, Y. A., Lee, B. H. Effect of action observation training on spasticity, gross motor function, and balance in children with diplegia cerebral palsy. Children (Basel). 7 (6), 64 (2020).
- Gupta, M., Lal Rajak, B., Bhatia, D., Mukherjee, A. Effect of r-TMS over standard therapy in decreasing muscle tone of spastic cerebral palsy patients. J Med Eng Technol. 40 (4), 210-216 (2016).
- Ryan, D., et al. Effect of action observation therapy in the rehabilitation of neurologic and musculoskeletal conditions: a systematic review. Arch Rehabil Res Clin Transl. 3 (1), 100106 (2021).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеThis article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены