Mapeamento Quantitativo de Tensão de um Aneurisma da Aorta Abdominal
Visão Geral
Fonte: Hannah L. Cebull1, Arvin H. Soepriatna1, John J. Boyle2 e Craig J. Goergen1
1 Weldon School of Biomedical Engineering, Purdue University, West Lafayette, Indiana
2 Engenharia Mecânica & Ciência dos Materiais, Universidade de Washington em St. Louis, St Louis, Missouri
O comportamento mecânico dos tecidos moles, como vasos sanguíneos, pele, tendões e outros órgãos, são fortemente influenciados por sua composição de elastina e colágeno, que proporcionam elasticidade e força. A orientação de fibras dessas proteínas depende do tipo de tecido mole e pode variar de uma única direção preferencial a redes intrincadas de malha, que podem se tornar alteradas em tecido doente. Portanto, os tecidos moles muitas vezes se comportam anisotropicamente no nível celular e órgão, criando uma necessidade de caracterização tridimensional. Desenvolver um método para estimar de forma confiável os campos de cepas dentro de tecidos ou estruturas biológicas complexas é importante para caracterizar e entender a doença mecanicamente. A cepa representa como o tecido mole se deforma relativamente ao longo do tempo, e pode ser descrito matematicamente através de várias estimativas.
A aquisição de dados de imagem ao longo do tempo permite que a deformação e a tensão sejam estimadas. No entanto, todas as modalidades de imagem médica contêm alguma quantidade de ruído, o que aumenta a dificuldade de estimar com precisão a tensão in vivo. A técnica aqui descrita supera esses problemas com sucesso usando um método de estimativa de deformação direta (DDE) para calcular campos de cepa 3D espacialmente variados a partir de dados de imagem volumosas.
Os métodos atuais de estimativa de tensão incluem correlação de imagem digital (DIC) e correlação de volume digital. Infelizmente, o DIC só pode estimar com precisão a tensão de um plano 2D, limitando severamente a aplicação deste método. Embora úteis, métodos 2D como DIC têm dificuldade em quantificar a cepa em regiões que sofrem deformação 3D. Isso ocorre porque o movimento fora do avião cria erros de deformação. A correlação de volume digital é um método mais aplicável que divide os dados de volume inicial em regiões e encontra a região mais semelhante do volume deformado, reduzindo assim o erro fora do plano. No entanto, este método se mostra sensível ao ruído e requer suposições sobre as propriedades mecânicas do material.
A técnica aqui demonstrada elimina essas questões utilizando um método DDE, tornando-o muito útil na análise de dados de imagem médica. Além disso, é robusto para tensão alta ou localizada. Aqui descrevemos a aquisição de dados de ultrassom 4D fechados, volumétricos, sua conversão em um formato analisável e o uso de um código Matlab personalizado para estimar a deformação 3D e as cepas verdes-lagrange correspondentes, um parâmetro que melhor descreve grandes deformações. O tensor de cepa Green-Lagrange é implementado em muitos métodos de estimativa de cepas 3D porque permite que f seja calculado a partir de um Ajuste De Menor Quadrado (LSF) dos deslocamentos. A equação abaixo representa o tensor de cepa Green-Lagrange, E, onde F e I representam o gradiente de deformação e tensor de identidade de segunda ordem, respectivamente.
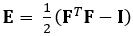 (1)
(1)
Princípios
O ultrassom 4D é um volume dinâmico que é adquirido utilizando um motor de tradução linear ligado a um transdutor de ultrassom, permitindo a aquisição de loops de vídeo cardíacos e respiratórios sequenciais em uma região de interesse. Este método é útil para visualizar estruturas complexas como o coração, onde a hipertrofia ou infarto causa geometrias únicas, ou aneurismas de aorta, onde a expansão e dissecção de vasos assimétricos ocorrem frequentemente em vasos tortuosos. Além disso, os dados 4D podem fornecer informações espaciais e temporais de alta resolução, o que também é importante para imagens cardiovasculares.
O método DDE aplicado aos dados de ultrassom 4D é superior a outros métodos porque usa registro de imagem não rígido. Os tensores de gradiente de deformação são tradicionalmente estimados a partir de campos de deslocamento após a correlação de volume digital. Em contraste, o método DDE estima intrinsecamente tensores gradientes de deformação durante o registro de volume, otimizando uma função de deformagem que é cuidadosamente escolhida para ser diretamente análoga ao tensor de deformação. A função de deformagem depende tanto da posição espacial quanto do parâmetro de deformagem(p):
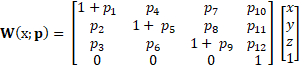 (2)
(2)
Os três primeiros elementos desta função representam o tensor de gradiente de deformação, F,permitindo que o cálculo da deformação seja diretamente incorporado na função de deformação. Este método de deformação tem sido comprovado para aumentar a precisão e precisão da estimativa de tensão quando comparado com técnicas anteriores semelhantes, pois permite deformações grandes ou localizadas comumente encontradas em tecidos moles.
Procedimento
1. Configuração de ultrassom 4D
- Ao usar o software de imagem, use um laptop capaz de executar software matemático de computação para automatizar o processo de aquisição 4D. Conecte o laptop com este código personalizado ao sistema de ultrassom através da porta USB. Observe que o software de imagem tem um recurso de ultrassom 4D integrado ao software.
- Depois de ligar o sistema de ultrassom, configure a unidade de monitoramento fisiológico e, ao mesmo tempo, garanta que os botões de frequência cardíaca e temperatura estejam ligados. Inicialize o estágio do motor 3D ligado ao suporte do transdutor.
- Use o estágio apropriado e o transdutor de ultrassom para aquisição de imagens. Certifique-se de que todas as conexões adequadas sejam feitas.
- Continue anestesiando e preparando o animal para a imagem. Adicione a pomada oftalmológica aos olhos para evitar a dessecação da córnea, fixar as patas nos eletrodos do estágio e inserir uma sonda de temperatura retal lubrificada. Remova a pele na área de interesse usando um creme depilatório.
- Certifique-se de que o creme depilatório esteja concluído. Em seguida, aplique uma quantidade generosa do gel de transdução ultrassônico aquecido ao animal. Isso é especialmente importante para criar uma boa conexão sobre toda a região de interesse para imagens 4D.
2. Aquisição de Ultrassom 4D
- Inicie um novo estudo sobre o sistema de ultrassom e abra a janela de imagem no Modo B (modo de brilho). Abaixe o transdutor sobre o animal e localize a região de interesse usando os botões x e y-axis no palco, certificando-se de que a taxa respiratória não diminua substancialmente. Monitore isso na parte inferior da tela.
- Posicione o transdutor no meio da região de interesse. A partir daí, aproxime-se da distância necessária para que o transdutor se mova para cima e para baixo de tal forma que toda a região de interesse seja incluída.
- Digite as dimensões aproximadas no código do software de computação, incluindo um tamanho de passo que normalmente é ~0,08 mm para imagens de aneurisma de aoórtica abdominal. Comece a executar o código depois de garantir que as taxas cardíacas e respiratórias do animal estejam estáveis. Isso é importante para reduzir erros ao reconstruir imagens.
- Após concluir a aquisição de imagem, exporte os dados como arquivos XML brutos.
3. Conversão de Dados de Ultrassom 4D
- Insira os arquivos XML brutos em software que pode converter os dados no formato adequado para a análise de manchas 3D. Aqui usamos matlab para converter arquivos XML em arquivos MAT. O roteiro completo do Matlab está disponível aqui.
- Para a conversão adequada, o número de quadros, o tamanho da etapa e a resolução de saída desejada também precisarão ser inseridos.
- Depois de resampling a matriz através do avião, importe o novo arquivo MAT para o código de análise de cepas 3D.
Análise de código de tensão .3D 4
- Comece a analisar ajustando corretamente o arquivo MAT importado. Por exemplo, o volume de imagem pode precisar ser redimensionado para reduzir o tempo de computação.
- Insira a região a ser analisada e determine o modelo de malha apropriado para segmentar os dados da imagem como caixas simples ou polígonos escolhidos manualmente. O tamanho da caixa das regiões e o espaçamento entre os pontos centrais podem precisar ser alterados para cada conjunto de dados. Os números ideais escolhidos para o tamanho da caixa estarão em torno da ordem dos pixels do recurso que está sendo rastreado, que podem ser aproximados olhando para o número de pixels em duas dimensões em uma fatia. O espaçamento das caixas determinará a resolução dos campos de tensão. Mais caixas aumentarão a resolução, mas também podem aumentar substancialmente o tempo de computação.
- Comece a computar os jacobianos e gradientes iterativamente dentro de cada uma dessas regiões. Após a pré-comparação ser concluída, aplique a função de deformação.
- Calcule o tensor de gradiente de deformação. Primeiro calcule a tensão e, em seguida, calcule os valores de eigen e eigenvectors usando o método de estimativa de deformação direta.
- Plotar esses resultados nos planos desejados usando uma técnica como mapeamento de cores de um plano de corte para representar o campo de tensão sobre sua região de interesse.
Resultados
Utilizando o procedimento descrito acima, foi adquirido ultrassom 4D de um angiotensin i-induzido por dissecação abdominal aorísmo abdominal (AAA) de um rato. Vários loops de vídeo EKV de curto eixo foram adquiridos ao longo da aorta e combinados para criar dados 4D, como mostrado na Figura 1. Esses dados foram então convertidos em um arquivo MAT usando um código personalizado, que foi então analisado em um código de cálculo de tensão 3D usando uma função de warping. Após a otimização dos parâmetros do código para um conjunto de dados específico, foi produzida uma visão representativa de eixo longo com valores correspondentes de tensão, bem como um gráfico de visualização de fatias 3D com um mapa de cor de tensão sobreposta(Figura 2). Esta técnica de DDE e os dados de tensão destacam as variações espaciais heterogêneas na tensão, particularmente quando um trombo está presente. Esses resultados podem então ser correlacionados com a estrutura do vaso para determinar a relação entre deformação in vivo e composição de aneurisma.

Figura 1: As alças de visualização kilohertz (EKV) com porta-ECG (EKV) da aorta são adquiridas a partir de locais de partida e término inseridos manualmente, seguindo um tamanho de passo de 0,2 mm.
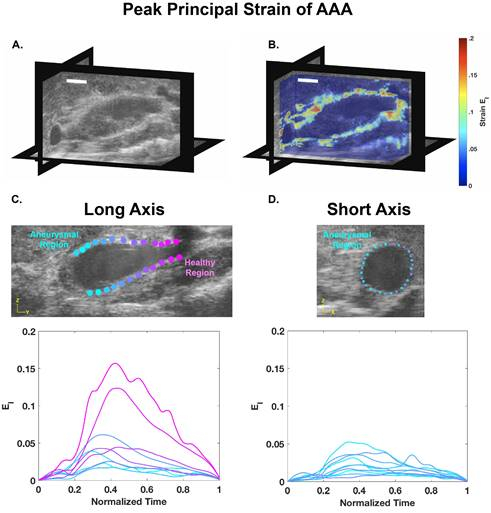
Figura 2: Dados de ultrassom de alta frequência 4D de um aneurisma de aorta abdominal dissecando murina representado em systole (A) com os principais campos de tensão estimados e sobrepostos (B) (Scalebar = 5 mm). Vistas de eixo longo e curto representando regiões aneurismals e saudáveis correspondentes a tensão principal ao longo de um ciclo cardíaco (systole: t= 0,4) (C, D). Esses dados mostram níveis de tensão relativamente altos em regiões saudáveis e valores reduzidos de tensão dentro do aneurisma dissetante.
Aplicação e Resumo
A caracterização mecânica in vivo localizada é uma parte importante na compreensão do crescimento e remodelação dos tecidos biológicos. Em comparação com as abordagens existentes, o procedimento de quantificação da cepa descrito aqui utiliza um método aprimorado de calcular com precisão a cepa 3D através de distorcer a imagem não deformada antes da correlação cruzada. Este método não utiliza quaisquer suposições materiais na determinação de cepas dentro dos volumes teciduais. Infelizmente, a estimativa de tensão é confiável apenas até um tamanho de kernel de voxels 15x15x15 ao usar dados de ultrassom, sugerindo que esta abordagem DDE pode não detectar características sutis dentro de um campo de tensão. Apesar dessa limitação, continua sendo uma ferramenta importante para investigar respostas mecânicas, diagnosticar patologia e melhorar modelos de doenças.
Muitas áreas de pesquisa além de aneurismas de aoórtico podem se beneficiar desta ferramenta de medição de cepas. A cepa cardíaca também pode ser facilmente quantificada usando este método. Como o miocárdio sofre deformação 3D durante o ciclo cardíaco, quantificar a tensão em três dimensões é essencial para caracterizar de forma confiável a dinâmica desse tecido. Dados de tensão confiáveis são especialmente importantes ao rastrear a progressão da doença em modelos animais.
A análise da cepa 3D também pode ser aplicada à imagem de ultrassom intestinal. A caracterização mecânica do tecido intestinal é mais comumente conduzida in vitro. No entanto, nem sempre se trata de uma verdadeira representação do comportamento real dos intestinos in vivo por causa dos efeitos das estruturas circundantes. Como exemplo de tradução clínica dessa abordagem, calcular a cepa a partir de imagens de fibrose intestinal devido à pressão luminal anormal poderia fornecer detecção precoce de áreas problemáticas que requerem intervenção cirúrgica.
Além das aplicações em maior escala, esse método também pode ser aplicado ao nível celular usando técnicas de imagem de resolução mais alta, como a microscopia confocal. Caracterizar a matriz extracelular é importante para entender como as células se comunicam. Muita pesquisa tem sido realizada sobre a caracterização bioquímica, mas entender como a comunicação pode ser conduzida através de respostas mecânicas requer uma compreensão da deformação e da tensão. A cepa em massa não é benéfica porque não há como determinar a origem da mudança de deformação. A aplicação de uma abordagem DDE de alta resolução pode revelar diretamente como a matriz extracelular responde a alterações mecânicas.
AGRADECIMENTOS
Gostaríamos de reconhecer John Boyle, Guy Genin e Stavros Thomopoulos pela contribuição do código Matlab personalizado do DDE capaz de estimar diretamente a tensão Lagrange-Green.
Pular para...
Vídeos desta coleção:

Now Playing
Mapeamento Quantitativo de Tensão de um Aneurisma da Aorta Abdominal
Biomedical Engineering
4.6K Visualizações

Imageamento de amostras biológicas com microscopia ótica e confocal
Biomedical Engineering
35.7K Visualizações

Imageamento por MEV de Amostras Biológicas
Biomedical Engineering
23.5K Visualizações

Biodistribuição de Nano-fármacos Transportadores: Aplicações de MEV
Biomedical Engineering
9.3K Visualizações

Ultrassonografia de alta frequência da aorta abdominal
Biomedical Engineering
14.4K Visualizações

Tomografia fotoacústica para imageamento de sangue e lipídios na aorta infrarrenal
Biomedical Engineering
5.7K Visualizações

Ressonância Magnética Cardíaca
Biomedical Engineering
14.7K Visualizações

Simulações computacionais de fluidodinâmica do fluxo sanguíneo em um aneurisma cerebral
Biomedical Engineering
11.7K Visualizações

Imageamento de fluorescência de infravermelho próximo de aneurismas da aorta abdominal
Biomedical Engineering
8.2K Visualizações

Técnicas não invasivas de medição da pressão arterial
Biomedical Engineering
11.9K Visualizações

Aquisição e análise de um sinal de ECG (eletrocardiografia)
Biomedical Engineering
104.8K Visualizações

Resistência à Tração de Biomateriais Reabsorvíveis
Biomedical Engineering
7.5K Visualizações

Imagem de micro-TC de uma medula espinal de camundongo
Biomedical Engineering
8.0K Visualizações

Visualização da degeneração da articulação do joelho após lesão não invasiva do LCA em ratos
Biomedical Engineering
8.2K Visualizações

Combinação de imagens de SPECT e TC para visualizar a funcionalidade cardíaca
Biomedical Engineering
11.0K Visualizações
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados