Method Article
Estudos Termoquímicos de Ni(II) e Zn(II) Complexos Ternários utilizando Espectrometria de Ion Mobility-Mass
Neste Artigo
Resumo
Este artigo descreve um protocolo experimental usando espectrometria eletrospray-ion mobilidade-massa, cálculos quânticos semi-empíricos e dissociação induzida por colisão limiar resolvida pela energia para medir a termoquímica relativa da dissociação de complexos metálicos ternários relacionados.
Resumo
Este artigo descreve um protocolo experimental usando espectrometria eletrospray-ion mobilidade-massa (ES-IM-MS) e dissociação induzida por colisão limiar (TCID) para medir a termoquímica de a dissociação de complexos ternários carregados negativamente [amb+M(II)+NTA]- complexos ternários em dois canais de produto: [amb+M(II)] + NTA ou [NTA+M(II)]- + amb, onde M = Zn ou Ni e NTA é ácido nitrilotriactico. Os complexos contêm um dos heptapeptides de ligação metálica alternativa (amb) com as estruturas primárias acetil-His 1-Cys2-Gly 3-Pro 4-Tyr5-His 6-Cys 7 ou acetil-Asp1-Cys 2-Gly 3-Pro 4-Tyr 5-His 6-Cys 7, onde os aminoácidos Aa1,2,6,7 posições são os potenciais locais de ligação metálica. Estados estacionários otimizados pela geometria dos complexos ternários e seus produtos foram selecionados a partir de cálculos de química quântica (atualmente o PM6 semi-empírico Hamiltoniano) comparando suas energias eletrônicas e suas seções transversais de colisão (CCS) às medidas pelo ES-IM-MS. A partir dos cálculos de frequência PM6, os parâmetros moleculares do complexo ternário e seus produtos modelam as intensidades dependentes de energia dos dois canais de produto utilizando um método TCID competitivo para determinar as energias limiares das reações que se relacionam com os 0 Kenthalpies de dissociação (ΔH0). Correções térmicas e entropias estatísticas utilizando as frequências rotacionais e vibracionais PM6 fornecem os 298 K de dissociação (ΔH298). Esses métodos descrevem uma rotina de EI-IM-MS que pode determinar as constantes termoquímicas e de equilíbrio para uma gama de complexos de íons metálicos ternários.
Introdução
Este estudo descreve uma nova técnica utilizando um espectrômetro de mobilidade de mobilidade de íons comercialmente disponível que permite a determinação da termoquímica relativa para a dissociação de um complexo metálico ternário de ligação metálica alternativa (amb) (amb+M(II)+NTA], onde M = Zn ou Ni e NTA = ácido nitrilotriactico (Figura 1). Essas reações modelam a dissociação da proteína recombinante amb marcada ligada ao metal imobilizado NTA durante a cromatografia de afinidade metálica imobilizada (IMAC)1,2. Como exemplo, este método é descrito utilizando as etiquetas amb heptapeptide de amb A e H (Figura 2) (escolhidas nos estudos anteriores 3,4,5,6,7,8,9,10,11,12 ), que exibem propriedades de ligação Zn(II) e Ni(II) e, portanto, têm aplicações potenciais como etiquetas de purificação. No entanto, o processo descrito pode ser usado para avaliar energias termoquímicas em qualquer sistema organometólico. Estes peptídeos amb têm locais de ligação metálica nas posições Aa1-Aa 2 e Aa6-Aa 7 que competem com os locais de carboxilato e amina da NTA. Os três aminoácidos amb centrais fornecem um espaçador (Gly3), a dobradiça para os dois braços (Pro4) e uma interação de cation de π metais de longa distância (Tyr5).
O estado de carga geral 1− dos complexos [amb+M(II)+NTA]- é determinado pelo estado de protonação de seus potenciais locais de vinculação. Uma vez que existe Ni(II) ou Zn(II) com o estado de oxidação 2+, deve haver uma rede de três locais desprotosados negativamente carregados. A modelagem molecular dos complexos [amb+M(II)+NTA]- prevê que estes são dois prótons da NTA e um próton da amb (i.e., [amb-H+M(II)+NTA-2H]-). Os canais do produto contêm uma espécie iônica e uma espécie neutra (ou seja, [NTA-3H+M(II)]- + amb ou [amb-3H+M(II)]- + NTA). No manuscrito, "-3H" é excluído nos nomes dos complexos, mas o leitor deve saber que o -3H está implícito. O instrumento mede as intensidades relativas das duas espécies iônicas de massa a carga (m/z). Um dos principais atributos das análises do ES-IM-MS é que permite o exame da reatividade de uma espécie específica de m/z, conforme utilizado aqui e em estudos anteriores de AMB 3,4,5,6,7,8,9,10,11,12.
A aquisição de dados termoquímicos para grandes complexos por meio da dissociação induzida por colisão é um assunto de interesse significativo13,14. Metodologias, incluindo o método cinético, não são propícias à montagem de dados sobre uma série de energias, nem são responsáveis por ambientes multi-colisão 15,16,17,18. Aqui, o método CID (TCID) limiar, desenvolvido usando espectrometria de massa de feixe de íons guiados por Armentrout, Ervin e Rodgers é aplicado19 a uma nova plataforma de instrumentos ES-IM-MS utilizando guias de íons de ondas de viagem. O método TCID permite a análise termoquímica relativa da dissociação dos complexos ternários em seus dois canais de produtos e inclui uma lei limiar descrevendo a transferência de energia de colisão entre a energia translacional do reagente (complexo ternário nesta pesquisa) e um gás alvo inerte (argônio neste caso). O método inclui a integração sobre a distribuição interna de energia20 do reagente, as distribuições de energia translacional entre o reagente e o gás alvo21, e as distribuições totais de momento angular22,23. Uma probabilidade de dissociação e correção estatística de Rice-Ramsperger-Kassel-Marcus (RRKM) dos turnos cinéticos resultantes da janela de tempo limitada para observação dos produtos estão incluídos24. Para dois canais independentes de produtos, o método TCID competitivo permite o encaixe simultâneo dos dois canais de produtos concorrentes. A dissociação do complexo é através de um estado de transição em órbita, que tem as propriedades dos produtos, mas é mantido em conjunto por um dipolobloqueado 25. O método TCID é incorporado ao programa CRUNCH26, e o funcionamento da interface do usuário é descrito aqui para avaliar a termoquímica dos dois canais de dissociação dos complexos ternários [amb+M(II)+NTA]. O programa CRUNCH está disponível mediante solicitação dos desenvolvedores26.
Protocolo
NOTA: A Figura 1 mostra uma visão geral do protocolo.
1. Preparação de reagentes
- Compre peptídeos amb congelados (>98% de pureza) e armazene-os em um congelador de −80 °C.
- Compre >99% de pureza de zinco (II) hexahidrato de nitrato e níquel (II) hexahidrato de nitrato.
ATENÇÃO: O hexahidrato de nitrato de níquel (II) apresenta um risco ambiental e à saúde. - Compre o ácido nitrilotriactico, polímeros poli-DL-alanina, acetato de amônio de grau metálico ultrapure/trace, hidróxido de amônio, ácido acético glacial e acetonitrilo de grau HPLC.
2. Elaboração de soluções de estoque
- Solução de estoque peptídeo amb
- Prepare uma solução aquosa de concentração de 12,5 mM amb pesando 10-20 mg do peptídeo congelado usando nada menos que três dígitos significativos e colocando-o em um tubo de microcentrífugo de polipropileno de 1,7 mL.
- Adicione o volume apropriado de água deionizada (>17,8 MΩ cm) ao tubo de microcentrifusagem. Feche a tampa e misture bem com pelo menos 20 inversões.
- Crie alíquotas de 50 μL a partir da solução de 12,5 mM amb e coloque-as em tubos de microcentrifuuge marcados de 1,7 mL. Armazene as soluções de estoque de alíquota a −80 °C.
- Soluções de ações de íons metálicos
- Prepare as soluções aquosas Zn(II) e Ni(II) de concentração de 12,5 mM pesando 10-30 mg do hexahidrato de nitrato metálico usando nada menos que três dígitos significativos e colocando-o em um tubo de microcentrífugo de polipropileno de 1,7 mL.
- Adicione a quantidade apropriada de água DI ao tubo de microcentrifuuagem. Feche a tampa e misture bem com pelo menos 20 inversões. Armazene 50 soluções de estoque de alíquota de μL a −80 °C.
- Soluções de ações ion nta
- Prepare uma solução nta aquosa pesando 10-30 mgs da NTA usando nada menos que três dígitos significativos e colocando-a em um tubo de microcentrifuge de 1,7 mL.
- Adicione a quantidade apropriada de água DI à NTA no tubo de microcentrífuga para alcançar uma concentração final de 12,5 mM. Feche a tampa e misture bem com pelo menos 20 inversões. Armazene 50 soluções de estoque de alíquota de μL a −80 °C.
- Soluções de estoque de acetato de amônio: Pese 30,8 mg de acetato de amônio e adicione a 40 mL de água DI para produzir uma solução de 10 mM. Ajuste o pH da solução de acetato de amônio para pH 7.7 com hidróxido de amônio de 1 mM.
- Solução de estoque poli-DL-alanina: Faça uma solução de estoque de 1 mL, 1.000 ppm de poli-DL-alanina (PA) dissolvendo 1,0 mg de PA em água DI. Misture de forma abrangente. Crie alíquotas de 50 μL e coloque-as em tubos de microcentrifuuge rotulados individualmente. Armazene a solução de 1.000 ppm a −80 °C.
3. Análise de dissociação de massa de mobilidade eletrospray-íon (ES-IM-MS)
- Prepare o instrumento limpando o tubo de entrada ES e capilar de metal injetando 500 μL de ácido acético glacial de 0,1 M, seguido por 500 μL de hidróxido de amônio de 0,1 M e, finalmente, 500 μL de solução de acetato de amônio pH 7,7.
- Liquete a solução de estoque de 12,5 mM amb, trazendo-a à temperatura ambiente. Crie uma concentração final de 0,125 mM amb fazendo duas diluições sucessivas com água DI. Misture-se de forma abrangente após cada diluição.
- Liquefate a solução de 12,5 mM de ion de íons metálicos, trazendo-a à temperatura ambiente. Crie uma concentração final de íon metálico de 0,125 mM, fazendo duas diluições sucessivas com água DI. Misture-se de forma abrangente após cada diluição.
- Liquefate a solução de ações NTA de 12,5 mM. Crie uma concentração final de 0,125 mM NTA fazendo duas diluições sucessivas com água DI. Misture-se de forma abrangente após cada diluição.
- Para fazer uma amostra de 2 mL do complexo ternário, adicione 800 μL de solução 0,125 mM NTA e 400 μL de solução de íons metálicos de 0,125 a um tubo de microcentrifuuge de 2 mL e misture bem com pelo menos 20 inversões. Adicione 400 μL de solução de acetato de amônio (pH 7.7) e 400 μL de solução de 0,125 mM amb, misture bem com pelo menos 20 inversões e permita que a amostra se equilibre por 10 minutos à temperatura ambiente.
- Carregue a amostra de 2 mL em uma seringa de nariz sem corte de 2,5 mL e injete a amostra no ES do instrumento usando a bomba de seringa do instrumento a um fluxo de 10 μL/min.
- Coloque o instrumento no modo IM-MS negativo. Use as condições de funcionamento típicas do instrumento27 para esses experimentos da seguinte forma.
- Injete a amostra a uma taxa de fluxo de 10 μL/min no capilar ES mantido a −2 kV com uma taxa de fluxo de dessolvação de 500 L/h de nitrogênio. Defina as temperaturas de fonte e desolação do ES para 130 °C e 263 °C, respectivamente. Coloque os cones de amostragem e extração em 25 V e 3 V, respectivamente.
- Para os experimentos de CID, use o analisador de massa quadrupole para selecionar o padrão isotópico do complexo ternário [amb+M(II)+NTA]- utilizando o m/z do pico monoisotópico com configurações de resolução de baixa massa = 4,5 e massa alta = 16,5.
NOTA: Os íons [amb+M(II)+NTA]- são passados para os guias de íons sequenciais de três ondas itinerantes (onda T). - Certifique-se de que a onda T da armadilha tenha um fluxo de gás argônio de 3 mL/min e uma pressão de 2,83 x 10-2 mbar. Coloque a energia de colisão (CE) na armadilha em 5 V para evitar qualquer dissociação do complexo ternário. Deixe que a armadilha colete os íons do complexo ternário antes de liberá-los (200 μs tempo de liberação) no guia de íons de mobilidade de íons (IM) T-wave, usando um viés dc armadilha de 14 V, que mantém a dissociação do complexo na entrada IM ao mínimo.
- Certifique-se de que o guia de íons IM tenha uma pressão de 0,507 mbar usando uma taxa de fluxo de 20 mL/min de gás tampão ultrapure N2 . Rampa as ondas T no IM com alturas de 7 V a 30 V e com velocidades de 290 m/s a 801 m/s para cada varredura inicial e final do guia iM.
- Coloque o fluxo de argônio e a pressão da transferência T-wave como a armadilha T-wave. A transferência T-wave foi utilizada para a dissociação induzida por colisão do complexo ternário [amb+M(II)+NTA]- utilizando a transferência CE.
- Selecione o padrão de isótopos m/z do complexo de isótopos carregado negativamente [amb+M(II)+NTA]- usando o quadrupole de transmissão no modo de resolução.
- Identifique o padrão de isótopos m/z abrindo o programa de espectrometria de massa e selecionando o Spectrum. Selecione Ferramentas > modelo isótopo. Na janela pop-up, liste a fórmula molecular do complexo, verifique a caixa para Show Charged Ion, digite 1 para a carga de um negativo e clique em OK.
- No padrão de isótopos exibido do complexo, observe o pico de massa mais baixo. No software de instrumento, selecione Configuração > Quad Profile. Na janela que abre, selecione Manual Fixo e digite a massa do pico de padrão isotópico mais baixo. Clique em Atualizar e, em seguida, Feche.
- Selecione Configuração novamente e clique em Resolver Quad. Colete o espectro de íons negativos ES-IM-MS incrementalmente através de uma série de energias de colisão de transferência usando uma duração de execução de 5 minutos e tempo de varredura de 2 s.
NOTA: As energias preliminares de transferência podem ser testadas de 26-60 V em intervalos de 2 V. A gama final de energias de colisão de transferência examinadas não deve demonstrar nenhuma dissociação do complexo ternário com a menor energia e dissociação completa nos produtos com a maior energia. Para análise estatística de alta qualidade, esta análise ES-IM-MS deve ser realizada para cada complexo ternário amb pelo menos 3x por pessoas diferentes e em dias diferentes para determinar meios e desvios padrão.
4. Análise transversal de colisão ES-IM-MS (CCS)
- Limpe a tubulação de entrada ES e o capilar de metal com 500 μL de ácido acético glacial de 0,1 M, seguido por 500 μL de hidróxido de amônio de 0,1 M e, finalmente, 500 μL de solução de acetato de amônio pH 7,7.
- Liquefazer a solução de estoque de 1.000 ppm PA para temperatura ambiente e fazer duas diluições seriais; diluir para 100 ppm PA com água DI e, em seguida, diluir para 10 ppm solução PA diluindo com uma razão de 1:1 de água DI e acetonitrilo de grau HPLC.
- Colete o espectro de íon negativo IM-MS da amostra de 10 ppm PA por 10 min utilizando condições operacionais instrumentais.
NOTA: A taxa de fluxo de injeção e as condições de origem do ES foram as mesmas dos experimentos de CID (etapa 3.). Para as medições do CCS, o analisador de massa quadrupole estava em modo de não resolução e passou todos os íons para os três guias de íons de onda T sequenciais. O funcionamento da armadilha T-wave e guias de íons de ondas T foi o mesmo dos experimentos cid. A energia de colisão da célula de onda T de transferência estava em 4 V para permitir que íons passassem sem dissociação. - Prepare cada um dos complexos ternários descritos nas etapas 3.2.-3.6.
- Colete os espectros IM-MS de cada complexo ternário por 5 minutos.
NOTA: Utilize as mesmas condições instrumentais da etapa 4.3. - Colete o espectro de íon negativo IM-MS da amostra de 10 ppm PA por 10 min.
NOTA: A média dos tempos de chegada dos calibrantes pa coletados antes e depois dos complexos ternários amb são utilizados na determinação do CCS.
5. Análise dos dados do CID ES-IM-MS
- Identifique a espécie combinando os padrões teóricos de isótopos m/z do complexo ternário e seus produtos ao espectro experimental do IM-MS.
- Abra o programa de espectrometria de massa e selecione Chromatogram para abrir uma nova janela.
- Na janela Cromatograma , clique em Arquivo > Abra para encontrar e abrir o arquivo de dados IM-MS desejado.
- Clique com o botão direito do mouse, arraste pelo cromatograma e solte. O espectro MS será exibido em uma janela spectrum separada.
- Na nova janela que exibe o espectro, selecione Ferramentas > Modelo de Isótopo. Uma pequena janela vai aparecer. Digite a fórmula molecular da espécie amb, verifique a caixa de íons carregados e digite o estado de carga desejado. Clique em OK.
- Para distinguir todas as espécies do espectro IM-MS, repita esse processo na janela Spectrum e regissou sua gama de isótopos m/z .
- Para o complexo ternário de amb e seus produtos, use sua gama de isótopos m/z para identificá-los e extrair suas distribuições de tempo de chegada (ATD).
- Abra o software de separação de mobilidade de íons e selecione Arquivo > Aberto para encontrar e abrir o arquivo de dados.
- Clique esquerdo e arraste com o mouse para ampliar a gama de isótopos m/z do complexo ternário [amb+M(II)+NTA]-.
- Usando a ferramenta Seleção , clique à esquerda e arraste para selecionar o intervalo específico de isótopos para [amb+M(II)+NTA]- conforme identificado na etapa 5.1. Clique no botão Aceitar seleção atual .
- Para eliminar qualquer espécie coincidente m/z ou sinal de fundo, use a ferramenta Seleção para escolher o ATD associado ao complexo ternário. Clique no botão Aceitar seleção atual .
- Para exportar o arquivo ATD para o software de espectrometria de massa, vá para File > Export e clique em Reter tempo de deriva. Renomeie o arquivo se desejar e salve o arquivo na pasta apropriada.
- Determine pela integração da área sob a curva ATD extraída a intensidade relativa da espécie.
- Na janela Croromatograma , abra o arquivo exportado salvo do software de separação de mobilidade de íons. Selecione Processo e, em seguida, Integre. Use uma configuração de amplitude de pico para pico de 20 e clique em OK.
- Registre a área integrada como mostrado na janela cromatograma . Repetição passos 5.2.2.-5.2.5. para os dois produtos, ou seja, [NTA+M(II)]- e [amb+M(II)]-.
- Repetição passos 5.2.1.-5.3.2. para cada transferência de energia de colisão registrada.
- Utilize as áreas ATD integradas para o complexo ternário [amb+M(II)+NTA]- e dois produtos [NTA+M(II)]- e [amb+M(II)]- a cada ponto de energia de colisão de transferência para normalizar para uma escala percentual relativa.
- Crie uma planilha inserindo as identidades do complexo ternário e seus produtos e seu ATD integrado a cada energia de colisão.
- Para cada energia de colisão, utilize a soma dos ATDs integrados para [amb+M(II)+NTA]-, [NTA+M(II)]-, e [amb+M(II)]- para normalizar seus ATDs individuais em uma escala percentual relativa.
- A partir das medidas de TCID de replicação, encontre os desvios médios e padrão de cada ponto de dados. Converta a energia de colisão de transferência de quadro de laboratório (laboratório E) para a energia de colisão de massa central (Ecm) usando as massas médias do gás de colisão de argônio (mAr) e do complexo ternário (complexo m): Ecm = Laboratório E (mAr)/(mAr + mcomplexo).
NOTA: Ecm representa a energia máxima da colisão com o gás argônio, disponível para dissociação do complexo ternário. - Plotar o desvio médio e padrão das intensidades percentuais individuais de [amb+M(II)+NTA]-, [NTA+M(II)]-, e [amb+M(II)]- em um gráfico de intensidade relativa (%) vs. energia de colisão de centro de massa (eV) para exibir como as intensidades relativas da espécie mudam em função da energia de colisão.
6. Análise dos tempos médios de chegada para determinação de seções transversais de colisão (CCS)
- Abra o software de separação de mobilidade de íons e o arquivo contendo o espectro IM-MS da amostra de 10 ppm PA coletada com o conjunto de energia de colisão de transferência em 4 V. Extrair o ATD de cada uma das espécies pa cobradas negativamente e exportar os arquivos para o software de espectrometria de massa usando a opção Reter tempo de deriva (ver etapa 5.2.5.). Repita para o segundo arquivo calibradores PA.
- Abra o software de separação da mobilidade de íons. Use o File > Open para abrir um dos arquivos contendo o espectro IM-MS dos complexos ternários amb registrados entre os calibrantes pa. Extrair o ATD de cada um dos complexos ternários e exportar seus arquivos para o software de espectrometria de massa usando a opção Retain Drift Time (ver passo 5.2.5.).
- Use um método de calibração transversal28 para calcular o CCS do complexo ternário e seus produtos.
- Em uma planilha, calcule o CCS corrigido (Ωc) para cada uma das únicas espécies de PA carregadas negativamente a partir de seu CCS (Ω)29,30 medidos em gás tampão de hélio31 utilizando a Equação 1, onde z = carga do complexo ternário, ec = 1,602 x 10-19 C; m N2 = massa de nitrogênio (u), e íon m = massa do complexo ternário28.
 (1)
(1) - Encontre os tempos de deriva (tD) dos calibrantes pa e dos complexos ternários obtendo primeiro os tempos médios de chegada (tA) a partir da máxima das curvas ATD correspondentes e, em seguida, aplicando a Equação 2, onde c = coeficiente de atraso do detector (1,41 ms; verifique o instrumento, pois isso pode variar entre os instrumentos) e m/z = razão massa-para-carga do calibrante pa ou amb ternary complexo.
tD =tA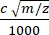 (2)
(2) - Crie um gráfico plotando o tD dos calibrantes de PA vs. Ωc. Em seguida, usando a Equação 3, encaixe os dados com uma regressão de menos quadrados para encontrar as constantes A' e B, onde A' corrige para o campo elétrico, temperatura e pressão no instrumento e B corrige para o comportamento não linear do dispositivo T-wave IM.
Ωc = A' tDB (3) - Utilizando as constantes A' e B e o valor tD dos complexos ternários amb, calcule suas Ωc usando a Equação 3 e seus Ω usando a Equação 1. Os valores ccs estimados por este método têm erros absolutos de cerca de 2%29.
- Em uma planilha, calcule o CCS corrigido (Ωc) para cada uma das únicas espécies de PA carregadas negativamente a partir de seu CCS (Ω)29,30 medidos em gás tampão de hélio31 utilizando a Equação 1, onde z = carga do complexo ternário, ec = 1,602 x 10-19 C; m N2 = massa de nitrogênio (u), e íon m = massa do complexo ternário28.
7. Métodos computacionais
- Use o método semi-empírico PM632 implementado em modelagem estrutural e software computacional33 para localizar conformadores otimizados em geometria dos [amb+M(II)+NTA]- complexos ternários e os pares de produtos íons e neutros: [amb+M(II)]- + NTA e [NTA+M(II)]- + amb observados a partir dos experimentos CID. Consulte o uso do visualizador de computação no Arquivo Suplementar para obter detalhes sobre como desenvolver e enviar cálculos.
NOTA: Para os sistemas atuais, o método PM6 reproduziu corretamente dados experimentais, mas, em geral, qualquer método de química quântica confiável e computacionalmente factível pode ser usado. - Execute otimizações de geometria e cálculos de frequência em várias estruturas iniciais diferentes para explorar diferentes conformações, estados de protonação e potenciais locais de ligação. Registo as energias eletrônicas + ponto zero de cada um dos pontos estacionários localizados para cada um dos complexos ternários e seus produtos.
NOTA: As estruturas iniciais para as otimizações de geometria devem investigar diferentes combinações possíveis de locais de ligação e arranjos conformais. As estruturas iniciais foram baseadas em conformadores B3LYP34 [amb+M(II)]- 3,4,6. Para [amb+M(II)+NTA]-, a NTA foi posicionada para competir com os locais substituentes da amb no Aa 1-Aa 2-Aa 6-Aa 7 e no terminus carboxilato para o estado de rotação singlet de Zn(II) ou o estado de giro trigêmeo de Ni(II). - Use um programa que possa realizar medições de seção transversal de colisão precisas medidas no gás tampão de hélio (CCSHe) usando as coordenadas atômicas destes cálculos químicos quânticos35.
NOTA: Programas desenvolvidos para cálculo de CCS precisosEle a partir de estruturas de peptídeos localizadas por cálculos químicos quânticos incluem MobCal36 e HPCCS37,38. - Escolha o conformador de energia mais baixo que exibe o LENnard-Jones CCSEle que concorda com o CCS medido pelo IM-MSEle para selecionar as estruturas de complexos ternários e produtos de dissociação para incluir na modelagem CRUNCH abaixo.
8. Modelagem CRUNCH
- Crie um arquivo de texto no formato descrito na seção de discussão ("formato de arquivo de texto de entrada CRUNCH").
NOTA: O arquivo inclui as seguintes colunas: (−1) energia de colisão de massa (Ecm), (1) média da intensidade relativa do produto [amb+M(II)], (2) desvio padrão da intensidade [amb+M(II)]- (3) da intensidade relativa do produto [NTA+M(II)]- e (4) desvio padrão da intensidade [NTA+M(II)]- intensidade. - Modelar o Ecentímetro-intensidades dependentes dos dois canais de reação [amb+M(II)+NTA]-para [amb+M(II)]- + NTA e [amb+M(II)+NTA]- para [NTA+M(II)]- + amb utilizando a técnica TCID no programa CRUNCH.
NOTA: Utilize as frequências vibracionais e rotacionais PM6 para o complexo ternário e os dois canais de produtos de íon e neutro. Use massas médias do complexo ternário, gás de colisão de argônio e produtos íons e neutros. Use valores dos cálculos PM6 ou do banco de dados NIST para as polarizabilidades (Å3) e momentos de dipolo (Debye) para os produtos neutros.- No menu principal do CRUNCH, abra o arquivo de texto (. GB5) contendo as intensidades relativas dependentes de cm E dos produtos. Resposta Não aos parâmetros de leitura.
- No menu principal do CRUNCH, selecione Modelagem > Definir todos os parâmetros. A partir das opções do modelo de reação, escolha a opção CID limiar padrão seguida por RRKM com integração sobre a distribuição de transferência de energia do complexo ternário20, digite 2 para canais independentes de produtos modelados e selecione Calcular seções transversais. Entrar no para fazer dois canais de produtos ter a mesma massa de íons?
- Para o Canal do Produto nº 1, digite a coluna [1] para os dados experimentais do produto [amb+M(II)]- coluna [2] para os desvios padrão do produto [amb+M(II)]- escoteria [amb+M(II)]- para a seção transversal do modelo não conconvolucido e coluna [6] para a seção transversal do modelo complicado. Digite 0 para resíduos de ajuste.
NOTA: Estes números de coluna correspondem às colunas do arquivo de entrada na etapa 8.1. como descrito na discussão ("formato de arquivo de texto de entrada CRUNCH"). - Para o Canal do Produto nº 2, digite a coluna [3] para os dados experimentais do produto [NTA+M(II)]- produto, coluna [4] para os desvios padrão do produto [NTA+M(II)]- produto, coluna [7] para a seção transversal do modelo não conconvolucido e coluna [8] para a seção transversal do modelo complicado. Digite 0 para resíduos de ajuste.
- Para o tipo de modelo não inconvolucido, escolha seção transversal 0 K (mudança cinética incluída), que inclui a correção estatística de RRKM dos turnos cinéticos devido à janela de tempo de 50 μs da célula de colisão para o detector TOF18.
- Para as opções de convolução, escolha a dupla integral de Tiernan, que inclui a convolução sobre distribuições de energia translacional entre o íon do complexo ternário e o gás de colisão de argônio21.
- Para o método de integração numérica, escolha a quadratura gaussiana com seções transversais pré-salvas, seguida pelo número de pontos de integração = 32, o número de desvios padrão = 3,0 e o número de desvios padrão para a segunda integral = 3,0.
- A massa de íon de complexo ternário (u) é lida automaticamente a partir do . Arquivo de texto GB5, seguido pela massa do gás de colisão (39.948 para argônio); usar os padrões de 0,20 eV para o FWHM do feixe de íons e 298,15 K para temperatura de gás. O programa lê automaticamente as energias mínimas e máximas de colisão de centro de massa do . Arquivo de texto GB5; usar o valor padrão para o incremento mínimo de energia.
- Use o valor padrão para o fator de escala Sig0, Não para permitir o dimensionamento de canais individuais de produtos e os valores padrão para N e M. Para o método para o cálculo g(i), escolha integrar-se sobre a densidade ro-vibracional dos estados, que inclui a distribuição interna de energia20 do complexo ternário [amb+M(II)+NTA]-.
- A partir das opções de entrada nos parâmetros moleculares, digite G para ler o arquivo de modelagem estrutural33 com as frequências vibracionais e rotacionais PM6 do complexo ternário. Resposta Sim à pergunta é um dos reagentes atômicos? Escreva a localização e o nome do arquivo de modelagem.
NOTA: As outras opções para entrar nas frequências vibracionais e rotacionais incluem o arquivo de parâmetro de leitura, que lerá nos parâmetros de um arquivo de texto ou editar/inserir constantes, o que permite a entrada manual de cada parâmetro. - Dimensione as frequências utilizando o fator de escala PM6 recomendado pelo NIST (1.062). Para obter mais detalhes sobre o dimensionamento, consulte a discussão ("fatores de escala para as frequências vibracionais"). O número de átomos no complexo ternário é lido a partir do arquivo. Resposta Não é a molécula linear? Digite a descrição dos reagentes (por exemplo, H+Zn+NTA- + Ar).
- Digite 1 para a carga em íon e 1.664 para a polarizabilidade do gás argônio39. A massa de íons e massa de alvo são para o complexo ternário e argônio, respectivamente, e são automaticamente lidos a partir do . Arquivo de texto GB5. Digite 0 para vibrações harmônicas.
NOTA: As seguintes opções são para escolher diferentes fatores de escala para frequências vibracionais altas ou baixas. Digite 1.062 para altas frequências e 0,0 para baixas frequências (veja discussão: fatores de escala para as frequências vibracionais). As frequências dimensionadas são mostradas. Escolha 0 para selecionar Sem Alteração. - Aperte Enter para ler as constantes rotacionais 1D e 2D do arquivo de modelagem estrutural33 inseridas na etapa 8.2.10. Selecione os valores padrão de 0 para os tratamentos de rotor dificultados e 1 para simetria de moléculas.
NOTA: O programa mostra os dados inseridos; hit Enter for No Changes. - Escolha os 300 Mil padrão para a temperatura de reação. Selecione Integração para o método de redução da densidade do array de estados. Selecione Sim para truncar a distribuição de energia. Digite 40000 cm-1 para energia máxima para distribuição, 2,0 cm-1 para o tamanho da lixeira e 32 para o número de pontos na distribuição de energia.
NOTA: Bata Enter 2x e verifique se a matriz truncada de 32 pt tem uma população >0,9. Se >0,9, digite Não para alterar lixeiras ou fator de condensação. Se <0,9, digite Sim e altere a energia máxima para distribuição e/ou tamanho da lixeira. - Para parâmetros para o modelo TCID/RRKM, escolha Sim para Alterar, digite 0 por tempo fixo e 0,000050 s para o limite superior da janela de detecção. Para o instrumento utilizado, este é o tempo que os íons levam para viajar da célula de colisão de transferência para o detector TOF e é calculado usando a Equação 2.
- Para moléculas energizadas, digite C para copiar valores dos reagentes já inseridos. Digite −1 para estado de transição de origem (TS), 0 para destino TS e P para prosseguir.
- Para o canal do produto 1, selecione 1 para estado de transição único a partir das opções do canal de dissociação e 0 para nenhum para a dissociação sequencial. Para o tipo de estado de transição, escolha 1 para órbita.
- Selecione G para ler os arquivos do programa de modelagem que contenham os parâmetros rotacionais e vibracionais PM6 para os produtos [amb+M(II)]- + NTA. Entrar no for é uma das espécies TS do PSL atômica? Digite o local e o nome do arquivo [ amb+M(II)]. Use 1.062 para frequências de escala, bata enter para o número de átomos, e digite Não para a molécula linear?
- Digite a localização e o nome do arquivo de modelagem que contém as frequências vibracionais e rotacionais para o produto NTA. Use 1.062 para frequências de escala, bata enter para o número de átomos, e digite Não para a molécula linear? Digite a descrição do TS em órbita, por exemplo, H+Zn-... A NTA.
- Digite 1 para carga de [amb+M(II)]-íon, e insira a polarizabilidade (16.12 Å3) e o momento do dipolo (4.6183 Debye) da NTA. Selecione 0 K para temperatura rotacional e dipolo bloqueado para o tratamento do estado de transição em órbita. Digite as massas médias (u) do íon [amb+M(II)]- íon e NTA.
- Digite 0 para vibrações harmônicas. Digite 1.062 para altas frequências e 0.0 para baixas frequências. Consulte a seção de discussão para obter mais detalhes sobre as frequências de dimensionamento; as frequências dimensionadas são mostradas. Escolha 0 para selecionar Sem Alteração. Aperte Enter para ler as constantes de rotação 1D e 2D dos arquivos de modelagem. Selecione 0 para rotores dificultados, 1 para simetria de moléculas e 1 para degeneração de reação. Digite a opção Sem Alterações.
- Para o canal do produto 2, selecione 1 para estado de transição único, 0 para nenhum para a dissociação sequencial e 1 para orbitar para o tipo de estado de transição.
- Selecione G para ler em arquivos de modelagem que contenham os parâmetros rotacionais e vibracionais PM6 para os produtos [NTA+M(II)]- e amb. Entrar no for é uma das espécies TS do PSL atômica? Escreva a localização e o nome do arquivo de modelagem [NTA+M(II)].
- Use 1.062 para frequências de escala, bata enter para ler o número de átomos, e entrar N pois a molécula linear? Escreva a localização e o nome do arquivo de modelagem amb. Use 1.062 para frequências de escala, bata enter para o número de átomos, e entrar N para é a molécula linear?
- Digite a descrição do TS em órbita (por exemplo, NTA+Zn-... H). Digite 1.0 para carga de [NTA+M(II)]- íon, e digite a polarizabilidade (Å3) e o momento do dipolo (Debye) do amb. Selecione 0,0 K para temperatura rotacional e dipolo bloqueado para o tratamento do estado de transição em órbita. Insira as massas médias (u) dos produtos [NTA+M(II)]- e amb.
NOTA: O arquivo de saída contém a polarizabilidade e os momentos do dipolo do amb. A polarizabilidade está nas unidades do Bohr3 e precisa ser convertida para as unidades de Å3. - Digite 0 para vibrações harmônicas. Digite 1.062 para altas frequências e 0 para baixas frequências. Consulte a discussão para obter mais detalhes sobre as frequências de dimensionamento. As frequências dimensionadas são mostradas. Escolha 0 para selecionar Sem Alteração. Aperte Enter para ler as constantes de rotação 1D e 2D dos arquivos de modelagem. Selecione 0 para rotores dificultados, 1 para simetria de moléculas e 1 para degeneração de reação. Enter Sem Alterações.
- Para lidar com rotações 2D iativas, selecione as opções padrão de distribuição de momento angular estatístico e integre P(E,J) sobre a distribuição J. Use o valor padrão de 32 no número de pontos na integração.
NOTA: Essas seleções escolhem o método de integração sobre o momento angular totalníveis J 16,17. A saída resultante permite ao investigador verificar se toda a entrada está correta. - Selecione as energias de ativação relativas à opção de molécula energizada e insira energia relativa (eV) para o canal do produto 1 que esteja próximo da energia limiar observada no gráfico da intensidade relativa versus energia de colisão de centro de massa do produto [amb+M(II)]- ( Figura 4).
- Para o canal do produto 2, digite energia relativa (eV) próxima à energia limiar observada no gráfico da intensidade versus energia de colisão em massa do produto [NTA+M(II)]. Para calcular o número de estados para cada canal do produto, use um tamanho de caixa de 2.0. Pressione Enter e, em seguida, Não para continuar.
- No menu Modelo , selecione Otimizar parâmetros para encaixar dados e inserir a energia mínima e energia máxima para iniciar e terminar o ajuste de dados, respectivamente.
NOTA: Use uma pequena faixa de energia que inclua os limiares de ambos os canais. Para mais detalhes, consulte discussão: faixa de energia para adequação do modelo TCID selecionado aos dados experimentais. - Selecione -1 para modos de ponderação de desvios padrão experimentais. Com base nos dados, selecione um desvio mínimo aceitável de 0,01 a 0,001. Selecione Não para dimensionamento otimizado de canais individuais e 0 para o número de iterações.
NOTA: Uma alternativa ao uso de desvios-padrão é a opção estatística . - Use o valor padrão para o limite de convergência E0 e selecione Não para manter qualquer parâmetro no valor atual. Digite 0.5 e 2.0 eV para os limites inferiores e superiores para evitar falha de otimização e selecione a diferença finita central para o método de avaliação de derivativos. Use o valor padrão para precisão numérica e selecione Não para alterar tamanhos de etapas derivativas.
NOTA: Um método alternativo é selecionar Sim para manter qualquer parâmetro no valor atual. Este método é descrito ainda mais na discussão: otimização de parâmetros. - A partir do menu Otimização , selecione iniciar a otimização. O programa CRUNCH otimizará o modelo TCID selecionado aos dados experimentais.
NOTA: Se a otimização não encontrar ajustes satisfatórios, a partir do menu de mudanças , tente alterar o intervalo de energia para cobrir apenas as primeiras intensidades que sobem dos limiares. Quando um ajuste razoável estiver localizado, aumente o alcance de energia e encaixe novamente. Outras opções que podem ajudar a encontrar ajustes nos dados incluem a escolha de manter qualquer parâmetro atualmente em parâmetros otimizados e mudar as opções de ponderação em pesos. Veja a discussão para essas opções. - Quando um modelo se encaixar nos dados for encontrado, aperte Enter até que o menu Modelo apareça. Se apenas parte da gama de energia de dados experimentais for equipada com o modelo TCID, selecione Calcular e modelo convolute para estender o modelo adequado a todas as energias experimentais de colisão.
- No menu Modelo , selecione Delta H e S em T.
NOTA: O modelo CRUNCH não desconvolucido relaciona as energias limiares de 0 K aos 0 K enthalpies (ΔH0) de dissociação do complexo ternário nos dois canais de produtos independentes (Tabela 2). As 298 K enthalpies (ΔH298) e as energias livres de Gibbs (ΔG298) de dissociação também são derivadas de correções térmicas e entropias de mecânica estatística usando as frequências rotacionais e vibracionais reagentes e produtos PM6.
Resultados
A dissociação competitiva induzida por colisão dos [amb+M(II)+NTA]- complexos ternários de A e H em [amb+M(II)]- + NTA ou [NTA+M(II)]- + amb, são mostrados na Figura 3. O amb é mostrado como A ou H e o M = Zn ou Ni. O complexo ternário [A+Zn(II)+NTA]- possui limiares aparentes de cerca de 0,7 eV de energia de colisão (CE) para produzir [A+Zn(II)]- e cerca de 0,9 eV para produzir [NTA+Zn(II)]-. A dissociação dos produtos [A+Ni(II)+NTA]- complexo (Figura 3B) exibe limiares semelhantes (~1,1 eV) tanto para os produtos [NTA+Ni(II)]- quanto [A+Ni(II)], com [NTA+Ni(II)]- aumentando para 90% de intensidade relativa, enquanto as intensidades de [A+Ni(II)]- não sobem acima de 18%. Para o complexo ternário [H+Zn(II)+NTA], o principal produto é [H+Zn(II)]- subindo de um limiar de cerca de 0,6 eV para cerca de 85% de intensidade relativa, e em energias acima de 1,0 eV, o [NTA+Zn(II)]- sobe para cerca de 30%. Há também um canal para perda de água de [H-H2O+Zn(II)]-. Para [H+Ni(II)+NTA]- (Figura 3D), o [H+Ni(II)]- sobe de um limiar de cerca de 0,9 eV para cerca de 40% de intensidade relativa, enquanto o [NTA+Ni(II)]- sobe de ~1,0 eV para cerca de 80%. Incluído nos gráficos está o CE onde o complexo ternário é 50% dissociado. Os complexos ternários ni(II) requerem 0,31-0,37 eV maiores do que suas contrapartes do complexo ternário Zn(II) para serem 50% dissociados. Isso sugere que os complexos Ni(II) são mais estáveis e requerem maior CE para dissociar, o que é ainda mais investigado usando a técnica TCID.
A Figura 4 ilustra o método TCID competitivo, que permite o encaixe simultâneo dos dois canais de produtos concorrentes.
[amb+M(II)+NTA] → [amb+M(II)]- + NTA (1)
[amb+M(II)+NTA] → [NTA+M(II)]- + amb (2)
A superfície de energia potencial (PES) ilustra o complexo ternário energizado dissociando-se nos canais de produtos concorrentes e mostra as espécies otimizadas para geometria PM6 usadas para modelar a dissociação de [ambH+Zn(II)+NTA]-. Inclusos no PES estão a densidade dos estados do complexo ternário e a soma dos estados dos produtos. As energias limiares de 0 K, E1 e E2, equivalem à mudança de 0 Kenthalpy para reações 1 e 2.
A Figura 5 mostra as estruturas dos outros três complexos ternários otimizados em geometria utilizados neste estudo. Essas espécies foram escolhidas com base em suas energias eletrônicas e de ponto zero previstas e seu acordo com as seções transversais de colisão medidas pelo IM-MS (CCSHe). A Tabela 1 mostra que há um acordo entre os complexos ternários LJ CCSEle e o experimental IM-MS CCSEle porque eles concordam dentro de suas incertezas mútuas. As conformações do [amb+M(II)] e da Amb foram baseadas nos achados da modelagem anterior de DFT 3,4,5,6. Os parâmetros moleculares desses conformadores PM6 foram utilizados na modelagem TCID das dissociações resolvidas pela energia dos complexos ternários, incluindo suas frequências ro-vibracionais para o cálculo de sua densidade e soma dos estados.
A Figura 6 mostra que o limiar de TCID CRUNCH complicado se encaixa nas intensidades do produto resolvidos com energia. Os ajustes complicados incluem as distribuições de energia disponíveis e momento angular dos reagentes [amb+M(II)+NTA]- + Ar. Os ajustes não desconvolucidos (não mostrados) previram a mudança de 0 K em inenthalpies (ΔH0) para a dissociação do complexo ternário, e a Tabela 2 mostra o ΔH0 e ΔH298 (kJ/mol) para reações 1 e 2. Para a dissociação dos complexos ternários Zn(II), ambos os A e H exibem ΔH0 para a reação 1, que são 31 kJ/mol e 15 kJ/mol inferiores aos ΔH0 para reação 2, respectivamente, indicando que tanto A quanto H têm maior afinidade Zn(II) do que o NTA. O complexo ternário [A+Ni(II)+NTA]- o complexo ternário exibe ΔH0 = 146 e 148 kJ/mol para reações 1 e 2, respectivamente, indicando que A e NTA têm afinidades semelhantes para Ni(II). No entanto, a dissociação de [H+Ni(II)+NTA]- mostra que o ΔH0 para reação 1 é 36 kJ/mol menor do que para a reação 2, indicando que H tem uma maior afinidade Ni(II) do que a NTA. No geral, os complexos [amb+Ni(II)+NTA]- apresentam maior dissociação de enthalpies do que suas contrapartes [amb+Zn(II)+NTA], com exceção de A dissociante em [NTA+Ni(II)]-. A Tabela 3 mostra as energias livres de Gibbs (ΔG298) de associação e as constantes de formação (K) para as reações inversas:
[amb+M(II)] - NTA → [amb+M(II)+NTA]- (3)
[NTA+M(II)] - + amb → [amb+M(II)+NTA]- (4)
A Tabela 3 demonstra que a formação dos complexos ternários Ni(II) é mais exergônica e exibe maiores constantes de formação K do que os complexos Zn(II) em todos os casos. A reação 4 (ou seja, a associação de tag amb com o complexo de íons metálicos NTA) é de particular interesse, pois representa a proteína recombinante marcada amb ao íon metálico imobilizado NTA dentro da coluna IMAC. A reação 4 para a formação de [ambA+Ni(II)+NTA] exibe o ΔG298 mais espontâneo = 53,1 kJ/mol e a maior constante de formação, K = 2,01 x 109.
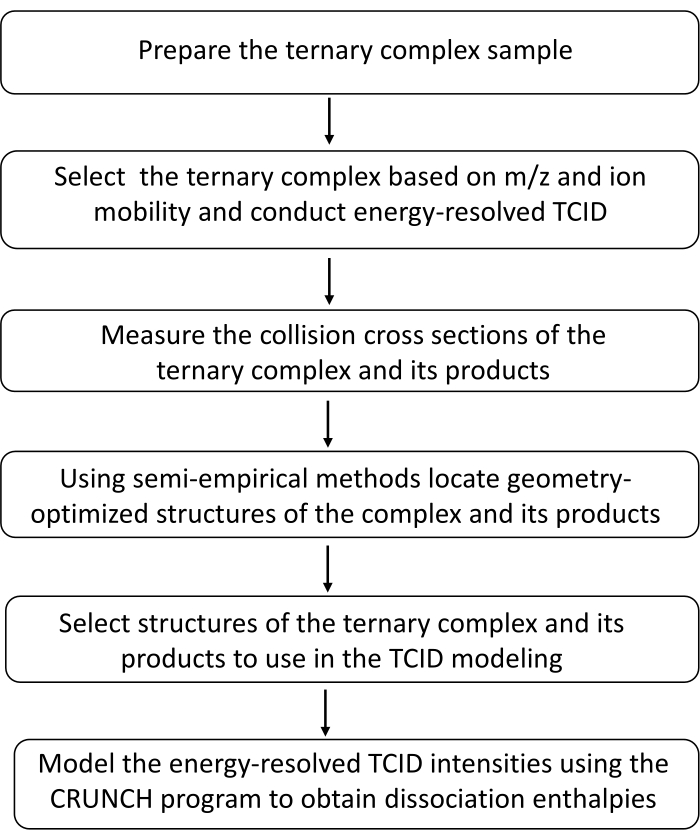
Figura 1: Visão geral do método TCID ES-IM-MS. Clique aqui para ver uma versão maior desta figura.
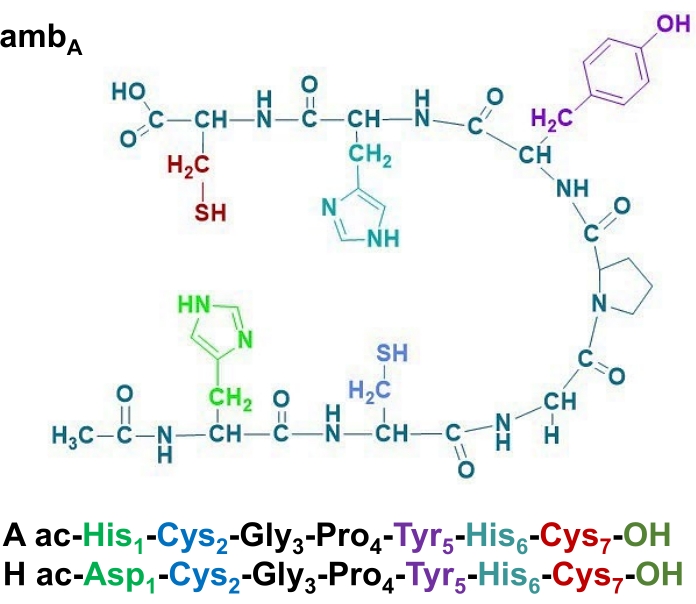
Figura 2: As estruturas primárias dos peptídeos Amb A e H. A cor destaca os potenciais locais de ligação metálica. Clique aqui para ver uma versão maior desta figura.
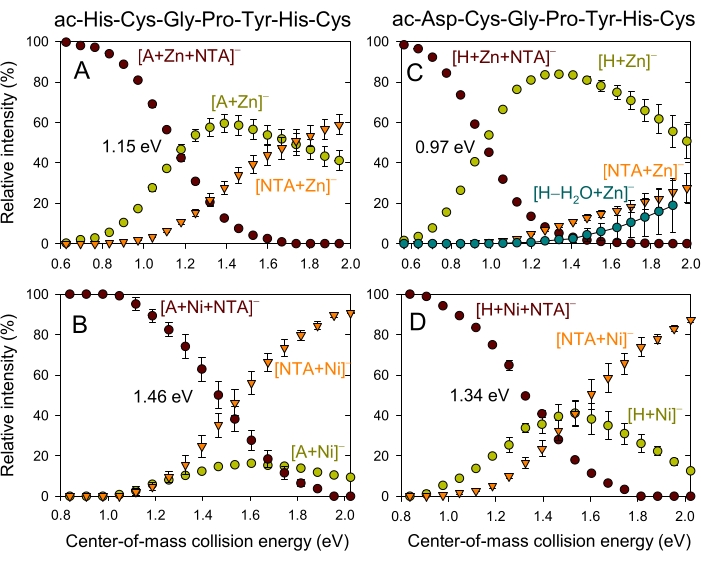
Figura 3: A dissociação induzida por colisão de limiar (eV) do limiar de massa, do centro de massa, resolvida pela energia (eV) da dissociação induzida por colisão de [amb+M(II)+NTA]-. A dependência energética dos íons do produto [amb+M(II)]- [NTA+M(II)]- e [amb-H2O+Zn(II)]- é mostrada. A energia de colisão em massa, onde há 50% de dissociação do complexo ternário [amb+M(II)+NTA], está incluída nos gráficos. Clique aqui para ver uma versão maior desta figura.
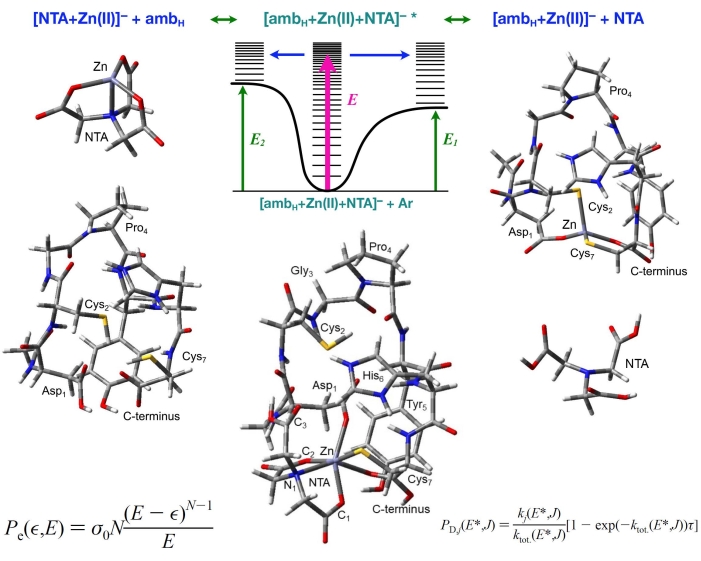
Figura 4: O modelo para o método TCID resolvido em energia. As colisões entre [ambH+Zn(II)+NTA]- + argônio resultam na dissociação aos produtos [ambH+Zn(II)]- + NTA ou [NTA+Zn(II)]- + produtos ambH . As energias limiares E1 e E2 equivalem aos 0 Kenthalpies de dissociação (ΔH0) para as reações [ambH+Zn(II)+NTA]- → [ambH+Zn(II)]- + NTA ou [ambH+Zn(II)+NTA]- → [NTA+Zn(II)]- + ambH, respectivamente. Clique aqui para ver uma versão maior desta figura.
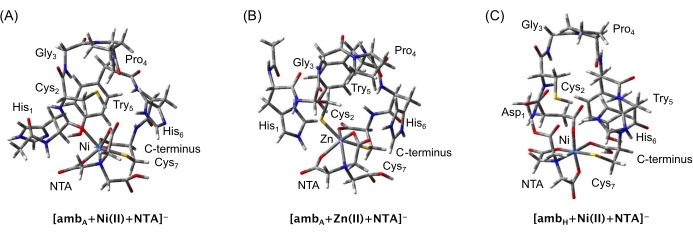
Figura 5: Os complexos ternários otimizados pela geometria PM6 [amb+M(II)+NTA]- complexos de A e H. Conformadores utilizados na modelagem TCID dos dados experimentais. Esses conformadores foram selecionados de outras estruturas candidatas comparando suas energias eletrônicas PM6 e como suas seções transversais de colisão LJ (CCSHe) em comparação com o CCS medido pelo IM-MS. Clique aqui para ver uma versão maior desta figura.

Figura 6: A dissociação induzida por colisão de [amb+M(II)+NTA]-. Para as espécies A e H, são mostrados os íons de produtos de [amb+M(II)]- e [NTA+M(II)]- com os ajustes de limiar CRUNCH complicados. Os valores de energia (eV) mostrados são os entalhes de dissociação em 0 K para as reações [amb+M(II)+NTA]- → [amb+M(II)]- + NTA ou [amb+M(II)+NTA]- → [NTA+M(II)]- + amb. Por favor clique aqui para ver uma versão maior desta figura.
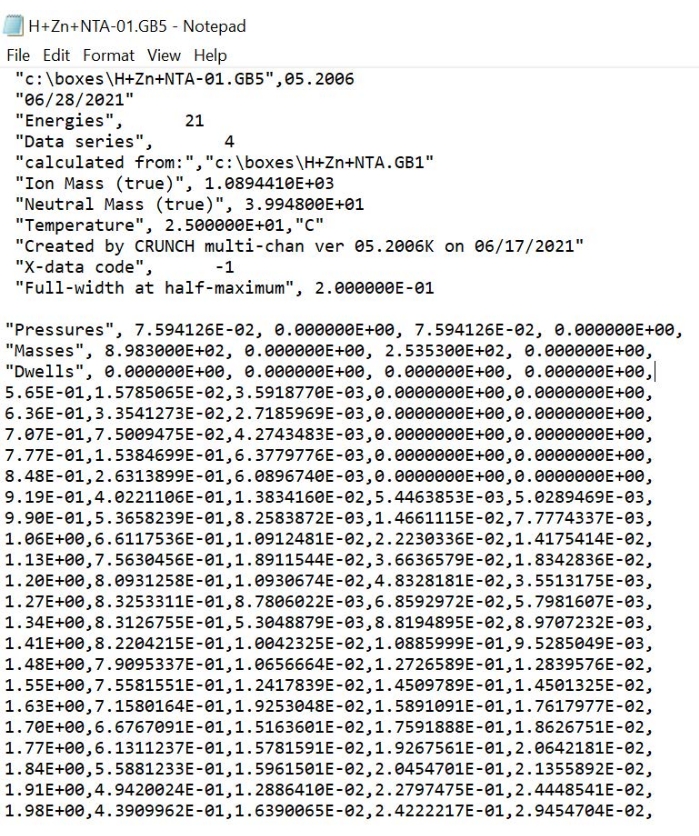
Figura 7: O formato do arquivo de entrada de texto CRUNCH. O arquivo contém as intensidades relativas médias e seus desvios padrão dos íons do produto formados em função da energia de colisão em massa. Clique aqui para ver uma versão maior desta figura.
| amb | [amb+Zn(II)+NTA] - | [amb+Ni(II)+NTA] - | ||
| PM6 | Exp.a | PM6 | Exp.a | |
| Um | 214±2 | 214 | 219±2 | 218 |
| H | 211±5 | 216 | 212±3 | 215 |
| um ES-IM-MS CCSEle mede as medidas de ±4 Å2. | ||||
Tabela 1: Comparação das seções transversais de colisão LJ dos conformadores PM6 de [amb+M(II)+NTA]-. As seções teóricas dos conformadores PM6 são comparadas com o CCS experimental queele mediu com o ES-IM-MS.
| [amb+Zn(II)+NTA] - → | [amb+Ni(II)+NTA] - → | |||||||
| [amb+Zn(II)] - + NTA | [NTA+Zn(II)] - + amb | [amb+Ni(II)] - + NTA | [NTA+Ni(II)] - + amb | |||||
| amb | ΔH0 | ΔH298 | ΔH0 | ΔH298 | ΔH0 | ΔH298 | ΔH0 | ΔH298 |
| Um | 118 | 127 | 149 | 182 | 146 | 171 | 148 | 154 |
| H | 96.4 | 92.3 | 111 | 115 | 125 | 140 | 161 | 216 |
Tabela 2: Resultados termoquímicos das análises do TCID. As reações dependentes de energia [amb+M(II)+NTA]- → [amb+M(II)]- + NTA ou [amb+M(II)+NTA]- → [NTA+M(II)]- + amb, mostrando os 0 K enthalpies de dissociação (ΔH0) derivados do ajuste não convolutado do modelo TCID, e 298 K enthalpies de dissociação (ΔH298) derivados de ΔH0 e correções térmicas mecânicas estatísticas usando as frequências rotacionais e vibracionais PM6. Os valores são dados em kJ/mol.
| [amb+Zn(II)] - + → NTA | [NTA+Zn(II)] - + amb → | [amb+Ni(II)] - + → NTA | [NTA+Ni(II)] - + amb → | |||||
| [amb+Zn(II)+NTA] - | [amb+Zn(II)+NTA] - | [amb+Ni(II)+NTA] - | [amb+Ni(II)+NTA] - | |||||
| amb | ΔG298 | K | ΔG298 | K | ΔG298 | K | ΔG298 | K |
| Um | -34.0 | 9.05 x 105 | -21.8 | 6,59 x 103 | -45.7 | 1.01 x 108 | -53.1 | 2.01 x 109 |
| H | -29.3 | 1,36 x 105 | -30.2 | 1,95 x 105 | -47.0 | 1,71 x 108 | -31.1 | 2,81 x 105 |
Tabela 3: Energias livres de associação de Gibbs (ΔG298) e constantes de formação de equilíbrio (K). ΔG298 e K em 298 K para as reações inversas [amb+M(II)]- + NTA → [amb+M(II)+NTA]- e [NTA+M(II)]- + amb → [amb+M(II)+NTA]-. Derivados de ΔH298 e cálculos estatísticos de entropia mecânica utilizando as frequências rotacionais e vibracionais PM6. Os valores para ΔG298 estão em kJ/mol.
Arquivo Suplementar. Clique aqui para baixar este Arquivo.
Discussão
Passos críticos
Análises de dissociação induzida por colisão de limiar eS-IM-MS (TCID). O TCID usou a célula de onda T de transferência na presença de argônio como célula de colisão. Antes da dissociação, os íons precursores são termeléculados por colisões de baixa energia com gás nitrogênio à medida que passam pela célula de mobilidade de íons (IM). Isso resulta em um TCID mais reprodutível resolvido pela energia do que é alcançado usando a armadilha como a célula de colisão 6,40. A termelétrica do [amb+M(II)+NTA]- antes da dissociação também permite que a energia interna disponível do complexo ternário seja caracterizada com temperatura de 298 K. A dissociação na célula de transferência também significa que o complexo ternário e seus íons de produto têm o mesmo tempo médio de chegada no detector, o que foi útil para identificar a dissociação do complexo ternário que só ocorreu na célula de transferência. Outras regiões onde a dissociação pode ocorrer são a fonte ES (o cone amostral é mantido a 25 V para evitar isso) ou na entrada da célula IM. Os íons de produto produzidos pela dissociação do complexo ternário nessas regiões têm tempos de deriva diferentes daqueles produzidos na célula de transferência porque os íons do produto são separados do complexo ternário na célula IM. Esses íons de produtos foram excluídos da análise. Neste protocolo, apenas as distribuições integradas de tempo de chegada para os íons precursores e de produtos que estão co-alinhados são usadas para determinar suas intensidades. O ajuste do viés da armadilha é a tensão que controla a tensão de injeção na célula IM, o que contribui para o CID na entrada da célula IM. O viés da armadilha foi definido em 14 V, o que manteve a dissociação de fundo ao mínimo, sem afetar excessivamente as intensidades globais. Um estudo anterior41 determinou que a temperatura efetiva (limite superior) do dimer peptídeo da enkephalina leucina era de 449 K na entrada da célula IM. No entanto, a temperatura efetiva diminuiu rapidamente à medida que o dimer passou para baixo da célula IM. Os tempos de chegada dos complexos de amb estudados aqui exibiam distribuições gaussianas, indicando que foram termelétricas à medida que passavam pela célula IM.
Análises transversais de colisão ES-IM-MS (CCS). Os tempos de deriva do CCS foram encontrados experimentalmente como resultado de colisões com nitrogênio. Esses valores foram convertidos em tempos de deriva CCS derivados de hélio usando uma curva de calibração de padrões conhecidos. Isso é essencial, pois os programas utilizados para medir o CCS dos conformadores PM6 exigem as normas de hélio mais utilizadas.
Modificações e solução de problemas da técnica
Formato de arquivo de texto de entrada CRUNCH. O arquivo de texto de entrada adequado para o programa CRUNCH é mostrado na Figura 7. Os cabeçalhos em ordem de cima para baixo são localização do arquivo e versão do CRUNCH; data; número de energias; número de séries de dados excluindo a primeira coluna de energias; arquivo fonte; massa do complexo precursor; massa de argônio; temperatura do experimento; data de criação; x-dados designados como −1 (as energias de colisão em massa); e a largura total à metade do máximo (FWHM) do feixe de íons. Esses valores devem ser modificados para cada experimento TCID. A propagação de energia FWHM do feixe de íons e da energia zero deve ser determinada retardando a análise potencial (RPA) através da varredura do CE através de baixas tensões e monitorando a corrente total de íons. No entanto, sob as condições de funcionamento do IM no presente estudo, o sinal de corrente de íon só diminuiu cerca de 50% quando a CE de transferência foi definida para seu menor valor. A energia do feixe de íons zero e FWHM só poderiam ser medidas após o retardo adicional, baixando a lente IM de saída. Neste último caso, o FWHM do derivado da curva RPA deu uma propagação típica de energia de íons de 1,5 V no quadro de laboratório ou 0,035 eV no quadro central de massa13.
A linha de pressões diz respeito à pressão dentro da célula de colisão, mas não é usada aqui. As pressões de argônio na célula de colisão podem ser variadas e os dados do TCID podem ser medidos a três pressões para extrapolar para condições de colisão única. No entanto, apenas uma pressão foi utilizada neste estudo, e a pressão resulta em múltiplas colisões. Desenvolver a nova plataforma para uma única colisão é uma área de pesquisa em andamento. As massas se relacionam com os dois íons de produto cujas intensidades estão nas colunas abaixo. Habitações podem ser deixadas como padrão. As cinco colunas são as energias de colisão em massa (designadas −1); a média das intensidades de íons da espécie com massa 898,30 u; os desvios padrão das intensidades de íons das espécies 898,30 u; a média das intensidades de íons da espécie com massa 253,53 u; e os desvios padrão das intensidades de íons das espécies 253,53 u.
Modelagem Molecular
O número de conformadores foi reduzido inicialmente por meio de modelos derivados de estudos anteriores 9,10,11,12,13. O encaixe CRUNCH requer uma triagem cuidadosa de reagentes, moléculas ativadas e estados de transição para obter energias precisas de limiar. A pesquisa anterior 9,10,11,12,13 incluiu uma triagem extensiva de conformadores [amb+M(II)] para obter as estruturas com os parâmetros utilizados na modelagem CRUNCH aqui. Apenas complexos com ligações de peptídeos trans foram utilizados porque apenas eles estão de acordo com o IM-MS medido CCSHe10. Os métodos de modelagem molecular B3LYP e PM6 prevêem a menor energia [amb+M(II)]- conformer que exibe Aa1-Cys 2-Cys 7 e coordenação do terminus carboxilato de Zn(II) ou Ni(II)10,11,12,13. A familiaridade com os comportamentos dos modelos conhecidos permitiu que os novos conformadores de [amb+M(II)+NTA]- fossem determinados de forma mais eficiente. Para auxiliar na determinação da conformidade, uma vez que os conformadores de energia inferiores foram localizados pelo método PM6, eles foram filtrados e reavaliados sistematicamente até que os conformadores de energia mais viáveis permanecessem.
Modelagem CRUNCH
Janela de tempo para observar a dissociação. Neste estudo, foi utilizada a janela de tempo de 50 μs desde o início da célula de transferência até o final do analisador TOF, onde o detector de placas multicanais está posicionado. Pode ser melhor usar a janela de tempo experimental entre a ativação na célula de transferência e a entrada para o analisador de massa TOF porque, se o íon ativado se dissociar durante seu tempo no refletor TOF, essa decadência metastável será medida em um m/z diferente. No entanto, neste estudo, os íons de produto observados nos espectros de massa foram todos identificáveis como as espécies m/z não modificadas mostradas na Figura 3. Isso indica que a decadência metastável não foi um problema. Outras pesquisas poderiam investigar isso examinando uma reação conhecida com um alto limiar e verificando se a energia de limiar correta é obtida usando a janela de tempo de 50 μs e a modelagem RRKM.
Fatores de escala para as frequências vibracionais. Foram utilizados os fatores de dimensionamento recomendados pelo NIST para frequências vibracionais PM6 (1.062). Estes foram satisfatórios para a montagem dos dados [A+Zn(II)+NTA]-, [A+Ni(II)+NTA]-, e [H+Zn(II)+NTA]- dados. Para alguns casos em que o canal de energia mais alto é entropicamente favorecido sobre o canal de energia mais baixo, pode ser necessário escalar adicionalmente as frequências do segundo canal. Uma abordagem é escalar as frequências abaixo de 900 cm−1 (pois estas são as menos precisas) para afrouxar as frequências e tornar o TS mais favorecido entropticamente.
Otimização de parâmetros. Usar a opção Sim para manter qualquer parâmetro no valor atual pode ser útil para encaixar os dados com sucesso. Para o primeiro ajuste, o E0(2) é mantido e o modelo TCID é ajustado aos dados otimizando as variáveis CONST, E0(1) e N. Uma vez localizado um bom ajuste, a opção parâmetros e Segure qualquer parâmetro no valor presente pode ser usado para segurar CONST, E0(1) e N, permitindo que o E0(2) otimize os dados. Finalmente, uma vez que o E0(2) é otimizado, na opção parâmetros , todos os quatro parâmetros CONST, E0(1), E0(2) e N devem ser autorizados a otimizar para os dados.
Faixa de energia para a montagem do modelo TCID selecionado aos dados experimentais. A faixa de energia usada para se adequar aos dados experimentais deve reproduzir o máximo possível dos dados de intensidade experimental, mantendo um bom ajuste na região limiar. Pode-se começar adaptando o modelo TCID a uma pequena faixa de energia nos limiares dos dados experimentais. Pode-se escolher uma energia inicial que exibe a intensidade de fundo pouco antes do comportamento do limiar de intensidade crescente. Uma vez que o ajuste TCID seja otimizado para a gama de dados experimentais, o alcance deve ser aumentado em 0,1 eV e o ajuste deve ser otimizado novamente. Este procedimento deve ser repetido para se encaixar o máximo possível do intervalo de dados, mantendo o ajuste da região limiar.
Análises termoquímicas. Os resultados termoquímicos da opção Delta H e S at T devem ser comparados com uma série de diferentes acessos de energia que se encaixam nos dados para estimar o desvio padrão do ajuste do modelo TCID. Ajustes para comparar devem incluir faixas menores que se encaixam bem nas intensidades iniciais de limiar de elevação com aquelas com faixas maiores que incluem as energias mais altas também.
Divulgações
Os autores não têm conflito de interesses para divulgar.
Agradecimentos
Este material é baseado em trabalho apoiado pela Fundação Nacional de Ciência sob 1764436, programa NSF REU (CHE-1659852), suporte a instrumentos NSF (MRI-0821247), Bolsa de Física e Astronomia para o Sucesso (PASS) Projeto NSF (1643567), Fundação Welch (T-0014) e recursos de computação do Departamento de Energia (TX-W-20090427-0004-50) e L3 Communications. Os autores agradecem a Kent M. Ervin (Universidade de Nevada - Reno) e Peter B. Armentrout (Universidade de Utah) por compartilharem o programa CRUNCH e por conselhos sobre a montagem da PBA. Os autores agradecem ao grupo de Michael T. Bower na Universidade da Califórnia - Santa Barbara por compartilhar o programa Sigma.
Materiais
| Name | Company | Catalog Number | Comments |
| Acetonitrile HPLC-grade | Fisher Scientific (www.Fishersci.com) | A998SK-4 | |
| Alternative metal binding (amb) peptides | PepmicCo (www.pepmic.com) | designed peptides were synthized by order | |
| Ammonium acetate (ultrapure) | VWR | 97061-014 | |
| Ammonium hydroxide (trace metal grade) | Fisher Scientific (www.Fishersci.com) | A512-P500 | |
| Driftscope 2.1 software program | Waters (www.waters.com) | software analysis program | |
| Gaussian 09 | Gaussian | Electronic Structure Modeling Software | |
| GaussView | Gaussian | Graphical Interface to Visualize Computations | |
| Glacial acetic acid (Optima grade) | Fisher Scientific (www.Fishersci.com) | A465-250 | |
| Ion-scaled Lennard-Jones (LJ) method | Sigma | Michael T. Bowers’ group of University of California at Santa Barbara | |
| MassLynx 4.1 | Waters (www.waters.com) | software analysis program | |
| Microcentrifuge Tubes | VWR | 87003-294 | 1.7 mL, polypropylene |
| Microcentrifuge Tubes | VWR | 87003-298 | 2.0 mL, polypropylene |
| Ni(II) nitrate hexahydrate (99% purity) | Sigma-Aldrich (www.sigmaaldrich.com) | A15540 | |
| Poly-DL-alanine | Sigma-Aldrich (www.sigmaaldrich.com) | P9003-25MG | |
| Waters Synapt G1 HDMS | Waters (www.waters.com) | quadrupole - ion mobility- time-of-flight mass spectrometer | |
| Zn(II) nitrate hexahydrate (99%+ purity) | Alfa Aesar (www.alfa.com) | 12313 |
Referências
- Kim, Y. -. M., Chen, P. Ligand binding energy in [(bipy)Rh(PCH)]+ by collision-induced dissociation threshold measurements. International Journal of Mass Spectrometry. 202 (1-3), 1-3 (2000).
- Plattner, D. Electrospray mass spectrometry beyond analytical chemistry: Studies of organometallic catalysis in the gas phase. International Journal of Mass Spectrometry. 207 (3), 125-144 (2001).
- Narancic, S., Bach, A., Chen, P. Simple fitting of energy-resolved reactive cross sections in threshold collision-induced dissociation (T-CID) experiments. Journal of Physical Chemistry A. 111 (30), 7006-7013 (2007).
- Ervin, K., Armentrout, P. B. Systematic and random errors in ion affinities and activation entropies from the extended kinetic method. Journal of Mass Spectrometry. 39 (9), 1004-1015 (2004).
- Cooks, R. G., Wong, P. S. H. Kinetic method of making thermochemical determinations: Advances and applications. Accounts of Chemical Research. 31 (7), 379-386 (1998).
- Ervin, K. Microcanonical analysis of the kinetic method. The meaning of the "apparent entropy". Journal of the American Society of Mass Spectrometry. 13 (5), 435-452 (2002).
- Amarasinghe, C., Jin, J. -. P. The use of affinity tags to overcome obstacles in recombinant protein expression and purification. Protein & Peptide Letters. 22 (10), 885-892 (2015).
- Bornhorst, J. A., Falke, J. J. Purification of proteins using polyhistidine affinity tags. Methods in Enzymology. 326, 245-254 (2000).
- Yousef, E. N., Angel, L. A. Comparison of the pH-dependent formation of His and Cys heptapeptide complexes of nickel(II), copper(II), and zinc(II) as determined by ion mobility-mass spectrometry. Journal of Mass Spectrometry. 55 (3), 4489 (2020).
- Lin, Y. -. F., et al. Weak acid-base interactions of histidine and cysteine affect the charge states, tertiary structure, and Zn(II)-binding of heptapeptides. Journal of the American Society of Mass Spectrometry. 30, 2068-2081 (2019).
- Wagoner, S. M., et al. The multiple conformational charge states of zinc(II) coordination by 2His-2Cys oligopeptide investigated by ion mobility - mass spectrometry, density functional theory and theoretical collision cross sections. Journal of Mass Spectrometry. 51 (12), 1120-1129 (2016).
- Flores, A. A., et al. Formation of Co(II), Ni(II), Zn(II) complexes of alternative metal binding heptapeptides and nitrilotriacetic acid: Discovering new potential affinity tags. International Journal of Mass Spectrometry. 463, 116554 (2021).
- Flores, A. A., et al. Thermochemical and conformational studies of Ni(II) and Zn(II) ternary complexes of alternative metal binding peptides with nitrilotriacetic acid. International Journal of Mass Spectrometry. 473, 116792 (2022).
- Sesham, R., et al. The pH dependent Cu(II) and Zn(II) binding behavior of an analog methanobactin peptide. European Journal of Mass Spectrometry. 19 (6), 463-473 (2013).
- Choi, D., et al. Redox activity and multiple copper(I) coordination of 2His-2Cys oligopeptide. Journal of Mass Spectrometry. 50 (2), 316-325 (2015).
- Vytla, Y., Angel, L. A. Applying ion mobility-mass spectrometry techniques for explicitly identifying the products of Cu(II) reactions of 2His-2Cys motif peptides. Analytical Chemistry. 88 (22), 10925-10932 (2016).
- Yousef, E. N., et al. Ion mobility-mass spectrometry techniques for determining the structure and mechanisms of metal ion recognition and redox activity of metal binding oligopeptides. Journal of Visualized Experiments. (151), e60102 (2019).
- Ilesanmi, A. B., Moore, T. C., Angel, L. A. pH dependent chelation study of Zn(II) and Ni(II) by a series of hexapeptides using electrospray ionization - Ion mobility - Mass spectrometry. International Journal of Mass Spectrometry. 455, 116369 (2020).
- Armentrout, P. B., Ervin, K. M., Rodgers, M. T. Statistical rate theory and kinetic energy-resolved ion chemistry: Theory and applications. Journal of Physical Chemistry A. 112 (41), 10071-10085 (2008).
- Dalleska, N. F., Honma, K., Sunderlin, L. S., Armentrout, P. B. Solvation of transition metal ions by water. Sequential binding energies of M+(H2O)x (x = 1-4) for M = Ti to Cu determined by collision-induced dissociation. Journal of the American Chemical Society. 116 (8), 3519-3528 (1994).
- Ervin, K. M., Armentrout, P. B. Translational energy dependence of Ar + XY → ArX+ + Y (XY = H2,D2,HD) from thermal to 30 eV c.m. Journal of Chemical Physics. 83, 166-189 (1985).
- DeTuri, V. F., Ervin, K. M. Competitive threshold collision-induced dissociation: Gas-phase acidities and bond dissociation energies for a series of alcohols. Journal of Physical Chemistry A. 103 (35), 6911-6920 (1999).
- Iceman, C., Armentrout, P. B. Collision-induced dissociation and theoretical studies of K+ complexes with ammonia: a test of theory for potassium ions. International Journal of Mass Spectrometry. 222 (1-3), 329-349 (2003).
- Rodgers, M. T., Ervin, K. M., Armentrout, P. B. Statistical modeling of collision-induced dissociation thresholds. Journal of Chemical Physics. 106, 4499-4508 (1997).
- Rodgers, M. T., Armentrout, P. B. Statistical modeling of competitive threshold collision-induced dissociation. Journal of Chemical Physics. 109, 1787-1800 (1998).
- Armentrout, P. B., Ervin, K. M. . CRUNCH, Fortran program, version 5.2002. , (2016).
- Pringle, S. D., et al. An investigation of the mobility separation of some peptide and protein ions using a new hybrid quadrupole/travelling wave IMS/oa-ToF instrument. International Journal of Mass Spectrometry. 261 (1), 1-12 (2007).
- Smith, D. P., et al. Deciphering drift time measurements from travelling wave ion mobility spectrometry-mass spectrometry studies. European Journal of Mass Spectrometry. 15 (2), 113-130 (2009).
- Forsythe, J. G., et al. Collision cross section calibrants for negative ion mode traveling wave ion mobility-mass spectrometry. Analyst. 140 (20), 6853-6861 (2015).
- Allen, S. J., Giles, K., Gilbert, T., Bush, M. F. Ion mobility mass spectrometry of peptide, protein, and protein complex ions using a radio-frequency confining drift cell. Analyst. 141 (3), 884-891 (2016).
- Salbo, R., et al. Traveling-wave ion mobility mass spectrometry of protein complexes: accurate calibrated collision cross-sections of human insulin oligomers. Rapid Communications in Mass Spectrometry. 26 (10), 1181-1193 (2012).
- Stewart, J. J. P. Optimization of parameters for semiempirical methods V: Modification of NDDO approximations and application to 70 elements. Journal of Molecular Modeling. 13, 1173 (2007).
- Frisch, M. J., et al. . Gaussian 09, Revision C.01. Wallingford CT: Gaussian, Inc. , (2012).
- Becke, A. D. Density-functional thermochemistry. III. The role of exact exchange. Journal of Chemical Physics. 98, 5648-5652 (1993).
- Wyttenbach, T., von Helden, G., Batka, J. J., Carlat, D., Bowers, M. T. Effect of the long-range potential on ion mobility measurements. Journal of the American Society of Mass Spectrometry. 8, 275-282 (1997).
- Shvartsburg, A. A., Jarrold, M. F. An exact hard-spheres scattering model for the mobilities of polyatomic ions. Chemical Physics Letters. 261 (1-2), 86-91 (1996).
- Heerdt, G., Zanotto, L., Souza, P. C. T., Araujo, G., Skaf, M. S. Collision cross section calculations using HPCCS. Methods in Molecular Biology. 2084, 297-310 (2020).
- Zanotto, L., Heerdt, G., Souza, P. C. T., Araujo, G., Skaf, M. S. High performance collision cross section calculation-HPCCS. Journal of Computational Chemistry. 39 (21), 1675-1681 (2018).
- . https://cccbdb.nist.gov/pollistx.asp Available from: https://cccbdb.nist.gov/pollistx.asp (2022)
- Raja, U. K. B., Injeti, S., Culver, T., McCabe, J. W., Angel, L. A. Probing the stability of insulin oligomers using electrospray ionization ion mobility mass spectrometry. European Journal of Mass Spectrometry. 21 (6), 759-774 (2015).
- Merenbloom, S. I., Flick, T. G., Williams, E. R. How hot are your ions in TWAVE ion mobility spectrometry. Journal of the American Society of Mass Spectrometry. 23 (3), 553-562 (2012).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados
Usamos cookies para melhorar sua experiência em nosso site.
Ao continuar usando nosso site ou clicando em 'continuar', você concorda em aceitar nossos cookies.
