Method Article
Thermochemische Untersuchungen von ni(II) und Zn(II) ternären Komplexen mittels Ionenmobilitäts-Massenspektrometrie
In diesem Artikel
Zusammenfassung
Dieser Artikel beschreibt ein experimentelles Protokoll unter Verwendung von Elektrospray-Ionen-Mobilitäts-Massenspektrometrie, semi-empirischen Quantenberechnungen und energieaufgelöster Schwellenkollisions-induzierter Dissoziation, um die relative Thermochemie der Dissoziation verwandter ternärer Metallkomplexe zu messen.
Zusammenfassung
Dieser Artikel beschreibt ein experimentelles Protokoll unter Verwendung der Elektrospray-Ionen-Mobilität-Massenspektrometrie (ES-IM-MS) und der energieaufgelösten Schwellenkollisions-induzierten Dissoziation (TCID) zur Messung der Thermochemie der Dissoziation von negativ geladenen [amb+M(II)+NTA]- ternären Komplexen in zwei Produktkanäle: [amb+M(II)] + NTA oder [NTA+M(II)]- + amb, wobei M = Zn oder Ni und NTA Nitrilotriessigsäure ist. Die Komplexe enthalten eines der alternativen metallbindenden (amb) Heptapeptide mit den Primärstrukturen Acetyl-His 1-Cys 2-Gly 3-Pro 4-Tyr 5-His 6-Cys 7 oder Acetyl-Asp 1-Cys 2-Gly3-Pro 4-Tyr 5-His 6-Cys 7, wobei die Aminosäuren Aa 1,2,6,7 Positionen sind die potenziellen Metallbindungsstellen. Geometrieoptimierte stationäre Zustände der ternären Komplexe und ihrer Produkte wurden aus quantenchemischen Berechnungen (derzeit der semi-empirische PM6-Hamiltonian) ausgewählt, indem ihre elektronischen Energien und ihre Kollisionsquerschnitte (CCS) mit denen von ES-IM-MS verglichen wurden. Aus den PM6-Frequenzberechnungen modellieren die molekularen Parameter des ternären Komplexes und seiner Produkte die energieabhängigen Intensitäten der beiden Produktkanäle mit einer kompetitiven TCID-Methode, um die Schwellenenergien der Reaktionen zu bestimmen, die sich auf die 0-K-Dissoziationsenthalpien (ΔH0) beziehen. Statistische mechanische thermische und Entropiekorrekturen unter Verwendung der PM6-Rotations- und Schwingungsfrequenzen liefern die 298 K-Dissoziationsenthalpien (ΔH298). Diese Methoden beschreiben eine EI-IM-MS-Routine, die Thermochemie und Gleichgewichtskonstanten für eine Reihe ternärer Metallionenkomplexe bestimmen kann.
Einleitung
Diese Studie beschreibt eine neue Technik unter Verwendung eines kommerziell erhältlichen Ionenmobilitätsmassenspektrometers, das die Bestimmung der relativen Thermochemie für die Dissoziation eines alternären Metallbindungskomplexes (amb+M(II)+NTA] ermöglicht, wobei M = Zn oder Ni und NTA = Nitrilotriessigsäure ist (Abbildung 1). Diese Reaktionen modellieren die Dissoziation des amb-markierten rekombinanten Proteins, das an das NTA-immobilisierte Metall während der immobilisierten Metallaffinitätschromatographie (IMAC) gebunden ist1,2. Als Beispiel wird diese Methode anhand der amb-Heptapeptid-Tags von amb A und H beschrieben (Abbildung 2) (ausgewählt aus den vorangegangenen Studien 3,4,5,6,7,8,9,10,11,12 ), die Zn(II)- und Ni(II)-bindende Eigenschaften aufweisen und daher potenzielle Anwendungen als Reinigungsmarken haben. Das beschriebene Verfahren kann jedoch verwendet werden, um thermochemische Energien in jedem metallorganischen System zu bewerten. Diese amb-Peptide haben Metallbindungsstellen in den Positionen Aa1-Aa 2 und Aa6-Aa 7, die mit den Carboxylat- und Aminstellen des NTA konkurrieren. Die drei zentralen amb-Aminosäuren bieten einen Spacer (Gly3), das Scharnier für die beiden Arme (Pro4) und eine Fern-π-Metall-Kationen-Wechselwirkung (Tyr5).
Der gesamte 1− Ladungszustand der [amb+M(II)+NTA]- Komplexe wird durch den Protonierungszustand ihrer potentiellen Bindungsstellen bestimmt. Da es Ni(II) oder Zn(II) mit der Oxidationsstufe 2+ gibt, muss es ein Netz von drei deprotonierten negativ geladenen Stellen geben. Die molekulare Modellierung der [amb+M(II)+NTA]- Komplexe sagt voraus, dass dies zwei Protonen aus dem NTA und ein Proton aus dem amb sind (d.h. [amb-H+M(II)+NTA-2H]-). Die Produktkanäle enthalten eine ionische Spezies und eine neutrale Spezies (d.h. [NTA-3H+M(II)]- + amb oder [amb-3H+M(II)]- + NTA). Im Manuskript wird "-3H" in den Namen der Komplexe ausgeschlossen, aber der Leser sollte wissen, dass das -3H impliziert ist. Das Instrument misst die relativen Intensitäten der beiden ionischen Masse-zu-Ladungs-Spezies (m/z). Ein wesentliches Merkmal von ES-IM-MS-Analysen ist, dass sie die Untersuchung der Reaktivität einer bestimmten m/z-Spezies ermöglichen, wie sie hier und in früheren amb-Studien 3,4,5,6,7,8,9,10,11,12 verwendet wurde.
Die Erfassung thermochemischer Daten für große Komplexe mittels kollisionsinduzierter Dissoziation ist ein Thema von erheblichem Interesse13,14. Methoden, einschließlich der kinetischen Methode, sind nicht förderlich für die Anpassung von Daten über einen Energiebereich, noch berücksichtigen sie Multikollisionsumgebungen15,16,17,18. Hier wird die Schwellen-CID-Methode (TCID), die unter Verwendung der geführten Ionenstrahl-Tandem-Massenspektrometrie von Armentrout, Ervin und Rodgers entwickelt wurde19 auf eine neue ES-IM-MS-Instrumentenplattform unter Verwendung von Wanderwellen-Ionenleitern angewendet. Die TCID-Methode ermöglicht die relative thermochemische Analyse der Dissoziation der ternären Komplexe in ihre beiden Produktkanäle und beinhaltet ein Schwellenwertgesetz, das die Übertragung der Kollisionsenergie zwischen der Translationsenergie des Reaktanten (ternärer Komplex in dieser Forschung) und einem inerten Zielgas (in diesem Fall Argon) beschreibt. Das Verfahren umfasst die Integration über die interne Energieverteilung 20 des Reaktanten, die translationalen Energieverteilungen zwischen dem Reaktanten und dem Zielgas21 und die Gesamtdrehimpulsverteilungen22,23. Eine Dissoziationswahrscheinlichkeit und statistische Rice-Ramsperger-Kassel-Marcus (RRKM)-Korrektur der kinetischen Verschiebungen, die sich aus dem begrenzten Zeitfenster zur Beobachtung der Produkte ergeben, sindenthalten 24. Für zwei unabhängige Produktkanäle ermöglicht das kompetitive TCID-Verfahren die gleichzeitige Anpassung der beiden konkurrierenden Produktkanäle. Die Dissoziation des Komplexes erfolgt durch einen umkreisenden Übergangszustand, der die Eigenschaften der Produkte aufweist, aber durch einen gesperrten Dipol25 zusammengehalten wird. Die TCID-Methode ist in das CRUNCH-Programm26 integriert, und die Funktionsweise der Benutzeroberfläche wird hier beschrieben, um die Thermochemie der beiden Dissoziationskanäle der ternären [amb+M(II)+NTA]-Komplexe zu bewerten. Das CRUNCH-Programm ist auf Anfrage bei den Entwicklern26 erhältlich.
Protokoll
HINWEIS: Abbildung 1 zeigt eine Übersicht über das Protokoll.
1. Herstellung von Reagenzien
- Kaufen Sie gefriergetrocknete AMB-Peptide (>98% Reinheit) und lagern Sie sie in einem Gefrierschrank von -80 °C.
- Kaufen Sie >99% Reinheit Zink(II)-nitrathexahydrat und Nickel(II)-nitrathexahydrat.
ACHTUNG: Nickel(II)-nitrathexahydrat stellt eine Gefahr für Umwelt und Gesundheit dar. - Kaufen Sie die Nitrilotriessigsäure, Poly-DL-Alanin-Polymere, Reinst-/Spurenmetall-Ammoniumacetat, Ammoniumhydroxid, Eisessig und HPLC-Acetonitril.
2. Vorbereitung von Stammlösungen
- Peptid-amb-Stammlösung
- Bereiten Sie eine wässrige Lösung mit einer Konzentration von 12,5 mM amb vor, indem Sie 10-20 mg des gefriergetrockneten Peptids unter Verwendung von nicht weniger als drei signifikanten Zahlen wiegen und in ein 1,7 ml Polypropylen-Mikrozentrifugenröhrchen geben.
- Geben Sie das entsprechende Volumen an entionisiertem Wasser (>17,8 MΩ cm) in das Mikrozentrifugenröhrchen. Schließen Sie den Deckel und mischen Sie ihn gut mit mindestens 20 Inversionen.
- Erstellen Sie 50 μL Aliquots aus der 12,5 mM amb Lösung und geben Sie sie in markierte 1,7 mL Mikrozentrifugenröhrchen. Lagern Sie die aliquoten Stammlösungen bei −80 °C.
- Metallionen-Stoff-Lösungen
- Die wässrigen Zn(II)- und Ni(II)-Lösungen mit einer Konzentration von 12,5 mM werden hergestellt, indem 10-30 mg des Metallnitrathexahydrats unter Verwendung von nicht weniger als drei signifikanten Zahlen gewogen und in ein 1,7-ml-Polypropylen-Mikrozentrifugenröhrchen gegeben werden.
- Geben Sie die entsprechende Menge DI-Wasser in das Mikrozentrifugenröhrchen. Schließen Sie den Deckel und mischen Sie ihn gut mit mindestens 20 Inversionen. Lagern Sie 50 μL aliquote Stammlösungen bei −80 °C.
- NTA-Ionenlagerlösungen
- Bereiten Sie eine wässrige NTA-Lösung vor, indem Sie 10-30 mg NTA unter Verwendung von nicht weniger als drei signifikanten Zahlen wiegen und in ein 1,7-ml-Mikrozentrifugenröhrchen geben.
- Geben Sie die entsprechende Menge DI-Wasser zum NTA im Mikrozentrifugenröhrchen, um eine Endkonzentration von 12,5 mM zu erreichen. Schließen Sie den Deckel und mischen Sie ihn gut mit mindestens 20 Inversionen. Lagern Sie 50 μL aliquote Stammlösungen bei −80 °C.
- Ammoniumacetat-Stammlösungen: Wiegen Sie 30,8 mg Ammoniumacetat und geben Sie 40 ml DI-Wasser hinzu, um eine 10 mM-Lösung zu erhalten. Stellen Sie den pH-Wert der Ammoniumacetatlösung mit 1 mM Ammoniumhydroxid auf pH 7,7 ein.
- Poly-DL-Alanin-Stammlösung: Stellen Sie eine 1 ml, 1.000 ppm Poly-DL-Alanin (PA) -Stammlösung her, indem Sie 1,0 mg PA in DI-Wasser auflösen. Umfassend mischen. Erstellen Sie 50 μL Aliquots und geben Sie sie in individuell beschriftete Mikrozentrifugenröhrchen. Lagern Sie die 1.000 ppm Lösung bei −80 °C.
3. Elektrospray-Ionen-Mobilitäts-Massenspektrometrie (ES-IM-MS) Kollisionsinduzierte Dissoziation (CID) Analyse
- Bereiten Sie das Gerät vor, indem Sie den ES-Einlassschlauch und die Metallkapillare reinigen, indem 500 μL 0,1 M Eisessig, gefolgt von 500 μL 0,1 M Ammoniumhydroxid und schließlich 500 μL pH 7,7-Ammoniumacetatlösung injiziert werden.
- Verflüssigen Sie die 12,5 mM amb Stammlösung, indem Sie sie auf Raumtemperatur bringen. Erzeugen Sie eine Endkonzentration von 0,125 mM amb durch zwei aufeinanderfolgende Verdünnungen mit DI-Wasser. Nach jeder Verdünnung umfassend mischen.
- Verflüssigen Sie die 12,5 mM Metallionen-Stammlösung, indem Sie sie auf Raumtemperatur bringen. Erzeugen Sie eine Endkonzentration von 0,125 mM Metallionen, indem Sie zwei aufeinanderfolgende Verdünnungen mit DI-Wasser durchführen. Nach jeder Verdünnung umfassend mischen.
- Verflüssigen Sie die 12,5 mM NTA-Stammlösung. Erzeugen Sie eine Endkonzentration von 0,125 mM NTA durch zwei aufeinanderfolgende Verdünnungen mit DI-Wasser. Nach jeder Verdünnung umfassend mischen.
- Um eine 2-ml-Probe des ternären Komplexes herzustellen, fügen Sie 800 μL 0,125 mM NTA-Lösung und 400 μL 0,125-Metallionenlösung zu einem 2-ml-Mikrozentrifugenröhrchen hinzu und mischen Sie gründlich mit mindestens 20 Inversionen. 400 μl Ammoniumacetatlösung (pH 7,7) und 400 μL 0,125 mM amb Lösung zugeben, gründlich mit mindestens 20 Inversionen mischen und die Probe 10 min bei Raumtemperatur ausgleichen lassen.
- Füllen Sie die 2-ml-Probe in eine 2,5-ml-Stumpfnasenspritze und injizieren Sie die Probe mit der Spritzenpumpe des Geräts bei einem Durchfluss von 10 μl/min in den ES des Geräts.
- Versetzen Sie das Gerät in den negativen IM-MS-Modus. Verwenden Sie die typischen Betriebsbedingungen des Instruments27 für diese Experimente wie folgt.
- Die Probe wird mit einer Durchflussrate von 10 μL/min in die ES-Kapillare bei −2 kV mit einer Desolvationsflussrate von Stickstoff von 500 l/h injiziert. Stellen Sie die ES-Quell- und Desolvationstemperaturen auf 130 °C bzw. 263 °C ein. Stellen Sie die Probenahme- und Extraktionskegel auf 25 V bzw. 3 V ein.
- Für die CID-Experimente verwenden Sie den Quadrupol-Massenanalysator, um das Isotopenmuster des [amb+M(II)+NTA]- ternären Komplexes unter Verwendung von m/z des monoisotopischen Peaks mit Auflösungseinstellungen von niedriger Masse = 4,5 und hoher Masse = 16,5 auszuwählen.
HINWEIS: Die [amb+M(II)+NTA]- Ionen werden an die sequentiellen drei Wanderwellen-Ionenführer (T-Welle ) weitergeleitet. - Stellen Sie sicher, dass die T-Welle der Falle einen Argongasfluss von 3 ml/min und einen Druck von 2,83 x 10-2 mbar aufweist. Stellen Sie die Kollisionsenergie (CE) auf die Falle auf 5 V ein, um eine Dissoziation des ternären Komplexes zu vermeiden. Lassen Sie die Falle die ternären Komplexionen sammeln, bevor sie (200 μs Freisetzungszeit) in den T-Wellen-Ionenführer der Ionenmobilität (IM) freigesetzt werden, wobei eine Fallen-DC-Vorspannung von 14 V verwendet wird, wodurch die Dissoziation des Komplexes am IM-Eingang auf ein Minimum reduziert wird.
- Stellen Sie sicher, dass der IM-Ionenführer einen Druck von 0,507 mbar unter Verwendung einer Durchflussrate von 20 ml/min hochreinemN2-Puffergas hat. Rampen Sie die T-Wellen im IM mit Höhen von 7 V bis 30 V und mit Geschwindigkeiten von 290 m/s bis 801 m/s für jeden Start- und Endschwung des IM-Ionenführers.
- Stellen Sie den Argonfluss und -druck der Transfer-T-Welle genauso ein wie die Trap-T-Welle. Die Transfer-T-Welle wurde für die kollisionsinduzierte Dissoziation des ternären [amb+M(II)+NTA]-Komplexes unter Verwendung des Transfer-CE verwendet.
- Wählen Sie das m/ z-Isotopenmuster des negativ geladenen [amb+M(II)+NTA]- Komplexes mit dem Transmissionsquadrupol im Auflösungsmodus.
- Identifizieren Sie das m/z-Isotopenmuster , indem Sie das Massenspektrometrieprogramm öffnen und Spektrum auswählen. Wählen Sie Werkzeuge > Isotopenmodell. Listen Sie im Popup-Fenster die Summenformel des Komplexes auf, aktivieren Sie das Kontrollkästchen Geladenes Ion anzeigen, geben Sie 1 für die Ladung des negativen Ions ein und klicken Sie auf OK.
- Beachten Sie im angezeigten Isotopenmuster des Komplexes den niedrigsten Massenpeak. Wählen Sie in der Gerätesoftware Setup > Quad Profile aus. Wählen Sie im sich öffnenden Fenster Manual Fixed und geben Sie die Masse des niedrigsten Isotopenmusterpeaks ein. Klicken Sie auf Aktualisieren und dann auf Schließen.
- Wählen Sie erneut Setup und klicken Sie dann auf Resolving Quad. Erfassen Sie die negativen Ionen-ES-IM-MS-Spektren inkrementell über einen Bereich von Transferkollisionsenergien mit einer Laufzeit von 5 Minuten und einer Scanzeit von 2 s.
HINWEIS: Vorläufige Übertragungsenergien können von 26-60 V in Intervallen von 2 V getestet werden. Der endgültige Bereich der untersuchten Transferkollisionsenergien sollte keine Dissoziation des ternären Komplexes bei der niedrigsten Energie und eine vollständige Dissoziation in die Produkte bei der höchsten Energie zeigen. Für eine qualitativ hochwertige statistische Analyse sollte diese ES-IM-MS-Analyse für jeden amb ternären Komplex mindestens 3x von verschiedenen Personen und an verschiedenen Tagen durchgeführt werden, um Mittelwerte und Standardabweichungen zu bestimmen.
4. ES-IM-MS-Kollisionsquerschnittsanalyse (CCS)
- Reinigen Sie den ES-Einlassschlauch und die Metallkapillare mit 500 μL 0,1 M Eisessig, gefolgt von 500 μL 0,1 M Ammoniumhydroxid und schließlich 500 μL pH 7,7 Ammoniumacetatlösung.
- Verflüssigen Sie die 1.000 ppm PA-Stammlösung auf Raumtemperatur und führen Sie zwei serielle Verdünnungen durch. Mit DI-Wasser auf 100 ppm PA verdünnt und anschließend mit einem Verhältnis von 1:1 aus DI-Wasser und HPLC-Acetonitril auf 10 ppm PA-Lösung verdünnt.
- Sammeln Sie die negativen Ionen-IM-MS-Spektren der 10-ppm-PA-Probe für 10 Minuten unter instrumentellen Betriebsbedingungen.
ANMERKUNG: Die Einspritzflussrate und die ES-Quellbedingungen waren die gleichen wie bei den CID-Experimenten (Schritt 3). Für Messungen des CCS befand sich der Quadrupol-Massenanalysator im Non-Resolvenz-Modus und leitete alle Ionen an die sequentiellen drei T-Wellen-Ionenleiter. Die Funktionsweise der T-Wellen- und IM-T-Wellen-Ionenleiter war die gleiche wie bei den CID-Experimenten. Die Kollisionsenergie der Transfer-T-Wellenzelle lag bei 4 V, damit Ionen ohne Dissoziation passieren konnten. - Bereiten Sie jeden der ternären Komplexe wie in den Schritten 3.2.-3.6 beschrieben vor.
- Sammeln Sie die IM-MS-Spektren jedes ternären Komplexes für 5 min.
HINWEIS: Verwenden Sie die gleichen instrumentellen Bedingungen wie in Schritt 4.3. - Sammeln Sie die negativen Ionen-IM-MS-Spektren der 10 ppm PA-Probe für 10 min.
ANMERKUNG: Der Mittelwert der Ankunftszeiten der PA-Kaliber, die vor und nach den ternären AMB-Komplexen gesammelt wurden, wird bei der CCS-Bestimmung verwendet.
5. Analyse von ES-IM-MS CID-Daten
- Identifizieren Sie die Spezies, indem Sie die theoretischen m/ z-Isotopenmuster des ternären Komplexes und seiner Produkte mit den experimentellen IM-MS-Spektren abgleichen.
- Öffnen Sie das Massenspektrometrie-Programm und wählen Sie Chromatogramm , um ein neues Fenster zu öffnen.
- Klicken Sie im Fenster Chromatogramm auf Datei > Öffnen , um die gewünschte IM-MS-Datendatei zu suchen und zu öffnen.
- Klicken Sie mit der rechten Maustaste, ziehen Sie es über das Chromatogramm, und lassen Sie es los. Das MS-Spektrum wird in einem separaten Spectrum-Fenster angezeigt.
- Wählen Sie im neuen Fenster, in dem die Spektren angezeigt werden, Extras > Isotopenmodell. Es öffnet sich ein kleines Fenster. Geben Sie die Summenformel der amb-Spezies ein, aktivieren Sie das Kontrollkästchen Geladene Ionen anzeigen und geben Sie den gewünschten Ladungszustand ein. Klicken Sie auf OK.
- Um alle Arten im IM-MS-Spektrum zu unterscheiden, wiederholen Sie diesen Vorgang im Spektrumfenster und notieren Sie ihren m/z-Isotopenbereich .
- Verwenden Sie für den ternären AMB-Komplex und seine Produkte ihren m/ z-Isotopenbereich, um sie zu identifizieren und ihre Ankunftszeitverteilungen (ATD) zu extrahieren.
- Öffnen Sie die Software zur Ionenmobilitätstrennung und wählen Sie Datei > Öffnen , um die Datendatei zu suchen und zu öffnen.
- Klicken Sie mit der linken Maus und ziehen Sie mit der Maus, um den m/z-Isotopenbereich des ternären Komplexes [amb+M(II)+NTA]- zu vergrößern.
- Klicken Sie mit dem Auswahlwerkzeug mit der linken Maustaste und ziehen Sie, um den spezifischen Isotopenbereich für [amb+M(II)+NTA] auszuwählen , wie in Schritt 5.1 beschrieben. Klicken Sie auf die Schaltfläche Aktuelle Auswahl akzeptieren .
- Um zufällige m/z-Spezies oder Hintergrundsignale zu eliminieren, verwenden Sie das Auswahlwerkzeug , um die ATD auszuwählen, die dem ternären Komplex zugeordnet ist. Klicken Sie auf die Schaltfläche Aktuelle Auswahl akzeptieren .
- Um die ATD-Datei in die Massenspektrometrie-Software zu exportieren, gehen Sie zu Datei > Export und klicken Sie dann auf Driftzeit beibehalten. Benennen Sie die Datei bei Bedarf um und speichern Sie die Datei im entsprechenden Ordner.
- Bestimmen Sie durch Integration der Fläche unter der extrahierten ATD-Kurve die relative Intensität der Art.
- Öffnen Sie im Fenster Chromatogramm die gespeicherte exportierte Datei aus der Software zur Ionenmobilitätstrennung. Wählen Sie Prozess und dann Integrieren aus. Verwenden Sie eine Spitze-zu-Spitze-Amplitudeneinstellung von 20 und klicken Sie auf OK.
- Notieren Sie den integrierten Bereich, wie im Chromatogrammfenster angezeigt. Wiederholen Sie die Schritte 5.2.2.-5.2.5. für die beiden Produkte [NTA+M(II)]- und [amb+M(II)]-.
- Wiederholen Sie die Schritte 5.2.1.-5.3.2. für jede übertragene Kollisionsenergie aufgezeichnet.
- Verwenden Sie die integrierten ATD-Bereiche für den ternären Komplex [amb+M(II)+NTA]- und zwei Produkte [NTA+M(II)]- und [amb+M(II)]- an jedem Transferkollisionsenergiepunkt, um auf eine relative Prozentskala zu normalisieren.
- Erstellen Sie eine Tabelle, indem Sie die Identitäten des ternären Komplexes und seiner Produkte sowie deren integrierte ATD bei jeder Kollisionsenergie eingeben.
- Verwenden Sie für jede Kollisionsenergie die Summe der integrierten ATDs für [amb+M(II)+NTA]-, [NTA+M(II)]- und [amb+M(II)]-, um ihre einzelnen ATDs auf eine relative Prozentskala zu normalisieren.
- Ermitteln Sie anhand der replizierten TCID-Messungen den Mittelwert und die Standardabweichungen jedes Datenpunktes. Umrechnung der Labor-Rahmen-Transferkollisionsenergie (E-Labor) in die Kollisionsenergie des Massenschwerpunkts (E cm) unter Verwendung der mittleren Massen des Argon-Kollisionsgases (m Ar) und des ternären Komplexes (m-Komplex): E cm = Elab (m Ar)/(m Ar + m-Komplex).
HINWEIS: Ecm stellt die maximale Energie aus der Kollision mit dem Argongas dar, die für die Dissoziation des ternären Komplexes zur Verfügung steht. - Zeichnen Sie den Mittelwert und die Standardabweichung der einzelnen prozentualen Intensitäten von [amb+M(II)+NTA]-, [NTA+M(II)]- und [amb+M(II)]- in einem Diagramm der relativen Intensität (%) vs. der Kollisionsenergie (eV) des Massenschwerpunkts auf, um zu zeigen, wie sich die relativen Intensitäten der Spezies als Funktion der Kollisionsenergie ändern.
6. Analyse der durchschnittlichen Ankunftszeiten zur Ermittlung von Kollisionsquerschnitten (CCS)
- Öffnen Sie die Ionenmobilitätstrennungssoftware und die Datei mit dem IM-MS-Spektrum der 10 ppm PA-Probe, die mit der auf 4 V eingestellten Transferkollisionsenergie gesammelt wurde. Extrahieren Sie die ATD jeder der einzelnen negativ geladenen PA-Spezies und exportieren Sie die Dateien mit der Option Driftzeit beibehalten in die Massenspektrometrie-Software (siehe Schritt 5.2.5.). Wiederholen Sie diesen Vorgang für die zweite PA-Kaliberdatei.
- Öffnen Sie die Software zur Ionenmobilitätstrennung. Verwenden Sie Datei > Öffnen , um eine der Dateien zu öffnen, die die IM-MS-Spektren der tantären amb-Komplexe enthalten, die zwischen den PA-Kalibern aufgezeichnet wurden. Extrahieren Sie die ATD jedes der ternären Komplexe und exportieren Sie ihre Dateien in die Massenspektrometrie-Software mit der Option Driftzeit beibehalten (siehe Schritt 5.2.5.).
- Verwenden Sie eine Querschnittskalibriermethode28 , um das CCS des ternären Komplexes und seiner Produkte zu berechnen.
- Berechnen Sie in einer Tabelle das korrigierte CCS (Ω c) für jede der einzelnen negativ geladenen PA-Spezies aus ihrem CCS (Ω)29,30, gemessen in Heliumpuffergas31 unter Verwendung von Gleichung 1, wobei z = Ladung des ternären Komplexes, ec = 1,602 x 10−19 C; mN2 = Masse des Stickstoffs (u) und mIon = Masse des ternären Komplexes28.
 (1)
(1) - Finden Sie die Driftzeiten (tD) der PA-Kaliber und der ternären Komplexe, indem Sie zuerst die durchschnittlichen Ankunftszeiten (tA) aus den Maxima der entsprechenden ATD-Kurven erhalten und dann Gleichung 2 anwenden, wobei c = Detektorverzögerungskoeffizient (1,41 ms; Instrument überprüfen, da dies zwischen Instrumenten variieren kann) und m / z = Masse-zu-Ladungs-Verhältnis des PA-Kalibers oder des tantären amb-Komplexes.
tD =tA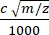 (2)
(2) - Erstellen Sie ein Diagramm, indem Sie die PA-Kaliber tD vs. Ωc darstellen. Passen Sie dann mithilfe von Gleichung 3 die Daten mit einer Regression der kleinsten Quadrate an, um die Konstanten A' und B zu finden, wobei A' das elektrische Feld, die Temperatur und den Druck im Instrument korrigiert und B das nichtlineare Verhalten des T-Wellen-IM-Geräts korrigiert.
Ωc = A' tDB (3) - Unter Verwendung der A'- und B-Konstanten und des tD-Werts der amb-ternären Komplexe berechnen Sie ihre Ωc mit Gleichung 3 und ihre Ω mit Gleichung 1. Die nach dieser Methode geschätzten CCS-Werte weisen absolute Fehler von etwa 2 % auf29.
- Berechnen Sie in einer Tabelle das korrigierte CCS (Ω c) für jede der einzelnen negativ geladenen PA-Spezies aus ihrem CCS (Ω)29,30, gemessen in Heliumpuffergas31 unter Verwendung von Gleichung 1, wobei z = Ladung des ternären Komplexes, ec = 1,602 x 10−19 C; mN2 = Masse des Stickstoffs (u) und mIon = Masse des ternären Komplexes28.
7. Berechnungsmethoden
- Verwenden Sie die semi-empirische PM632-Methode, die in Strukturmodellierungs- und Computersoftware33 implementiert ist, um geometrieoptimierte Konformere der [amb+M(II)+NTA]- ternären Komplexe und der Ionen- und neutralen Produktpaare [amb+M(II)]- + NTA und [NTA+M(II)]- + amb aus den CID-Experimenten zu lokalisieren. Einzelheiten zum Entwickeln und Senden von Berechnungen finden Sie in der Verwendung der Berechnungsschnellansicht in der Zusatzdatei.
HINWEIS: Für die vorliegenden Systeme hat die PM6-Methode experimentelle Daten korrekt reproduziert, aber im Allgemeinen kann jede quantenchemische Methode verwendet werden, die zuverlässig und rechnerisch machbar ist. - Führen Sie Geometrieoptimierungen und Frequenzberechnungen für mehrere verschiedene Ausgangsstrukturen durch, um verschiedene Konformationen, Protonierungszustände und potenzielle Bindungsstellen zu untersuchen. Zeichnen Sie die elektronischen + Nullpunktenergien jedes der stationären Punkte für jeden der ternären Komplexe und ihre Produkte auf.
HINWEIS: Die Ausgangsstrukturen für die Geometrieoptimierungen sollten verschiedene mögliche Kombinationen von Bindungsstellen und Konformationsanordnungen untersuchen. Die Ausgangsstrukturen basierten auf den zuvor lokalisierten B3LYP34 [amb+M(II)]- konformen 3,4,6. Für [amb+M(II)+NTA]- war NTA so positioniert, dass es mit den Substituenten des amb am Aa1-Aa 2-Aa 6-Aa 7 und dem Carboxylatterminus für den Singulett-Spinzustand von Zn(II) oder den Triplett-Spinzustand von Ni(II) konkurrierte. - Verwenden Sie ein Programm, das genaue Kollisionsquerschnittsmessungen durchführen kann, gemessen in Heliumpuffergas (CCSHe) unter Verwendung der Atomkoordinaten aus diesen quantenchemischen Berechnungen35.
HINWEIS: Programme, die zur Berechnung genauer CCSHe aus Peptidstrukturen entwickelt wurden, die durch quantenchemische Berechnungen lokalisiert werden, umfassen MobCal 36 und HPCCS37,38. - Wählen Sie den niedrigsten Energiekonformer mit dem Lennard-Jones CCS He, der mit dem IM-MS-gemessenen CCSHe übereinstimmt, um die Strukturen ternärer Komplexe und Dissoziationsprodukte auszuwählen, die in die CRUNCH-Modellierung unten aufgenommen werden sollen.
8. CRUNCH-Modellierung
- Erstellen Sie eine Textdatei in dem im Diskussionsabschnitt beschriebenen Format ("CRUNCH-Eingabetextdateiformat").
HINWEIS: Die Datei enthält die folgenden Spalten: (−1) Massenschwerpunkt-Kollisionsenergie (Ecm), (1) Mittelwert der relativen Intensität des [amb+M(II)]- Produkts, (2) Standardabweichung der [amb+M(II)]- Intensität, (3) Mittelwert der relativen Intensität des [NTA+M(II)]- Produkts und (4) Standardabweichung der [NTA+M(II)]- Intensität. - Modellieren Sie die EZentimeter-abhängige Intensitäten der beiden Reaktionskanäle [amb+M(II)+NTA]-bis [amb+M(II)]- + NTA und [amb+M(II)+NTA]- bis [NTA+M(II)]- + amb mit der TCID-Technik im CRUNCH-Programm.
HINWEIS: Verwenden Sie die PM6-Schwingungs- und Rotationsfrequenzen für den ternären Komplex und die beiden Ionen- und neutralen Produktkanäle. Verwenden Sie die durchschnittlichen Massen des ternären Komplexes, des Argon-Kollisionsgases sowie der Ionen- und Neutralprodukte. Verwenden Sie Werte aus den PM6-Berechnungen oder der NIST-Datenbank für die Polarisierbarkeiten (Å3) und Dipolmomente (Debye) für die neutralen Produkte.- Öffnen Sie im Hauptmenü CRUNCH die Textdatei (. GB5) mit den Ecm-abhängigen relativen Intensitäten der Produkte. Antworten Sie mit Nein , um Parameter zu lesen.
- Wählen Sie im Hauptmenü CRUNCH die Option Modellierung > Alle Parameter festlegen. Wählen Sie aus den Reaktionsmodelloptionen die Standardoption Threshold CID , gefolgt von RRKM mit Integration über die Energieübertragungsverteilung des ternären Komplexes20, geben Sie 2 für die modellierten unabhängigen Produktkanäle ein und wählen Sie Querschnitte berechnen. Geben Sie Nein ein, um Haben zwei beliebige Produktkanäle die gleiche Ionenmasse?
- Geben Sie für Produktkanal # 1 Spalte [1] für die experimentellen Daten des [amb+M(II)]- Produkts, Spalte [2] für die Standardabweichungen des [amb+M(II)]- Produkts, Spalte [5] für den ungewundenen Modellquerschnitt und Spalte [6] für den gewundenen Modellquerschnitt ein. Geben Sie 0 für Anpassungsreste ein.
Hinweis: Diese Spaltennummern entsprechen den Spalten in der Eingabedatei in Schritt 8.1. wie in der Diskussion beschrieben ("CRUNCH-Eingabetextdateiformat"). - Geben Sie für Produktkanal # 2 Spalte [3] für die experimentellen Daten des [NTA+M(II)]- Produkts, Spalte [4] für die Standardabweichungen des [NTA+M(II)]-Produkts, Spalte [7] für den unverworrenen Modellquerschnitt und Spalte [8] für den gewundenen Modellquerschnitt ein. Geben Sie 0 für Anpassungsreste ein.
- Für den Typ des unverworrenen Modells wählen Sie 0 K Querschnitt (einschließlich kinetischer Verschiebung), der die statistische RRKM-Korrektur der kinetischen Verschiebungen aufgrund des 50 μs Zeitfensters von der Kollisionszelle zum TOF-Detektor18 beinhaltet.
- Für die Faltungsoptionen wählen Sie das Doppelintegral von Tiernan, das die Faltung über translationale Energieverteilungen zwischen dem ternären Komplexion und dem Argon-Kollisionsgas21 umfasst.
- Wählen Sie für die numerische Integrationsmethode die Gaußquadratur mit vorgespeicherten Querschnitten, gefolgt von der Anzahl der Integrationspunkte = 32, der Anzahl der Standardabweichungen = 3,0 und der Anzahl der Standardabweichungen für das zweite Integral = 3,0.
- Die Masse des ternären Komplexions (u) wird automatisch aus dem gelesen. GB5-Textdatei, gefolgt von der Masse des Kollisionsgases (39,948 für Argon); Verwenden Sie die Standardwerte von 0,20 eV für die FWHM des Ionenstrahls und 298,15 K für die Gastemperatur. Das Programm liest automatisch die minimalen und maximalen Schwerpunktkollisionsenergien aus dem ein. GB5-Textdatei; Verwenden Sie den Standardwert für das minimale Energieinkrement.
- Verwenden Sie den Standardwert für den Skalierungsfaktor Sig0, Nein für die Skalierung einzelner Produktkanäle und die Standardwerte für N und M. Für die Methode für die g(i)-Berechnung wählen Sie integrate over ro-Schwingungsdichte von Zuständen, die die interne Energieverteilung20 des ternären Komplexes [amb+M(II)+NTA]- umfasst.
- Geben Sie aus den Optionen zur Eingabe der molekularen Parameter G ein, um die Strukturmodellierungsdatei33 mit den PM6-Schwingungs- und Rotationsfrequenzen des ternären Komplexes zu lesen. Antwort Ja auf die Frage ist einer der Reaktanten atomar? Schreiben Sie den Speicherort und den Namen der Modellierungsdatei.
HINWEIS: Die anderen Optionen für die Eingabe der Schwingungs- und Rotationsfrequenzen umfassen die Leseparameterdatei, die die Parameter aus einer Textdatei einliest, oder das Bearbeiten/Eingeben von Konstanten, die die manuelle Eingabe jedes Parameters ermöglichen. - Skalieren Sie die Frequenzen mit dem vom NIST empfohlenen PM6-Skalierungsfaktor (1,062). Weitere Details zur Skalierung finden Sie in der Diskussion ("Skalierungsfaktoren für die Schwingungsfrequenzen"). Die Anzahl der Atome im ternären Komplex wird aus der Datei gelesen. Antwort Nein zu Ist das Molekül linear? Geben Sie die Beschreibung der Reaktanten ein (z.B. H+Zn+NTA- + Ar).
- Geben Sie 1 für die Ladung am Ion und 1,664 für die Polarisierbarkeit des Argongases39 ein. Die Masse des Ions und die Masse des Ziels sind für den ternären Komplex bzw. Argon und werden automatisch aus dem gelesen. GB5-Textdatei. Geben Sie 0 für harmonische Schwingungen ein.
HINWEIS: Die folgenden Optionen dienen zur Auswahl verschiedener Skalierungsfaktoren für hohe oder niedrige Schwingungsfrequenzen. Geben Sie 1,062 für hohe Frequenzen und 0,0 für niedrige Frequenzen ein (siehe Diskussion: Skalierungsfaktoren für die Schwingungsfrequenzen). Die skalierten Frequenzen werden angezeigt. Wählen Sie 0, um Keine Änderung auszuwählen. - Drücken Sie die Eingabetaste, um die 1D- und 2D-Rotationskonstanten aus der in Schritt 8.2.10 eingegebenen Strukturmodellierungsdatei33 zu lesen. Wählen Sie die Standardwerte 0 für die behinderten Rotorbehandlungen und 1 für die Molekülsymmetrie.
HINWEIS: Das Programm zeigt die eingegebenen Daten an; Drücken Sie die Eingabetaste für Keine Änderungen. - Wählen Sie den Standardwert von 300 K für die Reaktantentemperatur. Wählen Sie Integration für die Methode zur Reduzierung der Zustandsdichte aus. Wählen Sie Ja, um die Energieverteilung zu kürzen. Geben Sie 40000 cm−1 für die maximale Energie für die Verteilung, 2,0 cm−1 für die Behältergröße und 32 für die Anzahl der Punkte in der Energieverteilung ein.
HINWEIS: Drücken Sie 2x die Eingabetaste und überprüfen Sie, ob das abgeschnittene 32-pt-Array eine Population >0,9 hat. Geben Sie bei >0,9 Nein ein, um die Behälter oder den Kondensationsfaktor zu wechseln. Wenn <0,9, geben Sie Ja ein, und ändern Sie die maximale Energie für die Verteilung und/oder die Lagerplatzgröße. - Wählen Sie für Parameter für das TCID/RRKM-Modell Yes (Ja) für Change (Ja) aus, geben Sie 0 für die feste Zeit und 0,000050 s für die obere Grenze des Erkennungsfensters ein. Für das verwendete Instrument ist dies die Zeit, die Ionen benötigen, um von der Transferkollisionszelle zum TOF-Detektor zu gelangen, und wird anhand von Gleichung 2 berechnet.
- Geben Sie für energetisiertes Molekül C ein, um Werte aus den bereits eingegebenen Reaktanten zu kopieren . Geben Sie −1 für den Quellübergangsstatus (TS), 0 für Ziel-TS und P ein, um fortzufahren.
- Wählen Sie für Produktkanal 1 1 für den einzelnen Übergangszustand aus den Dissoziationskanaloptionen und 0 für keine für die sequenzielle Dissoziation. Wählen Sie als Übergangszustandstyp 1 für die Umkreisung aus.
- Wählen Sie G , um die Modellierungsprogrammdateien zu lesen, die die PM6-Rotations- und Schwingungsparameter für die [amb+M(II)]- + NTA-Produkte enthalten. Geben Sie Nein ein, denn ist eine der PSL TS-Arten atomar? Geben Sie den Speicherort und den Namen der [amb+M(II)]- Datei ein. Verwenden Sie 1,062 für Skalenfrequenzen, drücken Sie die Eingabetaste für die Anzahl der Atome und geben Sie Nein ein, wenn das Molekül linear ist?
- Geben Sie den Speicherort und den Namen der Modellierungsdatei ein, die die Schwingungs- und Rotationsfrequenzen für das NTA-Produkt enthält. Verwenden Sie 1,062 für Skalenfrequenzen, drücken Sie die Eingabetaste für die Anzahl der Atome und geben Sie Nein ein, wenn das Molekül linear ist? Geben Sie die Beschreibung des umkreisenden TS ein, z. B. H+Zn-... NTA.
- Geben Sie 1 für die Ladung von [amb+M(II)]-Ion ein und geben Sie die Polarisierbarkeit (16,12 Å3) und das Dipolmoment (4,6183 Debye) von NTA ein. Wählen Sie 0 K für die Rotationstemperatur und den gesperrten Dipol für die Behandlung des umkreisenden Übergangszustands. Geben Sie die mittleren Massen (u) des [amb+M(II)]- Ions und NTA ein.
- Geben Sie 0 für harmonische Schwingungen ein. Geben Sie 1,062 für hohe Frequenzen und 0,0 für niedrige Frequenzen ein. Siehe den Diskussionsabschnitt für weitere Details zur Skalierung von Frequenzen; Die skalierten Frequenzen werden angezeigt. Wählen Sie 0, um Keine Änderung auszuwählen. Drücken Sie die Eingabetaste, um die 1-D- und 2-D-Rotationskonstanten aus den Modellierungsdateien zu lesen. Wählen Sie 0 für behinderte Rotoren, 1 für Molekülsymmetrie und 1 für Reaktionsdegeneration. Geben Sie die Option Keine Änderungen ein.
- Wählen Sie für Produktkanal 2 1 für den einzelnen Übergangszustand, 0 für keinen für die sequenzielle Dissoziation und 1 für die Umkreisung für den Übergangszustandstyp aus.
- Wählen Sie G , um Modellierungsdateien einzulesen, die die PM6-Rotations- und Schwingungsparameter für die [NTA+M(II)]- und amb-Produkte enthalten. Geben Sie Nein ein, denn ist eine der PSL TS-Arten atomar? Schreiben Sie den Speicherort und den Namen der [NTA+M(II)]- Modellierungsdatei.
- Verwenden Sie 1,062 für Skalenfrequenzen, drücken Sie die Eingabetaste, um die Anzahl der Atome zu lesen, und geben Sie N für ist das Molekül linear? Schreiben Sie den Speicherort und den Namen der amb-Modellierungsdatei. Verwenden Sie 1,062 für Skalenfrequenzen, drücken Sie Enter für die Anzahl der Atome und geben Sie N für ist das Molekül linear?
- Geben Sie die Beschreibung des umkreisenden TS ein (z. B. NTA+Zn-... H). Geben Sie 1,0 für die Ladung von [NTA+M(II)]- Ion ein und geben Sie die Polarisierbarkeit (Å3) und das Dipolmoment (Debye) des amb ein. Wählen Sie 0,0 K für die Rotationstemperatur und den gesperrten Dipol für die Behandlung des umkreisenden Übergangszustands. Geben Sie die durchschnittlichen Massen (u) der [NTA+M(II)]- und amb-Produkte ein.
HINWEIS: Die Ausgabedatei enthält die Polarisierbarkeit und Dipolmomente des amb. Die Polarisierbarkeit ist in Einheiten von Bohr 3 angegeben und muss in die Einheiten von Å3 umgerechnet werden. - Geben Sie 0 für harmonische Schwingungen ein. Geben Sie 1,062 für hohe Frequenzen und 0 für niedrige Frequenzen ein. Weitere Informationen zum Skalieren von Frequenzen finden Sie in der Diskussion. Die skalierten Frequenzen werden angezeigt. Wählen Sie 0, um Keine Änderung auszuwählen. Drücken Sie die Eingabetaste, um die 1-D- und 2-D-Rotationskonstanten aus den Modellierungsdateien zu lesen. Wählen Sie 0 für behinderte Rotoren, 1 für Molekülsymmetrie und 1 für Reaktionsdegeneration. Geben Sie Keine Änderungen ein.
- Um inaktive 2D-Rotationen zu verarbeiten, wählen Sie die Standardoptionen Statistische Drehimpulsverteilung und integrieren Sie die Verteilung von P(E,J) über J. Verwenden Sie den Standardwert von 32 für die Anzahl der Punkte in der Integration.
HINWEIS: Diese Auswahlen wählen die Methode für die Integration über den Gesamtdrehimpuls J Ebenen16,17. Die resultierende Ausgabe ermöglicht es dem Ermittler zu überprüfen, ob alle Eingaben korrekt sind. - Wählen Sie die Aktivierungsenergien relativ zur Option des energetisierten Moleküls und geben Sie die relative Energie (eV) für Produktkanal 1 ein, die nahe an der Schwellenenergie liegt, die in der Grafik der relativen Intensität vs. der Kollisionsenergie des [amb+M(II)]- Produkts beobachtet wird (Abbildung 4).
- Geben Sie für Produktkanal 2 die relative Energie (eV) ein, die nahe an der Schwellenenergie liegt, die in der Grafik der Intensität vs. Massenschwerpunkt-Kollisionsenergie des [NTA+M(II)]- Produkts beobachtet wird. Um die Anzahl der Status für jeden Produktkanal zu berechnen, verwenden Sie eine Lagerplatzgröße von 2,0. Drücken Sie die Eingabetaste und dann die Nein-Eingabetaste , um fortzufahren.
- Wählen Sie im Menü Modell die Option Parameter optimieren, um Daten anzupassen, und geben Sie die minimale Energie bzw. die maximale Energie ein, um die Datenanpassung zu beginnen bzw. zu beenden.
HINWEIS: Verwenden Sie einen kleinen Energiebereich, der die Schwellenwerte beider Kanäle enthält. Weitere Details finden Sie in der Diskussion: Energiebereich für die Anpassung des ausgewählten TCID-Modells an die experimentellen Daten. - Wählen Sie -1 für Gewichtungsmodi experimentelle Standardabweichungen. Wählen Sie basierend auf den Daten eine minimale akzeptable Standardabweichung von typischerweise 0,01 bis 0,001 aus. Wählen Sie Nein für die optimierte Skalierung einzelner Kanäle und 0 für die Anzahl der Iterationen.
HINWEIS: Eine Alternative zur Verwendung von Standardabweichungen ist die statistische Option. - Verwenden Sie den Standardwert für den Konvergenzgrenzwert E0, und wählen Sie Nein aus, um einen beliebigen Parameter mit Barwert beizubehalten. Geben Sie 0,5 und 2,0 eV für den unteren und oberen Grenzwert ein, um Optimierungsfehler zu vermeiden, und wählen Sie die zentrale endliche Differenz für die abgeleitete Bewertungsmethode. Verwenden Sie den Standardwert für numerische Genauigkeit, und wählen Sie Nein aus, um die Ableitungsschrittgrößen zu ändern.
Hinweis: Eine alternative Methode besteht darin, Ja auszuwählen, um einen beliebigen Parameter mit dem aktuellen Wert beizubehalten. Diese Methode wird in der Diskussion näher beschrieben: Optimierung von Parametern. - Wählen Sie im Menü Optimierung die Option Optimierung beginnen. Das CRUNCH-Programm optimiert das ausgewählte TCID-Modell auf die experimentellen Daten.
HINWEIS: Wenn die Optimierung keine zufriedenstellenden Anpassungen findet, versuchen Sie im Menü "Änderungen ", den Energiebereich so zu ändern, dass nur die ersten Intensitäten abgedeckt werden, die von den Schwellenwerten ausgehen. Wenn eine angemessene Passform gefunden ist, erhöhen Sie den Energiebereich und passen Sie wieder. Andere Optionen, die helfen können, Anpassungen an die Daten zu finden, umfassen die Entscheidung, einen beliebigen Parameter mit Barwert in optimierten Parametern beizubehalten, und das Ändern von Gewichtungsoptionen in Gewichtungen. Informationen zu diesen Optionen finden Sie in der Diskussion. - Wenn ein Modell gefunden wird, das zu den Daten passt, drücken Sie die Eingabetaste, bis das Menü Modell angezeigt wird. Wenn nur ein Teil des Energiebereichs der experimentellen Daten mit dem TCID-Modell ausgestattet ist, wählen Sie Modell berechnen und konvolutieren , um die Modellanpassung auf alle experimentellen Kollisionsenergien zu erweitern.
- Wählen Sie im Menü Modell die Option Delta H und S bei T.
ANMERKUNG: Das unverworrene CRUNCH-Modell setzt die 0-K-Schwellenenergien in Beziehung zu den 0-K-Enthalpien (ΔH0) der Dissoziation des ternären Komplexes in die beiden unabhängigen Produktkanäle (Tabelle 2). Die 298 K-Enthalpien (ΔH 298) und Gibbs-freien Energien (ΔG298) der Dissoziation werden ebenfalls mit statistisch-mechanischen thermischen und Entropiekorrekturen unter Verwendung des Reaktanten abgeleitet und Produkte PM6 Rotations- und Schwingungsfrequenzen.
Ergebnisse
Die kompetitive kollisionsinduzierte Dissoziation der [amb+M(II)+NTA]- ternären Komplexe von A und H in [amb+M(II)]- + NTA oder [NTA+M(II)]- + amb ist in Abbildung 3 dargestellt. Die amb wird entweder als A oder H und M = Zn oder Ni angezeigt. Der [A+Zn(II)+NTA]- ternäre Komplex (Abbildung 3A) weist scheinbare Schwellenwerte von etwa 0,7 eV Kollisionsenergie (CE) auf, um [A+Zn(II)]- und etwa 0,9 eV zur Erzeugung von [NTA+Zn(II)]- zu erzeugen. Die Dissoziation des [A+Ni(II)+NTA]-Komplexes (Abbildung 3B) weist ähnliche Schwellenwerte (~1,1 eV) für die beiden [NTA+Ni(II)]- und [A+Ni(II)]- Produkte auf, wobei [NTA+Ni(II)]- auf 90% relative Intensität ansteigt, während die Intensitäten von [A+Ni(II)]- nicht über 18% steigen. Für den [H+Zn(II)+NTA]- ternären Komplex (Abbildung 3C) ist das Hauptprodukt [H+Zn(II)]- von einem Schwellenwert von etwa 0,6 eV auf etwa 85% relativer Intensität ansteigend, und bei Energien über 1,0 eV steigt der [NTA+Zn(II)]- auf etwa 30%. Es gibt auch einen Kanal für den Wasserverlust von [H-H2O+Zn(II)]-. Für [H+Ni(II)+NTA]- (Abbildung 3D) steigt die [H+Ni(II)]- von einem Schwellenwert von etwa 0,9 eV auf etwa 40% relative Intensität, während die [NTA+Ni(II)]- von ~1,0 eV auf etwa 80% steigt. In den Diagrammen ist der CE enthalten, bei dem der ternäre Komplex zu 50% dissoziiert ist. Die ternären Ni(II)-Komplexe benötigen 0,31-0,37 eV mehr CE als ihre ternären Zn(II)-Komplex-Gegenstücke, um 50% dissoziiert zu sein. Dies deutet darauf hin, dass die Ni(II)-Komplexe stabiler sind und einen höheren CE-Wert benötigen, um zu dissoziieren, was mit der TCID-Technik weiter untersucht wird.
Abbildung 4 zeigt die wettbewerbsfähige TCID-Methode, die die gleichzeitige Anpassung der beiden konkurrierenden Produktkanäle ermöglicht.
[amb+M(II)+NTA] → [amb+M(II)]- + NTA (1)
[amb+M(II)+NTA] → [NTA+M(II)]- + amb (2)
Die potentielle Energieoberfläche (PES) veranschaulicht den energetisierten ternären Komplex, der in die konkurrierenden Produktkanäle dissoziiert, und zeigt die PM6-geometrieoptimierte Spezies, die zur Modellierung der Dissoziation von [ambH+Zn(II)+NTA]- verwendet wurden. In der PES enthalten sind die Zustandsdichte des ternären Komplexes und die Summe der Zustände der Produkte. Die 0 K-Schwellenenergien E 1 und E2 entsprechen der 0 K-Enthalpieänderung für die Reaktionen 1 und 2.
Abbildung 5 zeigt die Strukturen der anderen drei geometrieoptimierten ternären Komplexe, die in dieser Studie verwendet wurden. Diese Spezies wurden aufgrund ihrer vorhergesagten elektronischen Energien und Nullpunktenergien und ihrer Übereinstimmung mit den IM-MS-gemessenen Kollisionsquerschnitten (CCSHe) ausgewählt. Tabelle 1 zeigt, dass es eine Übereinstimmung zwischen den ternären Komplexen LJ CCS He und dem experimentellen IM-MS CCSHe gibt, weil sie innerhalb ihrer gegenseitigen Unsicherheiten übereinstimmen. Die Konformationen von [amb+M(II)] und amb basierten auf den Ergebnissen unserer vorherigen DFT-Modellierung 3,4,5,6. Die molekularen Parameter dieser PM6-Konformere wurden in der TCID-Modellierung der energieaufgelösten Dissoziationen der ternären Komplexe verwendet, einschließlich ihrer Ro-Schwingungsfrequenzen zur Berechnung ihrer Dichte und Summe der Zustände.
Abbildung 6 zeigt, dass der gewundene CRUNCH-TCID-Schwellenwert zu den energieaufgelösten Produktintensitäten passt. Die gewundenen Anpassungen umfassen die verfügbaren Energie- und Drehimpulsverteilungen der [amb+M(II)+NTA]- + Ar-Reaktanten. Die unkonvolutierten Fits (nicht gezeigt) sagten die 0 K Änderung der Enthalpien (Δ H 0) für die Dissoziation des ternären Komplexes voraus, und Tabelle 2 zeigt die Δ H 0 und Δ H298 (kJ/mol) für die Reaktionen 1 und 2. Für die Dissoziation der ternären Zn(II)-Komplexe weisen sowohl A als auch H Δ H 0 für Reaktion 1 auf, die 31 kJ/mol bzw. 15 kJ/mol niedriger sind als die Δ H 0 für Reaktion 2, was darauf hinweist, dass sowohl A als auch H eine größere Zn(II)-Affinität aufweisen als die NTA. Der [A+Ni(II)+NTA]- ternäre Komplex weist ΔH0 = 146 bzw. 148 kJ/mol für die Reaktionen 1 und 2 auf, was darauf hindeutet, dass A und NTA ähnliche Affinitäten zu Ni(II) aufweisen. Die Dissoziation von [H+Ni(II)+NTA]- zeigt jedoch, dass ΔH0 für Reaktion 1 36 kJ/mol niedriger ist als für Reaktion 2, was darauf hindeutet, dass H eine größere Ni(II)-Affinität als NTA hat. Insgesamt weisen die [amb+Ni(II)+NTA]- Komplexe höhere Dissoziationsenthalpien auf als ihre [amb+Zn(II)+NTA]- Gegenstücke, mit Ausnahme von A, das in [NTA+Ni(II)]- dissoziiert. Tabelle 3 zeigt die freien Gibbs-Energien (ΔG298) der Assoziation und die Bildungskonstanten (K) für die Umkehrreaktionen:
[amb+M(II)] - + NTA → [amb+M(II)+NTA]- (3)
[NTA+M(II)] - + amb → [amb+M(II)+NTA]- (4)
Tabelle 3 zeigt, dass die Bildung der ternären Ni(II)-Komplexe exergonischer ist und in allen Fällen größere Bildungskonstanten K aufweist als die Zn(II)-Komplexe. Reaktion 4 (d.h. die amb-Tag-Assoziation mit dem NTA-Metallionenkomplex) ist von besonderem Interesse, da sie das amb-markierte rekombinante Protein darstellt, das an das NTA-immobilisierte Metallion innerhalb der IMAC-Säule bindet. Reaktion 4 zur Bildung von [ambA+Ni(II)+NTA] zeigt die spontanste ΔG298 = 53,1 kJ/mol und die höchste Bildungskonstante, K = 2,01 x 109.
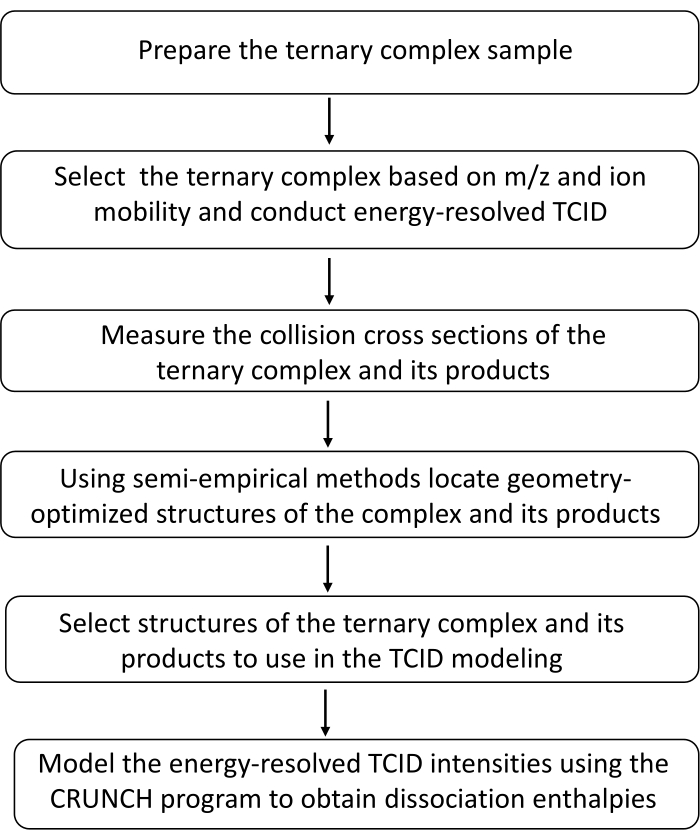
Abbildung 1: Übersicht über das ES-IM-MS TCID-Verfahren. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
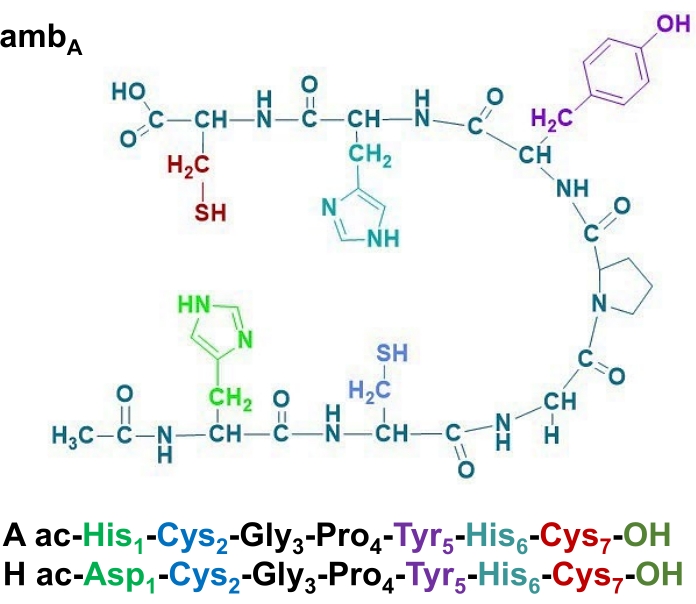
Abbildung 2: Die primären Strukturen von amb A und H Peptiden. Farbe hebt die potenziellen Metallbindungsstellen hervor. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
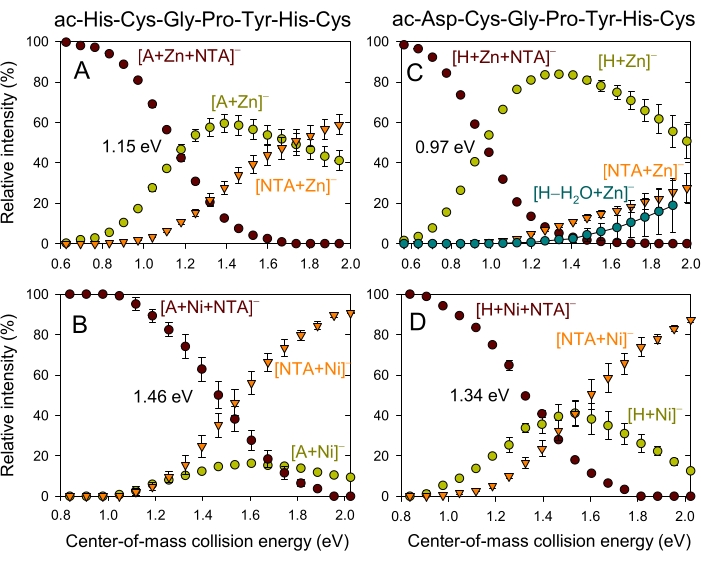
Abbildung 3: Die energieaufgelöste (eV) Kollisionsinduzierte Dissoziation von [amb+M(II)+NTA]-. Die Energieabhängigkeit der Produktionen [amb+M(II)]- [NTA+M(II)]- und [amb-H2O+Zn(II)]- wird gezeigt. Die Kollisionsenergie des Massenschwerpunkts, bei der 50% Dissoziation des [amb+M(II)+NTA]- ternären Komplexes vorliegt, ist in den Diagrammen enthalten. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
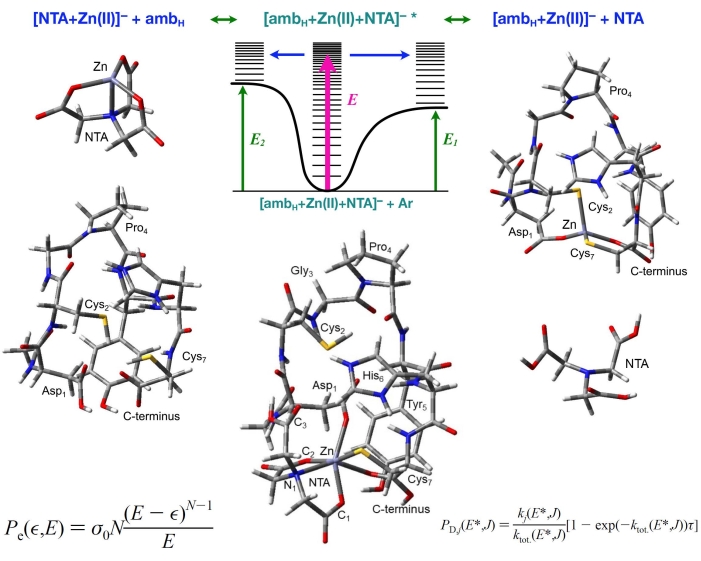
Abbildung 4: Das Modell für die energieaufgelöste TCID-Methode. Die Kollisionen zwischen [amb H+Zn(II)+NTA]- + Argon führen zur Dissoziation zu den Produkten [ambH+Zn(II)]- + NTA oder [NTA+Zn(II)]- + ambH. Die Schwellenenergien E1 und E2 entsprechen den 0 K-Dissoziationsenthalpien (Δ H0) für die Reaktionen [amb H+Zn(II)+NTA]- → [amb H+Zn(II)]- + NTA bzw. [amb H+Zn(II)+NTA]- → [NTA+Zn(II)]- + ambH. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
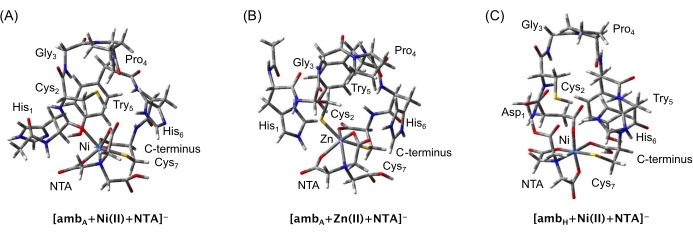
Abbildung 5: Die PM6-geometrieoptimierten ternären [amb+M(II)+NTA]- Komplexe von A und H. Konformer, die bei der TCID-Modellierung der experimentellen Daten verwendet werden. Diese Konformere wurden aus anderen Kandidatenstrukturen ausgewählt, indem ihre elektronischen PM6-Energien verglichen wurden und wie ihre LJ-Kollisionsquerschnitte (CCS He) mit dem IM-MS gemessenen CCSHe verglichen wurden. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.

Abbildung 6: Die energieaufgelöste, kollisionsinduzierte Dissoziation von [amb+M(II)+NTA]-. Für die Spezies A und H werden die Präparationen von [amb+M(II)]- und [NTA+M(II)]- mit den gewundenen CRUNCH-Schwellenwerten gezeigt. Die angegebenen Energiewerte (eV) sind die Dissoziationsenthalpien bei 0 K für die Reaktionen [amb+M(II)+NTA]- → [amb+M(II)]- + NTA oder [amb+M(II)+NTA]- → [NTA+M(II)]- + amb. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
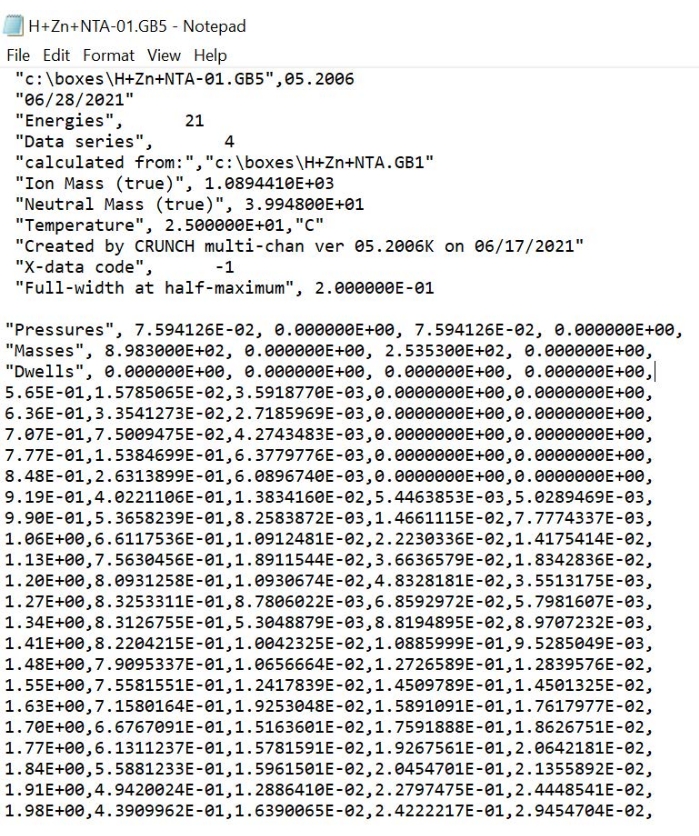
Abbildung 7: Das Format für die CRUNCH-Texteingabedatei. Die Datei enthält die mittleren relativen Intensitäten und ihre Standardabweichungen der produzierten Ionen, die als Funktion der Kollisionsenergie des Massenschwerpunkts gebildet werden. Bitte klicken Sie hier, um eine größere Version dieser Abbildung zu sehen.
| Amb | [amb+Zn(II)+NTA] - | [amb+Ni(II)+NTA] - | ||
| PM6 | Exp.a | PM6 | Exp.a | |
| Ein | 214±2 | 214 | 219±2 | 218 |
| H | 211±5 | 216 | 212±3 | 215 |
| ein ES-IM-MS CCSHe-Messungen haben Unsicherheiten von ±4 Å2. | ||||
Tabelle 1: Vergleich der LJ-Kollisionsquerschnitte der PM6-Konformere von [amb+M(II)+NTA]-. Theoretische Querschnitte der PM6-Konformere werden mit dem experimentellen CCSHe verglichen, das er mit ES-IM-MS gemessen hat.
| [amb+Zn(II)+NTA] - → | [amb+Ni(II)+NTA] - → | |||||||
| [amb+Zn(II)] - + NTA | [NTA+Zn(II)] - + amb | [amb+Ni(II)] - + NTA | [NTA+Ni(II)] - + amb | |||||
| Amb | ΔH0 | ΔH298 | ΔH0 | ΔH298 | ΔH0 | ΔH298 | ΔH0 | ΔH298 |
| Ein | 118 | 127 | 149 | 182 | 146 | 171 | 148 | 154 |
| H | 96.4 | 92.3 | 111 | 115 | 125 | 140 | 161 | 216 |
Tabelle 2: Thermochemische Ergebnisse der TCID-Analysen. Die energieabhängigen Reaktionen [amb+M(II)+NTA]- → [amb+M(II)]- + NTA oder [amb+M(II)+NTA]- → [NTA+M(II)]- + amb, die die 0 K-Dissoziationsenthalpien (Δ H 0) zeigen, die von der unkonvolutierten TCID-Modellanpassung abgeleitet sind, und 298 K-Dissoziationsenthalpien (Δ H 298), abgeleitet von ΔH0 und statistische mechanische thermische Korrekturen unter Verwendung der PM6-Rotations- und Schwingungsfrequenzen. Die Werte werden in kJ/mol angegeben.
| [amb+Zn(II)] - + NTA → | [NTA+Zn(II)] - + amb → | [amb+Ni(II)] - + NTA → | [NTA+Ni(II)] - + amb → | |||||
| [amb+Zn(II)+NTA] - | [amb+Zn(II)+NTA] - | [amb+Ni(II)+NTA] - | [amb+Ni(II)+NTA] - | |||||
| Amb | ΔG298 | K | ΔG298 | K | ΔG298 | K | ΔG298 | K |
| Ein | -34.0 | 9,05 x 105 | -21.8 | 6,59 x 103 | -45.7 | 1,01 x 108 | -53.1 | 2,01 x 109 |
| H | -29.3 | 1,36 x 105 | -30.2 | 1,95 x 105 | -47.0 | 1,71 x 108 | -31.1 | 2,81 x 105 |
Tabelle 3: Gibbs-freie Assoziationsenergien (ΔG298) und Gleichgewichtsbildungskonstanten (K). ΔG 298 und K bei 298 K für die Rückreaktionen [amb+M(II)]- + NTA → [amb+M(II)+NTA]- und [NTA+M(II)]- + amb → [amb+M(II)+NTA]-. Abgeleitet von ΔH298 und statistischen Mechanik-Entropieberechnungen unter Verwendung der PM6-Rotations- und Schwingungsfrequenzen. Die Werte für ΔG298 werden in kJ/mol angegeben.
Ergänzende Datei. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Diskussion
Kritische Schritte
ES-IM-MS Schwellenkollisions-induzierte Dissoziation (TCID) Analysen. Das TCID verwendete die Transfer-T-Wellenzelle in Gegenwart von Argon als Kollisionszelle. Vor der Dissoziation werden die Vorläuferionen durch niederenergetische Kollisionen mit Stickstoffgas thermalisiert, wenn sie die Zelle der Ionenmobilität (IM) passieren. Dies führt zu einer reproduzierbareren energieaufgelösten TCID als durch die Verwendung der Falle als Kollisionszelle 6,40. Die Thermalisierung des [amb+M(II)+NTA]- vor der Dissoziation ermöglicht es auch, die verfügbare innere Energie des ternären Komplexes mit einer Temperatur von 298 K zu charakterisieren. Die Dissoziation in der Transferzelle bedeutet auch, dass der ternäre Komplex und seine Produktionsionen die gleichen durchschnittlichen Ankunftszeiten am Detektor haben, was nützlich war, um die Dissoziation des ternären Komplexes zu identifizieren, die nur in der Transferzelle auftrat. Andere Regionen, in denen Dissoziation auftreten kann, sind die ES-Quelle (der Probenahmekegel wird bei 25 V gehalten, um dies zu vermeiden) oder am Eingang der IM-Zelle. Die durch die Dissoziation des ternären Komplexes in diesen Regionen erzeugten Produktionen haben andere Driftzeiten als die in der Transferzelle erzeugten, da die Produktionen vom ternären Komplex in der IM-Zelle getrennt sind. Diese Produktionen wurden von der Analyse ausgeschlossen. In diesem Protokoll werden nur die integrierten Ankunftszeitverteilungen für die Vorläufer- und Produktionen, die co-ausgerichtet sind, verwendet, um ihre Intensitäten zu bestimmen. Die Trap-Bias-Einstellung ist die Spannung, die die Einspeisespannung in die IM-Zelle steuert, die zum CID am Eingang der IM-Zelle beiträgt. Die Fallenverzerrung wurde auf 14 V festgelegt, wodurch die Hintergrunddissoziation auf ein Minimum reduziert wurde, ohne die Gesamtintensitäten übermäßig zu beeinflussen. Eine frühere Studie41 bestimmte die effektive Temperatur (obere Grenze) des Peptiddimers von Leucinenkephalin auf 449 K am Eingang der IM-Zelle. Die effektive Temperatur nahm jedoch schnell ab, als das Dimer die IM-Zelle passierte. Die Ankunftszeiten der hier untersuchten amb-Komplexe wiesen Gaußsche Verteilungen auf, was darauf hindeutet, dass sie thermalisiert wurden, als sie die IM-Zelle passierten.
ES-IM-MS Kollisionsquerschnitte (CCS) Analysen. CCS-Driftzeiten wurden experimentell als Folge von Kollisionen mit Stickstoff gefunden. Diese Werte wurden unter Verwendung einer Kalibrierkurve bekannter Standards in Helium-abgeleitete CCS-Driftzeiten umgerechnet. Dies ist wichtig, da die Programme, die zur Messung des CCS der PM6-Konformer verwendet werden, die gebräuchlicheren Heliumstandards erfordern.
Modifikationen und Fehlerbehebung der Technik
CRUNCH-Eingabetextdateiformat. Die für das CRUNCH-Programm geeignete Eingabetextdatei ist in Abbildung 7 dargestellt. Die Header in der Reihenfolge von oben nach unten sind Dateispeicherort und Version von CRUNCH; Datum; Anzahl der Energien; Anzahl der Datenreihen ohne die erste Energiespalte; Quelldatei; Masse des Vorläuferkomplexes; Masse von Argon; Temperatur des Experiments; Datum der Erstellung; x-Daten, die als −1 bezeichnet werden (die Kollisionsenergien des Massenschwerpunkts); und die volle Breite bei halbem Maximum (FWHM) des Ionenstrahls. Diese Werte müssen für jedes TCID-Experiment geändert werden. Die FWHM-Energieausbreitung des Ionenstrahls und der Energienullpunkt sollten durch Retarding-Potentialanalyse (RPA) bestimmt werden, indem der CE durch niedrige Spannungen abgetastet und der Gesamtionenstrom überwacht wird. Unter den Betriebsbedingungen des IM in der aktuellen Studie nahm das Ionenstromsignal jedoch nur um etwa 50% ab, wenn der Transfer CE auf seinen niedrigsten Wert eingestellt wurde. Die Ionenstrahlenergie Nullpunkt und FWHM konnten nur bei zusätzlicher Verzögerung durch Absenken der Austritts-IM-Linse gemessen werden. In letzterem Fall ergab die FWHM der Ableitung der RPA-Kurve eine typische Ionenenergiespreizung von 1,5 V im Lab-Frame bzw. 0,035 eV im Schwerpunkt-Frame13.
Die Druckzeile bezieht sich auf den Druck innerhalb der Kollisionszelle, wird hier aber nicht verwendet. Die Drücke von Argon in der Kollisionszelle können variiert werden und die TCID-Daten können bei drei Drücken gemessen werden, um auf einzelne Kollisionsbedingungen zu extrapolieren. In dieser Studie wurde jedoch nur ein Druck verwendet, und der Druck führt zu mehreren Kollisionen. Die Entwicklung der neuen Plattform für eine einzelne Kollision ist ein Bereich der laufenden Forschung. Massen beziehen sich auf die beiden Produktionsionen, deren Intensitäten in den folgenden Spalten liegen. Verweildauer kann als Standard beibehalten werden. Die fünf Spalten sind die Kollisionsenergien des Massenschwerpunkts (bezeichnet als −1); der Mittelwert der Ionenintensitäten der Spezies mit einer Masse von 898,30 U; die Standardabweichungen der Ionenintensitäten der Spezies 898,30 u; der Mittelwert der Ionenintensitäten der Spezies mit einer Masse von 253,53 U; und die Standardabweichungen der Ionenintensitäten der Spezies 253,53 u.
Molekulare Modellierung
Die Anzahl der Konformere wurde zunächst unter Verwendung von Modellen aus früheren Studien 9,10,11,12,13 eingegrenzt. Die CRUNCH-Anpassung erfordert ein sorgfältiges Screening von Reaktanten, aktivierten Molekülen und Übergangszuständen, um genaue Schwellenenergien zu erhalten. Frühere Forschungen 9,10,11,12,13 umfassten ein umfangreiches Screening von [amb+M(II)]-Konformeren, um die Strukturen mit den Parametern zu erhalten, die hier in der CRUNCH-Modellierung verwendet werden. Es wurden nur Komplexe mit trans-Peptidbindungen verwendet, da nur sie mit IM-MS-gemessenem CCSHe10 übereinstimmen. Die molekularen Modellierungsmethoden B3LYP und PM6 sagen beide den niedrigsten Energie-[amb+M(II)]-Konformer voraus, der Aa1-Cys 2-Cys7 und die Carboxylat-Terminus-Koordination von Zn(II) oder Ni(II)10,11,12,13 aufweist. Die Vertrautheit mit dem Verhalten der bekannten Modelle ermöglichte es, die neuen Konformere von [amb+M(II)+NTA]- effizienter zu bestimmen. Um die Konformitätsbestimmung zu unterstützen, wurden niederenergetische Konformer, die nach der PM6-Methode lokalisiert wurden, herausgefiltert und systematisch neu bewertet, bis die praktikabelsten Konformatoren mit der niedrigsten Energie übrig blieben.
CRUNCH-Modellierung
Zeitfenster für die Beobachtung der Dissoziation. In dieser Studie wurde das Zeitfenster von 50 μs vom Beginn der Transferzelle bis zum Ende des TOF-Analysators, wo der Mehrkanal-Plattendetektor positioniert ist, verwendet. Es kann besser sein, das experimentelle Zeitfenster zwischen der Aktivierung in der Transferzelle und dem Eingang zum TOF-Massenanalysator zu nutzen, denn wenn das aktivierte Ion während seiner Zeit im Reflektor-TOF dissoziiert, wird dieser metastabile Zerfall bei einem anderen m/z gemessen. In dieser Studie waren die in den Massenspektren beobachteten Produktionen jedoch alle als die in Abbildung 3 gezeigten unmodifizierten m/z-Spezies identifizierbar. Dies deutet darauf hin, dass metastabiler Zerfall kein Problem war. Weitere Forschungen könnten dies untersuchen, indem sie eine bekannte Reaktion mit einem hohen Schwellenwert untersuchen und überprüfen, ob die richtige Schwellenenergie unter Verwendung des 50 μs-Zeitfensters und der RRKM-Modellierung erhalten wird.
Skalierungsfaktoren für die Schwingungsfrequenzen. Es wurden die vom NIST empfohlenen Skalierungsfaktoren für PM6 (1,062) Schwingungsfrequenzen verwendet. Diese waren zufriedenstellend für die Anpassung der [A+Zn(II)+NTA]-, [A+Ni(II)+NTA]- und [H+Zn(II)+NTA]-Daten. In einigen Fällen, in denen der höhere Energiekanal entropisch gegenüber dem unteren Energiekanal bevorzugt wird, kann es notwendig sein, die Frequenzen des zweiten Kanals zusätzlich zu skalieren. Ein Ansatz besteht darin, die Frequenzen unter 900 cm−1 zu skalieren (da diese am wenigsten genau sind), um die Frequenzen zu lockern und den TS entropischer zu begünstigen.
Optimierung von Parametern. Die Verwendung der Option Ja, um einen beliebigen Parameter auf Barwert zu halten, kann hilfreich sein, um die Daten erfolgreich anzupassen. Für die erste Anpassung wird die E 0(2) gehalten und die Modell-TCID an die Daten angepasst, indem die Variablen CONST, E0(1) und N optimiert werden. Sobald eine gute Anpassung gefunden wurde, können die Parameteroption und Hold any parameter at present value verwendet werden, um CONST, E 0(1) und N zu speichern, während E0(2) die Daten optimieren kann. Sobald E 0(2) optimiert ist, sollten in der Parameteroption alle vier Parameter CONST, E 0(1), E0(2) und N für die Daten optimiert werden dürfen.
Energiebereich zur Anpassung des ausgewählten TCID-Modells an die experimentellen Daten. Der Energiebereich, der zur Anpassung der experimentellen Daten verwendet wird, sollte so viele der experimentellen Intensitätsdaten wie möglich reproduzieren und gleichzeitig eine gute Anpassung im Schwellenwertbereich beibehalten. Man kann damit beginnen, das TCID-Modell an einen kleinen Energiebereich an den Schwellenwerten der experimentellen Daten anzupassen. Man kann eine Startenergie wählen, die die Hintergrundintensität kurz vor dem Verhalten der steigenden Intensitätsschwelle aufweist. Sobald die TCID-Anpassung an den experimentellen Datenbereich optimiert ist, sollte die Reichweite um 0,1 eV erhöht und die Anpassung erneut optimiert werden. Dieses Verfahren sollte wiederholt werden, um so viel wie möglich in den Datenbereich einzupassen und gleichzeitig die Anpassung des Schwellenwertbereichs beizubehalten.
Thermochemische Analysen. Die thermochemischen Ergebnisse der Option Delta H und S bei T sollten mit einer Reihe unterschiedlicher Energiebereichsanpassungen an die Daten verglichen werden, um die Standardabweichung der TCID-Modellanpassung abzuschätzen. Zu vergleichende Anpassungen sollten kleinere Bereiche umfassen, die gut zu den anfänglich steigenden Schwellenintensitäten passen, mit solchen mit größeren Bereichen, die auch die höheren Energien umfassen.
Offenlegungen
Die Autoren haben keinen Interessenkonflikt offenzulegen.
Danksagungen
Dieses Material basiert auf Arbeiten, die von der National Science Foundation im Rahmen von 1764436, NSF REU-Programm (CHE-1659852), NSF-Instrumentenunterstützung (MRI-0821247), Physics and Astronomy Scholarship for Success (PASS) NSF-Projekt (1643567), Welch Foundation (T-0014) und Computerressourcen des Department of Energy (TX-W-20090427-0004-50) und L3 Communications unterstützt werden. Die Autoren danken Kent M. Ervin (University of Nevada - Reno) und Peter B. Armentrout (University of Utah) für das Teilen des CRUNCH-Programms und für die Beratung zur Anpassung durch PBA. Die Autoren danken der Gruppe von Michael T. Bower an der University of California - Santa Barbara für das Teilen des Sigma-Programms.
Materialien
| Name | Company | Catalog Number | Comments |
| Acetonitrile HPLC-grade | Fisher Scientific (www.Fishersci.com) | A998SK-4 | |
| Alternative metal binding (amb) peptides | PepmicCo (www.pepmic.com) | designed peptides were synthized by order | |
| Ammonium acetate (ultrapure) | VWR | 97061-014 | |
| Ammonium hydroxide (trace metal grade) | Fisher Scientific (www.Fishersci.com) | A512-P500 | |
| Driftscope 2.1 software program | Waters (www.waters.com) | software analysis program | |
| Gaussian 09 | Gaussian | Electronic Structure Modeling Software | |
| GaussView | Gaussian | Graphical Interface to Visualize Computations | |
| Glacial acetic acid (Optima grade) | Fisher Scientific (www.Fishersci.com) | A465-250 | |
| Ion-scaled Lennard-Jones (LJ) method | Sigma | Michael T. Bowers’ group of University of California at Santa Barbara | |
| MassLynx 4.1 | Waters (www.waters.com) | software analysis program | |
| Microcentrifuge Tubes | VWR | 87003-294 | 1.7 mL, polypropylene |
| Microcentrifuge Tubes | VWR | 87003-298 | 2.0 mL, polypropylene |
| Ni(II) nitrate hexahydrate (99% purity) | Sigma-Aldrich (www.sigmaaldrich.com) | A15540 | |
| Poly-DL-alanine | Sigma-Aldrich (www.sigmaaldrich.com) | P9003-25MG | |
| Waters Synapt G1 HDMS | Waters (www.waters.com) | quadrupole - ion mobility- time-of-flight mass spectrometer | |
| Zn(II) nitrate hexahydrate (99%+ purity) | Alfa Aesar (www.alfa.com) | 12313 |
Referenzen
- Kim, Y. -. M., Chen, P. Ligand binding energy in [(bipy)Rh(PCH)]+ by collision-induced dissociation threshold measurements. International Journal of Mass Spectrometry. 202 (1-3), 1-3 (2000).
- Plattner, D. Electrospray mass spectrometry beyond analytical chemistry: Studies of organometallic catalysis in the gas phase. International Journal of Mass Spectrometry. 207 (3), 125-144 (2001).
- Narancic, S., Bach, A., Chen, P. Simple fitting of energy-resolved reactive cross sections in threshold collision-induced dissociation (T-CID) experiments. Journal of Physical Chemistry A. 111 (30), 7006-7013 (2007).
- Ervin, K., Armentrout, P. B. Systematic and random errors in ion affinities and activation entropies from the extended kinetic method. Journal of Mass Spectrometry. 39 (9), 1004-1015 (2004).
- Cooks, R. G., Wong, P. S. H. Kinetic method of making thermochemical determinations: Advances and applications. Accounts of Chemical Research. 31 (7), 379-386 (1998).
- Ervin, K. Microcanonical analysis of the kinetic method. The meaning of the "apparent entropy". Journal of the American Society of Mass Spectrometry. 13 (5), 435-452 (2002).
- Amarasinghe, C., Jin, J. -. P. The use of affinity tags to overcome obstacles in recombinant protein expression and purification. Protein & Peptide Letters. 22 (10), 885-892 (2015).
- Bornhorst, J. A., Falke, J. J. Purification of proteins using polyhistidine affinity tags. Methods in Enzymology. 326, 245-254 (2000).
- Yousef, E. N., Angel, L. A. Comparison of the pH-dependent formation of His and Cys heptapeptide complexes of nickel(II), copper(II), and zinc(II) as determined by ion mobility-mass spectrometry. Journal of Mass Spectrometry. 55 (3), 4489 (2020).
- Lin, Y. -. F., et al. Weak acid-base interactions of histidine and cysteine affect the charge states, tertiary structure, and Zn(II)-binding of heptapeptides. Journal of the American Society of Mass Spectrometry. 30, 2068-2081 (2019).
- Wagoner, S. M., et al. The multiple conformational charge states of zinc(II) coordination by 2His-2Cys oligopeptide investigated by ion mobility - mass spectrometry, density functional theory and theoretical collision cross sections. Journal of Mass Spectrometry. 51 (12), 1120-1129 (2016).
- Flores, A. A., et al. Formation of Co(II), Ni(II), Zn(II) complexes of alternative metal binding heptapeptides and nitrilotriacetic acid: Discovering new potential affinity tags. International Journal of Mass Spectrometry. 463, 116554 (2021).
- Flores, A. A., et al. Thermochemical and conformational studies of Ni(II) and Zn(II) ternary complexes of alternative metal binding peptides with nitrilotriacetic acid. International Journal of Mass Spectrometry. 473, 116792 (2022).
- Sesham, R., et al. The pH dependent Cu(II) and Zn(II) binding behavior of an analog methanobactin peptide. European Journal of Mass Spectrometry. 19 (6), 463-473 (2013).
- Choi, D., et al. Redox activity and multiple copper(I) coordination of 2His-2Cys oligopeptide. Journal of Mass Spectrometry. 50 (2), 316-325 (2015).
- Vytla, Y., Angel, L. A. Applying ion mobility-mass spectrometry techniques for explicitly identifying the products of Cu(II) reactions of 2His-2Cys motif peptides. Analytical Chemistry. 88 (22), 10925-10932 (2016).
- Yousef, E. N., et al. Ion mobility-mass spectrometry techniques for determining the structure and mechanisms of metal ion recognition and redox activity of metal binding oligopeptides. Journal of Visualized Experiments. (151), e60102 (2019).
- Ilesanmi, A. B., Moore, T. C., Angel, L. A. pH dependent chelation study of Zn(II) and Ni(II) by a series of hexapeptides using electrospray ionization - Ion mobility - Mass spectrometry. International Journal of Mass Spectrometry. 455, 116369 (2020).
- Armentrout, P. B., Ervin, K. M., Rodgers, M. T. Statistical rate theory and kinetic energy-resolved ion chemistry: Theory and applications. Journal of Physical Chemistry A. 112 (41), 10071-10085 (2008).
- Dalleska, N. F., Honma, K., Sunderlin, L. S., Armentrout, P. B. Solvation of transition metal ions by water. Sequential binding energies of M+(H2O)x (x = 1-4) for M = Ti to Cu determined by collision-induced dissociation. Journal of the American Chemical Society. 116 (8), 3519-3528 (1994).
- Ervin, K. M., Armentrout, P. B. Translational energy dependence of Ar + XY → ArX+ + Y (XY = H2,D2,HD) from thermal to 30 eV c.m. Journal of Chemical Physics. 83, 166-189 (1985).
- DeTuri, V. F., Ervin, K. M. Competitive threshold collision-induced dissociation: Gas-phase acidities and bond dissociation energies for a series of alcohols. Journal of Physical Chemistry A. 103 (35), 6911-6920 (1999).
- Iceman, C., Armentrout, P. B. Collision-induced dissociation and theoretical studies of K+ complexes with ammonia: a test of theory for potassium ions. International Journal of Mass Spectrometry. 222 (1-3), 329-349 (2003).
- Rodgers, M. T., Ervin, K. M., Armentrout, P. B. Statistical modeling of collision-induced dissociation thresholds. Journal of Chemical Physics. 106, 4499-4508 (1997).
- Rodgers, M. T., Armentrout, P. B. Statistical modeling of competitive threshold collision-induced dissociation. Journal of Chemical Physics. 109, 1787-1800 (1998).
- Armentrout, P. B., Ervin, K. M. . CRUNCH, Fortran program, version 5.2002. , (2016).
- Pringle, S. D., et al. An investigation of the mobility separation of some peptide and protein ions using a new hybrid quadrupole/travelling wave IMS/oa-ToF instrument. International Journal of Mass Spectrometry. 261 (1), 1-12 (2007).
- Smith, D. P., et al. Deciphering drift time measurements from travelling wave ion mobility spectrometry-mass spectrometry studies. European Journal of Mass Spectrometry. 15 (2), 113-130 (2009).
- Forsythe, J. G., et al. Collision cross section calibrants for negative ion mode traveling wave ion mobility-mass spectrometry. Analyst. 140 (20), 6853-6861 (2015).
- Allen, S. J., Giles, K., Gilbert, T., Bush, M. F. Ion mobility mass spectrometry of peptide, protein, and protein complex ions using a radio-frequency confining drift cell. Analyst. 141 (3), 884-891 (2016).
- Salbo, R., et al. Traveling-wave ion mobility mass spectrometry of protein complexes: accurate calibrated collision cross-sections of human insulin oligomers. Rapid Communications in Mass Spectrometry. 26 (10), 1181-1193 (2012).
- Stewart, J. J. P. Optimization of parameters for semiempirical methods V: Modification of NDDO approximations and application to 70 elements. Journal of Molecular Modeling. 13, 1173 (2007).
- Frisch, M. J., et al. . Gaussian 09, Revision C.01. Wallingford CT: Gaussian, Inc. , (2012).
- Becke, A. D. Density-functional thermochemistry. III. The role of exact exchange. Journal of Chemical Physics. 98, 5648-5652 (1993).
- Wyttenbach, T., von Helden, G., Batka, J. J., Carlat, D., Bowers, M. T. Effect of the long-range potential on ion mobility measurements. Journal of the American Society of Mass Spectrometry. 8, 275-282 (1997).
- Shvartsburg, A. A., Jarrold, M. F. An exact hard-spheres scattering model for the mobilities of polyatomic ions. Chemical Physics Letters. 261 (1-2), 86-91 (1996).
- Heerdt, G., Zanotto, L., Souza, P. C. T., Araujo, G., Skaf, M. S. Collision cross section calculations using HPCCS. Methods in Molecular Biology. 2084, 297-310 (2020).
- Zanotto, L., Heerdt, G., Souza, P. C. T., Araujo, G., Skaf, M. S. High performance collision cross section calculation-HPCCS. Journal of Computational Chemistry. 39 (21), 1675-1681 (2018).
- . https://cccbdb.nist.gov/pollistx.asp Available from: https://cccbdb.nist.gov/pollistx.asp (2022)
- Raja, U. K. B., Injeti, S., Culver, T., McCabe, J. W., Angel, L. A. Probing the stability of insulin oligomers using electrospray ionization ion mobility mass spectrometry. European Journal of Mass Spectrometry. 21 (6), 759-774 (2015).
- Merenbloom, S. I., Flick, T. G., Williams, E. R. How hot are your ions in TWAVE ion mobility spectrometry. Journal of the American Society of Mass Spectrometry. 23 (3), 553-562 (2012).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten
Wir verwenden Cookies, um Ihre Erfahrung auf unserer Website zu verbessern.
Indem Sie unsere Website weiterhin nutzen oder auf „Weiter“ klicken, stimmen Sie zu, unsere Cookies zu akzeptieren.
