Method Article
Nasojejunal 튜브 배치를 위한 최소 침습적이고 시각화된 방법
* 이 저자들은 동등하게 기여했습니다
요약
본 연구는 중환자실 환자의 비관삽입을 개선하여 효율성을 높이고 환자의 불편함을 줄이기 위한 병상 시각화 방법을 소개합니다.
초록
영양실조는 중환자에서 흔히 발생하는 문제이며, 종종 질병, 부상 또는 수술로 인해 발생합니다. 장기간의 단식은 장 문제를 일으키며, 특히 제주널 영양을 통한 조기 경장 영양의 중요성을 강조합니다. 경장 영양 섭취가 중요하지만, 현재 기술로는 문제가 생깁니다. Nasojejunal(NJ) 튜브가 일반적으로 사용되며 삽입 방법은 외과적 또는 비수술적 방식으로 분류됩니다. 내시경 유도를 포함한 비수술적 방법은 성공률이 다양하며, 내시경 보조 배치가 가장 성공적이지만 전문적인 전문 지식과 물류가 필요합니다.
이 연구는 중환자실(ICU)에서 성공률을 높이고 환자의 불편함을 줄이기 위해 NJ 튜브 배치를 위한 병상 시각화 방법을 소개합니다. 19명의 ICU 환자를 대상으로 한 이 연구에서 이 방법은 94.74%의 초기 성공률을 달성했으며 평균 삽입 시간은 11.2분± 6.4분이었습니다. 이 시각화된 방법은 효율성을 입증하고 추가 이미징의 필요성을 줄여주며, 소형 내시경의 도입은 침대 옆에서 성공적인 삽관을 가능하게 하고 환자의 불편함을 최소화할 수 있는 가능성을 보여줍니다. 가이드와이어 렌즈와 카테터에 대한 조정이 필요하지만 향후 개선의 기회가 있습니다.
서문
영양실조는 중환자에서 흔한 합병증으로 자주 나타나며, 주로 질병, 부상 또는 외과적 개입의 결과로 음식을 정상적으로 섭취하거나 소화할 수 없게 됩니다 1,2,3,4. 입원 환자의 30-60%가 영양실조를 계속 경험하고 있다5. 결과적으로, 조기 경장 영양 지원을 제공하는 것이 중요한 것으로 간주된다6. 조기 제주날 영양 섭취는 위장 기능의 무결성을 유지하고 장 점막 장벽을 보호하는 데 도움이 될 뿐만 아니라 면역력 향상과 합병증 감소에 기여합니다 7,8. 영양 보충 지원의 필요성을 주장하는 의견이 일치하고 있으며, 영양 보충 지원이 환자의 예후를 향상시킬 수 있다는 증거가 있다 9,10. 이러한 상황에서는 장 영양(EN)으로 알려진 위 또는 소장에 삽입된 튜브를 통해 영양을 투여할 수 있습니다. 경장 접근 장치 및 배치 기술의 효과에 대한 연구가 더욱 중요해지고 있습니다.
침대 옆에서 비위관을 무턱대고 삽입하는 것은 일반적으로 성공적입니다. 방사선 사진에서 NG 튜브 팁이 위11 내에 올바르게 위치했음을 확인하면 튜브 공급이 시작될 수 있습니다. 그러나 중증 질환 중에는 위 배출이 지연되어 EN 분만 중 위 잔류 용적(GRV)이 증가할 수 있습니다12. GRV가 높으면 흡인의 위험이 있으므로 의료 제공자는 EN 투여를 중단해야 합니다12. 이에 대한 해결책으로, 비뇨병(NJ) 튜브는 중환자에게 영양을 공급하기 위해 일반적으로 사용되는 방법입니다. 현재 NJ 튜브를 배치하는 방법에는 주로 외과적 또는 비수술적 방법으로 분류되는 수많은 방법이 있습니다. 블라인드 삽입, 전자기 추적을 통한 X선 형광 투시법(예: Cortrak, ENvue), 초음파 유도 배치 및 내시경 유도를 포함하여 비대칭(NJ) 튜브를 배치하는 몇 가지 비수술적 방법이 있습니다 13,14,15,16.
블라인드 병상 NJ 튜브 배치는 광범위하게 연구되었지만 이 절차의 성공률은 환자의 경우 17%에서 83%까지 매우 다양합니다17,18. 가이드 튜브 배치가 없으면 NJ 튜브가 유문을 성공적으로 통과한 시점을 알기가 어려워집니다. 또한 카테터가 실수로 기도로 들어갈 위험이 있으며, 특히 의식이 없는 중증 환자의 경우 더욱 그렇습니다. 비수술적 방법 중에서는 내시경 보조 튜브 삽입이 가장 성공적이었으며 성공률은 73.3%에서 97.6%에 이릅니다14,19,20. 일반적으로 NJ 튜브의 내시경 배치는 일반적으로 내시경실에서 위장병 전문의의 전문 지식을 필요로 합니다. 또한 소화기 내시경의 직경이 상대적으로 크면 환자에게 상당한 불편함을 유발할 수 있으며 종종 전신 마취를 사용해야 합니다.
또한 환자를 위장관 내시경실로 이송하는 것은 특히 중환자실(ICU)의 중환자에게 상당한 물류 문제를 야기합니다. 이러한 환자들은 종종 쇼크와 심각한 호흡 부전을 포함한 불안정한 활력 징후를 보입니다. 중환자는 고위험군에 속하며 이송 중 부작용을 경험할 가능성이 높다21. 직접 내시경 시각화를 사용하여 NJ 튜브를 배치하는 다양한 방법이 논의되었습니다. 이러한 방법은 소규모 연구에서 80%에서 90%에 이르는 성공률을 보고했다 22,23,24. 그러나 이러한 절차는 종종 시간이 많이 걸리고 기술적으로 까다로우며 가파른 학습 곡선이 필요합니다.
따라서 우리 기관에서는 소형 시각화 장치를 사용하여 침대 옆에 있는 환자에게 NJ 튜브를 삽입합니다. 이렇게 하면 튜브의 끝이 유문을 가로지르고 우발적으로 기도로 유입되는 것을 방지할 수 있으며, 이 모든 것이 지속적인 시각적 모니터링 하에 이루어집니다. 이 방법의 목표는 의료 전문가, 특히 중환자실에 있는 전문가에게 중환자에서 NJ 튜브 삽입의 성공률을 높여 궁극적으로 환자의 불편함을 최소화하는 새로운 접근 방식을 제공하는 것입니다.
프로토콜
이 연구는 안지현 인민병원 임상연구윤리위원회의 승인을 받았다. 모든 절차는 기관에서 승인한 프로토콜과 환자의 정보에 입각한 동의에 따라 수행되었습니다.
1. 환자 선택 및 준비
- 다음 포함 및 제외 기준에 따라 환자를 선택합니다.
- 포함 기준을 급성 위장 기능 장애 환자로 설정합니다. 기계적 환기를 받고 있거나 의식이 손상되었거나 혼수 상태에 있는 사람; 삼키거나 씹는 데 어려움을 겪는 사람들; 위 수유를 견딜 수 없거나 위저류를 경험하는 개인; 췌장염, 과진대사 상태 또는 영양실조 환자; 외상성 뇌 손상을 입은 사람, 종양으로 화학 요법을 받는 사람 등과 같이 역류에 취약한 개인; 염증성 장 질환, 위식도 누공 또는 단장 증후군 환자; 구강, 인두 또는 식도 수술을 받은 환자를 포함한 다른 질환이 있는 개인; 18세 이상의 연령.
- 제외 기준을 상부 위장관 출혈로 설정하십시오. 유문 부종 또는 폐색; 마비 또는 기계적 장 폐색; 장 천공, 괴사 또는 흡수 장애; 위장 수술의 병력; 심한 스트레스 상태 또는 충격; 식도 협착 또는 심장 협착증 또는 폐색; 및 심각한 식도 위 하부 정맥류, 코 폐색, 급성 또는 만성 부비동염 등과 같은 기타 상태.
- 수술 전 평가
- 시술 전에 환자의 영양 상태, 의식, 전반적인 상태, 삼킴 기능, 구강 및 코 상태, 위장 기능 및 협력 수준을 평가합니다.
- 이 프로토콜을 따르기 위해서는 중환자실 환자를 위해 특별히 개발된 영양 위험 평가 도구인 NUTRIC(Nutrition Risk in the Critically Ill) 채점 시스템을 1차 영양 위험 평가 도구로 사용한다25. NUTRIC 점수에는 연령, 급성 생리학 및 만성 건강 평가(APACHE) II26, 순차적 장기 부전 평가(SOFA) 점수26, 동반 질환 수, 입원부터 중환자실 입원까지의 일수, 인터루킨-6 수치(사용 가능한 경우)가 포함됩니다. 총 NUTRIC 점수의 범위는 0에서 10까지이며 점수가 높을수록 영양학적 위험이 더 크다는 것을 나타냅니다. 0-4점은 영양 위험이 낮다는 것을 의미하고 5-9점은 영양 위험이 높음을 나타냅니다.
참고: NUTRIC 채점 시스템과 APACHE II 및 SOFA 점수에 대한 자세한 내용은 보충 표 S1을 참조하십시오.
- 이 프로토콜을 따르기 위해서는 중환자실 환자를 위해 특별히 개발된 영양 위험 평가 도구인 NUTRIC(Nutrition Risk in the Critically Ill) 채점 시스템을 1차 영양 위험 평가 도구로 사용한다25. NUTRIC 점수에는 연령, 급성 생리학 및 만성 건강 평가(APACHE) II26, 순차적 장기 부전 평가(SOFA) 점수26, 동반 질환 수, 입원부터 중환자실 입원까지의 일수, 인터루킨-6 수치(사용 가능한 경우)가 포함됩니다. 총 NUTRIC 점수의 범위는 0에서 10까지이며 점수가 높을수록 영양학적 위험이 더 크다는 것을 나타냅니다. 0-4점은 영양 위험이 낮다는 것을 의미하고 5-9점은 영양 위험이 높음을 나타냅니다.
- 참여하기 전에 연구 참가자로서 개인의 목적, 위험, 혜택 및 권리를 환자에게 설명합니다. 잠재적 참가자 또는 그 가족으로부터 정보에 입각한 동의를 얻고 서면으로 문서화합니다. 시술 중 환자가 기꺼이 협조할 수 있는지 확인합니다.
- NUTRIC Nutrition Scoring Table25 (중환자 환자를 위해 특별히 고안됨)를 활용하여 환자의 영양 상태를 평가합니다.
- 6-8시간 동안 수술 전 금식을 시행하고 위장 감압 옵션을 제공합니다.
- 시술 전에 환자의 영양 상태, 의식, 전반적인 상태, 삼킴 기능, 구강 및 코 상태, 위장 기능 및 협력 수준을 평가합니다.
- 물품 준비
- 휴대용 시각화 NJ 튜브 배치 본체의 기능을 검사하고(그림 1), 일회용 시각화 NJ 튜브 포장의 무결성 및 만료 날짜를 확인하고, 의사의 지시에 따라 메토클로프라미드 염산염 주사제, 2% 리도카인 젤 및 멸균 액체 파라핀 오일을 준비하고, 멸균 수건, 주사기, 식염수, 장갑 및 접착 테이프를 구합니다.
참고: 항목 준비에 대한 자세한 내용은 보충 파일 1을 참조하십시오.
- 휴대용 시각화 NJ 튜브 배치 본체의 기능을 검사하고(그림 1), 일회용 시각화 NJ 튜브 포장의 무결성 및 만료 날짜를 확인하고, 의사의 지시에 따라 메토클로프라미드 염산염 주사제, 2% 리도카인 젤 및 멸균 액체 파라핀 오일을 준비하고, 멸균 수건, 주사기, 식염수, 장갑 및 접착 테이프를 구합니다.
2. NJ 튜브 배치 절차
- 튜브 삽입 절차 전에 환자의 이름, 병원 번호 및 절차 이름을 다시 확인하여 정확성을 확인하십시오.
- 전원 공급 장치(220V, 60Hz)를 시각화된 NJ 튜브 배치 본체에 연결하고 START 버튼을 눌러 켭니다.
- 시각화 NJ 튜브의 포장을 열고 튜브를 멸균 처리 벤드에 담그십시오. 튜브 내강을 2 x 20mL의 멸균 식염수로 헹굽니다.
- 가이드 와이어 내시경을 NJ 튜브의 캐비티에 삽입하고 풍선과 물주머니를 연결하고 적절한 시각화를 위해 시각적 렌즈를 조정합니다. 적절한 윤활을 보장하기 위해 NJ 튜브 외부에 멸균 액체 파라핀을 바르십시오.
- 환자가 의식이 있는 경우 면봉에 2% 리도카인 젤을 적당량 도포한 후 환자의 코 점막에 도포하여 표면 마취를 실시합니다.
- 침대를 30-45° 각도로 들어 올린 상태에서 환자를 누운 자세로 배치합니다(그림 2A).
- 육안으로 관찰하면서 환자의 콧구멍을 통해 튜브를 삽입하고 한 번에 약 1-2cm씩 튜브를 천천히 전진시킵니다(그림 2A). 튜브의 끝이 구인두에 닿았을 때 환자가 의식이 있으면 자발적으로 삼키도록 지시합니다. 의식이 있는 혼수상태 환자의 경우 머리와 턱을 아래로 기울여 경추를 곧게 펴고 식도로 쉽게 들어갈 수 있습니다. 기관으로의 잘못된 배치를 방지하기 위해 육안으로 지속적으로 관찰합니다.
참고: 환자의 비강 개통에 주의하십시오. 비중격 이탈과 같은 문제로 인해 어려움이 발생하는 경우 반대쪽 콧구멍을 시도하는 것이 좋습니다. - 식도 점막의 잠재적인 손상을 방지하기 위해 튜브를 식도 쪽으로 천천히 전진시키는 동안 저항을 주의하십시오. 식도에 들어가면 세로로 주름이 있는 옅은 분홍색 점막을 관찰합니다.
- 식도의 좁은 지점을 통과하는 동안 삽입을 위해 튜브를 부드럽게 회전하여 역동적인 육안 관찰을 하십시오. 강압적인 행동을 삼가고, 세 개의 좁은 지점을 조심스럽게 탐색하고, 필요에 따라 공기 또는 식염수를 주입하고, 선명한 이미지를 위해 시각화된 NJ 튜브의 앞쪽 끝에 있는 가이드 와이어 렌즈의 청결을 보장합니다.
참고: 정상 식도에는 세 개의 좁은 지점이 있습니다. 첫 번째 좁아짐은 식도의 시작 부분에서, 두 번째는 왼쪽 주요 기관지 뒤를 가로지르는 곳이며, 세 번째는 횡격막을 통과하는 식도 열공에서 발생합니다. 정상 식도의 점막은 촉촉하고 매끄럽고 분홍색이며 하부 식도 점막은 약간 밝은 회색입니다. 점막에는 7-10개의 수직 주름이 있으며 공동은 볼록하게 보입니다. - 한 번에 약 1-2cm씩 환자의 호흡 움직임을 육안으로 관찰하면서 튜브를 천천히 전진시킵니다.
- 튜브가 위식도 접합부(Z-라인)를 통과하여 위강으로 들어갈 때 짙은 분홍색 위 점막과 연동 운동을 관찰합니다. 점막 표면은 일반적으로 불규칙한 주름과 함몰을 나타냅니다(그림 2B).
참고: 위식도 접합부(Z-line)는 식도 점막에서 위 점막으로의 이동을 설명하는 해부학적 지점입니다. 내시경 관찰을 통해 옅은 분홍색 또는 분홍빛이 도는 식도 점막에서 더 어두운 빨간색 또는 주황색-노란색 위 점막으로 전환되는 것을 볼 수 있습니다. 상당한 양의 위 내용물이 존재하면 튜브 배치에 영향을 미칠 수 있습니다. 수술 전 6-8시간의 공복 기간을 시행하고 시술 전에 지속적인 위장 감압을 고려하는 것이 좋습니다. - 위 내부의 시야가 불분명해 보이면 NJ 튜브에 식염수(매번 10-20mL)를 주입하여 프론트 엔드 가이드 와이어 렌즈를 덮고 있는 장애물을 제거합니다.
- 튜브가 위 안에서 말리거나 구부러지면 NJ 튜브를 55-65cm 길이로 후퇴시키고 부드럽게 빼내면서 동시에 시각화된 가이드 와이어가 부드럽게 움직일 때까지 전진시킵니다.
참고: 레트로플렉스 뷰(retroflex view)와 같은 실시간 시각화 기술을 사용하여 튜브의 궤적과 움직임을 꼼꼼하게 관찰하여 시술 중 컬링을 감지하여 코일링을 감지합니다. 여기에는 위장관을 통한 튜브의 진행 상황을 모니터링하고 컬링을 나타낼 수 있는 편차나 고리를 기록하는 것이 포함됩니다. 필요한 경우 복부 X-레이를 통해 컬링의 존재를 확인할 수도 있습니다. - 지속적인 동적 육안 관찰 하에서 천천히 튜브 삽입을 계속하고 위 연동 운동에 적응하고 유문을 찾습니다.
- 유문을 찾지 못하면 시각화된 내시경 가이드 와이어를 일시적으로 철회하고 NJ 튜브의 길이를 55-65cm로 조정합니다. 환자를 오른쪽 측면 위치로 보조하고 약 100-200mL의 식염수/공기를 주입한 다음 시각화된 내시경 가이드 와이어를 다시 삽입합니다. 위장 점막을 통해 위치를 확인하고 적절하게 조정한 다음 천천히 삽입합니다.
- 유문이 확인되면 핸들을 돌려 튜브의 방향을 조정하고 더 정밀하게 유문을 통과할 수 있도록 합니다. 천천히 전진하는 동안 튜브의 위치와 방향을 지속적으로 관찰하고 최적의 탐색을 위해 필요에 따라 필요한 조정을 수행합니다.
- 튜브가 유문을 통과하여 십이지장으로 들어간 후 십이지장 점막의 전형적인 손가락 모양의 융모를 관찰합니다(그림 2C). 시각화된 내시경 가이드 와이어를 부드럽게 회전시키고 부분적으로 후퇴시키면서 동시에 튜브를 전진시키면서 물(약 20mL)을 주입하고(꼬임 방지를 위해) 천천히 삽입합니다.
참고: 물 주입 방법은 장 배출을 용이하게 하여 선명한 이미지를 얻습니다. 점막 손상을 방지하기 위해 십이지장 점막을 통해 위치를 확인합니다. - 카테터를 천천히 삽입하면서 십이지장 전구를 통해 진행하고 십이지장의 하강, 횡 및 상승 부분을 순서대로 계속 삽입합니다. 튜브 헤드를 제주눔 내부에 놓습니다.
- 튜브 배치가 완료되면 가이드 와이어 렌즈를 천천히 집어넣습니다.
- 튜브 배치를 확인하는 다른 방법
- 주사기를 사용하여 소화액을 흡입하고 색상과 부피를 관찰하고 pH 값을 측정합니다. 튜브 끝이 장 내강에 있는 경우 황금빛 노란색과 pH > 7.0인 <10mL의 액체를 예상하십시오. 튜브 끝이 위장에 있는 경우 >20mL의 액체가 < pH 5.0에서 연한 녹색, 투명, 무색 또는 갈색으로 나타날 수 있습니다.
참고: 이 방법은 배치 과정에서 반드시 필요한 것은 아닙니다. 또한 흡입된 유체의 pH는 약물 또는 영양 용액과 같은 요인의 영향을 받을 수 있습니다. - 공기를 부드럽게 주입하여 진공 테스트를 수행하고 흡입하여 음압을 생성합니다. 10mL의 공기를 주입하고 <5mL를 흡인하면 튜브가 유문을 통과했음을 나타냅니다.
알림: 팁이 벽과 접촉하면 결과에 영향을 줄 수 있습니다. - 복부 X-레이: 환자를 평평하게 눕히고 침대 옆에서 X-레이를 찍습니다. X-ray가 튜브의 경로를 시계 반대 방향 "C"자 모양으로 보여주면 튜브 팁이 십이지장 공동에 있는 것입니다.
- 주사기를 사용하여 소화액을 흡입하고 색상과 부피를 관찰하고 pH 값을 측정합니다. 튜브 끝이 장 내강에 있는 경우 황금빛 노란색과 pH > 7.0인 <10mL의 액체를 예상하십시오. 튜브 끝이 위장에 있는 경우 >20mL의 액체가 < pH 5.0에서 연한 녹색, 투명, 무색 또는 갈색으로 나타날 수 있습니다.
- 튜브 고정
- 환자의 코 피부가 손상되지 않은 경우 하이 리프트 플랫폼과 함께 지그재그 방법을 사용하십시오. 코 피부에 피부 손상이 있는 경우 하이 리프트 플랫폼으로 버터플라이 고정 방법을 수행합니다.
참고: NJ 튜브의 튜브 고정 및 간호 세부 사항에 대한 자세한 내용은 보충 파일 1을 참조하십시오.
- 환자의 코 피부가 손상되지 않은 경우 하이 리프트 플랫폼과 함께 지그재그 방법을 사용하십시오. 코 피부에 피부 손상이 있는 경우 하이 리프트 플랫폼으로 버터플라이 고정 방법을 수행합니다.
결과
임상 결과
이 연구에서는 ICU에 있는 총 19명의 중환자가 시각화 지침에 따라 NJ 튜브 삽입을 받았습니다. 연구 대상자 중 남성 12명(63.16%)과 여성 7명(36.84%)으로 평균 연령은 64.47세± 13.43세였다. 진단은 중증 폐렴(n=6, 31.58%), 패혈증(n=1, 5.26%), 심정지 소생술(n=1, 5.26%), 급성 췌장염(n=1, 5.26%), 만성폐쇄성폐질환의 급성 악화(n=3, 15.79%), 소뇌위축(n=1, 5.26%), 뇌출혈(n=4, 21.05%), 뇌경색(n=1, 5.26%), 외상성 뇌손상(두개골 기저부 골절 없음)(n=1, 5.26%), 의식 변화(n=15, 78.95%), 침습적 기계적 환기가 필요한 환자(n=18, 94.74%)였다(표 1). 중환자실 입원 시 이 환자들의 NUTRIC 점수는 6.68 ± 1.11이었다(표 1). 이 모든 환자들은 급성 위장 기능 장애를 보였으며 위식도 역류 및 흡인의 위험이 높았습니다.
앞서 언급한 방법을 사용하여 튜브 배치 성공률이 100%에 도달했습니다. 구체적으로, 첫 번째 튜브 삽입의 초기 성공률은 94.74%였으며, 두 번째 튜브 삽입에 성공한 사례가 한 번 있었습니다. 평균 삽입 시간은 11.21분 ± 6.44분이었습니다(표 2). 가장 흔한 장기 합병증은 우발적인 튜브 제거였다14. NJ 튜브를 사용하는 동안 실수로 튜브를 당긴 후 또는 삽입 중 위 내부에서 튜브가 감겨 있는 것이 의심되는 경우 복부 X-ray를 통해 튜브의 팁 위치를 확인합니다. 5명의 환자에서는 십이지장의 하행 부분에서 튜브 팁의 위치가 복부 X-ray를 통해 확인되었으며(그림 3), 나머지 사례는 직접 시각화를 통해 확인되었습니다. 합병증으로는 경미한 위장관 출혈이 있었다(1건, 대변에 피가 보이지 않고, 혈구가 없으며, 위액에서 잠혈 검사에서 양성 반응, 표 2). 위장관 천공 사례는 없었으며, 우발적으로 기도로 들어간 사례도 없었다(표 2).
최소 침습적 가시 튜브 삽입을 받은 환자의 경우, 튜브 삽입 과정에서 배치 전 수준에 비해 심박수(HR)와 호흡수(R)가 약간 증가했습니다(P < 0.05, 표 3). 평균 동맥압(MAP)은 통계적 차이 없이 완만한 증가를 보였다(P > 0.05, 표 3). 2주간의 경장 영양 지원 후, 이 환자들은 배치 전 수치에 비해 혈청 알부민 및 프리알부민 수치가 유의하게 상승했으며(P < 0.05, 표 3), 통계적으로 유의미한 차이를 보였다. 영양 지원 및 기타 포괄적인 치료 조치에 따라 환자들은 ICU 입원 수치에 비해 APACHE II 및 SOFA 점수26 이 유의하게 감소하여 통계적으로 유의미한 차이를 나타냈다(P < 0.05, 표 3). 이 환자들의 평균 입원 기간은 표 2± 같이 34.74일에서 20.38일이었다.
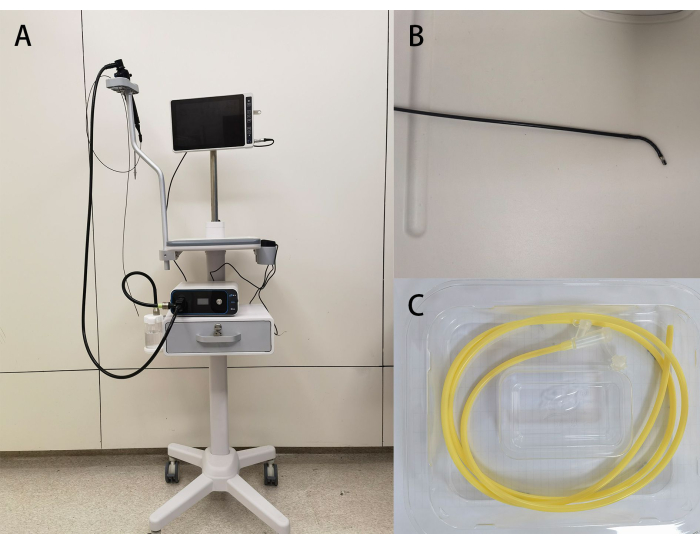
그림 1: 장치 이미지. (A) 의료용 내시경 이미지 프로세서의 개요; (B) 가이드 와이어 내시경의 조향 능력; (C) 동반되는 일회용 비관. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
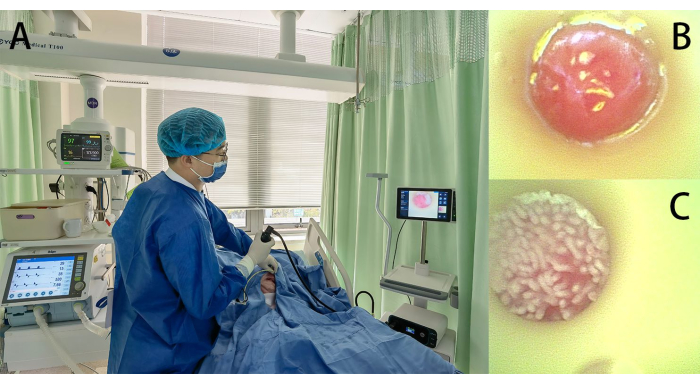
그림 2: 비관의 배치. (A) 작동 중 절차; (B) 가이드 와이어 내시경에 의해 포착된 위 점막의 내시경 이미지; (C) 가이드 와이어 내시경에 의해 포착된 소장 점막의 내시경 이미지로, 소장 융모의 존재를 드러냅니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 3: 복부 X-선 이미지. NJ 튜브 팁은 십이지장의 하강 부분에 위치하며 튜브의 코일 부분은 위에 있습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
| N=19, (평균값 ± SD) | |
| 특성 | |
| 나이(평균값 ± SD) | 64.47±13.43 |
| 섹스 번호 (%) | |
| 남성 | 12 (63.16) |
| 여성 | 7 (36.84) |
| 질병 번호 (%) | |
| 중증 폐렴 | 6 (31.58) |
| 패혈증 | 1 (5.26) |
| 증권 시세 표시기 | 3 (15.79) |
| 성공적인 심정지 소생술 | 1 (5.26) |
| 소뇌 위축증 | 1 (5.26) |
| 뇌출혈 | 4 (21.05) |
| 뇌경색 | 1 (5.26) |
| 외상성 뇌 손상(두개골 기저 골절 없음) | 1 (5.26) |
| 의식의 변화 | 15 (78.95) |
| 침습적 기계 환기가 필요한 환자 | 18 (94.74) |
| 의식 상태 no. (%) | |
| 혼수 | 15 (78.95) |
| 의식 | 4 (21.05) |
| NUTRIC 점수# | 6.68±1.11 |
표 1: 기준선에서 환자의 인구통계학적 및 임상적 특성. #NUTRIC 점수는 ICU 입원 시에만 평가됩니다. 약어: AECOPD = 만성 폐쇄성 폐 질환의 급성 악화, NUTRIC 점수 = 중증 질환에 대한 영양 위험 점수, 입원 기간(일) = ICU 모니터링 치료에 소요된 시간과 ICU를 떠난 후 일반 병동에서 보낸 시간의 합계, SD = 표준 편차; 평균값±표준 편차.
| N=19, (평균값 ± SD) | |
| 평균 삽입 시간(분) | 11.21 ± 6.44 |
| 초기 튜브 배치의 성공률 번호 (%) | 18 (94.74) |
| NJ 튜브 팁의 위치 번호 (%) | |
| 십이지장 전구 | 1 (5.26) |
| 십이지장의 내림차순 부분 | 3 (15.79) |
| 십이지장의 Transerse 부분 | 2 (10.53) |
| 십이지장의 오름차순 부분 | 5 (26.32) |
| 제주눔의 윗부분 | 8 (42.10) |
| *X-ray 번호 (%) | 5 (26.32) |
| 블리드 번호 (%) | 1 (5.26) |
| 위장 천공 번호 (%) | 0 (0) |
| 우발적으로 기도로 유입된 경우 no. (%) | 0 (0) |
| 입원 기간(일) | 34.74 ± 20.38 |
표 2: 초기 튜브 삽입의 성공률, 평균 삽입 시간, 합병증 비율 및 입원 비율. *X-ray: 복부 방사선 사진으로 NJ 튜브 끝의 위치가 확인된 환자 수. 약어: 입원 기간(일) = ICU 모니터링 치료에 소요된 시간과 ICU를 떠난 후 일반 병동에서 보낸 시간의 합계, SD = 표준 편차; 평균값±표준 편차.
| 카테터 삽입 전 | 카테터 삽입 중 | P-값 | |
| (n=19) | (n=19) | ||
| (평균값±SD) | (평균값±SD) | ||
| 지도 (mmHg) | 93.37±15.96년 | 96.39±11.67년 | 0.288 |
| 인사(bpm) | 83.11±15.61 | 92.21±14.92년 | 0.000 |
| 아르 자형(bpm) | 17.32±3.77 | 19.53±3.45초 | 0.009 |
| 카테터 삽입 전 | 카테터 삽입 후 | ||
| 알비 (g/L) | 27.10±5.05* | 34.51±5.08** | 0.000 |
| 프리알부민(mg/L) | 135.38±52.80* | 208.69±47.85** | 0.000 |
| 아파치 II 점수 | 20.26±5.05* | 10.84±4.15*** | 0.000 |
| SOFA 스코어 | 9.53±4.11* | 2.47±2.72*** | 0.000 |
표 3: 활력 징후, APACHE II 및 SOFA 점수, 실험실 결과. *ICU 입원 시. **2주에 경장 영양 요법. ICU에서 이송될 때. 심박수, 호흡수, 평균 동맥압, APACHE II 및 SOFA 점수, 혈청 알부민 및 혈청 프리알부민은 쌍 표본 t-테스트를 사용하여 통계 분석을 수행했습니다. 혈청 알부민의 정상 범위는 40-55g/L이고 혈청 프리알부민의 정상 범위는 200-430mg/L입니다. 약어: HR = 심박수, R = 호흡수, MAP = 평균 동맥압. APACHE II 점수 = 급성 생리학 및 만성 건강 상태 II 점수, SOFA 점수 = 순차적 장기 부전 점수, SD = 표준 편차.
보충 파일 1: NJ Tube의 간호 .NJ 튜브 간호에 대한 자세한 정보. 이 파일을 다운로드하려면 여기를 클릭하십시오.
보충 표 S1: NUTRIC 채점 시스템, APACHE II 및 SOFA 점수. 이 파일을 다운로드하려면 여기를 클릭하십시오.
토론
우리는 작은 시각화 도구를 사용하여 환자의 침대 옆에 NJ 튜브를 삽입했습니다. 시각화 방법을 채택하고 환자 위치를 조정함으로써 초기 튜브 삽입에 대해 94.47%의 성공률을 달성했습니다. 튜브를 삽입하는 데 걸린 평균 시간은 11.21분 ± 6.44분에 불과했습니다(표 2). 한 환자는 처음에는 삽관에 실패했으나 두 번째 시도 20분 전에 10mg의 메토클로프라마이드 근육 주사를 맞은 후 성공적으로 삽관을 했다(표 2).
최근 몇 년 동안 수많은 연구에서 경장 영양 지원에 다양한 방법과 기법이 적용되고 있음을 입증했습니다. 일부 연구에서는 비위관, NJ 튜브 및 위누공과 같은 특정 상황에서 다양한 유형의 튜브의 적용 가능성과 효과에 대해 논의했습니다 27,28,29. 중환자실 환자에서 위기능 장애가 자주 발생하여 위식도 역류 및 흡인의 위험이 높기 때문에 흡인성 폐렴이 발생하고 호흡 부전이 악화될 가능성이 높아집니다. 따라서 경장 영양에 대한 금기 사항이 없는 환자의 경우 NJ 튜브가 선호되는 옵션일 수 있습니다. 그러나 NJ 튜브를 정확한 위치에 효과적으로 배치하는 것은 임상 의료 서비스 제공자에게 어려움을 줍니다.
최근의 발전은 경장 영양 튜브 배치의 정밀도와 안전성을 향상시키기 위해 초음파 유도, 자기 유도, 경피 천자 유도 및 내시경 유도 방법과 같은 기술을 도입했습니다 16,29,30,31. 마그네틱 팁 가이드는 NJ 튜브 배치에 사용되며, 자기 팁 가이드와이어를 사용하여 튜브를 위장관을 통해 소장으로 이동합니다15. 그러나 모든 의료 시설에서 사용할 수 있는 것은 아닌 자기 이미징 장비에 대한 요구 사항으로 인해 보편적인 적용 가능성이 제한됩니다. 환자 근처에 자성 물체가 있으면 정확한 튜브 배치를 방해할 수도 있습니다32. 병상 초음파는 뉴저지 튜브 확인에 유용하다33. 그러나 해부학적 변형 또는 비만이 있는 환자에서는 문제가 발생할 수 있으며, 이는 정확한 튜브 팁 시각화에 영향을 미칠 수 있습니다. 위장관의 위 내용물이나 공기는 초음파 정확도를 저해하여 튜브 삽입 확인을 복잡하게 만들 수 있다34.
NJ 튜브가 자기 헤드에 의해 유도되든 초음파 국소화로 배치되든 유문을 빠르고 정확하게 탐색하는 것은 여전히 어려운 과제로 남아 있습니다. 이 프로세스에는 여전히 경험이 풍부하고 고도로 숙련되었으며 인내심 있는 수술 의사가 필요합니다. 성공적인 배치에는 일반적으로 상당한 시간이 소요되며, 복잡한 해부학적 구조를 가진 환자의 경우 성공적인 배치를 달성하는 것이 특히 어려울 수 있습니다. 또한 소장에서의 존재와 같은 튜브 팁의 특정 위치를 정확하게 결정하기 위해 침상 X-선과 같은 추가 방사선 검사가 여전히 필요할 수 있습니다. 튜브 팁이 소장에 있지 않거나 너무 깊숙이 위치한 경우 튜브 팁의 위치를 변경하거나 조정해야 하며 반복적인 방사선 검사가 필요한 경우가 많습니다. 이로 인해 환자는 여러 번의 X선 노출에 노출되어 의료 비용이 증가합니다. 이 연구에서는 내시경을 통해 소장 점막을 직접 시각화하여 튜브 팁의 위치를 즉시 확인할 수 있었습니다. NJ 튜브를 사용하는 동안 실수로 튜브를 당긴 후 또는 삽입 중 위 내부에서 튜브가 감겨 있는 것이 의심되는 경우, 일부 환자를 대상으로 침대 옆 복부 X-선 검사를 통해 튜브 팁의 위치를 추가로 검증했습니다(n = 5, 표 2). 결과적으로, 이 연구에서 시각적 방법을 사용하여 삽입한 NJ 튜브는 추가 이미징 검사의 필요성을 제거했습니다.
내시경 유도 NJ 튜브 삽입은 내시경을 사용하여 튜브를 소장으로 안내하는 고급 절차입니다35. 이 방법은 일반적으로 까다롭거나 복잡한 해부학적 구조를 가진 환자 또는 이전에 NJ 튜브 삽입 시도가 실패한 경험이 있는 환자를 위해 예약되어 있습니다. 그럼에도 불구하고 소화용 내시경은 직경이 더 크고 입을 통해서만 주입할 수 있어 환자의 불편함을 증가시킬 수 있습니다. NJ 튜브의 내시경 유도 배치는 표준 위내시경 검사에 비해 시간이 더 많이 소요되는 절차인 경우가 많습니다. 어떤 경우에는 전체 배치 과정에서 전신 마취가 필요할 수 있습니다. 이 연구에서는 전체 직경이 2mm에 불과한 일체형 가이드와이어와 렌즈를 특징으로 하는 소형 내시경을 활용하여 비강 횡단 접근을 용이하게 하여 환자의 불편함을 줄이는 데 기여했습니다. 배치 과정에서 환자의 심박수와 호흡수는 약간 증가했지만 평균 동맥압은 통계적으로 유의하지 않은 경미한 증가가 있었습니다(P > 0.05, 표 3). 또한, 이 연구의 모든 환자는 침대 옆에서 성공적으로 삽관을 하여 중증 환자를 이송할 필요가 없고 관련 위험을 완화했습니다.
기존 내시경과 유사하게 이 연구에 사용된 미니 내시경은 스티어링 기능을 갖추고 있습니다. 이 설계는 복잡한 해부학적 구조를 가진 환자에서도 NJ 튜브를 성공적으로 배치할 수 있도록 합니다. "through-the-scope" 방법은 내시경의 생검 채널을 통해 작은 영양 튜브(7F 또는 10F)를 제주눔으로 통과시킨 다음 내시경을 빼내고 튜브를 제자리에 두는 것입니다. 관을 구강에서 비강으로 옮긴 후 절차가 완료됩니다. Bosco 등[36 ]은 이 기법으로 90%의 성공률을 보였으며 평균 시술 시간은 19분이었다고 보고했습니다. 그러나 이 방법에는 제한 사항이 있습니다. 직경이 작은 튜브만 생검 채널에 들어갈 수 있습니다. 10F "through-the-scope" NJ 튜브를 통과하기 위한 치료용 상부 내시경의 요구 사항 외에도 구강-코 이식도 수행해야 합니다. 이 연구에서는 14F NJ 튜브를 삽입할 수 있었습니다. NJ 튜브의 직경이 더 크면 임상 응용 분야에서 더 다양한 영양 유체를 사용할 수 있으며 막힘 위험도 줄일 수 있습니다.
경피적 내시경 위루관(PEG-J)은 경구 또는 위 영양 공급을 견딜 수 없는 환자에게 경장 영양을 공급하는 데 사용되는 방법이다37. PEG-J 기법은 경장 영양 전달에 효과적이지만 주의가 필요한 단점이 있습니다. PEG-J 튜브를 삽입하려면 상당한 수준의 전문 지식과 경험이 필요하며, 모든 환자에게 적합하지 않을 수 있는 침습적 시술입니다38. 또한 배치 과정이 길어집니다. 이와는 대조적으로, 우리의 방법은 상대적으로 짧은 기간과 최소한의 외상으로 효율적으로 완료되어 의식이 있는 환자에게 특히 적합합니다. 또한, 위장 천공의 증거와 우발적인 기도 진입 사례는 연구 대상자에게서 발견되지 않았습니다. 경미한 위출혈이 발생한 사례는 단 한 건에 불과했다(표 2).
본 연구에서는 경장 영양 지원 요법 및 기타 종합적인 관리 치료를 받은 후 중환자실 입원 시 환자의 APACHE II 및 SOFA 점수가 중환자실 입원 시 점수에 비해 현저히 감소했다(표 3). 평균 입원 기간은 표 2와 같이 34.74일± 20.38일이었다. 이는 시각화 유도 튜브 배치 방법을 통해 경장 영양 지원 요법을 조기에 시작할 수 있어 환자의 상태와 예후를 개선할 수 있음을 보여줍니다.
그럼에도 불구하고 이 연구의 한계를 인정하는 것이 중요하며, 특히 마이크로 내시경의 가이드와이어 렌즈로 선명한 이미지를 얻으려면 NJ 튜브의 헤드 엔드가 열린 상태로 유지되어야 합니다. 결과적으로, 튜브 삽입을 시작하기 전에 가이드와이어 렌즈 헤드 엔드와 카테터의 위치를 조정해야 합니다. 이 조정은 가이드와이어 렌즈 헤드 엔드가 카테터를 능가하는 것을 방지하여 위장 점막 손상, 출혈 및 천공의 위험을 완화하는 데 필수적입니다. 향후 연구에서는 이미지 선명도를 개선하고 관련 위험을 완화하기 위해 가이드와이어 렌즈와 NJ 튜브의 설계를 개선할 계획입니다.
요약하면, 설명된 방법은 간단하고 안전하며 효율적이어서 병상에서 신속하게 구현하는 데 도움이 되며 특히 ICU의 중증 환자에게 적합합니다. 이 시각화된 방법은 중환자실 환자의 NJ 튜브 삽입을 위한 유망한 대안을 제공하여 성공률을 높이고 환자의 불편함을 최소화합니다. 기술을 최적화하고 잠재적인 한계를 해결하기 위해 설계에 대한 추가 개선과 추가 연구가 필요합니다.
공개
저자는 이해 상충이 없음을 선언합니다.
감사의 말
이 연구는 병원의 중환자 치료 의학과와 정형외과의 다양한 동료들의 지원을 받았습니다. 이 연구는 저장성 의료 및 보건 과학 기술 프로그램(2019RC170)과 저장성 교육부(Y201941857)의 일반 과학 연구 프로젝트로부터 외부 자금을 지원받았습니다.
자료
| Name | Company | Catalog Number | Comments |
| Disposable nasogastrointestinal tube | JiangSu Jianzhiyuan Medical Instrument Technology Co., Ltd. | W -4.7-1400mm -4.7-1400mm | The outer diameter of the guide tube is 4.7 mm. |
| Lidocaine Hydrochloride Gel | Manufacturers are not limited | For local anaesthesia | |
| Medical Endoscopy Image Processor | JiangSu Jianzhiyuan Medical Instrument Technology Co., Ltd. | HD1080 | The diameter of the guide wire lens is 2 mm. |
| Metoclopramide Dihydrochloride Injection | Manufacturers are not limited | Promote gastric motility | |
| SPSS 20.0 software | International Business Machines Corporation | Statistical analysis | |
| Sterile liquid paraffin oil | Manufacturers are not limited | For catheter lubrication |
참고문헌
- van Zanten, A. R. H., De Waele, E., Wischmeyer, P. E. Nutrition therapy and critical illness: practical guidance for the ICU, post-ICU, and long-term convalescence phases. Crit Care. 23 (1), 368(2019).
- Lambell, K. J., Tatucu-Babet, O. A., Chapple, L. A., Gantner, D., Ridley, E. J. Nutrition therapy in critical illness: a review of the literature for clinicians. Crit Care. 24 (1), 35(2020).
- Zaher, S. Nutrition and the gut microbiome during critical illness: A new insight of nutritional therapy. Saudi J Gastroenterol. 26 (6), 290-298 (2020).
- Ozdemir, U., Yildiz, S., Aygencel, G., Turkoglu, M. Ultrasonography-guided post-pyloric feeding tube insertion in medical intensive care unit patients. J Clin Monit Comput. 36 (2), 451-459 (2022).
- de-Aguilar-Nascimento, J. E., et al. ACERTO guidelines of perioperative nutritional interventions in elective general surgery. Rev Col Bras Cir. 44 (6), 633-648 (2017).
- Jia, Z. Y., et al. Screening of nutritional risk and nutritional support in general surgery patients: a survey from Shanghai, China. Int Surg. 100 (5), 841-848 (2015).
- Wan, B., Fu, H., Yin, J. Early jejunal feeding by bedside placement of a nasointestinal tube significantly improves nutritional status and reduces complications in critically ill patients versus enteral nutrition by a nasogastric tube. Asia Pac J Clin Nutr. 24 (1), 51-57 (2015).
- Jiang, W., et al. Early enteral nutrition in neonates with partial gastrectomy: a multi-center study. Asia Pac J Clin Nutr. 25 (1), 46-52 (2016).
- McClave, S. A., et al. Guidelines for the provision and assessment of nutrition support therapy in the adult critically ill patient: Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N). JPEN J Parenter Enteral Nutr. 40 (2), 159-211 (2016).
- Corrigan, M. L., Bobo, E., Rollins, C., Mogensen, K. M. Academy of Nutrition and Dietetics and American Society for Parenteral and Enteral Nutrition: Revised 2021 standards of practice and standards of professional performance for registered dietitian nutritionists (competent, proficient, and expert) in nutrition support. Nutr Clin Pract. 36 (6), 1126-1143 (2021).
- Caulfield, K. A., Page, C. P., Pestana, C. Technique for intraduodenal placement of transnasal enteral feeding catheters. Nutrition in Clinical Practice. 6 (1), 23-26 (1991).
- Blaser, A. R., Starkopf, J., Kirsimagi, U., Deane, A. M. Definition, prevalence, and outcome of feeding intolerance in intensive care: a systematic review and meta-analysis. Acta Anaesthesiol Scand. 58 (8), 914-922 (2014).
- Lai, C. W., Barlow, R., Barnes, M., Hawthorne, A. B. Bedside placement of nasojejunal tubes: a randomised-controlled trial of spiral- vs straight-ended tubes. Clin Nutr. 22 (3), 267-270 (2003).
- Wiggins, T. F., DeLegge, M. H. Evaluation of a new technique for endoscopic nasojejunal feeding-tube placement. Gastrointest Endosc. 63 (4), 590-595 (2006).
- Taylor, S. J., Karpasiti, T., Milne, D. Safety of blind versus guided feeding tube placement: Misplacement and pneumothorax risk. Intensive Crit Care Nurs. 76, 103387(2023).
- Mumoli, N., et al. Bedside abdominal ultrasound in evaluating nasogastric tube placement: A multicenter, prospective, cohort study. Chest. 159 (6), 2366-2372 (2021).
- Hillard, A. E., Waddell, J. J., Metzler, M. H., McAlpin, D. Fluoroscopically guided nasoenteric feeding tube placement versus bedside placement. South Med J. 88 (4), 425-428 (1995).
- Cresci, G., Martindale, R. Bedside placement of small bowel feeding tubes in hospitalized patients: a new role for the dietitian. Nutrition. 19 (10), 843-846 (2003).
- Patrick, P. G., Marulendra, S., Kirby, D. F., DeLegge, M. H. Endoscopic nasogastric-jejunal feeding tube placement in critically ill patients. Gastrointest Endosc. 45 (1), 72-76 (1997).
- Schwab, D., et al. Endoscopic placement of nasojejunal tubes: a randomized, controlled, prospective trial comparing suitability and technical success for two different tubes. Gastrointest Endosc. 56 (6), 858-863 (2002).
- Fanara, B., Manzon, C., Barbot, O., Desmettre, T., Capellier, G. Recommendations for the intra-hospital transport of critically ill patients. Crit Care. 14 (3), 87(2010).
- Neumann, D. A., DeLegge, M. H. Gastric versus small-bowel tube feeding in the intensive care unit: A prospective comparison of efficacy. Crit Care Med. 30 (7), 1436-1438 (2002).
- Levy, H. Nasogastric and nasoenteric feeding tubes. Gastrointest Endosc Clin N Am. 8 (3), 529-549 (1998).
- Dranoff, J. A., Angood, P. J., Topazian, M. Transnasal endoscopy for enteral feeding tube placement in critically ill patients. Am J Gastroenterol. 94 (10), 2902-2904 (1999).
- Rahman, A., et al. Identifying critically-ill patients who will benefit most from nutritional therapy: Further validation of the "modified NUTRIC" nutritional risk assessment tool. Clin Nutr. 35 (1), 158-162 (2016).
- Mutchmore, A., Lamontagne, F., Chasse, M., Moore, L., Mayette, M. Automated APACHE II and SOFA score calculation using real-world electronic medical record data in a single center. J Clin Monit Comput. 37 (4), 1023-1033 (2023).
- Zanley, E., et al. Guidelines for gastrostomy tube placement and enteral nutrition in patients with severe, refractory hypoglycemia after gastric bypass. Surg Obes Relat Dis. 17 (2), 456-465 (2021).
- Chen, M. C., Chao, H. C., Yeh, P. J., Lai, M. W., Chen, C. C. Therapeutic efficacy of nasoenteric tube feeding in children needing enteral nutrition. Front Pediatr. 9, 646395(2021).
- Wang, L., Tian, Z., Liu, Y. Nasoenteric tube versus jejunostomy for enteral nutrition feeding following major upper gastrointestinal operations: a meta-analysis. Asia Pac J Clin Nutr. 26 (1), 20-26 (2017).
- Liu, Z., et al. Evaluation of ultrasound-guided Freka-Trelumina enteral nutrition tube placement in the treatment of acute pancreatitis. BMC Gastroenterol. 20 (1), 21(2020).
- Chen, Y., et al. A multifaceted comparative analysis of image and video technologies in gastrointestinal endoscope and their clinical applications. Front Med (Lausanne). 10, 1226748(2023).
- Roy, S., Santosh, K. C. Analyzing overlaid foreign objects in chest X-rays-clinical significance and artificial intelligence tools. Healthcare (Basel). 11 (3), 308(2023).
- Ferraboli, S. F., Beghetto, M. G. Bedside ultrasonography for the confirmation of nasogastric tube placement: agreement between nurse and physician. Rev Gaucha Enferm. 43, 20220211(2022).
- Valla, F. V., Cercueil, E., Morice, C., Tume, L. N., Bouvet, L. Point-of-care gastric ultrasound confirms the inaccuracy of gastric residual volume measurement by aspiration in critically ill children: GastriPed Study. Front Pediatr. 10, 903944(2022).
- Lu, G., et al. Endoscopic- versus x-ray-guidance for placement of nasojejunal tubes in critically ill patients: a systematic review and meta-analysis of randomized controlled trials. Am J Transl Res. 14 (4), 2134-2146 (2022).
- Bosco, J. J., et al. A reliable method for the endoscopic placement of a nasoenteric feeding tube. Gastrointest Endosc. 40 (6), 740-743 (1994).
- Zafar, M., et al. Complexities of long-term care with gastro-jejunal (GJ) feeding tubes and enteral migration during COVID-19 pandemic times: A case report. Cureus. 14 (8), e27870(2022).
- Hawk, H., Valdivia, H. Bedside methods for transpyloric feeding tube insertion in hospitalized children: A systematic review of randomized and non-randomized trials. JPediatr Nurs. 60, 238-246 (2021).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유