Method Article
プロトタイプ小動物X線CTOによるレトロスペクティブ心臓ゲーティング
要約
私たちは、私たちの研究機関で設計および構築されたプロトタイプの小動物X線X線コンピューター断層撮影(CT)スキャナーであるCrumpCATの内因性レトロスペクティブ心臓ゲーティング法の包括的な説明を提供します。
要約
CrumpCATは、当研究所で開発された小動物用X線CTスキャナーの試作機です。最大フレームレートが29HzのCMOS検出器や、50kVpから80kVpの範囲のエネルギーを持つ同様のタングステンX線源は、市販の前臨床X線CT装置で広く使用されています。これにより、これらの検出器はマウスの高い心拍数(~600拍/分)のゲーティングには適していないという一般的に認識されている知恵にもかかわらず、説明された研究は他の機関に非常に関連性があります。このスキャナーは、中分解能(200μm)および高分解能(125μm)のイメージング、透視法、レトロスペクティブ呼吸ゲーティング、レトロスペクティブ心臓ゲーティングを特徴としており、反復またはフィルタリングされた投影画像再構成が可能です。これらの特徴の中で、心筋ゲーティングは、呼吸や心臓の動きによって引き起こされる画像のぼやけを効果的に排除するため、 in vivoでの心機能の研究に最も有用な特徴です。
ここでは、 in vivo 心機能および構造解析の研究を進めることを目的とした、前臨床の内因性レトロスペクティブ心筋同期CTイメージングの方法について説明します。心拍ゲーティング法は、最短の実用露光時間(~20 ms)で多数の投影を取得し、生の投影シーケンスの時間的変化から呼吸信号と心臓信号を遡及的に抽出します。これらの信号は、呼吸周期の高運動速度吸気フェーズに属する投影を拒否し、残りの投影を12のグループに分割し、それぞれが心周期の1つのフェーズに対応するために使用されます。各グループは、反復的な方法を使用して独立して再構築され、各心相の体積画像が生成され、4次元(4D)データセットが得られます。
これらの位相画像は、まとめてまたは個別に分析できるため、心機能の詳細な評価が可能になります。プロトタイプスキャナーの心臓ゲーティング機能の両方のアプローチの有効性を、代表的な in vivo イメージング結果を通じて実証しました。
概要
小動物研究では、非侵襲的なイメージングモダリティの組み合わせが採用されることが多く、X線コンピュータ断層撮影法(CT)は、その成熟度、費用対効果、速度1,2、および陽電子放出断層撮影法(PET)2,3や単一光子放出型コンピュータ断層撮影法(SPECT)2,4などの他のモダリティと並んで補完的な情報を提供する能力により、有力な選択肢となっています.しかし、他のイメージング技術と同様に、CTは心臓の鼓動や呼吸によって引き起こされる生理的な運動アーチファクトの影響を受けやすく、ぼやけを引き起こし、研究の精度を制限します。
この制限に対処するために、ゲーティング5、6、7、8と呼ばれる手法を使用して、データ取得を心筋または呼吸周期(またはゲート)の特定のフェーズと同期させることで、呼吸および心臓の動きのぼやけを軽減できます。これを達成するための1つのアプローチは、プロスペクティブゲーティング3,6として知られており、動物にセンサーを取り付けて、互換性のあるスキャナーにリアルタイムのゲーティング信号を提供することを含みます。この方法は効果的ですが、特にマウスなどの小動物の胸部や足にセンサーを取り付ける場合、労働集約的で時間がかかるため、研究の規模が制限されます。あるいは、内因性レトロスペクティブゲーティング7,9,10,11は、センサを使用せずに時系列データを取得することを含むが、心周期または呼吸周期における位相に基づいて結果を遡及的にソートすることを可能にするデータの特徴を特定することによって行われる。このアプローチでは、プロスペクティブゲーティングに匹敵する結果が得られますが、追加のハードウェアやパルスセンサーの取り付けに伴う労力は必要なく、したがって実験プロトコルが大幅に簡素化されます。
前臨床心臓CTイメージングの方法では、内因性レトロスペクティブゲーティングを利用して、連続するフレーム間で最も顕著な変化を示すX線投影領域の振幅変動から呼吸および心臓周期を抽出します。このプロセスを容易にするために、マウスの胸部テンプレートは、相互情報量12を用いて第1の後前方投影に共登録される。テンプレートが配置されると、横隔膜の近くのウィンドウのピクセル強度を合計して代理呼吸信号を生成し、心筋近くのピクセル強度を合計して代理心筋信号を導き出します。次に、これらの信号は時間領域でバンドパスフィルタリングされ、データセット内の各フレームには、呼吸期と心筋の位相に基づいて小数部の位相番号(0 から 1)が割り当てられます。これにより、位相値に従って投影を選択または拒否できます。通常、呼吸周期の終了-呼気期(0.15≤期<0.85)に対応するフレームは保持されますが、動きが最も顕著な吸気期のフレームは破棄されます。残りのフレームは、12の心相にグループ化され、各々は心周期の1/12(0.083)を表し、反復法(Ordered Subset Expectation Maximization[OSEM])13,14を用いて3D画像に再構成される。全体のプロセスを図 1 にまとめます。
プロトコル
動物実験プロトコルは、カリフォルニア大学ロサンゼルス校(UCLA)の施設動物管理および使用委員会によって審査され、承認されました。このプロトコルでは、C57BL/6Jマウス(8週齢、雄、24-26g)を使用しました。この研究で使用したCTスキャナーは、前臨床研究のために私たちの研究機関で開発されたプロトタイプであるCrumpCAT(図2)であり、取得および再構成プロトコルを最適化するために必要な制御と柔軟性を提供します。この方法は、麻酔をかけたマウスの心拍数が600拍/分以下で、呼吸数が20〜180呼吸/分であると仮定しています15。
1. 機器の設定
- X線源を50kVpのピーク電圧で200μAの連続電流で運転します。
- X 線カメラのピクセル ビニングを 2 に設定し、露光時間を実用最短の値 (露光時間 20 ミリ秒と読み取り時間 14 ミリ秒で、合計サンプリング時間 34 ミリ秒) に設定します。
注: ビニングなしオプション (ビニング 1) はフレーム レートが遅いため、ゲート集録には使用できません。 最大フレームレート は約 30フレーム/秒です。
2.動物の調理
- 酸素とイソフルランガスの混合物を2.0%濃度でマウスに麻酔します。
- CTイメージングの前に動物を10分間麻酔下に置いて、バイタルサインが安定していること、およびスキャン中の体の動きを避けるために動物がリラックスしていることを確認します。マウスの麻酔の深さは、指の爪で足の指の間のウェビングをしっかりとつまむときのつま先つまみ反射の欠如によって判断します。
- 心腔を視覚化するための心電図イメージングでは、CTイメージングの直前に尾静脈から100μLのCT造影剤を静脈内注射します(図3A)。
- 麻酔をかけたマウスをCTイメージングチャンバー内に置きます(図3B)。
3. データ取得
- CrumpCATソフトウェアの電源を入れます。
- 高分解能(125 μm、ビニング1)のノンゲートCTイメージング(図4A)
- ユーザーインターフェースにスタディIDを入力します。
- [プロトコル]ドロップダウンメニューで[マウス高解像度]を選択します。
- ユーザーインターフェースの「スキャン」ボタンをクリックすると、露光時間が80ms/プロジェクションで720個のプロジェクションを取得できます。
- 中分解能(200 μm、ビニング2)のノンゲートCTイメージング(図4B)
- ユーザーインターフェースにスタディIDを入力します。
- [プロトコル]ドロップダウンメニューで[マウス標準]を選択します。
- ユーザーインターフェースの「スキャン」ボタンをクリックすると、露光時間が100ms/プロジェクションで720のプロジェクションを取得できます。
- ゲートCTイメージング(200 μm、ビニング2)(図4C)
- ユーザーインターフェースにスタディIDを入力します。
- 「プロトコル」ドロップダウンメニューで「Cardiac Gating」を選択します。
- ユーザーインターフェースの「スキャン」ボタンをクリックし、露光時間20ms/プロジェクションで21,600個のプロジェクションを取得します。
4. データの前処理
注:前処理手順は、ゲート式集録の場合にのみ必要です。これらの手順はすべて、再構築ソフトウェアによって自動的に実行され、オペレーターの介入は必要ありません。
- 信号抽出
- 胸部テンプレートの共レジストレーションでは、肋骨、心臓、肺、肝臓を有するマウスの胸部を粗く表現した小さな画像(テンプレート)を、投影とテンプレートとの間の相互情報量12 を最大化して、最初のX線投影に自動的に共登録させる(図5)。
注: テンプレートに対しては平行移動操作のみが実行され、同時登録されたテンプレートは、すべての投影法で関心領域 (ROI) を特定するために使用されます。 - 呼吸信号の抽出では、各投影のROI-1内のピクセル強度を合計することにより、横膜と生成される呼吸信号を表す長方形のROI(ROI-1)をテンプレートで指定できます(図5)。
- 心電線の抽出では、心臓の近くのテンプレートで 2 つ目の四角形 ROI(ROI-2)を指定し、各投影法の ROI-2 のピクセル強度を合計して心電図を生成します(図 5)。
注: 胸部テンプレートは、信号抽出に使用する画像の行と列 (ウィンドウ) を識別するために、最初の投影でのみ共登録されます。その窓は、動物が適度に中央に配置されている限り、すべての投影を包含するのに十分な幅があり、それは私たちの動物用ベッド16を使用する場合の場合である。
- 胸部テンプレートの共レジストレーションでは、肋骨、心臓、肺、肝臓を有するマウスの胸部を粗く表現した小さな画像(テンプレート)を、投影とテンプレートとの間の相互情報量12 を最大化して、最初のX線投影に自動的に共登録させる(図5)。
- バンドパスフィルター
- 時間領域17 でカットオフ周波数が異なる 2 つの Sinc 関数 (以下で説明するように、周波数領域のローパス フィルターに対応する) を組み合わせてバンドパス フィルターを生成できるようにします。
- ソフトウェアで、[300, 600] min-1 の周波数帯域を使用して、心信号にバンドパスフィルタを適用します(図6A)。
注:フィルタリングされていない心臓信号(図6B)には、呼吸運動による大きな寄与がまだ含まれています。 - 同様に、呼吸信号を [20, 300] min-1 の周波数帯域を使用してフィルタリングします。高次高調波は、単に正弦波ではなく、吸気と呼気という2つの主要なフェーズをより明確に識別する信号を生成するために保持されます。
注:この時点で、呼吸信号と心臓信号の両方を容易に補間し、分数位相数を計算する目的で時間の連続関数と見なすことができます。
- フェーズの割り当て
- ソフトウェアに、信号の最初の導関数のゼロクロッシングを見つけることにより、各サイクル(呼吸器または心臓)の開始を識別させます。各ゼロクロッシングは信号の最大値に対応し、新しいサイクルの開始と前のサイクルの終了を示します。例については、 図 7 の呼吸信号を参照してください。
- 小数位相値 (0 から 1 の間) を 2 つの信号 (呼吸器または心臓) のそれぞれの各投影に割り当てることができます。
注: 定義上、開始点の小数位相値は 0 (現在のサイクルの場合) または 1 (前のサイクルの場合) です。
- 選択マスク
- 12 個のバイナリ マスク (心臓フェーズごとに 1 つ) を作成して、各フェーズに属する投影を選択します。各マスクには、0 または 1 の 21,600 エントリ (投影ごとに 1 つ) が含まれており、それぞれその投影を拒否または保持します。
- マスク (位相) ごとに、プロジェクションが保持 (1) されるか破棄 (0) されるかをソフトウェアが小数フェーズ番号に従って示していることを確認します。フェーズ 0 の場合、区間 [0, 1/12] に心筋フェーズ値を持つ投影が保持されます。フェーズ 1 では、間隔 [1/12、2/12] の心相値が保持されます。
- 各マスク(フェーズ)について、呼吸フェーズが0.15未満または0.85より大きい投影は、最大の動きを持つ吸気フェーズに属しているため、拒否されることに注意してください(マスクの0)(図8A)。 図8B は、最初の2秒間の予測への心臓相の割り当てを示しています。
注:この選択プロセスでは、フェーズごとの投影数が1,800±194と比較的一定であったため、有意なバイアスは導入されませんでした。
5. 画像の再構成
- ノンゲートCTスキャンの場合、Shepp-LoganフィルターとFilteredバックプロジェクション(Feldkamp18)アルゴリズムを使用して、中分解能(200 μm)または高分解能(125 μm)で画像を再構成します。
- 心同期CTスキャンの場合、反復OSEMアルゴリズム13を使用して、12のサブセットと8回の反復を使用して、特定のフェーズに寄与する選択された投影のみを考慮に入れて、各心臓フェーズ画像を再構築します(フェーズ選択バイナリマスクで示されているように)。
- ノイズを減らすには、時間次元 (つまり、画像全体) に再構成後メディアン フィルターを適用し、空間次元 (σ = 38 μm) に軽い 3D ガウス フィルターを適用します。
注:呼吸器同期画像再構成の場合は、すべての心相を不明瞭に使用してください。梁硬化補正(水質補正)は、すべての再構成に適用されます。
6. 画像評価と左心室(LV)容積定量化
- Amide19 などのDICOMビューアでCT画像を開きます(図9A)。
- CT値(ハウンズフィールドユニット[HU]で測定)の範囲を[-500、500]に設定して、可視画像のコントラストを強化します(図9A)。
- 画質評価
- 石灰化領域の ROI を描画します (これは、CT 値が最大 HU 値の 85% 以上の最大値の周囲の領域として定義されます (図 9B)。
- コントラスト対ノイズ比(CNR)20,21を指標として使用して、画像品質と、小さな石灰化などの小さな構造を識別する能力を評価します。
 ,
,
ここで、 I と σ は、領域の平均強度と標準偏差を表します: 石灰化 (下付き文字 C) または背景 (下付き文字 B)。
- 左心室容積の定量化
- 3DフリーハンドROIを描画して、各フェーズのLVを特定します(図10A)。
- しきい値CT値が730HUのボクセルを計算することにより、LVボリュームを定量化します(図10B)。LV ボリュームのプロットを 図 10C に示します。
注: CT 値のしきい値は絶対値ではありません。使用する造影剤、動物の大きさ、菌株、健康状態、注射からCT撮影までの時間によって異なります。Amideは当研究所で開発されたフリー配布ソフトウェアですが、それ以外にもより高度な画像ビューア(ORS Dragonfly22など)が用意されています。
結果
まず、マウス(雄、30-32g)の心石灰化を視覚化するために、非ゲートCT画像とゲートCT画像を比較しました。心臓石灰化のマウスモデルは、前述のように、心臓組織の急速な凍結融解(凍結損傷)によって心臓損傷を誘発することによって作成された23。ノンゲートCTイメージングプロトコルでは、高解像度(125μm、ビニング1)画像(図11A)で心臓の石灰化がより明確に特定されました。CNRは、中解像度(200 μm、ビニング2)および高解像度(125 μm、ビニング1)の画像でそれぞれ3.2±0.3および4.±0および0.2でした。ゲート画像(図11B)では、CNRは4.2 ± 0.1(呼吸器同期のみ)、5.2 ± 0.4(呼吸器同期および心臓同期)でした。したがって、呼吸ゲーティングは、高解像度画像よりもわずか 5% の改善しかもたらさなかった(CNR 4.2 対 4.0)。対照的に、心ゲーティングは30%の改善をもたらしました(5.2対4.0)。
次に、レトロスペクティブ心筋同期CTイメージング法を使用して、C57BL/6Jマウスの心周期中のLV容積を視覚化および定量化しました。心周期中のLVボリュームの変化をより明確にするために、短いビデオとしてのループを 補足ビデオS1で見つけることができます。心周期中、収縮期末のLV容積は平均14±4 mm3であったが、拡張期末のLV容積は平均33 ± 7 mm3であった。計算された駆出率は平均60±4%でした。 図10C に、3匹のマウスのLVボリュームプロットを示します。さらに、私たちのレトロスペクティブ心臓同期CTイメージング法は、急性虚血性心損傷のマウスモデルにおける梗塞後心機能障害の非侵襲的モニタリングに有用です24。
さらに、動物の心拍数は315〜425拍/分、呼吸数は25〜50呼吸/分でした。生の投影から抽出された呼吸信号と心臓信号の抜粋を 図12に示します。生の心筋信号は、呼吸信号よりも振幅が小さく、呼吸信号の一部を含んでおり、後でバンドパスフィルターによって除去されます。 補足ビデオS1 は、心臓の鼓動を示し、心臓の状態を定性的に評価します。

図1:心臓ゲーティングのグラフィカルな要約。 略語:LV =左心室;ROI = 関心領域。 この図の拡大版を表示するには、ここをクリックしてください。

図2:CrumpCATとその主要コンポーネントの図。略語:CMOS =相補型金属酸化物半導体。 この図の拡大版を表示するには、ここをクリックしてください。

図3:動物の調製((A)マウスに造影剤を注入し、(B)動物16のスキャンに使用した37°C加熱マウスチャンバー。この図の拡大版を表示するには、ここをクリックしてください。

図4:CrumpCATソフトウェアのユーザーインターフェース (A)高解像度(125 μm、ビニング1)のノンゲートCTイメージングのユーザーインターフェース設定。(B)中分解能(200μm、ビニング2)のノンゲートCTイメージングのユーザーインターフェース設定。(C)ゲートCTイメージングのユーザーインターフェース設定(200μm、ビニング2)。スキャナーを操作するには、(1)検査番号を入力し、(2)CTイメージングプロトコルを選択し、(3) スキャン ボタンを押す必要があります。 この図の拡大版を表示するには、ここをクリックしてください。

図5:呼吸器と心臓の信号を抽出するための窓の位置を特定するために使用された胸部テンプレート(心臓、胸郭、肝臓)。 略語: ROI = 関心領域。 この図の拡大版を表示するには、ここをクリックしてください。
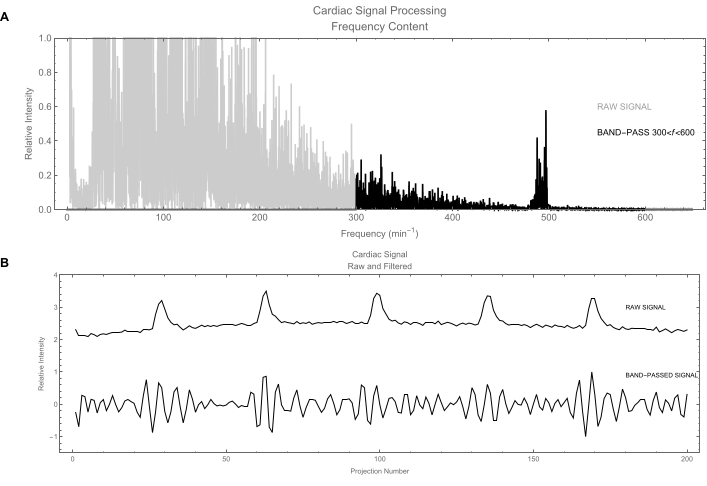
図6:心臓信号 (A)周波数領域での信号処理。灰色のトレースは、パワースペクトルを計算して得られた生の心臓信号の周波数内容を示しています。対象となる周波数は約500 /分です。黒いトレースは、バンドパスフィルタを適用して300〜600ビート/分の周波数のみを維持した後の信号を示しています。 (B)上:時間領域での生の心臓信号のプロット。この信号は、呼吸運動(大きな変動)によって支配されます。実際の心臓信号は、微弱な小刻みに動くものです。下:心臓信号のフィルタリングバージョン:呼吸信号が除去され、きれいな心臓信号が残っています。 この図の拡大版を表示するには、ここをクリックしてください。
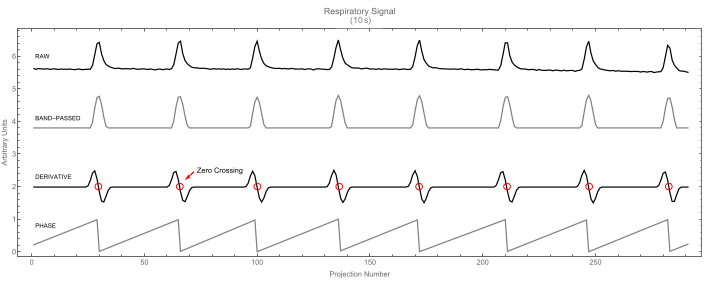
図7:呼吸信号。 生の呼吸信号(上)とそのバンドパスバージョン(2番目)。微分信号 (3 番目) は、ゼロクロッシングが強調表示されて表示されます。これらは、呼吸信号のピークを特定します。次に、これらのピークは、4 番目のトレースに示すように、サイクルの開始 (位相値 0) を示します。 この図の拡大版を表示するには、ここをクリックしてください。
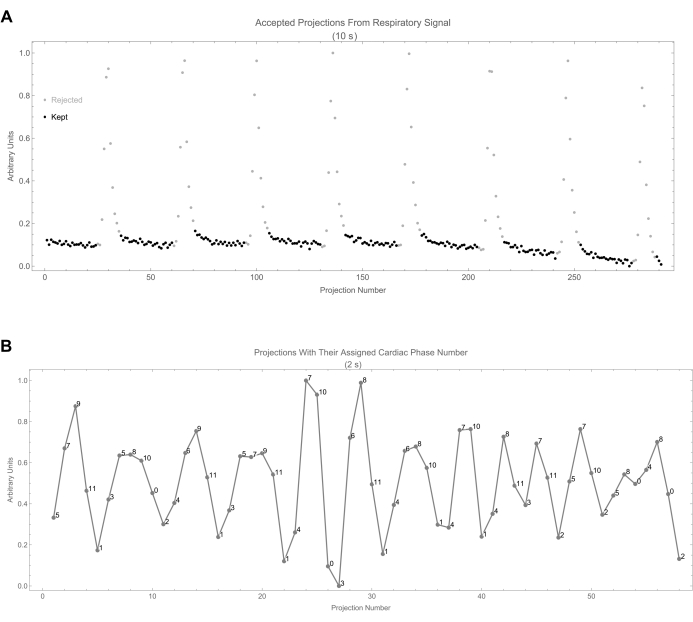
図8:投影選択 (A) これは、投影数の関数として呼吸信号を示しています。受け入れられた投影法は、黒い点で識別されます。(B)これは、各投影の割り当てられた心臓の位相番号とともに心臓信号を示しています。フェーズ番号は、投影と最新のサイクルの開始との間の時間差から計算されます。 この図の拡大版を表示するには、ここをクリックしてください。

図9:石灰化 (A) Amideでグレースケールで表示され、CT値[-500, 500] HUのウィンドウレベルで表示された画像ファイル。(B)石灰化の同定プロセス:非ゲート画像の横方向、冠状、および矢状図。 この図の拡大版を表示するには、ここをクリックしてください。
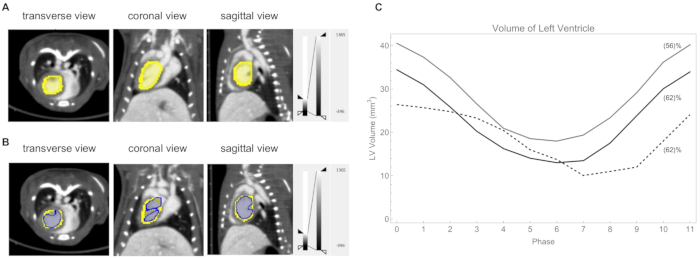
図10:左心室の分析。 (A)手動で描かれた左心室(黄色)。心拍数:418拍/分、呼吸数39呼吸/分(B)左心室はCT値730HU(青)で閾値を示しました。(C)3匹のマウスのサイクルの各フェーズでの左心室の体積のプロット。計算された駆出率は括弧内に示されています。これら3匹のマウスの心拍数/呼吸数は、灰色の線362拍/分および53呼吸/分でした。ブラックライン420ビート/分と59ブレス/分。破線 315 ビート/分と 45 呼吸/分。 この図の拡大版を表示するには、ここをクリックしてください。

図11:コントラスト対ノイズ比の比較(A)非ゲート画像と(B)ゲート画像(心拍数:408拍/分、呼吸数:49呼吸/分)。略語:CNR =コントラスト対ノイズ比;R-gated = 呼吸器ゲート;C-gated = 心臓ゲート。この図の拡大版を表示するには、ここをクリックしてください。
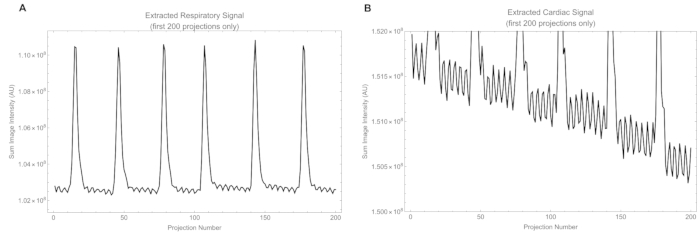
図12:信号の抜粋。 (A)呼吸窓の強度から抽出された生の呼吸信号、および(B)心臓窓の強度から抽出された生の心臓信号。 この図の拡大版を表示するには、ここをクリックしてください。
補足ビデオS1:マウスの心周期中のLVボリュームの変化を明らかにする心臓同期CTシネループ。 心拍数:418拍/分、呼吸数:39呼吸/分。 この ビデオをダウンロードするには、ここをクリックしてください。
ディスカッション
ここで説明する特定のハードウェア実装は、当研究所独自のカスタムメイドのX線CTシステムですが、特定の検出器は市販の前臨床X線CT装置全体で広く使用されているため、説明されている作業は他の機関に関連しています。このシステムは、機能的には、市販され広く使用されている2つの in vivo X線マイクロCTサブシステムのプロトタイプです
前臨床PET / CTスキャナーで。これらのマイクロCTスキャナーは、検出器のアーキテクチャと性能(ピクセルサイズ、感度、DQE、フレームレートなど)を共有しています。同じ検出器は、 in vivo 前臨床システムの他のいくつかの商業メーカーによる前臨床PET/CTおよびSPECT/CTシステムでも使用されています。したがって、検出器の性能は、世界中の市販および設置されている前臨床PET/CTおよびSPECT/CT機器の大部分で共有されています。そのため、適切にプログラムされていれば、これらすべてのシステムは同じフレームレートに到達でき、これは説明された作業を可能にする重要なパラメーターです。ほとんどのユーザーは、市販のマイクロCTシステムの生データにアクセスできませんが、ここで説明する作業は、 in vivo 前臨床機器のユーザーやベンダー向けのテンプレートとして使用でき、これらの機器にすでに含まれている限られたハードウェアで何が可能かを示すことができます。
検出器に加えて、タングステン(W)X線源は、同様のアルミニウムろ過を備えた事実上すべての市販の前臨床PET/CTシステム、および50〜80kVpの範囲のエネルギーを持つX線でも使用されています。kVpという用語は、公称管電圧によって生成されるX線のスペクトルを、電源から供給されるピーク電圧電位として表すために使用されます。これにより、これらすべてのシステム間で異なる最も重要なパラメーターは、ソース電源になります。この研究では、光源の電力(10 W)は、 in vivo 前臨床イメージングに使用される同様の W 光源の下限にあります。したがって、より強力な線源は、少なくとも記載されている作業と同等に、低騒音で、または放射線量の増加を犠牲にして取得時間を短縮して、優れた性能を発揮する必要があります。
マウスモデルでのゲーティングを考察した論文はほとんどなく、マウスの心拍数(~600拍/分または~10Hz)は利用可能なハードウェアに対して高すぎるというのが従来の常識です。この心拍数は、安静時または完全な運動時に意識のあるマウス用であり、マウスは主に駆出率を変化させて心拍数を維持するためです。麻酔下では、心拍数は低くなります(300〜500拍/分)。検出器のフレームレートは29Hzで、これらのレートのいずれかで周期的な心臓の動きの範囲と範囲を完全に再現できます。基本的な仮定は、周期的な心の動きについてナイキスト基準を満たす必要があり、そのためには 600 ビート/分 (10 Hz) で ~20 Hz のフレーム レートのみが必要であるというものです。ここで使用した特定のOEM検出器は、前臨床PET/CT機器の少なくとも4つの独立したメーカーによっても使用されており、したがって、この作業はこれらすべての機器で実際に可能です。
マウスの血液再循環時間は数秒で、通常、造影剤の注入と実際のスキャン開始時間の間には、動物の頭上の位置決め、X線、回転ガントリーハードウェアの構成/初期化により、2〜3分の時間が必要です。重要な点は、21,000の投影を取得するにはさらに約10分かかるため、ユーザーはスキャンの開始を遅らせないようにする必要があるということです。
私たちの研究では、1 つの心相の持続時間は 12 ミリ秒から 15 ミリ秒の範囲でした。露光時間が20ミリ秒であることを考えると、フェーズ間でのクロストークは避けられません。たとえば、フェーズ 2 には、隣接するフェーズ (フェーズ 1 と 3) からの 5 から 8 ミリ秒 (均等に分割) のデータが含まれる場合があり、拡張期などの急速な動きの期間にわずかなぼやけが発生する可能性があります。これを軽減するには、マウスが適切に麻酔され、心拍数が600拍/分(10Hz)未満になるようにすることが重要です。さらに、適切な麻酔により、比較的長いスキャン時間中のリラクゼーション動作を最小限に抑えることができます。動物への放射線量は、ゲートスキャンと非ゲートスキャンで、それぞれ~450mGyと50mGyでした。
このデータ集録プロセスはリアルタイムのコンピュータアプリケーションであるため、集録プログラムは最高の優先度で動作し、同時実行アプリケーションを最小限に抑えることが不可欠です。これらの予防措置を実施しないと、コンピューターが処理できるよりも速く画像フレームが受信され、オーバーランが発生し、スキャンが失敗する可能性があります。
レトロスペクティブ ゲーティング方式の主な欠点は、一部のデータが破棄されるが、データの損失は管理可能であることです。実際には、合計 21,000 の投影法を使用すると、データは角度方向に大幅にオーバーサンプリングされます。どのスキャンにも大きな角度ギャップはなく、画像の再構築に使用した0.5°の間隔(360°で720回の投影)よりもはるかに小さいことを確認しました。たとえば、フレームレートが 29 fps で、マウスが 1/s の速度で呼吸し、フレームの 30% を拒否した場合、呼吸あたり 8.7 フレーム (つまり、ギャップ サイズは 8.7 フレーム) -8.7/21600 または 1 ギャップあたり 0.145° を拒否しました。ちなみに、これがFeldkampではなく反復再構成法が使用された理由です。データを破棄することの二次的な潜在的影響は(プロスペクティブゲーティングと比較して)、拒否された期間(例えば、吸気段階)にX線ビームを遮断するハードウェアシャッター機構がないため、放射線量が増加する可能性があることである。しかし、これが要因となるためには、このようなシャッターメカニズムが完全に実装され、将来のゲート中にアクティブにする必要があります。
データ再構成の方法に関しては、他の方法がOSEMの現在のアプローチと同等またはそれ以上に優れている可能性がありますが、この作業の焦点は、可能な限り最良かつ最小のノイズ再構成を得ることではありません。それよりも、フレームレートが比較的制限され、X線源が低電力である一般的に使用される検出器を使用して、心臓ゲーティングを実行できることを実証したいと考えています。OSEM再構成法を使用すると、計算ハードウェアの制約内でうまく機能し、適切に機能する実装が行われていることがわかりました。
同時に、私たちの方法には、特別なハードウェアを必要としないため、シンプルさなど、いくつかの利点があります。私たちの方法の実装の主な制限要因は、X線カメラの最大フレームレート(29 Hz)と最短露光時間(20 ms)です。このカメラは、いくつかのメーカーの前臨床X線CT装置で広く使用されており、提案された方法は、ゲーティング信号を受け入れるように装備されていないものも含めて、これらのパラメータを達成できる任意のスキャナーで使用できます。さらに、タングステンX線源の性能が低いX線CTシステムは、長時間の露光を必要としますが、克服できない課題はありません。さらに、研究者は、呼吸や脈拍の情報を取得するために小動物にセンサーを取り付けたり、データ取得のための信号トリガーを微調整したりするための広範なトレーニングや練習を必要としません。
石灰化は、当社のCrumpCAT CTスキャナーのすべてのイメージングプロトコルで見られましたが、解像度が低くても、ゲート画像ではCNRが最も高かった。この知見は、心拍ゲーティングが、心臓の鼓動のダイナミックな側面に焦点を当てた研究に有益であるだけでなく、心臓の近くの小さな石灰化や、画像の鮮明さの向上が重要な生理学的運動の影響を受ける他の解剖学的部分を含む研究にも有利であることを示唆しています。
総再構成時間は、投影の数が多く、12フェーズであるため、通常の再構成時間の~30倍です。ただし、信号処理ステップにより、全体の再構成時間にはほとんどオーバーヘッド(<1%)が加わりません。再構成方法自体は、データがフェーズ間で相関しているという事実を利用することで改善できます。関節再構成(時間内)または深層学習法25 の使用は、ノイズの少ない画像を生成し、再構成後の中央値およびガウスフィルタの必要性を排除する。
開示事項
Richard Taschereau博士は、Sofie BiosciencesとXodus Imagingのコンサルタントです。アリオン・F・チャツィオアノウ博士は、ソフィー・バイオサイエンスの創設者です。
謝辞
UCLA Crump Preclinical Imaging Technology Centerのすべてのメンバーのご協力とご支援に感謝いたします。特に、心臓CTイメージングのための動物を準備してくれたMikayla Tamboline氏とIsabel Day氏、そして研究中に左心室のROIの一部を生成してくれたSophie Shumilov氏に感謝します。また、心臓石灰化マイクロCTイメージングのための急性虚血性心損傷のマウスモデルを提供してくださったArjun Deb博士とYijie Wang博士(UCLA)にも感謝します。この研究は、NIHがんセンター支援助成金(2 P30 CA016042-44)によってサポートされています。
資料
| Name | Company | Catalog Number | Comments |
| C57BL/6J mice | Jackson Laboratory | 664 | Male, 8 weeks old, 24-26 g |
| Dexela camera | Varex | 1512 | Detector, 20 ms exposure, 74.8/149.6 µm pixel |
| VivoVist | Nanoprobes | 1301-5X0.25ML | CT Contrast agent |
| X-ray source | Moxtek | TUB00082 | 50 kV peak, 200 µA, 1.0 mm-thick Al filter |
参考文献
- Schambach, S. J., Bag, S., Schilling, L., Groden, C., Brockmann, M. A. Application of micro-CT in small animal imaging. Methods. 50 (1), 2-13 (2010).
- Koba, W., Jelicks, L. A., Fine, E. J. MicroPET/SPECT/CT imaging of small animal models of disease. Am J Pathol. 182 (2), 319-324 (2013).
- Hutchins, G. D., Miller, M. A., Soon, V. C., Receveur, T. Small animal PET imaging. ILAR J. 49 (1), 54-65 (2008).
- Franc, B. L., Acton, P. D., Mari, C., Hasegawa, B. H. Small-animal SPECT and SPECT/CT: important tools for preclinical investigation. J Nucl Med. 49 (10), 1651-1663 (2008).
- Badea, C. T. H. L., Hedlund, L. W., Johnson, G. A. Micro-CT with respiratory and cardiac gating: Micro-CT with respiratory and cardiac gating. Med Phys. 31 (12), 3324-3329 (2004).
- Guo, X., Johnston, S. M., Qi, Y., Johnson, G. A., Badea, C. T. 4D micro-CT using fast prospective gating. Phys Med Biol. 57 (1), 257 (2011).
- Drangova, M., Ford, N. L., Detombe, S. A., Wheatley, A. R., Holdsworth, D. W. Fast retrospectively gated quantitative four-dimensional (4D) cardiac micro computed tomography imaging of free-breathing mice. Invest Radiol. 42 (2), 85-94 (2007).
- Blocker, S. J., Holbrook, M. D., Mowery, Y. M., Sullivan, D. C., Badea, C. T. The impact of respiratory gating on improving volume measurement of murine lung tumors in micro-CT imaging. PLoS One. 15 (2), e0225019 (2020).
- Bartling, S. H., et al. Retrospective motion gating in small animal CT of mice and rats. Invest Radiol. 42 (10), 704-714 (2007).
- Kuntz, J., et al. Fully automated intrinsic respiratory and cardiac gating for small animal CT. Phys Med Biol. 55 (7), 2069 (2010).
- Hahn, A., Sauppe, S., Lell, M., Kachelrieß, M. Automatic intrinsic cardiac and respiratory gating from cone-beam CT scans of the thorax region. SPIE Proc. Med Imaging. 9783, 200-205 (2016).
- Maes, F., Vandermeulen, D., Suetens, P. Medical image registration using mutual information. Proc IEEE. 91 (10), 1699-1722 (2003).
- Sheng, J., Chen, B., Ma, Y., Shi, Y. A novel reconstruction approach combining OSEM and split Bregman method for low dose CT. Biomedical Signal Processing and Control. 62, 102095 (2020).
- Romdhane, H., Cherni, M. A., Sallem, D. B. On the efficiency of OSEM algorithm for tomographic lung CT images reconstruction. 2016 Second International Image Processing, Applications and Systems (IPAS). , (2016).
- Ewald, A. J., Werb, Z., Egeblad, M. Monitoring of vital signs for long-term survival of mice under anesthesia. Cold Spring Harb Protoc. 2, 5563 (2011).
- Suckow, C., et al. Multimodality rodent imaging chambers for use under barrier conditions with gas anesthesia. Mol Imaging Biol. 11 (2), 100-106 (2009).
- Owen, M. . Practical signal processing. , 81 (2007).
- Feldkamp, L. A., Davis, L. C., Kress, J. W. Practical cone-beam algorithm. J Opt Soc Am. A-optics Image Sci Vision. 1 (6), 612-619 (1984).
- Loening, A. M., Gambhir, S. S. AMIDE: A free software tool for multimodality medical image analysis. Mol Imaging. 2 (3), 131-137 (2003).
- Rodriguez-Molares, A., et al. The generalized contrast-to-noise ratio: A formal definition for lesion detectability. IEEE Trans Ultrason Ferroelectr Freq Control. 67 (4), 745-759 (2020).
- Patterson, M. S., Foster, F. S. The improvement and quantitative assessment of B-mode images produced by an annular array/cone hybrid. Ultrason Imaging. 5 (3), 195-213 (1983).
- . Dragonfly 2022.2 Available from: https://www.theobjects.com/dragonfly (2022)
- Pillai, I. C. L., et al. Cardiac fibroblasts adopt osteogenic fates and can be targeted to attenuate pathological heart calcification. Cell Stem Cell. 20 (2), 218-232 (2017).
- Li, S., et al. A humanized monoclonal antibody targeting an ectonucleotidase rescues cardiac metabolism and heart function after myocardial infarction. Cell Rep Med. 5 (11), 101795 (2024).
- Nadkarni, R., Clark, D. P., Allphin, A. J., Badea, C. T. Investigating deep learning strategies for fast denoising of 5D cardiac photon-counting micro-CT images. Phys Med Biol. 69 (20), 205010 (2024).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved