Method Article
イシュ血症/再灌流の豚モデルにおける脊髄微小灌流のリアルタイム評価
要約
脊髄微小循環は脊髄損傷において極めて重要な役割を果たす。ほとんどの方法では、微小循環を標的とした治療法の開発に不可欠な脊髄微小循環のリアルタイム評価はできません。ここでは、虚血/再灌流の大型動物モデルでレーザードップラーフローニードルプローブを用いたプロトコルを提案する。
要約
脊髄損傷は大動脈修復の壊滅的な合併症です。脊髄損傷の予防および治療のための開発にもかかわらず、その発生率は依然としてかなり高く、したがって、患者の転帰に影響を与える。微小循環は組織灌流や酸素供給において重要な役割を果たし、しばしばマクロヘモダイナミクスから解離される。したがって、脊髄微小循環の直接的な評価は、微小循環療法の開発および脊髄微小循環に関する既存のアプローチの評価に不可欠である。しかし、ほとんどの方法は、脊髄微小循環のリアルタイム評価を提供しない。本研究の目的は、脊髄に直接挿入されたレーザードップラー針プローブを用いたリアルタイム脊髄微小循環評価のための標準化されたプロトコルを記述することである。私たちは、脊髄微小循環の悪化を誘発するために、虚血/再灌流のブタモデルを使用しました。また、蛍光微小球噴射技術も用いた。当初、動物は麻酔を受け、機械的に換気された。その後、レーザードップラー針プローブの挿入を行い、続いて脳脊髄液の排水の配置を行った。大動脈の大動脈の露出に対して大動脈の大動脈の露出に対して、大動脈切れの中央値を実行した。虚血/再灌流は、合計48分間の超セリアック大動脈クロスクランプによって誘発され、続いて再灌流および血行力学的安定化が行われた。レーザードップラーフラックスは、マクロヘモ力学的評価と並行して行った。さらに、脳脊髄液の排水を自動化して、安定した脳脊髄圧を維持した。プロトコルの終了後、動物を屠殺し、脊髄を組織病理学的および微小球解析のために採取した。このプロトコルは、レーザードップラープローブを用いた脊髄マイクロ灌流測定の実現可能性を明らかにし、再灌流後の回復と同様に虚血中の著しい減少を示す。結果は、蛍光微小球評価と同等の挙動を示した。結論として、この新しいプロトコルは、虚血/再灌流条件におけるリアルタイムの脊髄微小灌流評価を用いた将来の研究に有用な大型動物モデルを提供するかもしれない。
概要
虚血/再灌流(SCI)によって引き起こされる脊髄損傷は、減らされた転帰1、2、3、4に関連する大動脈修復の最も壊滅的な合併症の1つである。SCIの現在の予防および治療オプションには、大血体力学パラメータの最適化と、脊髄灌流圧2、5、6、7、8、9を改善するための脳脊髄液圧(CSP)の正常化が含まれる。これらの操縦の実施にもかかわらず、SCIの発生率は、大動脈修復10、11、12の複雑さに応じて、まだ2%から31%の範囲です。
最近、微小循環は13,14に注目を集めている。微小循環は、細胞酸素取り込みおよび代謝交換の領域であり、したがって、臓器機能および細胞完全性13において重要な役割を果たす。微小循環血流の障害は、15,16,17,18,19の増加死亡率に関連する組織虚血の主要な決定要因である。脊髄微小循環の障害は、神経機能の低下と結果20、21、22、23に関連する。従って、SCIの治療のためのマイクロ灌流の最適化が最も有望なアプローチである。微小循環障害の持続性は、マクロ循環最適化にもかかわらず、26、27、28、29と記載されている。この血行性の一貫性の喪失は、虚血/再灌流を含む様々な条件で頻繁に起こり、直接微小循環評価および微小循環標的療法26、27、30の必要性を強調する。
これまでのところ、脊髄微小循環挙動20,31のリアルタイム評価にレーザードップラープローブを使用した研究はごくわずかである。既存の研究は、しばしば微小球注入技術を使用してきましたが、これは断続的な使用および事後分析32,33によって制限される。マイクロスフィア注入技術を用いた異なる測定の数は、波長の異なる微小球の利用可能性によって制限される。さらに、レーザードップラー技術とは対照的に、この方法では事後組織の処理と分析が必要であるため、マイクロ灌流のリアルタイム評価は不可能です。ここでは、虚血/再灌流の豚大動物モデルにおける脊髄微小循環のリアルタイム評価のための実験プロトコルを提示する。
本研究は、虚血/再灌流における微小循環に対する結晶とコロイドの影響を比較する無作為化研究と、脊髄マイクロ灌流に対する流体対バソプレッサーの影響に関する探索的無作為化研究を組み合わせた大規模な動物プロジェクトの一環であった。フロープローブ2点キャリブレーションと圧力先端カテーテルキャリブレーションは、以前に説明した34.報告されたプロトコルに加えて、蛍光微小球は脊髄微小灌流の測定に用いられ、前述のように、各動物に対して12サンプルの脊髄組織を用い、下肢脊髄35,36を表す試料1~6と7-12を有する。マイクロスフィア注入は、レーザードップラー記録及びマクロヘモ力学的評価の完了後の測定工程ごとに行った。病理学的評価は、前述の37のようにクラインマンスコアを用いて行った。
プロトコル
この研究は、ハンブルク市の動物のケアと使用に関する政府委員会によって承認されました(参考番号60/17)。動物は「実験動物のケアと使用のためのガイド」(NIH出版第86-23号、改訂版2011)に従ってケアを受けただけでなく、FELASAの勧告および実験は、ARRIVEガイドライン24,25に従って行われました。この研究は急性の試験であり、すべての動物はプロトコルの最後に安楽死させた。
注:研究は、約40キロの重さの6つの3ヶ月の雄と雌の豚(ドイツのランドレース)で行われました。動物は実験の少なくとも7日前に動物のケア施設に持ち込まれ、動物福祉勧告に従って収容された。動物は食物と水のアドリビタムを提供され、その健康状態は責任ある獣医師によって定期的に評価された。実験前に12時間の断食時間を維持した。動物の実験手順および取り扱い全体は、責任ある獣医師によって監督された。
麻酔の誘導と維持
- 麻酔の誘導および維持のために、動物を予め投薬し、筋肉内注射を用いて深く鎮静し、必要に応じて静脈内注射を行い、気管内挿管を行う。その後、追加のオピオイドボーラス注射で補完する連続的なオピオイド塗布を用いた揮発性麻酔剤の組み合わせを用いて麻酔を誘導し維持する。
- ケタミンの筋肉内注射を行う 20 mg·kg-1、 アザペロン 4 mg·kg-1、 ミダゾラム 0.1 mg·kg-1 前投薬と鎮静.
- 静脈カテーテルを耳静脈に入れ、適切な固定を確保し、10 mLの生理食前の速い塗布によって機能性を評価する。
- 熱損失を防ぐために、動物を温まる毛布の上の上の上に上に置きます。
- 心電図(ECG)とパルスオキシメトリーで基本的なモニタリングを確立し、動物の心肺状態を監視し、基本モニタリングハードウェアに接続します。
- 前酸素化のために豚型マスクを介して酸素の15 L·min-1 を投与する。
- 必要に応じて0.1mg·kg-1%のプロポフォールの静脈内ボリを注入し、気管内挿管を行う。
- エンドタイダルカポノグラフィーとオースカルテーションで正しい配置を確保し、0.1 mg•kg-1のパンクロニウムを投与し、気管内チューブの適切な固定を確保します。
- 10 mL·kg-1 体重-1の潮量、10 cmH2Oの正の終値気圧、および麻酔装置を使用して0.3のインスパイアされた酸素(FiO2)の一部を使用して、体積制御換気を確立します。人工呼吸器の周波数を調整して、35-45 mmHgの二酸化炭素の終値張力(etCO2)を維持します。
- 胃管を導入し、胃液の吸引を行い、チューブを適切に固定し、回収バッグに接続します。動物の目を注意深く閉じて麻酔中の目の乾燥を防ぎます。
- フェンタニル(10 μg·kg-1·h-1)とセボフルラン(3.0%の期限切れ濃度、蒸気によって送達される)の連続注入によって麻酔を維持する。バイタルサインと換気パラメータを注意深く観察し、プロトコル全体の動きを欠いて、外科刺激の段階に特別な注意を払うことによって、十分なレベルの麻酔を確保します。痛みや苦痛の兆候がある場合は、フェンタニル(50 μg)の追加のボーラス用量を与えます。
注:全手順中に動物麻酔の経験を持つ研究者の存在を確認し、適切な麻酔を確保するために経験豊富な獣医師による監督を使用してください。 - 10 mL·kg-1·h -1バランス結晶質のベースライン注入率を投与して、麻酔、手術準備、実験プロトコルの実行中の流体損失を補正します。熱損失を防ぐために流体ウォーマーを使用してください。
- 石鹸水を使って豚の皮をそっと拭きます。ポビドネヨウ素を含む皮膚消毒液を使用して、皮膚汚染を減少させます。手術用手袋は、手術用に使用してください。300mgのクリンダマイシンを抗菌予防として適用し、6時間後に投与量を繰り返す。
2. プローブの配置
- 動物を右横の位置に置き、動物の背中を曲げて椎骨の間のスペースを広げます。
- 脊椎領域を外科的に露出して、脊椎間プロセスと椎体の準備を行う(図1A)。
- 血管14G末梢静脈カテーテルパラメディアを、2つの椎骨アーチの間に胸椎(Th)13/14または腰椎(L)1/2のレベルで脊髄に入れる(図1B)。
- 針を取り外し、レーザー/ドップラー針プローブを静脈カテーテル(図1C)に挿入し、指定されたハードとソフトウェアに接続して信号品質をテストします。中程度の脈動性を持つ安定した信号があることを確認してください。
- プローブを縫合線(図1D)で慎重に固定し、パディングを使用してプローブの転位やキンキングを防ぎます。
- 脳脊髄圧を測定および制御するための脳脊髄液排液の経皮的配置については、L4/5またはL5/6のレベルを特定し、皮膚および皮下腔を導入者の針で穿刺し、注射針を取り除く。
- 針に生理食音で満たされた注射器を置き、液体で満たされた注射器に一定の圧力で針を慎重に導入します。
- 硬膜外位置の証拠として抵抗の喪失が感じられると、インレー針を再導入し、さらに針を導入して硬膜を穿刺し、インレイ針を取り除く。
- 透明な酒の速い滴下によって、その中の位置を確認する。深さ20cmまでの排水を導入し、Luerロックアダプターを取り付け、酒類の注意深い吸引によって位置を確認します。
- 慎重に縫合糸で排水を固定し、脳脊髄液排水システムに接続します。
- 左耳の後ろの頭蓋骨を露出し、慎重に6ミリメートルドリルアタッチメントを使用して皮膚のドリル穴のトレパネーションを行います。
- 第2レーザードップラープローブを脳に直接導入する。プローブを縫合糸で慎重に固定し、指定されたハードとソフトウェアに接続して信号品質をテストします。ここでも、中程度の脈動性を持つ安定した信号があることを確認してください。
- すべてのプローブを取り外し、動物を慎重にサピーヌ位置に配置し、影響を受けないプローブの位置を確保します。少なくとも4〜5人の研究者がこの操縦を行うことを確認してください。
- プローブを再接続し、信号の品質を再確認します。
- レーザードップラーハードウェアの出力チャンネルをアンプに接続し、シンクロニシン集録ハードウェアとソフトウェアを接続して、レーザー/ドップラーフラックスをマクロヘモダイナミック信号と同時に記録します。
- 2点キャリブレーションでユニット(PU)ごとにフラックスをキャリブレーションします。
- Enterキーを押してメニューを開き、アナログ出力設定を選択します。
- 表示された変換係数(5.0 V = 1000 PU)を使用して、シンクロニシン集録ソフトウェアで使用するために2点キャリブレーションでフラックスを較正します。
- [ 戻る] を選択して前のメニューに戻り、[ 計測] を選択して測定を続行します。
- シンクロニケーション取得ソフトウェアを開きます。[設定]メニューからすべての入力をゼロにします。すべての入力を使用するデバイスおよびプローブに接続します。
- Flux チャンネルのドロップダウンメニューをクリックして、フラックスの 2 ポイントキャリブレーションを実行します。2 点キャリブレーション を選択します。単位変換を on に設定し、単位として[BPU]を選択します。ポイント 1の場合は、0 Vを 0 BPUに設定します。ポイント 2の場合は、5.0 Vを1000 BPUに設定します。[すべてのデータと新しいデータの単位を設定] を選択します。[OK] をクリックしてメニューを閉じます。
- 目標圧力10mmHg、排水量20mL·h-1で連続性脳脊髄液排水を開始する。
3. カテーテルの配置
- 両方の大腿動脈を露出する。
- 右大腿動脈の遠位部分をリゲートし、血管ループを用いて動脈の近位内腔を一時的に閉塞させ、ポッツのはさみを使用して容器の2mmカットを行い、ガイドワイヤーを導入する。
- さらにガイドワイヤーを導入し、抵抗のない挿入を保証し、ワイヤのキンキングを避けます。カテーテルをワイヤー上に導入する
- 縫合糸でカテーテルを固定します。
- 血液ガス分析と血圧と心肺間モニタリングハードとソフトウェアへの適切な接続後の動脈信号測定で検証された動脈血液の吸引によって正しい位置を確保します。
- 左大腿動脈に5mmのフロープローブを設置し、流量計に接続して信号品質をテストします。
- 縫合糸で両方の鼠径部を閉じます。
- 右頸動脈と8 Fr.インベラーシースの配置のための右の内部頸静脈を露出させる。
- カテーテルの配置については、3.2-3.4に記載の同じ方法で進める。
- 頚動脈導入者シースの側腔を動脈圧測定のための基本的な圧力モニタリングおよび肺熱希釈ハードウェアに接続します。
- 昇順大オルタに圧力先端カテーテルを導入し、アンプに接続してハードとソフトウェアを取得するシンクロニシンの位置を確認します。
- 肺動脈の静脈鞘を介してスワンガンズ肺動脈カテーテルを配置し、気球を20cmの深さで空気で膨らませ、血行力学的曲線にくさび圧が見えるまでそっと挿入する。バルーンを収縮させ、カテーテルを2cm戻します。肺動脈圧の信号品質を満たしていることを確認します。サーミスターを基本的な圧力監視および肺熱希釈ハードウェアに接続します。
- 薬物投与用の12 Fr. 5-Lumen中央静脈カテーテルの経皮的配置および外部右頸静脈への中央静脈圧測定にソノノグラフィガイダンスを使用する。ソノグラフィー配置に 6 ステップアプローチを使用する 38
- カテーテルの遠位内腔を血圧と心肺間モニタリングハードとソフトウェアに接続します。すべての薬剤と注入を中央静脈カテーテルに切り替えます。鎮痛薬、流体、カテコールアミンに異なるルーメンを使用し、ボリュームローディングステップ中にコロイドの投与のために大きなルーメンを惜しみます。
4. 手術準備
- ミニラパロトミーを行い、膀胱を動員し、尿排水のためのフォーリーカテーテルを挿入し、生理焼香でバルーンを膨らませ、カテーテルをポーチ縫合糸で固定します。
- mLの尿量を表示する尿の収集袋にカテーテルを接続します。
- FiO2 を1.0に増やし、0.1 mg·kg-1 パンクロニウムを静脈内に再投与する。
- 胸骨に準備するためにエレクトロケータリを使用して、中央値のステーテルノトミーを行います。周囲の組織から胸骨をそっと解剖する。怪我を防ぐために、圧縮後の後船尾配置を行います。
- 換気を停止し、振動鋸で骨を分割します。換気を続け、FiO2 を0.3に減らします。電気焼灼を使用して出血を軽減し、胸骨を骨ワックスで密封します。
- 左肺の頂点を慎重に動員し、横隔膜の左側部分を分け、外科的暴露を容易にする。
- 左肺の穏やかな引き込みによってセリアック幹に下降大胚近を露出させ、妨げられない換気を確保し、左肺への外傷を避け、周囲の組織を分割する(図2B)。血行力学的安定化が必要な場合は、7 mL·kg-1ヒドロキジエチルデンプンコロイドを投与する。
- 下降大高の周りにオーバーホールドを配置して、適切な露出を確保します(図2C)。
- 下降胸部大オルタの周りにフロープローブを取り付けます(図2D)。フローモジュールと同期収集ハードとソフトウェアに接続することで、適切な信号品質を確保します。必要に応じて、コンタクトゲルを使用して信号品質を向上させます。
- 船のループを下降大動脈の周りに取り付け、フロープローブに遠位して大動脈クロスクランプの面積をマークします。
5. 評価とデータ取得
- 右心房レベルに配置された流体充填ラインを使用して、すべてのカテーテルとレベルカテーテルをゼロにします。
- 針ECG電極を配置し、シンクロニシン集録ハードとソフトウェアにそれらを接続します。
- 心肺経熱希釈の評価、大動脈流および圧力測定の評価は、以前に34.
- 肺動脈熱希釈を用いた心拍出量測定では、10mLの冷塩水で3回の注射を行い、基本的な監視ハードウェアで表示される平均値を記録します。
- 単にスタートを押してレーザードップラーソフトウェアを起動し、慎重にM0からM5としてステップをラベル付けすることによって、各測定ステップのマークを設定します。
6. 実験プロトコル
- ベースライン測定(M0)を実行します。
- 7 mL·kg-1 hydroxyethylデンプンコロイドのボリュームローディングステップを使用して血行力学最適化を実行します。加圧注入を使用して、5分以上の各容積のステップを実行します。各ボリュームローディングステップが完了した後、平衡化のために5分を許可します。心拍出量の増加が<15%になるまで、容積負荷を開始する。
- 血行最適化の完了後に測定(M1)を繰り返します。
- マークされた領域に大動脈クランプを配置することにより、超セリアック大動脈クロスクランプの合計48分間の虚血/再灌流を誘導します。
- 大動脈クランプを1-、2-、5-、10-および30分間隔の昇順に適用して、研究プロトコル中の動物の生存率を向上させます。
- 最大5分経過後、または大腿動脈流の正常化後に各間隔の後に大動脈クロスクランプを継続します。
- 下の静脈の手動流入閉塞を行い、100mmHg平均動脈圧の血圧上昇>防ぎます。
- クランプ段階でノルエピネフリンまたはエピネフリンのボーラス注射を投与し、必要に応じて、40mmHg未満の平均動脈圧の低下を防ぎます。
- 再灌流(M2)の前に、30分クランプ間隔の終わりに測定を繰り返します。
- 徐々にクランプを開いて、血行力学的安定性を確保します。血圧があまりにも速く低下した場合はクランプを閉じ、安定させます。
- 7 mL·kg-1 のヒドロキシエチルデンプンコロイドと、安定化のためのノルエピネフリンおよび/またはエピネフリンの10〜20 μgの追加のボーラス注射を行います。pHが7.1を下回った場合、2 mLkg-1 の8.4%重炭酸ナトリウムを投与する。ノルモカプニアを確保するために呼吸速度を適切に調整してください。
- 再灌流後1時間(M3)を繰り返す。
- 6.2の下で説明したように血行力学の最適化を繰り返し、測定を繰り返します(M4)。
- 虚血/再灌流(M5)の誘導後4.5時間の最終測定を行います。
7. 安楽死
- 心室細動および収縮期を誘導するために安楽死のために静脈内に塩化カリウムの40ミリモルを投与する。
- 換気を終了し、すべてのカテーテルを取り外します。
8. 臓器収穫
- 動物を起こしやすい位置に置き、針プローブと排水を取り除きます。
- 皮膚の切開によって、頭皮と鉗子を使用して筋肉組織の除去によって背骨を露出させます.
- 振動鋸を使用して両側の椎骨アーチパラメディアンを分割し、脊髄の骨の後側部分を慎重に左右に動かして残りの接続を緩めます。
- 鉗子を使用して脊髄を頭蓋端まで慎重に持ち上げ、メスを使って脊髄を切断して脊髄を取り除きます。
- 脊髄を4%ホルマリンで保存し、組織病理学的評価または微小球定量のためにさらに利用します。
9. 統計分析
- 統計ソフトウェアを使用します。
- 必要に応じてヒストグラムとログ変換変数を検査して正規分布を確保します。
- 従属変数-脊髄フラックス、心拍出量、心拍数、脳卒中体積、収縮期動脈圧、平均動脈圧、拡張動脈圧、中央静脈圧、全身血管抵抗、ならびに必要に応じて蛍光微小球で評価される上下の脊髄微小灌流を対象とし、一般的な線形混合モデル分析に、一般的な線形混合モデルにルーチンGENLINMIXEDを使用する。
- ベースライン調整を使用します。
- 変数ベースラインと測定点の固定効果を持つモデルを指定します。測定ポイントは、動物の中で繰り返される測定点として考慮する。
- 各パラメータの測定点の固定効果のp値を報告します。
- 脊髄蛍光微小球分析では、領域(下脊髄、上部脊髄)を固定効果として使用し、領域と測定点間の相互作用を評価し、相互作用に対する固定効果のp値も報告します。
- 測定ポイントM1-M5ですべての従属変数に対して95%信頼区間(CI)を持つ計算ベースライン調整限界平均値、次に最小有意差検定による対比較を行います。
- 平均値として変数を表現します(95% CI)。平均±標準偏差として動物の体重を表現する。
- 未調整の p 値を示します。
結果
6匹の動物はすべてプロトコルが完成するまで生き残った。動物の体重は48.2±2.9 kgであった。5匹の動物が雄で、1匹が雌であった。脊髄針プローブの挿入と脊髄フラックスの測定は、すべての動物において実現可能であった。
虚血誘導のための大動脈クロスクランプ中の脳微循環および大血体的記録と組み合わせたリアルタイム脊髄微循環記録の例は、アンクランプおよび再灌流中に同様に図3Aに示されている、図3Bに示す。下降大動脈流の破壊の後に脊髄フラックスが著しく低下し、上昇大動脈の圧力が増加した(図3A)。再灌流は反対の効果につながった(図3B)。
マクロおよび微小循環パラメータの統計分析を 表1に示します。混合モデル推定限界平均及びその信頼区間は、虚血中の脊髄フラックスの著しい減少を示す。対照的に、脳フラックスは、推定限界平均とその信頼区間によって示されるように、虚血中に著しく増加した。これは、動脈圧、心拍数、全身血管抵抗の増加を伴い、心拍出量および脳卒中量が減少した。蛍光微小球分析は、下脊髄の脊髄微小循環血流の著しい減少を明らかにしたが、推定限界平均とその信頼区間によって示されるように、上部脊髄に有意な変化はなかった。再灌流は反対の効果につながった。プロトコルの最後には心拍出量、脳卒中量、動脈圧がさらに低下したが、脊髄フラックスならびに脊髄微小循環血流は安定していた。
この研究の結果は、脊髄マイクロ灌流のリアルタイム変化を検出するレーザー/ドップラー針プローブの能力を示しています。予想通り、虚血中の脊髄微小循環の減少は、微小循環フラックスを最小限に抑えて急激であった。脊髄フラックスの回復は再灌流後に起こった。より低い脊髄灌流は、蛍光微小球で評価されるように、同等の行動を示し、したがってこの方法を支持した。予想通り、上部脊髄灌流および脳フラックスは異なる行動を示した。脊髄微小循環は安定であったが、マクロ循環はプロトコルの最後に低下し、血行力学的一貫性の喪失を示した。下降大動脈の流れは虚血時にゼロであったが、再灌流は大動脈の流れの回復につながった。病理組織学的分析は、0と2の間の下脊髄と0と1の間の上部脊髄のクラインマンスコアを有する脊髄の軽度の壊死を明らかにした。
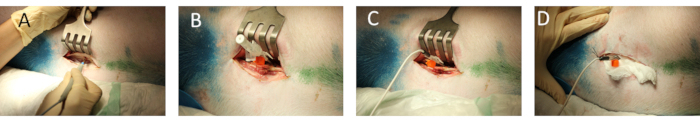
図1:脊髄におけるレーザー/ドップラー針プローブの配置(A)椎体構造の外科的暴露(B) 静脈カテーテルを用いた脊髄の穿刺(C)インレイ針の除去後の針プローブの挿入。(D)針プローブの固定。この図の大きなバージョンを表示するには、ここをクリックしてください。

図2:下降大オルタの露出とフロープローブと容器ループの配置(A)左肺の頂点を動員し、横隔膜の左横部分を分割した後の下降大オルタの露出。(B)外科的暴露のために周囲の組織を分割する。(C) 下降大オルタの周囲に見越し占いを配置し、適切な円形露出を確保する。(D) 流動プローブの配置と、下降大オルタの周りの容器ループ。この図の大きなバージョンを表示するには、ここをクリックしてください。

図3: 虚血中の微小循環およびマクロヘモ力学的信号のサンプル記録と再灌流 ECGのサンプル記録は、マイクロチップカテーテルを用いて測定された昇順大動脈の圧力、超音波フロープローブを用いて測定した下降大動脈内の流れ、脊髄ならびに脳微小循環型FLUXをレーザー/ドップラー針プローブを用いて測定した。(A)上セリアック大動脈クロスクランプによる虚血誘導時の50sサンプル。(B)大動脈クロスクランプの緩やかな再開きによる再灌流誘導時の20秒のサンプル。 この図の大きなバージョンを表示するには、ここをクリックしてください。
| M1 | M2 | M3 | M4 | M5 | ||
| 脊髄流束 | 61.35 (41.96-89.70) | 6.78 (4.63-9.91) | 58.97 (40.33-86.22) | 66.05 (45.17-96.57) | 59.09 (40.41-86.40) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.878 | p = 0.777 | p = 0.886 | |
| 脳フラックス | 41.12 (28.17-60.04) | 71.73 (49.13-104.73) | 60.34 (41.33-88.10) | 59.91 (36.93-78.71) | 49.82 (34.12-72.74) | |
| 主効果測定点: p = 0.023 | 対方向比較 M1 | p = 0.001 | p = 0.045 | p = 0.173 | p = 0.341 | |
| 脊髄マイクロ灌流(ml/分/g) | 上部脊髄 | 0.071 (0.058-0.087) | 0.063 (0.052-0.078) | 0.088 (0.072-0.11) | 0.082 (0.067-0.100) | 0.083 (0.068-0.102) |
| 対方向比較 M1 | p = 0.420 | p = 0.146 | p = 0.344 | p = 0.281 | ||
| 主効果測定点: p < 0.001 | ||||||
| 下部脊髄 | 0.079 (0.065-0.097) | 0.031 (0.026-0.039) | 0.111 (0.090-0.136) | 0.089 (0.073-0.110) | 0.105 (0.086-0.129) | |
| 相互作用測定ポイント ·脊髄領域: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.021 | p = 0.400 | p = 0.051 | |
| 心拍出量(l/分) | 4.15 (3.69-4.61) | 3.13 (2.67-3.60) | 3.30 (2.84-3.76) | 3.67 (3.20-4.13) | 2.67 (2.00-2.93) | |
| 主効果測定点:p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.007 | p = 0.125 | p < 0.001 | |
| 心拍数(bpm) | 74.42 (53.70-95.15) | 131.09 (110.36-151.82) | 88.92 (68.19-109.65) | 80.62 (59.89-101.35) | 99.38 (78.65-120.11) | |
| 主効果測定点: p = 0.002 | 対方向比較 M1 | p < 0.001 | p = 0.314 | p = 0.666 | p = 0.092 | |
| ストロークボリューム (ml) | 55.50 (49.20-61.81) | 25.33 (19.03-31.64) | 37.00 (30.69-43.31) | 45.33 (39.03-51.64) | 27.17 (20.86-33.47) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p < 0.001 | p = 0.004 | p < 0.001 | |
| 収縮期動脈圧昇圧大動脈(mmHg) | 94.36 (85.20-103.52) | 122.05 (112.89-131.20) | 76.72 (67.56-85.88) | 88.36 (79.20-97.52) | 73.36 (64.20-82.52) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.006 | p = 0.321 | p = 0.002 | |
| 平均動脈圧昇順大動脈(mmHg) | 78.18 (68.68-87.67) | 107.29 (97.80-116.78) | 59.08 (49.58-68.57) | 70.38 (60.89-79.87) | 58.35 (48.85-67.84) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.005 | p = 0.217 | p = 0.004 | |
| 拡張動脈圧昇圧大動脈(mmHg) | 59.20 (49.41-69.00) | 93.76 (83.97-103.56) | 45.18 (35.38-54.98) | 52.48 (42.69-62.28) | 45.33 (35.54-55.13) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.038 | p = 0.302 | p = 0.040 | |
| 全身血管抵抗(dyn x sec x cm-5) | 1421.13 (1236.94-1632.74) | 208089.94 (181128.10-239085.87) | 1335.36 (1162.29-1534.21) | 1412.62 (1229.54-1622.97) | 1807.46 (1573.21-2076.60) | |
| 主効果測定点: p < 0.001 | 対方向比較 M1 | p < 0.001 | p = 0.407 | p = 0.938 | p = 0.005 | |
| 流れ(l/分)降下大オルタ | 3.27 (0.96-5.58) | 0 | 3.27 (0.96-5.58) | 3.54 (1.23-5.85) | 4.54 (2.32-6.85) | |
| 主効果測定点: p = 0.003 | 対方向比較 M1 | p = 0.998 | p = 0.844 | p = 0.381 | ||
表1:プロトコル中の血行力学パラメータの変更 値は、95% 信頼区間を持つベースライン調整済みの推定限界平均として与えられます。測定点の主な効果のF検定の未調整のp値は、各パラメータに対して、ならびに上部および下部脊髄マイクロ灌流のための領域と測定点間の相互作用効果に与えられる。M1を用いて個々の測定点の対の比較の未調整のp値も提示される。測定ポイントは、M1=虚血/再灌流前の血行力学的最適化前、M2=虚血の間、M3=1時間再灌流後M4=虚血/再灌流後の血動力学的最適化、M5=4.5hの虚血/再灌流の誘導後である。
ディスカッション
脊髄虚血によって誘発されるSCIは、患者の転帰1、2、3、4、10、11、12に大きな影響を与える大動脈修復の主要な合併症である。SCIを予防し、治療するためのマイクロ循環療法が最も有望である。このプロトコルは、リアルタイムの脊髄微小循環評価のための再現可能な方法を提供し、虚血/再灌流条件下で脊髄微小循環に対する新しい治療アプローチの効果を評価する能力を提供する。
この実験モデルには、いくつかの重要な方法論的ステップがあります。動物の損失を防ぐために、研究者は麻酔技術(髄液排液挿入、大動脈暴露中のソノグラフィ血管アクセスおよび血行力学的治療、大動脈クロスクランプ、再灌流)および外科的技術(子宮管切裂、血管暴露、下降大動脈の外科的暴露)を経験する必要があります。脊髄針プローブの挿入には、経験、解剖学の深い知識、および健全な技術的スキルが必要です。しかし、私たちの経験では、学習曲線はかなり急であり、ほとんどの経験豊富な研究者は短時間で成功を収めますが、方法論に影響を与える可能性のある脊髄損傷を防ぐために複数の試みを避ける必要があります。
もう一つの重要なステップは、脊髄針プローブの転位または損傷を防ぐために、右横方向から上へ位置へ変化することです。この操縦のために、4-5人が推薦され、挿入場所の適切なパディングが不可欠であり、綿密な注意が、プローブを外さないよう注意する必要があります。下降大大体の露出は、同様にいくつかの重要なステップを必要とします。左肺の頂点は、外科的分野を露出させるために左肺の穏やかな引き込みができるように動員されなければならない。さらに、横隔膜の左側部分は、露出を容易にするために解剖されるべきである。大動脈準備中に、外科手術を行う研究者と、十分な心肺安定性を確保するために麻酔と血行力学的管理を提供する研究者との間の最適なコミュニケーションが必要である。大動脈クロスクランプの間、静脈のリターンを減らすために、下の静脈の手動圧縮が推奨される。この操縦がなければ、重篤な後負荷増加が起こり、有害な心筋損傷39、40を引き起こす可能性がある。
再灌流は、液体、血管圧器、および使用する準備ができてイトロープで慎重に行われるべきです。再灌流の間に、激しい低血圧、心臓アリトミア、および循環障害41を引き起こす可能性のある劇的な変化が起こる。しかし、血行行動の注意深い観察、介入の迅速な開始、ならびにこの重要な段階での構造化された穏やかなパフォーマンスの使用は、動物の喪失を防ぐことができます。また、大動脈クロスクランプの昇順間隔の使用は、続いて再生を改善する期間を経て、プロトコルで使用される場合、再灌流時の血行力学的安定性を高める虚血性前調節効果を誘発する42,43。
このモデルは、マクロ循環評価に加えて、脊髄微小循環を監視する機能を提供します。高リスク手術や重症患者に頻繁に見られる血力学的一貫性の喪失のために、脊髄微小循環の直接評価が必要である13,30。サブリンガル微小循環は、関心の器官44における直接的な微小循環評価を置き換えるためにしばしば使用される。しかしながら、亜リンガル微小循環と重要臓器との解離が示されており、実験モデル45で用いられているように、脊髄における直接的微小循環評価の価値を強調する。最後に、このモデルは、蛍光微小球評価と比較して脊髄血流のリアルタイムモニタリングという利点を有し、これは間欠的使用および事後分析46によって制限される。リアルタイム評価の影響は、虚血中の記録例と再灌流誘導を見る際に最もよく見ることができ、脊髄マイクロ灌流の急速な変化を示す。しかし、脊髄にレーザードップラープローブ挿入が脊髄の小さいが、かなりの傷害につながる可能性があることを考慮すべきである。
脊髄の完全性が血行力学的パラメータに影響を与える可能性があるため、これはこの方法の欠点である可能性があります。しかし、脊髄マイクロ灌流を評価するためのレーザードップラー技術の使用は、以前47、48、49、50を使用されてきた。また、プローブ挿入後の血行力変化は見当たらなかったものの、この方法で誘導される血行力学的効果を排除することはできません。血行力学的変化はまた、微小球注射の使用によって誘発され得るが、これは、しかし、大型動物51において軽微な重要性を持つであろう。また、感覚や運動機能は、プローブ挿入の影響を受ける可能性があるため、レーザードップラー評価と組み合わせて、感覚的または運動誘発電位評価の使用を慎重に行う必要があります。
この点に関して、マイクロスフィア注入技術が有利である可能性がある。さらに、この技術は慢性試験には使用しないでください。しかし、これは、死後の組織分析に依存するため急性期試験に限定される微小球注射にも当てはまります。レーザードップラー技術を用いた研究は、小動物47、48、49、50ここでは、大型動物モデルとして、ブタで使用するための技術を説明し、臨床研究への翻訳を容易にする可能性がある。パラメディアン導入技術は、豚の大きな棘プロセスの問題を克服し、脊髄プローブの適切な配置を複雑にする。また、この技術は、液の一定の損失を防ぎ、ラミネクトミーまたは硬膜組織の除去が必要とされないという利点を有する。脳脊髄液圧は脊髄灌流32に多大な影響を及ぼすため、脊髄マイクロ灌流に加えて脳脊髄液圧を測定および最適化する利点があり、将来のプロジェクトにおける脊髄微小灌流に対する脳脊髄液圧の影響に対処する。
プロトコルには、言及すべきいくつかの制限があります。正確なプローブ位置の違いと大きな脊髄血管の近接性により、脊髄フラックスの絶対値は動物間で大きく異なります。したがって、値を比較する際にはベースライン調整を実行する必要があります。しかし、測定ポイント間の個人間の差は、プロトコル中に針プローブの動きを避けるために細心の注意が払われている限り、非常に一貫しています。さらに、この研究は、レーザードップラーと蛍光微小球法の比較研究として設計されていません。動物の数を考えると、これら2つの方法の間に相関分析を行わなかった。
どちらの方法も、虚血中の有意な減少と両者の再灌流後の回復と同等の行動を示したが、方法の比較は、将来的に適切に設計された研究を使用して対処すべきである。それにもかかわらず、微小球の使用は、上部および下部脊髄マイクロ灌流のための異なる行動の評価をさらに可能にした。さらに、組織病理学的分析は、脊髄虚血の他のモデルと比較して中程度の脊髄壊死のみを明らかにした37.虚血の持続時間を延長するだけでなく、事前調整措置を省略すると、一部の研究者が望む可能性のあるより深刻な変化につながる可能性があります。軽度の病理組織変化のみを評価したが、これは虚血の持続期間が長いほど異なる可能性がある。この点に関して、プロトコルの終了前に虚血/再灌流後のより長い期間はまた、より深刻な病理組織学的変化を導いたかもしれない。しかし、このプロトコルは、追加または連続的なinotropeまたはvaso圧機能アプリケーションを必要とせずに再灌流の1時間後に血行力学的安定性を可能にした。
異なる血行力学的介入の評価のために、このモデルは最適条件を提供する。血行力学的介入の例として流体最適化を用いたが、他のアプローチはこの方法で評価されるかもしれない。このプロトコルは虚血/再灌流のモデルで微小循環評価を提供するが、虚血の持続期間は、再灌流前の虚血時の治療アプローチの評価を制限する。さらに、虚血の間に、血行力学的変化の変化(例えば、高血圧、低血圧、頻脈、徐脈、ならびに心臓アリトミア)の変化が起こった。手動流入閉塞は、このフェーズ中の血行力学変数にさらに影響を与えます。したがって、プロトコルは、再灌流前の虚血時の治療アプローチの評価には推奨されません。しかしながら、塞栓やライゲーション技術の使用などの他の実験設定は、このプロトコルに記載されているように、脊髄レーザー/ドップラー針プローブ評価と組み合わせることができる。
開示事項
コンスタンティンJ.Cトレプテは、マケの講義で名誉賞を受賞しました。他のすべての著者は、利益相反を宣言しません。この研究は、欧州麻酔学会ヤング・インカテ立探偵助成金2018によって支援されました。
謝辞
著者らは、ハノーバー医科大学動物研究所のレナ・ブリックス(V.M.D)と、ドイツのハンブルク・エペンドルフ大学医療センターの研究動物ケア施設であるジュッタ・ダムマン夫人に、術前および周産期動物ケアと動物の取り扱いに関する技術的支援を提供してくれたことに感謝したいと考えている。著者らはさらに、ルクセンブルクのオピタル・キルヒベルク血管外科のダニエル・マンゾーニ博士の技術支援に感謝したいと考えています。
資料
| Name | Company | Catalog Number | Comments |
| CardioMed Flowmeter | Medistim AS, Oslo, Norway | CM4000 | Flowmeter for Flow-Probe Femoral Artery |
| CardioMed Flow-Probe, 5mm | Medistim AS, Oslo, Norway | PS100051 | Flow-Probe Femoral Artery |
| COnfidence probe, | Transonic Systems Inc., Ithaca, NY, USA | MA16PAU | Flow-Probe Aorta |
| 16 mm liners | |||
| DIVA Sevoflurane Vapor | Dräger Medical, Lübeck, Germany | Vapor | |
| Hotline Level 1 Fluid Warmer | Smiths Medical Germany GmbH, Grasbrunn, Germany | HL-90-DE-230 | Fluid Warmer |
| Infinity Delta | Dräger Medical, Lübeck, Germany | Basic Monitoring Hardware | |
| Infinity Hemo | Dräger Medical, Lübeck, Germany | Basic Pressure Monitoring and Pulmonary Thermodilution Hardware | |
| LabChart Pro | ADInstruments Ltd., Oxford, UK | v8.1.16 | Synchronic Laser-Doppler, Blood Pressure, ECG and Blood-Flow Aquisition Software |
| LiquoGuard 7 | Möller Medical GmbH, Fulda, Germany | Cerebrospinal Fluid Drainage System | |
| Millar Micro-Tip Pressure Catheter (5F, Single, Curved, 120cm, PU/WD) | ADInstruments Ltd., Oxford, UK | SPR-350 | Pressure-Tip Catheter Aorta |
| moor VMS LDF | moor Instruments, Devon, UK | Designated Laser-Doppler Hardware | |
| moor VMS Research Software | moor Instruments, Devon, UK | Designated Laser-Doppler Software | |
| Perivascular Flow Module | Transonic Systems Inc., Ithaca, NY, USA | TS 420 | Flow-Module for Flow-Probe Aorta |
| PiCCO 2, Science Version | Getinge AB, Göteborg, Sweden | v. 6.0 | Blood Pressure and Transcardiopulmonary Monitoring Hard- and Software |
| PiCCO 5 Fr. 20cm | Getinge AB, Göteborg, Sweden | Thermistor-tipped Arterial Line | |
| PowerLab | ADInstruments Ltd., Oxford, UK | PL 3516 | Synchronic Laser-Doppler, Blood Pressure, ECG and Blood-Flow Aquisition Hardware |
| QuadBridgeAmp | ADInstruments Ltd., Oxford, UK | FE 224 | Four Channel Bridge Amplifier for Laser-Doppler and Invasive Blood Pressure Aquisition |
| Silverline | Spiegelberg, Hamburg, Germany | ELD33.010.02 | Cerebrospinal Fluid Drainage |
| SPSS statistical software package | IBM SPSS Statistics Inc., Armonk, New York, USA | v. 27 | Statistical Software |
| Twinwarm Warming System | Moeck & Moeck GmbH, Hamburg, Germany | 12TW921DE | Warming System |
| Universal II Warming Blanket | Moeck & Moeck GmbH, Hamburg, Germany | 906 | Warming Blanket |
| VP 3 Probe, 8mm length (individually manufactured) | moor Instruments, Devon, UK | Laser-Doppler Probe | |
| Zeus | Dräger Medical, Lübeck, Germany | Anesthesia Machine |
参考文献
- Etz, C. D., et al. Contemporary spinal cord protection during thoracic and thoracoabdominal aortic surgery and endovascular aortic repair: a position paper of the vascular domain of the European Association for Cardio-Thoracic Surgerydagger. The European Journal of Cardio-Thoracic Surgery. 47 (6), 943-957 (2015).
- Schraag, S. Postoperative management. Best Practice & Research Clinical Anaesthesiology. 30 (3), 381-393 (2016).
- Cambria, R. P., et al. Thoracoabdominal aneurysm repair: results with 337 operations performed over a 15-year interval. Annals of Surgery. 236 (4), 471-479 (2002).
- Becker, D. A., McGarvey, M. L., Rojvirat, C., Bavaria, J. E., Messe, S. R. Predictors of outcome in patients with spinal cord ischemia after open aortic repair. Neurocritical Care. 18 (1), 70-74 (2013).
- McGarvey, M. L., et al. The treatment of spinal cord ischemia following thoracic endovascular aortic repair. Neurocritical Care. 6 (1), 35-39 (2007).
- Fukui, S., et al. Development of collaterals to the spinal cord after endovascular stent graft repair of thoracic aneurysms. European Journal of Vascular and Endovascular Surgery. 52 (6), 801-807 (2016).
- Augoustides, J. G., Stone, M. E., Drenger, B. Novel approaches to spinal cord protection during thoracoabdominal aortic interventions. Current Opinion in Anesthesiology. 27 (1), 98-105 (2014).
- Bicknell, C. D., Riga, C. V., Wolfe, J. H. Prevention of paraplegia during thoracoabdominal aortic aneurysm repair. European Journal of Vascular and Endovascular Surgery. 37 (6), 654-660 (2009).
- Feezor, R. J., Lee, W. A. Strategies for detection and prevention of spinal cord ischemia during TEVAR. Seminars in Vascular Surgery. 22 (3), 187-192 (2009).
- Heidemann, F., et al. Incidence, predictors, and outcomes of spinal cord ischemia in elective complex endovascular aortic repair: An analysis of health insurance claims. Journal of Vascular Surgery. , (2020).
- Rizvi, A. Z., Sullivan, T. M. Incidence, prevention, and management in spinal cord protection during TEVAR. Journal of Vascular Surgery. 52 (4), 86-90 (2010).
- Wortmann, M., Bockler, D., Geisbusch, P. Perioperative cerebrospinal fluid drainage for the prevention of spinal ischemia after endovascular aortic repair. Gefasschirurgie. 22, 35-40 (2017).
- Saugel, B., Trepte, C. J., Heckel, K., Wagner, J. Y., Reuter, D. A. Hemodynamic management of septic shock: is it time for "individualized goal-directed hemodynamic therapy" and for specifically targeting the microcirculation. Shock. 43 (6), 522-529 (2015).
- Moore, J. P., Dyson, A., Singer, M., Fraser, J. Microcirculatory dysfunction and resuscitation: why, when, and how. British Journal of Anaesthesia. 115 (3), 366-375 (2015).
- De Backer, D., Creteur, J., Preiser, J. C., Dubois, M. J., Vincent, J. L. Microvascular blood flow is altered in patients with sepsis. American Journal of Respiratory and Critical Care Medicine. 166 (1), 98-104 (2002).
- De Backer, D., Creteur, J., Dubois, M. J., Sakr, Y., Vincent, J. L. Microvascular alterations in patients with acute severe heart failure and cardiogenic shock. American Heart Journal. 147 (1), 91-99 (2004).
- Sakr, Y., Dubois, M. J., De Backer, D., Creteur, J., Vincent, J. L. Persistent microcirculatory alterations are associated with organ failure and death in patients with septic shock. Critical Care Medicine. 32 (9), 1825-1831 (2004).
- Trzeciak, S., et al. Early microcirculatory perfusion derangements in patients with severe sepsis and septic shock: relationship to hemodynamics, oxygen transport, and survival. Annals of Emergency Medicine. 49 (1), 88-98 (2007).
- Donati, A., et al. From macrohemodynamic to the microcirculation. Critical Care Research and Practice. 2013, 892710 (2013).
- Hamamoto, Y., Ogata, T., Morino, T., Hino, M., Yamamoto, H. Real-time direct measurement of spinal cord blood flow at the site of compression: relationship between blood flow recovery and motor deficiency in spinal cord injury. Spine. 32 (18), 1955-1962 (2007).
- Soubeyrand, M., et al. Real-time and spatial quantification using contrast-enhanced ultrasonography of spinal cord perfusion during experimental spinal cord injury. Spine. 37 (22), 1376-1382 (2012).
- Han, S., et al. Rescuing vasculature with intravenous angiopoietin-1 and alpha v beta 3 integrin peptide is protective after spinal cord injury. Brain. 133, 1026-1042 (2010).
- Muradov, J. M., Ewan, E. E., Hagg, T. Dorsal column sensory axons degenerate due to impaired microvascular perfusion after spinal cord injury in rats. Experimental Neurology. 249, 59-73 (2013).
- Guillen, J., , . FELASA guidelines and recommendations. J Am Assoc Lab Anim Sci. 51, 311-321 (2012).
- Kilkenny, C., Browne, W. J., Cuthill, I. C., Emerson, M., Altman, D. G. Improving bioscience research reporting: the ARRIVE guidelines for reporting animal research. Osteoarthritis Cartilage. 20, 256-260 (2012).
- Ospina-Tascon, G., et al. Effects of fluids on microvascular perfusion in patients with severe sepsis. Intensive Care Medicine. 36 (6), 949-955 (2010).
- Pottecher, J., et al. Both passive leg raising and intravascular volume expansion improve sublingual microcirculatory perfusion in severe sepsis and septic shock patients. Intensive Care Medicine. 36 (11), 1867-1874 (2010).
- De Backer, D., Ortiz, J. A., Salgado, D. Coupling microcirculation to systemic hemodynamics. Current Opinion in Critical Care. 16 (3), 250-254 (2010).
- van Genderen, M. E., et al. Microvascular perfusion as a target for fluid resuscitation in experimental circulatory shock. Critical care medicine. 42 (2), 96-105 (2014).
- Ince, C. Hemodynamic coherence and the rationale for monitoring the microcirculation. Critical care. 19, 8 (2015).
- Kise, Y., et al. Directly measuring spinal cord blood flow and spinal cord perfusion pressure via the collateral network: correlations with changes in systemic blood pressure. Journal of Thoracic and Cardiovascular Surgery. 149 (1), 360-366 (2015).
- Haunschild, J., et al. Detrimental effects of cerebrospinal fluid pressure elevation on spinal cord perfusion: first-time direct detection in a large animal model. European Journal of Cardio-Thoracic Surgery. 58 (2), 286-293 (2020).
- Wipper, S., et al. Impact of hybrid thoracoabdominal aortic repair on visceral and spinal cord perfusion: The new and improved SPIDER-graft. Journal of Thoracic and Cardiovascular Surgery. 158 (3), 692-701 (2019).
- Kluttig, R., et al. Invasive hemodynamic monitoring of aortic and pulmonary artery hemodynamics in a large animal model of ARDS. Journal of Visualized Experiments. (141), e57405 (2018).
- Detter, C., et al. Fluorescent cardiac imaging: a novel intraoperative method for quantitative assessment of myocardial perfusion during graded coronary artery stenosis. Circulation. 116 (9), 1007-1014 (2007).
- Wipper, S., et al. Distinction of non-ischemia inducing versus ischemia inducing coronary stenosis by fluorescent cardiac imaging. International Journal of Cardiovascular Imaging. 32 (2), 363-371 (2016).
- Etz, C. D., et al. Spinal cord blood flow and ischemic injury after experimental sacrifice of thoracic and abdominal segmental arteries. European Journal of Cardio-Thoracic Surgery. 33 (6), 1030-1038 (2008).
- Saugel, B., Scheeren, T. W. L., Teboul, J. L. Ultrasound-guided central venous catheter placement: a structured review and recommendations for clinical practice. Critical care. 21 (1), 225 (2017).
- Marty, B., et al. Partial inflow occlusion facilitates accurate deployment of thoracic aortic endografts. Journal of Endovascular Therapy. 11 (2), 175-179 (2004).
- Matyal, R., et al. Monitoring the variation in myocardial function with the Doppler-derived myocardial performance index during aortic cross-clamping. Journal of Cardiothoracic and Vascular Anesthesia. 26 (2), 204-208 (2012).
- Miller, R. D. . Miller'sanesthesia. 8th Edition. , (2015).
- Martikos, G., et al. Remote ischemic preconditioning decreases the magnitude of hepatic ischemia-reperfusion injury on a swine model of supraceliac aortic cross-clamping. Annals of Vascular Surgery. 48, 241-250 (2018).
- Lazaris, A. M., et al. Protective effect of remote ischemic preconditioning in renal ischemia/reperfusion injury, in a model of thoracoabdominal aorta approach. Journal of Surgical Research. 154 (2), 267-273 (2009).
- Ince, C., et al. Second consensus on the assessment of sublingual microcirculation in critically ill patients: results from a task force of the European Society of Intensive Care Medicine. Intensive Care Medicine. 44 (3), 281-299 (2018).
- Edul, V. S., et al. Dissociation between sublingual and gut microcirculation in the response to a fluid challenge in postoperative patients with abdominal sepsis. Annals of intensive care. 4, 39 (2014).
- Schierling, W., et al. Sonographic real-time imaging of tissue perfusion in a porcine haemorrhagic shock model. Ultrasound in Medicine and Biology. 45 (10), 2797-2804 (2019).
- Jing, Y., Bai, F., Chen, H., Dong, H. Using Laser Doppler Imaging and Monitoring to Analyze Spinal Cord Microcirculation in Rat. Journal of Visualized Experiments. (135), e56243 (2018).
- Jing, Y., Bai, F., Chen, H., Dong, H. Meliorating microcirculatory with melatonin in rat model of spinal cord injury using laser Doppler flowmetry. Neuroreport. 27 (17), 1248-1255 (2016).
- Jing, Y., Bai, F., Chen, H., Dong, H. Melatonin prevents blood vessel loss and neurological impairment induced by spinal cord injury in rats. Journal of Spinal Cord Medicine. 40 (2), 222-229 (2017).
- Phillips, J. P., Cibert-Goton, V., Langford, R. M., Shortland, P. J. Perfusion assessment in rat spinal cord tissue using photoplethysmography and laser Doppler flux measurements. Journal of Biomedical Optics. 18 (3), 037005 (2013).
- Glenny, R. W., Bernard, S. L., Lamm, W. J. Hemodynamic effects of 15-microm-diameter microspheres on the rat pulmonary circulation. Journal of Applied Physiology. 89 (1985), 499-504 (2000).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved