Simulazioni fluidodinamiche computazionali del flusso sanguigno in un aneurisma cerebrale
Panoramica
Fonte: Joseph C. Muskat, Vitaliy L. Rayz e Craig J. Goergen, Weldon School of Biomedical Engineering, Purdue University, West Lafayette, Indiana
L'obiettivo di questo video è descrivere i recenti progressi delle simulazioni fluidodinamiche computazionali (CFD) basate sulla vascolarizzazione specifica del paziente o dell'animale. Qui sono state create segmentazioni delle navi basate su argomenti e, utilizzando una combinazione di strumenti open source e commerciali, è stata determinata una soluzione numerica ad alta risoluzione all'interno di un modello di flusso. Numerosi studi hanno dimostrato che le condizioni emodinamiche all'interno della vascolarizzazione influenzano lo sviluppo e la progressione dell'aterosclerosi, degli aneurismi e di altre malattie delle arterie periferiche; allo stesso tempo, le misurazioni dirette della pressione intraluminale, dello sforzo di taglio della parete (WSS) e del tempo di residenza delle particelle (PRT) sono difficili da acquisire in vivo.
La CFD consente di valutare tali variabili in modo non invasivo. Inoltre, la CFD viene utilizzata per simulare le tecniche chirurgiche, il che fornisce ai medici una migliore lungimiranza per quanto riguarda le condizioni di flusso post-operatorio. Due metodi di risonanza magnetica (MRI), angiografia a risonanza magnetica (MRA) con tempo di volo (TOF-MRA) o MRA con contrasto potenziato (CE-MRA) e contrasto di fase (PC-MRI), ci consentono di ottenere geometrie dei vasi e campi di velocità 3D risolti nel tempo, rispettivamente. TOF-MRA si basa sulla soppressione del segnale dal tessuto statico mediante impulsi RF ripetuti che vengono applicati al volume dell'immagine. Un segnale è ottenuto da spin insaturi che si muovono nel volume con il sangue che scorre. CE-MRA è una tecnica migliore per l'imaging di vasi con flussi di ricircolo complessi, in quanto utilizza un agente di contrasto, come il gadolinio, per aumentare il segnale.
Separatamente, PC-MRI utilizza gradienti bipolari per generare sfasazioni proporzionali alla velocità di un fluido, fornendo così distribuzioni di velocità risolte nel tempo. Mentre la PC-MRI è in grado di fornire velocità di flusso sanguigno, l'accuratezza di questo metodo è influenzata dalla limitata risoluzione spaziotemporale e dalla gamma dinamica della velocità. La CFD fornisce una risoluzione superiore e può valutare la gamma di velocità dai getti ad alta velocità ai vortici a ricircolo lento osservati nei vasi sanguigni malati. Pertanto, anche se l'affidabilità della CFD dipende dalle ipotesi di modellazione, apre la possibilità di una rappresentazione completa e di alta qualità dei campi di flusso specifici del paziente, che possono guidare la diagnosi e il trattamento.
Principi
TOF-MRA, CE-MRA e PC-MRI sono spesso usati come geometria di input e condizioni al contorno del flusso per le simulazioni CFD. Come discusso in precedenza, la geometria del vaso e le condizioni al contorno dell'afflusso (profili di velocità attraverso una sezione trasversale) sono misurate per ciascun soggetto. Per i dati inclusi in questo studio, la risoluzione TOF-MRA era 0,26 x 0,26 x 0,50 mm, mentre la risoluzione PC-MRI era 1,00 x 1,00 x 1,20 mm. La sequenza 4D Flow MRI è stata utilizzata per acquisire la distribuzione tridimensionale della velocità attraverso il ciclo cardiaco. I dati TOF vengono segmentati pseudo-automaticamente con una varietà di strumenti. La risoluzione dell'immagine, cioè la dimensione di un voxel, influenza direttamente la qualità del modello risultante della geometria. 4D Flow MRI determina la velocità  del sangue ad ogni voxel utilizzando lo sfasamento secondo le seguenti
del sangue ad ogni voxel utilizzando lo sfasamento secondo le seguenti 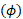 equazioni:
equazioni:
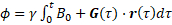 (1)
(1)
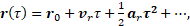 (2)
(2)
Gli sfasamenti e le velocità misurati dipendono dal campo del 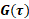 gradiente, dal rapporto giromagnetico,
gradiente, dal rapporto giromagnetico,  dalla posizione iniziale dello
dalla posizione iniziale dello 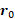 spin, dalla velocità di spin
spin, dalla velocità di spin  e dall'accelerazione di
e dall'accelerazione di 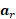 spin. I campi magnetici e le costanti di materiale vengono definiti durante l'inizializzazione della risonanza magnetica. La risonanza magnetica 4D Flow codifica in tre direzioni ortogonali per ottenere campi di velocità tridimensionali. Quindi, è possibile generare modelli 3D per ogni caso specifico del paziente o dell'animale. I metodi dettagliati nella sezione della procedura ci porteranno a una simulazione CFD risolvendo numericamente le equazioni di Navier-Stokes, che sono generalizzate come:
spin. I campi magnetici e le costanti di materiale vengono definiti durante l'inizializzazione della risonanza magnetica. La risonanza magnetica 4D Flow codifica in tre direzioni ortogonali per ottenere campi di velocità tridimensionali. Quindi, è possibile generare modelli 3D per ogni caso specifico del paziente o dell'animale. I metodi dettagliati nella sezione della procedura ci porteranno a una simulazione CFD risolvendo numericamente le equazioni di Navier-Stokes, che sono generalizzate come:
 (3)
(3)
dove  è densità,
è densità, 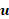 è velocità di flusso, p è pressione e mu è la viscosità dinamica del flusso.
è velocità di flusso, p è pressione e mu è la viscosità dinamica del flusso.
Procedura
Un precursore del tutorial è la creazione di un modello vascolare specifico per il paziente. In questa dimostrazione, gli strumenti Materialise Mimics, 3D Systems Geomagic Design X e Altair HyperMesh sono stati utilizzati per generare una mesh di volume tetraedrico dai dati MRA.
1. Genera le mezze linee di mezzeria della nave per il modello
- Apri la GUI python di vmtk-launcher. In PypePad, digitare: vmtkcenterlines -ifile [file STL salvato sul desktop].stl -ofile [nome STL]centerlines.vtp
- Selezionare Esegui, Esegui tutto per caricare i dati nel programma. Si aprirà una nuova finestra che visualizza le istruzioni e un rendering del modello di input. Ruotate il modello e posizionate il curser su ogni posizione di ingresso. Premere la barra spaziatrice per posizionare un seme.
- Dopo aver posizionato i semi su tutte le insenature, premere 'Q' per continuare. Ripeti lo stesso posizionamento dei semi per tutte le prese. Dopo aver posizionato i semi di uscita, premere nuovamente 'Q' e lasciare che il programma funzioni. In questo modo il file della linea di mezzeria verrà salvato sul desktop.
2. Configurazione dei dati nel software di visualizzazione
- Avviare lo strumento di visualizzazione open source ParaView (versione 5.4.1 utilizzata in questa procedura).
- Selezionare File, Apri...e individuare i file creati in precedenza: la mesh del volume specifica del paziente, i file centerline e i file EnSight.case. Dopo aver fatto clic su Ok, tutti i dati devono essere caricati nell'interfaccia.
- Nella tabella Proprietà in basso a sinistra, selezionare Applica. Questo comando caricherà e leggerà tutte le informazioni che un utente ha caricato o modificato in ParaView. Evidenziate la mesh del volume facendo clic sul relativo nome nel Browser pipeline per attivare questa selezione.
- Ancora una volta, nella tabella Proprietà, scorrere e modificare il valore di Opacità in un valore compreso tra 0,2 e 0,5. Ora, gli assi di mezzeria e i rendering geometrici dovrebbero essere visibili.
3. Rimappare i dati MRI 4D Flow con la griglia mesh volumetrica ed eliminare il rumore
- Dal menu in alto, selezionare Filtri, Alfabetico, RicampionaWithDataset. Si aprirà una nuova finestra. Impostate Source come mesh del volume e Input come file EnSight.case. Selezionare OK una volta impostati.
- Nella tabella Proprietà selezionare Applica per applicare il filtro.
- Come in precedenza, evidenziare il nuovo nome ResampleWithDataset# per attivarlo. Ridurre l'opacità di questo nuovo rendering come accennato in precedenza. Inoltre, modificate gli assi di mezzeria da Superficie a Punti (Points) nel menu in alto.
4. Determinare le condizioni al contorno del flusso in ingresso e in uscita
- Sul lato destro dell'interfaccia, accanto a ingrandire e ridurre al minimo le opzioni di rendering, selezionare lo strumento Crea vista (quadrato con linea verticale). Selezionare l'opzione Visualizzazione foglio di 146.
- Dalla casella a discesa Visualizzazione, selezionare i file dell'asse di mezzeria. È possibile selezionare un solo tipo di file alla volta. Scorrere i dati, selezionando vari punti per identificare una posizione all'interno di ciascun ingresso e uscita.
- Ora, usa la vista Foglio di calcolo sotto i punti per calcolare il vettore normale tra due punti vicino alle stesse posizioni trovate in (4.2).
- Dopo aver trovato il vettore normale per ogni posizione di ingresso e uscita, selezionare Filtri, Alfabetico, Sezione. Assicurarsi di attivare resampleWithDataset# in anticipo.
- Il filtro Slice deve essere visualizzato sotto un nuovo ramo proveniente da ResampleWithDataset#. Nella tabella Proprietà,impostate l'origine del piano come la stessa posizione del punto XYZ per uno dei due punti utilizzati per calcolare il vettore normale. Utilizzare il vettore normale da (4.3) per compilare i valori normali. Seleziona Applica.
- Evidenziare/attivare il filtro Slice# appena creato e selezionare Filtri, Alfabetico, Flusso superficiee quindi Applica. Attivare il nuovo elemento SurfaceFlow# nel Browser pipelinee applicare Filtri, Alfabetico , Raggruppa passi temporali, Applica.
- In Visualizzazione Foglio di disegno di disegnoaprire i dati GroupTimeSteps#. Esporta questi dati in Microsoft Excel tramite copia e incolla o usa Esporta foglio di calcolo.
- In Excel, calcolare i valori ponderati corrispondenti al rapporto tra la portata in ogni uscita e la portata totale in ingresso. A causa del rumore intrinseco e dell'errore dei dati MRI 4D Flow, identificare la nave più piccola (generalmente con dati meno affidabili) da lasciare "aperta" per garantire la conservazione della massa.
- Nel software di simulazione CFD, le forme d'onda a flusso transitorio vengono importate utilizzando il comando read-transient-tables; pertanto, salvare i dati del flusso di ingresso in un formato compatibile e .txt descritto nelle esercitazioni online.
5. Impostare simulazioni CFD
- Software di simulazione CFD aperto. Qui usiamo ANSYS Fluent (versione 18.1 descritta in questa procedura come predefinita). Scegliete File, Letturae Maiuscole/minuscole...e aprite il file .cas della mesh del volume utilizzato in precedenza in ParaView. Visualizzare la mesh (questa procedura utilizza un file .cas generato con Altair HyperMesh) selezionando Visualizza..., Visualizza.
- È importante ridimensionare la geometria per garantire la dimensione fisica corretta del modello. Selezionare Scala... e applicare la conversione dell'unità necessaria per il caso specifico, quindi Chiudi.
- Selezionare Materiali, Crea/Modifica per immettere le proprietà del materiale per il sangue. Questo tutorial utilizza valori fisiologicamente rilevanti di 1060 kg/s e 0,0035 kg/ms rispettivamente per densità e viscosità.
- Impostare le condizioni al contorno del flusso transitorio prescrivendo il flusso di massa o le portate di velocità in funzione del tempo per ciascun ingresso. Utilizzare le forme d'onda ottenute dalla misurazione MRI 4D Flow per prescrivere le condizioni al contorno di ingresso. Alle prese vengono indicati valori ponderati che si trovano in (4.8).
- In Soluzione, Metodi, imposta gli schemi numerici utilizzati per la discretizzazione spaziale e temporale delle equazioni di Navier-Stokes. Per questa procedura, utilizzare Accoppiato , che consente l'accoppiamentopressione-velocità completa, Least Squares Cell Based (gradiente), Schema del Secondo Ordine per la pressione, Schema MUSCL del Terzo Ordine per le equazioni della quantità di moto e Schema implicito del Secondo Ordine per la discretizzazione nel tempo. Assicurarsi che il parametro Time in alto a sinistra sia stato impostato su Transient.
- In Soluzione, Inizializzazione, selezionare Inizializzazione standard. Con tutti i valori iniziali impostati su 0, selezionare Inizializza. Ora il programma è impostato per l'esecuzione. Designare una cartella della soluzione per salvare i risultati ogni salvataggio automatico ogni (passaggi temporali) sotto Attività di calcolo.
- Nei passaggi finali, impostare le dimensioni dei passaggi temporaliin Esegui calcolo. Utilizzare i dati delle condizioni al contorno di Excel in (4.7) per determinare questo valore. La riduzione del passo temporale facilita la convergenza e migliora la precisione della soluzione numerica, aumentando al contempo il tempo di soluzione. È buona norma eseguire la simulazione per almeno tre cicli cardiaci completi per eliminare l'effetto dei transitori iniziali.
- Infine, imposta Iterazioni massime per ogni passaggio temporale compreso tra 300 e 500. Il software interromperà automaticamente le iterazioni ad ogni passaggio temporale una volta raggiunta la convergenza e procederà al passaggio temporale successivo. La convergenza può essere migliorata eseguendo una simulazione di flusso costante con valori di velocità medi e quindi utilizzando i risultati come condizioni iniziali per la simulazione del flusso pulsatile. Selezionare Calcola quando si è pronti per eseguire il risolutore.
- Il software eseguirà ogni iterazione fino a quando non viene raggiunta la convergenza o Max Iterations fa sì che l'iterazione continui. I file verranno salvati automaticamente nella posizione da (5.5) e i dati della soluzione potranno essere visualizzati nel software ANSYS CFD-Post o ParaView.
Risultati
In questa dimostrazione, è stato generato un modello specifico per soggetto di un aneurisma cerebrale e la CFD è stata utilizzata per simulare il campo di flusso. Fornendo caratteristiche di flusso dettagliate e quantificando le forze emodinamiche non ottenibili dai dati di imaging, la CFD può essere utilizzata per aumentare i dati MRI 4D Flow a bassa risoluzione. La Figura 1 mostra come la CFD fornisce una descrizione più completa del flusso nelle regioni vicine alla parete e ricircolanti.
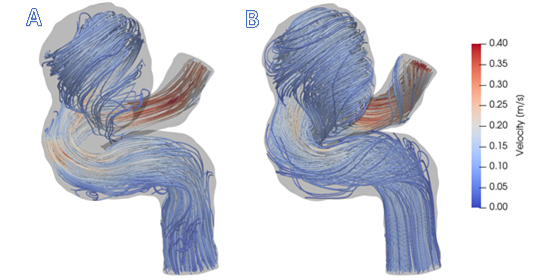
Figura 1: A) Visualizzazione dei dati MRI 4D Flow all'interno della geometria del vaso. B) Visualizzazione dei risultati della simulazione CFD. In generale, le semplificazioni CFD forniscono una comprensione più completa dei modelli di flusso sanguigno all'interno di questo aneurisma cerebrale.
La Figura 1 mostra che i risultati CFD sono in accordo con la risonanza magnetica a flusso 4D in vivo. La Figura 1 (A) mostra i complessi modelli di flusso a ricircolo all'interno della regione aneurismatica, la dilatazione a palloncino dell'arteria, che sono stati rilevati con la risonanza magnetica 4D Flow. Tuttavia, le regioni di flusso stagnante nelle sezioni superiore e inferiore della lesione non sono piene di linee aerodinamiche. Questo perché il rapporto segnale/rumore in queste regioni è basso. Il flusso simulato da CFD, mostrato nella Figura 1 (B), fornisce un campo di velocità di risoluzione più elevato, in particolare vicino alle pareti del vaso. Pertanto, i modelli CFD sono in grado di fornire stime di maggiore accuratezza di metriche derivate dal flusso clinicamente rilevanti, come pressione, WSS e PRT, che possono essere utilizzate per prevedere la progressione della malattia aneurismatica.
Inoltre, le simulazioni CFD possono essere utilizzate per modellare le condizioni del flusso postoperatorio che risulterebbero da opzioni di trattamento alternative. Ad esempio, la Figura 2 (A) e (B) confrontano il flusso attraverso la stessa nave con diverse velocità di afflusso. Prescrivendo varie condizioni al contorno, come simulare l'occlusione dei vasi senza flusso, viene mostrato il flusso dopo una varietà di trattamenti chirurgici.

Figura 2: A) Simulazione per il clipping chirurgico dell'arteria cerebrale anteriore destra (ACA). B) Simulazione per il clipping chirurgico dell'ACA sinistro. Per semplicità, questa cifra mantiene la velocità di afflusso preoperatoria all'ingresso non modificato; in realtà, la portata aumenterebbe nella nave aperta per compensare. C) Le normali velocità di flusso sanguigno prescrivono le condizioni di ingresso per questo modello. I dati dei pazienti provenienti dalla risonanza magnetica 4D Flow forniscono le condizioni di ingresso per una visualizzazione realistica dei modelli di flusso.
La capacità di simulare i campi di flusso postoperatorio derivanti da vari trattamenti chirurgici è un importante vantaggio dei modelli CFD. Applicando geometrie realistiche e specifiche del paziente e dati di afflusso, è possibile dimostrare diversi scenari di trattamento per fornire ai medici informazioni sull'effetto di una procedura pianificata sui modelli di flusso. Ad esempio, la Figura 2 (A) e (B) mostrano i flussi di ricircolo che si verificherebbero se l'una o l'altra arteria prossimale fosse tagliati. Trattamenti come il clipping dei vasi o l'implementazione di un deviatore di flusso possono essere simulati, consentendo a medici e pazienti di decidere cosa funzionerà meglio in ogni caso specifico.
Applicazione e Riepilogo
Il framework qui descritto può essere utilizzato per eseguire simulazioni CFD specifiche per il paziente. Una mesh ad alta risoluzione viene utilizzata per interpolare i dati MRI 4D Flow a bassa risoluzione; questo isola i dati di flusso e riduce al minimo gli errori associati al rumore esterno alla parete del serbatoio. Utilizzando condizioni al contorno basate sul paziente per i flussi di ingresso e uscita, la simulazione è in grado di abbinare le condizioni emodinamiche immaginate con la risonanza magnetica.
Nuovi metodi per PC-MRI sono in grado di mostrare intervalli di velocità dinamiche più ampi. Tuttavia, questo è severamente limitato dal tempo di scansione del paziente. Spesso, i dati dei pazienti vengono acquisiti a risoluzioni inferiori per ridurre il tempo trascorso all'interno dello scanner. Sfortunatamente, ciò può comportare dati con alias o drop-off del segnale, un problema esacerbato quando il gradiente di codifica della velocità (VENC) è impostato su un livello troppo alto. Questo può perdere dati di flusso lenti e a ricircolo. L'associazione del flusso e della geometria specifici del paziente con la CFD fornisce un metodo efficace per catturare le dinamiche del flusso sanguigno ad alta risoluzione.
Ciò che rende la modellazione basata sul paziente intrinsecamente utile è la sua capacità di fornire informazioni dettagliate senza la necessità di generalizzare tra pazienti, malattie o trattamenti che in genere possiedono caratteristiche molto diverse. Le simulazioni consentono a medici e ingegneri di modellare scenari di trattamento alternativi prima di eseguire una procedura effettiva. La simulazione della dinamica del flusso sanguigno può essere utilizzata per modellare stent devianti di flusso, innesto di bypass arterioso e iniezione di contrasto basata su catetere, tra le altre applicazioni. Mentre i medici e i pazienti desiderano il miglior risultato, la CFD fornisce un metodo per esaminare il flusso post-operatorio, che fornisce una migliore previsione. Oltre a rappresentare il flusso dopo l'introduzione di un dispositivo o di un trattamento, la CFD consente di stimare le sollecitazioni di taglio alla parete. Questo, abbinato alla conoscenza che un basso WSS è spesso correlato alla progressione della malattia arteriosa, consente la previsione o la modellazione delle probabilità. L'utilizzo di strumenti computazionali per identificare i precursori della crescita dell'aneurisma, della formazione di coaguli o dell'emorragia apre la possibilità di identificare prima i pazienti a rischio. In sintesi, la combinazione di dati di immagine specifici del paziente con simulazioni CFD è un potente strumento per la valutazione della malattia e la previsione chirurgica.
RICONOSCIMENTI
Gli autori desiderano ringraziare la dott.ssa Susanne Schnell e Michael Markl della Northwestern University per averci fornito i dati dei pazienti 4D utilizzati nelle nostre figure.
Vai a...
Video da questa raccolta:

Now Playing
Simulazioni fluidodinamiche computazionali del flusso sanguigno in un aneurisma cerebrale
Biomedical Engineering
11.9K Visualizzazioni

Imaging di campioni biologici con microscopia ottica e confocale
Biomedical Engineering
36.3K Visualizzazioni

Imaging di campioni biologici con microscopio elettronico a scansione (SEM)
Biomedical Engineering
24.1K Visualizzazioni

Biodistribuzione dei vettori di nanofarmaci: applicazioni del microscopio elettronico a scansione (SEM)
Biomedical Engineering
9.5K Visualizzazioni

Imaging a ultrasuoni ad alta frequenza dell'aorta addominale
Biomedical Engineering
14.8K Visualizzazioni

Mappatura quantitativa della deformazione di un aneurisma dell'aorta addominale
Biomedical Engineering
4.6K Visualizzazioni

Tomografia fotoacustica per l'immagine di sangue e lipidi nell'aorta infrarenale
Biomedical Engineering
5.9K Visualizzazioni

Imaging a risonanza magnetica cardiaca
Biomedical Engineering
15.0K Visualizzazioni

Imaging a fluorescenza nel vicino-infrarosso di aneurismi dell'aorta addominale
Biomedical Engineering
8.4K Visualizzazioni

Tecniche non invasive di misurazione della pressione sanguigna
Biomedical Engineering
12.1K Visualizzazioni

Acquisizione e analisi di un segnale ECG (elettrocardiogramma)
Biomedical Engineering
106.9K Visualizzazioni

Resistenza alla trazione dei biomateriali riassorbibili
Biomedical Engineering
7.7K Visualizzazioni

Imaging micro-CT di un midollo spinale di topo
Biomedical Engineering
8.3K Visualizzazioni

Visualizzazione della degenerazione dell'articolazione del ginocchio dopo lesione del LCA non invasiva nei ratti
Biomedical Engineering
8.3K Visualizzazioni

Imaging combinato SPECT e CT per la visualizzazione della funzionalità cardiaca
Biomedical Engineering
11.2K Visualizzazioni