Mediciones electroquímicas de catalizadores soportados utilizando un potenciostato/galvanostato
Visión general
Fuente: Laboratorio del Dr. Yuriy Román — Massachusetts Institute of Technology
Un Potenciostato/Galvanostato (referido a menudo como simplemente un potenciostato) es un instrumento que mide la corriente a un potencial aplicado (operación potentiostatic) o medidas de potencial en una corriente aplicada (operación de caracterización) (figura 1). Es el instrumento más comúnmente utilizado en la caracterización electroquímica de materiales del ánodo y del cátodo para las pilas de combustible, electrolizadores, baterías y supercondensadores.
Convencionalmente, estos materiales del ánodo y el cátodo se interconectó con un potenciostato mediante una celda electroquímica de tres electrodos. Los cables de los electrodos de la potenciostato están conectados al electrodo de referencia, el contraelectrodo (a menudo llamado el electrodo auxiliar) y el electrodo de trabajo (que contiene el material de la prueba de interés). La celda electroquímica se llena entonces con una solución de electrolitos de alta fuerza iónica, como una solución ácida, alcalina o sal. Los medios de comunicación para esta solución de alta fuerza iónica son típicamente acuosa; sin embargo, para aplicaciones que requiere mayor operativo windows potencial de la célula, tales como baterías y supercondensadores, medios no acuosos es de uso frecuente. Los medios de comunicación de la célula se desgasifica con un gas inerte (para evitar reacciones secundarias no deseadas) o con un gas de prueba (si la reacción de la prueba consiste en un gas en uno de los electrodos).
Por otra parte, un puente de sal o membrana se emplea para mantener un contacto iónico si las dos mitad células deben medirse en electrolitos diferentes. En Electrocatálisis heterogéneos, este tipo de célula "dos compartimiento" se utiliza a menudo si la molécula de prueba en el electrodo de trabajo es también reactiva en el counterelectrode. Esto sucede con frecuencia como la counterelectrode típicamente empleado es platinum, que es un catalizador muy activo para muchas reacciones. Aquí, se utilizarán las células solo compartimiento, donde todos los tres electrodos están en el mismo medio.
Este video le explicará el proceso de pulido de un electrodo de trabajo, preparar una tinta de catalizador, la tinta de catalizador sobre el electrodo de trabajo de montaje, preparación de la celda electroquímica y luego realizar mediciones electroquímicas. Las mediciones que se realizan incluyen: voltametría cíclica (CV), voltametría de barrido lineal (LSV), redisolución (CP) y chronoamperometry (CA).
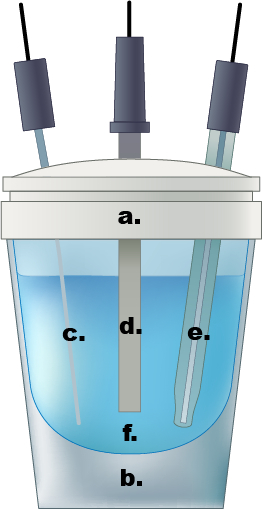
Figura 1. Un ejemplo de una celda electroquímica de compartimiento único. casquillo Teflon a.), b). vidrio celular, c.) Pacífico cable contraelectrodo, d.) electrodo de trabajo, e.) Electrodo de referencia de Ag/AgCl, f.) 0,5 solución de electrolito acuoso ácido sulfúrico M.
Principios
El potenciostato permite aplicar un constante anódico o catódico potencial para el electrodo de trabajo y medir la corriente anódica o catódica resultante (chronoamperometry) o el potenciostato puede ser galvanostatically funcionado vía un circuito de control de retroalimentación y aplicar una constante corriente anódica o catódica con medida potencial variando con el tiempo a mantener esto aplica corriente (redisolución). Como alternativa, espacio potencial puede ser explorada con tiempo usando voltametría cíclica o voltamperometría de barrido lineal para medir los potenciales anódicos y catódicos frente a un tipo de exploración potencial aplicado (la derivada del potencial con respecto al tiempo).
En todas estas técnicas, incluso durante el funcionamiento de la caracterización, el potenciostato controla el potencial aplicado y mide el flujo de electrones desde (el electrodo de trabajo a (desde) el electrodo contador a) cuando el electrodo de trabajo actúa como el ánodo (cátodo). El potencial aplicado es referencia contra el electrodo de referencia, que contiene un sistema redox (por ejemplo, un electrodo de cloruro de plata o un electrodo de calomelanos saturado) con un potencial conocido y estable que está interconectado con la solución electrolítica mediante una frita porosa. Durante el funcionamiento normal, el potenciostato dibuja una corriente insignificante pero distinto de cero por el electrodo de referencia para que un potencial preciso puede ser aplicado al electrodo de trabajo. Mientras que el potenciostato mide el flujo de electrones o de media reacción para el siguiente, la solución electrolítica completa el circuito previniendo la acumulación de carga en el ánodo o el cátodo.
Procedimiento
1. catalizador tinta y preparación del electrodo de trabajo
Precauciones de seguridad: Metales en negro de carbón se deben manejar una caja de campana o equilibrio de humo hasta que quede en forma de suspensión ya que estos polvos son riesgos de inhalación.
- Con un balance cerrado, pesar 5-10 mg de catalizador de metal/carbono negro y añadir a un frasco de vidrio con una tapa.
- Usando una micropipeta, diluir el catalizador con agua, tal que la concentración final es de 7,5 mg de catalizador por cada mL de agua.
- Mientras sonicando, 100 μl de solución de Nafion 117 por mL de agua se añade a la suspensión.
- La tinta debe ser sonicada durante al menos 10 minutos asegurar la dispersión uniforme y completa mezcla de la ayuda del negro de carbón con el agente de enlace.
- Mientras que la tinta es sonicando, un electrodo de disco de 3 mm carbón vidrioso limpias y pulido por frotamiento en un movimiento circular que remolina en un cojín suave alúmina cubierto con la solución de alúmina de 0.05 μm. Se debe luego Enjuagar copiosamente con agua para eliminar la alúmina.
- A continuación, 7 μl de tinta se gotee sobre un electrodo de disco de pulido, de orientación vertical 3 mm carbón vidrioso. El electrodo de trabajo entonces se seca a 80 ° c durante 1 hora si el catalizador es aire-estable o evaporada bajo un vacío débil durante 30 minutos si el catalizador es sensible al aire.
2. celda electroquímica preparación
Precauciones de seguridad: Guantes, labcoat y gafas de seguridad siempre deben ser usados pero es sobre todo primordiales para trabajar con la solución de ácido sulfúrico. Deben derramar cualquier gotas de solución en las muñecas, se debe lavar con jabón y agua durante 15 minutos. Para derrames grandes, eliminación de la ropa contaminada y el uso de los Lavaojos o duchas puede usarse durante 15 min, seguido de una consulta médica. Los conductores eléctricos no deben ser tocados una vez colocado en la celda electroquímica.
- Una celda de vidrio se llena con 10 mL de 0,5 M de H2SO4 y desgasificada para por lo menos 30 min con un flujo de nitrógeno de ultra alta pureza
- Los casquillos de Teflon de las células electroquímicas tienen 3 puertos para el electrodo de referencia, el electrodo de trabajo y contraelectrodo
- El electrodo de referencia Ag/AgCl es quitado de su solución de KCl de 1 M, enjuagarse con agua desionizada y luego colocado en la celda.
- El electrodo de alambre de platino platinados contador es enjuagarse con agua desionizada y luego colocado dentro de la célula.
- El electrodo de trabajo secado enjuagar con agua desionizada y colocan dentro de la célula.
- El potenciostato está activada.
- El cable blanco del electrodo es conectado primero y conectado al electrodo de referencia.
- El cable rojo del electrodo se conecta al electrodo de contador del alambre de Pt.
- El plomo del electrodo verde se conecta al electrodo de trabajo de metal/negro de carbón.
- Una pequeña secuencia de purga de2 N se deja continuamente burbujeo en el electrolito.
- Asegurar cables no se toquen y que no es ningún contacto eléctrico directo entre los 3 electrodos que con la de 0,5 M de H24 electrolito.
3. Análisis electroquímica
- Después de activar el potenciostato, realizar al menos 20 acondicionado ciclos entre 0 y 0.4 V vs RHE a 50 mV/s con CV. Esto se realiza eligiendo CV como técnica y entrar en el potencial superior e inferior límites así como la frecuencia de barrido.
- Voltametría de barrido lineal (LSV) entonces puede realizarse eligiendo LSV como técnica y especificando un potencial inicial, un potencial final y una tarifa de exploración. La frecuencia de barrido para LSV es típicamente mucho menos que CV, generalmente 1-2 mV/s para que sean mucho más bajas que las corrientes derivadas de las reacciones superficiales faradaic corrientes capacitivas
- Chronoamperometry (CA) se realiza eligiendo CA o "amperométrico i t curva como una técnica y especificando el potencial fijo así como la longitud del tiempo el instrumento debe sostener el electrodo de trabajo como este potencial fijo.
- Redisolución (CP) se realiza eligiendo CP como una técnica. CP puede realizarse en una serie de pasos actuales donde se especifica una corriente por un cierto periodo de tiempo seguido de una nueva corriente para un período de tiempo especificado. Estas corrientes aplicadas pueden abarcar anódicos y catódicas corrientes dentro de la misma medida de CP.
- Cuando se termina el análisis electroquímico, apague el potenciostato.
- Desconecte los cables de los electrodos y guardarlos en un lugar seco lejos de líquidos para evitar la corrosión.
- Quitar el electrodo de referencia y enjuague con abundante cantidad de agua desionizada. Vuelva el electrodo de referencia directamente a su solución de almacenamiento de información de KCl de 1 M. La punta de este electrodo no se debe nunca llegar a ser seco.
- Quite el electrodo de Pt alambre contador y enjuague con agua desionizada
- Quite el electrodo de trabajo y enjuague bien con agua DI y entonces utilice un Kimwipe con acetona para quitar fácilmente la tinta catalizador secado de la superficie del electrodo de trabajo. Se recomienda pulir electrodos inmediatamente después del uso.
- Apague la purga de2 N.
- Vaciar el electrolito usado en un recipiente de desechos ácido. Enjuagar la celda de vidrio y tapón de teflón con cantidades copiosas de agua DI.
Resultados
Este procedimiento dará como resultado cifras que contienen diagramas de corriente medida vs potencial para cada una de las cuatro técnicas. Por Convención para CV y LSV, las parcelas se también se genera como corriente medida vs potencial a pesar de la realidad que son técnicas transitorias que miden vs el derivado del tiempo de potencial.
Aplicación y resumen
CV, LSV, CP y CA son técnicas indispensables para determinar la eficacia de los nuevos materiales de electrodo para las pilas de combustible, electrolizadores, baterías y supercondensadores, así como para desarrollar campos tales como la oxidación parcial selectiva o la reducción de productos químicos de la materia. Estos métodos permiten determinar overpotentials de reacciones materiales de electrodo diferentes en comparación con su potencial de equilibrio termodinámico. Estos métodos también permiten la capacidad volumétrica o gravimétrica de supercondensadores que se determinarán. Del mismo modo, las tasas de carga y descarga de electrodos de baterías o supercondensadores pueden determinarse con estas técnicas. Estas técnicas también permiten la caracterización de la estabilidad electroquímica de materiales por determinar. Más allá de estas técnicas básicas, técnicas más avanzadas incluyen la combinación de las técnicas potenciométricas con métodos in situ como IR y espectrometría de masas.
Saltar a...
Vídeos de esta colección:

Now Playing
Mediciones electroquímicas de catalizadores soportados utilizando un potenciostato/galvanostato
Analytical Chemistry
51.4K Vistas

Preparación de muestras para la caracterización analítica
Analytical Chemistry
84.7K Vistas

Estándares internos
Analytical Chemistry
204.8K Vistas

Método de adición estándar
Analytical Chemistry
320.0K Vistas

Curvas de calibración
Analytical Chemistry
796.7K Vistas

Espectroscopía ultravioleta-visible (UV-Vis)
Analytical Chemistry
623.4K Vistas

Espectroscopía de Raman para el análisis químico
Analytical Chemistry
51.2K Vistas

Fluorescencia de rayos x (XRF)
Analytical Chemistry
25.4K Vistas

Cromatografía de gases (CG) con detección de ionización de llama
Analytical Chemistry
282.0K Vistas

Cromatografía de líquidos de alto rendimiento (HPLC)
Analytical Chemistry
384.5K Vistas

Cromatografía de intercambio iónico
Analytical Chemistry
264.5K Vistas

Electroforesis capilar (EC)
Analytical Chemistry
93.9K Vistas

Introducción a la espectrometría de masas
Analytical Chemistry
112.2K Vistas

Microscopía electrónica de barrido (MEB)
Analytical Chemistry
87.2K Vistas

Voltametría cíclica (CV)
Analytical Chemistry
125.1K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados