Cromatografía de gases (CG) con detección de ionización de llama
Visión general
Fuente: Laboratorio del Dr. B. Jill Venton - Universidad de Virginia
Cromatografía de gases (GC) se utiliza para separar y detectar compuestos de pequeño peso molecular en la fase gaseosa. La muestra es un gas o un líquido que se vaporiza en el puerto de inyección. Por lo general, los compuestos analizados son Da menos de 1.000, porque es difícil vaporizar los compuestos más grandes. GC es popular para aplicaciones industriales y monitoreo del medio ambiente porque es muy confiable y puede funcionar casi continuamente. GC se utiliza normalmente en aplicaciones donde se detectan pequeñas moléculas volátiles y con soluciones no acuosas. Cromatografía de líquidos es más popular para mediciones en muestras acuosas y puede ser utilizada para el estudio de moléculas más grandes, porque las moléculas no es necesario vaporizar. GC es favorecido para las moléculas no polares, mientras que LC es más común para la separación de analitos polares.
La fase móvil para cromatografía de gases es un gas portador, típicamente helio debido a su bajo peso molecular y ser químicamente inerte. Se aplica presión y la fase móvil mueve el analito a través de la columna. La separación se logra utilizando una columna recubierta de una fase estacionaria. Columnas capilares tubulares abiertas son las columnas más populares y la fase estacionaria en las paredes del tubo capilar. Fases estacionarias son a menudo derivados de polidimetilsiloxano, con 5 – 10% de los grupos funcionalizados para afinar la separación. Grupos funcionales típicos son los grupos fenilo, cianopropilo o trifluoropropyl. Columnas capilares suelen ser 5-50 m de largo. Columnas más estrechas tienen mayor resolución pero requieren presiones más altas. También pueden utilizar columnas llenas donde la fase estacionaria está revestida sobre granos de lleno en la columna. Columnas llenas son más cortos, 1 – 5 m. capilares tubulares abiertos son generalmente preferidos porque permite una mayor eficiencia, análisis más rápidos y tienen mayor capacidad.
Detección de ionización de llama (FID) es un buen detector general de compuestos orgánicos en GC que detecta la cantidad de carbono en una muestra. Después de la columna, las muestras se queman en una llama de hidrógeno-aire caliente. Los iones de carbono son producidos por la combustión. Mientras que la eficiencia global del proceso es baja (sólo 1 de cada 105 iones de carbono producen un ion en la llama) la cantidad total de iones es directamente proporcional a la cantidad de carbono en la muestra. Electrodos se utilizan para medir la corriente de los iones. FID es un detector destructivo, ya que toda la muestra es pyrolyzed. FID es inafectado por el agua y los gases no combustibles.
Principios
El equilibrio para cromatografía de gases es repartir, y los componentes de la muestra serán la partición (es decir, distribuir) entre las dos fases: la fase estacionaria y la fase móvil. Compuestos que tienen mayor afinidad por la fase estacionaria pasan más tiempo en la columna y elución después así y tienen un tiempo de retención (tR) que las muestras que tienen una mayor afinidad por la fase móvil. Afinidad por la fase estacionaria es conducida principalmente por interacciones intermoleculares y la polaridad de la fase estacionaria puede ser elegida para maximizar las interacciones y por lo tanto la separación. Ideal picos son distribuciones Gaussian y simétrico, debido a la naturaleza aleatoria de la interacción del analito con la columna. Características de pico asimétrico, como el pico al frente o jales, pueden ser debido a la sobrecarga de la columna, problemas de inyección o la presencia de adsorción grupos funcionales tales como ácidos carboxílicos.
En cromatografía gaseosa, la temperatura se ajusta para cambiar el equilibrio y por lo tanto los tiempos de elución. Separaciones en GC se basan en volatilidad porque sustancias de punto de ebullición más alto pueden condensarse en una columna si la temperatura es baja, así que no se eluyen o toman mucho tiempo en eluir. Se realizan separaciones isotérmicas a una temperatura o gradiente separaciones se llevan a cabo donde la temperatura es intensificada durante la separación. Rampas de temperatura permiten ambos compuestos de punto bajo - y alto punto de ebullición que se separará en la misma separación.
La lectura producida por GC es un cromatograma que da la señal con el tiempo. Se observan picos para cada compuesto en la muestra. Para cada pico, se pueden calcular una altura y un área de pico. Área de pico se utiliza generalmente para hacer curvas de calibración y para calcular las concentraciones de las muestras incógnitas. El número de platos teóricos (N) se calcula a partir de cada pico para dar una medida de la eficiencia de la columna. Una ecuación práctica para medición N es N = 16(tR/W)2 dondeR es el tiempo de retención del analito y W es el ancho de la parte inferior del pico. N se utiliza para comparar separaciones en diferentes columnas.
El detector de ionización de llama es masa sensible. Así, la cantidad de señal que es proporcional a la masa de carbono en la muestra, no el número de moles. Compuestos con carbono más darán mayores señales. La quema de carbón produce iones que son detectados como una corriente. FID es uno de los detectores generales más sensibles para la GC con un límite de detección en el rango del picogramo. La respuesta es lineales en siete órdenes de magnitud, lo que le da un amplio rango lineal.
Procedimiento
1. inicialización de la GC
- Encienda el gas portador de helio y aire y ajuste de los manómetros en el instrumento.
- Encender el horno de la columna a una temperatura alta (típicamente 250 ° C o superior) para hornear en la columna. No exceda la temperatura máxima de la columna. Esto eliminará cualquier contaminante. Dejarlo cocer durante al menos 30 minutos antes de ejecutar una muestra.
2. haciendo un archivo de métodos
- El software controla el instrumento, todos los valores deseados para un archivo de métodos de entrada. En primer lugar, establecer la configuración de muestreadores. Establecer el número de enjuagues pre ejecución, ejecutar los enjuagues y enjuagues con la muestra. Estos enjuagues limpiar la columna entre diferentes muestras.
- La cantidad inyectada es típicamente 1 μl. Una relación de split se encuentra generalmente porque la inyección de una muestra puede sobrecargar la columna. Si la relación de split es 100: 1, esto significa que por cada 1 parte que se inyecta en el instrumento 100 partes va a perder.
- De entrada los parámetros de la fase móvil. El caudal es controlado por el sistema de presión. Las tasas de flujo más rápidas llevan a separaciones más rápidos, pero hay menos tiempo para el analito a interactuar con la columna.
- Entrar en la programación de la temperatura. Para un funcionamiento isotérmico, ingrese la temperatura de la separación y luego un tiempo para la separación. Una elución gradiente, introduce la temperatura inicial y tiempo, la temperatura final de espera y mantener el tiempo y la velocidad de rampa en ° C/min. Un tiempo de equilibrado se establece también que permite la columna espalda fría a la temperatura original entre carreras.
- Introducir los parámetros del detector. Se introducirá una tasa de temperatura y muestreo del detector. El detector debe ser siempre una temperatura más alta que la temperatura de la columna por lo que no hay analito se condensa en el detector.
- Guarde el archivo de métodos. Los parámetros también necesitará descargarse por lo que leen por el GC.
3. recogida de datos GC
- Encienda el gas de hidrógeno y asegúrese de que ajustar correctamente el medidor de presión. Luz de la llama de la FID.
- En el estante de muestreadores, llenar la cubeta de lavado con el solvente de lavado, como el acetonitrilo o metanol. Asegúrese de que el frasco de residuos es vacío.
- Preparar la muestra. Si existe alguna posibilidad de partículas en la muestra, filtrar la muestra. Porque a veces se observan residuos plásticos con GC, uso único vidrio jeringas y frascos para preparar la muestra de vidrio.
- Llene el frasco por lo menos la mitad con la muestra por lo que se asegura la jeringa del inyector automático para recoger la muestra. Automuestreador viales suelen ser 2 mL, pero si el volumen de muestra es limitada, insertos vial están disponibles para reducir el volumen de muestra necesario.
- Cargar los frascos de muestra en el estante del muestreador automático. El seguimiento de qué posición en cada muestra.
- Antes de la carrera, cero la base del registrador de carta en el software de computadora.
- Los archivos pueden recogerse como una única prueba o usando una tabla de lote para múltiples pistas. Asegúrese de especificar el número correcto del frasco para la muestra. Pulsa el botón "Inicio" y hacer un archivo.
- Datos normalmente son analizados con un programa de software. Parámetros que pueden medirse son tiempo de retención, altura, área de pico y número de platos teóricos.
4. resultados: Análisis de GC de muestras de café
- En este ejemplo, se realizó análisis de GC-FID para cafeína y ácido palmítico, dos compuestos que se encuentran en el café. La cafeína es menos polar que el ácido palmítico, que tiene una cola de alcanos de cadena larga. Así, la cafeína se retiene menos y elutes primero en la columna no polar de 95% dimetilpolisiloxano y 5% fenil-arylene (figura 1).
- Desde el cromatograma, se pueden calcular las áreas de pico. Las áreas de pico son proporcionales a la masa de carbono que pasa por el detector y pueden ser utilizados para hacer una curva de calibración de concentración del instrumento respuesta vs. Figura 1, el área de pico es 27.315 para cafeína y 18.852 de ácido palmítico.
- Es una medida de la eficiencia de la columna N, el número de platos teóricos. N puede calcularse a partir del cromatograma para cada pico. Figura 1, N es 283.000 para cafeína y 261.000 de ácido palmítico.
- La figura 2 muestra el efecto de la temperatura en separaciones isotérmicos. Dos separaciones son overlaid de la misma muestra de cafeína y ácido palmítico. La primera es a 180 ° C y la segunda a 200 ° C. Los tiempos de retención son mucho menores para el funcionamiento a temperaturas elevadas.
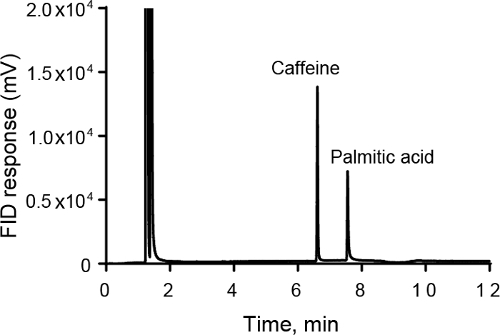
Figura 1. Análisis de GC-FID de muestras cafeína y ácido palmítico. La cafeína 5 mM estándar elutes en primer lugar, seguida por la muestra de 1 mM de ácido palmítico. La rampa de temperatura fue 0,1 min a 150 º C seguido de una rampa de 10 ° C/min a 220 ° C donde la temperatura se llevó a cabo durante 5 minutos.

Figura 2. Análisis de GC-FID de carreras isotérmicas de una muestra de café de tueste oscuro. Una comparación de GC-FID corre a 180 ° C y 200 ° C para una muestra de café de tueste oscuro. Los picos elución mucho más rápidamente con la temperatura de 200 ° C.
Aplicación y resumen
GC se utiliza para una variedad de aplicaciones industriales. Por ejemplo, se utiliza para probar la pureza de un producto químico sintetizado. GC también es popular en aplicaciones ambientales. GC se utiliza para detectar plaguicidas, hidrocarburos poliaromáticos y ftalatos. Más aplicaciones de calidad de aire utilizan GC-FID para controlar contaminantes del ambiente. GC se utiliza también para el análisis de espacios vacíos, donde se recogen y miden los volátiles que se evaporan de un líquido. Esto es útil para las industrias de cosméticos y alimentos y bebidas. GC se utiliza para aplicaciones forenses, así como detectar drogas de abuso o explosivos. Además, GC es útil en la industria del petróleo para la medición de hidrocarburos. Los usos extensos hace GC 1 billón de dólares al mercado mundial del año.
La figura 3 muestra un ejemplo de cómo la GC podría utilizarse en la industria alimentaria. La figura 3 muestra un cromatógrafo de vainilla artificial (negro) y la vainilla real (rojo). GC puede utilizarse para identificar la muestra real, que contiene un gran pico de vainillina pero no contiene un segundo pico de ethylvanillin.
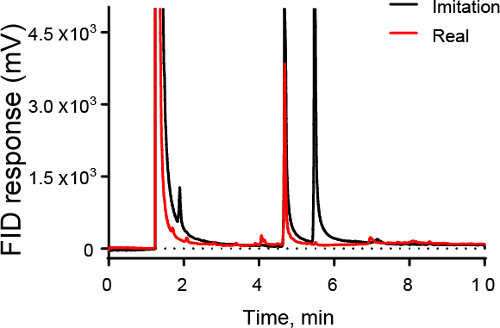
Figura 3. Cromatograma GC-FID de muestras vainillas. Imitación y vainilla real muestran picos grandes a 4,7 min debido a la vainillina, el componente del principio de la vainilla. Sin embargo, imitación vainilla también tiene un pico grande en min 5,3, ethylvanillin, un compuesto que no está presente en grandes cantidades de vainilla real.
Tags
Saltar a...
Vídeos de esta colección:

Now Playing
Cromatografía de gases (CG) con detección de ionización de llama
Analytical Chemistry
281.9K Vistas

Preparación de muestras para la caracterización analítica
Analytical Chemistry
84.6K Vistas

Estándares internos
Analytical Chemistry
204.7K Vistas

Método de adición estándar
Analytical Chemistry
320.0K Vistas

Curvas de calibración
Analytical Chemistry
796.5K Vistas

Espectroscopía ultravioleta-visible (UV-Vis)
Analytical Chemistry
623.3K Vistas

Espectroscopía de Raman para el análisis químico
Analytical Chemistry
51.2K Vistas

Fluorescencia de rayos x (XRF)
Analytical Chemistry
25.4K Vistas

Cromatografía de líquidos de alto rendimiento (HPLC)
Analytical Chemistry
384.3K Vistas

Cromatografía de intercambio iónico
Analytical Chemistry
264.4K Vistas

Electroforesis capilar (EC)
Analytical Chemistry
93.8K Vistas

Introducción a la espectrometría de masas
Analytical Chemistry
112.2K Vistas

Microscopía electrónica de barrido (MEB)
Analytical Chemistry
87.1K Vistas

Mediciones electroquímicas de catalizadores soportados utilizando un potenciostato/galvanostato
Analytical Chemistry
51.4K Vistas

Voltametría cíclica (CV)
Analytical Chemistry
125.1K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados