Cinética de la polimerización por adición de polidimetilsiloxano
Visión general
Fuente: Kerry M. Dooley y Michael g. Benton, Departamento de ingeniería química, Universidad Estatal de Louisiana, Baton Rouge, LA
Los polímeros son moléculas que consta de muchas unidades de monómero repetición que se adhieren químicamente en cadenas largas. Exhiben una amplia gama de propiedades físicas, que son afectadas por su estructura química, peso molecular y grado de polimerización. La industria del polímero fabrica miles de materias primas utilizadas en una amplia variedad de productos comerciales. 1 , 2
El objetivo de este video es realizar una reacción de polimerización de la adición y luego evaluar el producto resultante para entender cómo la viscosidad se puede utilizar para determinar el peso molecular de polímero. Además, este experimento investigará cómo peso molecular pueden ser relacionados con conversión de monómero.
Principios
Muchos polímeros son producidos en reactores de tanque agitado, ya sea por lotes o continua. Por ejemplo, la polimerización de poly(dimethylsiloxane) (PDMS) se muestra en la figura 1. En esta reacción, "" representa grupos metilo e hidróxido de potasio es el catalizador. El [Me2SiO]5 es un anillo de 5 miembros que se abre para formar el bloque de edificio básico (el "link") del polímero. El segundo producto representa acabado de polímero (reacciona con algo llamado un "endblocker" para detener el crecimiento), la primera es un polímero de crecimiento ("vivir"). Todo el crecimiento ocurre mientras que la cadena está sujetada al catalizador.
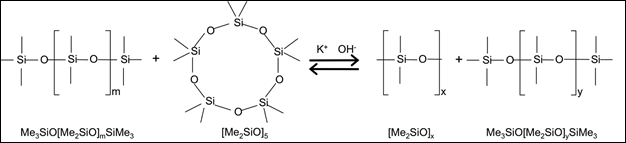
Figura 1: Polimerización de apertura de anillo de PDMS.
Este es un tipo de polimerización de adición, que se discute en muchos cinética3 y todos los libros de ciencia de los polímeros básicos. 4 la reacción es sobre todo de temperatura neutra y es generalmente entre 110-140 ° C y presión atmosférica. Una pequeña cantidad de modificador de peso molecular ("endblocker") se utiliza para detener el crecimiento de la cadena, pero el catalizador entonces comienza una nueva cadena. Endblockers comunes son dimethylsiloxanes con trimethylsiloxy final-grupos. Una cadena de «vivir» reacciona con la endblocker, formando un producto de polisiloxano "muerto" tope de extremo con un grupo final de trimetil.
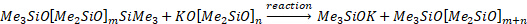
La Me3SiOK reacciona con otra de polisiloxano para crear otro trimethylsiloxy final-grupo. El efecto global no es sólo el endcapping del polímero, pero también control de la longitud de la cadena. Longitudes de cadena media (m + n) entre 43 205 son típicos para PDMS industrial en el que se sintetizan varios grados diferentes de producto. Porque la tasa de adición de monómero >> velocidad de reacción con endblocker (de lo contrario nunca llegar a un alto peso molecular), el endblocker no influyen en la cinética de la reacción, sólo la distribución del peso molecular.
En el análisis de cinética de polimerización, el paso más difícil es determinar el peso molecular de una propiedad física, como viscosidad cinemática y calcular la conversión de fracción. El peso molecular de viscosidad media, que se mide en esta demostración, es una medida intermedia con un valor entre el peso molecular medio en número y peso promedio del polímero. El peso molecular promedio en número es el peso molecular promedio estadístico e indica que 50% de las cadenas de polímero por debajo del peso molecular promedio en número, y 50% están por encima de. Se calcula el peso molecular promedio en peso de las fracciones de peso en el que el 50% del peso de la muestra se compone de cadenas de peso molecular más bajo y 50% consiste en cadenas de peso molecular más alto.
Dividiendo el número MW promedio por el peso del monómero da el número promedio grado de polimerización, que está relacionado con la conversión de fracción. Las conversiones de fracción vs tiempo se utilizan para determinar el orden de la reacción como aprendió en las clases de química física y diseño de reactores.
Procedimiento
El sistema es controlado mediante la ejecución de secuencias de control PS1-PS5 en un sistema de control distribuido industrial estándar que es operado desde una PC. Las secuencias abrir/cerrar/ajustar las válvulas en la correcta secuencian e informan Cuándo y cómo agregar componentes al reactor.
1. configuración del reactor
- Abierto el cilindro de2 N conectado al recipiente de reacción.
- Ejecute la secuencia de control PS1 para probar el equipo.
- Luego, cierre la válvula manual a la bomba de vacío para verificar que el sistema esté libre de fugas.
- Espere 5 minutos y verificar que la presión no sea mayor que 600 mm Hg.
- Llene el sistema con N2. Nitrógeno es necesario para la seguridad y razones de la cinética. O2 inhibe muchas polimerizaciones y puede conducir a explosiones.
- Ejecute la secuencia de control PS3 para agregar monómero en el reactor.
- Cuando se le solicite por la secuencia, añadir la solución de catalizador y endblocker. a través de un embudo pequeño llamado "tanque de la serpiente".
2. polímero fabricación
- Iniciar la secuencia de PS4 y monitorear la temperatura de reacción.
- Una vez que la temperatura alcanza > 105 ° C, con frecuencia recogemos muestras líquidas (por lo menos cada 8 minutos) desde el punto de drenaje de la muestra (PRECAUCIÓN: caliente, guantes térmicos).
- Permita que la reacción de polimerización hasta casi equilibrio. Supervisar el uso de la potencia del agitador para confirmar que la reacción ha alcanzado el equilibrio. Una vez que el poder ha dejado de aumentar, entonces la reacción está cerca de equilibrio.
- Asegúrese de recoger muestras de por lo menos 7.
- Cuando termine, abra la válvula del tanque de CO2 y presiona "Reacción completa" para neutralizar el catalizador con CO2. Esto ocurrirá como parte de la secuencia de la PS4.
- Empezar la secuencia de desmontaje de PS5.
- Abrir la válvula manual de la bomba de vacío y permite el desmontaje funcionar durante 15 minutos.
- Seleccione "Desnudando completa".
- Recoger las calderas de bajo de la reacción en un matraz.
- Enfriar el reactor mediante el proceso de enfriamiento automático. Bombeo se realizará más tarde.
- Follwong las instrucciones del fabricante, medir las muestras colectadas con un viscosímetro rotacional (Copa y bob).
- Si la velocidad de giro es demasiado alta, no se obtiene lectura de viscosidad, y se elige una velocidad más baja. Estos valores de viscosidad se utilizará para determinar la distribución del peso molecular del polímero.
Resultados
El peso molecular se puede determinar por relaciones empíricas, como la relación de Barry de polidimetilsiloxanos con pesos moleculares por encima de ~ 2.500. 5
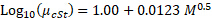
Esto le da el peso molecular medio de viscosidad. De peso molecular predicciones < 2.500, interpolar los datos experimentales encontrados en Kuo,6 utilizando la viscosidad cinemática del monómero DC-245 para la longitud de la cadena 1. Divida la viscosidad (cP) por la densidad del polímero (g/cm3) para obtener la viscosidad cinemática en cSt. Divida la media viscosidad MWs por 1.6 (factor empírico de PDMS) para obtener el peso molecular promedio en número y dividir este valor por el peso molecular de monómero para obtener la longitud de cadena media, (PN)avg, que incluye el monómero no reaccionado.
Para obtener la conversión de la fracción (fm), comience con el balance de masa para el promedio de PN (polímero solamente):
 (1)
(1)
El lado izquierdo es el promedio de PN (polímero sólo) hasta el tiempo t, donde f = fm. Pero el promedio de PN que mides incluye el monómero. Para tener en cuenta para el monómero en (PN)avg, recordemos que por definición:3-4
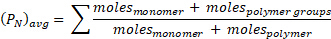
y por lo tanto:
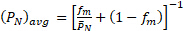 (2)
(2)
El polímero promedio  y (PN)promedio para todo el lote son casi iguales en el último lote, donde fm se acerca a 1. Calcular fm para el último punto con un balance de masa y la cantidad de calderas de baja que fue recogida. Resolver
y (PN)promedio para todo el lote son casi iguales en el último lote, donde fm se acerca a 1. Calcular fm para el último punto con un balance de masa y la cantidad de calderas de baja que fue recogida. Resolver  . Para muchas polimerizaciones de adición,
. Para muchas polimerizaciones de adición,  es constante para todo el lote, lo que permite fm ser computado en otros momentos de la ecuación 2. También, calcular la constante de equilibrio K (modelo de primer orden cinética reversible) para la reacción por balance de masa.
es constante para todo el lote, lo que permite fm ser computado en otros momentos de la ecuación 2. También, calcular la constante de equilibrio K (modelo de primer orden cinética reversible) para la reacción por balance de masa.
Una vez fm se ha determinado en función del tiempo, asumir cinética irreversible y determinar el orden de reacción con respecto al monómero. Usar análisis estadístico para determinar la calidad de los ajustes y el límite de confianza de la tasa constante kp. Determinar el ajuste para la cinética de primer orden (espera que de la teoría),3-4 y prueba si los dos se ajusta realmente difieren.
En condiciones similares, otros han divulgado una constante de velocidad de primer orden de 10-3 s-1 para el monómero de DC-245 y un K > 60.

Figura 2. Resultados de la polimerización típico." DOP"= grado de polimerización. La MW se computaron los datos disponibles (ver Ref. 6) o ecuación de Barry (> 2500). 5
El workup de datos crudos representativos se muestra en la figura 2. Estos datos son para la polimerización de monómero de Dow Corning CC-245. Las condiciones de reacción fueron: 0,04 solución de catalizador de % wt, 12 wt % endblocker (modificador), 130 ° C y 1 presión atm. Con una cantidad relativamente grande de endblocker utilizado, el grado final de la polimerización (DOP) era bastante bajo.
En este experimento, 11,36 litros de monómero se reaccionó, y se recuperaron sólo calderas bajo de 15 mL, indicando que los datos deben seguir cinética irreversible. El ajuste a la cinética de primer orden (en monómero) se muestra en la figura 3 . Las conversiones de fracción (f) se determinaron utilizando las ecuaciones 1 y 2 con la presunción de que el polímero producido en longitud de la cadena constante (PN). El ajuste resultante es razonable, pero no perfecto. Desviaciones leves de la cinética de primer orden teóricamente esperada pueden surgir por varias razones como efectos difusionales, que es cuando la viscosidad aumenta y el diffusivities reducir de forma significativa. Otras dos razones para las desviaciones son sugeridas por los datos de temperatura de reacción cruda (oscilaciones de la temperatura afectan la constante de velocidad) y por fugas pequeñas que pueden estar presentes en bombas, reactores y cambiadores de calor. Si hay fugas, algunas O2 podría entrar en el sistema y gradualmente inhiben la reacción.
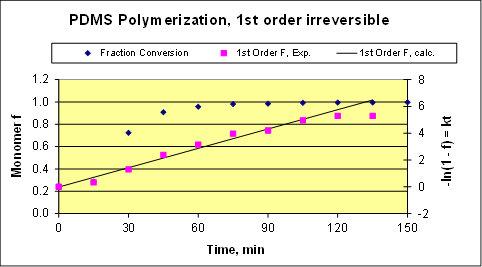
Figura 3. Análisis de la cinética. "F" es la función de orden 1 dest , la solución del balance de masas para una reacción irreversible de la orden 1 dest del reactor por lotes.
Aplicación y resumen
Ciencia de los polímeros proporciona muchos ejemplos de los principios básicos de la cinética química y diseño de reactores. Expresiones de tipo simple pueden describir bastante complejos procesos químicos, como en este experimento. Diseño de sistema del reactor debe encontrar el tipo de reactor óptimo (lote, tanque agitado, flujo de enchufe o híbrido) Considerando la cinética, los costos de capital y distribución de peso molecular. En particular, el último factor es generalmente el más importante, porque define en gran medida el producto. Dependiendo de este factor solo el producto a menudo puede ir desde un sólido quebradizo duro hasta una goma a un líquido. Una polimerización a granel (sin solvente), tales como el realizado en este experimento, tiene la ventaja de que el procesamiento posterior para obtener un polímero puro es simple - sólo se tira a las calderas de baja y filtrar el catalizador neutralizado. Sin embargo, la desventaja de la polimerización a granel es que si uno pierde el control de la temperatura (demasiado alto), incluso en una polimerización de temperatura neutra, otras reacciones de dominar y conducir a "runaway", que es una reacción exotérmica descontrolada que puede resultar en explosión. Polimerizaciones con mayores calores de reacción están reaccionados ya sea en solución, suspensión (una fase continua del agua está presente, y el monómero es en forma de gota), o en la fase gaseosa.
Los puntos principales del experimento son cómo uno puede procesar datos en bruto de una propiedad física fácilmente medible (viscosidad) para determinar en última instancia, las conversiones de fracción de monómero y la cinética de la reacción. Muchas otras propiedades físicas, por ejemplo, densidad y partícula ligera dispersión, se utilizan para este propósito en otras polimerizaciones.
Polímeros de polimerizaciones de apertura incluyen Nylon-6 de caprolactama, copolímeros de acetal con óxido de etileno y dioxolane, que se utilizan en todo, desde los tanques de combustible para aspersores, poly(ethyleneimines), que se utilizan en detergentes y cosméticos, y muchos otros polímeros de silicio-columna vertebral. Con la excepción de Nylon-6, la mayoría de estos polímeros es producida comercialmente por polimerizaciones aniónicas o catiónicas. Otros polímeros que son semejantemente son copolímeros de estireno (especialmente con isopreno) caucho isobuteno-isopreno (butilo) y sus variantes halogenadas y poli (éteres de vinilo Alquilo), que se suelen utilizar en pinturas y adhesivos. Para algunos estas polimerizaciones, las terminaciones de cadena son tan controladas que una distribución casi homogénea de peso molecular es posible. Excepción de ciertos grados de especialidad, se ha encontrado que tales distribuciones estrechas presentan otros problemas, como dificultades de extrusión.
Muchos polímeros son vacío despojado como la primera parte de su purificación para un producto comercial. Entre ellos están los copolímeros poly(vinylidene chloride), poly(chloroprene) y muchos grados de poly(styrene) y sus copolímeros como SAN (estireno-acrilonitrilo).
Polímeros de silicona se utilizan en muchos productos, incluyendo lubricantes, productos de cuidado personal, aparatos médicos, antiespumantes, Sellantes, recubrimientos impermeables y como componentes de pinturas, detergentes y aislamiento eléctrico. 8 dispositivos médicos compuesto por silicona de reticulado de muy alto peso molecular pueden ser aprobados por la FDA para la implantación. Usos médicos más comunes son consumibles tales como catéteres, tubos, bolsas gástricas y drenaje de la incisión quirúrgica. Comercial PDMS es no peligroso con un punto de inflamación mayor que 300 º C, mínimos efectos toxicológicos y buena resistencia a ácidos y moderadamente concentrado álcali acuoso. 8 , 9 no corroe materiales más comunes. Pero como muchos polímeros puede oxidativamente descomponer, en este caso por encima de ~ 150 ° C.
Lista de materiales
| Nombre | Empresa | Número de catálogo | Comentarios |
| Equipo | |||
| Viscosímetro rotacional (Copa y bob) | Brookfield | Utilice para medir la viscosidad de las muestras de polímero | |
| Reactor de tanque agitado | personalizados | 20 L | |
| Agitador reactor
|
McMaster-Carr | 46-460 RPM; tipo turbina de 6 hojas, planas (Rushton), diámetro de ~ 4" . | |
| Reactivos | |||
| Monómero de Dimethlysiloxane | Dow Corning | CC-245 | gravedad específica = 0.956 a 25 °C; viscosidad = 4.2 cSt; m = número promedio de dimethylsiloxanes = 5 |
| EndBlock A | Dow Corning | 10082-147 | gravedad específica = 0.88 a 25°C; m = 4.5 (sin contar los grupos de dos extremos) |
| Catalizador KOH | VWR | 470302-140 | 45 wt % solución en agua |
| Nitrógeno | Airgas | Grado UHP | Utilizado para cubrir el sistema |
| Dióxido de carbono | Airgas | Grado de la tecnología | Utilizado para neutralizar el catalizador |
Datos de densidad en el bajo peso Molecular y viscosidad
Datos de: Dow Corning. 10
| MW, g/mol | 162 | 410 | 1250 | 28000 |
| Viscosidad, cs, 25 °C | 0.65 | 2.0 | 10 | 1000 |
| Densidad, 25 °C | 0.760 | 0.872 | 0,935 | 0,970 |
Referencias
- http://www.essentialchemicalindustry.org/polymers/polymers-an-overview.html and http://www.pslc.ws/mactest/maindir.htm (both accessed 8/22/16).
- MatWeb, Material Property Data, http://www.matweb.com/ and Plastics General Polymers Brand Name Listing, http://www.plasticsgeneral.com/BRAND-NAMES-LIST1.htm (both accessed 8/25/16).
- Fogler, F.S., Elements of Chemical Reaction Engineering, 3rd Ed., Prentice-Hall, 2001, pp. 354-382 (sections 7.1.2-7.1.5).
- Odian, G., Principles of Polymerization, 4th Ed., Wiley-VCH, 2004 (ch. 3), or Rodriguez, F., Principles of Polymers Systems, 2nd Ed., McGraw-Hill, 1982 (ch. 4); Fried, J.R., Polymer Science and Technology, Prentice-Hall, 1995 (ch. 2).
- Barry, A.J., Viscometric Investigation of Dimethylsiloxane Polymers, J. Appl. Phys., 1946, 17, 1020-1024.
- Kuo, A.C.M. Poly(dimethylsiloxane), in Polymer Data Handbook, Oxford University Press, 1999, 411.
- Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2012 or the Encyclopedia of Polymer Science and Technology, 3rd Ed., Wiley-Interscience, Hoboken, 2003-04.
- http://www.dowcorning.com/content/discover/discoverchem/properties.aspx (accessed 8/25/16)
- Shin-Etsu Silicone Fluid Technical Data, Shin-Etsu Silicones of America, Akron, 2005.
- Dow Corning, Product Information, Silicon Fluids, http://www.dowcorning.com/applications/Product_Finder/Products.aspx (accessed 9/23/16).
Tags
Saltar a...
Vídeos de esta colección:

Now Playing
Cinética de la polimerización por adición de polidimetilsiloxano
Chemical Engineering
16.1K Vistas

Prueba de la eficiencia de transferencia de calor de un intercambiador de calor de tubos con aletas
Chemical Engineering
17.9K Vistas

Uso de una bandeja de secado para investigar la transferencia de calor convectiva y conductiva
Chemical Engineering
43.9K Vistas

Viscosidad de las soluciones de propilenglicol
Chemical Engineering
32.8K Vistas

Porosimetría de un polvo de alúmina de sílice
Chemical Engineering
9.6K Vistas

Demostración del modelo de ley de energía a través de extrusión
Chemical Engineering
10.0K Vistas

Amortiguador de gas
Chemical Engineering
36.7K Vistas

Equilibrio vapor-líquido
Chemical Engineering
88.9K Vistas

El efecto de la relación de reflujo en la eficiencia de destilación de bandeja
Chemical Engineering
77.7K Vistas

Eficiencia de la extracción líquido-líquido
Chemical Engineering
48.5K Vistas

Reactor de fase líquida: Inversión de sacarosa
Chemical Engineering
9.7K Vistas

Cristalización del ácido salicílico mediante modificación química
Chemical Engineering
24.2K Vistas

Flujo monofásico y bifásico en un reactor de lecho compacto
Chemical Engineering
18.9K Vistas

Reactor catalítico: Hidrogenación de etileno
Chemical Engineering
30.4K Vistas

Spin y Chill
Chemical Engineering
7.4K Vistas
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados