Method Article
Extracción y caracterización de los agentes tensioactivos de los aerosoles atmosféricos
En este artículo
Resumen
Métodos se presentan para la extracción selectiva de tensioactivos presentes en los aerosoles atmosféricos y la determinación de sus concentraciones absolutas y las curvas de tensión superficial en el agua, incluyendo su concentración micelar crítica (CMC).
Resumen
Se espera que los compuestos de superficie activa, o tensioactivos, presentes en los aerosoles atmosféricos para jugar papeles importantes en la formación de nubes de agua líquida en la atmósfera de la Tierra, un proceso central en la meteorología, la hidrología, y para el sistema climático. Pero debido a la extracción y caracterización específica de estos compuestos han faltado durante décadas, se sabe muy poco sobre su identidad, propiedades y modo de acción y orígenes, lo que impide la plena comprensión de la formación de nubes y sus posibles vínculos con los ecosistemas de la Tierra.
En este trabajo se presentan recientemente desarrollado métodos para 1) la extracción selectiva de todos los agentes tensioactivos a partir de muestras de aerosoles atmosféricos y para la determinación de 2) sus concentraciones absolutas en la fase de aerosol y 3) sus curvas de tensión superficial estática en el agua, incluyendo su crítico concentración micelar (CMC). Estos métodos se han validado con 9 Referencias tensioactivos, ianiónico ncluding, catiónicos y los no iónicos. Ejemplos de resultados se presentan para los tensioactivos que se encuentran en partículas de aerosol finas (diámetro <1 M) recogidas en un sitio costero de Croacia y sugerencias para futuras mejoras y otras caracterizaciones que las presentadas se discuten.
Introducción
Las nubes son esenciales en la atmósfera de la Tierra, para la hidrología de la mayoría de los ambientes y ecosistemas, y para el sistema climático. Sin embargo, algunos aspectos de sus mecanismos de formación aún no se comprenden, en particular, las contribuciones de los compuestos químicos presentes en las partículas de aerosol que actúan como núcleos de condensación. Teoría 1 predice que los compuestos tensioactivos, o agentes tensioactivos, presentes en las partículas de aerosol deben mejorar fuertemente la formación de gota de nube mediante la reducción de su tensión superficial, por lo tanto su energía formación. Sin embargo, estos efectos han sido difícil de alcanzar a observación durante décadas y el papel de los tensioactivos en la formación de nubes Actualmente es negado por una gran parte de la comunidad atmosférica e ignorado en todas las investigaciones de las nubes y los modelos atmosféricos y climáticos.
Una razón de la falta de comprensión del papel de los tensioactivos de aerosol en la formación de nubes ha sido la ausencia de método para isotarde y caracterizarlos. A diferencia de muestras de otros entornos, el análisis de muestras atmosféricas enfrenta desafíos recurrentes 2 como el volumen de muestra muy pequeña y la masa (en este caso, típicamente entre 10 y 100 mg) y la complejidad química (mezclas de sales, minerales, y numerosos compuestos orgánicos). Para superar estos desafíos y mejorar la comprensión de aerosol tensioactivos algunos métodos se han desarrollado recientemente por nuestro grupo a 1) Extracto específicamente estos compuestos a partir de muestras de aerosoles atmosféricos, 2) determinar sus concentraciones absolutas en la fase de aerosol y 3) determinar sus curvas de tensión superficial en agua, incluyendo su concentración micelar crítica (CMC), la concentración a la que los agentes tensioactivos están saturados en la superficie y comienzan a formar micelas en la mayor parte. Las últimas versiones de estos métodos se presentan en este documento.
Otras mejoras y otros tipos de caracterizaciones, que podrían ser utilizados en loslement a los presentados, será discutido. Las aplicaciones recientes de estos métodos ya han mostrado cómo este tipo de análisis pueden mejorar la comprensión del papel de los tensioactivos en la formación de nubes, por evidenciando este papel en sí, 3 la determinación de las concentraciones de tensioactivo en los aerosoles atmosféricos 3, 4, 5, 6 y modo de acción en formación de la nube de gotas, 3, 6 evidenciando su origen biogénico, 3, 4, 7 y explicar su falta de observación por instrumentos clásicos. 8, 9, 10
Protocolo
1. Preparar el material para el Protocolo que se enumeran en la Tabla 1
| Material | Preparación / lavado |
| Consumibles (jeringas de plástico, agujas, 4-mL viales, pipetas Pasteur, puntas de micropipeta) | Para ser utilizado directamente sin pre-tratamiento y desechado después de su uso. |
| De vidrio reutilizables (vasos de precipitados (por agua ultrapura); 15, 30, y 60 botellas ml con tapones de corcho; tubos para extracción en fase sólida (SPE), y barras de agitación magnéticas) | Lavar con etanol (sólo para los viales usados para el método colorimétrico). |
| secuencialmente Enjuague con agua del grifo, etanol, agua del grifo, y agua ultrapura. | |
| Llenar los viales de vidrio y el vaso que contiene los corchos, agitadores magnéticos, y SPE tubes con agua ultrapura y colocarlos en un baño de ultrasonidos durante 15 min. | |
| Eliminar el agua y enjuague con agua ultrapura. | |
| Secar el material de vidrio en el aire a temperatura ambiente. | |
| Una vez seco, cierre todas las botellas y almacenarlos bajo cubierta para evitar la recolección de polvo. | |
| Para evitar la contaminación, el uso de vidrio distinto para la extracción de agua y el método colorimétrico. | |
| Pinzas y tijeras | Lavar con etanol y agua y después ultrapura. |
| Secar con aire comprimido. | |
| Platos de Petri de vidrio y tapas | Lavar con agua del grifo y un cepillo y después con etanol. |
| Enjuague con agua del grifo y agua ultrapura a continuación. | |
| Secar al aire a temperatura ambiente. | |
| Una vez seco, cerrar las cajas y store ellos bajo cubierta para evitar la recolección de polvo. | |
| SPE colector de vacío | Lavar con etanol y agua y después ultrapura. |
| Secar con aire comprimido. | |
| Cubeta de cuarzo (por análisis UV-Vis) | Lavar con etanol y enjuague con agua del grifo y agua y luego ultrapura. |
| Secar con aire comprimido. |
Tabla 1: Lista de materiales y artículos de vidrio usado para el protocolo, incluyendo su preparación y lavado.
2. manipulación de las muestras de aerosol
NOTA: El método de extracción que aquí se presenta ha sido desarrollado para muestras de aerosoles atmosféricos recogidos en filtros de fibra de cuarzo de un peso total de al menos 8 g. El método de recogida de muestras de aerosoles en los filtros en la atmósfera no se explicará aquí, pero numerososdescripciones se pueden encontrar en la literatura, tales como las referencias 2, 3, 4, 5, 6 Sólo los siguientes pasos están subrayados.
- Número cada filtro individual.
NOTA: durante todo el protocolo de los filtros deben ser manipulados con pinzas limpias y se mantienen por su borde. - Pre-condición de los filtros y láminas de aluminio o platos de Petri de vidrio antes del muestreo por cocción ellos en 773 K durante 6 h.
- Pre-pesar, bajo condiciones de temperatura y humedad controladas, los filtros utilizando una microbalanza tiene una precisión de al menos 1 g, para determinar el peso pre-muestra.
- Tomar muestras en blanco regularmente al inicio, durante y al final del periodo de muestreo, mediante la colocación de un filtro en el soporte del filtro de la toma de muestras, pero manteniendo la bomba para la misma duración que para la recolección de la muestra real ( por ejemplo. Si la recogida de la muestra tiene una duración de 24 h, el filtro en blanco debe ser dejado en el muestreador, con la bomba, para 24 h). Analizar estos espacios en blanco con el mismo protocolo que para las muestras reales.
- Tan pronto como sea posible después del muestreo, el paquete de los filtros en contenedores (hojas de aluminio respaldados o platos de Petri de vidrio) y almacenarlos en un congelador a -18 ° C (255 K) hasta el análisis.
- Deje los filtros para equilibrar en un desecador durante 24 h antes del pesaje. Determinar cada volumen de la muestra (masa aerosol recogido en filtros) pesando después de muestreo (y restar peso pre-muestreo) bajo la misma temperatura controlada y humedad relativa como durante la pre-pesaje.
3. Extracción de los agentes tensioactivos a partir de muestras de aerosol
- La extracción de agua
- Sumergir las muestras de filtro en agua ultrapura durante 2 horas a 279 ± 1 K en platos de Petri de vidrio, cerrar la tapa y agitar las placas de Petri mientras mantiene ellos plana, sobre emismas 30 min.
NOTA: Los filtros 47 mm se sumergen en 7 ml y los 150 mm en 35 ml. Con 120 mm platos Petri de vidrio, los filtros de 150 mm necesitan ser cortados en cuatro piezas con tijeras limpias antes de ser colocado en el plato. - Limpiar una filtros de jeringa (PVDF 0,40 m) con 3 x 1 mL de agua ultrapura.
- Filtrar la solución obtenida en la etapa 3.1.1 con el filtro de jeringa limpia y colocarlo en un 60 botella de vidrio pesado previamente mL. Enjuague la placa de Petri con 5 ml de agua ultrapura, filtrar el agua con el filtro de jeringa y añadirlo a la solución en la botella 60 ml de vidrio. Entonces ponderar la botella de vidrio 60 ml que contiene la solución para determinar el volumen de agua filtrada y la concentración de tensioactivo en el paso 4.4.5.
- Sumergir las muestras de filtro en agua ultrapura durante 2 horas a 279 ± 1 K en platos de Petri de vidrio, cerrar la tapa y agitar las placas de Petri mientras mantiene ellos plana, sobre emismas 30 min.
- SPE extracción (fase sólida extracción)
- Coloque la sílice SPE cartuchos C18 base (ver Lista de Materiales para detalles acerca de los cartuchos) en el colector de vacío SPE, que es conectado por sí mismoa una bomba.
- Lavar los cartuchos haciendo fluir 6 ml de acetonitrilo con un caudal a 1 ml / min y aplicando un vacío con la bomba. Repetir con 6 ml de agua ultrapura. Detener la bomba para mantener el nivel de agua lo suficientemente alta y mantener el cartucho mojado.
- El flujo de la muestra obtenida en la etapa 3.1.3 a través del cartucho SPE a una velocidad de menos de 1 ml / min.
- Flujo 1 ml de agua ultrapura a través del cartucho para la limpieza y secar el cartucho mediante la aplicación de un vacío más fuerte en el SPE set-up.
- Eluir la fracción de tensioactivo absorbido en la columna por el flujo de 4 ml de acetonitrilo a través de ella a una velocidad de flujo de menos de 1 ml / min.
- Se evapora la solución de acetonitrilo obtenido con un flujo de N 2 para obtener un extracto de surfactante seco y volver a disolver el extracto seco en 60 l de agua ultrapura.
NOTA: Los 60 extractos mu l obtenidos a partir de este método se pueden usar entonces como solución madre para diversas caracterizaciones de los tensioactivos.
- Se evapora la solución de acetonitrilo obtenido con un flujo de N 2 para obtener un extracto de surfactante seco y volver a disolver el extracto seco en 60 l de agua ultrapura.
- Determinación de las eficiencias de extracción
NOTA: Las eficiencias del método de extracción para los diferentes tipos de tensioactivos necesitan ser determinado para la determinación de sus concentraciones absolutas en la Sección 4. Para esto, el siguiente protocolo se necesita aplicar para hacer referencia a agentes tensioactivos tales como, por ejemplo, dodecil sulfato de sodio (SDS), dioctil sulfosuccinato de sodio (AOT), benzyltetradecyl dimetilamonio (zephiramine), cloruro de cetiltrimetilamonio (CTAC), (1,1,3,3-tetrametilbutil) glicol fenil-polietileno (ver Lista de Materiales), éter de polietilenglicol de dodecilo ( ver Materiales Lista), surfactina, ramnolípido, o L-α-fosfatidilcolina.- Pico de la soluciones de referencia acuosas estándar (10 -9 a 10 -4 moles de tensioactivos en 1 mL de agua ultrapura) sobre filtros de cuarzo limpias (gramaje 0,85 gm -2) con una micropipeta. En paralelo, añadir la misma cantidad de estas soluciones directly en viales como "soluciones iniciales".
- Se secan los filtros (colocados en placas de Petri) en un desecador durante 24 h y extraer los filtros con agentes tensioactivos de acuerdo con el protocolo en la Sección 3.1 a 3.2.
- Medir la concentración de los compuestos de referencia en el inicial (soluciones de referencias en viales de la etapa 3.3.1) y soluciones extraídas (de la etapa 3.3.2) con los métodos descritos en la Sección 4. Las eficiencias de extracción se determina como la relación de las tesis concentraciones.
NOTA: Por lo general, en este trabajo, para SDS y AOT (tensioactivos aniónicos), se encontró que esta eficiencia para ser 65 ± 10%, para zephiramine y CTAC (tensioactivos catiónicos), que fue de 20 ± 5%, y para (1,1 , 3,3-tetrametilbutil) glicol fenil-polietileno (ver Lista de Materiales), polietileno glicol dodecil éter (ver Lista de Materiales), surfactina, ramnolípidos, y L-α-fosfatidilcolina (tensioactivos no iónicos) que era de 90 ± 10%.
- extractien de la fracción de tensioactivo total en muestras
NOTA: Para verificar que el método de extracción propuesto elimina todos los tensioactivos presentes en las muestras analizadas (es decir, todos los compuestos que reducen su tensión superficial), el siguiente ensayo se puede realizar.- Medir la tensión superficial (véase la sección 5) de una solución conocida de compuesto de referencia (o de un extracto de la muestra) después de la primera extracción (etapa 3.1.3). Debe ser alrededor de 50 mN m -1.
- Medir la tensión superficial de la solución que queda después de las segundas etapas de extracción, es decir, recogido después de pasar por la columna de la SPE en el paso 3.2.3. Este valor debe estar cerca de 72,8 ± 1 mN m -1, el de agua pura, que muestra que la mayoría o todos los compuestos tensioactivos presentes en las muestras se han eliminado por la extracción.
4. Determinación de tensioactivo Concentraciones de fase Aerosol
NOTA:Una técnica colorimétrica ha sido elegido para la determinación de concentraciones de tensoactivo de fase aerosol, que proporciona concentraciones absolutas y tiene sensibilidad adecuada para los tensioactivos en muestras ambientales. 11, 12, 13, 14 pero se requiere para medir por separado las concentraciones de tensioactivos aniónicos, tensioactivos catiónicos y no iónicos ya que diferentes reactivos tienen que ser utilizados para cada tipo de agente tensioactivo. Todas las soluciones para el siguiente protocolo deben estar preparados con micropipetas de precisión y todas las reacciones se deben realizar en viales de vidrio.
- Titulación colorimétrica de tensioactivos aniónicos
- Preparar una solución de tampón de acetato en agua a pH = (solución de acetato sódico 0,2 M / ácido acético solución 0,2 M, 70/30 en volumen) 5 con un volumen de al menos n 200! L, en donde n es el número de muestras que se analizado.
- Preparar una solución de EDTA 0,1 M con un volumen de al menos nx 100! l, donde n es el número de muestras a analizar.
- Preparar una solución de sulfato de sodio 1 M en agua con un volumen de al menos nx 500! L, donde n es el número de muestras a analizar.
- Preparar una solución de violeta de etilo (C 31 H 42 N 3) 11, 15, 16, 17 0,49 g L -1 en agua con un volumen de al menos nx 200! L, donde n es el número de muestras a analizar.
- Si a partir de los extractos de muestra 60 mu L obtenidos en la Sección 3, se diluye a 10 ml con agua ultrapura utilizando micropipetas en una botella de vidrio de 60 ml con una tapa. De lo contrario, tomar 10 ml de muestra y añadir 200 l de solución de tampón de acetato, 100 l de la solución de EDTA, 500 l de la solución de sulfato de sodio y 200 l de acetato desolución de violeta usando micropipetas.
- Añadir 2,5 ml de tolueno a la solución con una micropipeta, una barra de agitación magnética, y se agita durante 1 hora a 500 rpm.
- Deje las fases acuosa y orgánica para establecer durante aproximadamente 10 min. Una vez que se separaron, eliminar la fase de tolueno (fase superior) con una pipeta Pasteur de vidrio para realizar el análisis UV-vis (véase la Sección 4.4).
- Titulación colorimétrica de tensioactivos catiónicos
- Preparar una solución de tampón de acetato en agua a pH = (solución de acetato sódico 0,2 M / ácido acético solución 0,2 M, 70/30 en volumen) 5 con un volumen de al menos nx 1 ml, donde n es el número de muestras que se analizado.
- Preparar una solución de azul de disulfina (C 27 H 32 N 2 O 6 S 2) 11, 18 en 2,58 g L -1 en una mezcla 90:10 de agua / etanol (diluir el colorante primero con el volumen de agua y luego la adición de la volumen de etanol), con un volumen de al menos nx 500! l, donde n es el número de muestras a analizar.
- Colocar 10 ml de muestra en una botella de vidrio de 30 ml con una tapa y añadir 1 ml de la solución tampón de acetato y 500 l de la solución de azul de disulfina usando micropipetas.
- Añadir 2,5 ml de cloroformo con una micropipeta, una barra de agitación magnética, y se agita durante 1 hora a 500 rpm.
- Después de salir de las fases acuosa y orgánica para separar por alrededor de 10 min, eliminar el cloroformo (fase inferior) con una jeringa para realizar el análisis UV-Vis (véase la Sección 4.4).
- Titulación colorimétrica de tensioactivos no iónicos
NOTA: Para la valoración de los tensioactivos no iónicos, no fue posible identificar un colorante que reacciona con todos los tensioactivos no iónicos, pero tiocianato de cobalto (Co (NCS) 2) se eligió ya que reacciona con la gama más amplia de compuestos. 12, 19- Prepara unsolución de tiocianato de cobalto mezclando nx 6,2 g de tiocianato de amonio y NX 2,8 g de hexahidrato de nitrato de cobalto en nx 10 ml de agua, donde n es el número de muestras a analizar.
- Coloque 3 ml de la muestra en una botella de vidrio 15 ml con una tapa y añadir 1 ml de la solución de tiocianato de cobalto con una micropipeta.
- Añadir 2 ml de cloroformo con una micropipeta, una barra de agitación magnética, y se agita durante 1 h a 500 rpm
- Después de salir de las fases acuosa y orgánica para separar por alrededor de 10 min, eliminar el cloroformo (fase inferior), utilizando una jeringa para realizar el análisis de absorción UV-Vis (véase la Sección 4.4).
- Las curvas de calibración y cuantificación por espectroscopia UV-Vis
- Establecer una curva de calibración (absorbancia vs curvas de concentración) para los tensioactivos aniónicos mediante la medición de la absorbancia a 612 nm de serie de soluciones conocidas de un compuesto de referencia, tales como SDS o AOT.
Nota: Normalmente 12 soluciones con concentracionesentre 0 y 5 M (e incluyendo algunas repeticiones) debe ser utilizado para establecer la curva.
Una curva de calibración única debe obtenerse con ambos compuestos aniónicos (SDS y AOT) con una pendiente de ε = 0,37 ± 0,02 cm mu M -1 y un límite de detección de 0,054 M, de todos los tensioactivos aniónicos. - Establecer una curva de calibración para los tensioactivos catiónicos por un enfoque similar, pero midiendo la absorbancia a 628 nm y el uso de compuestos de referencia tales como Zephiramine o CTAC.
NOTA: la pendiente debe ser varepsilon = 0,35 ± 0,05 cm mu M -1 y el límite de detección de 0,059 M, de todos los tensioactivos catiónicos. - Establecer una curva de calibración para los tensioactivos no iónicos por un enfoque similar, pero para una gama de concentración de 0 a 20 M, midiendo la absorbancia a 317 nm, y el uso de polietileno glicol éter de dodecilo (ver Lista de Materiales) como compuesto de referencia.
- Para determinar las concentraciones de tensioactivo-dyecomplejo en las soluciones orgánicas obtenidas en la Sección 4.1, 4.2 y 4.3, el lugar ~ 1,5-2 ml de estas soluciones en una célula de cuarzo de 1 cm y medir su absorbancia a 612, 628 y 317 nm, respectivamente, con un Espectrofotómetro UV-Vis. Antes de cada medición solución, tomar un espacio en blanco del disolvente orgánico (tolueno para el método de tensioactivo aniónico y cloroformo para los métodos catiónicos y no iónicos)
NOTA: A diferencia para los tensioactivos aniónicos y catiónicos, utilizando tiocianato de cobalto como colorante dará diferentes curvas de calibración con diferentes tensioactivos no iónicos. El uso de polietilenglicol éter de dodecilo, como se sugiere aquí, subestimará las concentraciones de la mayoría de los tensioactivos no iónicos, asegurando así que los errores en las mediciones son siempre del mismo signo, es decir subestimar concentraciones reales. La pendiente usando polietilenglicol dodecil éter como referencia debe dar una pendiente de ε = 0.013 ± 0.001 M -1 y un límite de detección de 0,3? M.
NOTA: En base a la diferente calibración pistas obtiene con diferentes tensioactivos no iónicos y el hecho de que algunos tensioactivos podrían no detectarse en absoluto por tiocianato de cobalto se estimó 6 la subestimación sistemática sobre la concentración de tensioactivo no iónico con este método a aproximadamente un factor 2, que es la fuente más grande de las incertidumbres en las concentraciones de tensioactivo en total. - Determinar la concentración total de tensioactivo en cada muestra como la suma de las concentraciones de tensioactivos aniónicos, catiónicos, y tensioactivos no iónicos miden por separado 6 y después de la corrección de cada concentración por la eficiencia de volumen extraído en el paso 3.1.3 y por el respectivo eficiencia de extracción determinado en paso 3.3.
NOTA: Las incertidumbres globales en estas concentraciones totales se estima que 33%, principalmente debido a las incertidumbres en las concentraciones de tensioactivo no iónicos. - Determinar las concen promedio de tensioactivostraciones en la muestra aerosol multiplicando la concentración obtenida para el extracto por la relación del volumen de muestra aerosol al volumen de extracto (60! l).
- Establecer una curva de calibración (absorbancia vs curvas de concentración) para los tensioactivos aniónicos mediante la medición de la absorbancia a 612 nm de serie de soluciones conocidas de un compuesto de referencia, tales como SDS o AOT.
5. Determinación de las curvas tensión superficial surfactante absolutas en agua
- Mediciones de la tensión superficial por colgando tensiometría gota
NOTA: Para las muestras de aerosol, las mediciones de tensión superficial se hacen mejor con el método colgante gotita, ya que este es el método que requiere el volumen de muestra más pequeña (para los detalles sobre el tensiómetro, ver Lista de Materiales). Aunque tales mediciones se realizan en gotitas de diámetros entre 1,4 y 2,4 mm, los experimentos han demostrado que la tensión superficial medida es idéntica a la de las gotitas de tamaño micrométrico que contienen la misma concentración de agente tensioactivo. 10, 20 A lo largo de las mediciones, la temperatura debe ser constante a al menos0; ± 3 K, y el volumen de la gotita debe controlarse continuamente para descartar efectos de evaporación. Cada gotita se debe dejar que se equilibre (el valor de tensión superficial no varía más) antes de hacer una medición y cada medición debe repetirse 3 a 5 veces.- Iniciar la cámara tensiómetro y el software (ver Lista de Materiales para las referencias). Calibrar el tensiómetro mediante la medición de la tensión superficial de las gotas de agua ultrapura, siguiendo el protocolo en los pasos 5.1.2-5.1.5 a continuación.
- Llene una jeringa de 1 ml con una aguja mm Ø 0.30 (por σ <45 mN m -1) o un Ø 0.51 mm (por σ> 45 mN m -1) de la aguja con la solución de tensioactivo obtenido en la etapa 3.2.6 y colocarlo en el tensiómetro, asegurándose de que la punta de la aguja está en el campo de la cámara.
- Producir una gotita de diámetro entre 1 y 3 mm en la punta de la aguja empujando el pistón.
- Tomar una foto o un vídeo de la gota antes de que caiga con esoftware de correo.
- Ejecutar la función de análisis del software para adaptarse de la forma de la gotita a la ecuación de Young-Laplace y obtener un valor de tensión superficial. A se ha indicado anteriormente, esta operación se debe repetir varias veces para la misma gota hasta que la tensión superficial no varía más, para asegurarse de que los agentes tensioactivos han alcanzado el equilibrio en la gota.
NOTA: las incertidumbres globales sobre estas mediciones de tensión superficial son típicamente de ± (0,3-1,0) mN m -1.
- Las curvas de tensión superficial completos y CMC
- Medir la tensión superficial del extracto inicial, obtenida en la etapa 3.2.6, siguiendo el protocolo en 5.1.
- Medir la concentración total de tensioactivo en el mismo extracto, siguiendo los protocolos en la sección 4. Esta concentración y tensión superficial de este extracto proporcionará el punto de partida de la curva.
- Para trazar el resto de la curva, diluir el extracto por un factor de 2 por adagua ultrapura ding con una micropipeta. Medir la tensión superficial de la solución diluida.
- Repita el paso 5.2.2 hasta que la solución ha alcanzado (o está cerca de) la tensión superficial del agua pura (72,8 ± 1 mN m -1). Los valores de tensión superficial y factores de dilución para cada una de estas soluciones diluidas proporcionarán los puntos que definen la curva de la tensión superficial.
- Determinar la concentración media de agente tensioactivo en la muestra inicial aerosol multiplicando la concentración en el extracto por la relación del extracto a volumen de muestra.
NOTA: A medida que el volumen de la muestra de aerosol es generalmente más pequeño que el extracto de 60 l, la concentración de tensioactivo aerosol es generalmente más grande que la concentración del extracto, por lo tanto el punto más lejano en el eje x de la curva. - Trazar la curva de tensión superficial (Figura 2). Para ello, colocar el primer punto que corresponde a las condiciones en el aerosol (eje x = concentrati tensioactivosen en la muestra aerosol determinado en la etapa 5.2.5; eje Y = tensión superficial mínima medida en la solución de extracto de 60 l en la etapa 5.2.1). Después se coloca el segundo punto correspondiente al extracto de 60! L de la etapa 5.2.1 (eje x = concentración de tensioactivo en el extracto de 60! L; eje Y = mínimo la tensión superficial medida en la solución de extracto de 60! L). A continuación, coloque el tercer punto correspondiente al extracto aerosol diluida de la fase 5.2.2 (eje x = concentración de agente tensioactivo en los 120 l solución de extracto diluido = concentración en la solución de extracto de 60 l dividido por un factor de 2; eje y: superficie mínima tensión medida en la solución de extracto de 120! l), y así sucesivamente hasta la última tensión superficial medido (etapa 5.2.3)
- Una vez que la curva de la tensión superficial establecido, determinar la CMC gráficamente mediante la determinación de la intersección entre la pendiente agudo y el nivel mínimo de tensión superficial (véase la Figura 2).
NOTA: Sólo si ºconcentración de agente tensioactivo e en el extracto es significativamente por encima de la CMC (por encima de la transición brusca en la curva) el valor de la CMC y de la tensión superficial mínimo puede determinarse con precisión. Pero si esta concentración es inferior a la CMC, el valor exacto de la CMC no puede ser determinada y la tensión superficial del extracto sólo dará un límite superior de la una de la muestra.
Resultados
Nota: Antes de ser aplicado a muestras atmosféricas, todos los protocolos presentados en esta sección se han probado con 9 tensioactivos de referencia y las curvas de la tensión superficial, tensiones superficiales mínimas, y CMC obtenidos estaban en excelente acuerdo con la literatura. 21, 22
1. concentraciones
aerosoles Bellas (<1 m de diámetro, o "PM1") se recogieron muestras en filtros de fibra de cuarzo en el lugar costero de Rogoznica, Croacia, en febrero de 2015. Estas muestras se manejaron y se extrajeron como se describe en las secciones 2 y 3, respectivamente, de este manuscrito. Las concentraciones para tensioactivos aniónicos, tensioactivos catiónicos y no iónicos y la concentración total de tensioactivo en el volumen de muestra aerosol, C resaca, p (M), se midieron de acuerdo a la Sección 4. Tque los resultados se presentan en la Figura 1, y la evidencia el predominio de los tensioactivos aniónicos y no iónicos Entre los tensioactivos medidos.
2. tensión superficial de la muestra y la superficie de la curva de tensión para extraídos Surfactants
La combinación de mediciones de tensión superficial como se describe en la Sección 5, y las mediciones de concentración, dio lugar a curvas de tensión superficial absolutos para las mismas muestras, como se muestra en la Figura 2. Estas curvas indican la concentración de tensioactivo en la muestra de aerosol y la tensión superficial de estas muestras ( "σ min") y permiten determinar gráficamente los valores de CMC (Figura 2).

Figura1: Las concentraciones de tensioactivo en aerosoles finos (PM1) recogidos en Rogoznica, Croacia. Las concentraciones para aniónico (en azul), catiónicos (en rojo), tensioactivos no iónicos (en verde) y la concentración total de tensioactivo en la fase de aerosol (suma de cada concentraciones de tensioactivo), C resaca, p (M), medida con el colorimétrico método en (<1 M) los aerosoles atmosféricos finos recogidos en el lugar costero de Rogoznica, Croacia, en febrero de 2015. los resultados muestran claramente el predominio de los tensioactivos aniónicos y no iónicos. Haga clic aquí para ver una versión más grande de esta figura.
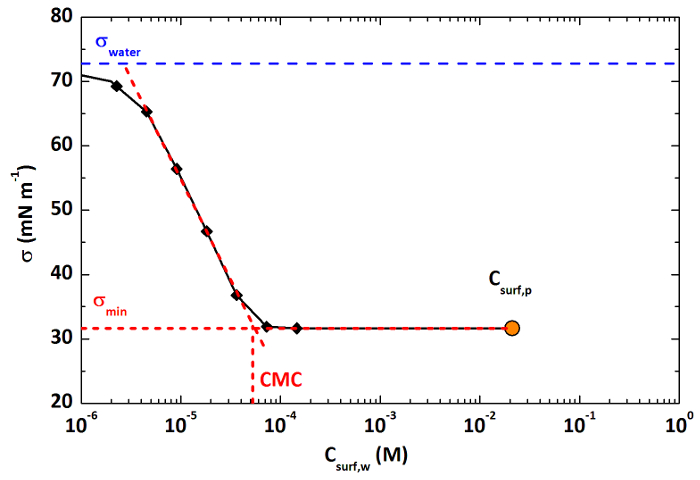
Figura 2: curva de tensión superficial típica y CMC para los tensioactivos en aerosoles a partir deRogoznica, Croacia. curva de la tensión superficial absoluta para los tensioactivos en la muestra de 02.03.2015 obtenido mediante la combinación de las mediciones de tensión y concentración superficial. Los puntos negros representan la tensión superficial medido de la extracto de surfactante. El punto de color naranja al final de las curvas representa la concentración calculada en la muestra de aerosol (etapa 4.4.6), y su tensión superficial "σ min". La determinación gráfica de la CMC se ilustra. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
En el protocolo, todos los pasos críticos se han detallado. Ellos incluyen la recogida de los aerosoles en los filtros, la extracción de los tensioactivos de ellos (usando una extracción doble: a extracción con agua seguido de una extracción SPE) y el análisis de los extractos (tensión superficial y las mediciones de concentración).
Para todo el método, un control de calidad se ha hecho 1) por la aplicación del método de extracción y análisis sobre filtros en blanco (desviación <5 mN m -1 en comparación con agua ultrapura en la tensión superficial y la absorbancia bajo el límite de detección para la colorimétrico método), 2) mediante la determinación de la eficacia de la extracción y sus incertidumbres, incluyendo la reproducibilidad / repetibilidad, el% de tensioactivos extraídos en un rango dado de concentración, 3) mediante la comprobación de los interferentes potenciales en el método colorimétrico, es decir, mediante la comprobación de que los detecta método sólo el tipo específico de tensioactivo (anionic, catiónicos y no iónicos) y no ver a los otros como totalmente detallada en las referencias 4, 6) mediante la comprobación de interferentes potenciales de los extractos de aerosol (sales inorgánicas, ácidos pequeñas) en el método colorimétrico como totalmente detallada en referencia 6.
Para nuestro conocimiento, el método de extracción para los tensioactivos de muestras atmosféricas presentados en este artículo es actualmente el más selectivo en la química atmosférica. En particular, es mucho más selectiva que las extracciones de agua simples realizadas en el pasado para la investigación de estos compuestos. 11, 23, 24 La segunda etapa de extracción es importante ya que se ha demostrado para eliminar los componentes iónicos, tales como sales inorgánicas y ácidos orgánicos pequeños, que se encuentran en grandes concentraciones en las muestras de aerosol e interfieren con la measur concentraciónements. 6 Este método de extracción también se ha demostrado para eliminar todos los tensioactivos presentes en las muestras, en la superficie y en la masa. Los extractos resultantes se concentraron por lo tanto suficiente para permitir caracterizaciones precisas de estos compuestos.
Sin embargo, además de los tensioactivos, es posible que otros compuestos no polares o ligeramente polares se extraen de los aerosoles atmosféricos. Por ejemplo, "húmico-como Sustancias" (Hulis), que normalmente se extraen por métodos similares 25 y, dependiendo de la región de muestreo, podrían estar presentes en los extractos. Estos compuestos son sólo ligeramente surfactante en comparación con los tensioactivos se caracterizan en nuestras muestras, 26, 27, 28 por lo tanto no debe contribuir significativamente a la tensión superficial o CMC medido. Sin embargo, son poliácidos y podrían interferir con la conce aniónico mediciones ntration. En el futuro, tendrá que ser determinado su contribución a las concentraciones de tensioactivo (es decir, si o no reaccionan con violeta de etilo, el colorante utilizado para valorar tensioactivos aniónicos). Si su contribución es significativa, pasos adicionales podrían añadirse al método de extracción, para eliminar, por ejemplo, todos los compuestos que son activos en el UV-Vis o por fluorescencia, que incluiría Hulis pero no tensioactivos.
Hasta ahora, ningún otro método para la medición de la tensión superficial de los aerosoles y de la curva de tensión superficial para los tensioactivos de aerosol que el presentado en este manuscrito está disponible. La técnica de gota colgante se recomienda para estas mediciones, ya que es el único que requieren volúmenes de muestra consistente con muestras atmosféricas. técnicas ópticos, de medida directamente la tensión superficial sobre las partículas de tamaño micrométrico sin ninguna extracción, se están desarrollando. 10,culo = "xref"> 20, 29 Hasta el momento, sólo se aplican a las partículas producidas en el laboratorio, pero potencialmente podría algún día ser aplicado a las atmosféricas.
El método colorimétrico presentado en este trabajo para la medición de la concentración de tensioactivo que se ha aplicado previamente a las muestras de aerosol atmosférico 11, 13, 14, 30, pero sólo para los extractos de agua y no duplicar extractos, como en nuestro método. Esta es una diferencia importante como, como se ha subrayado anteriormente, la segunda etapa de extracción elimina compuestos tales como sales inorgánicas y ácidos orgánicos pequeños, que interfieren con las mediciones de la concentración. 6
Una técnica electroquímica, desarrollado inicialmente para el agua de mar y las muestras acuosas más grandes, también se ha utilizado para medir la concentración de tensioactivos en atmosaerosoles atmosféri-. 31, 32 Este método es relativa, es decir, las concentraciones de tensioactivo obtenidos dependen de los compuestos de referencia escogidos y se supone que la sensibilidad de detección de todos los tensioactivos es idéntico. El límite de detección reportados para esta técnica es 0,02 mg L -1 utilizando tetra-octylphenolethoxylate como referencia, por tanto, 0,03 M, y comparable a la del límite de detección de aproximadamente 0,05 M para los tensioactivos aniónicos y catiónicos por el método colorimétrico. Pero debido a las incertidumbres en la determinación de las concentraciones de tensioactivo no iónicos y total con el método colorimétrico, sería interesante comparar los dos métodos (inter-calibración).
Unos pocos puntos en los métodos presentados podrían mejorarse aún más.
Otro colorante de tiocianato de cobalto que pueda detectar todos los tensioactivos no iónicos y el ingenio la misma sensibilidad sería muy USEFul y reducir la fuente principal de las incertidumbres en las mediciones de concentración de corriente.
La eficacia de la extracción para los tensioactivos catiónicos, que actualmente se estima a 20%, también podría mejorarse, ya que estos compuestos están a menudo en el límite de detección en muestras atmosféricas. Esto podría hacerse, por ejemplo, mediante el uso de una columna específica SPE.
Las extracciones y condiciones de valoración podrían mejorarse aún más. Por ejemplo, utilizando en paralelo tres SPE diferentes reglajes, cada uno optimizado para una clase de tensioactivos, podría mejorar la eficacia de la extracción, y mejorar la calidad del procedimiento (menos riesgos de contaminación). La densidad sorbente óptima del cartucho de SPE para la masa de la muestra a ser analizada también podría sido determinada. Las condiciones para las reacciones de titulación (pH, aditivos) también podrían optimizarse aún más, para mejorar aún más la sensibilidad de las mediciones de la concentración, es decir, disminuir los límites de detección.
pruebas o medidas adicionales podrían añadirse al protocolo de extracción de excluir los compuestos no tensioactivos que podrían haber sido extraídos. Por ejemplo, la presencia potencial de Hulis en las muestras podría ser investigada mediante técnicas ópticas (UV-VIS o fluorescencia).
Otras modificaciones, aunque no la mejora de la calidad de la propia análisis, traerían más información sobre agentes tensioactivos atmosféricos, tales como la aplicación del presente método a diferentes tamaño-fracciones (es decir, sub-poblaciones) del aerosol en lugar de en todas las partículas recogidas, como que aquí se presenta. Otros tipos de análisis también se podrían aplicar a los extractos tales como, LC / HR MS, MS en tándem, o RMN para determinar la estructura química de los agentes tensioactivos o UV-Vis absorbancia, fluorescencia, o polarimetría, para indicar la presencia de altamente compuestos conjugados o quirales en los extractos.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue financiado por SONATA, un proyecto conjunto entre la Agence Nationale de la Recherche (ANR-13-IS08-0001) y la Fundación Nacional de Ciencias de Estados Unidos. Christine Baduel es financiado por la Agencia Nacional Francesa de Investigación (ANR) a través del proyecto ANR-16-ACHN-0026. Los autores también agradecen calurosamente Marija Marguš, Ana Cvitesic, Sanja Frka Milosavljević e Irena Ciglenecki, del Instituto Rudjer Boskovic de Zagreb, Croacia para la ayuda en la toma de muestras de aerosoles en Marina Frapa, Rogoznica, Croacia.
Materiales
| Name | Company | Catalog Number | Comments |
| Quartz filters | Fioroni | for example Ø47mm or Ø150mm, Grammage 85g/m2 | |
| Aluminium foils or glass Petri dishes | backed in oven (773 K, 6h) | ||
| Tweezers, scissors | |||
| Desiccator | |||
| SPE (Solid Phase Extraction) set-up | |||
| SPE vacuum manifold Ac-Elut | Varian | ||
| Pump Laboxat | Knf LAB | ||
| Nitrogen dryer set-up | hand-made | ||
| Compressed Nirogen 4.5 in bottle B50, 200 bar at 15°C | Linde | ||
| Tensiometer | Dataphysics | OCA 15EC | |
| Software | SCA software for OCA version 4-4.1 | ||
| UV-Vis spectrometer | Agilent | 8453 | |
| Stir-plates | |||
| Glassware | |||
| Glass Petri dishes | for the water extraction step | ||
| Beakers | |||
| 15 mL, 30 mL, 60 mL glass bottles with corks | |||
| Tubes for SPE | |||
| Magnetic stirring bars | |||
| Ultrasound bath | for glassware washing | ||
| Micropipettes (0.5 - 5 mL, 0.100 - 1mL, 10 - 100 μL) | Rainin Pipette-Life XLS | ||
| Disposable small equipment | |||
| Syringe filters 0.40μm PVDF | Fisherbrand | ||
| SPE C18 cartridges Strata C18-E cartridges 500 mg / 3 mL | Phenomenex | ||
| Plastic syringes | |||
| Needles | |||
| 4 mL-vials | |||
| Pasteur glass pipettes | |||
| Micropipette tips | |||
| Chemicals | |||
| Sodium dodecyl sulfate (SDS) ≥ 98.5 % Bioreagent | Sigma- Aldrich | L3771 | |
| Dioctyl sulfosuccinate sodium salt (AOT) ≥ 97% | Sigma- Aldrich | 323586 | |
| Benzyltetradecyldimethylammonium (zephiramine) ≥ 99.0 % anhydrous Fluka | Sigma- Aldrich | 13401 | |
| Cetyltrimethylammonium chloride solution (CTAC) 25 wt % in H2O | Sigma- Aldrich | 292737 | |
| (1,1,3,3-tetramethylbutyl)phenyl-polyethylene glycol (Triton X114) laboratory grade | Sigma- Aldrich | X114 | |
| Polyethylene glycol dodecyl ether (Brij35) Fluka Bio Chemika | Sigma- Aldrich | 858366 | |
| L-α-phosphatidylcholine from egg yolk type XVI-E lyophilized powder ≥ 99 % | Sigma- Aldrich | P3556 | |
| Surfactin from Bacillus subtilis ≥ 98 % | Sigma- Aldrich | S3523 | |
| R-95Dd rhamnolipid (95 % dirhamnolipid, 5 % monorhamnolipid) | Sigma- Aldrich | L510025 | |
| Ethyl violet cationic triarylmethane dye | Sigma- Aldrich | 228842 | |
| Patent Blue VF dye content 50 % | Sigma-Aldrich | 198218 | |
| Ammonium thiocyanate ≥ 99 % puriss. p.a., ACS reagent | Sigma-Aldrich | 31120 | |
| Cobalt(II) nitrate hexahydrate ≥ 98 % ACS reagent | Sigma-Aldrich | 239267 | |
| Acetic anhydride ≥ 99 % ReagentPlus | Sigma-Aldrich | 320102 | |
| Sodium acetate ≥ 99.0 % anhydrous Reagent Plus | Sigma-Aldrich | S8750 | |
| Ethylenediaminetetraacetic acid 99.4− 100.6 % ACS reagent powder | Sigma-Aldrich | E9884 | |
| Sodium sulfate anhydrous ≥ 99.0 % granulated puriss. p.a. ACS reagent Fluka | Sigma-Aldrich | 71960 | |
| Ethanol puriss. p.a. ACS Reagent reag. Ph. Eur. 96% (v/v) | Sigma-Aldrich | 32294 | |
| Acetonitrile ≥ 99.9 % HiPerSolv CHROMANORM Reag. Ph. Eur. (European Pharmacopoeia Reagent) grade gradient for HPLC | VWR BDH Prolabo | 20060.32 | to be manipulated under hood |
| Chloroform 99 % stable with 0.8−1 % ethanol | Alfa Aesar | L13200-0F | to be manipulated under hood |
| Toluene > 99 % | Chimie Plus | 24053 | to be manipulated under hood |
| Denatured ethanol for washing | |||
| Ultra-Pure water | Ultrapure water system Purelab Classic, Elga |
Referencias
- Köhler, H. The nucleus in and the growth of hygroscopic droplets. Trans. Faraday Soc. 32, 1152-1161 (1936).
- Noziere, B. CLOUDS. Don't forget the surface. Science. 351, 1396-1397 (2016).
- Onaizi, S. A., Nasser, M. S., Twaiq, F. Adsorption and thermodynamics of biosurfactant, surfactin, monolayers at the air-buffered liquid interface. Colloid Polym Sci. 292, 1649-1656 (2014).
- Ekström, S., et al. A possible role of ground-based microorganisms on cloud formation in the atmosphere. Biogeosci. 7, 387-394 (2010).
- Baduel, C., Nozière, B., Jaffrezo, J. -. L. Summer/winter variability of the surfactants in aerosols from Grenoble, France. Atmos. Environ. 47, 413-420 (2012).
- Gérard, V., et al. Anionic, Cationic, and Nonionic Surfactants in Atmospheric Aerosols from the Baltic Coast at Askö, Sweden: Implications for Cloud Droplet Activation. Environ. Sci. Technol. 50, 2974-2982 (2016).
- Renard, P., et al. Screening of cloud microorganisms isolated at the Puy de Dôme (France) station for the production of biosurfactants. Atmos Chem Phys. 16, 12347-12358 (2016).
- Nozière, B., Baduel, C., Jaffrezo, J. -. L. The dynamic surface tension of atmospheric aerosol surfactants reveals new aspects of cloud activation. Nature Comm. 5, 4335 (2014).
- Ruehl, C. R., Davies, J. F., Wilson, K. R. An interfacial mechanism for cloud droplet formation on organic aerosols. Science. 351, 1447-1450 (2016).
- Jimenez, J. L., et al. Evolution of Organic Aerosols in the Atmosphere. Science. 326, 1525-1529 (2009).
- Latif, M. T., Brimblecombe, P. Surfactants in Atmospheric Aerosols. Environ. Sci. Technol. 38, 6501-6506 (2004).
- Amirov, R. R., Skvortsova, E. A., Saprykova, Z. A. Complexation of Cobalt(II) with Thiocyanate Ions in Aqueous Solutions of Nonionogenic Surfactants. Russ. J. Coord. Chem. 29, 554-558 (2003).
- Jaafar, S. A., et al. Surfactants in the sea-surface microlayer and atmospheric aerosol around the southern region of Peninsular Malaysia. Mar. Pollut. Bull. 84, 35-43 (2014).
- Mustaffa, N., Latif, M., Ali, M., Khan, M. Source apportionment of surfactants in marine aerosols at different locations along the Malacca Straits. Environ Sci Pollut Res. 21, 6590-6602 (2014).
- Motomizu, S., Fujiwara, S., Fujiwara, A., Toei, K. Solvent extraction-spectrophotometric determination of anionic surfactants with ethyl violet. Anal. Chem. 54, 392-397 (1982).
- Yamamoto, K., Motomizu, S. Solvent extraction-spectrophotometric determination of anionic surfactants in sea water. Analyst. 112, 1405-1408 (1987).
- Schmitt, T. M. . Analysis of Surfactants (Surfactant Science). 96, 421-443 (2001).
- Hummel, D. O. . Handbook of Surfactant Analysis: Chemical, Physico-chemical and Physical Methods. , 203 (2000).
- Pacheco e Silva, V., al, e. Method to measure surfactant in fluid. US patent. , (2013).
- Bzdek, B. R., Power, R. M., Simpson, S. H., Reid, J. P., Royall, C. P. Precise, contactless measurements of the surface tension of picolitre aerosol droplets. Chem Sci. 7, 274-285 (2016).
- Desai, J. D., Banat, I. M. Microbial production of surfactants and their commercial potential. Microbiol. Mol. Biol. R. 61, 47-64 (1997).
- Christofi, N., Ivshina, I. B. Microbial surfactants and their use in field studies of soil remediation. J. Appl. Microbiol. 93, 915-929 (2002).
- Facchini, M. C., Mircea, M., Fuzzi, S., Charlson, R. J. Cloud albedo enhancement by surface-active organic solutes in growing droplets. Nature. 401, 257-259 (1999).
- Mircea, M., et al. Importance of the organic aerosol fraction for modeling aerosol hygroscopic growth and activation: a case study in the Amazon Basin. Atmos. Chem. Phys. 5, 3111-3126 (2005).
- Varga, B., Kiss, G., Ganszky, I., Gelencsér, A., Krivácsy, Z. Isolation of water-soluble organic matter from atmospheric aerosol. Talanta. 55, 561-572 (2001).
- Kiss, G., Tombácz, E., Hansson, H. -. C. Surface Tension Effects of Humic-Like Substances in the Aqueous Extract of Tropospheric Fine Aerosol. J Atmos Chem. 50, 279-294 (2005).
- Salma, I., Ocskay, R., Varga, I., Maenhaut, W. Surface tension of atmospheric humic-like substances in connection with relaxation, dilution, and solution pH. J. Geophys. Res. 111, D23205 (2006).
- Taraniuk, I., Graber, E. R., Kostinski, A., Rudich, Y. Surfactant properties of atmospheric and model humic-like substances (HULIS). Geophys. Res. Lett. 34, L16807 (2007).
- Morris, H. S., Grassian, V. H., Tivanski, A. V. Humidity-dependent surface tension measurements of individual inorganic and organic submicrometre liquid particles. Chemical Science. 6, 3242-3247 (2015).
- Roslan, R. N., et al. Surfactants in the sea-surface microlayer and their contribution to atmospheric aerosols around coastal areas of the Malaysian peninsula. Mar. Pollut. Bull. 60, 1584-1590 (2010).
- Orlović-Leko, P., Kozarac, Z., Ćosović, B., Strmečki, S., Plavšić, M. Characterization of atmospheric surfactants in the bulk precipitation by electrochemical tools. J Atmos Chem. 66, 11-26 (2010).
- Frka, S., et al. Surface-active substances in atmospheric aerosol: an electrochemical approach. Tellus B. 64, 12 (2012).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados