Method Article
Bau erschwinglicher, langlebiger ballistischer Gelphantome mit mittlerer Wiedergabetreue für das ultraschallgesteuerte Training von Nervenblockaden
* Diese Autoren haben gleichermaßen beigetragen
In diesem Artikel
Zusammenfassung
Hier demonstrieren wir das Design und die Herstellung von vier kundenspezifischen ballistischen Gelatine-Ultraschallphantomen für das ultraschallgesteuerte Regionalanästhesietraining. Wir entwarfen die Phantome mit computergestützter Designsoftware, verwendeten 3D-gedruckte Modelle, um Silikonformen zu erstellen, und gossen dann geschmolzenes ballistisches Gel in die Formen, um benutzerdefinierte Gewebeschichten zu erstellen.
Zusammenfassung
Ultraschallphantome - Alternativen zu lebendem menschlichem Gewebe - geben den Lernenden die Möglichkeit, eine ultraschallgesteuerte Regionalanästhesie zu üben, ohne den Patienten ein unangemessenes Risiko auszusetzen. Phantome auf Gelatinebasis bieten Pädagogen langlebige und wiederverwendbare Aufgabentrainer. Im Handel erhältliche Phantome auf Gelbasis sind jedoch teuer. In dieser Arbeit untersuchen wir die Herstellung von langlebigen, kostengünstigen, ballistischen Gel-basierten Ultraschallphantomen für mediane, femorale, suprainguinale Faszien iliaca plane und Serratus anterior plane Nervenblockaden sowie eine Methodik zur Herstellung eines Phantoms für jedes ultraschallgesteuerte Nervenblockadeverfahren.
Computer-Aided Design (CAD)-Software wurde verwendet, um vier Phantome zu entwerfen, die die Anatomie der Nervenblöcke der Median-, Femur-, suprainguinalen Faszien-Ilia-Ebene und des Serratus anterior plane nachbilden, einschließlich relevanter Orientierungspunkte und Gewebeebenen. Kunststoffmodelle der gewünschten Gewebeebenen wurden 3D-gedruckt und zur Herstellung von Silikonformen verwendet. Ballistisches Gel wurde geschmolzen und mit Mehl und Farbstoff zu einem flüssigen, echogenen ballistischen Gel vermischt, das in die Silikonformen gegossen wurde. Die Gefäße wurden simuliert, indem mit Hilfe von Metallstäben ein negativer Raum im ballistischen Gel erzeugt wurde. Die Nerven wurden mit Garn simuliert, das in Ultraschallgel getaucht wurde. Simulierte Knochen wurden mittels CAD entworfen und 3D-gedruckt.
Ballistisches Gel ist ein vielseitiges, langlebiges Medium, das zur Simulation einer Vielzahl von Geweben verwendet werden kann und in jede beliebige Form geschmolzen und geformt werden kann. Im Ultraschall liefern diese Phantome realistische Gewebeebenen, die die Grenzen zwischen verschiedenen Haut-, Muskel- und Faszienschichten darstellen. Die Echogenität der Muskelgewebeschichten, Nerven, Gefäße und Knochen ist realistisch, und die Knochen weisen eine signifikante hintere Verschattung auf, wie sie bei einem menschlichen Subjekt beobachtet werden würde. Diese Phantome kosten jeweils 200 $ für das erste Phantom und 60 $ für jedes weitere Phantom. Diese Phantome erfordern einiges an technischem Geschick, um sie zu entwickeln, aber sie können für nur 4 % der Kosten ihrer kommerziellen Gegenstücke gebaut werden.
Einleitung
Ultraschallphantome - Alternativen zu lebendem menschlichem Gewebe - geben den Lernenden die Möglichkeit, medizinische Eingriffe, einschließlich ultraschallgesteuerter Regionalanästhesie (UGRA), zu üben, ohne den Patienten ein unangemessenes Risiko auszusetzen1. Während sie am häufigsten im Spritzgussverfahren von Flüssigsilikonkautschuk hergestellt werden, können kundenspezifische Phantome aus vielseitigen Materialien zu geringeren Kosten hergestellt werden. Organische Gewebe wie Tofu, Schweine- und Rindfleisch sind preiswert, verderben aber schnell und sind schwierig herzustellen2. Menschliches Leichengewebe ist ideal für die anatomische Genauigkeit, aber schwierig und kostspielig zu gewinnen und zu konservieren1. In jüngerer Zeit wurde Virtual Reality eingesetzt, um UGRA-Schulungen anzubieten. Haptisches Feedback ist jedoch eine Schlüsselkomponente des prozeduralen Lernens und wird nur selten umgesetzt. Selbst wenn ein Hardware-Software-Hybridmodell eine hohe visuelle Wiedergabetreue und taktiles Feedback bietet, sind die für die Durchführung eines solchen Trainings erforderliche Hard- und Software häufig unerschwinglich3. Phantome auf Gelatinebasis schaffen ein Gleichgewicht zwischen Kosten, Langlebigkeit und Wiedergabetreue2.
Ballistische Gelatinemodelle sind im Handel erhältlich, aber teuer für eine verderbliche Ressource, die in medizinischen Simulationszentren stark genutzt wird. Kleine, einfache, gelbasierte Ultraschallphantome mit homogenem Parenchym und zwei oder drei simulierten Gefäßen kosten im Einzelhandel Hunderte von Dollar. Zum Beispiel kostet der CAE Blue Phantom Basis-Ultraschall-Trainingsblock mehr als 800 US-Dollar4. Phantome mit höherer Wiedergabetreue, die für einzelne Nervenblockadeverfahren spezifisch sind, kosten Tausende von Dollar. Das CAE Blue Phantom Oberschenkel-Regionalanästhesie-Ultraschall-Trainingsmodell kostet 5.000 US-Dollar (Tabelle 1)5. Um die Kosten zu senken, haben Pädagogen mit maßgefertigten Phantomen experimentiert, bei denen Gelatine oder andere kostengünstige oder wiederverwendbare Materialien verwendetwurden 6,7,8. Zusätze wie Mehl, Maisstärke, Graphitpulver und Metamucil können verwendet werden, um die Gelatine zu trüben und die Echogenität des Phantoms anzupassen, wodurch seine Genauigkeit 8,9,10,11,12,13,14 erhöht wird.
Frühere Versuche mit hausgemachten Nervenblockiertrainern auf Gelatinebasis waren entweder nicht in der Lage, das Aussehen der Nerven unter Ultraschall angemessen nachzubilden, oder es wurden verderbliche Gegenstände verwendet, wodurch die Haltbarkeit eingeschränktwurde 15,16. Auch ohne diese Nachteile enthielten frühere Iterationen keine relevanten anatomischen Orientierungspunkte und Faszienebenen, die es den Auszubildenden ermöglicht hätten, spezifische Nervenblockadeverfahren zu üben. In dieser Arbeit untersuchen wir die Herstellung von langlebigen, kostengünstigen, ballistischen Gel-Ultraschallphantomen für mediane, femorale, suprainguinale Faszien-iliaca-Ebene und Serratus-Nervenblockaden in der anterioren Ebene sowie eine Methodik zur Herstellung eines Phantoms für ultraschallgesteuerte Nervenblockadeverfahren.
Protokoll
Für dieses Projekt stellten sich die Autoren JR und PS freiwillig als Ultraschall-Probanden zur Verfügung, und von beiden wurde die mündliche Zustimmung eingeholt. Diejenigen, die dieses Protokoll befolgen, sollten die Genehmigung einer Ethikkommission oder eines institutionellen Prüfungsausschusses (IRB) einholen, bevor sie Patienten oder menschliche Freiwillige als Studienteilnehmer verwenden.
1. Phantomdesign und Erstellung von Silikonformen
- Erstellung eines Referenz-Ultraschallbildes
- Lassen Sie für jedes Ultraschallphantom von einem Arzt mit Ultraschall-Subspezialisierung und Vertrautheit mit dem Nervenblockadeverfahren, das durch das gewünschte Phantom simuliert wird, ein Referenz-Ultraschallbild von einem freiwilligen menschlichen Probanden erstellen (Abbildung 1). Stellen Sie sicher, dass dieses Ultraschallbild einen Blick quer zu der entsprechenden Nerven- oder Gewebeebene hat, in die das Anästhetikum injiziert werden würde.
- Design und 3D-Druck von Gewebeschichtmodellen
- Zeichnen Sie Querschnittspläne für jedes Phantom (Abbildung 2) und verwenden Computer-Aided Design (CAD), um plastische Modelle der gewünschten Gewebeschichten und einen äußeren Behälter für die Gesamtform des Phantoms (Abbildung 3A, Ergänzende Akte 1, Ergänzende Akte 2, Ergänzende Akte 3und Ergänzende Akte 4).
HINWEIS: Vom Designstandpunkt aus können Faszienebenenblöcke als eine Reihe eng anliegender Prismen betrachtet werden, die in einem hohlen rechteckigen Prisma mit 5 mm Wänden eingeschlossen sind. Wände von weniger als 5 mm waren zu zerbrechlich für eine zuverlässige Produktion. Dieses rechteckige Prisma dient als äußerste Schicht des Phantoms, in die die anderen Gewebeschichten eingefügt und platziert werden. Das Modell des Nervus medianus (siehe Abbildung 3 und Abbildung 4) verwendet einen gewölbten Behälter anstelle eines rechteckigen Prismas, um die Form eines menschlichen Arms zu simulieren.- Erstellen Sie in einer CAD-Software eine flache Leinwand aus einem Ultraschall-, CT- oder anderen Zielbild mit bekannten Abmessungen. Klicken Sie auf Volumenkörper | Einfügen | Leinwand, wählen Sie Datei, klicken Sie auf die XY-Ebene, ziehen Sie in den +X +Y-Bereich und ziehen Sie so, dass die Bildlänge den bekannten Einheiten entspricht.
- Erstellen Sie ein rechteckiges Prisma über dem Bereich des Bildes, der das Modell umreißt, indem Sie auf Volumenkörper | Skizze erstellen | XY-Ebene | 2-Punkt-Rechteck-Werkzeug. Ziehen Sie das Rechteck über den Bereich und verfeinern Sie es innerhalb der Längen-/Breitenfelder, wenn es geschlossen ist. drücken Sie die Eingabetaste; klicken Sie auf Skizze fertig; Klicken Sie auf Rechteck | Festkörper | Extrudieren; Ziehen Sie das Rechteck auf die gewünschte Höhe und verfeinern Sie es beim Schließen mit dem Höhenfeld. und drücken Sie die Eingabetaste.
HINWEIS: Jedes unserer Modelle hat eine andere Länge und Breite, basierend auf der Anatomie, die sie repräsentieren, aber wir haben in der Regel festgestellt, dass ~100 mm eine effektive Modellhöhe ist. - Erstellen Sie eine weitere Skizze auf dem rechteckigen Prisma, indem Sie auf den oberen Rand des rechteckigen Prismas klicken | Erstellen Sie eine Skizze und zeichnen Sie die gewünschte Anatomie sowie den inneren Rand des umschließenden rechteckigen Prismas, indem Sie auf Skizze | Erstellen und Skizzieren | Ändern von Werkzeugkästen. Verwenden Sie die hinter dem Prisma sichtbare Leinwand, um das Design zu führen. Wenn die Leinwand nicht durch das rechteckige Prisma zu sehen ist, ändern Sie dies über die Anzeigeeinstellungen. Sobald die Skizze, die den Querschnitt des Modells darstellt, erstellt wurde, klicken Sie auf Skizze fertig.
HINWEIS: Es gibt kein spezifisches ideales Werkzeug, um die gewünschte Anatomie und den inneren Rand des Umhüllungsprismas zu zeichnen. Der obige Schritt wurde in diesem Protokoll verwendet. - Erstellen Sie als Nächstes jedes interne Prisma aus der Skizze, indem Sie auf die Form in der Skizze klicken | Festkörper | Extrudieren; Ziehen Sie die Form in der gewünschten Länge zurück in das rechteckige Prisma, in der Regel 5 mm weniger als die volle Rechtecklänge. und klicken Sie auf Operation = Neuer Körper | Eintreten. Um dieses neue Objekt anzuzeigen, deaktivieren Sie die Sichtbarkeit aller anderen Objekte, indem Sie auf Körper | das Augensymbol neben dem Namen des neuen Körpers klicken.
HINWEIS: Gefäße sollten durch kreisförmige oder elliptische prismenförmige Löcher dargestellt werden, die in die Kanten oder Zentren von Faszienebenen eingearbeitet sind. Wenn Sie an dieser Stelle das virtuelle Modell auf der ursprünglichen Leinwand betrachten, können die einzelnen Modellteile und deren Zusammenfügung visualisiert werden. - Exportieren Sie jeden Körper einzeln für den 3D-Druck, indem Sie auf Körper | das Augensymbol neben jedem Körper außer dem zu exportierenden klicken; klicken Sie auf Datei | Exportieren | Typ = .stl-Datei | Eintreten.
HINWEIS: Sie sollten jetzt über mehrere .stl-Dateien verfügen, die jeweils eine eindeutige Faszienebene oder einen eigenen Knochen darstellen, sowie über eine zusätzliche .stl-Datei, die den rechteckigen Begrenzungsrahmen darstellt, in den die Faszienebenenteile passen.
- Öffnen Sie die STL-Datei in einer Slicer-Software, die mit dem 3D-Drucker kompatibel ist, der zum Drucken der Modelle verwendet wird.
- Verwenden Sie die Schaltfläche Auf Gesicht legen, um das Modell so auf das Bett zu legen, dass die Unterseite des Modells das Druckbett berührt.
- Wählen Sie unter Drucker den Drucker aus. Wählen Sie unter Druckeinstellungen die Option 0,20 mm SPEED und unter Filament die Option Generisches PLA aus. Wählen Sie 15-20 % für Füllung, wählen Sie Überall im Menü Stützen und fügen Sie bei Bedarf eine Krempe hinzu, um die Druckstabilität zu gewährleisten. Klicken Sie auf Jetzt aufteilen.
- Exportieren Sie die G-Code-Datei auf eine SD-Karte, schließen Sie sie an den 3D-Drucker an und drucken Sie die Datei mit Polymilchsäure (PLA)-Filament.
- Zeichnen Sie Querschnittspläne für jedes Phantom (Abbildung 2) und verwenden Computer-Aided Design (CAD), um plastische Modelle der gewünschten Gewebeschichten und einen äußeren Behälter für die Gesamtform des Phantoms (Abbildung 3A, Ergänzende Akte 1, Ergänzende Akte 2, Ergänzende Akte 3und Ergänzende Akte 4).
- Erstellung von Silikonformen
- Kleben Sie jedes 3D-gedruckte Modell auf den Boden eines Oben-ohne-Plexiglasbehälters, bevor Sie es gemäß den Herstellerrichtlinien17 in schnell aushärtenden Silikonkautschuk tauchen.
- Sobald das Silikon ausgehärtet ist, entfernen Sie das Hartplastikmodell und das Plexiglasgehäuse, und hinterlassen Sie eine flexible, haltbare und wiederverwendbare Silikonform aus jeder gewünschten Gewebeschicht und jedem Behälter, in die ballistisches Gel gegossen wird (Abbildung 3B).
HINWEIS: Zu diesem Zeitpunkt kann das Protokoll pausiert und später neu gestartet werden.
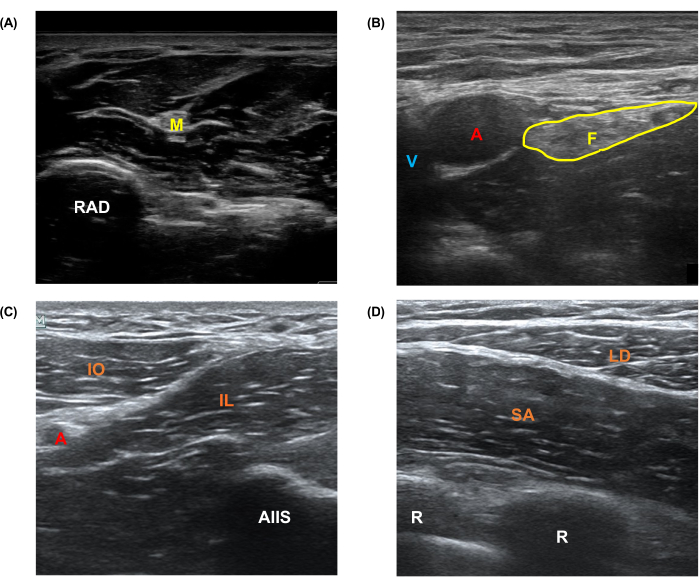
Abbildung 1: Repräsentative Ultraschallbilder, die von einem menschlichen Probanden aufgenommen wurden. Repräsentative Bilder für die Nervenblockmodelle (A) Median, (B) Femur, (C) suprainguinale Faszie iliaca und (D) serratus anterior plane Nervenblockademodelle, die von freiwilligen menschlichen Probanden erhalten wurden. Abkürzungen: A = Arterie; V = Ader; M = Nervus medianus; F = Nervus femoralis; RAD = Radius; U = Ulna; AIIS = vordere untere Beckenwirbelsäule; R = Rippe; SART = Sartorius-Muskel; IL = Iliacus-Muskel; IO = interner schräger Bauch; SA = Musculus serratus anterior; LD = Musculus latissimus dorsi. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Schnittschemata von Nervenblock-Ultraschallphantomen. (A) Mediane, (B) femorale, (C) suprainguinale Faszien-iliaca-Ebene und (D) serratus anteriore Ebene Nervenblock-Ultraschallphantome. Die Schaltpläne wurden auf der Grundlage der in Abbildung 1 gezeigten repräsentativen menschlichen Ultraschallbilder erstellt. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 3: Erstellung von Komponenten des Phantoms der Blockade des Nervus medianus. (A) Repräsentatives Bild der computergestützten Designdatei, die zum Drucken von plastischen Modellen jeder Gewebeschicht für das Phantom der Blockade des Nervus medianus verwendet wird. (B) Silikonformen für jede Gewebeschicht des Blockphantoms des Nervus medianus, einschließlich Metallstäben, die eingesetzt werden, um Gefäße innerhalb des ballistischen Gels zu erzeugen. (C) Gießen Sie heißes, flüssiges, gefärbtes ballistisches Gel in die Silikonformen. (D) Versiegeln des offenen Endes simulierter Gefäße mit flüssigem ballistischem Gel, nachdem die Gefäße mit simuliertem Blut gefüllt wurden. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
2. Erstellung weiterer Phantom-Landmarken
- Simuliertes Knochendesign und -erstellung
- Wenn der Bereich des in CAD entworfenen Modells Knochen anstelle von Weichgewebe darstellt, drucken Sie mit den obigen Schritten einen künstlichen Knochen in 3D, verwenden Sie jedoch stattdessen Acrylnitril-Butadien-Styrol (ABS)-Filament.
VORSICHT: ABS-Filamentdämpfe können flüchtige organische Verbindungen (VOCs) enthalten, die körperliche Beschwerden wie Schläfrigkeit, Augen- oder Atemwegsreizungen, Übelkeit und/oder Kopfschmerzen verursachen können18. ABS sollte auf einem geschlossenen 3D-Drucker oder einem nicht geschlossenen Drucker in einem Raum mit guter Belüftung und/oder Luftfilterung gedruckt werden.
- Wenn der Bereich des in CAD entworfenen Modells Knochen anstelle von Weichgewebe darstellt, drucken Sie mit den obigen Schritten einen künstlichen Knochen in 3D, verwenden Sie jedoch stattdessen Acrylnitril-Butadien-Styrol (ABS)-Filament.
- Simulierte Nervenbildung
- Tauchen Sie 80 % Acryl- und 20 % Wollgarn in einen mit Ultraschallgel gefüllten Plastikbecher. Stellen Sie den Becher in eine Druckkammer mit -1 atm.
- Verwenden Sie eine einstufige Vakuumpumpe, um wiederholt Druck in der Kammer aufzubauen und dann abzulassen, bis alle Blasen aus dem Ultraschallgel entfernt wurden, was nach ca. 4-6 Zyklen erreicht wird.
HINWEIS: Dieser Schritt hilft bei der Simulation von Nerven. Zu diesem Zeitpunkt kann das Protokoll pausiert und später neu gestartet werden.
3. Ballistisches Gel Schmelzen und Gießen
- Schmelzen des ballistischen Gels
- Handelsübliches ballistisches Gel und Farbstoff in einem Volumenverhältnis von ca. 20:1 unter intermittierendem Rühren erhitzen, bis die Flüssigkeit in einem handelsüblichen Konvektionsofen 132 °C erreicht.
VORSICHT: Erhitztes, flüssiges ballistisches Gel sollte aufgrund der Gefahr von Verbrennungen beim Umgang mit heißen Flüssigkeiten mit Vorsicht gehandhabt werden. Verwenden Sie Ofenhandschuhe, wenn Sie mit Pfannen hantieren, die mit flüssigem ballistischem Gel gefüllt sind. Vermeiden Sie den direkten Kontakt zwischen Haut und flüssigem ballistischem Gel.
- Handelsübliches ballistisches Gel und Farbstoff in einem Volumenverhältnis von ca. 20:1 unter intermittierendem Rühren erhitzen, bis die Flüssigkeit in einem handelsüblichen Konvektionsofen 132 °C erreicht.
- Additive für die Echogenität
- Rühren Sie ca. 4,5 g fein granuliertes Mehl pro kg ballistisches Gel in das flüssige ballistische Gel ein. Lassen Sie das Gel mindestens 20 Minuten unter intermittierendem Rühren im Ofen, um ein gleichmäßiges Mischen zu ermöglichen und eventuelle Blasen entweichen zu lassen.
- Fügen Sie bei Bedarf zusätzliches klares ballistisches Gel oder Farbstoff hinzu, um die Farbe der Mischung so anzupassen, dass sie menschliches Gewebe simuliert.
- Ballistisches Gel, das in Silikonformen gegossen wird
- Führen Sie massive Stahlstäbe mit unterschiedlichen Durchmessern in die dafür vorgesehenen Stellen auf den wiederverwendbaren Silikonformen ein, falls dies für das jeweilige Nervenblockmodell geeignet ist, um Kanäle in den endgültigen Ultraschallphantomen zu schaffen, die Blutgefäße darstellen (Abbildung 3C).
- Gießen Sie flüssiges ballistisches Gel, jetzt durch Farbstoff gefärbt, mit suspendierten Mehlpartikeln und ohne zurückgehaltene Luftblasen, in die Silikonformen und lassen Sie es abkühlen.
- Entfernen Sie nach dem Abkühlen die Metallstäbe und die letzten ballistischen Gelgewebeschichten aus den Formen. Wenn sie zusammen mit einer Ultraschall-Gelbeschichtung platziert werden, richten sich benachbarte Gewebestücke nahezu perfekt aus und erzeugen zusammen eine simulierte Faszienebene im Ultraschall.
HINWEIS: Jedes Ultraschallphantom benötigt ca. 0,7 kg ballistisches Gel. Die Kühlzeit ist abhängig von der Größe der Gewebeschicht und variiert zwischen 20 min und 1,5 h.
- Zugabe von simuliertem Blut und Versiegelung der Gefäße
- Bei den Gewebeschichten mit simulierten Gefäßen tauchen Sie eine Seite der Gewebeschicht in das flüssige ballistische Gel und lassen Sie es abkühlen, um so eine Seite des Gefäßkanals zu verschließen.
- Halten Sie diese Gewebeschichten aufrecht und verwenden Sie eine Nadel und eine Spritze, um simuliertes Blut in jedes Gefäß einzuführen.
HINWEIS: Wir haben Wasser mit roter oder blauer Lebensmittelfarbe verwendet, um arterielles bzw. venöses Blut darzustellen. - Verwenden Sie noch flüssiges ballistisches Gel, um die verbleibende Gefäßöffnung abzudecken und so jedes mit Flüssigkeit gefüllte Gefäß vollständig abzudichten (Abbildung 3D).
HINWEIS: Zu diesem Zeitpunkt kann das Protokoll angehalten und später neu gestartet werden. Das ballistische Gel muss jedoch erneut geschmolzen werden, um mit dem nächsten Schritt fortzufahren.
4. Phantom-Montage
- Montage von Gewebeschichten, Nerven und Knochen
HINWEIS: Abbildung 4A zeigt die einzelnen Komponenten des Blockphantoms des Nervus medianus unmittelbar vor dem Zusammenbau, einschließlich der Gewebeschichten, simulierten Nerven und simulierten Knochen.- Bauen Sie die Phantome zusammen, indem Sie jede Komponente mit Ultraschallgel beschichten, die Komponenten wie durch die Querschnitte in Abbildung 2 gezeigt zusammenfügen und sie in ihre jeweiligen rechteckigen Gelprismen einsetzen (Abbildung 4B). Platzieren Sie in diesem Schritt alle 3D-gedruckten Knochen oder Fadennerven richtig.
- Abdichten der Enden des Phantoms
- Versiegeln Sie die Modelle, indem Sie sie auf beiden Seiten in eine mit flüssigem ballistischem Gel gefüllte Pfanne tauchen (Abbildung 4C). Wiederholen Sie den Versiegelungsvorgang auf jeder Seite mehrmals.
- Verwenden Sie zum Schluss eine Heißluftpistole, um die Kanten des Phantoms zu glätten, Blasen und Unebenheiten zu entfernen und die Seitendichtungen zu verstärken.
- Zugabe von Pseudohaut (optional)
HINWEIS: Eine Erweiterung der Faszien-Ebenen-Modelle ist die Hinzufügung von Pseudo-Haut.- Gießen Sie flüssiges ballistisches Gel über ein versiegeltes und gekühltes Modell, das locker mit Ultraschallgel bedeckt wurde, um ein Glühen zwischen der neu gegossenen Hautschicht und dem vorhandenen Modell zu verhindern (Abbildung 4D und ergänzendes Video S1).

Abbildung 4: Aufbau eines Ultraschallphantoms einer Blockade des Nervus medianus. (A) Einzelne Komponenten eines zerlegten Phantoms einer Blockade des Nervus medianus, einschließlich ballistischer Gelgewebeschichten, 3D-gedruckter Radius und Elle, eines in Ultraschallgel getauchten Garnnervs medianus, einer Flasche mit Ultraschallgel und einer mit flüssigem ballistischem Gel gefüllten Pfanne. (B) Assemblierung des Phantoms der Blockade des Nervus medianus, einschließlich des Einsetzens von Gewebeschichten und simulierten Knochen, die mit Ultraschallgel bedeckt sind. (C) Versiegeln eines Endes des Phantoms durch Eintauchen in einen Topf mit flüssigem ballistischem Gel. (D) Erstellen einer Pseudohautschicht durch Gießen von flüssigem ballistischem Gel über ein fertiges Phantom der Blockade des Nervus medianus. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Ergebnisse
Vier Ultraschallphantome wurden erfolgreich mit den oben beschriebenen Methoden konstruiert und gebaut. In Abbildung 5 ist ein Ultraschallquerschnitt jedes Modells dargestellt, der mit einem Ultraschall der äquivalenten menschlichen Anatomie ausgerichtet ist. Im Ultraschall liefern diese Phantome realistische Gewebeebenen, die die Grenzen zwischen verschiedenen Haut-, Muskel- und Faszienschichten darstellen. Das Muskelgewebe ist angemessen und homogen echogen. Diese Echogenität kann basierend auf der Menge an Mehl eingestellt werden, die dem ballistischen Gel während des Schmelzens zugesetzt wird. Die Fasziengrenzen sind im Vergleich zum Hintergrundmuskelgewebe hyperechoarm. Das Garn erscheint unregelmäßig echoarm, mit gut definierten Rändern, die das Aussehen eines Nervs angemessen simulieren. Das Garn befindet sich zwischen den Gewebeschichten, und dieser Teil des Phantoms kann die Flüssigkeitsinjektion aufnehmen, um die Injektion eines Lokalanästhetikums während einer Nervenblockade zu simulieren. Darüber hinaus stößt die Injektion in einen ballistischen Gelblock im Vergleich zur Injektion in eine simulierte Faszienebene auf einen erheblichen Widerstand, was als vorteilhafter Feedback-Mechanismus für die Lernenden dienen kann. Die 3D-gedruckten Blöcke aus ABS-Filament simulieren bei der Visualisierung unter Ultraschall den hyperechoischen Kortex und die akustische Abschattung des menschlichen Knochens entsprechend. Simulierte Gefäße erscheinen reflexionsfrei mit klar definierten Rändern, wie sie auch bei ihren lebenden menschlichen Gegenstücken zu sehen sind. Gefärbtes Wasser kann mit einer Nadel aspiriert werden, um den intravaskulären Zugang bei der Durchführung relevanter ultraschallgesteuerter Verfahren zu bestätigen.

Abbildung 5: Repräsentative Ultraschallbilder, die von Ultraschallphantomen im Vergleich zu menschlichen Probanden aufgenommen wurden. (A) Der Median, (B) der femorale, (C) die suprainguinale Faszie iliaca-Ebene und (D) der Nervus serratus anterior plane blockieren die Ultraschallphantome (links) und ein menschliches Subjekt (rechts). Für jedes Ultraschallphantom (links) wurden mehrere Standbilder, die durch das Scannen der Ultraschallphantome erhalten wurden, zusammengefügt, um das gesamte Phantom unter Ultraschall zu demonstrieren. Es wurden keine weiteren Änderungen an den Bildern vorgenommen. Die gestrichelten gelben Kästchen stellen den Bereich des Ultraschallphantoms dar, der mit dem Bild des menschlichen Motivs unmittelbar rechts korreliert. Abkürzungen: A = Arterie; V = Ader; M = Nervus medianus; F = Nervus femoralis; RAD = Radius; U = Ulna; AIIS = vordere untere Beckenwirbelsäule; R = Rippe; SART = Sartorius-Muskel; IL = Iliacus-Muskel; IO = interner schräger Bauch; SA = Musculus serratus anterior; LD = Musculus latissimus dorsi. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Ergänzende Datei 1: Computergestütztes Design von plastischen Modellen, die jede gewünschte Gewebeschicht für das Ultraschallphantom der Mediannervenblockade darstellen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 2: Computergestützte Konstruktion von plastischen Modellen, die jede gewünschte Gewebeschicht für das Ultraschallphantom der Femurnervenblockade darstellen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 3: Computergestütztes Design von plastischen Modellen, die jede gewünschte Gewebeschicht für das Ultraschallphantom des suprainguinalen Faszien iliaca plane blocks darstellen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Datei 4: Computergestütztes Design von Kunststoffmodellen, die jede gewünschte Gewebeschicht für das Ultraschallphantom des Serratus-Blocks in der anterioren Ebene darstellen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzendes Video S1: Hinzufügung von Pseudohaut zum Ultraschallphantom der Blockade des Nervus medianus. Durch das Gießen von flüssigem ballistischem Gel über ein fertiges Ultraschallphantom mit einer minimalen Schicht Ultraschallgel darüber entsteht eine dünne Abdeckung, die sich wie Haut anfühlt und bewegt. Dieses Video zeigt die Fähigkeit der Pseudohaut, die Bewegung der menschlichen Haut nachzuahmen, wenn sie dagegen gedrückt wird. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Diskussion
Diese kundenspezifischen ballistischen Gel-basierten Phantome bieten den Auszubildenden ein Training von Nervenblockaden in der Median-, Femur-, suprainguinalen Faszien-, Ilia-Ebene und Serratus in der anterioren Ebene zu einem Bruchteil der Kosten kommerziell erhältlicher Nervenblockphantome (Tabelle 1). Unsere ersten Trainer für Blockaden des Nervus medianus und des Nervus femoralis wurden im eigenen Haus für 12 % bzw. 9 % des Preises der billigsten im Handel erhältlichen Trainer für Blockaden des Nervus medianus und des Nervus femoralis hergestellt. Keines der verfügbaren Phantome der Blockade des Nervus femoralis ist in der Lage, den suprainguinalen Zugang zur Fascia iliaca-Blockade zu simulieren, wie es unser Phantom tut. Wir konnten keine kommerziell erhältlichen Serratus-Ultraschallphantome in der anterioren Ebene finden.
Tabelle 1: Zusammenfassung der kommerziell erhältlichen ultraschallgesteuerten Regionalanästhesiephantome. Bitte klicken Sie hier, um diese Tabelle herunterzuladen.
In den letzten zehn Jahren ist die 3D-Drucktechnologie zugänglicher und erschwinglicher geworden. Zum Beispiel kostet der Original Prusa i3 MK3S+ 3D-Drucker, der in diesem Protokoll verwendet wird, zwar nicht die neueste Ausgabe, aber nur 64919 US-Dollar. Selbst der kleinere Prusa MINI+, der für die Herstellung der hier beschriebenen Modelle ausreicht, kostet nur 42920 US-Dollar. Die meisten Ersatzteile für diese Drucker werden selbst in 3D gedruckt, wodurch die Reparaturkosten weiter minimiert werden. Studenten und Dozenten können in der Regel über den Makerspace oder das Designlabor ihrer Institution kostenlos auf 3D-Drucker zugreifen. Das Entwerfen von Objekten für den 3D-Druck ist bequemer denn je mit CAD-Programmen (Computer-Aided Design), von denen einige kostenlos verfügbar sind21.
Die Zeit, die für die Konstruktion der 3D-gedruckten Modelle und simulierten Knochen benötigt wird, hängt von den Fähigkeiten und der Vertrautheit des Benutzers mit der CAD-Software ab. Dieser Prozess kann jedoch ohne Kosten mit Software wie FreeCAD oder mit CAD-Software, die von der Gastinstitution lizenziert wurde,durchgeführt werden 21. Die Herstellung von Silikonformen jeder Gewebeschicht ist nicht zeitintensiv. Silikon kostet 28 $ pro kg, wobei jedes Phantom 4-6 kg Silikon benötigt (insgesamt 140 $). Da die Silikonformen wiederverwendbar sind, handelt es sich um eine einmalige Ausgabe.
Unser kommerzielles ballistisches Gel kostet 86 US-Dollar pro kg, und jedes Phantom benötigte etwa 0,7 kg zu einem Preis von 60 US-Dollar pro Phantom. 3D-Druckstrukturen, die für das Formen benötigt werden, erfordern vernachlässigbare Kosten für PLA- oder ABS-Filament. Zwei unserer Phantome erforderten 100 mm Garn zu 10 $ pro m oder 0,01 $ pro Phantom. Insgesamt kostete jedes Phantom ~200 US-Dollar für die Herstellung des ersten Modells und 60 US-Dollar für jedes weitere Modell. Der Produktionsprozess erforderte 1 Mannstunde und 3-4 h Erhitzen und Kühlen des Gels. Wir waren in der Lage, vier Modelle gleichzeitig im gleichen Zeitraum zu bauen.
Ballistisches Gel ist aufgrund seiner Vielseitigkeit ein ideales Medium. Es kann verwendet werden, um eine Vielzahl von Geweben zu simulieren und kann geschmolzen und in jede beliebige Form gebracht werden. Sobald das Gel verfestigt ist, heilen sich Unvollkommenheiten oder Nadeleinstiche etwas von selbst und können mit einer Heißluftpistole weiter geflickt werden. Wenn es einen Fehler im Phantom gibt, wenn es beschädigt oder überbeansprucht wird, können die ballistischen Gelkomponenten jederzeit zerlegt, gereinigt und wieder eingeschmolzen werden, um mit minimalem Materialverlust wiederverwendet zu werden. Ballistisches Gel ist auch kostengünstig. Obwohl diese Phantome mit 86 US-Dollar pro kg die teuerste Komponente dieser Phantome sind, sind sie immer noch weitaus günstiger als kommerziell erhältliche Ultraschallphantome (Tabelle 1). Phantome, die aus hausgemachter Gelatine hergestellt werden, wurden bereits beschrieben und sind vermutlich noch erschwinglicher, aber diese Phantome entwickeln innerhalb von Tagen bis Wochen Schimmel, selbst wenn sie im Kühlschrank gelagert werden16. Wir haben die Phantome in einer sauberen, trockenen Umgebung bei Raumtemperatur für Monate bis Jahre gelagert, ohne zu verderben oder zu verderben.
Die Simulation von Nerven in Gelatine für ultraschallgesteuerte Nervenblockmodelle hat sich für Pädagogen als schwierig erwiesen. Frühere Versuche haben tierische Sehnen22, 23, 24, elektrische Drähte25, Holzdübel25, Schnürsenkel26, Metallstangen27, Bündel von Gummibändern15, Schaumstoff28, Erbsen29, Spaghetti30 und sogar ein Ethernet-Kabel31 verwendet. Diese Optionen sind unrealistisch, verderblich oder erzeugen eine signifikante hintere akustische Abschattung unter Ultraschall. Wir haben einen Haushaltsgegenstand, Garn, verwendet, um simulierte Nerven mit hoher Wiedergabetreue mit wenig bis gar keiner hinteren Abschattung für nur 0,10 US-Dollar pro m oder 0,01 US-Dollar pro Phantom herzustellen.
ABS-Filament wurde für den 3D-Druck von Knochenimitat verwendet, da es eine höhere Hitzetoleranz als PLA aufweist und sich in den nachfolgenden Schritten während der Entwicklung dieses Verfahrens verzog. Wir haben die Backtemperatur maximiert, um die Schmelzzeiten zu minimieren und die Viskosität und Anzahl der Blasen zu verringern. Dies ermöglicht ein glatteres, raumfüllenderes Eingießen in die Silikonformen und hält gleichzeitig die Temperatur unter der Brenntemperatur des Gels, wodurch eine übermäßige Rauchentwicklung vermieden wird.
Der Hauptnachteil dieser Phantome ist die Zeit und Energie, die für ihre Konstruktion und ihren Bau erforderlich ist. Das Entwerfen von Gewebeebenen mit CAD erfordert technisches Geschick, und der 3D-Druck von Modellen erfordert Grundkenntnisse über 3D-Drucker, das Schneiden einer STL-Datei, die Auswahl eines Filaments und die zu verwendenden Einstellungen und Temperaturen. Die Herstellung von Silikonformen für jede Gewebeebene verursacht zusätzliche Kosten, da Silikon mit 28 US-Dollar pro kg die zweitteuerste Komponente dieses Protokolls ist. Diese Silikonformen sind jedoch langlebig und wiederverwendbar, so dass sie nach ihrer Herstellung zur Herstellung zahlreicher Ultraschallphantome wiederverwendet werden können. Zu den weiteren Nachteilen gehören die Lernkurve, die mit dem Mischen und Ausgießen von ballistischem Gel verbunden ist, sowie die mangelnde technologische Integration dieser Phantome im Vergleich zu kommerziellen High-Fidelity-Schaufensterpuppen. Wir sind jedoch der Meinung, dass die relative Leichtigkeit der Konstruktion, die einfache Materialbeschaffung, die Anpassbarkeit, die niedrigen Kosten und die Recyclingfähigkeit dieses Modelldesigns seine Nachteile bei weitem überwiegen. Wir hoffen, dass die Verbreitung ihrer Konstruktionsmethode ein verbessertes Training von Nervenblockadeverfahren in Einrichtungen ermöglichen wird, die es sich nicht leisten können, teure kommerzielle medizinische Simulationsgeräte häufig zu ersetzen. Zukünftige Studien sollten benutzerdefinierte Phantome für zusätzliche Nervenblockadeverfahren untersuchen und die Zufriedenheit und klinische Leistung von Auszubildenden, die diese Phantome verwenden, im Vergleich zu ihren Mitschülern bewerten.
Offenlegungen
Die Autoren dieses Papiers haben keine Interessenkonflikte offenzulegen.
Danksagungen
Dieses Projekt wurde vom Simulation Training Center (STC) an der University of California, San Diego School of Medicine in La Jolla, Kalifornien, finanziert. Wir danken Blake Freechtle für seine Beiträge zu Abbildung 5.
Materialien
| Name | Company | Catalog Number | Comments |
| ABS Filament - 1.75 m+B+A2:A14 | Hatchbox (Pomona, CA) | https://www.hatchbox3d.com/collections/abs-1-75mm | |
| Adobe Photoshop | Adobe (San Jose, CA) | https://www.adobe.com/products/photoshop.html | |
| Amber Tone Dye | Humimic Medical (Greenville, SC) | 852844007925 | Ballistic gel dye; https://humimic.com/product/amber-tone-dye/ |
| Fusion 360 | Autodesk (San Franciso, CA) | Computer-assisted design (CAD) software; https://www.autodesk.com/products/fusion-360/overview?term=1-YEAR&tab=subscription&plc=F360 | |
| Gelatin #1 - Medical Gel by the Pound | Humimic Medical (Greenville, SC) | 852844007406 | Ballistic gel; https://humimic.com/product/gelatin-1-medical-gelatin-by-the-pound/ |
| Gluten-Free All-Purpose Flour | Arrowhead Mills (Hereford, TX) | Flour for echogenicity; https://arrowheadmills.com/products/gluten-free/organic-gluten-free-all-purpose-flour/ | |
| Microsoft PowerPoint | Microsoft (Redmond, WA) | https://www.microsoft.com/en-us/microsoft-365/powerpoint | |
| Mold Star 16 FAST Pourable Silicone Rubber | Smooth-On (Macungie, PA) | Pourable silicone rubber; https://www.smooth-on.com/products/mold-star-16-fast/ | |
| Peach Tone Dye | Humimic Medical (Greenville, SC) | 852844007895 | Ballistic gel dye; https://humimic.com/product/peach-tone-dye/ |
| PLA Filament - 1.75 mm | Hatchbox (Pomona, CA) | https://www.hatchbox3d.com/collections/pla-1-75mm | |
| Prusa Original i3 MK3S+ printer | Prusa Research (Prague, Czech Republic) | 3D printer; https://www.prusa3d.com/category/original-prusa-i3-mk3s/ | |
| Prusa Slicer 2.6.1 | Prusa Research (Prague, Czech Republic) | 3D printer slicer software; https://www.prusa3d.com/page/prusaslicer_424/ | |
| Wool-Ease Thick & Quick Yarn | Lion Brand Yarn (Lyndhurst, NJ) | 640-610B | Yarn for simulated nerves; https://www.lionbrand.com/products/wool-ease-thick-and-quick-yarn?variant=32420963516509 |
Referenzen
- Hocking, G., Hebard, S., Mitchell, C. A review of the benefits and pitfalls of phantoms in ultrasound-guided regional anesthesia. Reg Anesth Pain Med. 36 (2), 162-170 (2011).
- Culjat, M. O., Goldenberg, D., Tewari, P., Singh, R. S. A review of tissue substitutes for ultrasound imaging. Ultrasound Med Biol. 36 (6), 861-873 (2010).
- Grottke, O. Virtual reality-based simulator for training in regional anaesthesia. Br J Anaesth. 103 (4), 594-600 (2009).
- CAE Healthcare. Regional anesthesia ultrasound training block. , https://medicalskillstrainers.cae.com/regional-anesthesia-ultrasound-training-block/p (2023).
- CAE Healthcare. Gen II femoral vascular access & regional anesthesia ultrasound training model. , https://medicalskillstrainers.cae.com/gen-ii-femoral-vascular-access-and-regional-anesthesia-ultrasound-training-model/p (2023).
- Osmer, C. L. A gelatine-based ultrasound phantom. Anaesthesia. 63 (1), 107(2008).
- Nicholson, R. A., Crofton, M. Training phantom for ultrasound guided biopsy. Br J Radiol. 70, 192-194 (1997).
- Bude, R. O., Adler, R. S. An easily made, low-cost, tissue-like ultrasound phantom material. J Clin Ultrasound. 23 (4), 271-273 (1995).
- Patel, A. S., Harrington, T. J., Saunt, K. S., Jones, W. K. Construction of an ultrasound biopsy phantom. Australas Radiol. 40 (2), 185-186 (1996).
- Culp, W. C. Relative ultrasonographic echogenicity of standard, dimpled, and polymeric-coated needles. J Vasc Interv Radiol. 11 (3), 351-358 (2000).
- Morehouse, H., Thaker, H. P., Persaud, C. Addition of Metamucil to gelatin for a realistic breast biopsy phantom. J Ultrasound Med. 26 (8), 1123-1126 (2007).
- Phal, P. M., Brooks, D. M., Wolfe, R. Sonographically guided biopsy of focal lesions: a comparison of freehand and probe-guided techniques using a phantom. AJR Am J Roentgenol. 184 (5), 1652-1656 (2005).
- McNamara, M. P., McNamara, M. E. Preparation of a homemade ultrasound biopsy phantom. J Clin Ultrasound. 17 (6), 456-458 (1989).
- Gibson, R. N., Gibson, K. I. A home-made phantom for learning ultrasound-guided invasive techniques. Australas Radiol. 39 (4), 356-357 (1995).
- Lollo, L., Stogicza, A. R. Low-cost, high-fidelity ultrasound phantom gels for regional anesthesia training programs. MedEdPORTAL. 8, (2023).
- Rathbun, K. M., Brader, W. T., Norbury, J. W. A simple, realistic, inexpensive nerve phantom. J Ultrasound Med. 38 (8), 2203-2207 (2019).
- Smooth-On. Mold Star™ 16 FAST Product Information. , https://www.smooth-on.com/products/mold-star-16-fast/ (2023).
- Wojtyła, S., Klama, P., Baran, T. Is 3D printing safe? Analysis of the thermal treatment of thermoplastics: ABS, PLA, PET, and nylon. J Occup Environ Hyg. 14 (6), D80-D85 (2017).
- Prusa Research. Original Prusa i3 MK3S+ 3D Printer kit. , https://www.prusa3d.com/product/original-prusa-i3-mk3s-3d-printer-kit/ (2023).
- Prusa Research. Original Prusa MINI+ kit. , https://www.prusa3d.com/product/original-prusa-mini-kit-2/ (2023).
- The FreeCAD Team. FreeCAD: Your own 3D parametric modeler. , https://www.freecad.org/ (2023).
- Xu, D., Abbas, S., Chan, V. W. Ultrasound phantom for hands-on practice. Reg Anesth Pain Med. 30 (6), 593-594 (2005).
- de Oliveira Filho, G. R., et al. Learning curves and mathematical models for interventional ultrasound basic skills. Anesth Analg. 106 (2), table of contents 568-573 (2008).
- Koscielniak-Nielsen, Z. J., Rasmussen, H., Hesselbjerg, L. An animal model for teaching ultrasound-guided peripheral nerve blocks. Reg Anesth Pain Med. 34 (4), 379-380 (2009).
- Pollard, B. A. New model for learning ultrasound-guided needle to target localization. Reg Anesth Pain Med. 33 (4), 360-362 (2008).
- Wells, M., Goldstein, L. The polony phantom: a cost-effective aid for teaching emergency ultrasound procedures. Int J Emerg Med. 3 (2), 115-118 (2010).
- van Geffen, G. J., et al. A needle guidance device compared to free hand technique in an ultrasound-guided interventional task using a phantom. Anaesthesia. 63 (9), 986-990 (2008).
- Liu, Y., Glass, N. L., Power, R. W. Technical communication: new teaching model for practicing ultrasound-guided regional anesthesia techniques: no perishable food products. Anesth Analg. 110 (4), 1233-1235 (2010).
- Sultan, S., Iohom, G., Shorten, G. A novel phantom for teaching and learning ultrasound-guided needle manipulation. J Med Ultrasound. 21 (3), 152-155 (2013).
- Micheller, D. A low-fidelity, high-functionality, inexpensive ultrasound-guided nerve block model. CJEM. 19 (1), 58-60 (2017).
- Sparks, S., Evans, D., Byars, D. A low cost, high fidelity nerve block model. Crit Ultrasound J. 6 (1), 12(2014).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten