Method Article
Schnelle enzymatische Prozessierung von Proteinen für MS-Detektion mit einem Durchfluss-Mikroreaktor
In diesem Artikel
Zusammenfassung
A quick protocol for proteolytic digestion with an in-house built flow-through tryptic microreactor coupled to an electrospray ionization (ESI) mass spectrometer is presented. The fabrication of the microreactor, the experimental setup and the data acquisition process are described.
Zusammenfassung
Die überwiegende Mehrheit der Massenspektrometrie (MS) -Basis Proteinanalyseverfahren beinhalten ein enzymatisches Verdauungsschritt der Detektion vor, typischerweise mit Trypsin. Dieser Schritt ist für die Erzeugung von niedermolekularen Peptide erforderlich, in der Regel mit MW <3000-4000 Da, die innerhalb des effektiven Scan-Bereich der Massenspektrometrie Instrumentierung fallen. Herkömmliche Protokolle beinhalten O / N enzymatische Verdauung bei 37 ºC. Jüngste Fortschritte haben zu der Entwicklung einer Vielzahl von Strategien geführt, in der Regel die Verwendung eines Mikroreaktor mit immobilisierten Enzymen oder aus einer Reihe von komplementären physikalischen Prozessen beteiligt, die die Zeit , die für proteolytischen Verdau zu einigen Minuten (beispielsweise Mikrowellen- oder Hoch reduzieren Druck). In dieser Arbeit beschreiben wir eine einfache und kostengünstige Lösung, die in einem Labor für die Erreichung schnelle enzymatische Verdauung eines Proteins umgesetzt werden können. Das Protein (oder Proteingemisch) adsorbiert an C18-gebundene Umkehrphasen-Hochleistungormance Flüssigchromatographie (HPLC) Siliciumdioxidteilchen in einer Kapillarsäule vorgespannt, und Trypsin in wässrigem Puffer wird für eine kurze Zeit über die Teilchen infundiert. Zu ermöglichen Online-MS-Detektion, die tryptischen Peptide werden mit einem Lösungsmittelsystem mit einem erhöhten Gehalt an organischen Stoffen direkt in der MS-Ionenquelle eluiert. Dieser Ansatz vermeidet die Verwendung von hochpreisigen immobilisiertem Enzympartikel und erforderlich macht keine Hilfe für den Prozess abzuschließen. Protein Verdauung und vollständige Probenanalyse kann in weniger als ~ 3 min und ca. 30 min bzw. erreicht werden.
Einleitung
Die Identifizierung und Charakterisierung der gereinigten Proteine wird unter Verwendung von MS-Techniken häufig erreicht. Das Protein wird mit einem Enzym verdaut und die Peptide werden weiter durch MS analysiert, indem eine einfache Infusionsversuchsaufbau verwendet. Proteolytische Verdauung ist zur Erzeugung von kleinen Peptidfragmente notwendig, die in der nützlichen Massenbereich von den meisten MS-Analysatoren fallen, und das kann leicht durch geringe Energiestoßinduzierte Dissoziation fragmentiert werden, um Aminosäuresequenzinformation zu erzeugen. Für isolierte Proteine oder Proteingemische einfache, gibt es keine weitere Notwendigkeit für die chromatographische Trennung von Peptiden vor der MS-Detektion. Eine Mischung aus 25-50 Peptide können leicht durch Infundieren der Probe mit einer Spritzenpumpe in den MS-Ionenquelle direkt analysiert werden.
Das Massenspektrometer kann die Analyse durchzuführen und die Sequenz eines Proteins innerhalb einer kurzen Zeitrahmen zu bestätigen. Bei modernen Datenerfassungsverfahren kann dieses Verfahren durchgeführt werden wnnerhalb ein paar Minuten oder sogar Sekunden. Der begrenzende Faktor des gesamten Prozesses in Vollendung auf einer kurzen Zeitskala ist die proteolytischen Verdauungsschritt. Normalerweise ist dies ein paar Stunden (oder O / N) durchgeführt über, in Lösung, bei 37 ° C, unter Verwendung von Substrat: Enzym-Verhältnisse von (50-100): 1. Um die enzymatische Digestionszeit auf Minuten oder Sekunden, immobilisierte Enzym Mikroreaktoren, in Form von Mikrofluidik - Reaktoren oder handelsüblichen Kartuschen zu verringern, sind beschrieben worden. 1-6 Typischerweise wird das Enzym durch kovalente, nicht-kovalente / physikalische Adsorption, Komplex immobilisiert 3,6 die verbesserte Effizienz des enzymatischen Verfahrens durch die große Oberfläche-zu-Volumen und Enzym-zu-Substrat - Verhältnisse Bildung oder Verkapselung, aktiviert zu werden. Weitere Vorteile von immobilisierten Reaktoren sind ua Autolyse und Störungen durch das Enzym in MS-Analyse reduziert, Enzymstabilität und Wiederverwertbarkeit verbessert. Eine Vielzahl von Ansätzen unter Verwendung von Glas- oder Polymer mikrofabrizierten Vorrichtungen beschrieben worden sind,Enzyme immobilisiert auf magnetischen Kügelchen durch Antikörper-Antigen - Wechselwirkungen unter Verwendung 7,8 in Gold - Nanopartikel Netzwerke eingeschlossen, 9 in Titandioxid-Aluminiumoxid - Sol-Gele 10 und nanozeolites verkapselt, 11 oder gefangen durch Ni-NTA oder His-Tag - Komplexbildung. 6 Alternativ ebenso wurden 12 Darüber hinaus hat gezeigt , verbesserte proteolytischen Spaltung wurde, offenen Rohr Kapillaren mit immobilisierten Enzymen entwickelt., unter Verwendung von gesteuerten Mikrowellenbestrahlung 13 oder druckunterstützten oder Druckzyklisierung Technologie (PCT) zur Verringerung der Reaktionszeiten auf 30-120 min. 14
Trotz der vielen Vorteile von immobilisierten Enzymreaktoren, die die Kosten der kommerziellen Patronen hoch ist, die Verfügbarkeit von Mikrofluidik-Vorrichtungen für die Routineanwendung ist begrenzt, und die Verwendung von Mikrowellen- oder PCT Technologien führt Notwendigkeit zusätzlicher Instrumentierung. Das Ziel dieser Arbeit war es, ein Verfahren zu entwickeln, die circumvezur Durchführung einer enzymatischen Spaltung von Proteinen in der Vorbereitung für MS-Analyse innerhalb von Minuten ngen diese Nachteile, und das kann leicht in jedem Labor durchgeführt werden Forscher mit einem einfachen und effektiven Ansatz zu stärken. Der Ansatz beruht auf der Verwendung von hydrophoben, C18-Teilchen, die in einer Kapillare oder mikrofluidische Vorrichtung vorbelastet sind, und die Adsorption des Protein (e) von Interesse auf den Teilchen durch enzymatischen Verdau während der Infusion des Enzyms über den gefolgten gepackte Bett und nahm Protein (e). In diesem Ansatz wird das Substrat durch nicht-kovalente Wechselwirkungen immobilisiert sind, und das Enzym wird über das immobilisierte Protein infundiert. Die proteolytische Verdauung Effizienz wird durch die große Partikeloberfläche Bereichen erhöht, die das Protein für die enzymatische Verarbeitung, reduzierte Abstände und Diffusionszeiten zu und von der Oberfläche der Teilchen, verbesserte Massenübertragung, keine kovalente Bindung belichten, die die Aktivität des Enzyms beeinflussen können, die Fähigkeit, schnell evaluate Kombinationen verschiedener Enzyme, Entsorgbarkeit und Multiplexen, wenn das Verfahren in einem mikrofluidischen Format ausgeführt. Dieser Ansatz wird unter Verwendung einer Mischung von Standardproteinen und Trypsin-das am häufigsten verwendete Enzym für proteolytischen Verdau vor der ESI-MS-Detektion nachgewiesen. Das Massenspektrometer zur Detektion in dieser Studie verwendet wurde, war eine lineare Quadrupol-Falle (LTQ) -Instrument.
Protokoll
1. Herstellung der Kapillarreaktor
- Schneiden die 100 & mgr; m Innendurchmesser (ID) x 360 um Außendurchmesser (OD) Kapillare auf eine Länge von 7-8 cm, und die 20 & mgr; m ID x 90 um OD Kapillare 3-5 cm mit der Glaskapillare Spalter; unter dem Mikroskop zu überprüfen, dass beide Kapillarenden eine saubere, gerade geschnitten haben, ohne vorstehende Grate.
- Legen Sie die 20 & mgr; m ID x 90 & mgr; m OD Kapillare in ein Ende der 100 & mgr; m ID x 360 & mgr; m OD Kapillare, auf einer Länge von ca. 6 mm; im Bedarfsfall zu beachten, diese Operation unter dem Mikroskop.
- Tragen Sie eine kleine Tröpfchen Kleber E6000 um die Kreuzung der 90 & mgr; m OD / 100 & mgr; m ID Kapillaren mit dem Ende eines Q-Tip, und lassen Sie den Leim Heilung O / N bei RT.
- Schneiden die eingelegte 20 um ID x 90 um OD Kapillare auf eine Länge von ~ 10-15 mm; dies wird der Elektrospray-Ionisations-Emitter sein.
- Vorgeschnittene die 1/32 "OD PEEK, 1/16" OD PEEK und 1/16 "OD PTFE Wanneing in Stücke von 4-5 cm in der Länge; diese werden die Hülsen in der Kapillar-Gewerkschaften verwendet werden, um eine leckfreie Verbindung bereitstellt.
- Schließen Sie das andere Ende der 100 & mgr; m ID x 360 & mgr; m OD Kapillare zu einer PEEK Vereinigung; verwenden, um eine 1/32 "PEEK Hülse für eine leckagefreie Verbindung bereitstellt.
- Insert / ziehen ein Stück ~ 5 cm lange 1/16 "PTFE-Schlauch in das entgegengesetzte Ende der Union.
- Wiegen ca. 4 mg C18 (5 um) Teilchen in einer vorgereinigten / getrocknete 2 ml Glasphiole; 0,5 ml Isopropanol, schließen Sie die Aufschlämmung in dem Ultraschallgerät Bad das Fläschchen und zu verteilen.
- Ziehen Sie mit einer 250 & mgr; l-Spritze etwa 200 & mgr; l Brei, legen Sie die Spritzennadel in den 1/16 "PTFE-Schlauch der PEEK-Vereinigung, und verzichten Sie langsam den Schlamm in den 100 & mgr; m ID x 360 & mgr; m OD Kapillare, beobachten unter dem Mikroskop als die Kapillare füllt sich mit Teilchen bis zu einer Länge von 2-3 mm Verpackung erreicht wird, dies wird der Mikroreaktor (Abbildung 1) werden , um die 20 μ.m ID Kapillare behält die Partikel im Mikroreaktor durch eine Keystone - Effekt. 15
- Spülen Sie das Mikroreaktor mit ~ 50 & mgr; l Lösung von H 2 O / CH 3 CN 50:50 v / v, und dann mit ~ 50 & mgr; l Lösung von H 2 O / CH 3 CN 98: 2 v / v.
2. Herstellung von Beispiellösungen
Hinweis: Operationen, die aus organischen Lösungsmitteln und Säuren und Herstellung der Lösung beinhalten Handhabung sind in einem Abzug durchgeführt werden. Schutzbrille, Handschuhe und Schutzkleidung.
- Spülen mit CH 3 OH und trocknen einige Glasfläschchen (4 ml) und Polypropylenröhrchen (15 ml).
- Herstellung von 10 ml einer Lösung von H 2 O / CH 3 CN (98: 2 v / v) in einem 15 ml Polypropylenröhrchen durch Mischen von 9,8 ml H 2 O mit 200 & mgr; l CH 3 CN; mischen durch Beschallung.
- Herstellung von 10 ml einer Lösung von H 2 O / CH 3 CN (50:50 v / v) in einem 15 ml Polypropylenröhrchen durch Mischen von 5 ml H 2 </ sub> O mit 5 ml CH 3 CN; mischen durch Beschallung.
- Herstellung von 4 ml einer angesäuerten wässerigen Lösung (TFA 0,01% v / v) durch Zugabe von 4 & mgr; l TFA (10%) auf 4 ml H 2 O / CH 3 CN (98: 2 v / v) in einem 4 ml - Glasfläschchen; mischen durch Beschallung.
- Herstellung von 4 ml einer angesäuerten organischen Lösung (TFA 0,01% v / v) durch Zugabe von 4 & mgr; l TFA (10%) auf 4 ml H 2 O / CH 3 CN (50:50 v / v) in ein 4 - ml - Glasgefß; mischen durch Beschallung.
- Man wiegt 16 mg NH 4 HCO 3 mit einer analytischen Mikrowaage in einem 4-ml-Glasampulle; 4 ml des H 2 O / CH 3 CN (98: 2 v / v) Lösung und zu dispergieren durch Beschallung; dies führt zu einer 50 mM Lösung von NH 4 HCO 3 (pH ~ 7,8) in wässrigem Puffer.
- Wiegen 5 mg eines Standard - Proteins (beispielsweise Rinderserumalbumin, Hämoglobin - α / β, Cytochrom C, Carboanhydrase, α-2-HS-Glycoprotein, etc.) mit einem analytischen Mikrowaage in einem 4 - ml - Glasampulle; 4 ml DI water und zerstreuen durch Beschallung; Dies führt in der Regel in einem hohen & mgr; M-Ebene Konzentration Lösung.
- Bereiten Sie 1 ml Proteinlösung (1-2 uM) durch die hohe uM-Level - Konzentration Lösung mit einem geeigneten Volumen von NH 4 HCO 3 (50 mM) wässrigen Puffer verdünnt; mischen durch Beschallung.
- Bereiten Sie die Trypsin - Lösung (5 uM) durch Auflösen von 20 & mgr; g - Sequenzierung-Grade - Trypsin in 170 & mgr; l NH 4 HCO 3 (50 mM) wässrigen Puffer; zerstreuen durch Beschallung.
3. Versuchsaufbau
Anmerkung: Die LTQ-MS-System mit einer modifizierten ESI-Quelle ausgestattet ist, der ein Haus gebaut XYZ-Stufe enthält, die verschiedenen Probeneingabe Ansätze des Massenspektrometers ermöglicht Schnittstelle.
- Trennen Sie das Kapillarreaktor aus der PEEK-Anschluss und eine Verbindung mit dem PEEK-T-Stück.
- Legen Sie eine ~ 2 cm lange Pt-Draht in der Seiten Arm des PEEK-T; verwenden, um eine 1/32 "PEEK Hülse für die Bereitstellung einerleckagefreie Verbindung und für die Pt-Draht isolierend.
- Verbinden einer 50 um x 360 um ID OD (~ 0,5 m lang) Probenübertragungs Kapillare zu dem entgegengesetzten Ende des PEEK Tee; verwenden, um eine 1/32 "PEEK Hülse für eine leckagefreie Verbindung bereitstellt.
- Sichern Sie die PEEK-T-Stück auf der XYZ-Bühne und positionieren Sie den ESI Emitter ~ 2 mm entfernt von dem Massenspektrometer Einlasskapillare.
- Schließen Sie den Pt-Draht an die ESI-Stromversorgungsquelle des Massenspektrometers.
- Schließen Sie das andere Ende der Proben Transferkapillare auf die Edelstahl-Vereinigung; verwenden, um eine 1/16 "PEEK Hülse für eine leckagefreie Verbindung bereitstellt.
- Schließen Sie einen 4-5 cm langen 1/16 "PTFE - Schlauch mit dem gegenüberliegenden Ende des Edelstahl Union und legen Sie die 250 & mgr; l Spritzennadel in dem PTFE - Schlauch, biegen Sie an der Pumpe und stellen Sie die Durchflussrate auf den gewünschten Wert (zB 2 & mgr; l / min).
- Eingangs Tandem-MS-Datenerfassungsparameter in das Softwarepaket, das die MS-Gerät ein steuertals eine Methode Datei bereit Setup-d speichern Sie die Analyse für die Durchführung; für das LTQ-MS-System verwenden, um die abhängigen Analyseparameter folgende Daten: dynamische Ausschluss für 180 Sekunden mit Ausschluss Masse Breite ± 1,5 m / z freigegeben; ein MS um eine Zoom gefolgt Scan und MS 2 Scans auf den Top - 5 - intensivsten Peaks, Zoom Scanbreite von ± 5 m / z; stoßinduzierte Dissoziation (CID) auf Isolationsbreite eingestellt Parameter 3 m / z, normalisierten Kollisionsenergie von 35%, die Aktivierung Q 0,25 und Aktivierungszeit 30 ms.
4. Mikrofluidik-Setup
- Bereiten einer mikrofluidischen Vorrichtung aus Glas oder polymeren Substraten; 16-18 die Anordnung der Vorrichtung ist in Figur 2A, die aus einem Mikroreaktor (1) (0,13 mm Breite x 2 mm Länge x 50 um tief) , die mit einem Einlass (2 ), Auslass (3) und einer Seitenöffnung (4); die Verbindungskanäle für fluidische Manipulationen sind ~110 & mgr; m breit und ca. 50 & mgr; m tief; eine mehrkanalige Struktur (5), bestehend aus ~ 1,5-2 & mgr; m tief x 10 um breit x 100 um lang platziert Mikrokanäle 25 & mgr; m voneinander entfernt, als ein Filter wirken , werden die Partikel in den Mikroreaktor zum Halten.
- Aktivieren Fluidabgabe Verbindungen zu dem Chip durch spezialisierte Verbinder mit den Einlassöffnungen Kleben oder durch ein polymeres Stand Konzeption , die Armaturen für Flüssigkeitsabgabe (2B) aufnimmt. 16
- Bereiten einer Aufschlämmung von Teilchen C18 (5 um), wie in Schritt 1.8; die Aufschlämmung auf den Mikroreaktor mit einer Spritze zu liefern unter Verwendung von 1/16 "PTFE - Schlauch mit dem Chip - Seitenanschluß (4) verbunden, dichten den Port nach Partikelbeladung mit Epoxidkleber und Heilung für 1 h in einem Ofen bei 90 ºC 16.
- Legen Sie eine Kapillare (20 & mgr; m ID x 90 & mgr; m Außendurchmesser x 10 mm Länge) in der Austrittsöffnung, Dichtung mit E6000 Leim und lassen Heilung O / N; dies wird der ESI Emitter werden ( 6).
- Schließen Sie eine 50 & mgr; m ID x 360 & mgr; m OD (~ 0,5 m lang) Probentransfer Kapillare mit dem Chip Einlassöffnung (2); das entgegengesetzte Ende der Kapillare verbinden, wie beschrieben in einen 250 & mgr; l-Spritze und der Spritzenpumpe, in 3,6-3,7.
- Legen Sie eine leichte PEEK T - Anschluss auf der Probenübertragungsleitung kurz vor dem Einlassöffnung (2) und legen Sie eine Pt - Draht auf der Seite-Arm des T, wie in 3.2 beschrieben; dies wird die ESI-Elektrode sein.
- Sichern Sie die Mikrofluidik-Vorrichtung auf der XYZ-Bühne mit dem ESI-Emitter positioniert ~ 2 mm entfernt von dem Massenspektrometer Einlasskapillare; die MS für die Analyse vorzubereiten, wie in 3.8 beschrieben.
5. Probe Beladen, proteolytischen Abbau und Elution für MS-Analyse
Anmerkung: Alle Lösung / sample Transferschritte werden mit Hilfe einer Spritzenpumpe durchgeführt, und sollte für einige weitere Minuten ermöglichen abzuschließen, für die Toten-Volum zu kompensierenes mit den Übertragungsleitungen verbunden sind und von dem Mikroreaktor; die notwendige Zeit hängt von den Strömungsgeschwindigkeiten abhängig beteiligt.
- Spülen Sie das Mikroreaktor und bereiten sie für die Analyse durch eine wässrige Lösung von NH 4 HCO 3 Infundieren (50 mM) in H 2 O / CH 3 CN (98: 2 v / v) bei 2 & mgr; l / min für 5 min; verwenden, um eine 250 & mgr; l-Spritze.
- Laden Sie die Proteinprobe (1 & mgr; M) auf dem Mikroreaktor durch Infundieren der Probenlösung bei 2 ul / min für 5 min; verwenden, um eine 250 & mgr; l-Spritze.
- die Trypsin-Lösung (5 & mgr; M) über das adsorbierte Protein auf der Mikroreaktor bei 2 ul / min für 1-3 min ziehen lassen.
- Quenche die proteolytische Verdauung durch den Mikroreaktor mit einer angesäuerten wässrigen Lösung von TFA Spülen (0,01% v / v) in H 2 O / CH 3 CN (98: 2 v / v) bei 2 & mgr; l / min für 5 min; verwenden, um eine 250 & mgr; l-Spritze.
- Starten Sie das Protein unter Elution aus dem Mikroreaktor verdauen durch eine angesäuerte organische Lösung von TFA Infusion (0,01%v / v) in H 2 O / CH 3 CN (50:50 v / v) bei 300 nl / min.
- Schalten Sie den MS-Daten-Erfassungsprozesses und der ESI-Spannung (~ 2000 V); erwerben MS-Daten die Datenerfassungsparameter zur Verfügung gestellt in Schritt 3.8 verwendet wird; Die Elution der tryptischen Peptide beobachten.
6. Datenverarbeitung
- Verarbeiten Sie die Tandem-MS-Daten mit einer Suchmaschine kompatibel mit dem rohen MS-Datenformat.
- Verarbeiten Sie die LTQ-MS Raw-Dateien einen Organismus spezifischen minimal redundanten Proteindatenbank verwendet wird; laden die Rohdaten in der Suchmaschine, stellen Sie die Eltern und Fragmentionenmassentoleranzen zu 2 und 1 Da jeweils nur voll tryptischen Fragmente verwenden, um mit bis zu zwei für die Suche verpasst cleavages; nicht für posttranslationale Modifikationen ermöglichen; stellen Sie die oberen und mittleren Vertrauen False Discovery Rate (FDR) bis 1% und 3%, bzw., und erlauben keine posttranslationalen Modifikationen.
- Filtern Sie die Daten nur hoch Vertrauen zu wählenPeptid entspricht den Proteinen in der Datenbank; bewerten die Protein- und Peptid-Level-Ergebnisse.
Ergebnisse
Ein repräsentatives Ergebnis eines proteolytischen Verdauungsprozess gleichzeitig durchgeführt auf einer Mischung von Proteinen, mit den oben beschriebenen Mikroreaktoren (Figuren 1 oder 2) ist in Tabelle 1 zur Verfügung gestellt. Die Tabelle , die die einzigartigen Peptidsequenzen umfasst, die ein bestimmtes Protein zu identifizieren, wobei der Quer Korrelation Score (Xcorr) (dh eine Punktzahl, die für die entsprechenden Tandem - Massenspektrum der Qualität der experimentellen zu theoretischen Spiel charakterisiert), die Anzahl der verpassten cleavages das Peptid Ladezustand (z), und die Masse / Ladungs ( m / z) der protonierten Peptiden. Auf Protein-Ebene stellt die Tabelle die UniProt Protein-ID, die Beschreibung (Name) des Proteins, das Protein-Score und die Protein-Abdeckung. Alle Proteine wurden identifiziert durch mehrere Peptide nach einer proteolytischen Abbau für 90 Sekunden durchgeführt.
Die Zeit, die für dieElution aller Peptide war abhängig von der Länge der Kapillare, die Übertragung der angesäuerten organischen Lösung bei 300 nl / min, einer Strömungsrate kompatibel mit nano-ESI optimalen Betrieb ausgeliefert. In-Kapillar-Vermischung der wässrigen und organischen angesäuerten Lösungen führte in den frühen Elution von einigen Peptiden, aber die große Mehrheit über mehrere Minuten nur in der organischen Lösung eluiert. Ein Massenspektrum der Co-Elution von mehreren Peptiden Vertreter der fünf Proteine, erzeugt mit dem kapillaren Mikroreaktor anzeigt, ist in 3 bereitgestellt.
Tabelle 1. Liste der tryptischen Peptide erzeugt durch den proteolytischen Abbau von fünf Proteinen unter Verwendung der Kapillarreaktor und O / N Verdauung Protokolle. Nur einzigartige Sequenzen, mit dem höchsten Xcorr, werden angezeigt. Bitte hier klicken , um diese Datei herunterzuladen.

Abbildung 1. Kapillarreaktor. (A) Versuchsaufbau zur Herstellung des Mikroreaktors. (B) Kapillarreaktor in der Ionenquelle MS positioniert. Der Mikroreaktor wird manuell mit C18-gebundene Silica - Partikel und auf einem XYZ-Bühne geladen, die in der ESI-MS Quelle richtige Positionierung erleichtert. Bitte klicken Sie hier , um eine größere Version dieser Figur zu sehen.
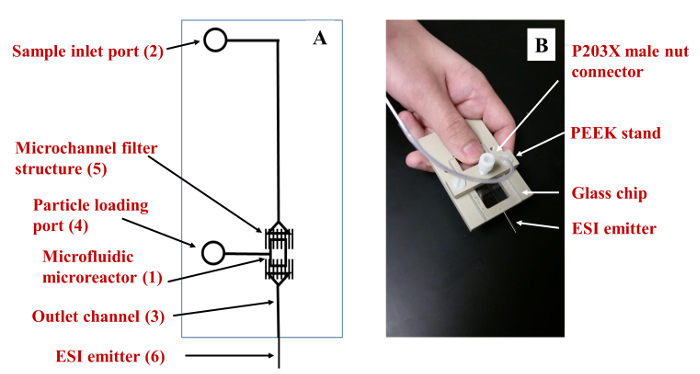
Abbildung 2. Mikrofluidik Mikroreaktor. (A) Schematische Darstellung des mikrofluidischen Reaktors. (B) Mikrofluidik - Reaktor in einem PEEK Ständer befestigt ist . Die mikrofluidischen Reaktor einnd Transferleitungen sind in einem Glassubstrat hergestellt , das in einem hausgemachten polymeren PEEK stehen für die weitere Positionierung in der MS - Quelle mit der XYZ - Bühne gesichert werden kann. Bitte hier klicken , um eine größere Version dieser Figur zu sehen.

Abbildung 3. Massenspektrum umfasst tryptischen Peptide aus dem Proteingemisch zu Proteolyse im Mikroreaktor ausgesetzt erzeugt. Die intensivsten tryptischen Peptidionen werden mit der Sequenz der Aminosäuren markiert und die entsprechenden Protein - Kennung. Bitte hier klicken , um eine größere Version zu sehen diese Figur.
Diskussion
Der Mikroreaktor in dieser Arbeit beschriebenen bietet eine einfach zu implementierende Versuchsaufbau zur Durchführung einer enzymatischen Verdauung der Proteine MS-Analyse und Identifizierung in weniger als 30 min zu ermöglichen. Die klaren Vorteile dieses Systems im Vergleich zu herkömmlichen Ansätzen, sind Einfachheit, Geschwindigkeit, niedrige Reagenzienverbrauch und niedrige Kosten. Insbesondere gibt es keine Notwendigkeit für teure immobilisiertem Trypsin Perlen und Patronen. Die Herstellung der Kapillarreaktor ist einfach (1A), und kann innerhalb von Minuten von der Standardversorgung erreicht werden, die üblicherweise in einer Chromatographie - Labor gefunden. Während die Umkehrphasen - C18 - Teilchen mit einer hohen organischen Gehalt Lösungsmittel (CH 3 CN oder CH 3 OH) für eine vollständige Entfernung von adsorbierten Proteinen oder Peptiden, und der Mikroreaktor kann wiederverwendet werden gespült werden, die einfach und kostengünstiger Herstellungsprozess lädt zur Herstellung von Einweg-Geräte für den Einmalgebrauch applictionen. Die kapillare Mikroreaktor kann in einem selbstgebauten ESI - Quelle montiert werden, wie in 1B gezeigt ist , oder kann in einem handelsüblichen Ionenquelle eingesetzt werden. Während das Teilchenbett zur Probenaufnahme und Verdauung braucht nicht länger zu sein als ~ 1-2 mm, gerade genug, um ausreichend Material für die optimale Detektion von MS zu erfassen, kann die Länge der Kapillare selbst die Größe eines bestimmten passen eingestellt werden Ionenquelle.
Für Labors , die Fähigkeiten zur Herstellung mikrofluidischer Vorrichtungen haben, ein einfaches Design (2A) , die in einen Ständer zum Erleichtern Schnittstelle zu MS - Detektion (2B) befestigt werden kann , ist vorgesehen. Die Abmessungen der Mikroreaktor und Übertragungskanäle können auf die Anforderungen einer bestimmten Anwendung eingestellt werden, und die Vorrichtung kann in einem einzigen oder gemultiplexten Format entwickelt werden. Für die meisten kommerziellen Massenspektrometern würde jedoch die Ionenquelle Modifikationen benötigen th zu ermöglichene Anordnung der Vorrichtung in der Quelle. Die Photomaske Zeichnung für die Chipherstellung wurde mit AutoCAD-Software ausgeführt und die Photomaske von HTA Photomask hergestellt. Die Herstellung der Mikrochips wurde gemäß Protokollen früher beschrieben durchgeführt: 17,18 Ausrichtung des Substrats mit der Photomaske, Belichtung mit UV - Licht (360 nm), das Entfernen des bestrahlten Photoresists und der darunterliegenden Chromschicht, nasschemisches Ätzen von Kanälen mit Puffer Oxidätzung, Entfernen der restlichen Chromschicht, Bohren der Zugangsöffnungen, Reinigen, Hydrolyse der Mikrochipoberfläche (NH 4 OH + H 2 O 2) und thermisches Verbinden des Substrats mit der Deckplatte durch allmähliches Erhitzen auf 550 ºC. Sowohl Substrat und Deckplatte wurden geätzt, eine für tiefe Kanäle für das Probenhandling (~ 20-50 & mgr; m), und die andere für flache Mikrokanalfilterelemente (1,5-2 & mgr; m tief). 16
Die Ergebnisse erzeugt mit dem oben beschriebenen microreactor sind vergleichbar mit den Ergebnissen aus O / N, 19 herkömmliche Verdau Protokolle , die Substrat verwenden: Enzymverhältnisse von (50-100): 1, gefolgt von einem Peptid Infusionsexperiment mit MS - Detektion (300 nl / min, gelöst in H Peptide 2 O / CH 3 CN (50:50 v / v) angesäuert mit CH 3 COOH, 0,1% v / v). Sowohl Mikroreaktor und konventionelle Protokolle aktiviert die Identifizierung aller Proteine durch mehrere einzigartige Peptide (Tabelle 1). Typischerweise waren eine etwas größere Anzahl von einzigartigen Peptiden pro Protein beobachtbaren mit dem Mikroreaktor als mit dem herkömmlichen Aufbau. Dies war ein Ergebnis einer unvollständigen enzymatischen Spaltung an bestimmten Stellen. Ein paar zusätzliche Minuten von proteolytischen Abbau reduziert oder dieses Ergebnis eliminiert. Auch einige enzymatische Peptide mit den Mikroreaktor erzeugten unterschieden sich von den in Lösung erzeugt diejenigen, aufgrund der Tatsache, dass für die Proteine an den C18-Teilchen adsorbiert verschiedenen Stellen an das Enzym t ausgesetzt warenhan in homogenen Lösungen. 20 Die Xcorr Noten zeigen, dass war aber von hoher Qualität die Qualität der Tandem - Massenspektren mit dem Mikroreaktor erzeugt wird , und dass eine ausreichende Abdeckung Proteinsequenz (11-75%) ist für eine eindeutige Proteinidentifikationen erreichbar .
Die Technik, wie beschrieben, auf die Analyse von ziemlich einfachen Proteingemische beschränkt, die bei den meisten ~ 25-50 Peptide erzeugen, die durch einfache Infusionsexperimenten untersucht werden kann, und dass erfordern keine Flüssigkeit chromatographischen Trennung vor der MS-Analyse. Entscheidend für den Erfolg ist die Verwendung von frisch aufgetauten und Trypsin Lösungen hergestellt, um nicht zu verringern oder die Aktivität des proteolytischen Enzyms auf der operativen pH des Mikroreaktors (dh pH ~ 8) verlieren. Darüber hinaus muss ein ausgewogenes Verhältnis zwischen der optimalen Strömungsgeschwindigkeiten für Elektrospray-Ionisation (150-300 nl / min) und die maximale Durchflussraten gefunden werden, die durch den Versuchsaufbau toleriert werden kann, und dass ermöglichenschnelle Peptid Elution von der Mikroreaktor (2-3 & mgr; l / min). Höher als optimale ESI Flussraten führen zu Empfindlichkeitsverluste und schlechte Nachweisgrenzen. Infolgedessen sollte die Länge der Übertragungs Kapillaren so kurz wie möglich gehalten werden, um die notwendige Zeit für die Elution von Peptiden aus dem Mikroreaktor zu reduzieren, wenn bei ≤300 Nl / min betrieben wird. Alle Komponenten, die für den Versuchsaufbau verwendet wurden, können durch Komponenten anderer Hersteller ersetzt werden, die ähnliche Funktionen ausführen. Wenn die Abmessungseigenschaften dieser Komponenten unterscheiden (Länge, Durchmesser, Volumen), um die Optimierung des Elutionsmittels Flußraten, Probenkonzentration, die Zeit für die Ausführung bestimmter Schritte und der ESI-Spannung um ähnliche Ergebnisse zu erhalten, kann erforderlich sein.
Ein einzigartiger Vorteil durch die mikrofluidische Setup aktiviert ist die Fähigkeit , auf dem Chip ein Pumpsystem weiter zu integrieren, beispielsweise eine elektroosmotische Strömung angetriebene Pumpe, 21,22 zum Aktivieren des Stand-aleinen Betrieb der Plattform und die Integration eines zusätzlichen Trennungsschritt. Die Fähigkeit, On-Chip-Trennungen der Peptide durch proteolytischen Verdau erzeugt auszuführen in verbesserten Nachweisgrenzen führt, und wird die Analyse komplexer Proteingemische aus Zellextrakten erleichtern. Dies wird die Integration der Technik in Workflows ermöglichen die Verwendung von mikrostrukturierten Plattformen und High-Speed - MS - Detektion für biomedizinische Anwendungen zu machen. 23
Offenlegungen
The authors declare no competing financial interests.
Danksagungen
This work was supported by NSF/DBI-1255991 grant to IML.
Materialien
| Name | Company | Catalog Number | Comments |
| Ion trap ESI-MS | Thermo Electron | LTQ | The LTQ mass spectrometer is used for acquiring tandem MS data |
| XYZ stage | Newport | Multiple parts | The home-built XYZ stage is used to adapt the commercial LTQ nano-ESI source to receive input from various sample delivery systems |
| Stereo microscope | Edmund optics | G81-278 | The microscope is used to observe the microreactor packing process |
| Analytical balance/Metler | VWR | 46600-204 | The balance is used to weigh the protein samples |
| Ultrasonic bath/Branson | VWR | 33995-540 | The sonic bath is used for mixing/homogenizing the samples and dispersing the C18 particle slurry |
| Syringe pump 22 | Harvard Apparatus | 552222 | The micropump is used for loading, rinsing and eluting the sample and the enzyme on and from the packed capillary microreactor |
| Milli-Q ultrapure water system | EMD Millipore | ZD5311595 | The MilliQ water system is used to prepare purified DI water |
| Pipettor/Eppendorf (1,000 µl) | VWR | 53513-410 | The pipettor is used to measure small volumes of sample solutions |
| Pipettor/Eppendorf (100 µl) | VWR | 53513-406 | The pipettor is used to measure small volumes of sample solutions |
| Pipettor/Eppendorf (10 µl) | VWR | 53513-402 | The pipettor is used to measure small volumes of sample solutions |
| Fused silica capillary (100 µm ID x 360 µm OD) | Polymicro Technologies | TSP100375 | This capillary is used for the fabrication of the microreactor |
| Fused silica capillary (20 µm ID x 100 µm OD) | Polymicro Technologies | TSP020090 | This capillary is used for the fabrication of the ESI emitter |
| Fused silica capillary (50 µm ID x 360 µm OD) | Polymicro Technologies | TSP050375 | This capillary is used to transfer the samples and the eluent from the syringe pump to the capillary microreactor |
| Glass capillary cleaver | Supelco | 23740-U | This is a tool for cutting fused silica capillaries at the desired length |
| Glue | Eclectic Products | E6000 Craft | This glue is used for securing the ESI emitter into the capillary microreactor or the microfluidic chip |
| Epoxy glue | Epo-Tek | 353NDT | This glue is used to seal the microfluidic inlet hole through which the C18 particles are loaded |
| Reversed phase C18 particles (5 µm) | Agilent Technologies | Zorbax 300SB-C18 | These are C18 particles on which the proteins are adsorbed; the particles were extracted from a 4 mm x 20 cm C18 LC column from Agilent |
| Syringe/glass (250 µl) | Hamilton | 81130-1725RN | The glass syringes are used to load the C18 particle slurry in the capillary microreactor and to deliver the sample and eluents to the microreactor |
| Internal reducing PEEK Union (1/16” to 1/32”) | Valco | ZRU1.5FPK | This union is used to connect the 250 µl syringe to the microreactor for loading the 5 µm particle slurry |
| Stainless steel union (1/16”) | Valco | ZU1XC | The stainless steel union is used to connect the glass syringe needle to the infusion capillary |
| Microvolume PEEK Tee connector (1/32”) | Valco | MT.5XCPK | The Peek tee is used to connect the sample transfer capillary to the capillary microreactor; on its side arm, it enables the insertion of the Pt wire |
| Tee connector (light weight) | Valco | C-NTXFPK | This Tee connector is used to apply ESI voltage to the microfluidic chip through the sample transfer line |
| Pt wire (0.404 mm) | VWR | 66260-126 | The Pt wire provides electrical connection for ESI generation and is connected to the mass spectrometer ESI power supply |
| PTFE tubing (1/16” OD) | Valco | TTF115-10FT | The Teflon tubing is used to enable an air-tight connection between the syringe needle and the stainless steel union |
| PEEK tubing (0.015” ID x 1/16” OD) | Upchurch Scientific | 1565 | The Peek tubing is used as a sleeve to enable an air-tight connection between the stainless steel union and the 50 µm ID transfer capillary |
| PEEK tubing (0.015” ID x 1/32” OD) | Valco | TPK.515-25 | The Peek tubing is used as a sleeve to enable a leak-free connection between the fused silica capillaries and the Peek Tee |
| Clean-cut polymer tubing cutter | Valco | JR-797 | This cutter is used to pre-cut the 1/16” and 1/32’ Peek polymer tubing that is used as sleeve for leak-free connections in pieces of ~4-5 cm in length |
| Amber vial (2 ml) | Agilent | HP-5183-2069 | The vials are used to prepare sample solutions and the C18 particle slurry |
| Amber vial (4 ml) | VWR | 66011-948 | The vials are used to prepare sample solutions |
| Polypropylene tube (15 ml) | Fisher | 12-565-286D | The vials are used to prepare buffer solutions |
| Cylinder (100 ml) | VWR | 24710-463 | The cylinder is used to measure volumes of solvent |
| Cylinder (10 ml) | VWR | 24710-441 | The cylinder is used to measure volumes of solvent |
| Pipette tips (1,000 µl) | VWR | 83007-386 | The pipette tips are used to measure small volumes of sample solutions |
| Pipette tips (100 µl) | VWR | 53503-781 | The pipette tips are used to measure small volumes of sample solutions |
| Pipette tips (10 µl) | VWR | 53511-681 | The pipette tips are used to measure small volumes of sample solutions |
| Glass substrates | Nanofilm | B270 white crown, 3” x 3” | These are glass substrates for microchip fabrication |
| Male nut fitting (1/16”) | Upchurch | P203X | This fitting is used for connecting transfer capillaries to the microfluidic chip |
| Nanoport assembly | Upchurch | N-122H | This fitting is used for connecting transfer capillaries to the microfluidic chip |
| Protein standards | Sigma | Multiple # | |
| Acetonitrile, HPLC grade | Fisher | A955 | |
| Methanol, HPLC grade | Fisher | A452 | |
| Isopropanol, HPLC grade | Sigma | 650447 | |
| Trifluoroacetic acid | Sigma | 302031 | |
| Ammonium bicarbonate | Aldrich | A6141 | |
| Trypsin, sequencing grade | Promega | V5111 |
Referenzen
- Petersen, D. H. Microfluidic Bioreactors. Encyclopedia of Microfluidics and Nanofluidics. , Springer Science+Business Media. New York. (2014).
- Matosevic, S., Szita, N., Baganz, F. Fundamentals and applications of immobilized microfluidic enzymatic reactors. J. Chem. Technol. Biotechnol. 86 (3), 325-334 (2011).
- Liu, Y., Liu, B., Yang, P., Girault, H. H. Microfluidic enzymatic reactors for proteome research. Anal. Bioanal. Chem. 390 (1), 227-229 (2008).
- Wu, H., Zhai, J., Tian, Y., Lu, H., Wang, X., Jia, W., Liu, B., Yang, P., Xu, Y., Wang, H. Microfluidic enzymatic-reactors for peptide mapping: strategy, characterization, and performance. LabChip. 4 (6), 588-597 (2004).
- Jin, L. J., Ferrance, J., Sanders, J. C., Landers, J. P. A microchip-based proteolytic digestion system driven by electroosmotic pumping. LabChip. 3 (1), 11-18 (2003).
- Asanomi, Y., Yamaguchi, H., Miyazaki, M., Maeda, H. Enzyme-immobilized microfluidic process reactors. Molecules. 7 (16), 6041-6059 (2011).
- Aravamudhan, S., Joseph, P. J., Kuklenyik, Z., Boyer, A. E., Barr, J. R. Integrated microfluidic enzyme reactor mass spectrometry platform for detection of anthrax lethal factor. 31.st. Annual International Conference of the IEEE EMBS, , 1071-1074 (2009).
- Liu, X., Lo, R. C., Gomez, F. A. Fabrication of a microfluidic enzyme reactor utilizing magnetic beads. Electrophoresis. 30 (12), 2129-2133 (2009).
- Liu, Y., Xue, Y., Ji, J., Chen, X., Kong, J., Yang, P., Girault, H. H., Liu, B. Gold nanoparticle assembly microfluidic reactor for efficient on-line proteolysis. Mol. Cell. Proteomics. 6 (8), 1428-1436 (2007).
- Wu, H., Tian, Y., Liu, B., Lu, H., Wang, X., Zhai, J., Jin, H., Yang, P., Xu, Y., Wang, H. Titania and alumina sol-gel-derived microfluidics enzymatic-reactors for peptide mapping: design, characterization, and performance. J. Proteome Res. 3 (6), 1201-1209 (2004).
- Ji, J., Zhang, Y., Zhou, X., Kong, J., Tang, Y., Liu, B. Enhanced protein digestion through the confinement of nanozeolite-assembled microchip reactors. Anal. Chem. 80 (7), 2457-2463 (2008).
- Hustoft, H. K., Brandtzaeg, O. K., Rogeberg, M., Misaghian, D., Torsetnes, S. B., Greibrokk, T., Reubsaet, L., Wilson, S. R., Lundanes, E. Integrated enzyme reactor and high resolving chromatography in "sub-chip" dimensions for sensitive protein mass spectrometry. Scientific Reports. 3 (3511), 1-7 (2013).
- Pramanik, B. N., Mirza, U. A., Ing, Y. H., Liu, Y. H., Bartner, P. L., Weber, P. C., Bose, A. K. Microwave-enhanced enzyme reaction for protein mapping by mass spectrometry: A new approach to protein digestion in minutes. Protein Sci. 11 (11), 2676-2687 (2002).
- Olszowy, P. P., Burns, A., Ciborowski, P. S. Pressure-assisted sample preparation for proteomic analysis. Anal. Biochem. 438 (1), 67-72 (2013).
- Lord, G. A., Gordon, D. B., Myers, P., King, B. W. Tapers and restrictors for capillary electrochromatography and capillary electrochromatography-mass spectrometry. J. Chromatogr. A. 768, 9-16 (1997).
- Lazar, I. M., Kabulski, J. L. Microfluidic LC Device with Orthogonal Sample Extraction for On-Chip MALDI-MS Detection. Lab Chip. 13 (11), 2055-2065 (2013).
- Harrison, D. J., Manz, A., Fan, Z. H., Ludi, H., Widmer, H. M. Capillary electrophoresis and sample injection systems on a planar glass chip. Anal. Chem. 64 (17), 1926-1932 (1992).
- Jacobson, S. C., Hergenroder, R., Koutny, L. B., Warmack, R. J., Ramsey, J. M. Effects of Injection Schemes and Column Geometry on the Performance of Microchip Electrophoresis Devices. Anal. Chem. 66 (7), 1107-1113 (1994).
- Armenta, J. M., Perez, M. J., Yang, X., Shapiro, D., Reed, D., Tuli, L., Finkielstein, C. V., Lazar, I. M. Fast Proteomic Protocol for Biomarker Fingerprinting in Cancerous Cells. J. Chromatogr. A. 1217, 2862-2870 (2010).
- Doucette, A., Craft, D., Li, L. Mass Spectrometric Study of the Effects of Hydrophobic Surface Chemistry and Morphology on the Digestion of Surface-Bound Proteins. J. Am. Soc. Mass Spectrom. 14, 203-214 (2003).
- Lazar, I. M., Trisiripisal, P., Sarvaiya, H. A. Microfluidic Liquid Chromatography System for Proteomic Applications and Biomarker Screening. Anal. Chem. 78 (15), 5513-5524 (2006).
- Lazar, I. M., Karger, B. L. Multiple Open-Channel Electroosmotic Pumping System for Microfluidic Sample Handling,". Anal. Chem. 74 (24), 6259-6268 (2002).
- Lazar, I. M., Rockwood, A. L., Lee, E. D., Sin, J. C. H., Lee, M. L. High-speed TOFMS Detection for Capillary Electrophoresis. Anal. Chem. 71 (13), 2578-2581 (1999).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten