Method Article
Graphene Coatings for Biomedical Implants
In diesem Artikel
Zusammenfassung
Graphene bietet Potenzial als Beschichtungsmaterial für biomedizinische Implantate. In dieser Studie zeigen wir, ein Verfahren zur Beschichtung Nitinollegierungen mit Nanometer dicken Schichten von Graphen und bestimmen, wie Graphen kann Implantat Reaktion beeinflussen.
Zusammenfassung
Atomar glatten Graphen als Oberflächenbeschichtung hat Potential Implantat zu verbessern. Dies zeigt ein Verfahren zur Beschichtung Nitinollegierungen mit Nanometer dicke Schichten aus Graphen für Anwendungen als Stentmaterial. Graphen wurde auf Kupfer Substrate durch chemische Dampfabscheidung gezüchtet und dann auf Nitinolsubstraten übertragen. Um zu verstehen, wie die Graphen Beschichtung könnte biologische Reaktion zu ändern, wurde die Lebensfähigkeit der Zellen von Ratten-Endothelzellen und Rattenaorta glatten Muskelzellen untersucht. Außerdem wurde die Wirkung von Graphen-Beschichtungen auf Zelladhäsion und Morphologie mit fluoreszierendem konfokale Mikroskopie untersucht. Zellen wurden für Actin und Kerne angefärbt, und es waren deutliche Unterschiede zwischen unberührten Nitinol Proben verglichen, um Graphen-beschichteten Proben. Insgesamt Aktin Expression von Rattenaorta glatten Muskelzellen gefunden wurde mittels Western Blot. Proteinadsorption Eigenschaften, ein Indikator für potenzielle Thrombogenität, were für Serumalbumin und Fibrinogen mit Gelelektrophorese bestimmt. Darüber hinaus wurde die Übertragung von Ladung von Fibrinogen an das Substrat hervorgerufen, die mittels Raman-Spektroskopie. Es wurde festgestellt, dass Graphen Beschichtung auf Nitinolsubstraten die funktionalen Anforderungen für eine Stent-Material erfüllt und verbessert die biologische Reaktion im Vergleich zu unbeschichteten Nitinol. So ist Graphen-beschichteten Nitinol ein brauchbarer Kandidat für einen Stent Material.
Einleitung
Die letzten drei Jahrzehnte haben Entdeckung neuartiger Materialien-basierten Therapien und Geräte für die Erkrankung von Medikamenten und diagnostischen erlebt. Neuartige Legierungen wie Nitinol (NiTi) und Edelstahl sind oft in der biomedizinischen Implantate Herstellung aufgrund ihrer hervorragenden mechanischen Eigenschaften verwendet. 1-3 jedoch zahlreiche Herausforderungen durch exogene Material Zytotoxizität bleiben, Bio-und Hämokompatibilität. Die Natur dieser metallischen Legierungen führt zu schlechter Bioverfügbarkeit und Hämokompatibilität durch Metall Auslaugen, mangelnde Zell-Adhäsion, Proliferation und Thrombose, wenn es in Kontakt mit strömenden Blutes (wie Katheter, Transplantaten Blutgefäß, vaskulären Stents, künstliche Herzklappen etc.). 1, 4, 5 Das Zusammenspiel von Proteinen oder lebenden Zellen mit der Oberfläche des Implantats kann zu einer starken Immunantwort und der anschließenden Kaskade von biochemischen Reaktionen führen kann negative Auswirkungen auf die Gerätefunktionen. Daher wird pertinENT, um die Kontrolle über die Wechselwirkungen zwischen biomedizinischen Implantaten und Umgebung biologischen Umgebung zu erreichen. Oberflächenmodifizierung wird oft verwendet, um Reduktion oder Prävention der nachteiligen physiologischen Reaktion, die aus dem Implantatmaterial. Eine ideale Oberflächenbeschichtung soll hohe Haftfestigkeit, chemische Trägheit hohe Glätte und gute Hämo-und Bioverträglichkeit aufweisen. Bisher wurden zahlreiche Materialien einschließlich diamantartigem Kohlenstoff (DLC), SiC, TiN, TiO 2 und viele Polymermaterialien als biokompatiblen Implantats Oberflächenbeschichtungen getestet. 1, 6-23 Jedoch sind diese Materialien noch nicht alle treffen die funktionalen Kriterien für ein geeignetes Implantat Oberflächenbeschichtung.
Die Entdeckung-dicke Schicht von sp 2 Kohlenstoff als Graphen bekannt, hat Türen für die Entwicklung neuartiger Multifunktionsmaterialien geöffnet. Graphene wird erwartet, dass ein idealer Kandidat für Implantat Oberflächenbeschichtung sein, da esist chemisch inert, atomar glatt und sehr langlebig. In diesem Brief, untersuchen wir die Lebensfähigkeit von Graphen als Oberflächenbeschichtung für biomedizinische Implantate. Unsere Untersuchungen zeigen, dass die Graphen beschichteten Nitinol (NiTi-Gr) alle funktionellen Kriterien erfüllt, und unterstützt zusätzlich ausgezeichnete glatte Muskelzellen und Endothelzellen Zellwachstum führt zu besseren Zellproliferation. Wir finden auch, dass die Serum-Albumin Adsorption auf Gr-NiTi höher als Fibrinogen ist. Wichtig ist, dass (i) unsere detaillierte spektroskopische Messungen bestätigten das Fehlen von Ladungstransfer zwischen Graphen und Fibrinogen darauf hindeutet, dass Graphen Beschichtung hemmt Thrombozytenaktivierung durch Implantate, (ii) Graphen Beschichtungen zeigen keine signifikante in vitro Toxizität für Endothelzellen und glatten Muskelzellen Zelllinien bestätigt ihrer Biokompatibilität, und (iii) Graphen Beschichtungen sind chemisch inert, robust und undurchlässigen im fließenden Blut Umwelt. Diese Hämo-und biokompatiblen Eigenschaften, zusammen mit hoher strength, chemische Beständigkeit und Langlebigkeit, machen Graphen Beschichtungen als ideale Oberflächenbeschichtung.
Protokoll
Ein. Graphen-Beschichtung von NiTi
- Die Graphen-Proben in dieser Studie verwendet wurden auf Kupfer (Cu)-Substraten unter Verwendung des chemischen Dampfabscheidungstechnik aufgewachsen, und anschließend zu 4,5 mm 2 NiTi Substrate übertragen.
- Cu-Folien (1 cm x 1 cm) wurden in einer 1 in. Quarzrohrofen vorgelegt und auf 1000 ° C in Gegenwart von 50 sccm H 2 und 450 sccm Ar.
- Weiter, Methan (1 und 4 sccm) wurde in den Ofen in verschiedenen Strömungsgeschwindigkeiten für 20-30 min eingeführt. Die Proben wurden schließlich auf Raumtemperatur unter strömendem H 2, Ar und CH 4 gekühlt.
- Als nächstes wurden die Cu-Folien Schleuderbeschichtung mit PMMA (verdünnt mit 4% Anisol) bei 4.000 Umdrehungen pro Minute durch eine Wärmebehandlung für 5 min bei 150 ° C, gefolgt Graphen an PMMA-Schicht wurde durch Ätzen des Cu-Folie mit TRANSENE Inc., CE-100 Ätzmittel, und anschließendes Spülen in 10% HCl und deionisiertem Wasser für 10 min erhalten.
- Die sBeispiele wurden auf NiTi Substrate (4,5 mm 2) überführt und getempert bei 450 ° C in Ar (300 sccm) und H 2 (700 sccm) für 2 Stunden, um die PMMA zu entfernen. Schließlich wurden die Substrate mit Aceton gewaschen, um das restliche PMMA löst, um den Gr-NiTi Probe zu erhalten. Ein XY Dilor Dreifach Gittermonochromator wurde für die Mikro-Raman-Charakterisierung (100X mit Objektiv) aller Gr-NiTisamples mit 514,5 nm Anregung von einem Ar +-Ionen-Laser verwendet.
2. In vitro-Toxizität von Gr-NiTi
Ratte-Endothelzellen (Cell Anwendung Inc.) wurden auf einem 8 Kammern gelatinebeschichteten Schieber kultiviert. Für die Prüfung des Zellwachstums, makellos und Gr-NiTisubstrates wurden in Brunnen ohne Gelatineschicht platziert. Rasterelektronenmikroskopie-Bilder wurden mit einem Hitachi S-4800 SEM. Zusätzlich wurden Rattenaorta Glattmuskelzellen auch in Cellbind gezüchtet 96-Well-Platten als Kontrollgruppe (Corning) in Dulbecco-modifiziertes Eagle Medium (ATCC).
- Zum Testen Zelllebensfähigkeit wurden Zellen (sowohl Endothel-und glatten Muskelzellen) bei 10 5 Zellen / Vertiefung in Vertiefungen, die unberührten NiTi, 1 sccm oder 4 sccm Gr-NiTi Substraten, wobei die angegebenen sccm Methan entspricht der Strömung in der verwendete ausgesät CVD-Wachstum von Graphen. Die Zellen wurden für den gewünschten Zeitraum in einem Brutschrank bei 37 ° C und 5% CO 2, den Austausch von Medien jeder andere Tag.
- Am Ende Zeitpunkt wurde das Medium entfernt und frisches Medium, das 0,5 mg / ml Thiazolyl Blau tetrazoliumbromid (MTT oder von Sigma bezogen) wurde zu jeder Vertiefung zugegeben. Die Zellen wurden dann für weitere 3 Stunden inkubiert. Für den MTS-Assay wurde das Medium in der letzten Zeitpunkt entfernt und durch 120 ul MTS Arbeitslösung (Cell 96 Grad wässrigen, Promega) und inkubiert für drei Stunden.
- Weiter wurde das Medium vorsichtig entfernt und mit 100 ml Dimethylsulfoxid (Sigma) wurde zu jeder Vertiefung zugegeben. Nach alloFlügel 10 min für die MTT-Kristalle aufzulösen, wurde die Lösung in ein anderes Well-Platte transferiert. Für den MTS-Assay wurde kein Dimethylsulfoxid in die Vertiefungen gegeben. Nun Inhalte wurden auf eine neue Platte bewegt.
- Absorption wurde bei 490 nm abgelesen, und die prozentuale Lebensfähigkeit wurde durch Normalisierung der durchschnittlichen Absorption Extinktion der unberührten NiTi Probe bestimmt. Mindestens fünf Wiederholungen wurden für jede Probe gemacht Typs.
3. Konfokale Mikroskopie Studium der Zellmorphologie
- Für die konfokale Abbildung der Rattenaorta Glattmuskelzellen, wurden Substrate in einer 8-Kammer Schieber (Thermo Scientific) platziert. Die Zellen wurden bei 25.000 Zellen / Kammer ausgesät und 3 Tage bei 37 ° C und 5% CO 2.
- Zellen wurden auf dem Substrat mit 4% Formaldehyd in Phosphat gepuffertem Kochsalz 20 min.
- Permeabilisiert mit 0,1% Triton-X für 1 min.
- Actin wurde mit Alexa Fluor 488 Phalloidin (Lif gefärbte Technologies). 100 ul AlexaFluor 488 Phalloidin bei 200 Einheiten / ml in Methanol wurde auf 1,9 ml Phosphat-gepufferter Kochsalzlösung zugegeben. Zellen wurden mit 250 ul AlexaFluor 488 Phalloidin für 45 min gefärbt und dann zweimal mit phosphatgepufferter Kochsalzlösung.
- Zellkerne wurden mit fluoreszierenden Vectashield Eindeckmedium enthaltenden DAPI (Vector Laboratories) montiert ist. Konfokale Bilder wurden unter Verwendung eines Nikon Konfokale TI. Eine Kammer mit Zellen ohne Substrat ausgesät wurde als Kontrolle verwendet.
4. Proteinadsorptionsstudien
- Substrat Dimensionen wurden mit einer Schieblehre, bevor Sie die Proteinadsorption Experimenten gemessen. Drei Messungen wurden für jede Seite der etwa quadratischen Proben genommen und gemittelt, um die Länge und Breite erhalten.
- Jede Probe, unberührte NiTi, 1sccm und 4sccm Gr-NiTiwere mit 1 mg / ml Albumin in Phosphat gepufferter Kochsalzlösung inkubiert (PBS) oder 1 mg / ml Fibrinogen in PBS bei Raumtemperatur temperatur für 3 Stunden.
- Proben wurden unter gleichen Bedingungen in einem Mikrozentrifugenröhrchen mit 200 ul reduzierenden Probenpuffer versetzt und für 5 min gekocht.
- Proben wurden dann in einem Tris / Glycine / SDS Puffer (Bio-Rad) verdünnt und durch eine 4-15% Tris Polyacrylamid-Elektrophorese-Gel (Bio-Rad) bei 90 V für 100 min.
- Die Gele wurden dann mit SYPRO Red angefärbt. Verdünnen SYPRO Red (Life Technologies) Stammlösung bei 1:5.000 in 7,5 v / v% Essigsäure. Stain Gele für 60 min.
- Bild Gele mit einem Flourchem SP (Alpha Innotech). Fluoreszenzintensität quantifiziert wurde mit ImageJ Software. Fluoreszenzintensität jeder Probe wurde durch die Gesamtfläche des Substrats normalisiert und Fibrinogen-Adsorption wurde Adsorption an Albumin verglichen.
5. Western Blot für die Protein-Expression
- Western-Blot wurde durchgeführt, um insgesamt Aktin in Rattenaorta glatten Muskelzellen zu analysieren. Die Zellen wurden mit 10.000 Zellen / Substrat in einer 96-Gew ausgesätell Platte.
- Die Zellen wurden drei Tage vor dem Entfernen Medium gezüchtet. Gesamtprotein wurde extrahiert mit RIPA-Puffer und ein Standard-BCA-Assay (Lamda) wurde durchgeführt, um Gesamtprotein quantifizieren.
- Proben wurden auf die gleiche Konzentration in RIPA verdünnt und dann in einer reduzierenden Probenpuffer für 5 min gekocht.
- Proteine wurden durch einen 4-15% Tris Polyacrylamidgel über Elektrophorese bei 90 V für 100 min getrennt. Ein Kaleidoskop Proteinstandard (Bio-Rad) wurde verwendet, um Protein-Molekulargewicht zu beurteilen.
- Proteine wurden auf eine PVDF-Membran übertragen und blockiert mit einer 1% fettfreier Trockenmilch (Bio-Rad)-Lösung.
- Insgesamt Aktin wurde mit einem Kaninchen-anti-Ratte Aktin-Antikörper (Sigma) markiert. Eine chemilumineszente BM Kits (Roche) wurde verwendet, um den primären Antikörper erkennt. Membranen wurden unter Verwendung FlourChem SP bildgebenden Geräten und Fluoreszenzintensität wurde mit ImageJ Software. Fluoreszenzintensität wurde durch Vergleich mit der pri normalisiertstine NiTisample.
Ergebnisse

. Abbildung 1 a) CVD gewachsen polykristallinen Graphen auf Cu-Folien imitiert die Metall-Kristallkörner (Maßstab: 10 um). b) Raman-Spektrum von 1 sccm (4 sccm) Graphen zeigt intensive (relativ schwächer) G 'Bande, die Monoschicht (wenige Schicht) Art des so hergestellten Graphen. c) AFM-Bild von Graphen auf NiTi übertragen zeigt eine Rauheit von ~ 5 nm. Maßstab = 500 nm.

Abbildung 2 Konfokale optische Mikroskopie Bilder für auf einem SMCs) Kontrolle Glasobjektträger gezüchtet, b) unberührten NiTi, c) 1 sccm Gr-NiTi und d) 4 sccm Gr-NiTi Substrate (Maßstab. 50 um).
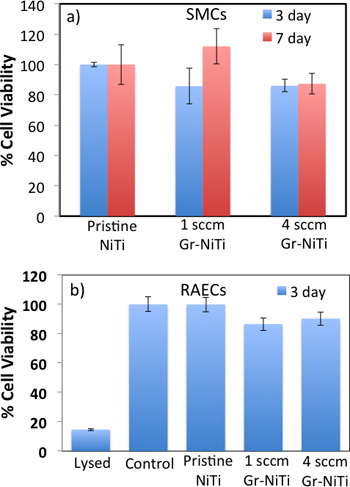
Abbildung 3. A) MTT-Test zeigt, dass Gr-NiTi Substrate (1 und 4 sccm) zeigen keine signifikanten Unterschiede in der Lebensfähigkeit der Zellen SMC relativ unberührten NiTi. B) MTS-Assay zeigt, dass die 3-Tages Lebensfähigkeit von Zellen nicht signifikant RAECs anders als Kontrollen.

Abbildung 4. Rasterelektronenmikroskopie Bilder für RAECs gezüchtet a) unberührten NiTi, b) 1 sccm Gr-NiTi und c) 4 sccm Gr-NiTi Substraten zeigen, dass Graphen Beschichtungen besser sphärischen Zellmorphologie von RAECs führen. Maßstab = 10 um.

Abbildung 5. A) Fibrinogen / Albumin-Verhältnis für unberührte NiTi, Gr-NiTi (1 und 4 sccm Proben). B) Energy Pegeldiagramm für Fibrinogen und elektronische Zustandsdichte für Graphen zeigt die Equilibrierung des Fermi-Niveaus. Ein Elektronentransfer von Fibrinogen zu Gr-NiTi ist nur aus den besetzten elektronischen Zustände des Fibrinogenmolekül in leere elektronischen Zustände von Gr-NiTi mit der gleichen Energie-Level möglich. Sowohl Einzel-und Graphen-Mehrfachschichten sind semi-Metallen bei Raumtemperatur mit niedrigen Zustandsdichte bei EF, die in einem schwachen (im Gegensatz zu bloßen Nitinol Vergleich) Ladungstransfer von Fibrinogen zu Graphen führt.

Abbildung 6. Graphen zeigt keine Änderungen in der G-Bande Linienform oder Frequenz, was die Abwesenheit jeglicher Ladungstransfer von der Plasmaproteine. Die deconvoluted Peaks aus Kurvenanpassung sind in schwarz dargestellt.

Abbildung 7. A) Graphene beschichtete Teil eines Cu Pfennig bis 5% ausgesetzt H 2 O 2 bleibt unverändert, während der abgedeckte Teil verfärbt. B) Keine Änderung in der G-Bande in unserer in situ Raman Studien beobachtet Gr- NiTi eingetaucht in 70% HNO 3 bestätigt die Haltbarkeit von Graphen Beschichtungen. c) Die Ätzzeit für Cu in CE 100 Lösungsmittel verdoppelt wird, wenn Cu mit Graphen (wie in Gr-NiTi), die die Dichtigkeit der Graphen-Schichten beschichtet ist.
Diskussion
Biokompatibilität und Zytotoxizität: Die chemische Gasphasenabscheidung (CVD)-Verfahren ergab polykristallinen Graphenproben die Cu Kristallkörner, wie in 1a gezeigt nachgeahmt. Wir beschäftigten Raman-Spektroskopie, um das Vorhandensein von Monolayer (wenige Schicht) Graphen auf 1 sccm (4 sccm) Proben (siehe Abbildung 1b) bestätigen. Offensichtlich weisen 1 sccm (4 sccm) Proben intensiv (relativ schwächere) G 'band Hinweis auf Monoschicht (wenige Schicht) Graphen. Abbildung 1c zeigt eine Rasterkraftmikroskopie (AFM)-Bild von wenigen Schicht Graphen auf NiTi Substraten. Unsere detaillierte Messungen ergab einen Wert von Oberflächenrauheit R q = 5 nm für übertragene Graphenschichten (Gr-NiTi). Es ist wohlbekannt, dass die nanostrukturierte Oberflächentopographie stark beeinflusst Zellform und Zytoskelett-Baugruppe in Endothelzellen und glatten Muskelzellen. Diese Zelllinien, um den mechanischen Beanspruchungen reagieren durch Veränderung ihrer Lipid-DoppelschichtFlüssigkeit, die sich nachteilig auf Protein-Translokation und den Eintrag von Aktivatoren wie Kalzium in die Zellen. Noch wichtiger ist, kann ein Anstieg in der Zellmembran Spannungsgradient ändern Konformation und Dichte von Rezeptoren auf der Zelloberfläche. Um den Einfluss von Graphen Beschichtung auf den Spannungsgradienten der Zellen zu testen, untersuchten wir die glatten Muskelzellen und Endothelzellen Zellmorphologie Verwendung mikroskopischer Techniken.
Wie in 2, glatten Muskelzellen (SMC) Morphologie auf unberührten NiTi gezeigte nicht kugelförmige. Ferner werden die Zellen dünn verteilt auf eine schwache Adhäsion von SMCs zum unberührten NiTi. Im Gegenteil, sind SMCs dicht und auf der sphärischen Gr-NiTi (beide 1 und 4 sccm) Oberflächen ähnlich der Steuerung. Graphene Beschichtung reduziert Spannungsgradienten in den Zellen durch glattere Oberflächen (ersichtlich aus niedrigen R q-Werte in Abbildung 1c) und damit zu einer besseren Zellmorphologie.Um die Lebensfähigkeit der Zellen und die Proliferation zu messen, führten wir MTT-Test auf den SMCs auf unberührten und Gr-NiTisubstrates bei 3 und 7 Tage gezüchtet Zeitpunkten. In diesem Assay wird der MTT-Farbstoff (gelbe Farbe) in Formazanfarbstoff (violett) durch die aktiven Enzyme Reduktase reduziert und damit die gesund und proliferierenden Zellen (oder des Materials Zytotoxizität) kann durch Durchführen kolorimetrischen Messungen quantifiziert werden. Wie in Abbildung 3a dargestellt, haben wir nicht beobachten, keine wesentlichen Änderungen in der Toxizität für die Gr-NiTi Substrate nach 3 und 7 Tagen. Diese Ergebnisse bestätigen, dass die Graphen Beschichtungen kein Erbrechen übermäßiger Toxizität im Vergleich zum ursprünglichen NiTi Substrate selbst.
Um die Auswirkungen von Graphen Beschichtung bestätigen, führten wir ausführliche Elektronenmikroskopie bildgebende Experimente an Ratten-Endothelzellen (siehe Abbildung 4). Die Zellen auf unberührten NiTi Substrate sind spärlich und längliche, während sie ellipsoid und dense auf der Gr-NiTi Substraten. Solche verbesserten Zellmorphologie und Dichte erwies sich als ähnlich SMCs Bestätigung der Verringerung Spannungsgradienten durch die Graphen Beschichtung versehen ist. Ferner ermittelten wir Graphen Beschichtung Cytotoxizität auf RAEC mit MTS 3 - (4,5-Dimethylthiazol-2-yl) -5 - (3-Carboxymethoxyphenyl) -2 - (4-sulfophenyl)-2H-tetrazolium-Assay. Der Grund für die Verwendung MTS-Assay (statt MTT) liegt in seiner besseren Verträglichkeit mit den RAEC Wachstumsmedien und Bedingungen. Wie in 3b gezeigt, wies unserer MTS-Assay auf der Endothelzelle sehr gute Lebensfähigkeit der Zellen und die Proliferation der Bestätigung keine überschüssige Toxizität von den Graphen Beschichtungen sogar für RAEC. Wichtig ist, zeigten sowohl 1 und 4 sccm Gr-NiTi keine signifikanten Veränderungen in der Zellproliferation was darauf hindeutet, keine Abhängigkeit von der Morphologie der Zellen nach Anzahl der Graphen-Schichten.
Proteinadsorption und Hämokompatibilität: Die Blutgerinnung in der Nähe des Implantatmaterials has war eine der wichtigsten Hürden bei der Implantat-Technologie seit 2003. Wie bereits erwähnt, löst das Implantatmaterial Gerinnungskaskade, wenn es in Kontakt mit Blut kommt. Die Wechselwirkung zwischen biomedizinischen Implantats und Blut beginnt mit der Adsorption von Plasmaproteinen (Albumin, Fibrinogen, etc.) Auf seiner Oberfläche. Anfänglich sind hoch vorkommenden Proteine, wie Serumalbumin, flbrinogen und flbronectin adsorbiert sind aber später durch Faktoren XII und hochmolekulares Kininogen ersetzt. Das Verhältnis von adsorbiertem flbrinogen und Albumin ist entscheidend bei der Festlegung der Hämokompatibilität des Biomaterials. Zuvor ein niedriges Verhältnis von Fibrinogen / Albumin auf einer Oberfläche adsorbiert biomedizinischen Implantats mit niedriger Adhäsion und Thrombusbildung korreliert. 1 Wie in 5a gezeigt, Gr-NiTi weisen niedrige Fibrinogen / Albumin-Verhältnis relativ zu unberührten NiTi hindeutet besser Hämokompatibilität entstehenden von Graphen. Die fib / alb ratio signifikant niedriger war für beide 1 und 4 sccm Gr-NiTi anzeigt, dass die Hämokompatibilität von Graphen-Schicht unabhängig ist.
Es ist bekannt, dass die Elektronenübertragung von Fibrinogen-Moleküls an das Implantat für die Bildung von Fibrin in einem ersten Schritt zur Thrombusbildung Wachstum ist. Wie in 5b gezeigt, weist Fibrinogen Halbleiters wie Dichte von elektronischen Zuständen oder DOS (bezeichnet mit p (E)) mit einem Bandabstand von 1,8 eV. Die Fermi-Niveaus (EF) von Fibrinogen und Gr-NiTi an ihrer Grenzfläche äquilibrieren. Ladungsübertragungsvorrichtung der ein Elektron pro Fibrinogen für die Bildung von Fibrin auf unberührten NiTi und Elektronentransfer vom Fibrinogen-Moleküls in Gr-NiTi erforderlich ist nur von den besetzten elektronischen Zuständen der Fibrinogen-Moleküls in leerer elektronischer Zustände Gr-NiTi zur gleichen Energieniveau. Sowohl Einzel-und Graphen-Mehrfachschichten sind semi-Metallen bei Raumtemperatur mit einem niedrigen p (E) in der Nähe von E F. 24 Somit ist der Ladungsaustausch Strom aus Fibrinogen zu Graphen unbedeutend (im Gegensatz zu bloßen Nitinol Vergleich) aufgrund der niedrigen Werte von p (E). Diese intrinsische Eigenschaft von Graphen Beschichtungen ist entscheidend für die Hemmung jeder Charge-Transfer aus Fibrinogen (und nachfolgende Blutgerinnung).
Wir beschäftigten Mikro-Raman-Spektroskopie, um zu bestätigen, dass die Charge-Transfer-Dynamik zwischen Fibrinogen und Gr-NiTi Tat unbedeutend ist. Das Raman-Spektrum von Graphen weist mehrere scharfen Gesichtszügen aufgrund der Resonanz-Effekte. Insbesondere stellt sich die tangentiale Band (G-Band) von der planaren Schwingung der Kohlenstoffatome und wurde zuvor festgestellt, dass sehr empfindlich auf Ladungstransfer. 25 Der G-Bande um Hochschalten ist bekannt (Rückschaltung), wenn irgendeine Akzeptor (Donor)-Spezies interagiert mit Graphen über Loch (Elektron) übertragen. Wichtig ist, dass die Linienform der G-Bande deviates aus einem symmetrischen Lorentz zu einer asymmetrischen Breit-Wigner-Fano (BWF) Linienform durch Ladungstransfer. 25 Wie erwartet, haben wir nicht beobachten eine Verschiebung der G-Bande von Graphen bei der Adsorption von Fibrinogen Bestätigung der Abwesenheit von Charge-Transfer- zwischen Gr-NiTi und Fibrinogen (Abbildung 6). Eine solche Hemmung des Ladungstransfers und niedrige fib / alb-Verhältnis weisen auf eine gute Hämokompatibilität von Graphen Beschichtungen.
Chemische Beständigkeit von Graphen Coatings: Graphen ist bekannt als Schutzschicht aufgrund seiner einzigartigen physikalisch-chemischen Eigenschaften zu handeln. Seine sp 2 Wabengitter stellt eine natürliche Diffusionsbarriere und verhindert daher Metallion Auslaugen aus dem Implantatmaterial. Vor kurzem hat Graphen als mikroskopische luftdichten Ballons 26 und Schutzschicht für Cu / Ni verwendet worden. 27 Obwohl die Stabilität und Dichtigkeit von Graphen auch in der l dokumentiert werdentur, präsentieren wir unsere Daten in Bezug auf Ätzen einer Cu-Coin in Abbildung 7, um die Nützlichkeit und die Lebensfähigkeit von Graphen als Implantatbeschichtungen wiederholen. Wie in 7a gezeigt, bleibt der Graphen beschichteten Bereich der Münze (~ 95% Cu) vor Oxidation geschützt wird, wenn zu H 2 O 2 ausgesetzt, während die blanke Bereich der Münze wurde bei Kontakt verfärbt mit 5% H 2 O 2 (siehe das vergrößerte Lichtmikroskop in Abbildung 7a).
Um die Haltbarkeit von Graphen Beschichtungen zu testen, ausgesetzt wir Gr-NiTi Substrate bis 70% Salpetersäure, bis die NiTi teilweise geätzt wurde entfernt. Unsere in situ Raman-Spektroskopie von Gr-NiTi in HNO 3 getaucht zeigte keine Veränderung in der D-und G-Bande von Graphen impliziert, dass das Graphen-Beschichtung extrem langlebig (Abbildung 7b). Außerdem fanden wir, dass das Graphen Beschichtung in Gr-NiTi die Ätzrate des darunterliegenden coppe reduziertr wie in 7c gezeigt.
Zusammenfassend bestätigen unsere detaillierte spektroskopische Messungen der Mangel an Ladungstransfer zwischen Graphen und Fibrinogen darauf hindeutet, dass Graphen Beschichtung Thrombozytenaktivierung durch Implantate hemmt. Darüber hinaus müssen Graphen Beschichtungen keine signifikante in vitro Toxizität für Endothelzellen und glatten Muskelzellen Zelllinien Bestätigung ihrer Biokompatibilität. Ferner wurden Graphen Beschichtungen gefunden, chemisch inert, robust und undurchlässigen im fließenden Blut Umwelt. Die Bio-und Hämokompatibilität von Graphen Beschichtungen zusammen mit seiner chemischen Beständigkeit, machen Haltbarkeit und Dichtigkeit Graphen ein einzigartiges Material zur Beschichtung biomedizinische Implantate. Schließlich stellen wir fest, dass wir bei der Übertragung von Graphen-Schichten auf einzelne NiTi Fasern gelungen, mit dem der Graphen-beschichtetes Gewebe hergestellt werden können. Wir haben auch chemisch abgeblätterten Graphenschichten, die direkt aufgeschleudert ont können entwickelto die netzartige Stents. Darüber hinaus zeigen unsere Vorversuche, dass es tatsächlich möglich ist, wachsen direkt auf NiTi-Legierung Graphen.
Offenlegungen
Keine Interessenskonflikte erklärt.
Materialien
| Name | Company | Catalog Number | Comments |
| Reagens | |||
| Dulbeccos Modified Eagle Medium | ATCC | 30-2002 | |
| Thiazolylblau tetrazoliumbromid | Sigma-Aldrich | M2128 | |
| CellTiter 96 Aqueous Eine Lösung Zellproliferationsassay (MTS) | Promega | G3582 | |
| Dimethylsulfoxid | Sigma-Aldrich | D8418 | |
| 36,5% Formaldehyd | Sigma-Aldrich | F8775 | |
| Triton X-100 | Sigma-Aldrich | T8787 | |
| AlexaFluor 488 Phalloidin | Life Technologies | A12379 | |
| Vectashield Eindeckmedium mit DAPIch | Vector Laboratories | H-1200 | |
| Humanserumalbumin | Sigma-Aldrich | A9511 | |
| Humanes Fibrinogen | |||
| Tris / Glycin / SDS | Bio-Rad | 161-0732 | |
| Ready Gel Tris-HCl Gel | Bio-Rad | 161-1158 | |
| Essigsäure | Sigma-Aldrich | 45726 | |
| SYPRO Red | Life Technologies | S-6653 | |
| Protein Low BCA-Assay | Lamda Biotech | G1003 | |
| Precision Plus Protein Kaleidoscope Norm | Bio-Rad | 161-0375 | |
| Immun-Blot PVDF-Membran | Bio-Rad | 162-0177 | |
| Blot Grade Blocker fettfreie Trockenmilch | Bio-Rad | 170-6404XTU | |
| Anti-Aktin-Antikörper in Kaninchen produziert | Sigma-Aldrich | A2066 | |
| BM Chemilumineszenz Western Blot Kit (Maus / Kaninchen) | Roche Applied Science | 11520709001 | |
| RIPA Puffer | Sigma-Aldrich | R0278 | |
| NiTi (51% Ni, 49% Ti) | Alfa-Aesar | 44953 | |
| Ausrüstung | |||
| Horiba JobinYvon | Raman-Spektrometer | Dilor XY 98 | |
| Nikon | Konfokalmikroskop | Eclipse-TI-Mikroskop | |
| Thermoscientific | Plattenlesegerät | ||
| Bio-Rad | Stromversorgung | 164-5050 | PowerPac grundlegende Versorgung |
| Bio-Rad | Elektrophoresezelle | 165-8004 | Mini-PROTEAN Tetra Zelle |
| Bio-Rad | Gelhalterung Kassette | 170-3931 | Mini-Kassette Gelhalterung |
Referenzen
- Roy, R. K., Lee, K. -R. Biomedical applications of diamond-like carbon coatings: A review. Journal of Biomedical Materials Research Part B-Applied Biomaterials. 83 B (1), 72-84 (2007).
- Shah, A. K., Sinha, R. K., Hickok, N. J., Tuan, R. S. High-resolution morphometric analysis of human osteoblastic cell adhesion on clinically relevant orthopedic alloys. Bone. 24 (5), 499-506 (1999).
- Huang, N., Yang, P., Leng, Y. X., Chen, J. Y., Sun, H., Wang, J., Wang, G. J., Ding, P. D., Xi, T. F., Leng, Y. Hemocompatibility of titanium oxide films. Biomaterials. 24 (13), 2177-2187 (2003).
- Gutensohn, K., Beythien, C., Bau, J., Fenner, T., Grewe, P., Koester, R., Padmanaban, K., Kuehnl, P. In vitro analyses of diamond-like carbon coated stents: Reduction of metal ion release, platelet activation, and thrombogenicity. Thrombosis Research. 99 (6), 577-585 (2000).
- Gillespie, W. J., Frampton, C. M. A., Henderson, R. J., Ryan, P. M. The Incidence of Cancer Following Total Hip-Replacement. Journal of Bone and Joint Surgery-British Volume. 70 (4), 539-542 (1988).
- Sperling, C., Schweiss, R. B., Streller, U., Werner, C. In vitro hemocompatibility of self-assembled monolayers displaying various functional groups. Biomaterials. 26 (33), 6547-6557 (2005).
- Mikhalovska, L. I., Santin, M., Denyer, S. P., Lloyd, A. W., Teer, D. G., Field, S., Mikhalovsky, S. Fibrinogen adsorption and platelet adhesion to metal and carbon coatings. Thrombosis and Haemostasis. 92 (5), 1032-1039 (2004).
- Airoldi, F., Colombo, A., Tavano, D., Stankovic, G., Klugmann, S., Paolillo, V., Bonizzoni, E., Briguori, C., Carlino, M., Montorfano, M., Liistro, F., Castelli, A., Ferrari, A., Sgura, F., Mario, C. D. i Comparison of diamond-like carbon-coated stents versus uncoated stainless steel stents in coronary artery disease. American Journal of Cardiology. 93 (4), 474-477 (2004).
- Allen, M., Myer, B., Rushton, N. In vitro and in vivo investigations into the biocompatibility of diamond-like carbon (DLC) coatings for orthopedic applications. Journal of Biomedical Materials Research. 58 (3), 319-328 (2001).
- Butter, R., Allen, M., Chandra, L., Lettington, A. H., Rushton, N. In-vitro Studies of DLC Coatings with Silicon Intermediate Layer. Diamond and Related Materials. 4 (5-6), 857-861 (1995).
- Dearnaley, G., Arps, J. H. Biomedical applications of diamond-like carbon (DLC) coatings: A review. Surface & Coatings Technology. 200 (7), 2518-2524 (2005).
- Dorner-Reisel, A., Schurer, C., Nischan, C., Seidel, O., Muller, E. Diamond-like carbon: alteration of the biological acceptance due to Ca-O incorporation. Thin Solid Films. 420, 263-268 (2002).
- Dowling, D. P., Kola, P. V., Donnelly, K., Kelly, T. C., Brumitt, K., Lloyd, L., Eloy, R., Therin, M., Weill, N. Evaluation of diamond-like carbon-coated orthopaedic implants. Diamond and Related Materials. 6 (2-4), 390-393 (1997).
- Grill, A. Diamond-like carbon coatings as biocompatible materials - an overview. Diamond and Related Materials. 12 (2), 166-170 (2003).
- Hauert, R. A review of modified DLC coatings for biological applications. Diamond and Related Materials. 12 (3-7), 583-589 (2003).
- Windecker, S., Mayer, I., De Pasquale, G., Maier, W., Dirsch, O., De Groot, P., Wu, Y. P., Noll, G., Leskosek, B., Meier, B., Hess, O. M. Working Grp Novel Surface, C., Stent coating with titanium-nitride-oxide for reduction of neointimal hyperplasia. Circulation. 104 (8), 928-933 (2001).
- Zhang, F., Zheng, Z. H., Chen, Y., Liu, X. G., Chen, A. Q., Jiang, Z. B. In vivo investigation of blood compatibility of titanium oxide films. Journal of Biomedical Materials Research. 42 (1), 128-133 (1998).
- Bolz, A., Schaldach, M. Artificial-Heart Valves - Improved Blood Compatibility By PECVD a-SiC-H COATING. Artificial Organs. 14 (4), 260-269 (1990).
- Haude, M., Konorza, T. F. M., Kalnins, U., Erglis, A., Saunamaki, K., Glogar, H. D., Grube, E., Gil, R., Serra, A., Richardt, H. G., Sick, P., Erbel, R., Invest, C. T. Heparin-coated stent placement for the treatment of stenoses in small coronary arteries of symptomatic patients. Circulation. 107 (9), 1265-1270 (2003).
- Suggs, L. J., Shive, M. S., Garcia, C. A., Anderson, J. M., Mikos, A. G. In vitro cytotoxicity and in vivo biocompatibility of poly(propylene fumarate-co-ethylene glycol) hydrogels. Journal of Biomedical Materials Research. 46 (1), 22-32 (1999).
- Clarotti, G., Schue, F., Sledz, J., Benaoumar, A. A., Geckeler, K. E., Orsetti, A., Paleirac, G. Modification of the biocompatible and haemocompatible properties of polymer substrates by plasma-deposited fluorocarbon coatings. Biomaterials. 13 (12), 832-840 (1992).
- Gombotz, W. R., Guanghui, W., Horbett, T. A., Hoffman, A. S. Protein adsorption to poly(ethylene oxide) surfaces. Journal of Biomedical Materials Research. 25 (12), 1547-1562 (1991).
- Ishihara, K., Fukumoto, K., Iwasaki, Y., Nakabayashi, N. Modification of polysulfone with phospholipid polymer for improvement of the blood compatibility. Part 2. Protein adsorption and platelet adhesion. Biomaterials. 20 (17), 1553-1559 (1999).
- Jung, N., Kim, B., Crowther, A. C., Kim, N., Nuckolls, C., Brus, L. Optical Reflectivity and Raman Scattering in Few-Layer-Thick Graphene Highly Doped by K and Rb. ACS Nano. 5 (7), 5708-5716 (2011).
- Rao, A. M., Eklund, P. C., Bandow, S., Thess, A., Smalley, R. E. Evidence for charge transfer in doped carbon nanotube bundles from Raman scattering. Nature. 388 (6639), 257-259 (1997).
- Bunch, J. S., Verbridge, S. S., Alden, J. S., vander Zande, A. M., Parpia, J. M., Craighead, H. G., McEuen, P. L. Impermeable atomic membranes from graphene sheets. Nano Letters. 8 (8), 2458-2462 (2008).
- Chen, S., Brown, L., Levendorf, M., Cai, W., Ju, S. -Y., Edgeworth, J., Li, X., Magnuson, C. W., Velamakanni, A., Piner, R. D., Kang, J., Park, J., Ruoff, R. S. Oxidation Resistance of Graphene-Coated Cu and Cu/Ni Alloy. Acs Nano. 5 (2), 1321-1327 (2011).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten