Method Article
柔性神经微探针的使用附加与Biodissolvable胶粘剂刚性加劲肋插入
摘要
的柔性神经微探针插入是通过将探针以刚性加强板与聚乙二醇(PEG)使能。独特的装配工艺确保了统一的和可重复的附件。插入到组织中后,所述PEG溶解和加强件被提取。 体外试验方法评估在琼脂糖凝胶的技术。
摘要
预期微电极阵列所做生物相容性薄膜聚合物的神经接口设备已经扩展功能寿命,因为柔性材料可以减少因微动不良组织反应。然而,他们的灵活性,防止它们被准确地插入到神经组织。本文介绍的方法,以一种灵活的微电极探针临时性地连接到刚性加强板使用biodissolvable聚乙二醇(PEG),以促进所述探针的精确,手术插入。一个独特的加强筋的设计允许对PEG粘合剂的均匀分布沿着探针的长度。倒装芯片接合,在微电子封装中使用的常用工具,能够进行精确的和可重复的对准和连接的探针与加强筋。探针和加强件被手术植入在一起,然后将PEG使其溶解,使得加强筋可以被提取离开探头到位。最后, 在体外试验方法用于评价加强筋提取脑组织的琼脂糖凝胶模型。这种方法植入已被证明更长的柔性探头特别有利的(> 3毫米)。它还提供了植入双面柔性探头一个可行的方法。迄今为止,该技术已被用来获得从大鼠皮层各种体内的记录数据。
引言
微电极阵列在神经科学的一个重要工具,以及新兴的临床应用,如假肢。特别是,插入的微电极探针通过与细胞在大脑,脊髓和周围神经亲密接触使刺激神经元的活动和记录。对于植入式神经探针的一个主要挑战是稳定的刺激和记录功能,延年益寿。微电极探针和神经组织之间的相互作用的建模和实验研究表明,1机制降解是微撕裂神经组织,由于在探头和组织1-3之间轻微的相对运动。一种解决方案是制造匹配更紧密神经组织,以减少相对微动的体积压缩刚度特性灵活的探针。因此,生物相容的薄膜的聚合物,例如聚酰亚胺和聚对二甲苯已被采用为有利的基板为微电子处接上的电流探头4-8。
柔性探头的权衡是,他们是难以插入到神经组织。研究人员已经采取了各种方法,以便于插入的柔性探头,同时保留所希望的机械性能。一类设计的修改聚合物探针的几何形状,同时遵守其他地区,以增加刚度在某些部分或轴。这已经完成通过将肋或其它材料9,10层。另一种方法中集成了一个3-D信道到聚合物探针设计填充有可生物降解的材料11。该探针可以被临时硬化,并插入该材料在通道中溶解并排出,之后。然而,方法如上述那永久修改最终植入的装置的几何形状可能会损害一些的柔性探针的理想特征。
一种方法,做Ñ加时改变最终探针的几何形状是封装在聚合物装置与可生物降解的材料,以暂时硬化装置12-14。然而,典型的可生物降解材料具有的杨氏模量幅度比硅小的订单,并作相应需要更大的厚度,以达到相同的刚度。充分涂覆探针可产生更圆的或钝头,使得插入更加困难。此外,由于可分解涂层暴露,有他们的危险接触后立即溶解,甚至近在咫尺,与组织。
另一类方法采用新型探头的基板材料,以减少刚度被植入组织后。这样的材料包括形状记忆聚合物15和一个机械适应性纳米复合材料16。这些材料能够在弹性模量显著插入后下降,并可能导致探针更紧密MATC神经组织h的机械性能。然而,刚性的可实现的范围仍然是有限的,因此它们可能不能够提供非常高的刚度等于硅或钨丝。因此,在柔性探针是很长的( 例如 > 3毫米),或具有非常低的刚度的情况下,可能仍然需要的临时固定更刚性的加强筋的方法。
报道又一个有前途的方法是涂层具有永久自组装单层(SAM)来定制班车和灵活的探头17之间的表面相互作用的加强班车。在干燥时,探针附着于涂穿梭静电。插入后,水将迁移到该亲水表面,从航天飞机分离探针,使得往复可以被提取。穿梭萃取减小探针位移被证明(85微米)。然而,仅静电相互作用保持探头吨他穿梭,有探头打滑相对于航天飞机之前和期间插入一定的风险。
我们已经开发了在该柔性探头连接到与该牢固地保持在插入过程中探针的临时biodissolvable粘合剂材料的加强件的方法。所用的探针是聚酰亚胺,其具有2-4京帕数量级的弹性模量进行。加强件是由硅制成,具有〜为200GPa的弹性模量。在连接时,硅的刚性支配,便于插入。一旦插入到组织中,粘合剂材料溶解和加强件被提取到探针恢复到其初始的灵活性。我们选择了聚乙二醇(PEG)作为biodissolvable粘合材料。 PEG已被用于在植入的应用,如神经探针,组织工程和药物递送11,18,19。一些证据表明,PEG可以减轻神经炎症反应在脑组织18,20。相对于其他可能的材料,包括蔗糖,聚乳酸 - 共 - 乙醇酸(PLGA),和聚乙烯醇(PVA),聚乙二醇具有的溶解时间在生物流体,它是一个合适的规模对许多植入手术(数量级几十分钟,这取决于分子量)。此外,它是固体在室温和液体温度范围为50-65℃。这个属性使得它特别适合于我们的精密装配过程。此外,在17个类似的SAM所描述的,溶解PEG是亲水性的,有利于提取的加强筋。这种有利的做法是由一种新型的加强筋设计和有条不紊的装配工艺,确保均匀的粘合剂覆盖面和准确的和可重复的对齐方式启用。除了 装配过程中,我们提出了在手术过程中实现可移动的加强件的方法,以及在体外程序来评价提取STI的ffener。
这里介绍的协议假定用户具有柔性聚合物微电极探针。关于这个探头的加强筋与组件的制造到加强筋的协议的一部分,假设获得的微细加工设备中常见的工具。有关插入和提取的协议可能会在神经科学为导向的实验室进行。
研究方案
1。探头大会补强
本节中的协议的描述制造的硅加劲肋,并且薄膜的聚合物探针的装配到刚性元件, 图1示出了沿与提出的加强件的典型聚合物的神经探针。的加强筋设计的细节示于图2。这种设计的新颖特征是在浅“芯吸”通道沿其长度是用来在组装过程中分配液体粘合剂运行。加强板的较宽部分为装配和外科插入时处理的标签。该选项卡上的水库连接到的通道。该组件是由硅使用标准微制造工艺制造。
- 硅加强筋用芯吸通道是从一个硅 - 绝缘体(SOI)晶片上的器件层的厚度等于所述加强件的所需厚度(制造的图3A)。一个合理的范围内加强筋厚度为20-100微米。建议加强筋的宽度比探针的宽度,这样有助于防止从键合界面的粘接剂溢出到该探针的顶端20-30微米以下。第一毛细作用通道进行干蚀刻使用标准的Bosch工艺( 图3B)。接着,将加强件的几何形状是由一个较长的蚀刻掩埋氧化物层( 图3C)上,停止所定义。最后,该加强件被释放通过在49%的氢氟酸( 图3D)湿蚀刻掩埋氧化物层。后彻底冲洗加强筋,浸泡在去离子水中15分钟。
- 把聚乙二醇的分子量为10,000克/摩尔的沉淀(PEG)进入贮存器( 图4)。加热所述加劲肋至65℃,使聚乙二醇熔化,并通过毛细管作用灯芯进入通道。然后冷却至室温凝固。
- 图5示出了倒装焊接机的示意性设置。将加强件上的倒装焊接机的基台倒置,然后拿起加强筋与工具头。把探头上的基台倒置。使用覆晶焊接机,对准加强筋和探头,然后放下加强筋,并将其放置在探头上。
- 倒装焊接机的基台应该有施加热到所述衬底的加热元件。将所述加强板后,再次加热该组件至65℃。等待一分钟,对PEG重熔,并开始填写探头和加强筋之间的接口。冷却至凝固。
- 打开装配过来,从顶部检查。根据需要,以允许所述PEG以完全填充所述探针和所述加强件之间的界面上重新加热。这可以在视觉上进行评估,因为探头是透明的。由于组件坐在加热器顶部(探针)朝上,手动放置1-3Ë固体PEG与Xtra的丸粒上的标签,使它们熔化过的探针,可提供在该区域的其他加强件( 图6)。最后,请允许组件冷却,以使PEG凝固。在这一点上,该组件已准备好手术插入。
2。插拔
- 安装探针刚性组件到一个显微操作器通过粘附加强板的背面的显微操作臂在选项卡区域, 如图7A所示 。这可以用双面胶或水泥做的,但要注意不要接触探头用胶粘剂。探头的连接器端暂时固定在用一小片粘合剂腻子,使得它可以容易地用小的力去除的微操作。
- 定位探针组件对目标以及与所需的插入速度插入探头。为0.13-0.5毫米/秒的速度插入发展这个协议的时候被使用。
- 立即从显微操纵器轻轻探头的连接器端取出并放于附近的表面,如第二操纵臂( 图7B)。这是一定要做的PEG开始溶解,以避免取代前探。
- 等待一段时间以PEG溶解。此量的时间将取决于PEG的分子量和探针与加强板之间的接触面积。例如,为10,000克/摩尔,微电极探针约6mm和匹配的加强件是306μm宽的PEG分子量,15分钟已发现的时间足够量。该协议的第3提出了一种方法来测试所要求的溶解时间。在此期间,应用磷酸盐缓冲盐水(PBS)用滴管周围的标签和插入点以溶解任何PEG即上面的目标( 图7C)。
- 使用机动微定位器,通过应用的位移开始提取的加强筋为100μm以5mm /秒的速度。这最初的快速运动有助于克服任何静摩擦和减少探针位移。然后,完成加强筋提取在大约0.1mm /秒( 图7D)以较慢的速度。
- 在实际手术的情况下,继续正常的程序申请凝胶,硅胶,和/或牙科丙烯酸在插入位点,以确保和保护探头,这表现在21。
3。琼脂糖凝胶测试
本节中的协议描述了一种设置和程序来检查加强筋中,接近本体的机械性能,pH值,和脑组织17,22的盐度为0.6%的琼脂糖凝胶提取。由于凝胶几乎是透明的,通过短距离,加强筋的分离和探针位移可以观察到。
- 制备在磷酸盐缓冲盐水(PBS)的0.6%琼脂糖溶液。在混合的元素vated温度以完全溶解琼脂糖粉末。将溶液倒入一个浅压克力盒;凝胶应该是3/4- 1深。允许对凝胶设置在室温一小时。
- 确保硬化的凝胶是饱和的PBS,使其不会变干,然后将凝胶加热到37°C。
- 设置微操作,框琼脂糖凝胶中,并且显微摄像系统, 如图8。
- 插入玻璃参考基准成凝胶的盒由凝胶和盒子的侧面( 图8)之间滑动。用牙科挑广场上的参考基准的功能,以视数码显微镜领域。
- 安装探头组件的显微操纵器,如步骤2.1中所述。
- 定位探针组件在凝胶约1mm后面的参考基准。
- 将探头插入凝胶中,在使用相机来指导它在视场中所需的深度。
- 紧随探头的连接器端移动到休息在附近的表面。
- 进行必要的调整摄像机图像聚焦探头(参考基准特征可能会稍微失焦)。取探头位置的快照。
- 允许PEG溶解(此时可能会发生变化,而事实上可能是一个参数进行测试)。应用PBS附近的标签,以溶解聚乙二醇是凝胶上面。
- 如果需要启动视频拍摄,并且按照步骤2.5中所述的提取开始加劲肋。解压缩完成后,把探头位置的最终快照。
- 使用图像处理工具图像之前和之后加强筋抽出来比较。使用的参考基准是可见的,以登记该字段的功能(对齐)的图像。校准的基础上的探针上已知的特征的尺寸的图像的尺度。测量探头位移的距离。
结果
这种插入技术被用于与LLNL的薄膜聚酰亚胺探头,它已通过ISO 10993生物相容性标准,并适用于慢性植入相结合。一个典型的薄膜聚酰亚胺探针沿着与硅刚性元件是大约10毫米长的狭窄区域, 如图1所示。此加强筋具有沿其长度延伸的1毛细通道, 如图2,图3示出了用于创建该加强筋出硅的mimcrofabrication过程, 图4示出固体的PEG的沉淀,它被放置成片的油藏,通过倒装焊接机系统上的摄像头所看到。一旦使用内建在倒装焊接机的基台的加热器加热,所述PEG熔融,并开始芯吸进入通道。相机视图使我们能够监视排汗过程,直到PEG完全充满通道,whicħ花了大约一个小时,分子量为10,000克/摩尔的聚乙二醇。的PEG,然后再固化,并在探针和加强筋分别设置在倒装焊接机, 如图5。图9A示出被排列和连接的,用PEG完全填充界面后的探针和加强件的俯视图, 图9B所示示出了一个气泡其中PEG是因为粒子的不存在的实例。在装配的最后一步是在处理过程中对PEG添加到标签区域在探头的电缆部分,为额外加固。因为该区域将不被插入到目标,这是可以接受的PEG的一个较大的容积在这里, 如图6。这种装配方法已被用于探针的各种形状附着到加强板,包括多杆装置,如在示于图10。
在体外琼脂糖凝胶试验已被用于qualitativ伊利评估不同的参数,如PEG的分子量,允许PEG溶解时间,并加强件的几何形状。用PEG和加强件的几何形状的每一种组合,就可以使之溶解在设定的时间量。然后,提取,同时观察探针位移实时尝试。如果探针不可见的分离或滑动相对于所述加强件显著(> 200μm)的拖动,我们的结论是,PEG未完全溶解。 表1给出的PEG溶解的一些有代表性的观察具有不同时间和不同分子量的带加强筋这是长6毫米和306微米宽。在随后的测试中的另一个发现是,当所述加强件是比较窄的( 例如 220微米),所述PEG溶解在更短的时间(只需5分钟)。这很可能是因为粘合剂的接触面积降低,因此,有PEG的一个较小的体积以使其溶解。这似乎没有影响PEG参数解散或探针位移为加强筋的厚度(厚度为20微米至100微米的测试)和排汗通道数(1比3)。
体外试验也被用来量化平均探针位移对于给定的探针/加强板/粘合剂配置。在这个例子中,使用图7所示的插入/提取序列,其中所述探针刚性组件被插入的琼脂糖凝胶中,连接器端被移动到附近的表面进行试验中,PEG被溶解,并且加劲终于提取离开探头。实验设置在图8示出附加到显微操纵器臂和定位在所述凝胶中的探针刚性组件。参考基准是与对放置在视数码显微镜领域的压克力盒金点阵列一个小玻璃芯片。
在这个例子中的器件分别约为10微米厚,536微米宽的带8 100微米直径的电极。的痕迹组成的Ti-Au的Ti的金属堆栈。硅加强筋为220μm宽,长6毫米和50微米厚。该探针刚性组件插入大约5mm进入凝胶。 图11显示的快照之前和之后的提取从在琼脂糖凝胶测试探针组件的加强筋。在图像中的浅金色特征是从参考基准,并以此作为参考特征的图像对齐到对方。所述电极(200微米)之间的已知间距被用于校准的像素大小,因为该尺寸是变化的制造过程不那么敏感。净探针位移由于加强筋提取,估计是28±9微米(平均值±标准误差中,n = 5)。
迄今为止,该方法一直延伸到实际的多次进制手术植入到大鼠皮质探针。装配后,探针和50微米厚的加强筋进行灭菌一起在EtOH中在室温下进行。插入和提取均采用附着到立体定位框架上的微操作。探针 - 刚性组件被插入0.13毫米/秒大约4mm到大鼠皮质。 15分钟后,加劲肋萃取,离开探头。从手术恢复后,神经录音, 如图12,被成功地从清醒动物证明该方法的可行性,在实际手术23获得的。这种植入技术也被用于获得在体内的录音与具有同时在正面和背面电极的双面阵列, 如图13所示。
pload/50609/50609fig1.jpg“/>
图1。一个典型的神经探针和建议的加强件的原理图。一个典型的薄膜聚合物探针具有在探针端部的一个或多个电极。金属迹线从电极上运行沿电缆部分的长度,并终止于一个连接到电连接器的衬垫。刚性元件的长度(在本例中约为10mm)取决于探头的插入深度,并且在加强筋更宽的标签允许进行处理。 ( 图片由戴安娜乔治)
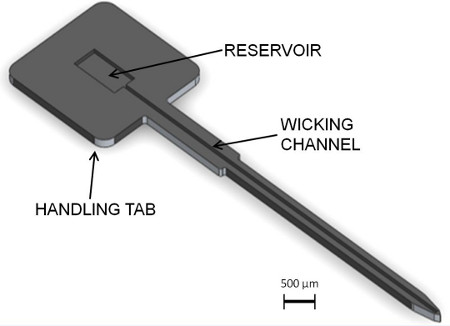
图2。加强筋的设计细节 。虹吸通道利用毛细作用来分发已存入储液体胶。该水库是在更广泛的选项卡区域,便于搬运。 ( 图片由戴安娜乔治)

图3。制作顺序为硅加劲肋。硅加强筋是制作在硅-绝缘体(SOI)晶片(A),第一毛细作用通道都使用标准的Bosch工艺(B)的干法蚀刻,接着,将加强件的几何形状是由一个较长的蚀刻,停止定义掩埋氧化物层(C)上,最后,加强筋被释放通过在49%的氢氟酸(D)的湿蚀刻的掩埋氧化物层。

图4。聚乙二醇在所述加强水库。聚乙二醇的薄片放置在加强件的水库。一旦加热,就会熔化,填充贮存和流进入毛细通道。

图5。示意性的倒装芯片接合的加强件是通过在倒装芯片接合机的工具头的真空保持与通道向下。神经探针在于在基台正面朝下。

图6。聚乙二醇对加强筋选项卡。额外的聚乙二醇慷慨地应用了加强筋加固的标签上。聚酰亚胺探针的电缆部分上的加强筋的顶部可见。

图7。在示意图插入可以和提取序列。一)探针刚性组件是使用显微操作B)连接器端移动到附近的表面插入组织。C)PBS是用于溶解聚乙二醇。 四)加强筋提取的加强筋的选项卡上,留下探头中的目标。

图8。 体外测试设置的设置进行检测探头的插入和提取筋在磷酸盐缓冲盐水中0.6%的琼脂糖凝胶。探针 - 刚性组件被安装在微操作器臂和定位在靠近参考基准的凝胶目标。数码显微镜是用来观察在琼脂糖凝胶探头和加强筋。
图9。探头坚持加强筋。连接到具有良好的定位和完整的粘结覆盖B)在胶粘剂覆盖面的差距的一个例子,由于粒子加强筋探针的)顶视图。

图10。多杆探头为例,提出了装配过程中使用到这个四杆探头连接到一个匹配的硅加强筋。

图11。的加强筋的提取结果。快照从之前(上图)和后(底)加强筋的提取与琼脂糖凝胶薄膜聚酰亚胺探针的例子 。光黄金点上参考基准和被用作参考特征进行比较的图像和测量探头的位移。该探针的位移估计是28±9微米(平均值±标准误差,n = 5)。
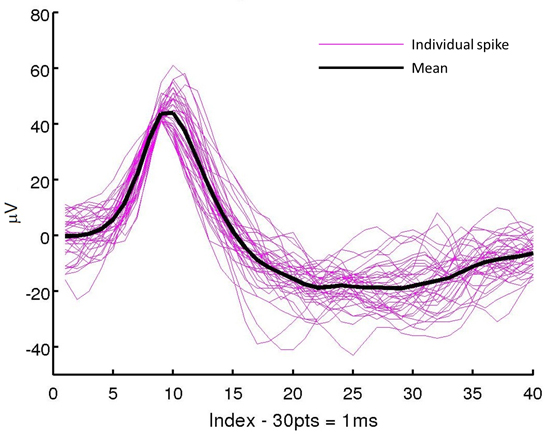
图12。生理记录的例子。这些单神经元尖峰是从植入如本协议中所述可拆卸的加强筋的柔性微电极探测获得的。

图13。 LFP记录从一个双面探针。插入具有柔性阵列,对正面和背面表面上的电极的一个可移动的加强筋使测试。这些LFP录音证明ç植入后两侧omparable电极的性能。
| PEG溶解后: | |||||
| 探头长度(mm) | 加强筋宽度(微米) | PEG分子量(克/摩尔) | 10分钟 | 15分钟 | 30分钟 |
| 6 | 306 | 6,000 | 是的 | 是的 | |
| 10,000 | 是的 | ||||
| 20,000 | 无 | 是的 | |||
表1中。上的PEG的溶出不同分子量的聚乙二醇溶解时间在0.6%的琼脂糖凝胶。观测采用灵活的探头连接到一个硅加强筋,不同的时间量之后。
讨论
这里描述的方法提供了一个良好的控制过程附加薄膜聚合物探针来分离加强筋与biodissolvable粘合剂。还提出,建议外科手术,以实现这些可移动的加强筋和技术验证过程在体外对于一个给定探针加强筋的配置。由于加强件可以由任意刚性的,该方法可以方便地插入相对长的探针(> 3mm)的中。因此,该插入方法有望成为一个有利的技术在脑深部刺激(DBS),脊髓刺激,和外周神经接口的应用程序。
新颖的加强筋用芯吸通道和倒装芯片安装工艺适用于各种材料和探头的配置。几何上,该加强件不具有相匹配的探针足迹,并可能,例如,是比探针窄。 STI的厚度 ffener可能也有所不同。虽然我们已经描述了由硅制成,与其它材料的加强件,它可以是能够实现更理想的机械性能对于特定的应用。组装过程也适用于其他类型的液体粘合剂。 PEG是由于其能力得到巩固和重熔多次特别易于使用。在不具有该属性的其他液体粘合剂的情况下,装配顺序可能需要进行修改。有可能使用不同分子量的聚乙二醇。较高的分子量需要较长的时间溶解,在手术过程中可能是可取的。探针和加强件之间的接触面积也将影响到溶解探针插入后的粘合剂所需的时间。因此建议使用选择的分子量的探针加劲肋的配置可以在体外如第3节中所述,以溶解粘合剂所需要的时间来表征测试。
_content“>我们发现,可以精确地控制提取速度是用于提取以最小的探头位移的刚性元件的关键。具体而言,初始的快速运动有助于克服静摩擦,并从所述探针分开的加强筋。在此之后,将提取的剩余部分可以可以以较慢的速度可以忽略附加的探头位移完成,如在琼脂糖凝胶上观察到的测试。许多神经科学实验室使用Kopf立体系统,并且有从KOPF( 如型号2662)的机动mircopositioner模块,该模块可被添加到这些系统。我们选择了纽波特电动致动器,因为它有类似的动态性能,但成本较低并且有更灵活的速度控制(这是必要的,制作一个简单的支架安装在致动器连接到我们的微定位系统)的KOPF系统可以应用2萃取速度类似于我们开发的协议,不过,KOPF致动器的最大速度为4毫米/秒,而我们用5毫米/秒,使用新港执行器的初始位移。在体外和体内试验中,进行或者与一个手动驱动的微操作,或机动显微操纵探针-刚性组件的插入,速度范围为0.13-0.5毫米/秒。没有损坏或探针的剥离进行了观察。较高的插入速度没有被评估,以确定损坏探针刚性组件的风险。
修改,插入/提取过程都在进步,使这一过程更加健壮。特别地,一个非常敏感的步骤是移动所述探针的连接器端关闭微操作到一个附近的表面上。有一个在干扰探头已抵押之前,这一步的危险。它也有可能是在电缆的弯曲可能会导致应力在探头的插入部分,从而导致探针的意外位移后加强筋提取。目前,这些风险通过使用一个探头和电缆,至少2.5厘米长的缓解。然而,理想的是在插入/提取过程是较少依赖于探针的设计。修改了微操作工具端或增加分期,可以暂时支持连接器固定装置将有可能使加强筋的更可靠的提取。
有几个开放式的问题,可能会导致从此方法扩展未来的研究。首先,在0.6%琼脂糖凝胶上提供探针位移的最佳已知的体外脑组织替代,并使其成像分析,它不完全复制的脑组织。需要进一步的研究来检查的位置和探头体内的位移。其次,长期植入及组织学检测是需要量化灵活探头的好处有一个可拆卸的加强筋。这样的研究可以探讨理论该探头符合减少微动,延长电极的性能。最后,这将有利于更精确地表征PEG的降解速率。这可以帮助我们更好地调整的溶解时间为特定的手术需要。这样的测量也可以量化的溶解PEG多长时间保持探头和加强件,这是很重要的,因为聚乙二醇的亲水性有利于提取的加强板的。
披露声明
该作者有没有竞争的财务权益。
致谢
这项工作是由美国国立卫生研究院NIDCD Y1-DC-8002-01的支持。根据合同DE-AC52-07NA27344美国能源署的主持下进行了劳伦斯利弗莫尔国家实验室这项工作。
材料
| Name | Company | Catalog Number | Comments |
| Polyethylene glycol, 10,000 g/mol | Sigma Aldrich | 309028 | |
| Agarose | Sigma Aldrich | A9539 | |
| Flexible Sub-micron Die Bonder | Finetech | Fineplacer lambda | |
| Micromanipulator | KOPF | 1760-61 | |
| Digital Microscope | Hirox | KH-7700 | |
| Dual Illumination Revolver Zoom Lens | Hirox | MXG-2500REZ | |
| Precision Motorized Actuator | Newport | LTA-HS | w/ CONEX-CC controller |
参考文献
- Polikov, V., Tresco, P., Reichert, W. Response of brain tissue to chronically implanted neural electrodes. Journal of Neuroscience Methods. 148, 1-18 (2005).
- Lee, Y. T., Hitchcock, R. W., Bridge, M. J., Tresco, P. A. Chronic response of adult rat brain tissue to implants anchored to the skull. Biomaterials. 25 (12), 2229-2237 (2004).
- Subbaroyan, J., Martic, D. C., Kipke, D. R. A finite-element model of the mechanical effects of implantable microelectrodes in the cerebral cortex. Journal of Neural Engineering. 2, 103-113 (2005).
- Lacour Sun, Y., S,, et al. Assessment of the biocompatibility of photosensitive polyimide for implantable medical device use. Journal of Biomedical Materials Research A. 90 (3), 648-655 (2009).
- Kipke, D. R., Pellinen, D. S., Vetter, R. J. Advanced neural implants using thin-film polymers. IEEE International Symposium on Circuits and Systems. 4, 173-176 (2002).
- Mercanzini, A., Cheung, K., et al. Demonstration of cortical recording using novel flexible polymer neural probes. Sensors and Actuators A. 143, 90-96 (2008).
- Stieglitz, T. Flexible biomedical microdevices with double-sided electrode arrangements for neural applications. Sensor and Actuators A. 90, 203-211 (2001).
- Tooker, A., Tolosa, V., Shah, K. G., Sheth, H., Felix, S., Delima, T., Pannu, S. Polymer neural interface with dual-sided electrodes for neural stimulation and recording. Proceedings of the International Conference of the Engineering in Medicine and Biology Society. , 5999-6002 (2012).
- Parylene microprobes with engineered stiffness and shape for improved insertion. Egert, D., Peterson, R. L., Najafi, K. Proceedings of Transducers '11, Beijing, China, , (2011).
- Lee, K. -K., He, J., et al. Polyimide-based intracortical neural implant with improved structural stiffness. Journal of Micromechanics and Microengineering. 14, 32-37 (2004).
- Takeuchi, S., Ziegler, D., et al. Parylene flexible neural probes integrated with microfluidic channels. Lab On A Chip. 5, 519-523 (2005).
- Improving mechanical stiffness of coated benzocyclobutene (bcb) based neural implant. Singh, A., Zhu, H., He, J. Proceeding of the International Conference of the Engineering in Medicine and Biology Society, , 4298-4301 (2004).
- Lewitus, D., Smith, K. L., et al. Ultrafast resorbing polymers for use as carriers for cortical neural probes. Acta Biomaterialia. 7, 2483-2491 (2011).
- An ultra-compliant, scalable neural probe with molded biodissolvable delivery vehicle. Gilgunn, P. J., Khilwani, R., et al. Proceedings of the 2012 IEEE 25th International Conference on Micro Electro Mechanical Systems (MEMS), , 56-59 (2012).
- Ware, T., Simon, D., et al. Fabrication of responsive, softening neural interfaces. Advanced Functional Materials. 22 (16), 3470-3479 (2012).
- Harris, J. P., Capadona, J. R., et al. Mechanically adaptive intracortical implants improve the proximity of neuronal cell bodies. Journal of Neural Engineering. 8, 1-13 (2011).
- Kozai, T. D. Y., Kipke, D. R. Insertion shuttle with carboxyl terminated self-assembled monolayer coatings for implanting flexible polymer neural probes in the brain. Journal of Neuroscience Methods. 184 (2), 199-205 (2009).
- Bjugstad, K. B., Lampe, D. S., Kern, D. S., Mahoney, M. Biocompatibility of poly(ethylene glycol)-based hydrogels in the brain: An analysis of the glial response across space and time. Journal of Biomedical Materials Research Part A. 95 (1), 79-91 (2010).
- Greenwalk, R. B., Choe, Y. H., McGuire, J., Conover, C. D. Effective drug delivery by pegylated drug conjugates. Advanced Drug Delivery Reviews. 55 (2), 217-250 (2003).
- Effects of adsorbed proteins and an antifouling agent on the impedance of silicon-based neural microelectrodes. Sommakia, S. S., Rickus, J. L., Otto, K. J. Proceedings of the 31st Annual IEEE EMBC International Conference, , 7139-7142 (2009).
- Gage, G. J., Stoetzner, C. R., Richner, T., Brodnick, S. K., Williams, J. C., Kipke, D. R. Surgical Implantation of Chronic Neural Electrodes for Recording Single Unit Activity and Electrocorticographic Signals. J. Vis. Exp. (60), e3565(2012).
- Chen, Z. -J., Gillies, G. T., et al. A realistic brain tissue phantom for intraparenchymal infusion studies. Journal of Neurosurgery. 101 (2), 314-322 (2004).
- Removable silicon insertion stiffeners for neural probes using polyethylene glycol as a biodissolvable adhesive. Felix, S., Shah, K. G., George, D., Tolosa, V., Tooker, A., Sheth, H., Delima, T., Pannu, S. Proceedings of the International Conference of the Engineering in Medicine and Biology Society, , 871-874 (2012).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。