Method Article
Измерение содержания растворенного метана в водных экосистемах с помощью газоанализатора методом оптической спектроскопии
В этой статье
Резюме
В данном исследовании демонстрируется подход к измерению концентраций метана в водных пробах с помощью портативных оптических анализаторов, соединенных с камерой впрыска в замкнутом контуре. Результаты аналогичны результатам традиционной газовой хроматографии, представляя собой практичную и недорогую альтернативу, особенно подходящую для дистанционных полевых исследований.
Аннотация
Измерение потоков парниковых газов (ПГ) и пулов в экосистемах становится все более распространенным в экологических исследованиях из-за их актуальности для изменения климата. Вместе с этим растет и потребность в аналитических платформах, адаптируемых к измерению различных пулов и потоков в исследовательских группах. Данное исследование направлено на разработку процедуры использования портативных газоанализаторов на основе оптической спектроскопии, первоначально разработанных и продаваемых для измерения газовых потоков, для измерения концентраций парниковых газов в водных пробах. Протокол включает в себя традиционный метод уравновешивания свободного пространства с последующим впрыском подпробы газа в камеру, соединенную через замкнутый контур с входным и выходным отверстиями газоанализатора. Камера изготовлена из обычной каменной банки и простых лабораторных принадлежностей и является идеальным решением для образцов, которые могут потребовать предварительного разбавления. Концентрации метана, измеренные с помощью камеры, тесно коррелируют (r2 > 0,98) с концентрациями, определенными отдельно с помощью газовой хроматографии и пламенной ионизационной детекции (GC-FID) на подобразцах из тех же флаконов. Эта процедура особенно актуальна для полевых исследований в отдаленных районах, где хроматографическое оборудование и расходные материалы недоступны, предлагая практичное, более дешевое и эффективное решение для измерения концентраций метана и других растворенных парниковых газов в водных системах.
Введение
Экосистемы на стыке наземных и водных организмов, такие как водно-болотные угодья, озера, водохранилища, реки и ручьи, являются важными поглотителями и источниками парниковых газов (ПГ), таких как углекислый газ (CO2), метан (CH4) и закись азота (N2O)1,2. CH4, в частности, образуется при анаэробном дыхании в насыщенных поровых пространствах осадочных пор. После его производства часть окисляется и превращается в CO2, в то время как остальная часть в конечном итоге диффундирует через толщу воды и растительность или взрывается впузырьки. КонцентрацияCH4 в воде, насыщающей поры осадочных пород (т.е. в поровой воде) в данный момент времени, дает представление о балансе междуCH4, производимым, потребляемым и транспортируемым4. При измерении по вертикальным профилям или во времени концентрация поровой воды также позволяет определить зоны, более активные в производстве и потреблении CH4, а также их сезонные колебания.
Традиционно методы определения концентрации парниковых газов из поровых вод в экосистемах включают обработку проб воды, собранных в полевых условиях, для уравновешивания газов в созданном пространстве. Затем пространство для головного убора анализируется с помощью газовой хроматографии для определения концентраций5. Несмотря на то, что этот метод широко применяется в экологических исследованиях, он требует настольных систем газовой хроматографии и пламенно-ионизационного детектирования (GC-FID), которые требуют выделения обычного лабораторного пространства и высокой степени экспертных знаний для калибровки и эксплуатации (например,6). Это также требует использования специализированных расходных материалов, таких как большие резервуары с газами-носителями (т. е. азотом (N2) и гелием (He)), которые не всегда доступны в отдаленных местах. Эти требования и связанная с ними логистика транспортировки образцов в лабораторию могут ограничивать разработку образцов и, в некоторых случаях, ограничивать объем исследования при отсутствии хроматографического оборудования.
Целью данного исследования была разработка альтернативного метода измерения концентраций растворенных парниковых газов в пробах водных растворов в открытом космосе с помощью портативных газоанализаторов на основе оптической спектроскопии. Этот тип оптического газоанализатора является экономичной альтернативой стандартным системам GC-FID, а его портативность делает его идеальным выбором для полевых работ. Портативные газоанализаторы на основе оптической спектроскопии позволяют проводить высокочастотные измерения концентрации газа (т.е. ~ 1 с-1) с временем отклика от 2 до 5 с, в зависимости от марки и модели. Эти приборы разработаны и продаются в первую очередь для определения газовых потоков с поверхностей, выбрасывающих ПГ, таких как почва, вода и растительность 7,8,9. Оптические анализаторы позволяют рассчитывать поток на основе непрерывных измерений концентрации в нестационарных камерах свободного пространства, развернутых на излучающих поверхностях. При их регулярном использовании в поверхностных камерах высокочастотные измерения скорости изменения концентраций, наблюдаемых в камере, и известных размеров камеры, давления и температуры, позволяют интерпретировать эти данные как скорость излучения (или поглощения) на площадь поверхности (т.е. поверхностные потоки)10. Тем не менее, портативные газоанализаторы не оборудованы и не оптимизированы для концентраций растворенных в водных средах, что требует дополнительной адаптации и интерпретации для этого типа анализа.
Используя предыдущие демонстрации использования оптических анализаторов для определения концентраций в дискретных образцах из свободного пространства8, мы разработали небольшую закрытую камеру (т.е. без излучающих поверхностей), которая подключается к анализатору в замкнутом контуре. Изменение концентраций после закачки подпробы газа из свободного пространства с последующим расчетом разбавления позволяет определить исходные концентрации в свободном пространстве. Точность данного подхода оценивалась путем сравнения его результатов с результатами, полученными с помощью GC-FID в тех же образцах. Этот метод был дополнительно продемонстрирован на примере использования, в котором были проанализированы вертикальные профилиCH4 в пробах поровой воды, собранных на экспериментальных участках в пресноводном болоте в Луизиане.
протокол
1. Отбор проб и анализ поровых вод
- Соберите образцы с помощью пробоотборников для диализа поровой воды (глазок)11. Разверните гляделки в соответствующих местах исследуемого участка. В демонстрационном исследовании 6 глазков были размещены на двух доминирующих участках растительности пресноводного болота: три на участке с преобладанием Sagitaria lancifolia , а остальные три на участке с совместным преобладанием растительности S. lancifolia и Typha latifolia .
- Собирайте образцы 4 раза в июне, сентябре, октябре и декабре. Соберите образцы на 10 различных глубинах от поверхности почвы до ~50 см ниже нее. Отбор проб проводился по методу, описанному в12,13.
- Заполните ячейки для отбора проб 61 мл деионизированной воды ~ за 20 дней до отбора проб. Пузырьковая деионизированная вода сN2 в течение 5 минут в лаборатории для удаления кислорода перед использованием в полевых условиях.
- Во время отбора проб следует извлечь 25 мл воды из камеры с помощью шприца, подключенного к линии экстракции клетки. Затем наполните ячейки свежей деионизированной водой, предварительно пузырчатойN2 , через вторичную линию подпитки ячеек. Если измерения концентрации требуются сразу после сбора, перейдите к шагу 2.1.
- Экстрагированную воду добавить в стеклянные флаконы объемом 10 мл, законсервированные 0,2 мл 0,1 М HCl, закрыть перегородкой и поставить в холодильник до анализа в лаборатории.
ПРИМЕЧАНИЕ: Пользователи этого метода могут изменять глубину сбора, график отбора проб и частоту в зависимости от конкретных потребностей исследования.
2. Измерение концентрации парниковых газов
- Выполнение балансировки пробы поровой воды в шприце
- Создание образцов газа в открытом пространстве с использованием метода уравновешивания14. С помощью шприца объемом 30 мл наберите 5 мл воды (Vpw) из образцов, собранных в поле, а затем добавьте 15 мл N2 (сверхвысокая чистота 99,999%), чтобы создать свободное пространство (Vhs).
- Энергично и последовательно помешивайте шприц в течение 5 минут, вручную или с помощью качалки (при наличии). Введите 12 мл подпробы газа в свободное пространство в предварительно вакуумированный флакон объемом 10 мл, используемый для измерения концентрации газа с помощью оптического анализатора, в следующих шагах (рис. 1). Откачайте флаконы перистальтическим насосом15 или вручную потяните поршень шприца объемом 60 мл на закрытый флакон и откачайте воздух 3 раза.
ПРИМЕЧАНИЕ: Его можно использовать вместо N2 для создания свободного пространства. Процедура добавления N2 или He в шприц зависит от конкретной адаптации или регулятора фактического бака, доступного пользователям. Это дополнение обычно включает в себя соединение шприца с резервуаром с помощью подходящей трубки или экстракцию со шприцем из отверстия для отбора проб, адаптированного к резервуару. В зависимости от условий на площадке и связанной с этим логистики пользователи могут использовать окружающий воздух для создания свободного пространства.
- Создание камеры впрыска
- Изготовьте камеру впрыска, которая может принимать небольшой объем воздуха (~1 - 5 мл) в герметичный объем воздуха, который соединяется с входом и выходом газоанализатора, образуя замкнутый контур (Таблица материалов). Камера впрыска и анализатор являются двумя основными элементами системы (Рисунок 2).
- Модифицируйте металлическую крышку каменной банки объемом 365 мл, просверлив одно отверстие диаметром 11 мм, чтобы вместить одну перегородку в качестве порта впрыска, и два отверстия диаметром 7 мм, чтобы вставить клапаны запорного крана, которые соединяются с анализатором. Используйте эпоксидный клей для затяжки отверстия впрыска и фитингов и обеспечения герметизации камеры.
- Подключите камеру впрыска к оптическому анализатору
- Соедините банку с входными и выходными отверстиями оптического анализатора, используя внутренний диаметр 5/32 дюйма (I.D.) и 1/4 дюйма внешний диаметр (O.D.) Пластиковые трубки PFA и их дополнительный объем. Убедитесь, что трубка соответствует рекомендациям производителя прибора и является чистой и сухой без образования конденсата.
- Откройте клапаны, соединяющие камеру впрыска с прибором, чтобы создать замкнутый воздушный контур. Подождите, пока концентрация газа стабилизируется.
- Введение образца в камеру
- Когда концентрация в камере и сигнал в анализаторе стабилизируются (т.е. стандартное отклонение <0,03 ppm), введите 2 мл подпробы из флаконов, содержащих пробу свободного пространства, созданную на шаге 2.1.2. Подождите, пока концентрации в анализаторе снова стабилизируются, прежде чем вводить следующую подпробу (рис. 3).
- Вводите до 20 подобразцов последовательно или меньше, если концентрация приближается к 100 ppm (см.8для влияния на точность выше этого порога). Проанализируйте стандарты CH4 для проверки каждых 5 образцов и оцените разницу с помощью фактических измерений с использованием относительного стандартного отклонения (RSD).
- После завершения работы с набором штабелированных впрысков отсоедините одну из линий, подключенных к прибору, чтобы сбросить камеру на давление окружающей среды и избежать значительного повышения давления и концентрации метана.
ПРИМЕЧАНИЕ: На основе многочисленных тестовых прогонов было определено, что сигнал стабилизировался через ~15 с после инжекции, но может потребоваться другое время в ответ на другие спецификации записи прибора (Рисунок 3). Расход используемого прибора составлял ~1 л/мин с временем отклика 5 с и давлением в полости во время различных анализов в разные дни в диапазоне от 720 до 745 мм рт. ст.
- Рассчитать концентрациюCH4 в свободном пространстве
- Для каждой подпробы рассчитать концентрацию целевого ПГ (например, CH4, CO2, N2O) в свободном пространстве (Chs - μмоль/моль) с помощью уравнения 1:
 уравнение [1]
уравнение [1]
Где Vhs — объем подвыборки свободного пространства. - Рассчитайте концентрации до (Cbi - μmol mol-1) и после (Cai - μmol mol-1) впрыскиваний как среднее значение 15 измерений (~15 с) до впрыска и 15 после стабилизации сигнала после впрыска. Рассчитаем объемы в мл до (Vbi) и после (Vai) инъекций с помощью уравнений 2 и 3:
 [2]
[2]
и
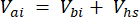 [3]
[3]
Где Vj (мл) – добавленный объем банки (365 мл) и шланга (125,4 мл), а Vi (мл) – накопленный объем введенных подобразцов.
- Для каждой подпробы рассчитать концентрацию целевого ПГ (например, CH4, CO2, N2O) в свободном пространстве (Chs - μмоль/моль) с помощью уравнения 1:
- Рассчитать концентрацию поровых вод
- Рассчитать парциальное давление (Pi - МПа) CO2, CH4 или N2O в свободном пространстве с использованием молярной доли газа в свободном пространстве и атмосферного давления (P) во время обработки образца с помощью уравнения 4:
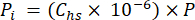 [4]
[4] - Рассчитайте водный эквивалент концентрации ПГ в поровой воде с помощью уравнения разбавления (уравнение 5) с учетом свободного пространства и водных эквивалентных концентраций и объемов:
 [5]
[5]
Где R — универсальная газовая постоянная (0,008314 л МПа моль−1 K−1), — температура воздуха (K), Vhs — объем свободного пространства (мл), KHcp — постоянная летучести Генри CO2,CH4 или N2O (2,96, 67,13 и 3,82 л МПа/моль соответственно)16, а Vpw — объем жидкого подобразца, используемого для создания свободного пространства (мл). - Используйте записанные T и P во время измерений. Средние Т и Р при анализе образцов демонстрационного проекта составили 295,15 К и 0,101325 МПа соответственно.
- Рассчитать парциальное давление (Pi - МПа) CO2, CH4 или N2O в свободном пространстве с использованием молярной доли газа в свободном пространстве и атмосферного давления (P) во время обработки образца с помощью уравнения 4:
3. Валидация по стандартным хроматографическим измерениям
- Проанализируйте различные известные концентрации CH4 во флаконах объемом 10 мл на обычном газовом хроматографе. Используйте три одинаковые группы по 20 стандартов в каждой. Самые низкие концентрации варьировались от 5 до 100 ppm и увеличивались с шагом 5 ppm.
- Определение концентрацииCH4 с помощью пламенно-ионизационного детектирования на газовом хроматографе. В хроматографе использовалась пористая полимерная абсорбирующая колонка с He (25 мл/мин) в качестве газа-носителя. Для проведения измерений концентраций эталонов откалибруйте хроматограф в соответствии с аппроксимацией кривой (r2) > 0,99.
- После хроматографии приступают к определению концентрации CH4 в тех же стандартных флаконах с помощью описанного выше метода, с использованием откалиброванного производителем оптического анализатора (т.е. прецизионный (300 с, 1σ): 0,3 ppb CH4).
- Оценить точность метода путем подгонки линейной регрессии к результатам хроматографии и оптического анализатора трех стандартных групп. Оценка воспроизводимости метода путем сравнения наклонов и пересечений регрессий, выполненных в рамках каждой группы стандартов. Оцените сравнение, используя стандартную модель наименьших квадратов с акцентом на рычаг эффекта. Оценивайте все регрессии и сравнения с уровнем значимости 0,05.
Результаты
Оптический анализатор в сравнении с газовой хроматографией
Результаты, полученные с помощью газовой хроматографии и оптического анализатора для трех групп стандартов, показали хорошие линейные аппроксимации ( т.е. r2 > 0,98) с наклонами, близкими к единице (рис. 4). Наклоны регрессий в трех экспериментах были статистически схожими (F(2) = 0,478, p = 0,623), что свидетельствует о воспроизводимости результатов. Важно отметить, что наклоны во всех трех случаях были больше единицы, что указывает на то, что в среднем можно ожидать незначительного занижения концентраций газов, измеренных с помощью оптического анализатора, по сравнению с концентрациями, полученными с помощью хроматографии. Тем не менее, пересечения на нуле различаются (F(1) = 1648,49, p <0,0001), что предупреждает об осторожности при интерпретации низких концентрацийCH4 (т.е. <10 мкмоль/моль). Фактически, при этих самых низких концентрациях оптический анализатор и хроматография показали наибольшие относительные ошибки (Таблица 1), что свидетельствует о проблемах измерения при низких концентрациях.
Полевые испытания: использование протокола для определения концентрации метана в поровой воде на двух участках растительности в прибрежных водно-болотных угодьях Луизианы
Концентрации CH4 в поровой воде, определенные из полевых проб, демонстрируют отчетливую вертикальную и временную динамику (рис. 5). Эти закономерности ожидаются в экогидрологических условиях водно-болотных угодий, подобных тем, которые были отобраны, где разнообразная растительность водно-болотных угодий может модулировать производство и окислениеCH4 и, как следствие, газообмен с атмосферой17,18. ОД составил ± 10,03%, что меньше 15%, обычно используемых в качестве порогового значения в протоколах контроля и обеспечения качества (QC/QA) с использованием хроматографии при анализе парниковых газов19.

Рисунок 1: Обзор протокола. Схема, показывающая основные этапы протокола. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
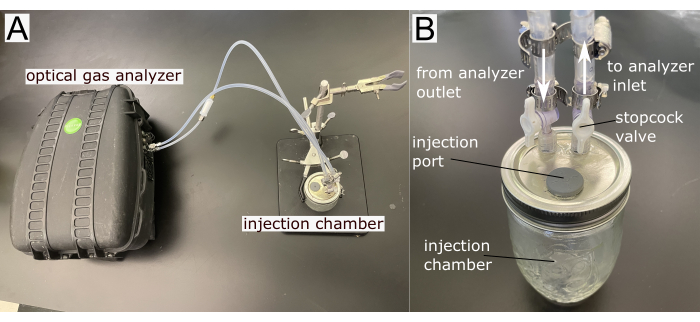
Рисунок 2: Компоненты системы. (А) Основные компоненты и (Б) подробный вид камеры впрыска. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 3: Концентрации во время инъекций. КонцентрацииCH4 в камере впрыска во время выбранного измерения показывают типичную реакцию после впрыска пробы. Выделенные области указывают на концентрации до и после закачки, учитываемые для расчетов. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
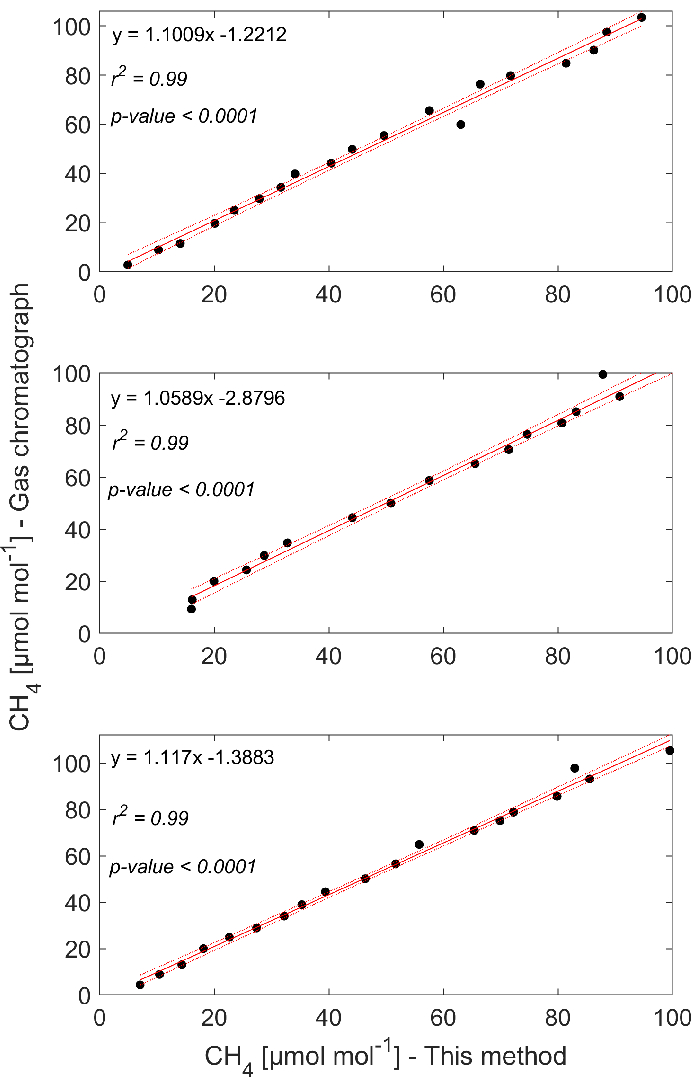
Рисунок 4: Сравнение измерений с помощью этого метода и хроматографии. Линейные зависимости между концентрациямиCH4 в свободном пространстве, определенными с помощью газовой хроматографии (GC-FID), и концентрациями, определенными этим методом для трех экспериментов, показали хорошие линейные аппроксимации (т.е. r2 > 0,98). Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.

Рисунок 5: Демонстрация сценария использования. Концентрация поровой воды на участках с преобладанием (A) Sagittaria lancifolia, и (B) смеси Sagittaria lancifolia и Typha latifolia. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этой цифры.
| Канальный4 стандартный [ppm] | GC [%] | Оптический анализатор [%] |
| 5 | 24.3 | 22.8 |
| 10 | 9.6 | 3.4 |
| 15 | 16.7 | 6.1 |
| 20 | 0.6 | 3.4 |
| 25 | 1 | 6 |
| 30 | 1.5 | 6.7 |
| 35 | 1.7 | 8 |
| 40 | 1.3 | 13.3 |
| 45 | 1.4 | 8.2 |
| 50 | 0.2 | 6.9 |
| 55 | 1.4 | 7.9 |
| 60 | 1.6 | 4.6 |
| 65 | 0.4 | 8.8 |
| 70 | 2.4 | 4.3 |
| 75 | 1.4 | 6.3 |
| 80 | 0.9 | 7 |
| 85 | 0.4 | 4.1 |
| 90 | 1.6 | 3.3 |
| 95 | 3.4 | 9 |
| 100 | 4.2 | 3.3 |
Таблица 1: Относительная погрешность (%). Измерения методом газовой хроматографии (ГХ) и оптического анализатора одного и того же контрольного стандартного флакона.
Обсуждение
Это исследование продемонстрировало применимость портативных газоанализаторов на основе оптической спектроскопии в сочетании с специально изготовленной камерой впрыска для анализа свободного пространства, созданного из проб воды. Демонстрация была сосредоточена наCH4, но протокол может быть применен для анализа других соответствующих парниковых газов, таких как CO2 и N2O8. Цель состояла в том, чтобы расширить предыдущие систематические оценки этих систем замкнутого цикла, которые представляют собой альтернативную аналитическую платформу традиционной газовой хроматографии в исследованиях по измерению концентрации парниковых газов.
Как и в случае с газовой хроматографией, в этом подходе крайне важно использовать стандарты проверки для обеспечения контроля качества и оценки в процессе анализа. Стандарты, проанализированные с помощью метода, были сопоставимы с эталонами стандартной хроматографии (рис. 4). Тем не менее, к основным предполагаемым преимуществам можно отнести отсутствие газов-носителей или частых процедур калибровки. Пользователи также могут запускать пробы сразу после отбора проб в полевых условиях, сокращая время, необходимое для микробного окисления реакционноспособных веществ, таких как CH4 , в пробах воды. Даже когда газ без выбросов парниковых газов для создания свободного пространства, необходимого для подготовки образцов, недоступен, пользователи все равно могут создать свободное пространство с использованием окружающего воздуха, предполагая, что концентрация в интересующей воде выше концентрации воздуха20. Существуют также очевидные недостатки, такие как время, необходимое для измерения больших наборов образцов. Несмотря на то, что анализ одного образца может занимать столько же времени, сколько и при использовании ГХ-ФИД, в оптических анализаторах не существует автоматизированных способов проведения инжекций, и для этого подхода требуется больше времени работы, чем для более устоявшихся систем ГХ-автоподатчиков.
Основное различие между этим подходом и другими системами с замкнутым контуром и встроенными отверстиями впрыска (например, 8) заключается в добавлении камеры впрыска. В нем пробы высокой концентрации могут быть разбавлены в рамках обычной операции во время анализа, избегая дополнительных этапов разбавления проб перед их впрыском в контур. На практике оператор может продолжать впрыскивание из свободного пространства в камеру вместо создания разведений для образцов с предполагаемыми высокими концентрациями. Объем камеры может быть изменен и увеличен для размещения образцов с высокой концентрацией или меньше для образцов с низкой концентрацией. Еще одним преимуществом данного метода по сравнению с другими системами замкнутого контура с поточным впрыском с точки зрения эффективности при анализе нескольких образцов является возможность стековых впрысков без промывки камеры сразу после каждого впрыска. Разбавление в камере впрыска позволило концентрации метана в контуре постоянно оставаться ниже 100 ppmCH4 во время тестируемого нами подхода с 20-уровневой закачкой, который в предыдущей работе был определен как порог концентрации в контуре, при котором точность анализаCH4 начинаетснижаться3.
В целом, этот метод подходит для анализа образцов в удаленных местах или в случаях, когда хроматографы, в том числе портативные21, невозможны или недоступны. Например, ученые, участвующие в полевых экспедициях в отдаленных местах, смогут определить фактические концентрации парниковых газов в водоемах и водных системах после выполнения некоторых простых шагов для создания пространства для анализа и принятия решений относительно приоритетов и потребностей отбора проб на месте, вместо того чтобы доставлять образцы обратно в лабораторию или полевую станцию, оснащенную хроматографом.
Раскрытие информации
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Эта работа финансировалась за счет наград Министерства энергетики DE-SC0021067, DE-SC0023084 и DE-SC0022972. Данные о концентрации поровых вод на участках отбора проб на болоте находятся в открытом доступе в архиве данных ESS-DIVE (https://data.ess-dive.lbl.gov/view/doi:10.15485/1997524 , по состоянию на 21 июня 2024 года)
Материалы
| Name | Company | Catalog Number | Comments |
| 1/4 in. I.D. x 3/8 in. O.D. Clear Vinyl Tubing | Home Depot | SKU # 702098 | Use to couple stopcocks and tubing connected to the instrument. Two short pieces (~4 cm). |
| 5/16 - 5/8 in. Stainless Steel Hose Clamp | Everbilt | 6260294 | Use to secure tubing connecting the stopcock valves and tubing connected to the instrument. |
| Crack-Resistant Teflon PFA Semi-Clear Tube for chemicals, 5/32" ID, 1/4" OD | McMaster-Carr | 51805K86 | Use to connect the injection chamber to the inlet and outlet ports of the instrument. We used two 0.68 m-long tubing in our experiment. |
| Drill with titanium step drillbit | Multiple companies | Use to drill the holes for septum and stopcocks in the jar's metallic lid. | |
| Gay butyl septum (stopper) | Weathon Microliter | 20-0025-B | Use as injection port and as vial septum (if compatible). |
| Headspace vials 20ml (23x75mm), Clear, Crimp Rounded Bottom | Restek | 21162 | Use to store the headspace sample. |
| Heavy Duty Steel Bond Epoxy GorillaWeld | Gorilla | 4330101 | Use to glue stopcock valves and septum to the jar's metallic lid. |
| Hypodermic Needles | Air-Tite Products Co. | N221 | Use to extract water from field vials, inject heaspace sample in vial and inject subsample to the injection chamber. |
| Mason jar (12 oz) | Ball, Kerr, Jarden | Larger or smaller chamber volumes can be chosen depending on sample concentrations. | |
| Optical spectroscopy-based gas analyzer | Multiple companies | Picarro G4301, Licor 7810, Licor 7820, ABB GLA131-GGA | These are some specific examples of analyzers that could be coupled to the injection chamber. We recognize that it is not an extensive list and other optical spectroscopy analyzers may also be suitable for the method. |
| Stopcock valve | DWK Life Sciences | 420163-0001 | Keep the valves open during normal operation. |
| Syringe (2.5 mL) | Air-Tite Products Co. | R2 | Use to extract subsamples from the headspace vials and inject them in the injecion chamber for analysis. |
| Syringe (30 mL) | Air-Tite Products Co. | R30HJ | Use to create headspace for gas analysis. |
Ссылки
- Bastviken, D., Tranvik, L. J., Downing, J. A., Crill, P. M., Enrich-Prast, A. Freshwater methane emissions offset the continental carbon sink. Science. 331 (6013), 50 (2011).
- Quick, A. M., et al. Nitrous oxide from streams and rivers: A review of primary biogeochemical pathways and environmental variables. Earth-Sci Rev. 191, 224-262 (2019).
- Bridgham, S. D., Cadillo-Quiroz, H., Keller, J. K., Zhuang, Q. Methane emissions from wetlands: biogeochemical, microbial, and modeling perspectives from local to global scales. Glob Chang Biol. 19 (5), 1325-1346 (2013).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- McAuliffe, C. Gas chromatographic determination of solutes by multiple phase equilibrium. Chem Technol. 1, 46-51 (1971).
- Hoyos Ossa, D. E., Gallego Rios, S. E., Rodríguez Loaiza, D. C., Peñuela, G. A. Implementation of an analytical method for the simultaneous determination of greenhouse gases in a reservoir using FID/µECD gas chromatography. Int J Environ Anal Chem. 103 (12), 2915-2929 (2023).
- Kittler, F., et al. Long-term drainage reduces CO2 uptake and CH4 emissions in a Siberian permafrost ecosystem. Glob Biogeochem Cycles. 31 (12), 1704-1717 (2017).
- Wilkinson, J., Bors, C., Burgis, F., Lorke, A., Bodmer, P. Measuring CO2 and CH4 with a portable gas analyzer: Closed-loop operation, optimization and assessment. PLoS One. 13 (4), e0193973 (2018).
- Villa, J. A., et al. Ebullition dominates methane fluxes from the water surface across different ecohydrological patches in a temperate freshwater marsh at the end of the growing season. Sci Tot Environ. 767, 144498 (2021).
- Holland, E. A., et al. Soil CO2, N2O and CH4 exchange. Std Soil Meth Long-Term Ecol Res. , 185-201 (1999).
- MacDonald, L. H., Paull, J. S., Jaffé, P. R. Enhanced semipermanent dialysis samplers for long-term environmental monitoring in saturated sediments. Environ Monitor Assess. 185 (5), 3613-3624 (2013).
- Villa, J. A., et al. Plant-mediated methane transport in emergent and floating-leaved species of a temperate freshwater mineral-soil wetland. Limnol Oceanography. 65, 1635-1650 (2020).
- Villa, J. A., et al. Methane and nitrous oxide porewater concentrations and surface fluxes of a regulated river. Sci Tot Environ. 715, 136920 (2020).
- Kampbell, D. H., Wilson, J. T., Vandegrift, S. A. Dissolved oxygen and methane in water by a GC headspace equilibration technique. Int J Environ Anal Chem. 36 (4), 249-257 (1989).
- Rochette, P., Bertrand, N. Soil air sample storage and handling using polypropylene syringes and glass vials. Canadian J Soil Sci. 83 (5), 631-637 (2003).
- Sander, R. Compilation of Henry's law constants (version 4.0) for water as solvent. Atmos Chem Phys. 15 (8), 4399-4981 (2015).
- Keller, J. K., Wolf, A. A., Weisenhorn, P. B., Drake, B. G., Megonigal, J. P. Elevated CO2 affects porewater chemistry in a brackish marsh. Biogeochemistry. 96 (1), 101-117 (2009).
- Comer-Warner, S. A., et al. Seasonal variability of sediment controls of carbon cycling in an agricultural stream. Sci Total Environ. 688, 732-741 (2019).
- U.S. Government Publishing Office. Title 42 - The Public Health and Wefare. U.S. Government Publishing Office. , (2009).
- Magen, C., et al. A simple headspace equilibration method for measuring dissolved methane. Limnol Oceanography Meth. 12 (9), 637-650 (2014).
- Regmi, B. P., Agah, M. Micro gas chromatography: An overview of critical components and their integration. Anal Chem. 90 (22), 13133-13150 (2018).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены
Мы используем файлы cookie для улучшения качества работы на нашем веб-сайте.
Продолжая пользоваться нашим веб-сайтом или нажимая кнопку «Продолжить», вы соглашаетесь принять наши файлы cookie.
