Method Article
подготовки и
В этой статье
Резюме
Этот протокол описывает получение и характеристика дендритного магнитно-резонансная томография (МРТ) контрастного агента, который несет Cyclen на основе макроциклических хелатов координирующие парамагнитные ионы гадолиния. В серии экспериментов МРТ в пробирке, этот агент произвел усиленный сигнал МРТ по сравнению с коммерчески доступным мономерного аналога.
Аннотация
Парамагнитные комплексы гадолиния (III) с ациклическими или макроциклических хелатов являются наиболее часто используемые контрастные вещества (КАС) для магнитно-резонансной томографии (МРТ). Их цель состоит в том, чтобы повысить скорость релаксации протонов воды в тканях, тем самым увеличивая MR контраст изображения и специфичность измерений МРТ. В настоящее время клинически апробирована контрастные агенты низкой молекулярной массой молекулы, которые быстро выводятся из организма. Использование дендримеров в качестве носителей парамагнитных энтеросорбенты могут играть важную роль в будущем развитии более эффективных MRI контрастных агентов. В частности, увеличение локальной концентрации парамагнитных результатов видов в более высокой контрастности сигнала. Кроме того, этот центр сертификации обеспечивает более длительное время удерживания ткани вследствие его высокой молекулярной массой и размером. Здесь мы демонстрируем удобную процедуру получения высокомолекулярных MRI контрастных агентов на основе поли (амидоамин) (ПАМАМ) дендримеров с monomacroциклические энтеросорбенты DOTA типа (DOTA - 1,4,7,10-тетраазациклодекана-1,4,7,10-тетраацетат). Устройство хелатирующий было приложено путем использования реакционной способности изотиоцианат (NCS) группы, к поверхности аминогруппами ПАМАМ-дендримера, с образованием тиомочевины мостов. Дендритные продукты очищают и анализируют с помощью спектроскопии ядерного магнитного резонанса, масс-спектрометрии и элементного анализа. И, наконец, высокое разрешение MR печатали изображения и сравнивали сигнал контрасты, полученные из подготовленного дендритный и коммерчески доступных мономерных агентов.
Введение
Магнитно-резонансная томография (МРТ) является мощным и неионизирующих метод визуализации широко используется в медико-биологических исследований и клинической диагностики благодаря своей неинвазивной природы и превосходной внутренней контраста мягких тканей. Наиболее часто используемые методы МРТ используют сигнал, полученный от протонов воды, обеспечивая изображения высокого разрешения и подробную информацию в тканях, основанных на различиях в плотности воды сигналов. Интенсивность сигнала и специфичность экспериментов МРТ может быть дополнительно улучшена с использованием контрастных агентов (КАН). Они являются парамагнитные или суперпарамагнитныо виды , которые влияют на продольную (Т 1) и поперечные (T 2) времена релаксации, соответственно 1,2.
Комплексы лантанидов иона гадолиния с полиаминокислоты лигандами поликарбоновых кислот являются наиболее часто используемыми T 1 центры сертификации. Гадолиния (III) укорачивает релаксации T 1Время протонов воды, тем самым увеличивая контраст сигнала в МРТ экспериментов 3. Тем не менее, ионная гадолиний токсичен; его размер приблизительно равен кальция (II), и это серьезно влияет на кальций-помощь сигнализации в клетках. Поэтому, ациклические и макроциклические хелаты используются для нейтрализации этой токсичности. Различные мультидентатные лиганды были разработаны до сих пор, что приводит к гадолиний (III) комплексов с высокой термодинамической устойчивостью и кинетической инертности 1. Те, которые основаны на 12-членных azamacrocycle циклена, в частности, его тетракарбоновой производное DOTA (1,4,7,10-тетраазациклодекана-1,4,7,10-тетраацетат) являются наиболее исследованные и прикладные комплексы этого класса СА.
Тем не менее, GdDOTA типа СА представляют собой системы с низким молекулярным весом, отображающие определенные недостатки, такие как низкая эффективность контраста и быстрой почечной экскреции. Макромолекулярные и многовалентного центры сертификации может быть хорошим решением 4 этих проблем. Так как CA biodistribuния в основном определяется их размерами, высокомолекулярные центры сертификации отображать гораздо более длительное время удерживания в тканях. Не менее важно то , что поливалентность этих агентов приводит к увеличению локальной концентрации мономерного MR зонда (например, GdDOTA комплекс), существенно улучшая полученного сигнала MR и качество измерений.
Дендримеров являются одними из наиболее предпочтительных подмостей для получения поливалентной КАС для МРТ 4,5. Эти высоко разветвленные макромолекулы с четко определенными размерами склонны к различным реакциям сочетания на их поверхности. В этой работе мы сообщаем о подготовке, очистку и характеристику дендритного CA для МРТ, состоящей из 4-го поколения (G4) поли (амидоамин) (ПАМАМ) дендример в сочетании с GdDOTA-как хелатов (DCA). Описаны синтез реакционно-способного производного DOTA и то его связь с ПАМАМ-дендримера. После комплексообразования с Gd (III), стандартной физико-химических характеристик процедуры, применяемыеповторное АКН была выполнена. Наконец, эксперименты были проведены МРТ, чтобы продемонстрировать способность DCA производить МР-изображений с более сильным контраст, чем полученные с низкой молекулярной массой УЦ.
протокол
1. Получение DCA
- Синтез мономерного звена 4 6.
- Синтез 4- (4-нитрофенил) -2- (4,7,10-три- трет-бутоксикарбонилметил 1,4,7,10-tetraazacyclododec-1-ил) бутановой кислоты трет - бутилового эфира (2).
- Растворите (4,7-бис - трет-бутоксикарбонилметил 1,4,7,10-тетрааза-cyclododec-1-ил) уксусной кислоты трет - бутилового эфира 1 (1,00 г, 1,94 ммоль) в N, N - диметилформамиде ( ДМФ, 5 мл), добавляют карбонат калия (0,67 г, 4,86 ммоль, 2,5 экв.) и перемешивали смесь при комнатной температуре в течение 45 мин.
Примечание: макроцикла 1 получали из циклена и трет - бутил эфир бромуксусной в соответствии с ранее опубликованным способом 7. - Добавить трет - бутил-2-бром-4- (4-нитрофенил) бутановой кислоты (0,87 г, 2,53 ммоль, 1,3 экв.) Порци ми в течение 1 ч. Продолжайте перемешивание смеси при тон же условия реакции для следующих 18 часов.
Примечание: Трет - бутиловый-2-бром-4- (4-нитрофенил) бутановой кислоты получают из 4- (4-нитрофенил) бутановой кислоты, тионилхлорид, и брома в соответствии с ранее опубликованным способом 8. - Удалить DMF с помощью лампы-к-колбы вакуумной перегонки при 40-60 ° C 9.
- Очищают остаток методом колоночной хроматографии (силикагель, 7% метанол / дихлорметан) с получением указанного продукта 2 в виде коричневого аморфного твердого вещества (1,09 г, 72%) 10.
- Растворите (4,7-бис - трет-бутоксикарбонилметил 1,4,7,10-тетрааза-cyclododec-1-ил) уксусной кислоты трет - бутилового эфира 1 (1,00 г, 1,94 ммоль) в N, N - диметилформамиде ( ДМФ, 5 мл), добавляют карбонат калия (0,67 г, 4,86 ммоль, 2,5 экв.) и перемешивали смесь при комнатной температуре в течение 45 мин.
- Синтез 4- (4-аминофенил) -2- (4,7,10-три- трет-бутоксикарбонилметил 1,4,7,10-tetraazacyclododec-1-ил) бутановой кислоты трет - бутилового эфира (3).
- Растворить производного нитробензола 2 (1,00 г, 1,28 ммоль) в этаноле (10 мл) и 7 н раствора аммиака в метаноле (150 мкл). Добавить палладий на активированном угле в качестве катализатора (Pd / C, 150 мг, 15% мас) до Solutiна.
- Взболтать гетерогенную смесь в течение 16 ч в атмосфере водорода (2,5 бара) в Hydrogenator аппарате Парра.
- Приготовьте торт кизельгура, приостановив его в этаноле и фильтрации суспензии через воронку из спеченного стекла. Налейте суспензии из 1.1.2.2 по подготовленной торт, чтобы удалить катализатор Pd / C фильтрованием.
- Растворитель удаляют путем осторожного перегонке на роторном испарителе (температура бани воды ~ 40 ° C) , чтобы получить соединение 3 в виде коричневого аморфного твердого вещества (0,91 г, 95%).
- Синтез 4- (4-изотиоцианатофенил) -2- (4,7,10-три- трет tetraazacyclododec-1-ил бутоксикарбонилметил-1,4,7,10-) трет - бутилового эфира бутановой кислоты (4).
- Добавить тиофосген (0,124 мл, 1,58 ммоль, 1,3 экв.) В смеси 3 (0,91 г, 1,22 ммоль) и триэтиламин (0,685 мл, 4,87 ммоль, 4 экв.) В дихлорметане (15 мл).
- Энергично размешайте ми реакцииxture с магнитной мешалкой при комнатной температуре в течение 16 ч.
- Растворитель удаляют путем осторожного перегонке на роторном испарителе (температура бани воды ~ 40 ° C), а затем очищают сырого продукта с помощью хроматографии на колонке (силикагель, 5% метанол / дихлорметан) с получением продукта 4 в виде светло - коричневого аморфного твердого вещества (0,51 г, 53%).
- Синтез 4- (4-нитрофенил) -2- (4,7,10-три- трет-бутоксикарбонилметил 1,4,7,10-tetraazacyclododec-1-ил) бутановой кислоты трет - бутилового эфира (2).
- Синтез дендримеров DCA.
- Синтез дендримера 5.
- Возьмем G4-ПАМАМ-дендримера (667 мг, 10% раствор дендримера в метаноле, 4,67 мкмоль), выпаривание метанола путем осторожного перегонке на роторном испарителе (температура воды в ванне ~ 40 ° C), и остаток растворяют в ДМФА (4 мл) ,
- Добавить триэтиламин (0,105 мл, 0,75 ммоль, 160 экв.), Перемешивают в течение 45 мин при 60 ° С, и добавляют изотиоцианат 4 (354 мг, 0,45 ммоль, 1,5 экв. По отношению к амино поверхностных групп дендримера) порционного Овег 1 ч.
- Реакционную смесь перемешивают с помощью магнитной мешалки при 45 ° C в течение 48 часов.
- Растворитель удаляют с помощью лампы-к-колбы вакуумной перегонки при 40-60 ° С.
- Очищают остаток с помощью эксклюзионной хроматографии с использованием липофильную среду гель-фильтрации и метанола в качестве элюента. Чтобы упаковать колонку, набухают фильтрующей среды в метаноле в течение не менее 3 ч при комнатной температуре (> 4 мл метанола на 1 г порошка) без применения давления. Выполнение гравитационного разделения путем сбора 1 мл фракции.
- Анализ собранных фракций тонкослойной хроматографии (ТСХ). Разработка пластины тонкослойной хроматограммы, в 15% метанол / дихлорметан (только наиболее полярное пятно расположено на базовой линии является производным от дендримерного продукта). Выпарить собранных фракций путем осторожного перегонке на роторном испарителе (температура бани воды ~ 40 ° C) , чтобы получить продукт 5 (270 мг, 91%).
- Синтез дендримера 6.
- Растворить защищенный дендритное хелатор 5 (270 мг, 4,23 мкмоль) в муравьиной кислоте (5 мл) и перемешивали смесь при 60 ° С в течение 24 ч.
- Упаривают муравьиной кислоты путем перегонки в роторном испарителе (~ 15 мбар давления, температуры водяной бани ~ 40 ° C) и подвергают сублимационной сушки продукта , чтобы дать 6 (давление ~ 0,2 мбар) 9.
- Синтез дендритного контрастного вещества (DCA)
- Растворите дендритное хелатор 6 (4,35 мкмоль) в воде и доведения рН до 7,0 с помощью гидроксида натрия 0,1 М.
- Растворите GDCL 3 · 6H 2 O (113 мг, 304 мкмоль) в воде (1 мл) и добавляют его по каплям к раствору хелатор 6 в течение периода 4 часов; поддерживать рН на уровне 7,0 с помощью водного раствора гидроксида натрия (0,05 М) путем измерения рН с помощью рН-метра.
- Перемешать смесь с помощью магнитной мешалки при комнатной темпера тура в течение 24 часов.
- Добавить этилендиаминтетрауксусную кислоту (ЭДТА, 158 мг, 426 мкмоль) в порционно раствор в течение 4 ч, чтобы удалить избыток Gd (III), при поддержании рН на уровне 7,0 с водным раствором гидроксида натрия (0,05 М). Смесь перемешивают при комнатной температуре в течение 24 ч.
- Выполнение эксклюзионной хроматографии для удаления большинства GdEDTA и избыток ЭДТА. Используйте гидрофильную среду гель-фильтрации набуханию в воде для упаковки колонки. Снизить смесь до подходящего объема и загрузить колонку. Элюируют колонку деионизированной воды без применения давления.
- Центрифуга образца с использованием центробежного блока фильтров 3 кД в течение 30 мин при центробежной силы 1,800 XG, чтобы удалить остатки GdEDTA и ЭДТА. Повторите этот шаг (около пяти раз) до тех пор, пока фильтрат не показывает отсутствие ЭДТА и GdEDTA. Переноса образца в колбу, испарить его, и затем подвергают сублимационной высушить растворитель с получением не совсем белого продукта в качестве окончательного DCA (186 мг, 71%).
ПРИМЕЧАНИЕ: Проверьте отсутствие ЭДТА и GdEDTA с помощью ESI-MS. - Подтвердите отсутствие Gd (III) в виде свободного иона с использованием тест ксиленол оранжевый. Растворите фильтрат (0,5 мл) в качестве ацетатный буферный раствор (рН 5,8). Добавьте несколько капель ксиленол оранжевого раствора и отслеживать изменение цвета (желтый или фиолетовый цвет указывает на отсутствие или наличие свободного Gd (III) ионов в растворе, соответственно) 11.
- Синтез дендримера 5.
2. In Vitro Характеристика дендритного продуктов
- Оценка числа макроциклических DOTA-единиц , соединенных с ПАМАМ - дендримера (загрузка с дендримером с DOTA-подобных макроциклов)
- Оценка с 1 H ЯМР (ЯМР - спектроскопии ядерного магнитного резонанса).
Примечание: Эта процедура возможна на дендримеров 5 и 6, но не на АКН.- Запись спектра 1 H ЯМР 12.
- Интеграция ароматическую область и двух отдельных алифатических областей (1. сигналы алифатической дендримера и макроциклических протонов; 2. сигналы т - Bu групп) , или просто алифатический область для дендримеров 5 и 6, соответственно.
Примечание: Там нет отдельного сигнала в алифатической области возник из Т - Bu групп в дендримера 6 , так как они были гидролизованы. - С помощью уравнения. 1 или уравнение. 2 для оценки числа макроциклических единиц (п), где R = отношение интегралов (алифатические / ароматические в уравнении. 1 или алифатического-дендример / Bu t- алифатические в уравнении. 2), H = dend число протонов в дендримера, H Ar = количество ароматических протонов, Н т Ви = число протонов в т - Bu групп и H = макинтош число протонов в одном макроцикла.
Примечание: В любом уравнение. 1 или уравнение. 2 может быть использован FOг дендример 5, в то время как только уравнения. 1 может быть использован для дендримера 6. Поскольку обмениваемые протоны (на амины, амиды, тиомочевины, или карбоксилаты), как правило, заменяются дейтерием, они не принимались в расчетах. Здесь H dend использовались = 1128 (на 5) или 1000 (для 6), H Ar = 4, и H = 27 макинтош. (1)
(1)  (2)
(2)
- Оценка с помощью элементного анализа, используя соотношение количества азота к сере.
- Выполните элементный анализ на твердом дендритного образце (DCA в этой работе).
- С помощью уравнения. 3 для оценки количества макроциклических единиц (п), где R = соотношение определяется% N и% S, N или S dend dend = числоазота или атомы серы в дендримера, и N или Макинтош S = макинтош число атомов азота или серы в одном макроциклических блоке.
Примечание: Коэффициент 2,29 получается из соотношения в атомных масс серы и азота. В этой работе были использованы N dend = 250, S dend = 2, N = 5 макинтош, и S = 1 макинтош. (3)
(3)
- Оценка с матрицей при содействии лазерного времени десорбции / ионизации полета (MALDI-TOF).
- Проведение анализа MALDI-TOF MS 13.
- Подсчитать количество макроциклических единиц (п) в соответствии с уравнением. 4, где М г = наблюдаемая масса (м / г), г = заряд вида, M = dend масса дендритного части, а М макинтош = масса одного макроциклического единицы.
НЕТTE: M dend = 14306 и М = макинтош 719 были использованы в данной работе.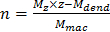 (4)
(4)
- Оценка с 1 H ЯМР (ЯМР - спектроскопии ядерного магнитного резонанса).
- Определение концентрации DCA ([DCA]): Bulk измерение магнитной восприимчивости (BMS)
- Растворите DCA (5-10 мг) в воде (360 мкл) в пластиковом флаконе трубки ([DCA] ~ 5-10 мМ).
Примечание: [DCA] должна находиться в диапазоне 5-10 мм , чтобы избежать возможного дублирования Т- BuOH резонансов при концентрации образца> 15 мм, с резонансом воды при & delta ; = 4,7 частей на миллион. - Добавьте 60 мкл D 2 O: t- смесь BuOH (2: 1 об / об) к водному раствору DCA и смешивают полученный раствор (420 мкл) с использованием вихревой мешалки.
- Передача 400 мкл образца в наружную ЯМР трубки и поместить коаксиальный ЯМР вставная измерительная трубка с t- BuOH: Н смесь 2 O (10:90 об / об) в пробирку для образца.
- запись1 Н - ЯМР - спектр и измерить сдвиг частоты между резонансных сигналов , вытекающих из Т- BuOH во внутренних и внешних трубок ЯМР (эталон) 12.
- С помощью уравнения. 5 для определения [DCA], где Т = абсолютная температура, Δχ = зарегистрированный сдвиг, ц эфф = эффективный магнитный момент для иона лантанида (М эфф = 7.94 для Gd (III) 14, и S = константа , зависящая от формы образца и его положение в магнитном поле (0, 1/3, и 1/6 в случае сферы, цилиндра, параллельной и цилиндра, перпендикулярной к магнитному полю, соответственно).
Примечание: Вычисленное значение , полученное для [DCA] должно быть скорректировано до исходной концентрации из - за добавления D 2 O: t- раствор BuOH (60 мкл).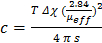 (5)
(5)
- Растворите DCA (5-10 мг) в воде (360 мкл) в пластиковом флаконе трубки ([DCA] ~ 5-10 мМ).
- Динамический светрассеяния (DLS) измерения.
- Приготовьте отфильтрованного раствора DCA (0,2 мкм политетрафторэтилена / PTFE фильтр, 0,75 мМ на Gd (III)), в 4- (2-гидроксиэтил) -1-пиперазинэтансульфонова кислота (HEPES) буфере (25 мМ, рН 7,4) и передать его в кювета для измерения DLS.
- Поместите кювету в DLS аппарата и установите следующие параметры: 5 повторений 15 сканирований (1 сканирование = 12 сек, показатель преломления = 1,345, поглощение = 1%), без задержек между сканирований и уравновешивания температуры 30 сек до записи ,
- Экспорт полученных данных и получить гистограмму распределения частиц по размерам, откладывая населения (%) в зависимости от размера (гидродинамический диаметр).
- Измерение продольной и поперечной relaxivities.
Примечание: Аналогичная процедура была описана уже с использованием анализатора времени релаксации 15; Эта процедура была выполнена с использованием 300 МГц ЯМР-спектрометр с Topspinпрограммного обеспечения.- Подготовить набор решений DCA в H 2 O: D 2 O (500 мкл, 10% D 2 O в H 2 O, [DCA] = 2,0, 2,5, 3,0, 3,5, 4,0, 4,5 и 5,0 мМ, [HEPES ] = 25 мМ) от DCA фондовой образца (смотри раздел 2.2).
- Передача 450 мкл раствора в ЯМР-трубки и поместить его в прибор.
- Оптимизация параметров измерения (длительность 90 ° импульс возбуждения (p1), и облучения сдвиг частоты (O 1)) , а затем выполнить Т 1 и Т 2 эксперименты с использованием восстановления инверсии (ИК) и автомобилей-Перселла-Meiboom-Gill (CPMG ) импульсных последовательностей, соответственно.
- Определение времени Т 1 и Т 2 релаксации.
- Выберите Записанная измерения, обрабатывать 2D-спектр в размерности F2, а также выполнять интерактивную коррекцию фазы.
- Выберите нужный фрагмент (пик с максимальной интенсивностью) в анализе / T 1 / T 2 окна релаксации, интегрировать его, а также экспортировать область к модулю релаксации.
- Выберите соответствующую функцию фитинга (invrec или uxnmrt2 для ИК и CPMG экспериментов соответственно) , чтобы получить времена релаксации T 1 или T 2.
- Повторите шаги 2.4.4.2-2.4.4.4 для всех остальных [DCA] решений.
- Расчет скорости релаксации (R 1 и R 2) из полученных значений T 1 (R 1,2 = 1 / T 1,2).
- Участок R 1 и R 2 (с -1) в зависимости от концентрации Gd (III) , в мм.
- Определить продольные и поперечные relaxivities, R 1 и R 2 (мм -1 с -1), из наклона подобранной линии, как определено формулой. 6, где R я, набл = продольная (я = 1) или поперечной (я = 2) диамагнитны скорость релаксациивода в отсутствие парамагнитных частиц и [Gd] = концентрации Gd (III), используемых в эксперименте.
 (6)
(6)
3. In Vitro МРТ; Сравнение между АКН и GdDOTA
- Подготовка труб фантомов
- Готовят водные растворы DCA (4 х 350 мкл) и GdDOTA (4 х 350 мкл), а также проб воды (4 х 350 мкл) для двух наборов экспериментов, в которых рассчитывается концентрация контрастных веществ: (3.1.1.1) в Б-г (III), или (3.1.1.2) на молекулу.
- Подготовить два образца DCA и два GdDOTA Образцы с концентрацией 0,5 и 1,0 мМ на Gd (III), соответственно. Кроме того, подготовить две пробы воды (в качестве контрольных трубок).
- Подготовить два образца DCA (2,5 и 5,0 мм в Б-га (III) или 0,05 и 0,1 мм в дендритного молекулы), два образца GdDOTA (0,25, 0,5 мм) и две пробы воды (CONTROл трубы).
Примечание: Соответствующие концентрации DCA и GdDOTA должны быть получены путем разбавления соответствующих образцов сырья с концентрацией определяемых с помощью метода BMS (смотри раздел 2.2) с HEPES буфера (рН 7,4). Для упрощения вычислений, п = 50 предполагалось, для среднего числа макроциклических звеньев на молекулу дендримера. Таким образом, отношение DCA: GdDOTA было 1: 5, рассчитанный на одну молекулу основе.
- Поместите образцы в 300 мкл пластиковый флакон пробирки, избегая наличие пузырьков воздуха в растворе.
Примечание: Размер пластиковых флаконах труб зависит от типа и размера катушки, используемой радиочастотная (здесь приведен пример с катушкой объема дается). - Вставьте образцы внутри шприца (60 мл объема), залейте его 1 мМ GdDOTA решение, и поместить его в сканер.
Примечание: Образцы помещали в водный раствор GdDOTA, чтобы избежать восприимчивости эффектов (вариации в поле с магнитнойtrength, которые происходят вблизи границы раздела между веществами различной магнитной восприимчивости).
- Готовят водные растворы DCA (4 х 350 мкл) и GdDOTA (4 х 350 мкл), а также проб воды (4 х 350 мкл) для двух наборов экспериментов, в которых рассчитывается концентрация контрастных веществ: (3.1.1.1) в Б-г (III), или (3.1.1.2) на молекулу.
- Оптимизация параметров и обработки изображений.
- Используйте анатомическое сканирование (локализатор / Tripilot), чтобы поместить шприц с образцами в изоцентру магнита.
- Нажмите светофор (настройка сканирования) для выполнения регулировок для подкладок (регулировка однородности магнитного поля) всего объема, центральная частота (O 1), усиление приемника (RG), а также усиления передачи (Tx0 и TX1).
- Для T 1 -weighted (T 1w) изображения, выберите способ быстрого низкий угол выстрела (FLASH).
- Выберите корональной кусочек для образцов, помещенных вертикально (шприц горизонтально) в сканер с помощью радиомаяка сканирования.
- С помощью уравнения. 7 для оптимизации контраста к шуму (CNR) приобретения параметров 16, где α = угол флип, TE = эхо времени, TR =время повторения, и T 1, A, T 1, B = Т 1 раз образца А (Т 1, А) и образца В (Т 1, B) , для которых CNR должен быть максимальным (то же самое справедливо для T 2 раза: T 2, а и Т 2, Б).
Примечание: Т 1 и Т 2 времена релаксации должны быть установлены в значения , полученные из измерений продольных и поперечных relaxivities (раздел 2.4), в то время как ТЕ, ТР, и α должны быть получены из расчета оптимизации CNR.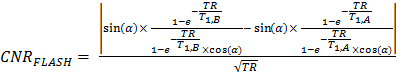 (7)
(7) - Приобретать изображение, используя параметры, полученные на предыдущем этапе (3.2.5).
- Вычислить отношение сигнал-шум (SNR).
- Загрузите приобретенный T 1w изображение (Сканирование) на дисплей и обработка изображенийокно и нажмите Определить области интереса (ROI).
- Выберите круглую ROI и нарисуйте его на позиции образца и фона. Затем нажмите на дисплее для получения средней амплитуды сигнала (S) сигнала и стандартного отклонения фона (S - шум).
- Повторите шаг 3.2.7.2 для АКН, GdDOTA и проб воды.
- Вычислить SNR , используя формулу: SNR = S сигнал / шум S.
- После слегка измененной процедуры выполнения T 2 -weighted (T 2W) изображений с помощью быстрого приобретения с (редком) методом улучшения релаксации. Для оптимизации параметров приобретения CNR, использовать уравнение. 8.
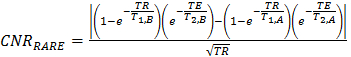 (8)
(8)
Результаты
Получение DCA состояла из двух этапов: 1) синтез мономерный DOTA типа хелатор (рисунок 1) и 2) сочетания комплексообразователя с G4 ПАМАМ - дендримера и последующей подготовки дендритного Gd (III) комплекса (Рисунок 2) , На первом этапе был подготовлен Циклен на основе DOTA типа хелатор, содержащий четыре карбоновых кислот и ортогональная группа пригодна для дальнейших синтетических модификаций. Подготовка началась с 1 (DO3A- - бутилового эфира трет) 7, которое алкилируют трет - бутил 2-бром-4- (4-нитрофенил) бутаноата 8 , чтобы обеспечить DOTA-производное 2. Палладий-катализируемое гидрирование уменьшило ароматическую нитрогруппы в 2 с получением анилина 3. Превращение 3 с тиофосгеном привело к изотиоцианата 4, whicч ранее был использован в качестве аминного-реактивного агента для получения дендритного УЦ 17.
На следующем этапе макроцикла 4 был использован в качестве основного мономерного звена в реакции сочетания с имеющейся в продаже G4 - ПАМАМ - дендримера. Поверхностные аминогруппами дендримера реагируют с изотиоцианатных группами мономера 4 в присутствии основания. Избыток 4 удаляли эксклюзионной хроматографии с использованием липофильную среду гель - фильтрации с помощью метанола в качестве элюента. Трет - бутиловый эфиры на полученной дендример-макроциклических конъюгата 5 гидролизуют с муравьиной кислотой с получением 6, которую затем подвергали лиофилизации и использовали на следующей стадии без дополнительной очистки. Формирование Gd (III) комплексов макроциклов DOTA типа проводили путем добавления GDCL 3 · 6H 2 O , к водному раствору OF 6 при поддержании рН на уровне около 7. Избыток Gd (III) , смешали с общим хелатор этилендиаминтетрауксусной кислоты (ЭДТА). GdEDTA комплекс и избыток ЭДТА были удалены из системы при помощи вытеснительной хроматографии с использованием гидрофильного среду гель-фильтрации с водой в качестве элюента. Остальные примеси малогабаритные были удалены из раствора центрифугированием, используя 3 кД единиц Центробежный фильтрации.
После синтеза дендример-макроцикл конъюгатов, комбинированный аналитический подход был применен для характеристики продуктов. Для определения поверхностного амина заполненность 5 и 6, были проанализированы Спектры 1 Н - ЯМР. Результаты сопоставлены и подтверждены с конечным продуктом (DCA), где нагрузка на дендример с макроциклов, был оценен с помощью элементного анализа и масс - спектрометрии MALDI-TOF (рис3). Сочетание этих трех методов привел к среднему значению из 49 макроциклических единиц, конъюгирован с G4 дендримера, что соответствует ~ 75% амина группа поверхности заселению.
Дальнейшая характеристика дендримерного комплекса включала в себя определение значений релаксивностью, что приводит к 6,2 ± 0,1 мМ -1 с -1 за Gd (III) (или примерно около 300 мм -1 с -1 на дендример) для продольной релаксивностью и 30,5 ± 0,6 мМ -1 с -1 за Gd (III) (почти 1500 мм - 1 с - 1 на дендример) для поперечной релаксивностью. DLS измерения показали , гидродинамический диаметр 7,2 ± 0,2 нм для DCA (рисунок 4).
И, наконец, чтобы продемонстрировать эффект дендримерного МРТ контрастного агента, МРТ проводили на двух наборах фантомах с DCA и клиникисоюзника доступны GdDOTA для сравнения (Рисунок 5). Первый набор фантомов были подготовлены с целью сравнения этих двух контрастных агентов при одинаковых концентрациях Gd (III), в то время как второй комплект был разработан, чтобы продемонстрировать эффект в сопоставимых концентрациях молекулу дендритных и мономерных контрастных агентов, соответственно.
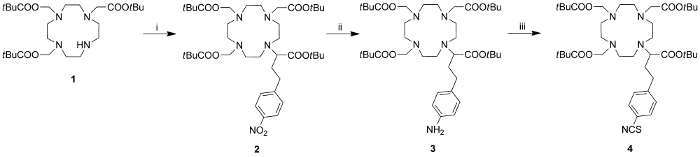
Рисунок 1: Синтез макроциклических DOTA типа хелатор 4. Реагенты, условия и изолированные выходы: (I) трет - бутил - 2-бром-4- (4-нитрофенил) бутановой кислоты, К 2 СО 3, ДМФА, 45 & deg ; С , 16 ч, 72%; (II) H 2, Pd / C, EtOH, РТ, 16 ч, 95%; (III) CSCL 2, Et 3 N, RT, 2 часа, 53%. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этого фи фигура.
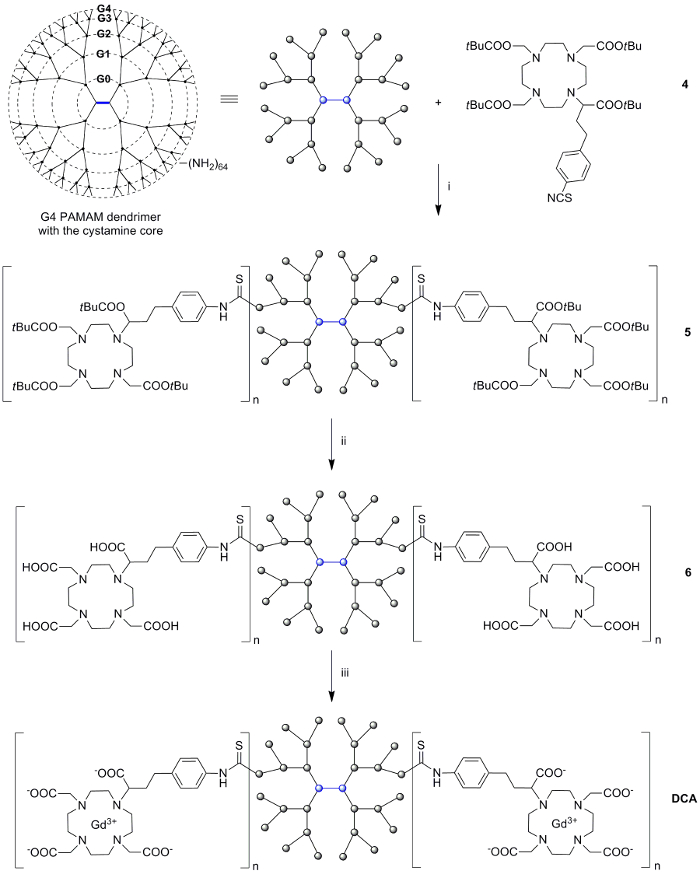
Рисунок 2: Синтез дендримерного МРТ контрастного вещества DCA Реагенты и условия: (I) 4, Et 3 N, ДМФА, 45 ° С, 48 ч, 91%;. (II) муравьиной кислоты, 60 ° С, 24 ч, колич; (III) GDCL 3 ∙ 6H 2 O, рН 7,0, RT, 24 часа в сутки, 71%. Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
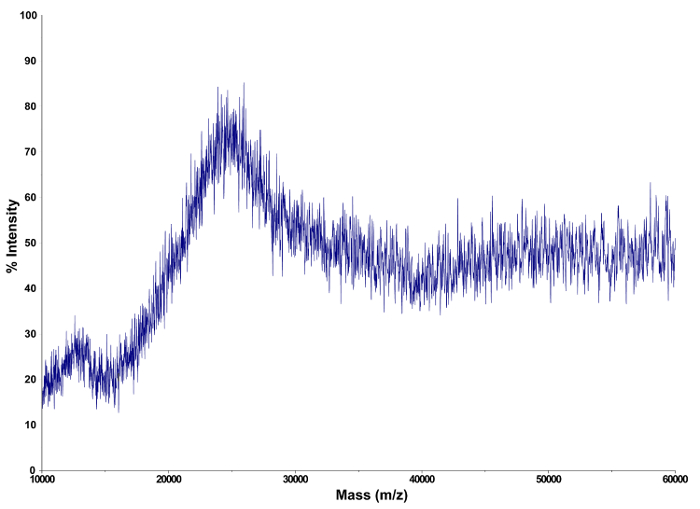
Рисунок 3:. Определение характеристик дендримерного продукта с помощью масс - спектрометрии MALDI-TOF Типичный масс - спектр MALDI-TOF , полученные для DCA.rget = "_blank"> Пожалуйста, нажмите здесь, чтобы посмотреть увеличенную версию этой фигуры.

Рис . 4:. Характеристика дендритного продукта с помощью динамического рассеяния света (DLS) измерения DLS АКН (HEPES, рН 7,4) Пожалуйста , нажмите здесь , чтобы посмотреть увеличенную версию этой фигуры.
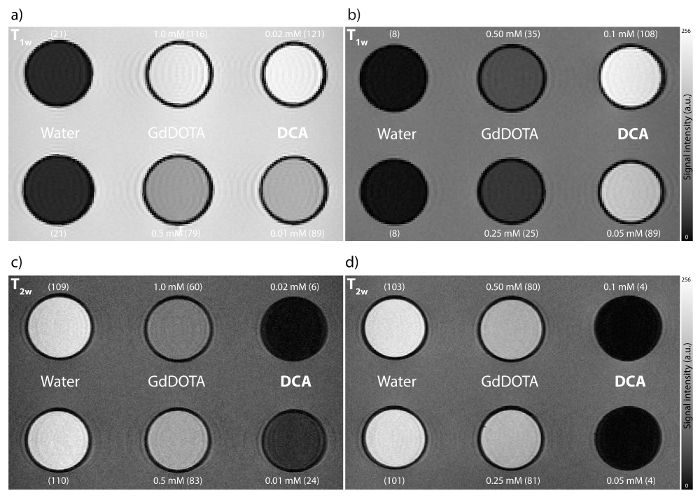
Рисунок 5: В пробирке МРТ эксперименты на фантомах трубки на 7 Т магнитного поля (а, Ь) Т 1 -weighted и (с, d) T 2 -weighted МРТ DCA и GdDOTA.. Каждый эксперимент МРТ проводили с две различные концентрации контрастного агента: (а, в) с сопоставимым Gd (III) , концентрации (HEPES, рН 7,4); (Б, г) с DCA: коэффициент концентрации GdDOTA 1: 5 (HEPES, рН 7,4). Концентрации выражены на молекулу, и значения SNR отображаются в скобках. Параметры , используемые в этих экспериментах были: поле-обзора (FOV) = 40 х 40 мм 2, толщина среза = 0,5 мм, число возбуждений (NEX) = 30; (А) размер матрицы (МТХ) = 256 х 256, время повторения (TR) = 100 мс, эхо времени (TE) = 2,95 мс, флип угол (FA) = 90 °, время приема (TA) = 12 мин 48 сек ; (Б) MTX = 256 х 256, TR / TE = 20 / 2,95 мс, FA = 90 °, TA = 2 мин 34 сек; (С) MTX = 512 х 512, TR / TE = 10000/130 мсек, Rare фактор (RF) = 16, ТП = 26 мин 40 сек; (D) MTX = 512 х 512, TR / TE = 10000/100 мсек, RF = 16, ТП = 26 мин 40 сек.776fig5large.jpg "целевых =" _blank "> Пожалуйста, нажмите здесь, чтобы посмотреть увеличенную версию этой фигуры.
Обсуждение
Подготовка дендритного МРТ контрастного агента требует соответствующего выбора мономерной единицы (т.е. хелатор для Gd (III)). Они снижают токсичность этого парамагнитного иона и, на сегодняшний день широкий спектр ациклических и макроциклических энтеросорбенты Этой цели служат 1-3. Среди них, макроциклические комплексоны DOTA типа обладают самой высокой термодинамической стабильностью и кинетической инертностью и, следовательно, являются наиболее предпочтительным выбором для приготовления инертны MRI контрастных агентов 1,18. Кроме того, они склонны к различным синтетическим преобразований, которые приводят к бифункциональных комплексонов, способных св зыватьс различными функциональными молекулами (например, адресные переносчики или нанометровых носителей), все еще образуя стабильный Gd (III) , комплексы 19. С этой целью, DOTA-типа мономерное звено описанный в этой процедуре , был получен из DO3A- трет - бутилового эфира, общей и легкодоступной предшественника, а также производное бромидом4- (4-нитрофенил) бутановой кислоты. Эта молекула является производным от DOTA и обладает аналогичную структуру для координации Gd (III). Синтетический модификация стремится сделать этот Хелатор склонны к реакции на соединения различных функциональных молекул и носителей. А именно, при подготовке DOTA-модифицированных результатов молекулы в хелатор еще с четырьмя карбоксильных групп, доступных координации по отношению к Б-гу за (III) с образованием комплекса и инертный ортогональный нитрофенильную группу, которая при преобразовании крепит этот хелатор к поверхности дендримера. Эта процедура также обеспечивает гибкость в выборе ортогонального реактивной группы (например, NH 2 или СООН), которые могут служить для соединения Gd (III) хелатор на желаемый носитель предпочтительным образом.
Полученный бифункциональный хелатор может быть соединен с другими молекулами , двумя различными способами (т.е. синтетических процедур). Когда нитрогруппу восстанавливают до аминогруппы, полученный анилин может подидут реакции конденсации с карбоксильной группой другой молекулы 8. Кроме того, ароматический первичный амин функциональную группу , в присутствии тиофосгеном может быть легко превращена в изотиоцианат, группа , которая легко вступает в реакцию с аминами в полярных органических растворителях, а также воды, предлагая больше возможностей реакции для связывания мономерных единиц до дендримеров 17 , 20,21.
Для связывания бифункциональный хелатор на дендримерного носитель, соответствующий дендритный подмости должны быть выбраны. Несколько факторов, связанных с окончательной дендример сопряженной структуры и требуемое приложение должно быть учтено в этом шаге. Благодаря широкой коммерческой доступности дендритных носителей, продуктов с различными структурами, основными поверхностно-реактивных групп или поколений можно выбрать. Следовательно, реакции конъюгации будет зависеть от поверхностной группы дендримера и ортогональной группы хелатообразующего агента, в то время какОкончательный конъюгат может быть нейтральным, заряжена, или имеют различные размеры (до 15-20 нм, в зависимости от поколения дендримера) 22. Все эти аспекты должны быть приняты во внимание до подготовки дендритное СА, так как они могут влиять на растворимость, релаксивность (усиление сигнала МРТ), диффузии и другие фармакокинетические свойства контрастного вещества, которое потенциально может поставить под угрозу его применение в МРТ. Например, катионные дендримеры могут проявлять токсичность в биологических системах. Тем не менее, этот эффект может быть уменьшен путем конъюгации отрицательно заряженных групп на поверхности дендримера, тем самым снижая их общий положительный заряд 23.
В этом протоколе, мы приготовили дендритное контрастный агент АКН с использованием процедуры , в которой изотиоцианат группа мономерной макроцикла 4, соединенный с коммерческим цистамин сердечником G4-ПАМАМ оборудованного 64 первичной поверхности аминных групп. Первоначальная очистка hydrophOBIC дендритный продукт 5 проводили с помощью гель - хроматографии с использованием колонки с липофильной среды для гель - фильтрации и метанола в качестве элюента , с тем , чтобы удалить большую часть непрореагировавших мономерных звеньев. Гидролиз трет - бутилового эфиров муравьиной кислотой проста, что приводит к водорастворимого дендритного продукт , который может быть очищен с вытеснительной хроматографии с использованием гидрофильной гель - фильтрационной среды. Комплексообразование Мультимерные и дендритных комплексонов с Gd (III) была выполнена при сохранении раствора при нейтральном рН для того, чтобы облегчить образование комплекса. В противном случае, комплексообразование Gd (III), (добавлен в виде соли хлорида) снижает рН, замедление реакции. Наконец, следует отметить, что аминогруппы в ядре дендримера также, как правило, координировать свои действия с Gd (III), но только с избытком, что не может быть хелатной с единицами DOTA. Как избежать присутствия Gd (III) за пределами хелатор DOTA имеет важное значение, так как леakage Б-га (III) из СА может иметь нежелательные последствия; а именно, он может вызвать токсичность в естественных условиях 18. Избыток Gd (III) могут быть эффективно удалены путем комплексообразования с ЭДТА с последующей ультрафильтрации GdEDTA и свободного ЭДТА с использованием 3 кДа молекулярную массу среза (MWCO) фильтры. Более низкие фильтры MWCO могут быть использованы при дендримерного конъюгаты имеют более низкие молекулярные массы.
Есть два основных вопроса по устранению неполадок, связанных с подготовкой АКН. Из-за большого эффекта расширения Gd (III) по сигналам ЯМР, анализ DCA с помощью ЯМР-спектроскопии не информативен. Вместо этого, этот анализ следует проводить в более ранних этапах (соединений 5 и 6). Далее, конъюгация monomacrocyclic единиц на поверхности дендримера никогда не достигается при 100% -ной конверсии, но это, вероятно, будет между 50-90% (см ниже). Как правило, выходы реакции может быть увеличена путем добавления второй части monomeriС - реактивный блок после первого сопряжения дендримера и мономерной единицы завершена 24. Тем не менее, каждый препарат периодического действия приводит к несколько различным средним числом энтеросорбенты, конъюгированных на поверхности дендримера, даже при одинаковых дендримеров и DOTA единицы используются в качестве материалов для сцепления. Несмотря на то, конечное количество Gd (III), присутствующее в DCA может быть определено независимо друг от друга с помощью метода BMS (смотри раздел 2.2), для лучшего определения характеристик дендримерных конъюгатов, необходимо выполнить оценку связанных мономерных единиц каждый раз, когда новая партия DCA подготовлен (см 2.1 и обсуждение ниже).
Аналитическую характеристику выделенных дендритных продуктов может быть осуществлено с помощью 1 Н - ЯМР - спектроскопии (только на продукты 5 и 6), элементного анализа и MALDI-TOF MS. Типичные выходы для конверсии поверхностных аминогрупп лежат между 50-90%, в зависимости от дендримером generatiна, типа хелатор и реакционных условий , используемых (растворитель и температура) 6,20,24,25. В данном конкретном случае, расчетные массы , полученные из комбинированных анализов соответствуют в среднем на 49 мономерных хелатов соединен с дендримером (т.е. ~ 75% заполненности дендримером поверхностных аминов). Хотя небольшое несоответствие в конечном количестве прореагировавших аминогрупп можно было бы ожидать от этих методик 25, их непосредственное сравнение дает разумные доказательства для формирования желаемой DCA с определенным средним количеством присоединенных хелатных единиц.
Характеристика в пробирке с целью оценить потенциал DCA для повышения контрастности в экспериментах МРТ состоял из DLS, relaxometric и экспериментов МРТ. Гидродинамический диаметр АКН было определено, что 7,2 ± 0,2 нм путем измерения DLS, что согласуется с ранее сообщенных конъюгатов такого родас 4 поколения G4 ПАМАМ дендримеров 26. Определение продольного релаксивностью АКН следуют ранее описанной процедуры 15 и показал значение 6,2 ± 0,1 мм - 1 с - 1 в Gd (III). Около 50% повышения в R 1 парамагнитного Gd (III) в АКН по отношению к молекулам малоразмерных подобного типа (например, GdDOTA) можно объяснить с промежуточным размером дендритного контрастного агента. А именно, восстановленное движение Gd-хелатов прикрепленным к поверхности дендримера увеличивает время вращательной корреляции и, следовательно, R 1; этот эффект все еще может наблюдаться при больших магнитных полях для меньших наноразмерных агентов. В противном случае, увеличение времени вращательной корреляции доминантно способствует повышению R 1 при низких магнитных полей 27. С другой стороны, размер дендримерного контрастного вещества имели выраженный эффект на поперечную отноxivity 28, что приводит к значению 30,5 ± 0,6 мм - 1 с - 1 в Gd (III). Таким образом, методы оценки в пробирке DCA просты и требуют только тщательной подготовки образца, поэтому никаких трудностей не ожидается при получении данных и анализа результатов.
Чтобы продемонстрировать производительность дендритного контрастного агента и его способность влиять на контраст изображения, мы провели эксперименты на МРТ трубчатых фантомов с недавно подготовленной контрастного вещества DCA. Мы также использовали раствор коммерчески доступного и клинически апробирована MRI контрастного агента, GdDOTA, как сравнение и труб с водой в качестве контроля. В первом T 1 -weighted МРТ эксперимента, когда использовались равными (III) концентрации Gd (0,5 или 1 мМ Gd (III) , в АКН или GdDOTA), ОСШ в трубах с DCA было уже до 12% из - за более высокой на увеличение примерно на 50% в продольном релаксивностью АКН по сравнению с GdDOTA (Figure 5а). Второй Т 1 -weighted эксперимент МРТ был разработан , чтобы продемонстрировать эффект DCA , когда концентрации были рассчитаны на молекулу. Несмотря на то, в 5 раз меньше АКН наносили по сравнению с GdDOTA (50 против 250 мкМ или 100 мкМ против 500 АКН против GdDOTA соответственно), высокой загрузке DCA с Gd (III), привело к существенному приросту контрастности изображения, что в свою очередь привело к наблюдаемым значениям SNR, по меньшей мере в три раза выше в фантомных трубок, заполненных DCA. Ожидаемо, как Т - 2 -weighted МРТ эксперименты выставлены большие (3-20 раз) различия в SNR между пунктирными трубок , заполненных DCA и GdDOTA.
В заключение, этот протокол описывает удобную подготовку дендритного CA для МРТ с использованием общих методик синтеза, чтобы обеспечить DCA с улучшенными свойствами по сравнению с малогабаритной центров сертификации. DCA проявляет предпочтительными термодинамической стабильностью и кинетическую инертность по сравнениюего мономерных аналогов СА. Тем не менее, поливалентность АКН и, следовательно, высокая локальная концентрация парамагнитных в целевом регионе вызывает высокий контраст в МР-изображений. Учитывая часто предпочтительные фармакокинетические свойства (например, больше ткани время удерживания) по сравнению с их мономерными аналогами CA, или способность выполнять дополнительные функциональные возможности (например, целевые векторы), эти дендримерные-макроцикл конъюгаты представляют собой перспективный и ценный класс контрастных агентов для различное будущее МРТ и приложения молекулярной визуализации.
Раскрытие информации
The authors have nothing to disclose.
Благодарности
The financial support of the Max-Planck Society, the Turkish Ministry of National Education (PhD fellowship to S. G.), and the German Exchange Academic Service (DAAD, PhD fellowship to T. S.) are gratefully acknowledged.
Материалы
| Name | Company | Catalog Number | Comments |
| Cyclen | CheMatech | C002 | |
| tert-Butyl bromoacetate | Alfa Aesar | A14917 | |
| N,N-Dimethylformamide | Fluka | 40248 | |
| Potassium carbonate | Sigma-Aldrich | 209619 | |
| 4-(4-Nitrophenyl)butryic acid | Aldrich | 335339 | |
| Thionyl chloride | Acros Organics | 382662500 | Note: Corrosive substance; toxic if inhaled |
| Bromine | Acros Organics | 402841000 | Note: causes severe skin burns, fatal if inhaled |
| Diethyl ether | any source | ||
| Sodium sulphate | Acros Organics | 196640010 | |
| Chloroform | VWR Chemicals | 22711.29 | |
| tert-Butyl 2,2,2-trichloroacetimidate | Aldrich | 364789 | Note: flammable substance; irritrant to skin and eyes |
| Boron trifluoride etherate | Acros Organics | 174560250 | 48% BF3. Note: Flammable substance; causes skin burns, fatal if inhaled |
| Sodium bicarbonate | Acros Organics | 424270010 | |
| Ethyl-acetate | any source | For column chromatography | |
| n-Hexane | any source | For column chromatography | |
| Bulb-to-bulb (Kugelrohr) distillation apparatus | Büchi | Model type: Glass oven B-585 | |
| Silicagel | Carl Roth GmbH | P090.2 | |
| Methanol | any source | For column chromatography | |
| Dichloromethane | any source | For column chromatography | |
| Ethanol | VWR Chemicals | 20821.296 | |
| Ammonia | Acros Organics | 428381000 | 7 N Solution in Methanol |
| Palladium | Aldrich | 643181 | 15% wet |
| Hydrogenation apparatus PARR | PARR Instrument Company | ||
| Celite 503 | Aldrich | 22151 | |
| Sintered glass funnel | any source | ||
| Thiophosgen | Aldrich | 115150 | Note: irritrant to skin; toxic if inhaled |
| Triethylamine | Alfa Aesar | A12646 | |
| Dichloromethane | Acros Organics | 348460010 | Extra dry |
| Magnetic stirrer | any source | ||
| PAMAM G4 Dendrimer | Andrews ChemService | AuCS - 297 | 10% wt. solution in MeOH |
| Lipophylic Sephadex LH-20 | Sigma | LH20100 | |
| Thin-layer chromatography plates | Merck Millipore | 1.05554.0001 | |
| Formic acid | VWR Chemicals | 20318.297 | |
| Lophylizer | any source | ||
| Gadollinium(III) chloride hexahydrate | Aldrich | G7532 | |
| Sodium hydroxide | Acros Organics | 134070010 | |
| pH meter | any source | ||
| Ethylenediaminetetraacetic acid disodium salt dihydrate | Aldrich | E5134 | |
| Mass spectrometer (ESI) | Agilent | Ion trap SL 1100 | |
| Acetate buffer | any source | pH 5.8 | |
| Xylenol orange | Aldrich | 52097 | 20 μM in acetate buffer |
| Hydrophylic Sephadex G-15 | GE Healthcare | 17-0020-01 | |
| Amicon Ultra-15 Centrifugal Filter Unit | Merck Millipore | UFC900324 | Ultracel-3 membrane (MWCO 3000) |
| Centrifuge | any source | ||
| NMR spectrometer | Bruker | Avance III 300 MHz | |
| Topspin | Bruker | Version 2.1 | |
| Combustion analysis instrument | EuroVector SpA | EuroEA 3000 Elemental Analyser | |
| MALDI-ToF MS instrument | Applied Biosystems | Voyager-STR | |
| Deuteriumoxid | Carl Roth GmbH | 6672.3 | |
| tert-Butyl alcohol | Carl Roth GmbH | AE16.1 | |
| Vortex mixer | any source | ||
| Norell NMR tubes | Deutero GmbH | 507-HP-7 | |
| NMR coaxial tube | Deutero GmbH | coaxialb-5-7 | |
| DLS instrument | Malvern | Zetasizer Nano ZS | |
| 0.20 μm PTFE filter | Carl Roth GmbH | KC94.1 | |
| HEPES | Fisher BioReagents | BP310 | |
| Plastic tube vials | any source | ||
| Dotarem | Guerbet | NDC 67684-2000-1 | |
| MRI scanner | Bruker | BioSpec 70/30 USR magnet (7 T). Note: potential hazards related to high magnetic fields | |
| RF coil | Bruker | Dual frequency volume coil (RF RES 300 1H/19F 075/040 LIN/LIN TR) | |
| Paravision (software) | Bruker | Version 5.1 |
Ссылки
- Merbach, A. E., Helm, L., Tóth, É The chemistry of contrast agents in medical magnetic resonance imaging. 2nd ed. , Wiley. (2013).
- Geraldes, C. F. G. C., Laurent, S. Classification and basic properties of contrast agents for magnetic resonance imaging. Contrast Media Mol. Imaging. 4 (1), 1-23 (2009).
- Caravan, P., Ellison, J. J., McMurry, T. J., Lauffer, R. B. Gadolinium(III) chelates as MRI contrast agents: Structure, dynamics, and applications. Chem. Rev. 99 (9), 2293-2352 (1999).
- Villaraza, A. J. L., Bumb, A., Brechbiel, M. W. Macromolecules, Dendrimers, and Nanomaterials in Magnetic Resonance Imaging: The Interplay between Size, Function, and Pharmacokinetics. Chem. Rev. 110 (5), 2921-2959 (2010).
- Langereis, S., Dirksen, A., Hackeng, T. M., van Genderen, M. H. P., Meijer, E. W. Dendrimers and magnetic resonance imaging. New J. Chem. 31 (7), 1152-1160 (2007).
- Gündüz, S., Power, A., Maier, M. E., Logothetis, N. K., Angelovski, G. Synthesis and Characterization of a Biotinylated Multivalent Targeted Contrast Agent. ChemPlusChem. 80 (3), 612-622 (2015).
- Pope, S. J. A., Kenwright, A. M., Heath, S. L., Faulkner, S. Synthesis and luminescence properties of a kinetically stable dinuclear ytterbium complex with differentiated binding sites. Chem. Commun. (13), 1550-1551 (2003).
- Vibhute, S. M., et al. Synthesis and characterization of pH-sensitive, biotinylated MRI contrast agents and their conjugates with avidin. Org. Biomol. Chem. 11 (8), 1294-1305 (2013).
- Vogel, A. I., Furniss, B. S. Vogel's textbook of practical organic chemistry. 5th ed. , Longman. (1989).
- Lundanes, E., Reubsaet, L., Greibrokk, T. Chromatography : basic principles, sample preparations and related methods. , Wiley-VCH. (2013).
- Barge, A., Cravotto, G., Gianolio, E., Fedeli, F. How to determine free Gd and free ligand in solution of Gd chelates. A technical note. Contrast Media Mol. Imaging. 1 (5), 184-188 (2006).
- Keeler, J. Understanding NMR spectroscopy. 2nd ed. , Wiley. (2010).
- Hillenkamp, F., Peter-Katalinić, J. MALDI MS : a practical guide to instrumentation, methods and applications. , Wiley-VCH. (2007).
- Peters, J. A., Huskens, J., Raber, D. J. Lanthanide induced shifts and relaxation rate enhancements. Prog. Nucl. Magn. Reson. Spectrosc. 28, 283-350 (1996).
- Averill, D. J., Garcia, J., Siriwardena-Mahanama, B. N., Vithanarachchi, S. M., Allen, M. J. Preparation, Purification, and Characterization of Lanthanide Complexes for Use as Contrast Agents for Magnetic Resonance Imaging. J. Vis. Exp. (53), e2844(2011).
- Hagberg, G. E., Scheffler, K. Effect of r1 and r2 relaxivity of gadolinium-based contrast agents on the T1-weighted MR signal at increasing magnetic field strengths. Contrast Media Mol. Imaging. 8 (6), 456-465 (2013).
- Boswell, C. A., et al. Synthesis, characterization, and biological evaluation of integrin alpha(v)beta(3)-targeted PAMAM dendrimers. Mol. Pharmaceut. 5 (4), 527-539 (2008).
- Sherry, A. D., Caravan, P., Lenkinski, R. E. Primer on Gadolinium Chemistry. J. Magn. Reson. Imaging. 30 (6), 1240-1248 (2009).
- Cakić, N., Gündüz, S., Rengarasu, R., Angelovski, G. Synthetic strategies for preparation of cyclen-based MRI contrast agents. Tetrahedron Lett. 56 (6), 759-765 (2015).
- Polasek, M., Hermann, P., Peters, J. A., Geraldes, C. F. G. C., Lukes, I. PAMAM Dendrimers Conjugated with an Uncharged Gadolinium(III) Chelate with a Fast Water Exchange: The Influence of Chelate Charge on Rotational Dynamics. Bioconjugate Chem. 20 (11), 2142-2153 (2009).
- Ali, M. M., et al. Synthesis and relaxometric studies of a dendrimer-based pH-responsive MRI contrast agent. Chem. Eur. J. 14 (24), 7250-7258 (2008).
- Jackson, C. L., et al. Visualization of dendrimer molecules by transmission electron microscopy (TEM): Staining methods and Cryo-TEM of vitrified solutions. Macromolecules. 31 (18), 6259-6265 (1998).
- Jain, K., Kesharwani, P., Gupta, U., Jain, N. K. Dendrimer toxicity: Let's meet the challenge. Int. J. Pharm. 394 (1-2), 122-142 (2010).
- Rudovsky, J., et al. PAMAM dendrimeric conjugates with a Gd-DOTA phosphinate derivative and their adducts with polyaminoacids: The interplay of global motion, internal rotation, and fast water exchange. Bioconjugate Chem. 17 (4), 975-987 (2006).
- Xu, H., et al. Toward improved syntheses of dendrimer-based magnetic resonance imaging contrast agents: New bifunctional diethylenetriaminepentaacetic acid ligands and nonaqueous conjugation chemistry. J. Med. Chem. 50 (14), 3185-3193 (2007).
- Nwe, K., Bryant, L. H., Brechbiel, M. W. Poly(amidoamine) Dendrimer Based MRI Contrast Agents Exhibiting Enhanced Relaxivities Derived via Metal Preligation Techniques. Bioconjugate Chem. 21 (6), 1014-1017 (2010).
- Livramento, J. B., et al. First in vivo MRI assessment of a self-assembled metallostar compound endowed with a remarkable high field relaxivity. Contrast Media Mol. Imaging. 1 (1), 30-39 (2006).
- Norek, M., Kampert, E., Zeitler, U., Peters, J. A. Tuning of the Size of Dy2O3 Nanoparticles for Optimal Performance as an MRI Contrast Agent. J. Am. Chem. Soc. 130 (15), 5335-5340 (2008).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены