Method Article
Ultrassom no local de atendimento para oxigenação periférica por membrana extracorpórea veno-arterial sem ventilação ventricular esquerda
Neste Artigo
Resumo
Este protocolo descreve o uso de ultrassom point-of-care (POCUS) para monitorar pacientes em oxigenação por membrana extracorpórea veno-arterial periférica (ECMO VA) sem ventilação ventricular esquerda. Ele avalia a distensão ventricular esquerda, trombo intracardíaco ou da raiz da aorta e identifica parâmetros POCUS cardíacos úteis para o desmame da ECMO VA.
Resumo
Nas últimas décadas, a oxigenação por membrana extracorpórea veno-arterial (V-A ECMO) tornou-se uma ferramenta crítica no tratamento de pacientes com choque cardiogênico grave e insuficiência cardiopulmonar. Devido à instabilidade inerente a esses pacientes, seu transporte para fora das unidades de terapia intensiva é repleto de riscos. Como resultado, as ferramentas de diagnóstico à beira do leito são essenciais para seus cuidados diários. Uma dessas ferramentas é o ultrassom point-of-care (POCUS) do coração, que pode avaliar de forma não invasiva vários parâmetros: desempenho do ventrículo esquerdo (VE) (tamanho, função sistólica, volume sistólico, abertura da válvula aórtica), desempenho do ventrículo direito (VD) (tamanho, função sistólica) e presença de trombo intracardíaco. Além disso, o POCUS pode ajudar a avaliar a prontidão para o desmame da ECMO VA e eventual decanulação. Apesar de seu potencial, o uso de POCUS no contexto da ECMO V-A permanece inconsistente devido à variabilidade no treinamento do provedor. Este estudo visa preencher essa lacuna detalhando a aquisição de imagens POCUS na ECMO VA, particularmente na ausência de ventilação do VE. Abrange aspectos-chave, como posicionamento do paciente, seleção do transdutor, posicionamento da sonda, sequência de aquisição e otimização da imagem.
Introdução
A oxigenação por membrana extracorpórea (ECMO) é uma estratégia de contemporização potencialmente salvadora de vidas para os pacientes, que tem visto uma taxa de utilização cada vez maior 1,2. A ECMO tem duas configurações diferentes: veno-venosa (V-V) e veno-arterial (V-A). Nas últimas décadas, a ECMO V-A emergiu como uma ferramenta fundamental no cuidado de pacientes com choque cardiogênico grave e insuficiência cardiopulmonar 3,4,5,6. As duas estratégias de canulação para ECMO V-A são central e periférica7. A ECMO V-A central geralmente requer esternotomia para canulação direta do átrio direito para drenagem venosa e aorta proximal para retorno arterial anterógrado. Por outro lado, a ECMO periférica V-A tem retorno arterial através da artéria femoral por meio de um mecanismo retrógrado. Esse fluxo retrógrado pode causar os seguintes problemas: oxigenação diferencial da parte superior e inferior do corpo, piora da função biventricular e distensão do VE, principalmente se não houver uma estratégia para descarregar o VE8. Essas complicações da ECMO periférica V-A, além dos riscos inerentes à ECMO, requerem monitoramento frequente e vigilante 9,10,11. Devido à instabilidade inerente a esses pacientes, não é prático transferi-los frequentemente para fora da unidade de terapia intensiva (UTI) para testes diagnósticos e avaliação de seu suporte circulatório mecânico e evolução do estado cardiopulmonar 3,6. Portanto, as ferramentas de diagnóstico à beira do leito são essenciais em seus cuidados diários. Uma dessas ferramentas é o ultrassom point-of-care (POCUS)12,13,14,15 do coração, que pode ser usado para avaliar todos os seguintes aspectos de forma não invasiva: desempenho do ventrículo esquerdo (VE) (tamanho, função sistólica, volume sistólico, abertura da valva aórtica)3,13,14,16,17,18,19 , desempenho do ventrículo direito (VD) (tamanho, função sistólica)20,21 e presença versus ausência de trombo intracardíaco10,11. Além disso, o POCUS pode ser usado para avaliar a prontidão para o desmame da ECMO V-A e eventual decanulação 22,23,24,25,26,27,28.
A ultrassonografia diagnóstica geralmente se enquadra em duas categorias: no local de atendimento e consultiva29,30 A ultrassonografia consultiva é um exame solicitado pelo provedor de tratamento primário de um paciente, mas realizado por uma equipe especializada separada29,30, enquanto o ultrassom de ponto de atendimento é realizado e interpretado pelo provedor de tratamento primário de um paciente 29,30,31. Embora a avaliação ultrassonográfica do coração na ECMO VA tenha sido tradicionalmente realizada por meio de serviços consultivos, esses serviços nem sempre estão imediatamente disponíveis 24 horas por dia para atender às necessidades ultrassonográficas imprevisíveis e de alto volume de uma unidade de ECMO. Assim, cabe aos intensivistas de ECMO serem capazes de realizar exames seriados de ultrassom cardíaco no local de atendimento (POCUS) em seus próprios pacientes para um atendimento mais eficiente e oportuno ao paciente.
A utilização de POCUS no cenário de ECMO VA, no entanto, permanece heterogênea devido à variabilidade no treinamento entre os provedores. Este estudo tem como objetivo abordar essa lacuna no treinamento, descrevendo a aquisição de imagens POCUS na ECMO periférica V-A, particularmente na ausência de ventilação do VE, incluindo detalhes sobre o posicionamento do paciente, seleção do transdutor, colocação da sonda, sequência de aquisição e otimização da imagem. Outros cenários de ECMO, como ventilação de VE no local, serão abordados separadamente em outros manuscritos desta coleção especial sobre aquisição de imagens de POCUS diagnósticas.
Protocolo
Todos os procedimentos realizados em estudos envolvendo participantes humanos estavam de acordo com os padrões éticos do comitê de pesquisa institucional do Vanderbilt University Medical Center e com a Declaração de Helsinque de 1964 e suas emendas posteriores ou padrões éticos comparáveis. O protocolo foi derivado após uma revisão da literatura publicada por um painel de especialistas de intensivistas 16,21,22,23,25,28,32,33 representando cinco sistemas de saúde nos Estados Unidos. A imagem foi realizada nos próprios autores para as imagens normais e como parte de exames de ultrassom educacionais de rotina feitos para fins de ensino para as imagens positivas. O critério de inclusão foi qualquer paciente em V-A ECMO, e o critério de exclusão foi a recusa em realizar um exame de ultrassonografia. Os equipamentos utilizados no estudo estão listados na Tabela de Materiais.
1. Procedimentos de segurança
- Utilize luvas sem nitrilo ou látex. Siga os processos de controle de infecção para a instituição individual, conforme aplicável.
NOTA: Se o paciente tiver feridas cirúrgicas em estágios de cicatrização ativa, use pacotes de gelatina de ultrassom estéreis processados individualmente.
2. Seleção da sonda
- Utilize um arco de setor ou sonda de matriz de setor (coloquialmente chamada de "sonda de matriz de fase-)34,35,36,37.
3. Pré-ajuste da máquina
- Defina a máquina para a função predefinida de cardiologia (CARDIAC), que terá o indicador no lado direito da tela de ultrassom.
4. Posicionamento do paciente
- Coloque o paciente em decúbito dorsal.
NOTA: Se a supinação não for possível, mantenha o paciente na posição mais favorável para que as cânulas de ECMO não sejam deslocadas. - Coloque cobertores ou rampas para posicionar levemente o paciente em uma trajetória para baixo do lado esquerdo, mantendo a segurança com a colocação da cânula de ECMO se a qualidade da imagem for abaixo do padrão.
5. Monitoramento do paciente
- Visão paraesternal de eixo longo
- Obtenha a visão paraesternal de eixo longo38 do coração (Figura 1) e clique em Adquirir.
- Avalie a valva aórtica 3,13,14,18,38.
- Avalie a abertura da válvula: poço vs. de forma alguma (Figura 2; Vídeo 1). Avaliação de trombo radicular aórtico: presente vs. ausente vs. indeterminado (Figura 2).
- Dimensão interna do ventrículo esquerdo (DDVE)38
- Ative a ferramenta paquímetro . Meça o LVIDD durante a onda R do traçado QRS no ECG (Figura 2) e clique em Adquirir.
- Vista apical de 4 câmaras
- Obtenha a visão apical de 4 câmaras38 (Figura 3) e clique em Adquirir. Avaliar a cavidade do VE quanto à presença de trombo: presente vs. ausente vs. indeterminado10,11 (Figura 2; Vídeo 2).
6. Avaliação da tolerância ao desmame da ECMO VA
NOTA: Para obter detalhes sobre o procedimento, consulte os relatórios publicados anteriormente32,33.
- Avalie a recuperação cardíaca e a viabilidade do desmame da ECMO VA fazendo as seguintes perguntas aos pacientes:
- Avalie se houve recuperação do processo da doença subjacente que levou ao início da ECMO VA.
- Determinar se o paciente recuperou a estabilidade hemodinâmica, definida pelos padrões específicos da instituição 16,32,33.
- Confirme se os problemas de oxigenação e ventilação não são mais graves (por exemplo, verifique se a paO2/FiO2 > 100 e a paCO2 < 60)32.
NOTA: Não há protocolo acordado para determinar quando um paciente se recuperou de sua etiologia subjacente, o que o levou a ser canulado para ECMO VA. Recomenda-se que uma equipe multidisciplinar e abordagem sejam usadas para tomar essa decisão clínica.
- Realize o teste de desmame da ECMO VA se as respostas do paciente às perguntas da lista de verificação forem sim32.
NOTA: Os protocolos de desmame diferem entre os centros e não há um protocolo padronizado acordado.- Diminua as taxas de fluxo de ECMO em incrementos de 0,5 L/min sob vigilância ecocardiográfica constante.
NOTA: A cada queda incremental no fluxo de ECMO, se a PAM cair mais de 10-15 mmHg ou abaixo de 65 mmHg, considere retomar o fluxo total, pois isso sugere que o paciente ainda não está pronto para o desmame. - Realize avaliação ecocardiográfica de cada ECMO wean.
- Visão paraesternal de eixo longo
- Obtenha a visão do eixo longo paraesternal38 e clique em Adquirir. Repita a Etapa 5.1.3. Avaliar qualitativamente a função sistólica do VE (acinética vs. algum grau de função)39 (Vídeo 3).
- Vista apical de 4 câmaras
- Obtenha a vista apical de 4 câmaras38 e clique em Adquirir. Avalie qualitativamente a relação tamanho VD/VE40 (Figura 4). Ative o modo M para medir a Excursão Sistólica do Plano Anular da Válvula Tricúspide (TAPSE)40 (Figura 5).
- Realize imagens Doppler teciduais ativas. Meça o VD S'40 (Figura 6). Meça o S'38 do anel mitral lateral (Figura 7).
- Visão paraesternal de eixo longo
- Vista apical de 5 câmaras
- Obtenha a visão apical de 5 câmaras38,41 e clique em Adquirir (Figura 8).
- Para realizar a integral de tempo de velocidade (VTI) da via de saída do ventrículo esquerdo (VSVE), ative o Doppler de onda de pulso (PWD). Coloque a caixa PWD no LVOT. Meça a VSVE VTI41 (Figura 9).
- Diminua as taxas de fluxo de ECMO em incrementos de 0,5 L/min sob vigilância ecocardiográfica constante.
- Diminua os fluxos para 1-1,5 L/min de fluxo de ECMO se forem tolerados desmames anteriores de ECMO.
- Realize a avaliação ecocardiográfica sob configurações mínimas de ECMO seguindo as etapas 6.2.2.2.
7. Procedimentos de acompanhamento
- Depois que o paciente passar por uma tolerância à beira do leito para o desmame da ECMO VA com base na triagem ecocardiográfica bem-sucedida, hemodinâmica estável e função do órgão-alvo, realize uma avaliação para decanulação com base em protocolos institucionais com informações multidisciplinares.
- Monitore continuamente os sinais de complicações relacionadas à ECMO, como sangramento, infecção, tromboembolismo ou disfunção de órgãos. Ajuste o tratamento conforme necessário.
Resultados
Este artigo descreve a interpretação da ultrassonografia cardíaca point-of-care em pacientes suportados em ECMO periférica V-A em dois cenários clínicos: (1) como uma ferramenta de monitoramento durante o suporte de ECMO para avaliar a presença de distensão do ventrículo esquerdo (VE) e a presença de trombo intracardíaco ou da raiz da aorta, e (2) como uma ferramenta de triagem para avaliar a prontidão da liberação do suporte mecânico.
Não existe uma definição única aceita do que determina a distensão do VE que requer intervenção durante o suporte periférico de ECMO V-A. Além disso, há uma ausência de diretrizes padronizadas que delineiem a frequência das avaliações ultrassonográficas no local de atendimento para monitorar a distensão do VE e informar as estratégias de descarga. No entanto, avaliações seriadas da função biventricular - realizadas diariamente ou com maior frequência conforme indicação clínica - juntamente com avaliações da função valvar, abertura da valva aórtica e colocação de cânula são fortemente recomendadas 3,13.
Em um paciente que é efetivamente suportado em ECMO periférica em V-A, os achados ecocardiográficos que indicam suporte hemodinâmico adequado sem preocupação com a distensão do VE incluem uma cavidade do VE com diâmetro diastólico interno do ventrículo esquerdo (DDVE) dentro dos limites da normalidade, sugestivo de descompressão adequada (homens: <= 5,8 cm; mulheres <= 5,2 cm)42; a ausência de trombos intracardíacos ou radiculares; e uma válvula aórtica que se abre a cada ciclo cardíaco.
Os achados ecocardiográficos que levantam preocupação com a distensão do VE incluem qualquer um dos seguintes: (1) evidência de estase (por exemplo, trombos intracardíacos ou trombos radiculares da aorta); (2) um LVIDD acima dos limites superiores do normal; (3) falha na abertura da válvula aórtica; e/ou (4) piora da regurgitação mitral. Mesmo o contraste de eco espontâneo (SEC) na ECMO VA demonstrou resultar em um risco aumentado de trombo intracardíaco e acidente vascular cerebral, e esse achado em um exame no local de atendimento deve levar a um ecocardiograma consultivo ou à consideração precoce da estratégia de descarga do VE43.
Embora o POCUS isoladamente seja geralmente insuficiente para determinar a adequação e o momento para o emprego de uma estratégia de descarga de LV, o POCUS pode ajudar a informar a seleção de uma estratégia de descarga. Além disso, a ecocardiografia no local de atendimento e a ecocardiografia consultiva facilitam o monitoramento da eficácia da estratégia de descarga do ventrículo esquerdo escolhida, garantindo a descarga adequada e, assim, reduzindo o risco associado à distensão do VE.
A adequação e o momento ideais para a liberação do suporte de ECMO dependem de vários parâmetros clínicos, hemodinâmicos e ecocardiográficos. Atualmente, há uma ausência de diretrizes padronizadas para determinar a prontidão para a liberação do suporte periférico de ECMO V-A, mas a ecocardiografia pode ser empregada para confirmar que ocorreu recuperação cardíaca suficiente. Os parâmetros ecocardiográficos que têm sido associados à liberação bem-sucedida do suporte de ECMO V-A incluem FEVE > 20%-25%, VSVE VTI > 10 cm, velocidade do anel mitral com Doppler tecidual sistólica > 6 cm/s, excursão sistólica do plano do anel tricúspide > 10 mm e FEVD > 25%16,20,44,45.
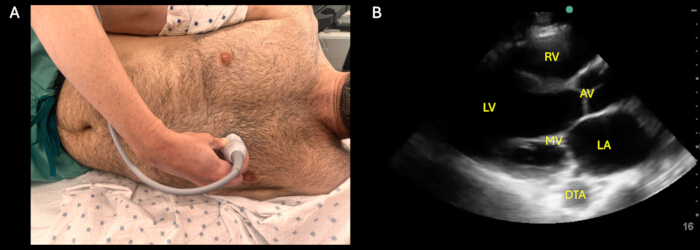
Figura 1: Visualização PLAX. (A) Posicionamento da sonda externa para obter a visão do eixo longo paraesternal (PLAX), com a sonda colocada ao longo da borda esternal esquerda normalmente aproximadamente no 4ºao 6º espaço intercostal com o indicador da sonda apontando para o ombro direito do paciente. (B) Visualização PLAX otimizada mostrando as principais estruturas que devem ser visualizadas nesta visualização: ventrículo direito (VD), valva aórtica (AV), ventrículo esquerdo (VE), valva mitral (MV), átrio esquerdo (AE) e aorta torácica descendente (DTA). Clique aqui para ver uma versão maior desta figura.

Figura 2: Complicações da ECMO VA não ventilada. Ilustração mostrando quais complicações da ECMO VA não ventilada são mais críticas para rastrear com ecocardiografia (sentido horário a partir do canto superior esquerdo): (i) trombo radicular aórtico; (ii) ausência de abertura da valva aórtica; (iii) hiperdistensão do ventrículo esquerdo (VE); e (iv) trombo do VE. A figura foi reimpressa com a permissão do autor (DC) da masterthemachines.com46. Clique aqui para ver uma versão maior desta figura.
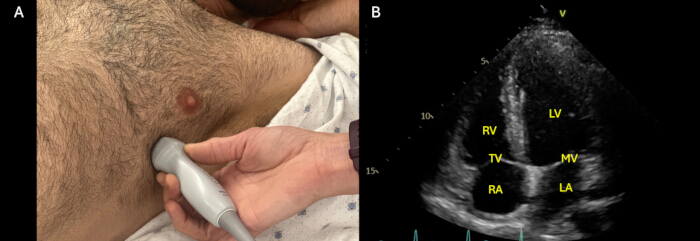
Figura 3: Visão apical de 4 câmaras. (A) Posicionamento da sonda externa para obter a visão apical de 4 câmaras (A4C), com a sonda colocada perto da linha axilar anterior entre o 5ºe o7º espaço intercostal com o indicador de sonda apontando para a axila esquerda do paciente. (B) Visão A4C otimizada mostrando as principais estruturas que devem ser visualizadas nesta visão: ventrículo direito (VD), valva tricúspide (VC), átrio direito (AD), ventrículo esquerdo (VE), valva mitral (VM) e átrio esquerdo (AE). Clique aqui para ver uma versão maior desta figura.

Figura 4: Razões de tamanho VD-VE na visão A4C. Quatro exemplos de uma visão apical de 4 câmaras (A4C), cada uma mostrando uma proporção diferente de tamanhos bidimensionais do ventrículo direito (VD) para o ventrículo esquerdo (VE): (A) RVLV < 1; (B) VD/LV @1; (C) RV/VE > 1; e (D) relação VD/VE indeterminada devido à incapacidade de visualizar a parede livre do VD. Clique aqui para ver uma versão maior desta figura.

Figura 5: TAPSE. Três exemplos representativos de valores de excursão sistólica do plano do anel tricúspide (TAPSE): (A) > 1,0 cm; (B) <= 1,0 cm; e (C) TAPSE indeterminado devido à baixa qualidade da imagem. TAPSE > 1,0 cm é um dos vários parâmetros ecocardiográficos preditivos de desmame bem-sucedido da ECMO VA Clique ou toque aqui para inserir o texto. Clique aqui para ver uma versão maior desta figura.

Figura 6: RV S'. Dois exemplos representativos da velocidade do tecido sistólico do anel lateral do ventrículo direito (VD S'): (A) > 9,5 cm/s (macroscopicamente normal) e (B) < 9,5 cm/s (grosseiramente anormal). Clique aqui para ver uma versão maior desta figura.

Figura 7: S lateral do VE. Dois exemplos representativos de velocidade do tecido sistólico do anel lateral lateral do ventrículo esquerdo (VE S'): (A) > 6 cm/s e (B) <= 6 cm/s. O VE S' > 6 cm/s é um dos vários parâmetros ecocardiográficos preditivos do desmame bem-sucedido da ECMO VA Clique aqui para ver uma versão maior desta figura.

Figura 8: Visão apical de 5 câmaras. (A) Posicionamento da sonda externa para obter a visão apical de 5 câmaras (A5C), com sonda colocada perto da linha axilar anterior entre os espaços intercostais5º a 7º com indicador de sonda apontando para a axila esquerda do paciente. Uma vez que a sonda é colocada nesta posição, geralmente é mais fácil encontrar primeiro a visão apical de 4 câmaras e, em seguida, ventilar o feixe de ultrassom ligeiramente anteriormente para encontrar a visão A5C. (B) Visualização otimizada de A5C mostrando as principais estruturas que devem ser visualizadas nesta visualização: ventrículo direito (VD), átrio direito (AR), ventrículo esquerdo (VE), átrio esquerdo (AE) e via de saída do ventrículo esquerdo. Clique aqui para ver uma versão maior desta figura.

Figura 9: LVOT VTI. Três exemplos representativos de valores integrais de tempo de velocidade da via de saída do ventrículo esquerdo (VSVE LVO): (A) > 10 cm; (B) <= 10 cm; e (C) indeterminado devido à baixa qualidade da imagem, causando limites mal definidos para o traçado Doppler de onda de pulso. LVOT VTI > 10 cm é um dos vários parâmetros ecocardiográficos preditivos de desmame bem-sucedido da ECMO VA. Clique aqui para ver uma versão maior desta figura.
Vídeo 1: Vista PLAX da abertura da válvula aórtica. Três incidências paraesternais de eixo longo ilustrando diferentes achados possíveis ao rastrear a abertura da valva aórtica: (1) alguma abertura durante a sístole; (2) nenhuma abertura durante a sístole; e (3) indeterminado porque a valva aórtica não é adequadamente visualizada. Clique aqui para baixar este vídeo.
Vídeo 2: A4C view sem e sem trombo. Três incidências apicais de 4 câmaras ilustrando diferentes achados possíveis na triagem de trombo ventricular esquerdo (VE), com ênfase especial no ápice do VE, onde os coágulos são mais prováveis de serem encontrados: (1) nenhum trombo macroscópico do VE; (2) densidade de eco dentro de um ápice do VE gravemente hipocinético suspeito de trombo apical do VE; e (3) indeterminado porque o ápice do VE não é adequadamente visualizado. Clique aqui para baixar este vídeo.
Vídeo 3: Graus de disfunção sistólica do VE. Três incidências paraesternais de eixo longo ilustrando diferentes achados possíveis ao rastrear a função sistólica do VE: (1) alguma função (paredes do VE ligeiramente espessadas); (2) sem função (VE parado); e (3) indeterminado porque a cavidade do VE e as bordas endocárdicas não são adequadamente visualizadas. Clique aqui para baixar este vídeo.
Discussão
Importância em relação aos métodos existentes
A utilização da ECMO V-A como terapia de resgate para insuficiência cardíaca aguda descompensada tem aumentado1. A ECMO periférica VA é utilizada como uma intervenção temporária para dar tempo para a recuperação do coração com insuficiência aguda enquanto otimiza a função do órgão-alvo 2,3. Embora não haja diretrizes estabelecidas sobre a aplicação da ecocardiografia no contexto do suporte de ECMO, em 2012, a Sociedade Americana de Ecocardiografia (ASE) publicou uma revisão abrangente de última geração sobre o papel da ecocardiografia em pacientes que receberam ECMO15. A ASE enfatizou que a ecocardiografia pode informar as decisões clínicas antes do início da ECMO, durante o início e a canulação, o monitoramento durante o suporte de ECMO e durante o período de recuperação do paciente, onde o desmame do suporte circulatório mecânico está sendo discutido 4,5,6. Na ausência de recomendações detalhadas para orientar o uso da ecocardiografia na ECMO V-A, esta revisão narrativa sintetiza os usos potenciais da ecocardiografia na forma de um protocolo proposto que poderia ser usado durante as fases de monitoramento e desmame para pacientes em suporte de ECMO VA periférico sem uma estratégia ativa de ventilação do VE em vigor.
As visualizações neste protocolo foram escolhidas especificamente porque, em nossa experiência, elas são mais consistentemente obtidas em pacientes em ECMO VA que geralmente têm tubos mediastinais no lugar de cirurgia cardíaca (ou seja, por isso a janela subcostal foi omitida). Além disso, os parâmetros escolhidos para este protocolo (LVIDD, LV lateral S', VR S', TAPSE e LVOT VTI) foram todos escolhidos por possuírem dados de validação existentes para uso durante as fases de monitoramento e desmame da V-A ECMO 16,20,44,45.
Etapas críticas
Os conceitos críticos do protocolo podem ser agrupados em três categorias gerais: (1) monitoramento da hiperdistensão do VE, (2) monitoramento de outras complicações e (3) consideração do desmame da ECMO.
Primeiro, o protocolo rastreia a distensão do ventrículo esquerdo (VE), o que pode levar à necessidade de estratégias de ventilação do VE. A ECMO periférica em V induz alterações substanciais na hemodinâmica do paciente, caracterizadas por uma diminuição da pré-carga ventricular esquerda devido à diminuição do fluxo sanguíneo transpulmonar associada a um aumento da pós-carga do VE resultante do retorno retrógrado pressurizado através da cânula arterial femoral. No cenário de disfunção grave do VE na ECMO periférica, a cavidade do VE pode ficar distendida, o que pode levar à congestão pulmonar, bem como promover estase e trombose na cavidade do VE e na raiz da aorta. Isso pode levar ao agravamento da regurgitação mitral, reversão do fluxo venoso pulmonar, RM diastólica, isquemia subendocárdica, trombo intracardíaco ou da raiz da aorta, edema pulmonar e/ou disritmias. Portanto, o monitoramento seriado da distensão do VE é fundamental para pacientes em suporte de ECMO V-A, pois fornece informações vitais sobre o momento e a necessidade de estratégias ativas de descarga. Embora uma discussão abrangente sobre estratégias de descarga esteja fora do escopo desta revisão atual, a ecocardiografia também pode contribuir para a tomada de decisões sobre a abordagem ideal de descarga. Isso é obtido estimando o nível adicional de suporte necessário e descartando possíveis contra-indicações para várias estratégias de descarga.
O segundo conceito crítico neste protocolo é o uso de POCUS cardíaco durante a manutenção da ECMO periférica V-A para monitorar todos os seguintes itens: desempenho do VE (tamanho, função sistólica, volume sistólico, abertura da valva aórtica)3,13,14,16,17,18,19; desempenho do VD (tamanho, função sistólica)20,21; e presença versus ausência de trombo intracardíaco10,11 O monitoramento dessas questões permite a análise macroscópica para suporte hemodinâmico adequado e o rastreamento das complicações catastróficas da dilatação e trombo do VE. O terceiro conceito crítico no protocolo é o uso potencial de POCUS cardíaco durante o desmame da ECMO VA. Embora o desmame da ECMO exija uma discussão multidisciplinar, é útil começar com uma avaliação ecocardiográfica básica. Conforme descrito no protocolo do manuscrito, algumas incidências que geralmente podem ser obtidas em pacientes com ECMO são as paraesternais longas, apicais de 4 câmaras e apical de 5 câmaras. As três incidências permitem, durante a tentativa de desmame dos fluxos de ECMO, a avaliação da função sistólica do VE e do VD usando vários parâmetros facilmente obteníveis e reprodutíveis que foram validados como úteis durante o desmame da ECMO: VE e VR S', TAPSE, VVV e relação VD/VE 16,20,44,45.
Solução de problemas e modificações
A solução de problemas do protocolo se concentra na otimização da imagem. Mesmo para pacientes em ECMO VA, o posicionamento das janelas paraesternal e apical pode ser otimizado com o uso de cobertores ou rampas para colocar o paciente em uma leve inclinação do lado esquerdo para baixo (ou seja, cada grau do lado esquerdo para baixo ajuda). No entanto, em alguns casos, os pacientes podem ser muito instáveis para permitir tal posicionamento. Além disso, em outros pacientes com ECMO VA, mesmo a inclinação lateral esquerda ainda pode gerar visualizações abaixo do ideal. Nessas situações, a ecocardiografia transesofágica (ETE) pode ser necessária para obter imagens interpretáveis. No entanto, o ETE não é a ferramenta de avaliação preferida para monitoramento regular, uma vez que os pacientes em ECMO são anticoagulados sistemicamente, têm alta probabilidade de trombocitopenia adquirida e apresentam edema sistêmico associado à falência de múltiplos órgãos - todos fatores que aumentam o risco de trauma com a colocação de ETE. Como tal, mesmo as incidências limitadas obtidas com POCUS cardíaco transtorácico podem ser preferidas como uma modalidade de monitoramento para limitar o risco de complicações adicionais.
Alguns provedores podem optar por modificar esse protocolo com base na preferência local por outros parâmetros. A lista de tais modificações possíveis é quase interminável, então vamos nos concentrar em quatro exemplos. Primeiro, pode-se usar a visão PLAX para rastrear a função sistólica do VE durante o desmame da ECMO V-A usando medidas seriadas de encurtamento fracionário do VE (FS) e/ou avaliação qualitativa da função do VE na visão paraesternal de eixo curto do VE. Enquanto nas instituições do autor outros parâmetros são preferencialmente usados para rastrear a função sistólica do VE (por exemplo, VE S', VVVI VTI), seria razoável usar a FS do VE e/ou a avaliação qualitativa na visão paraesternal de eixo curto em situações em que o coração é adequadamente visualizado de uma janela paraesternal, mas não de uma apical. Em segundo lugar, pode-se usar a visão PLAX para medir o diâmetro da VSVE e, assim, estimar o volume sistólico/débito cardíaco em vez de apenas o VTI da VSVE. No entanto, tal etapa é considerada desnecessária por dois motivos: (i) o erro na medição do diâmetro da VSVE é elevado ao quadrado e, portanto, pode fornecer falsa precisão a qualquer estimativa de volume sistólico resultante, e (ii) o VTI LVOT é usado como um monitor de tendência, de modo que os valores absolutos do volume sistólico tornam-se menos relevantes. Terceiro, para rastrear a abertura da válvula aórtica, pode-se complementar a visão PLAX com uma visão paraesternal de eixo curto da válvula aórtica. É provável que isso seja especialmente útil quando a valva aórtica está parcialmente calcificada, de modo que os folhetos visíveis na incidência PLAX não permitem a visualização precisa da abertura da valva aórtica. Em quarto lugar, alguns provedores podem querer complementar as visões deste protocolo ou substituí-las inteiramente por visões subcostais. No entanto, as visões neste protocolo foram escolhidas especificamente porque, em nossa experiência, elas são mais consistentemente obtidas em pacientes em ECMO VA que geralmente têm tubos mediastinais instalados em cirurgia cardíaca (ou seja, por isso a janela subcostal foi omitida).
Limitações
Este protocolo tem várias limitações. Primeiro, atualmente não há diretrizes publicadas sobre o uso da ecocardiografia para guiar a ECMO VA, então o protocolo foi desenvolvido a partir de uma combinação de revisão da literatura existente e da própria experiência coletiva do grupo de autores multi-institucionais. Embora o protocolo incorpore parâmetros ultrassonográficos que foram validados individualmente no atendimento de pacientes com ECMO VA Assim, este protocolo deve ser visto em grande parte como um ponto de partida para o desenvolvimento de práticas específicas da instituição, onde atualmente não existem. Em segundo lugar, o processo de desmame da ECMO V-A é complexo e requer discussões multidisciplinares além da ecocardiografia. Portanto, tais discussões (que estão fora do escopo deste estudo) devem complementar o protocolo atual para que o desmame da ECMO VA seja realizado de forma ponderada e bem-sucedida. Em terceiro lugar, todos os parâmetros deste protocolo estão sujeitos à variabilidade interoperadores devido à variabilidade entre os provedores no treinamento em aquisição e interpretação de imagens. Assim, o exame deve ser idealmente realizado por profissionais com treinamento avançado em ecocardiografia para minimizar o risco de má interpretação (por exemplo, certificação do conselho em qualquer um dos seguintes caminhos de treinamento ou equivalentes oferecidos pelo Conselho Nacional de Ecocardiografia: Ecocardiografia de Cuidados Intensivos, Ecocardiografia Transesofágica Perioperatória Avançada e/ou Exame de Competência Especial em Ecocardiografia Avançada).
Direções futuras
Este protocolo foi desenvolvido para utilizar parâmetros ecocardiográficos que foram clinicamente validados no cenário de ECMO V-A e também são facilmente obtidos no ponto de atendimento. No entanto, como todos os parâmetros do protocolo sofrem com o potencial de variabilidades entre operadores, trabalhos futuros nessa área devem se concentrar em fornecer ferramentas de avaliação ecocardiográfica mais independentes do operador no local de atendimento. Por exemplo, atualmente, a grande maioria das máquinas usadas para POCUS cardíaco não tem a capacidade de realizar esforço, ecocardiografia tridimensional e interpretação automatizada de imagens. A incorporação dessas ferramentas avançadas em dispositivos de ultrassom no local de atendimento ajudaria muito os médicos ocupados encarregados do atendimento de ECMO VA.
Em resumo, a ecocardiografia é um complemento essencial para a avaliação clínica à beira do leito e o monitoramento hemodinâmico padrão em pacientes suportados em ECMO periférica V-A. As possíveis complicações que podem se desenvolver no suporte de ECMO podem ser rastreadas ativamente por meio de ecocardiografia à beira do leito. Embora o processo de desmame do suporte de ECMO exija uma discussão multidisciplinar que vai além da ecocardiografia, a POCUS cardíaca pode, no entanto, ser usada nesse processo como uma ferramenta adjuvante.
Divulgações
Os Autores declaram não haver divulgações relevantes.
Agradecimentos
Este trabalho foi apoiado em parte pelo Centro de Aprendizagem e Avaliação Experiencial (CELA) do Vanderbilt University Medical Center (VUMC), Nashville, TN, EUA. Os autores também gostariam de agradecer à equipe, corpo docente e pessoal do CELA por sua orientação, assistência e apoio ao longo deste projeto. Quaisquer opiniões, descobertas, conclusões ou recomendações expressas nesta publicação são de responsabilidade dos autores e não refletem necessariamente as opiniões da CELA ou da VUMC.
Materiais
| Name | Company | Catalog Number | Comments |
| Affiniti | Philips | Affiniti 70 | |
| Edge 1 ultrasound machine | SonoSite | Edge II | |
| Vivid iq | GE |
Referências
- Guglin, M., et al. Venoarterial ECMO for adults. J Am Coll Cardiol. 73 (6), 698-716 (2019).
- Extracorporeal Life Support Organization (ELSO). . ELSO General Guidelines for all ECLS Cases. Version 1.4, (2017).
- Lorusso, R., et al. ELSO interim guidelines for venoarterial extracorporeal membrane oxygenation in adult cardiac patients. ASAIO J. 67 (8), 827-844 (2021).
- Combes, A., Price, S., Slutsky, A. S., Brodie, D. Temporary circulatory support for cardiogenic shock. Lancet. 396 (10245), 199-212 (2020).
- Abrams, D., Combes, A., Brodie, D. Extracorporeal membrane oxygenation in cardiopulmonary disease in adults. J Am Coll Cardiol. 63 (25), 2769-2778 (2014).
- Abrams, D., et al. Position paper for the organization of ECMO programs for cardiac failure in adults. Intensive Care Med. 44 (6), 717-729 (2018).
- Saeed, D., et al. Femoro-femoral versus atrio-aortic extracorporeal membrane oxygenation: selecting the ideal cannulation technique. Artif Organs. 38 (6), 549-555 (2014).
- Pavlushko, E., Berman, M., Valchanov, K. Cannulation techniques for extracorporeal life support. Ann Transl Med. 5 (6), 70-70 (2017).
- Roumy, A., Liaudet, L., Rusca, M., Marcucci, C., Kirsch, M. Pulmonary complications associated with venoarterial extracorporeal membrane oxygenation: a comprehensive review. Crit Care. 24 (1), 212 (2020).
- Xie, A., Forrest, P., Loforte, A. Left ventricular decompression in venoarterial extracorporeal membrane oxygenation. Ann Cardiothorac Surg. 8 (1), 9-18 (2019).
- Ezad, S. M., et al. Unloading the left ventricle in venoarterial ECMO: In whom, when, and how. Circulation. 147 (10), 1237-1250 (2023).
- Hussey, P. T., von Mering, G., Nanda, N. C., Ahmed, M. I., Addis, D. R. Echocardiography for extracorporeal membrane oxygenation. Echocardiography. 39 (2), 339-370 (2022).
- Douflé, G., Roscoe, A., Billia, F., Fan, E. Echocardiography for adult patients supported with extracorporeal membrane oxygenation. Crit Care. 19 (1), 326 (2015).
- Mayo, P. H., et al. Machines that save lives in the intensive care unit: The ultrasonography machine. Intensive Care Med. 48 (11), 1429-1438 (2022).
- Platts, D. G., Sedgwick, J. F., Burstow, D. J., Mullany, D. V., Fraser, J. F. The role of echocardiography in the management of patients supported by extracorporeal membrane oxygenation. J Am Soc Echocardiogr. 25 (2), 131-141 (2012).
- Douflé, G., et al. Head-to-toe bedside ultrasound for adult patients on extracorporeal membrane oxygenation. Intensive Care Med. 50 (4), 632-645 (2024).
- Ng, P. Y., et al. Sensitivity of ventricular systolic function to afterload during venoarterial extracorporeal membrane oxygenation. ESC Heart Fail. 9 (6), 3241-3253 (2022).
- Tavazzi, G., et al. How to unload the left ventricle during veno-arterial extracorporeal membrane oxygenation. Eur Heart J Cardiovasc Imaging. 24 (6), 696-698 (2023).
- Price, S., et al. Expert consensus document: Echocardiography and lung ultrasonography for the assessment and management of acute heart failure. Nat Rev Cardiol. 14 (7), 427-440 (2017).
- Aissaoui, N., et al. Right-left ventricular interdependence: A promising predictor of successful extracorporeal membrane oxygenation (ECMO) weaning after assistance for refractory cardiogenic shock. Intensive Care Med. 43 (4), 592-594 (2017).
- Kim, D., et al. Prognostic implication of RV coupling to pulmonary circulation for successful weaning from extracorporeal membrane oxygenation. JACC Cardiovasc Imaging. 14 (8), 1523-1531 (2021).
- Charbonneau, F., et al. Parameters associated with successful weaning of veno-arterial extracorporeal membrane oxygenation: A systematic review. Crit Care. 26 (1), 375 (2022).
- Aissaoui, N., et al. Predictors of successful extracorporeal membrane oxygenation (ECMO) weaning after assistance for refractory cardiogenic shock. Intensive Care Med. 37 (11), 1738-1745 (2011).
- Kim, D., et al. Echocardiographic predictors of successful extracorporeal membrane oxygenation weaning after refractory cardiogenic shock. J Am Soc Echocardiogr. 34 (4), 414-422.e4 (2021).
- Brahmbhatt, D. H., Daly, A. L., Luk, A. C., Fan, E., Billia, F. Liberation from venoarterial extracorporeal membrane oxygenation: A review. Circ Heart Fail. 14 (7), e007679 (2021).
- Uemura, K., et al. Prediction of circulatory equilibrium in response to changes in stressed blood volume. Am J Physiol Heart Circ Physiol. 289 (1), H301-H307 (2005).
- Aissaoui, N., et al. Two-dimensional strain rate and Doppler tissue myocardial velocities: Analysis by echocardiography of hemodynamic and functional changes of the failed left ventricle during different degrees of extracorporeal life support. J Am Soc Echocardiogr. 25 (6), 632-640 (2012).
- Ortuno, S., et al. Weaning from veno-arterial extracorporeal membrane oxygenation: Which strategy to use. Ann Cardiothorac Surg. 8 (1), 37-46 (2019).
- Díaz-Gómez, J. L., Frankel, H. L., Hernandez, A. National certification in critical care echocardiography: Its time has come. Crit Care Med. 45 (10), 1801-1804 (2017).
- Bronshteyn, Y. S., Blitz, J., Hashmi, N., Krishnan, S. Logistics of perioperative diagnostic point-of-care ultrasound: Nomenclature, scope of practice, training, credentialing/privileging, and billing. Int Anesthesiol Clin. 60 (4), 1-7 (2022).
- Kirkpatrick, J. N., et al. Recommendations for cardiac point-of-care ultrasound nomenclature. J Am Soc Echocardiogr. , (2024).
- Aissaoui, N., Brehm, C., El-Banayosy, A., Combes, A. Weaning strategy from veno-arterial extracorporeal membrane oxygenation (ECMO). Extracorporeal Membrane Oxygenation: Advances in Therapy. , (2016).
- Lüsebrink, E., et al. Update on weaning from veno-arterial extracorporeal membrane oxygenation. J Clin Med. 9 (1), 1012 (2020).
- Hoffman, M., Convissar, D. L., Meng, M. -. L., Montgomery, S., Bronshteyn, Y. S. Image acquisition method for the sonographic assessment of the inferior vena cava. J Vis Exp. (191), e64790 (2023).
- Pereira, R. O. L., et al. Point-of-care lung ultrasound in adults: Image acquisition. J Vis Exp. (193), e64722 (2023).
- Ritchie, J. D., et al. Focused assessment with sonography for trauma (FAST) exam: Image acquisition. J Vis Exp. (199), e65066 (2023).
- Turk, M., et al. Point-of-care kidney and genitourinary ultrasound in adults: Image acquisition. J Vis Exp. (208), e66802 (2024).
- Mitchell, C., et al. Guidelines for performing a comprehensive transthoracic echocardiographic examination in adults: Recommendations from the American Society of Echocardiography. J Am Soc Echocardiogr. 32 (1), 1-64 (2019).
- Prada, G., Fritz, A. V., Restrepo-Holguín, M., Guru, P. K., Díaz-Gómez, J. L. Focused cardiac ultrasonography for left ventricular systolic function. N Engl J Med. 381 (4), e36 (2019).
- Rudski, L. G., et al. Guidelines for the echocardiographic assessment of the right heart in adults: A report from the American Society of Echocardiography endorsed by the European Association of Echocardiography and the Canadian Society of Echocardiography. J Am Soc Echocardiogr. 23 (7), 685-713 (2010).
- Porter, T. R., et al. Guidelines for the use of echocardiography as a monitor for therapeutic intervention in adults: A report from the American Society of Echocardiography. J Am Soc Echocardiogr. 28 (1), 40-56 (2015).
- Lang, R. M., et al. Recommendations for cardiac chamber quantification by echocardiography in adults: An update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging. 16 (3), 233-270 (2015).
- Unai, S., et al. Clinical significance of spontaneous echo contrast on extracorporeal membrane oxygenation. Ann Thorac Surg. 103 (3), 773-778 (2017).
- Bailleul, C., Aissaoui, N. Role of echocardiography in the management of veno-arterial extracorporeal membrane oxygenation patients. J Emerg Crit Care Med. 3 (1), 25 (2019).
- Cha, S., Kostibas, M. P. Echocardiographic and point-of-care ultrasonography (POCUS) guidance in the management of the ECMO patient. J Clin Med. 13 (1), 1011 (2024).
- . Master the Machines Available from: https://www.masterthemachines.com/biography-and-cv (2024)
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados