Method Article
אולטרסאונד נקודתי לחמצון ממברנה חוץ-גופית ורידית-עורקית היקפית ללא אוורור החדר השמאלי
In This Article
Summary
פרוטוקול זה מתאר את השימוש באולטרסאונד נקודתי (POCUS) לניטור חולים בחמצון ממברנה חוץ-גופית ורידית-עורקית היקפית (V-A ECMO) ללא אוורור חדר שמאל. הוא מעריך נפיחות של החדר השמאלי, פקקת שורש תוך לבבית או אבי העורקים, ומזהה פרמטרים שימושיים של POCUS לבבי לגמילה מ-V-A ECMO.
Abstract
במהלך העשורים האחרונים, חמצון ממברנה חוץ-גופית ורידית-עורקית (V-A ECMO) הפך לכלי קריטי בניהול חולים עם הלם קרדיוגני חמור ואי ספיקת לב ריאה. בשל חוסר היציבות המובנה של חולים אלה, הובלתם הרחק מיחידות טיפול נמרץ כרוכה בסיכון. כתוצאה מכך, כלי אבחון ליד המיטה חיוניים לטיפול היומיומי שלהם. כלי אחד כזה הוא אולטרסאונד נקודתי (POCUS) של הלב, שיכול להעריך באופן לא פולשני מספר פרמטרים: ביצועי החדר השמאלי (LV) (גודל, תפקוד סיסטולי, נפח שבץ, פתיחת מסתם אבי העורקים), ביצועי החדר הימני (RV) (גודל, תפקוד סיסטולי) ונוכחות של פקקת תוך לבבית. בנוסף, POCUS יכול לסייע בהערכת המוכנות לגמילה מ-V-A ECMO ובסופו של דבר לביטול השימוש. למרות הפוטנציאל שלו, השימוש ב-POCUS בהקשר של V-A ECMO נותר לא עקבי עקב שונות בהכשרת הספקים. מחקר זה נועד לטפל בפער זה על ידי פירוט רכישת תמונות POCUS ב-V-A ECMO, במיוחד בהיעדר אוורור LV. הוא מכסה היבטים מרכזיים כגון מיקום המטופל, בחירת מתמר, מיקום בדיקה, רצף רכישה ואופטימיזציה של תמונה.
Introduction
חמצון ממברנה חוץ-גופית (ECMO) היא אסטרטגיית זמן שעלולה להציל חיים עבור חולים, שראתה שיעור ניצול הולך וגדל 1,2. ל-ECMO יש שתי תצורות שונות: ורידי-ורידי (V-V) וורידי-עורקי (V-A). במהלך העשורים האחרונים, V-A ECMO התגלה ככלי בסיסי בטיפול בחולים עם הלם קרדיוגני חמור ואי ספיקת לב ריאה 3,4,5,6. שתי אסטרטגיות הקנולציה עבור V-A ECMO הן מרכזיות והיקפיות7. ECMO מרכזי V-A דורש בדרך כלל סטרנוטומיה לקנולציה ישירה של הפרוזדור הימני לניקוז ורידי ואבי העורקים הפרוקסימלי להחזרת העורקים הקדמית. מצד שני, ל-V-A ECMO היקפי יש חזרה עורקית דרך עורק הירך באמצעות מנגנון נסיגה. זרימה לאחור זו עלולה לגרום לבעיות הבאות: חמצון דיפרנציאלי של פלג הגוף העליון והתחתון, החמרה בתפקוד הדו-חדרי והתנפחות LV, במיוחד אם אין אסטרטגיה לפרוק את ה-LV8. סיבוכים אלה של V-A ECMO היקפי, בנוסף לסיכונים הגלומים ב-ECMO, מחייבים ניטור תכוף וערני 9,10,11. בשל חוסר היציבות המובנה של חולים אלה, אין זה מעשי להעביר אותם לעתים קרובות מהיחידה לטיפול נמרץ (ICU) לבדיקות אבחון והערכה של התמיכה המכנית במחזור הדם שלהם ומצב לב-ריאה מתפתח 3,6. לכן, כלי אבחון ליד המיטה חיוניים בטיפול היומיומי שלהם. כלי אחד כזה הוא אולטרסאונד נקודתי (POCUS)12,13,14,15 של הלב, שניתן להשתמש בו כדי להעריך את כל הדברים הבאים באופן לא פולשני: ביצועי החדר השמאלי (LV) (גודל, תפקוד סיסטולי, נפח שבץ, פתיחת מסתם אבי העורקים)3,13,14,16,17,18,19ביצועי החדר הימני (RV) (גודל, תפקוד סיסטולי)20,21, ונוכחות לעומת היעדר פקקת תוך לבבית 10,11., יתר על כן, ניתן להשתמש ב-POCUS כדי להעריך את המוכנות לגמילה מ-V-A ECMO ובסופו של דבר לביטול 22,23,24,25,26,27,28.
אולטרסאונד אבחנתי מתחלק בדרך כלל לשתי קטגוריות: נקודת טיפול וייעוץ29,30 אולטרסאונד ייעוצי הוא בדיקה המבוקשת על ידי הספק המטפל העיקרי של המטופל אך מבוצעת על ידי צוות מומחים נפרד29,30, בעוד שאולטרסאונד נקודתי מבוצע ומפורש על ידי הספק המטפל העיקרי של המטופל 29,30,31. למרות שהערכת אולטרסאונד של הלב ב-V-A ECMO מבוצעת באופן מסורתי באמצעות שירותי ייעוץ, שירותים כאלה לא תמיד זמינים באופן מיידי מסביב לשעון כדי לענות על הצרכים הסונוגרפיים בנפח גבוה ובלתי צפויים של יחידת ECMO. לפיכך, ראוי למטפלים ב-ECMO להיות מסוגלים לבצע בדיקות אולטרסאונד לבביות סדרתיות (POCUS) על המטופלים שלהם לטיפול יעיל יותר ובזמן.
עם זאת, השימוש ב-POCUS במסגרת V-A ECMO נותר הטרוגני בשל השונות בהכשרה בין הספקים. מחקר זה נועד לטפל בפער זה בהכשרה על ידי תיאור רכישת תמונת POCUS ב-V-A ECMO היקפי, במיוחד בהיעדר אוורור LV, כולל פרטים על מיקום המטופל, בחירת מתמר, מיקום בדיקה, רצף רכישה ואופטימיזציה של תמונה. תרחישי ECMO אחרים, כגון אוורור LV במקום, יכוסו בנפרד בכתבי יד אחרים באוסף מיוחד זה על רכישת תמונות POCUS אבחנתיות.
Protocol
כל ההליכים שבוצעו במחקרים שכללו משתתפים אנושיים היו בהתאם לסטנדרטים האתיים של ועדת המחקר המוסדית של המרכז הרפואי של אוניברסיטת ונדרבילט ועם הצהרת הלסינקי משנת 1964 והתיקונים המאוחרים יותר שלה או סטנדרטים אתיים דומים. הפרוטוקול נגזר לאחר סקירת הספרות שפורסמה על ידי פאנל מומחים של מומחים לטיפול נמרץ 16,21,22,23,25,28,32,33 המייצגים חמש מערכות בריאות ברחבי ארצות הברית. הדמיה בוצעה על המחברים עצמם עבור התמונות הרגילות וכחלק מסריקות אולטרסאונד חינוכיות שגרתיות שנעשו למטרות לימוד התמונות החיוביות. קריטריון ההכללה היה כל מטופל ב-V-A ECMO, וקריטריון ההדרה היה סירוב לעבור בדיקת אולטרסאונד. הציוד ששימש במחקר מופיע בטבלת החומרים.
1. נהלי בטיחות
- השתמש בכפפות ללא ניטריל או לטקס. עקוב אחר תהליכי בקרת זיהום עבור המוסד הספציפי לפי העניין.
הערה: אם למטופל יש פצעים כירורגיים בשלבי ריפוי פעיל, השתמש בחבילות ג'לי אולטרסאונד סטריליות ומעובדות בנפרד.
2. בחירת בדיקה
- השתמש בבדיקה של קשת סקטור או מערך סקטור (נקראת בשפה המדוברת "בדיקה של מערך שלבים-)34,35,36,37.
3. הגדרה מוגדרת מראש של מכונה
- הגדר את המכונה לפונקציה המוגדרת מראש של הקרדיולוגיה (CARDIAC), אשר לאחר מכן יהיה המחוון בצד ימין של מסך האולטרסאונד.
4. מיקום המטופל
- הנח את המטופל במצב שכיבה.
הערה: אם שכיבה אינה אפשרית, שמור את המטופל במצב הנוח ביותר כדי שצינוריות ECMO לא ייעקרו. - הנח שמיכות או רמפות כדי למקם מעט את המטופל במסלול שמאלי כלפי מטה תוך שמירה על בטיחות עם מיקום צינורית ECMO אם איכות התמונה אינה תקנית.
5. ניטור מטופלים
- מבט על ציר ארוך Parasternal
- השיגו את הציר הארוך הפראסטרנליview 38 של הלב (איור 1) ולחצו על רכישה.
- הערך את המסתם האאורטלי 3,13,14,18,38.
- הערך את פתיחת השסתום: ובכן לעומת בכלל לא (איור 2; סרטון 1). הערכה לפקקת שורש אבי העורקים: נוכח לעומת נעדר לעומת לא מוגדר (איור 2).
- ממד פנימי של החדר השמאלי (LVIDD)38
- הפעל את כלי הקליפר . מדוד LVIDD במהלך גל R של מעקב ה-QRS ב-EKG (איור 2) ולחץ על רכישה.
- נוף אפיקלי של 4 חדרים
- השג תצוגה אפיקלית של 4 חדרים38 (איור 3) ולחץ על רכישה. הערכת חלל LV לנוכחות פקקת: נוכח לעומת נעדר לעומת לא מוגדר10,11 (איור 2; וידאו 2).
6. הערכת סבילות לגמילה מ-V-A ECMO
הערה: לפרטים על ההליך, עיין בדוחות שפורסמו בעבר32,33.
- העריכו את התאוששות הלב וההיתכנות של גמילה מ-V-A ECMO על ידי שאילת השאלות הבאות למטופלים:
- להעריך אם הייתה התאוששות מתהליך המחלה הבסיסי שהניע את התחלת V-A ECMO.
- קבע אם המטופל חזר ליציבות המודינמית, המוגדרת על ידי תקנים ספציפיים למוסד 16,32,33.
- ודא אם בעיות חמצון ואוורור אינן חמורות עוד (למשל, בדוק אם paO2/FiO2 > 100 ו-paCO2 < 60)32.
הערה: אין פרוטוקול מוסכם כדי לקבוע מתי מטופל התאושש מהאטיולוגיה הבסיסית שלו, מה שגרם לו להיות קנולציה ל-V-A ECMO. מומלץ להשתמש בצוות רב-תחומי ובגישה כדי לקבל החלטה קלינית זו.
- בצע ניסוי גמילה V-A ECMO אם תשובות המטופלים לשאלות רשימת הבדיקה הן כן32.
הערה: פרוטוקולי הגמילה שונים בין מרכזים, ואין פרוטוקול סטנדרטי מוסכם.- הפחת את קצב זרימת ה-ECMO במרווחים של 0.5 ליטר לדקה במעקב אקו לב מתמיד.
הערה: בכל ירידה מצטברת בזרימת ה-ECMO, אם ה-MAP יורד יותר מ-10-15 מ"מ כספית או מתחת ל-65 מ"מ כספית, שקול לחדש את הזרימה המלאה, מכיוון שהדבר מצביע על כך שהמטופל עדיין לא מוכן לגמילה. - בצע הערכה אקו לב של כל גמילה ECMO.
- מבט על ציר ארוך Parasternal
- השג את הציר הארוך הפרסטרנליview 38 ולחץ על רכישה. חזור על שלב 5.1.3. הערכה איכותית של תפקוד סיסטולי LV (אקינטי לעומת מידה מסוימת של תפקוד)39 (וידאו 3).
- נוף אפיקלי של 4 חדרים
- השג את 4 החדרים האפיקליים view38 ולחץ על רכישה. הערכה איכותית של יחס גודל RV/LV40 (איור 4). הפעל את מצב M כדי למדוד את החריגה הסיסטולית של המישור הטבעתי של המסתם התלת-שפתי (TAPSE)40 (איור 5).
- בצע הדמיית דופלר רקמות פעילה. מדוד RV S'40 (איור 6). מדוד את הטבעת המיטרלית הרוחבית S'38 (איור 7).
- מבט על ציר ארוך Parasternal
- נוף אפיקלי של 5 חדרים
- השג את התצוגה האפיקלית של 5 חדרים38,41 ולחץ על רכוש (איור 8).
- כדי לבצע אינטגרל זמן מהירות (VTI) של מערכת היציאה של החדר השמאלי (LVOT), הפעל דופלר גל דופק (PWD). הנח את קופסת ה-PWD ב-LVOT. מדוד LVOT VTI41 (איור 9).
- הפחת את קצב זרימת ה-ECMO במרווחים של 0.5 ליטר לדקה במעקב אקו לב מתמיד.
- הפחת את הזרימות לזרימת ECMO של 1-1.5 ליטר לדקה אם נסבלים גמילות ECMO קודמות.
- בצע הערכה אקו לב בהגדרות ECMO מינימליות לפי שלבים 6.2.2.2.
7. נהלי מעקב
- לאחר שהמטופל עובר סבילות ליד המיטה לגמילה מ-V-A ECMO על סמך בדיקת אקו לב מוצלחת, המודינמיקה יציבה ותפקוד איברי קצה, בצע הערכה לדקנולציה על סמך פרוטוקולים מוסדיים עם קלט רב תחומי.
- עקוב באופן רציף אחר סימנים לסיבוכים הקשורים ל-ECMO כגון דימום, זיהום, טרומבואמבוליזם או תפקוד לקוי של איברים. התאם את הטיפול לפי הצורך.
תוצאות
מאמר זה מתאר את הפרשנות של אולטרסאונד לב נקודתי בחולים הנתמכים ב-V-A ECMO היקפי בשני תרחישים קליניים: (1) ככלי ניטור במהלך תמיכה ב-ECMO כדי להעריך נוכחות של התנפחות החדר השמאלי (LV) ונוכחות של פקקת שורש תוך לבבית או אבי העורקים, ו-(2) ככלי סינון להערכת מוכנות משחרור תמיכה מכנית.
אין הגדרה מקובלת אחת של מה שקובע את נפיחות ה-LV הדורשת התערבות במהלך תמיכה ב-V-A ECMO היקפי. יתר על כן, חסרות הנחיות סטנדרטיות המתארות את תדירות הערכות האולטרסאונד בנקודת הטיפול כדי לנטר את התנפחות ה-LV וליידע אסטרטגיות פריקה. עם זאת, הערכות סדרתיות של תפקוד דו-חדרי - המתבצעות מדי יום או בתדירות גבוהה יותר כפי שמצוין קלינית - יחד עם הערכות של תפקוד מסתמי, פתיחת מסתם אבי העורקים ומיקום הצינוריתמומלצות בחום 3,13.
בחולה הנתמך ביעילות ב-V-A ECMO היקפי, ממצאים אקו-קרדיוגרפיים המצביעים על תמיכה המודינמית נאותה ללא חשש להתנפחות LV כוללים חלל LV עם קוטר דיאסטולי פנימי של החדר השמאלי (LVIDD) שנמצא בגבולות הנורמליים, מה שמרמז על דקומפרסיה נאותה (גברים: <= 5.8 ס"מ; נקבות <= 5.2 ס"מ)42; היעדר פקקת תוך לב או שורש; ומסתם אבי העורקים שנפתח עם כל מחזור לב.
ממצאים אקו לב המעוררים חשש להתנפחות LV כוללים כל אחד מהדברים הבאים: (1) עדות לקיפאון (למשל, פקקת תוך לבבית או פקקת שורש אבי העורקים); (2) LVIDD מעל הגבולות העליונים של הנורמה; (3) כשל בפתיחת המסתם האאורטלי; ו/או (4) החמרה של רגורגיטציה מיטרלית. אפילו ניגוד הד ספונטני (SEC) ב-V-A ECMO הוכח כגורם לסיכון מוגבר לפקקת תוך לב ושבץ מוחי, וממצא זה בבדיקה נקודתית אמור לעורר אקו לב מייעץ או חשיבה מוקדמת של אסטרטגיית פריקת LV43.
למרות ש-POCUS בבידוד בדרך כלל אינו מספיק כדי לקבוע את ההתאמה והתזמון להפעלת אסטרטגיית פריקת LV, POCUS יכול לסייע בבחירת אסטרטגיית פריקה. יתר על כן, אקו לב נקודתי וייעוץ מקלים על ניטור היעילות של אסטרטגיית הפריקה של החדר השמאלי שנבחרה, מבטיחים פריקה מספקת ובכך מפחיתים את הסיכון הקשור להתנפחות LV.
ההתאמה והתזמון האופטימליים לשחרור מתמיכת ECMO תלויים במספר פרמטרים קליניים, המודינמיים ואקו-לבביים. כיום אין הנחיות סטנדרטיות לקביעת מוכנות לשחרור מתמיכת V-A ECMO היקפית, אך ניתן להשתמש באקו-לב כדי לאשר שהתרחשה התאוששות לב מספקת. פרמטרים אקוקרדיוגרפיים שנקשרו לשחרור מוצלח מתמיכה ב-V-A ECMO כוללים LVEF > 20%-25%, LVOT VTI > 10 ס"מ, מהירות טבעתית מיטרלית דופלר דופלר > 6 ס"מ לשנייה, סטייה סיסטולית של מישור טבעתי תלת-שפתי > 10 מ"מ ו-RVEF > 25%16,20,44,45.
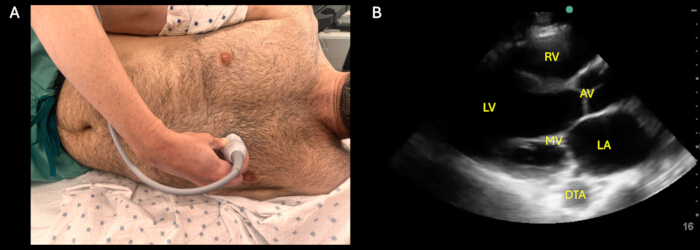
איור 1: תצוגת PLAX. (A) מיקום בדיקה חיצונית להשגת תצוגת הציר הארוך הפרסטרנלי (PLAX), כאשר הגשושית ממוקמת לאורך גבול החזה השמאלי בדרך כלל בערך בחלל הבין-צלעי 4-6 עם מחוון בדיקה המצביע לכיוון כתף ימין של המטופל. (B) תצוגת PLAX אופטימלית המציגה את מבני המפתח שיש לדמיין בתצוגה זו: חדר ימין (RV), מסתם אבי העורקים (AV), חדר שמאל (LV), מסתם מיטרלי (MV), אטריום שמאלי (LA) ואבי העורקים היורד של בית החזה (DTA). אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 2: סיבוכים מ-V-A ECMO שלא הומצא. איור המראה אילו סיבוכים של V-A ECMO שלא אוורר הם הקריטיים ביותר לבדיקה באמצעות אקו לב (בכיוון השעון משמאל למעלה): (i) פקקת שורש אבי העורקים; (ii) חוסר פתיחת מסתם אבי העורקים; (iii) חדר שמאלי (LV) יתר על התפשטות; ו-(iv) פקקת LV. האיור הודפס מחדש באישור המחבר (DC) מ-masterthemachines.com46. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
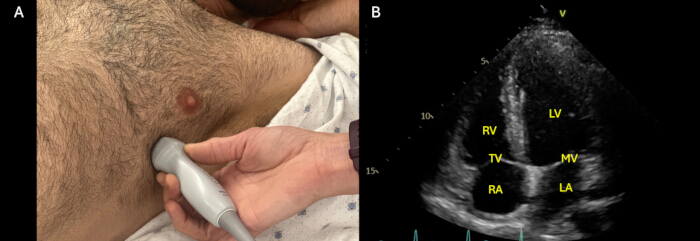
איור 3: מבט אפיקלי בן 4 חדרים. (A) מיקום בדיקה חיצונית להשגת תצוגת 4 חדרים אפיקלית (A4C), עם בדיקה הממוקמת ליד קו בית השחי הקדמי בין החלל הבין-צלעי 5-7 עם מחוון בדיקה המצביע לכיוון בית השחי השמאלי של המטופל. (B) תצוגת A4C אופטימלית המציגה את מבני המפתח שצריך לדמיין בתצוגה זו: חדר ימין (RV), מסתם תלת-שפתי (TV), עלייה ימנית (RA), חדר שמאל (LV), מסתם מיטרלי (MV) ואטריום שמאלי (LA). אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 4: יחסי גודל RV-LV בתצוגת A4C. ארבע דוגמאות לתצוגה אפיקלית של 4 חדרים (A4C), שכל אחת מהן מציגה יחס שונה של גדלים דו-ממדיים של החדר הימני (RV) לחדר השמאלי (LV): (A) RVLV < 1; (ב) RV/LV @1; (ג) RV/LV > 1; ו-(D) יחס RV/LV לא מוגדר עקב חוסר יכולת לדמיין את הקיר החופשי של הקרוואנים. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 5: TAPSE. שלוש דוגמאות מייצגות לערכי סטייה סיסטולית במישור טבעתי תלת-שפתי (TAPSE): (A) > 1.0 ס"מ; (B) <= 1.0 ס"מ; ו-(ג) TAPSE לא מוגדר עקב איכות תמונה ירודה. TAPSE > 1.0 ס"מ הוא אחד ממספר פרמטרים אקו לב המנבאים גמילה מוצלחת מ- V-A ECMO לחץ או הקש כאן כדי להזין טקסט. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 6: RV S'. שתי דוגמאות מייצגות למהירות רקמה סיסטולית טבעתית לרוחב החדר הימני (RV S'): (A) > 9.5 ס"מ לשנייה (נורמלי בעליל) ו-(B) < 9.5 ס"מ לשנייה (חריג בעליל). אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 7: LV לרוחב S'. שתי דוגמאות מייצגות למהירות רקמה סיסטולית טבעתית לרוחב החדר השמאלי (LV S'): (A) > 6 ס"מ לשנייה ו-(B) <= 6 ס"מ לשנייה. LV S > 6 ס"מ לשנייה הוא אחד מכמה פרמטרים אקו לב המנבאים גמילה מוצלחת מ-V-A ECMO. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 8: מבט אפיקלי בן 5 חדרים. (A) מיקום בדיקה חיצונית להשגת תצוגת 5 חדרים אפיקלית (A5C), עם בדיקה הממוקמת ליד קו בית השחי הקדמי בין החללים הבין-צלעיים 5-7 עם מחוון בדיקה המצביע לכיוון בית השחי השמאלי של המטופל. ברגע שהגשושית ממוקמת במצב זה, בדרך כלל הכי קל למצוא תחילה את התצוגה האפיקלית בת 4 החדרים ולאחר מכן לאוורר את קרן האולטרסאונד מעט קדימה כדי למצוא את תצוגת ה-A5C. (B) תצוגת A5C אופטימלית המציגה את מבני המפתח שיש לדמיין בתצוגה זו: חדר ימין (RV), עלייה ימנית (RA), חדר שמאל (LV), אטריום שמאלי (LA) ומערכת היציאה של החדר השמאלי. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.

איור 9: LVOT VTI. שלוש דוגמאות מייצגות לערכי אינטגרל זמן מהירות של דרכי היציאה של החדר השמאלי (LVOT VTI): (A) > 10 ס"מ; (B) <= 10 ס"מ; ו-(C) לא מוגדרים עקב איכות תמונה ירודה הגורמת לגבולות מוגדרים בצורה גרועה עבור מעקב דופלר גלי דופק. LVOT VTI > 10 ס"מ הוא אחד מכמה פרמטרים אקו לב המנבאים גמילה מוצלחת מ-VA ECMO. אנא לחץ כאן לצפייה בגרסה גדולה יותר של איור זה.
סרטון 1: תצוגת PLAX של פתיחת שסתום אבי העורקים. שלוש תצוגות ציר ארוך parasternal הממחישות ממצאים אפשריים שונים בעת בדיקת פתיחת מסתם אבי העורקים: (1) פתיחה מסוימת במהלך הסיסטולה; (2) אין פתיחה במהלך הסיסטולה; ו-(3) לא מוגדר מכיוון שהמסתם האאורטלי אינו נראה כראוי. אנא לחץ כאן להורדת סרטון זה.
סרטון 2: תצוגת A4C ללא ובלי פקקת. שלוש תצוגות אפיקליות של 4 חדרים הממחישות ממצאים אפשריים שונים בעת בדיקת פקקת חדר שמאל (LV), עם דגש מיוחד על קודקוד LV שבו סביר להניח שיימצאו קרישים: (1) אין פקקת LV גסה; (2) צפיפות הד בתוך קודקוד LV היפוקינטי חמור החשוד לפקקת אפיקלית LV; ו-(3) לא מוגדר מכיוון שקודקוד ה-LV אינו מומחש כראוי. אנא לחץ כאן להורדת סרטון זה.
סרטון 3: דרגות של תפקוד סיסטולי LV. שלוש תצוגות ציר ארוך parasternal הממחישות ממצאים אפשריים שונים בעת בדיקת תפקוד סיסטולי LV: (1) תפקוד כלשהו (דפנות LV מתעבות מעט); (2) אין פונקציה (עמידת LV); ו-(3) לא מוגדרים מכיוון שחלל ה-LV והגבולות האנדוקרדיאליים אינם נראים כראוי. אנא לחץ כאן להורדת סרטון זה.
Discussion
משמעויות ביחס לשיטות הקיימות
השימוש ב-V-A ECMO כטיפול הצלה לאי ספיקת לב חריפה נמצא במגמת עלייה1. V-A ECMO היקפי משמש כהתערבות זמנית כדי לאפשר זמן ללב הכושל החריף להתאושש תוך אופטימיזציה של תפקוד איברי הקצה 2,3. למרות שחסרות הנחיות מבוססות לגבי יישום אקו לב בהקשר של תמיכה ב-ECMO, בשנת 2012, האגודה האמריקאית לאקו לב (ASE) פרסמה סקירה מקיפה חדישה על תפקיד אקו לב בחולים המקבלים ECMO15. ה-ASE הדגיש כי אקו לב יכול להודיע על החלטות קליניות לפני התחלת ECMO, במהלך ההתחלה והקנולציה, ניטור בזמן תמיכה ב-ECMO, ובמהלך תקופת ההחלמה של המטופל שבה דנים בגמילה מתמיכה מכנית במחזור הדם 4,5,6. בהיעדר המלצות מפורטות להנחיית השימוש באקו-לב ב-V-A ECMO, סקירה נרטיבית זו מסנתזת שימושים פוטנציאליים באקו-לב בצורה של פרוטוקול מוצע שניתן להשתמש בו במהלך שלבי הניטור והגמילה עבור חולים המקבלים תמיכה היקפית ב-V-A ECMO ללא אסטרטגיית אוורור LV פעילה.
התצוגות בפרוטוקול זה נבחרו במיוחד מכיוון שמניסיוננו, ניתן להשיג אותן באופן העקבי ביותר בחולים ב-V-A ECMO שלעתים קרובות יש להם צינורות מדיאסטינליים במקום מניתוח לב (כלומר, מכאן הסיבה שהחלון התת-צלעי הושמט). יתר על כן, הפרמטרים שנבחרו לפרוטוקול זה (LVIDD, LV lateral S', RV S', TAPSE ו-LVOT VTI) נבחרו כולם מכיוון שיש להם נתוני אימות קיימים לשימוש במהלך שלבי הניטור והגמילה של V-A ECMO 16,20,44,45.
שלבים קריטיים
ניתן לקבץ את המושגים הקריטיים בפרוטוקול לשלוש קטגוריות כלליות: (1) ניטור לנפיחות יתר של LV, (2) ניטור לסיבוכים אחרים, ו-(3) התחשבות בגמילה מ-ECMO.
ראשית, הפרוטוקול בודק התרחבות של החדר השמאלי (LV), מה שעשוי לעורר צורך באסטרטגיות אוורור LV. V-A ECMO היקפי גורם לשינויים משמעותיים בהמודינמיקה של המטופל, המאופיינת בירידה בעומס המוקדם של החדר השמאלי עקב ירידה בזרימת הדם הטרנס-ריאתית יחד עם עלייה בעומס ה-LV הנובע מהחזרה בלחץ לאחור דרך צינורית עורקי הירך. במצב של תפקוד לקוי חמור של LV ב-ECMO היקפי, חלל ה-LV עלול להתנפח, מה שעלול להוביל לגודש ריאתי וכן לקדם קיפאון ופקקת בחלל ה-LV ובשורש אבי העורקים. זה יכול להוביל להחמרה של רגורגיטציה מיטרלית, היפוך זרימת ורידים ריאתיים, MR דיאסטולי, איסכמיה תת-אנדוקרדיאלית, פקקת שורש תוך לבבית או אבי העורקים, בצקת ריאות ו/או הפרעות קצב. לכן, ניטור סדרתי של התנפחות LV הוא קריטי עבור חולים הנתמכים ב-V-A ECMO, מכיוון שהוא מספק מידע חיוני לגבי העיתוי והנחיצות של אסטרטגיות פריקה פעילות. למרות שדיון מקיף באסטרטגיות פריקה נופל מחוץ לתחום הסקירה הנוכחית, אקו לב יכול גם לתרום לקבלת החלטות לגבי גישת הפריקה האופטימלית. זה מושג על ידי הערכת הרמה הנוספת של התמיכה הנדרשת ושלילת התוויות נגד פוטנציאליות לאסטרטגיות פריקה שונות.
הרעיון הקריטי השני בפרוטוקול זה הוא השימוש ב-POCUS לבבי במהלך תחזוקה של V-A ECMO היקפי כדי לנטר את כל הדברים הבאים: ביצועי LV (גודל, תפקוד סיסטולי, נפח שבץ, פתיחת מסתם אבי העורקים)3,13,14,16,17,18,19; ביצועי קרוואנים (גודל, פונקציה סיסטולית)20,21; ונוכחות לעומת היעדר פקקת תוך-לבבית10,11 ניטור בעיות אלה מאפשר ניתוח גס לתמיכה המודינמית מספקת וסינון לסיבוכים הקטסטרופלים של התרחבות LV ופקקת. הרעיון הקריטי השלישי בפרוטוקול הוא השימוש הפוטנציאלי ב-POCUS לבבי במהלך הגמילה מ-VA ECMO. למרות שגמילה מ-ECMO דורשת דיון רב תחומי, כדאי להתחיל בהערכה אקו לב בסיסית. כפי שמתואר בפרוטוקול כתב היד, כמה תצוגות שניתן להשיג בדרך כלל על חולי ECMO הן ה-parasternal long, apical 4-chamber ו-apical 5-chamber. שלוש התצוגות מאפשרות, במהלך ניסיון גמילה מזרימות ECMO, הערכה של תפקוד סיסטולי LV ו-RV באמצעות מספר פרמטרים הניתנים להשגה וניתנים לשחזור בקלות שאומתו כשימושיים במהלך גמילת ECMO: LV ו-RV S', TAPSE, LVOT VTI ויחס RV/LV 16,20,44,45.
פתרון בעיות ושינויים
פתרון בעיות בפרוטוקול מתמקד באופטימיזציה של תמונה. אפילו עבור מטופלים ב-V-A ECMO, ניתן לעתים קרובות לייעל את המיקום של החלונות הפאראסטרנליים והאפיקליים באמצעות שמיכות או רמפות כדי למקם את המטופל בהטיה קלה שמאלה כלפי מטה (כלומר, כל מעלה שמאלה כלפי מטה עוזרת). עם זאת, במקרים מסוימים, המטופלים עשויים להיות לא יציבים מכדי לאפשר מיקום כזה. יתר על כן, בחולי V-A ECMO אחרים, אפילו הטיה לרוחב שמאלה עדיין עשויה לייצר תצוגות לא אופטימליות. במצבים כאלה, ייתכן שתידרש אקו לב דרך הוושט (TEE) כדי להשיג תמונות הניתנות לפרשנות. עם זאת, TEE אינו כלי ההערכה המועדף לניטור קבוע בהתחשב בכך שחולים ב-ECMO הם נוגדי קרישה מערכתיים, בעלי סבירות גבוהה לטרומבוציטופניה נרכשת ויש להם בצקת מערכתית הקשורה לכשל רב-איברי - כל הגורמים המגבירים את הסיכון לטראומה עם מיקום TEE. ככזה, אפילו תצוגות מוגבלות המתקבלות עם POCUS לב דרך בית החזה עשויות להיות מועדפות כשיטת ניטור כדי להגביל את הסיכון לסיבוכים נוספים.
ספקים מסוימים עשויים לבחור לשנות פרוטוקול זה על סמך העדפה מקומית לפרמטרים אחרים. רשימת השינויים האפשריים הללו היא כמעט אינסופית, ולכן נתמקד בארבע דוגמאות. ראשית, ניתן להשתמש בתצוגת PLAX כדי לעקוב אחר תפקוד סיסטולי LV במהלך גמילת V-A ECMO באמצעות מדידות סדרתיות של קיצור חלקי LV (FS) ו/או הערכה איכותית של פונקציית LV בתצוגת הציר הקצר הפראסטרנלי של ה-LV. בעוד שבמוסדות המחבר, פרמטרים אחרים משמשים באופן מועדף למעקב אחר התפקוד הסיסטולי של LV (למשל, LV S', LVOT VTI), יהיה זה סביר להשתמש ב-LV FS ו/או בהערכה איכותית במבט על הציר הקצר הפרסטרנלי במצבים שבהם הלב נראה כראוי מחלון פרסטרנלי אך לא מחלון אפיקלי. שנית, אפשר להשתמש בתצוגת PLAX כדי למדוד את קוטר ה-LVOT ובכך להעריך את נפח השבץ/תפוקת הלב ולא רק LVOT VTI. עם זאת, צעד כזה נמצא מיותר משתי סיבות: (i) השגיאה במדידת קוטר ה-LVOT הופכת לריבועית ובכך יכולה לספק דיוק כוזב לכל אומדן נפח שבץ כתוצאה מכך, ו-(ii) ה-LVOT VTI משמש כמנטר מגמה, כך שערכים מוחלטים של נפח השבץ הופכים פחות רלוונטיים. שלישית, כדי לסנן את פתיחת המסתם האאורטלי, ניתן להשלים את תצוגת ה-PLAX עם מבט על ציר קצר פרה-סטרנלי של המסתם האאורטלי. סביר להניח שזה יהיה שימושי במיוחד כאשר המסתם האאורטלי מסוייד בחלקו כך שהעלים הנראים בתצוגת PLAX אינם מאפשרים הדמיה מדויקת של פתח המסתם האאורטלי. רביעית, ספקים מסוימים עשויים לרצות להשלים את השקפות הפרוטוקול הזה או להחליף אותן לחלוטין בתצוגות תת-צלעות. עם זאת, הדעות בפרוטוקול זה נבחרו במיוחד מכיוון שמניסיוננו, הן ניתנות להשגה באופן העקבי ביותר בחולים ב-V-A ECMO שלעתים קרובות יש להם צינורות מדיאסטינליים במקום מניתוח לב (כלומר, מכאן הסיבה שהחלון התת-צלעי הושמט).
מגבלות
לפרוטוקול זה מספר מגבלות. ראשית, אין כיום הנחיות שפורסמו לגבי השימוש באקו-לב להנחיית V-A ECMO, ולכן הפרוטוקול פותח משילוב של סקירת הספרות הקיימת והניסיון הקולקטיבי של קבוצת המחברים הרב-מוסדית עצמה. בעוד שהפרוטוקול משלב פרמטרים סונוגרפיים שאומתו באופן אינדיבידואלי בטיפול בחולי V-A ECMO, הפרוטוקול עצמו לא אומת באופן פרוספקטיבי. לפיכך, יש לראות בפרוטוקול זה במידה רבה נקודת מוצא לפיתוח פרקטיקות ספציפיות למוסד היכן שאינן קיימות כיום. שנית, תהליך הגמילה מ-V-A ECMO הוא תהליך מורכב הדורש דיונים רב-תחומיים מעבר לאקו לב בלבד. לכן, דיונים כאלה (שהם מחוץ לתחום מחקר זה) חייבים להשלים את הפרוטוקול הנוכחי על מנת שגמילת V-A ECMO תתבצע בצורה מחושבת ומוצלחת. שלישית, כל הפרמטרים בפרוטוקול זה כפופים לשונות בין מפעילים עקב שונות בין ספקים בהדרכה על רכישת תמונות ופרשנות. לפיכך, הבדיקה צריכה להתבצע באופן אידיאלי על ידי ספקים בעלי הכשרה מתקדמת באקו לב כדי למזער את הסיכון לפרשנות שגויה (למשל, הסמכת מועצה בכל אחד ממסלולי ההכשרה הבאים או המקבילים המוצעים על ידי המועצה הלאומית לאקוקרדיוגרפיה: אקו לב לטיפול נמרץ, אקו לב טרנס-וושטי פרי-ניתוחי מתקדם, ו/או בדיקת יכולת מיוחדת באקוקרדיוגרפיה מתקדמת).
כיוונים לעתיד
פרוטוקול זה פותח כדי להשתמש בפרמטרים אקוקרדיוגרפיים ששניהם אומתו קלינית במסגרת V-A ECMO וגם ניתנים להשגה בקלות בנקודת הטיפול. עם זאת, מכיוון שכל הפרמטרים בפרוטוקול סובלים מפוטנציאל לשונות בין מפעילים, עבודה עתידית בתחום זה צריכה להתמקד במתן כלי הערכה אקוקרדיוגרפיים בלתי תלויים יותר במפעיל בנקודת הטיפול. לדוגמה, נכון לעכשיו, הרוב המכריע של המכונות המשמשות ל-POCUS לב חסרות את היכולת לבצע מאמץ, אקו לב תלת מימדי ופרשנות תמונה אוטומטית. שילוב הכלים המתקדמים הללו במכשירי אולטרסאונד נקודתיים יסייע מאוד לרופאים עסוקים המופקדים על טיפול ב-V-A ECMO.
לסיכום, אקו לב הוא תוספת חיונית להערכה קלינית ליד המיטה ולניטור המודינמי סטנדרטי בחולים הנתמכים ב-V-A ECMO היקפי. ניתן לסנן באופן פעיל סיבוכים פוטנציאליים שעלולים להתפתח בתמיכה ב-ECMO באמצעות אקו לב ליד המיטה. בעוד שתהליך הגמילה מתמיכת ECMO דורש דיון רב-תחומי מעבר לאקו לב, POCUS לב יכול לשמש בתהליך זה ככלי משלים.
Disclosures
המחברים מצהירים שאין גילויים רלוונטיים.
Acknowledgements
עבודה זו נתמכה בחלקה על ידי המרכז ללמידה והערכה חווייתית (CELA) במרכז הרפואי של אוניברסיטת ונדרבילט (VUMC), נאשוויל, טנסי, ארה"ב. המחברים רוצים גם להודות לצוות, לסגל ולצוות האישי ב-CELA על ההדרכה, הסיוע והתמיכה לאורך כל הפרויקט. כל הדעות, הממצאים, המסקנות או ההמלצות המובעות בפרסום זה הן של המחברים ואינן משקפות בהכרח את העמדות של CELA או VUMC.
Materials
| Name | Company | Catalog Number | Comments |
| Affiniti | Philips | Affiniti 70 | |
| Edge 1 ultrasound machine | SonoSite | Edge II | |
| Vivid iq | GE |
References
- Guglin, M., et al. Venoarterial ECMO for adults. J Am Coll Cardiol. 73 (6), 698-716 (2019).
- Extracorporeal Life Support Organization (ELSO). . ELSO General Guidelines for all ECLS Cases. Version 1.4, (2017).
- Lorusso, R., et al. ELSO interim guidelines for venoarterial extracorporeal membrane oxygenation in adult cardiac patients. ASAIO J. 67 (8), 827-844 (2021).
- Combes, A., Price, S., Slutsky, A. S., Brodie, D. Temporary circulatory support for cardiogenic shock. Lancet. 396 (10245), 199-212 (2020).
- Abrams, D., Combes, A., Brodie, D. Extracorporeal membrane oxygenation in cardiopulmonary disease in adults. J Am Coll Cardiol. 63 (25), 2769-2778 (2014).
- Abrams, D., et al. Position paper for the organization of ECMO programs for cardiac failure in adults. Intensive Care Med. 44 (6), 717-729 (2018).
- Saeed, D., et al. Femoro-femoral versus atrio-aortic extracorporeal membrane oxygenation: selecting the ideal cannulation technique. Artif Organs. 38 (6), 549-555 (2014).
- Pavlushko, E., Berman, M., Valchanov, K. Cannulation techniques for extracorporeal life support. Ann Transl Med. 5 (6), 70-70 (2017).
- Roumy, A., Liaudet, L., Rusca, M., Marcucci, C., Kirsch, M. Pulmonary complications associated with venoarterial extracorporeal membrane oxygenation: a comprehensive review. Crit Care. 24 (1), 212 (2020).
- Xie, A., Forrest, P., Loforte, A. Left ventricular decompression in venoarterial extracorporeal membrane oxygenation. Ann Cardiothorac Surg. 8 (1), 9-18 (2019).
- Ezad, S. M., et al. Unloading the left ventricle in venoarterial ECMO: In whom, when, and how. Circulation. 147 (10), 1237-1250 (2023).
- Hussey, P. T., von Mering, G., Nanda, N. C., Ahmed, M. I., Addis, D. R. Echocardiography for extracorporeal membrane oxygenation. Echocardiography. 39 (2), 339-370 (2022).
- Douflé, G., Roscoe, A., Billia, F., Fan, E. Echocardiography for adult patients supported with extracorporeal membrane oxygenation. Crit Care. 19 (1), 326 (2015).
- Mayo, P. H., et al. Machines that save lives in the intensive care unit: The ultrasonography machine. Intensive Care Med. 48 (11), 1429-1438 (2022).
- Platts, D. G., Sedgwick, J. F., Burstow, D. J., Mullany, D. V., Fraser, J. F. The role of echocardiography in the management of patients supported by extracorporeal membrane oxygenation. J Am Soc Echocardiogr. 25 (2), 131-141 (2012).
- Douflé, G., et al. Head-to-toe bedside ultrasound for adult patients on extracorporeal membrane oxygenation. Intensive Care Med. 50 (4), 632-645 (2024).
- Ng, P. Y., et al. Sensitivity of ventricular systolic function to afterload during venoarterial extracorporeal membrane oxygenation. ESC Heart Fail. 9 (6), 3241-3253 (2022).
- Tavazzi, G., et al. How to unload the left ventricle during veno-arterial extracorporeal membrane oxygenation. Eur Heart J Cardiovasc Imaging. 24 (6), 696-698 (2023).
- Price, S., et al. Expert consensus document: Echocardiography and lung ultrasonography for the assessment and management of acute heart failure. Nat Rev Cardiol. 14 (7), 427-440 (2017).
- Aissaoui, N., et al. Right-left ventricular interdependence: A promising predictor of successful extracorporeal membrane oxygenation (ECMO) weaning after assistance for refractory cardiogenic shock. Intensive Care Med. 43 (4), 592-594 (2017).
- Kim, D., et al. Prognostic implication of RV coupling to pulmonary circulation for successful weaning from extracorporeal membrane oxygenation. JACC Cardiovasc Imaging. 14 (8), 1523-1531 (2021).
- Charbonneau, F., et al. Parameters associated with successful weaning of veno-arterial extracorporeal membrane oxygenation: A systematic review. Crit Care. 26 (1), 375 (2022).
- Aissaoui, N., et al. Predictors of successful extracorporeal membrane oxygenation (ECMO) weaning after assistance for refractory cardiogenic shock. Intensive Care Med. 37 (11), 1738-1745 (2011).
- Kim, D., et al. Echocardiographic predictors of successful extracorporeal membrane oxygenation weaning after refractory cardiogenic shock. J Am Soc Echocardiogr. 34 (4), 414-422.e4 (2021).
- Brahmbhatt, D. H., Daly, A. L., Luk, A. C., Fan, E., Billia, F. Liberation from venoarterial extracorporeal membrane oxygenation: A review. Circ Heart Fail. 14 (7), e007679 (2021).
- Uemura, K., et al. Prediction of circulatory equilibrium in response to changes in stressed blood volume. Am J Physiol Heart Circ Physiol. 289 (1), H301-H307 (2005).
- Aissaoui, N., et al. Two-dimensional strain rate and Doppler tissue myocardial velocities: Analysis by echocardiography of hemodynamic and functional changes of the failed left ventricle during different degrees of extracorporeal life support. J Am Soc Echocardiogr. 25 (6), 632-640 (2012).
- Ortuno, S., et al. Weaning from veno-arterial extracorporeal membrane oxygenation: Which strategy to use. Ann Cardiothorac Surg. 8 (1), 37-46 (2019).
- Díaz-Gómez, J. L., Frankel, H. L., Hernandez, A. National certification in critical care echocardiography: Its time has come. Crit Care Med. 45 (10), 1801-1804 (2017).
- Bronshteyn, Y. S., Blitz, J., Hashmi, N., Krishnan, S. Logistics of perioperative diagnostic point-of-care ultrasound: Nomenclature, scope of practice, training, credentialing/privileging, and billing. Int Anesthesiol Clin. 60 (4), 1-7 (2022).
- Kirkpatrick, J. N., et al. Recommendations for cardiac point-of-care ultrasound nomenclature. J Am Soc Echocardiogr. , (2024).
- Aissaoui, N., Brehm, C., El-Banayosy, A., Combes, A. Weaning strategy from veno-arterial extracorporeal membrane oxygenation (ECMO). Extracorporeal Membrane Oxygenation: Advances in Therapy. , (2016).
- Lüsebrink, E., et al. Update on weaning from veno-arterial extracorporeal membrane oxygenation. J Clin Med. 9 (1), 1012 (2020).
- Hoffman, M., Convissar, D. L., Meng, M. -. L., Montgomery, S., Bronshteyn, Y. S. Image acquisition method for the sonographic assessment of the inferior vena cava. J Vis Exp. (191), e64790 (2023).
- Pereira, R. O. L., et al. Point-of-care lung ultrasound in adults: Image acquisition. J Vis Exp. (193), e64722 (2023).
- Ritchie, J. D., et al. Focused assessment with sonography for trauma (FAST) exam: Image acquisition. J Vis Exp. (199), e65066 (2023).
- Turk, M., et al. Point-of-care kidney and genitourinary ultrasound in adults: Image acquisition. J Vis Exp. (208), e66802 (2024).
- Mitchell, C., et al. Guidelines for performing a comprehensive transthoracic echocardiographic examination in adults: Recommendations from the American Society of Echocardiography. J Am Soc Echocardiogr. 32 (1), 1-64 (2019).
- Prada, G., Fritz, A. V., Restrepo-Holguín, M., Guru, P. K., Díaz-Gómez, J. L. Focused cardiac ultrasonography for left ventricular systolic function. N Engl J Med. 381 (4), e36 (2019).
- Rudski, L. G., et al. Guidelines for the echocardiographic assessment of the right heart in adults: A report from the American Society of Echocardiography endorsed by the European Association of Echocardiography and the Canadian Society of Echocardiography. J Am Soc Echocardiogr. 23 (7), 685-713 (2010).
- Porter, T. R., et al. Guidelines for the use of echocardiography as a monitor for therapeutic intervention in adults: A report from the American Society of Echocardiography. J Am Soc Echocardiogr. 28 (1), 40-56 (2015).
- Lang, R. M., et al. Recommendations for cardiac chamber quantification by echocardiography in adults: An update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging. 16 (3), 233-270 (2015).
- Unai, S., et al. Clinical significance of spontaneous echo contrast on extracorporeal membrane oxygenation. Ann Thorac Surg. 103 (3), 773-778 (2017).
- Bailleul, C., Aissaoui, N. Role of echocardiography in the management of veno-arterial extracorporeal membrane oxygenation patients. J Emerg Crit Care Med. 3 (1), 25 (2019).
- Cha, S., Kostibas, M. P. Echocardiographic and point-of-care ultrasonography (POCUS) guidance in the management of the ECMO patient. J Clin Med. 13 (1), 1011 (2024).
- . Master the Machines Available from: https://www.masterthemachines.com/biography-and-cv (2024)
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved