Method Article
Cultura e Ensaio de Caenorhabditis em Grande Escala populações elegans
Neste Artigo
Resumo
Para usar caenorhabditis elegans (C. elegans) em pesquisas de omics, um método é necessário para gerar grandes populações de vermes onde uma única amostra pode ser medida entre plataformas para análises comparativas. Aqui, é apresentado um método para cultivar populações de C. elegans em placas de cultura em larga escala (LSCPs) e documentar o crescimento populacional.
Resumo
Caenorhabditis elegans (C. elegans) tem sido e continua sendo um organismo modelo valioso para estudar biologia do desenvolvimento, envelhecimento, neurobiologia e genética. O grande conjunto de trabalhos em C. elegans torna-se um candidato ideal para se integrar em estudos de grande população, em animais inteiros para dissecar os complexos componentes biológicos e suas relações com outro organismo. Para usar C. elegans em pesquisas colaborativas de omics, é necessário um método para gerar grandes populações de animais onde uma única amostra pode ser dividida e avaliada em diversas plataformas para análises comparativas.
Aqui, um método para cultivar e coletar uma abundante população de elegans em estágio misto em uma placa de cultura em larga escala (LSCP) e dados fenotípicos subsequentes é apresentado. Este pipeline produz número suficiente de animais para coletar dados fenotípicos e populacionais, juntamente com quaisquer dados necessários para experimentos de omics (ou seja, genômica, transcriômica, proteômica e metabolômica). Além disso, o método LSCP requer manipulação mínima para os próprios animais, menos tempo de preparação do usuário, fornece um controle ambiental rigoroso e garante que o manuseio de cada amostra seja consistente durante todo o estudo para a reprodutibilidade geral. Por fim, são apresentados métodos para documentar o tamanho populacional e a distribuição populacional das etapas de vida de C. elegans em uma determinada LSCP.
Introdução
C. elegans é um pequeno nematode de vida livre que é encontrado em todo o mundo em uma variedade de habitats naturais1. Sua relativa facilidade de crescimento, tempo de geração rápida, sistema de reprodução e corpo transparente fazem dele um poderoso organismo modelo que tem sido amplamente estudado em biologia do desenvolvimento, envelhecimento, neurobiologia e genética2,3. O trabalho abundante em C. elegans faz dele um candidato primordial a usar em estudos de omics para vincular de forma abrangente fenótipos com componentes biológicos complexos e suas relações em um determinado organismo.
Para usar C. elegans em pesquisas colaborativas de omics, é necessário um método para gerar grandes populações de animais em estágio misto onde uma única amostra pode ser dividida e usada em diversas plataformas e instrumentos para análises comparativas. Criar um pipeline para gerar tal amostra requer uma consciência aguçada da dieta, ambiente, estresse, estrutura populacional e manuseio e coleta de amostras. Portanto, é crucial ter condições de cultivo padrão e reprodutível integradas em dutos de grande escala. Na pesquisa de C. elegans, dois métodos tradicionais são usados para cultivar vermes - pratos ágar Petri e cultura líquida4.
Historicamente, quando grandes quantidades de C. elegans são necessárias, elas são cultivadas na cultura líquida4. As etapas envolvidas na geração de uma grande população de vermes na cultura líquida exigem múltiplas etapas de manuseio que muitas vezes incluem a sincronização alvejante para romper cutículas adultas gravid, liberando embriões para alcançar o tamanho populacional desejado. No entanto, quando a sincronização do alvejante é utilizada, o crescimento populacional depende do tamanho do censo inicial e, portanto, afeta o crescimento subsequente e o número populacional. Além disso, as cepas de C. elegans variam em sua sensibilidade cutícula, tempo de exposição e resposta ao estresse à sincronização alvejante, dificultando o ensaio de muitas cepas ao mesmo tempo5,6,7,8,9.
Além disso, o crescimento de vermes na cultura líquida requer algumas etapas de transferência, pois muitas vezes é recomendado cultivar apenas uma geração de vermes antes da colheita, pois a superlotação pode ocorrer facilmente se cultivada por várias gerações e levar à formação de dauer, apesar da presença de alimentos10. A formação de dauer ocorre através de pequenas moléculas de sinalização, como ascarosides, muitas vezes referidas como "feromônios dauer"11,12,13,14, são liberadas em mídia líquida e afetam o crescimento da população. Além disso, o crescimento de grandes populações de vermes na cultura líquida leva ao acúmulo excessivo de bactérias na cultura, criando dificuldades quando uma amostra limpa é necessária para ensaios fenotípicos a jusante. Por fim, quando uma cultura líquida se contamina, é mais difícil de manter, pois esporos fúngicos ou células bacterianas são facilmente dispersos pela mídia15.
O outro método tradicional de cultivo de C. elegans está em pratos de ágar Petri. As placas de Petri disponíveis comercialmente permitem que se cresça facilmente várias gerações de vermes de palco misto sem os efeitos rápidos da superlotação e alta formação de dauer, como visto em culturas líquidas. No entanto, uma desvantagem para o crescimento de vermes em pratos tradicionais de ágar Petri é que a maior placa de Petri comercialmente disponível não produz grandes populações de vermes para um estudo de omics sem adicionar uma etapa de sincronização alvejante. Em resumo, a cultura de populações mistas de C. elegans em pratos de ágar Petri é mais adequado para coletar dados de omics, mas exigimos um método para gerar tamanhos populacionais muito grandes sem cultivo líquido.
Aqui, apresentamos um método para a cultura e coletamos grandes populações de elegans de estágio misto em placas de cultura em larga escala (LSCP). A coleta de amostras através deste pipeline produz amostras suficientes para coletar dados fenotípicos e populacionais, juntamente com quaisquer dados necessários para experimentos de omics(ou seja,genômica, transcriômica, proteômica e metabolômica). Além disso, o método LSCP requer manipulação mínima dos animais, menos tempo de preparação do usuário, fornece um controle ambiental rigoroso e garante que o manuseio de cada amostra seja consistente ao longo do estudo para a reprodutibilidade geral.
Protocolo
1. Esterilize LSCP e equipamentos
- Prepare LSCPs de vidro por lavagem manual, seguido de lavagem de louça, e autoclaving subsequente para garantir que o vidro esteja livre de contaminantes antes de iniciar o experimento. Armazene LSCPs autoclaved em um local limpo e seco até que esteja em uso.
NOTA: Certifique-se de que os LSCPs são lavadores de pratos e autoclave seguros. Certifique-se de que as tampas LSCP são seguras para lava-louças. - Prepare as tampas LSCP por lavagem manual seguida de lavagem de louça. Armazene as tampas LSCP em uma lixeira limpa até que seja necessário.
- No dia em que o Nematode Growth Media Agarose (NGMA) estiver preparado, limpe as tampas do LSCP com 10% de solução alvejante duas vezes, seguida por 70% de etanol. Uma vez limpo com 10% de alvejante e 70% de etanol, mantenha as tampas de LSCP em uma lixeira limpa no capô de fluxo laminar onde o NGMA será preparado.
2. Prepare a mídia de crescimento de nematoide (NGMA)
- Prepare o NGMA combinando os seguintes reagentes em um frasco de 16 L Erlenmeyer autoclaved com barra de mexida em uma placa de agitação: 2,5 g de peptone, 3 g NaCl, 7 g de agarose, 10 g de ágar e 975 mL de água estéril16. Certifique-se de que o volume total é igual a 1 L. Grave uma tampa de papel alumínio no frasco.
NOTA: As etapas de preparação para o NGMA conforme descrito aqui produzirão material suficiente para 2,5 LSCPs. O protocolo pode ser adaptado ao tamanho do lote LSCP necessário em um determinado experimento. - Autoclave no ciclo líquido a 121 °C e 21 p.s.i. por 45 min.
- Ligue o banho de água e afina para 50 °C. Leve o NGMA autoclavado para o banho de água para esfriar a 50 °C.
- Leve 2 frascos L Erlenmeyer de NGMA para dentro do capô ou espaço limpo e coloque em uma placa de agitação. Use um termômetro para acompanhar a temperatura do NGMA.
- Depois que o NGMA atingiu 50 °C, adicionar o seguinte na ordem listada com uma pipeta descartável estéril dentro do capô ou espaço limpo: 25 mL de 1 M KH2PO4 (tampão de fosfato K), 1 mL de colesterol (5mg/mL no etanol), 1 mL de 1 M CaCl2, 1 mL de 1 M MgSO4, 1 mL de nystatina (10mg/mL) e 1 mL de estreptomicina (100 mg/mL)16.
- Despeje 400 mL de NGMA em um LSCP de vidro estéril, aproximadamente 1,3 cm de profundidade, permita que o LSCP solidifique sobre a superfície plana no capô e coloque a tampa de papel alumínio autoclaved de volta no LSCP.
- Uma vez que o ágar esteja definido, remova a folha e coloque uma tampa limpa e apertada no LSCP e mova-se para 4 °C para armazenamento. Armazene NGMA em LSCPs a 4 °C até usar e usar dentro de 5 dias.
3. Gerar alimentos E. coli para NGMA no LSCP
- Para gerar uma fonte de alimento estável, gere lotes de HT115 (DE3) E. coli utilizando um conceito de média de lote pequeno consistente com o teorema do limite central17. Armazenar a -80 °C. Quando necessário, puxe o estoque bacteriano E. coli de -80 °C para descongelar18.
NOTA: Neste protocolo, os estoques bacterianos E. coli foram cultivados em um bioreator. Ao final do crescimento da cultura, a cultura foi diluída 1:50, e o OD600 medido foi de 0,4. Assim, a cultura teve um600 de 20 de 20. As bactérias foram pelotas, pesadas e resuspengiadas em meio K a uma concentração de 0,5 g/mL (peso molhado), transferidas para alíquotas de 2 mL e congeladas19.
4. Gramado bacteriano no NGMA
- Leve os LSCPs ngma de 4 °C para a temperatura ambiente (RT) por várias horas antes de espalhar o gramado bacteriano para permitir que todo o LSCP chegue ao RT.
- Retirar o estoque bacteriano E. coli necessário de -80 °C para descongelar18.
- Diluir e. coli estoque bacteriano(s) com 2 mL de K-médio estéril para alcançar 0,5 g E. coli em 4 mL por NGMA LSCP. Pipeta cuidadosamente 4 mL de E. coli no meio do NGMA LSCP.
- Use um espalhador estéril para espalhar bactérias em um retângulo deixando aproximadamente 3,8 cm de espaço ao redor das bordas do NGMA E. coli livre.
- Deixe o LSCP NGMA com E. coli no capô com o ventilador ligado por 1h para garantir que a suspensão E. coli see totalmente.
- Uma vez que o gramado bacteriano esteja seco, empurre a tampa firmemente e armazene a 4 °C até usar.
5. Vermes de pedaços para reduzir o estresse e a variabilidade da idade entre as amostras
- Vermes de uma minhoca congelada para uma placa de 6 cm recém-semeadade 4. Esta placa servirá como a placa "pedaço mestre".
NOTA: O chunking é um método ideal para transferir worms de uma cepa homozigosa20. Se uma cepa é heterozigosa ou precisa ser mantida por meio da colheita e acasalamento, o em pedaços não é aconselhável. A frequência de emarares pode precisar ser otimizada dependendo dos genótipos de vermes usados, temperatura escolhida para o crescimento e passos a jusante. - Depois que a placa de bloco mestre estiver cheia de adultos gravid saudáveis (aproximadamente 3 dias) com muito gramado E. coli ainda presente, siga as diretrizes padrão de emção de C. elegans como descrito no WormBook para produzir quatro placas de pedaços totais4.
- Armazene todas as placas de pedaço em uma sala de temperatura controlada (CT) a 20 °C, a menos que seja especificada de outra forma para crescimento.
NOTA: Se os usuários deste protocolo não tiverem acesso a uma sala de tomografia como descrito aqui, recomenda-se usar uma pequena incubadora onde a temperatura possa ser controlada ou uma sala designada onde as condições ambientais possam ser controladas tanto quanto possível. Se nenhuma dessas opções alternativas estiver disponível, observe que a variação no crescimento da amostra pode ser maior. - Uma vez que muitos adultos gravid são observados na placa de4º pedaço, passe para o Passo 6.
6. Detectar branqueamento de adultos gravid no LSCP
NOTA: Esta técnica de branqueamento é usada para erradicar a maioria dos contaminantes e dissolver a cutícula das hermafroditas liberando embriões do verme adulto. A solução de alvejante mergulhará no NGMA antes da eclosão dos embriões.
- Leve LSCPs para RT por várias horas antes de detectar vermes branqueados.
- Prepare uma proporção de 7:2:1 de ddH2O : alvejante : 5 M NaOH. Faça esta solução alcalina hipoclorito fresca pouco antes do uso.
NOTA: Use o mesmo estoque de alvejante e NaOH durante toda a duração de um determinado experimento para evitar efeitos em lote de alvejante. Alvejante usado neste protocolo foi 5-10% hipoclorito de sódio. - Acenda um queimador bunsen e acenda uma picareta de vermes antes de prosseguir. Colher E. coli fresco em uma picareta estéril da borda do gramado bacteriano no LSCP.
- Escolha um único adulto gravid da placa de4º pedaço para branqueamento de manchas.
- Pipeta 5 μL da solução alcalina de hipoclorito em um canto do LSCP longe do gramado E. coli.
- Coloque o adulto gravid escolhido na solução de hipoclorito alcalino de 5 μL. Bata no nematoide para ajudar a interromper a cutícula e solte os ovos.
- Repita as etapas 6.4 – 6.6 para um total de 4x e coloque 5 adultos gravid uniformemente ao redor do gramado E. coli. Escolha todos os 5 adultos gravid da mesma placa de4º pedaço para garantir que indivíduos quase geneticamente isogênicos sejam adicionados a uma determinada amostra.
- Coloque a tampa de volta no LSCP.
- Repita os passos para todos os LSCPs.
7. Crescimento de vermes na sala de temperatura controlada (TC)
- Após o branqueamento do ponto, coloque a tampa firmemente sobre o LSCP e coloque na sala ct definida para 20 °C com fluxo de ar constante e um fotoperiod 12L:12D (luz de 12h e 12h de escuridão).
- Observe a hora e a posição onde a amostra foi colocada na sala de tomografia.
NOTA: A posição dentro da sala deve ser sempre documentada para registrar quaisquer diferenças ambientais que as amostras que possam encontrar potencialmente durante o crescimento. Uma vez que a amostra esteja na sala de tomografia, ela deve permanecer no local designado sem ser perturbada. Não abra a tampa do LSCP na sala de tomografia para diminuir a chance de contaminação. - Leve o LSCP a um microscópio, fora da sala de tomografia, para observar o crescimento populacional e a densidade.
NOTA: Cada cepa e amostra de C. elegans variam em seu crescimento, por isso monitore as amostras de perto. Embora seja recomendável não perturbar o crescimento do LSCP enquanto na sala de tomografia, as LSCPs foram transportadas para fora da sala de tomografia e as tampas foram abertas a cada 2 dias para monitorar o crescimento da amostra. Tirar as tampas seladas dos LSCPs a cada 2 dias também permite que o O2 flua para dentro do LSCP. - Antes de colher, certifique-se de que o LSCP se tornou cheio de uma grande população de vermes. Use os seguintes critérios para decidir se o LSCP está pronto para ser coletado.
- Certifique-se de que o LSCP está cheio de vermes adultos gravid.
- Certifique-se de que a placa contém um grande tamanho populacional (ou seja, os vermes cobrem toda a superfície do ágar).
- Certifique-se de que a placa não tenha muitos ovos na superfície do ágar (ou seja,o número máximo de vermes deveria ter eclodido).
- Certifique-se de que a placa tem mínimo a nenhum E. coli, indicando que os vermes morreriam de fome e gerariam larvas dauer se deixados na placa por mais dois dias.
NOTA: Embora a maioria dos LSCPs estejam prontos para colher entre 10 a 20 dias, dependendo da cepa e da amostra, verifique cada LSCP com frequência ao estabelecer este protocolo para determinar os tempos normais de colheita.
- Limpe luvas e área com 70% de etanol entre o manuseio de LSCPs para evitar contaminação cruzada entre as cepas.
8. Colhendo a amostra LSCP
- Ligue e deixe a centrífuga esfriar até 4 °C antes da colheita das amostras.
- Prepare três tubos cônicos de 50 mL com 50 mL de solução M9 por LSCP a ser colhida.
- Rotule um tubo cônico de 15 mL por LSCP.
NOTA: Todas as etapas de centrifugação são realizadas no tubo cônico de 15 mL, porque os vermes tendem a pelotar bem nestes tubos. - Despeje 50 mL de solução M9 (de um tubo cônico de 50 mL na Etapa 8.2) na superfície LSCP e gire ao redor para garantir que o M9 cubra toda a superfície NGMA.
- Enquanto m9 se senta na superfície LSCP, prime uma pipeta sorológica estéril com M9.
NOTA: Ao escorrizar a pipeta sorológica estéril com M9, isso garante que menos vermes grudem no interior da pipeta plástica, evitando a perda de amostras. - Incline o LSCP para que m9 e a população de vermes se reúnam em um canto do LSCP.
NOTA: A mistura de solução M9 e worms do LSCP será referida como a "suspensão do worm" em degraus a jusante. - Utilizando uma pipeta sorológica preparada com um pipettor automático, suspensão de worm pipeta e coloque no tubo cônico original de 50 mL. Uma vez que 50 mL de suspensão de vermes é coletado, coloque o tubo cônico em um roqueiro para interromper as bactérias aglomerados e detritos.
- Repetir as etapas 8.4 - 8.7 coletando 150 mL de suspensão de worm por LSCP.
- Transfira 15 mL de suspensão de vermes, de um dos três tubos cônicos de 50 mL, derramando em um tubo cônico de 15 mL rotulado na etapa 8.3. Centrifugar o tubo cônico de 15 mL a 884 x g por 1 min a 4 °C. A maioria dos vermes vai pelotar no fundo do tubo.
- Aspire fora do supernante garantindo não perturbar a pelota de verme.
- Continue adicionando aproximadamente 13 mL de suspensão de vermes ao mesmo tubo cônico de 15 mL repetindo as etapas 8.9 e 8.10 até que todos os 150 mL de suspensão de vermes sejam consumidos. Inverta o tubo e perturbe a pelota entre centrífugas para lavar e aspirar o máximo de bactérias e detritos possível.
NOTA: Nesta etapa, o conteúdo dos três tubos cônicos de 50 mL é condensado em um único tubo de 15 mL. - Adicione 10 mL de M9 limpo ao tubo cônico de 15 mL e agitar a pelota de verme invertendo. Centrifugar o tubo cônico de 15 mL a 884 x g por 1 min a 4 °C. Aspire fora do supernante garantindo não perturbar a pelota de verme. Repita duas vezes.
NOTA: Se houver uma grande quantidade de detritos ou bactérias na amostra, repita o passo 8.12 até que a amostra esteja limpa. - Uma vez que a amostra esteja limpa, adicione ddH2O à pelota de verme para um total de 10 mL de ddH2O e worms. Agitar a pelota de verme invertendo. Mova-se rapidamente para o passo 9.1, pois os vermes devem permanecer em ddH2O por 5 min ou menos para evitar o estresse osmótico.
NOTA: Suspender pelotas de vermes em ddH2O é o solvente preferido para passos de omics a jusante. Os worms podem ser suspensos em outros solventes ou buffers se forem compatíveis com um determinado fluxo de trabalho experimental.
9. Estimar o tamanho da população
NOTA: Passe rapidamente pelas etapas 9.1 – 9.7. A mistura de ddH2O e vermes da etapa 8.13 são referidos como a "amostra de verme" nas etapas subsequentes.
- Antes de pipetar a amostra de verme, a ponta de pipeta principal deve ser usada com M9 para evitar vermes grudados no interior da pipeta plástica prevenindo a perda de amostras e reduzindo a variação da contagem.
- Pegue uma alíquota de 100 μL de amostra de verme e dilua-a em 900 μL de M9. Misture bem e faça uma diluição seriada (1:10, 1:100, 1:1000). Repita esta etapa duas vezes para obter um total de três conjuntos de réplicas de alíquotas.
NOTA: Os vermes pipetadores podem causar alta variabilidade na contagem populacional da amostra. Certifique-se de que a amostra de verme é homogênea antes de pipetar a alíquota desejada. - Coloque o tubo cônico de 15 mL em um roqueiro para continuar a cultura em movimento enquanto as alíquotas são contadas.
- Certifique-se de que a amostra de vermes está bem misturada e homogênea. Pipeta 5 μL da amostra de vermes de 1:10, dispense-a em um slide de microscopia e conte o número de vermes. Se este número for inferior a aproximadamente 50 vermes, então também conte as diluições de 1:100 e 1:1000. Se for mais de 50, passe para a próxima diluição serial.
NOTA: Se muitos worms não puderem ser contados com precisão, use a próxima diluição serial para contar. - Conte cada réplica de alíquota de cada diluição 3x. Ao final da contagem, para a maioria das culturas, serão documentadas 9 contagens totais (ou seja,3 contagens totais para cada réplica de alíquota).
- A média da diluição conta para determinar o tamanho populacional estimado da amostra de vermes. Essas contagens de diluição determinarão o volume de amostra de verme necessário para criar o tamanho de alíquota desejada para etapas de -omics.
NOTA: Neste experimento, foram geradas alíquotas de aproximadamente 200.000 vermes em estágio misto. Além disso, uma alíquota de aproximadamente 50.000 vermes em estágio misto foi reservada para a classificação em um grande citômetro de fluxo de partículas (descrito na Etapa 10). - Uma vez que a amostra de verme tenha sido dividida em alíquotas apropriadas, o flash congele em nitrogênio líquido e armazene a amostra a -80 °C.
NOTA: Não congele a alíquota destinada a uma grande citometria de fluxo de partículas.
10. (Opcional) Preparar amostra para citometria de fluxo de partículas grandes
NOTA: As etapas 10, 11 e 12 são o método preferido dos autores para registrar o crescimento amostral (ou seja,o tamanho populacional e a distribuição populacional das etapas do ciclo de vida de C. elegans) e determinar o sucesso de uma cultura. Os usuários deste protocolo podem substituir as etapas 10, 11 e 12 opcionais por suas próprias métricas de sucesso de crescimento. As etapas 10, 11 e 12 são descritas aqui por duas razões; primeiro, para que os usuários que possuem equipamentos utilizados nas Etapas 10, 11 e 12 possam replicar essas etapas e segundo, para mostrar validação desse método de crescimento. O passo 9 acima fornece uma boa estimativa do número total de vermes para determinar tamanhos de alíquota, e o passo 10 é uma métrica mais quantitativa para estimar o número e a distribuição populacional de vermes em uma determinada amostra.
- Traga a alíquota de aproximadamente 50.000 worms de fase mista (reservado na Etapa 9.6) até 10 mL de volume total na solução M9.
- Faça uma solução composta de 1 mg/mL de E. coli e uma diluição de 1:50 de microesferas fluorescentes vermelhas de 0,5 μM19.
- Adicione 200 μL desta solução aos 10 mL de vermes de palco misto em M9 e incubar enquanto balança por 20 minutos.
- Após 20 min, centrifugar o tubo cônico de 15 mL a 884 x g por 1 min a 4 °C.
- Aspire fora do supernante garantindo não perturbar a pelota de verme.
- Lave a pelota de verme duas vezes com solução M9 para eliminar o excesso de bactérias e microesferas fluorescentes vermelhas.
- Adicione 5 mL de M9 à pelota de minhoca e certifique-se de que a pelota fique limpa. Se a pelota estiver limpa, adicione 5 mL de M9 com azida de sódio de 50 mM para endireitar e matar os vermes para contagem precisa e dimensionamentode 21.
- Hora e data do documento quando o azida de sódio é adicionado à amostra.
- Reserve a amostra no roqueiro até que seja necessário para uma grande citometria de fluxo de partículas.
NOTA: O azida de sódio é conhecido por afetar a fisiologia do nematodo (ou seja,o comprimento do corpo, o metabolismo e a termotolerância). Portanto, é fundamental notar o tempo em que os vermes são expostos ao azida de sódio, pois muitos desses afetos fisiológicos acontecem em questão de minutos22. Devido aos efeitos fisiológicos conhecidos do azida de sódio sobre os vermes, este tratamento afetará a qualidade da imagem a jusante e deve ser considerado.
11. (Opcional) Documentando a distribuição populacional e preparando placa de 384 poços para imagem
NOTA: O passo 11 usa um grande citômetro de fluxo de partículas (LPFC). O conhecimento básico de um LPFC é assumido neste protocolo. Outros métodos podem ser substituídos para documentar o crescimento e distribuição populacional das amostras. As etapas documentadas aqui são para usuários que planejam usar um LPFC em seu pipeline23.
- Ligue, limpe e prime o LPFC e permita que os lasers aqueçam por 1h antes de classificar amostras.
- Depois que o laser se aquecer, abra o perfil "Histograma" e escala para um Time of Flight (TOF) de 2050.
- Adicione uma região de barras ao "Histograma" abrangendo uma faixa TOF de 100. A primeira região do bar cobre um TOF de 50-150.
- Continue a criar vinte regiões de bar cada uma abrangendo uma faixa TOF de 100. Essas regiões de bares abrangerão toda a faixa TOF de 50 a 2050. Consulte a Tabela Suplementar 1 para obter as regiões fechadas exatas para usar em toda a distribuição TOF.
- Salve este Histograma configurado como um "Experimento" para usar em futuras corridas LPFC.
- Selecione placa calibrada de 384 poços ou calibrar o instrumento para uma placa de 384 poços para dispensar objetos.
- Uma vez no modelo calibrado de placa de 384 poços, defina o modelo para dispensar 20 objetos fechados em quatro poços (quatro réplicas técnicas de cada região fechada) para cada uma das 20 regiões de barras criadas durante as Etapas 11.3-4. Consulte a Tabela Suplementar 2 para obter um layout de exemplo de como distribuir worms na placa de 384 poços.
- Transfira a amostra da etapa 10.9 para um tubo cônico de 50 mL e adicione uma solução M9 adicional para atingir aproximadamente 40 mL de volume total.
- Comece a classificar automaticamente a amostra pelos parâmetros definidos na etapa 11.7 enquanto agita continuamente a amostra para evitar a fixação e, simultaneamente, a distribuição de objetos da amostra na placa calibrada de 384 poços.
NOTA: Certifique-se de que a taxa de fluxo do LPFC esteja operando entre 15-20 objetos por segundo e especifique nenhum duplo a ser classificado. - Uma vez que toda a amostra tenha sido classificada e o número máximo de regiões fechadas tenham sido dispensados na placa de 384 poços, tire a amostra do LPFC e do instrumento limpo.
NOTA: Quando regiões tof maiores são atingidas, pode se tornar desafiador continuar a encher a placa de 384 poços devido à baixa contagem de eventos naquela região tof. Preencha o maior número possível de regiões fechadas para obter a melhor ideia de onde c. elegans estágios de vida se enquadram na distribuição LPFC antes de ficar sem amostra. - Coloque uma filme de vedação em cima da placa 384-well até ser imaged.
NOTA: Placa de imagem o mais rápido possível após a classificação porque as amostras são tratadas com azida de sódio22. Microesferas fluorescentes vermelhas podem ser vistas nos arquivos de dados LPFC coletados (ou seja, PH Dados vermelhos no arquivo de texto de saída) com base no nível de fluorescência vermelha emitida em cada objeto ordenado para ajudar a identificar quais objetos são vermes vivos, vermes mortos, dauers ou lixo24.
12. (Opcional) Imagem 384-bem placa
NOTA: O passo 12 usa um microscópio micro confocal de leitura de placas. O conhecimento básico de um microscópio microconócal é assumido neste protocolo. Outros métodos podem ser substituídos para documentar o crescimento e distribuição populacional das amostras.
- Usando um microscópio micro confocal de leitura de placas com uma lente 20x.
- Abra a guia "Objetivo e Câmera" e ajuste para o modo " PlanoApoLambda".
- Abra a guia "Camera Binning" e defina para "2".
- Abra a guia "Sites to Visit on Plate" e defina para "4" sites por poço e "sobreponha sites 10%" para mais tarde costurar imagens.
- Abra a guia"Comprimento de onda" e defina para "Brightfield 1".
- Abra a guia"Iluminação" e coloque em "luz transmitida, amostra brilhante".
- Coloque a placa de 384 poços no microscópio e defina a "Z Stack" para "Calcular Deslocamento" e encontre o plano focal adequado para as amostras na placa de 384 poços.
- Execute a placa de 384 poços no microscópio micro confocal coletando quatro imagens por poço.
- Montar as quatro imagens juntas para criar uma imagem por poço.
Resultados
O crescimento de C. elegans usando o método LSCP produz uma média de aproximadamente 2,4 milhões de vermes em estágio misto por amostra ao longo de 12,2 dias. O crescimento de C. elegans usando o método LSCP permite que os usuários gerem grandes populações de estágios mistos de C. elegans com pouco manuseio e manipulação dos animais, o que é ideal para estudos de omics em larga escala(Figura 1). Uma vez que um LSCP se tornou cheio de vermes adultos, atingiu um grande tamanho populacional, e tem bactérias mínimas, os usuários podem colher e estimar o tamanho da população. Este ponto também pode servir como um controle de qualidade, avaliando se a população é suficiente para usar em um gasoduto -omics(Figura 2). A dinâmica populacional depende da tensão em si, do comportamento da cepa (ou seja,das cepas de escavação tendem a ter menor recuperação de vermes) e do sucesso do crescimento(ou seja,da contaminação). O método LSCP foi testado em 15 cepas de C. elegans contendo uma mistura de mutantes do Centro de Genética de Caenorhabditis (CGC) e caenorhabditis elegans Natural Diversity Resource (CeNDR) cepas selvagens25. Genótipos de cepa são descritos na Tabela Suplementar 3.
O método LSCP produziu tamanhos populacionais de aproximadamente 94.500 a 9.290.000. O tamanho médio da população dentro da cepa de referência, PD1074, e entre as cepas foi de aproximadamente 2,4 milhões de vermes(Figura 3). Não foram encontradas diferenças significativas nos tamanhos populacionais estimados entre as cepas de C. elegans ao longo de uma média de 12,2 dias de crescimento LSCP(Figura 4). Os LSCPs PD1074 levaram entre 10 a 14 dias para crescer em uma população mista completa. O tempo médio de crescimento em PD1074 foi de 10 dias. A cepa de crescimento mais lenta cresceu por um máximo de 20 dias, e a cepa de crescimento mais rápido cresceu por um mínimo de 10 dias(Figura 4).
Portanto, usando este método LSCP, os usuários podem facilmente integrar novas cepas de interesse em um estudo com pouco conhecimento de tempo de desenvolvimento e experiência em antecedentes. Observe que cepas e fenótipos que devem ser mantidos por meio da colheita, têm defeitos de fecundidade, são heterozigos, ou têm defeitos de crescimento podem não funcionar bem neste gasoduto.
A citometria de fluxo de partículas de grande porte e a imagem das amostras permitem que os usuários documentem a distribuição populacional. Uma grande variedade de plataformas pode ser usada para medir o crescimento populacional bem-sucedido.
Para medições reprodutíveis de omics, é importante cultivar culturas consistentes. As métricas da reprodutibilidade cultural são o número de vermes e uma distribuição de tamanho consistente para uma determinada cepa. Mostramos a distribuição amostral para a cepa de referência, PD1074 – uma variante da cepa original N2 Bristol, utilizando as imagens do microscópio LPFC23,26 e micro confocal como proxies para o sucesso do crescimento. Como os vermes foram medidos a partir da fase L1 através do gravid adulto na distribuição lpfc(Figura 5),imagem subsequente(Figura 6), e a variação na distribuição populacional entre amostras(Figura 7), podemos ver que este gasoduto gerou uma população em estágio misto de C. elegans.
Para ver de perto a distribuição populacional de nossas amostras de estágio misto, analisamos a distribuição de 35 LSCPs PD1074 olhando para o percentual de vermes que se enquadram em cada região em toda a distribuição time of flight (TOF) (ou seja,comprimento do corpo)(Figura 7A,B).
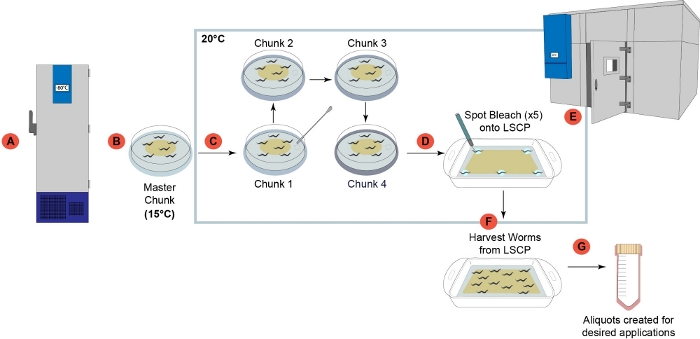
Figura 1: Visão geral do pipeline de crescimento de vermes LSCP. (A) Uma vez recebidas no laboratório, todas as cepas foram preparadas e congeladas para armazenamento a longo prazo a -80 °C2. (B) Uma placa "pedaço mestre" foi preparada a partir de um caldo de minhoca congelado e armazenada a 15 °C para ser usada por no máximo um mês. (C) Cada amostra passou por quatro etapas sucessivas de chunking para reduzir o estresse geracional antes de crescer no LSCP. (D) 5 adultos gravid individuais foram escolhidos da placa "chunk 4" 6 cm em Step (D) e manchas branqueadas em cinco áreas dadas do LSCP. (E) O LSCP foi colocado em uma sala de Temperatura Controlada e cresceu a 20 °C até que o LSCP estava cheio de vermes adultos, atingiu um grande tamanho populacional, e tinha bactérias mínimas. (F) A população de vermes foi colhida e coletada para passos a jusante. (G) As alíquotas foram criadas a partir do LSCP e foram congeladas por flash para aplicações desejadas a jusante. Clique aqui para ver uma versão maior desta figura.
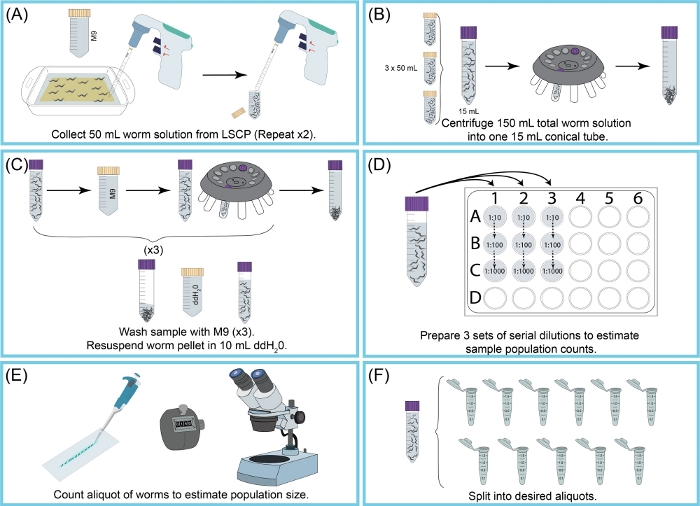
Figura 2: Visão geral da colheita do LSCP e estimativa do tamanho da população. (A) 50 mL de M9 foram usados para lavar vermes da superfície NGMA. A suspensão do verme foi escoada em um tubo cônico de 50 mL. Step (A) foi repetido duas vezes. (B) 15 mL de suspensão de vermes foi derramado em um novo tubo cônico de 15 mL. Vermes foram pelotados por centrifugação. M9 + detritos foram aspirados sem perturbar a pelota de verme. O passo (B) foi repetido até que todos os 150 mL de suspensão do verme foram coletados. (C) A pelota de verme foi lavada e centrifugada três vezes com M9 para eliminar detritos remanescentes. Uma vez que a amostra estava limpa, a pelota de verme foi resuspended em 10 mL de ddH2O. (D) Uma diluição serial da amostra foi criada para estimar o tamanho da população de vermes. Foram utilizados os fatores de diluição que permitiam a contagem de vermes com precisão. O fator de diluição utilizado mudou dependendo do tamanho populacional do LSCP. (E ) Uma vez escolhida a(E)fator de diluição, todos os vermes das três réplicas alíquotas dessa diluição foram esbofeinados em um slide limpo e os vermes foram contados sob um microscópio dissecando. (F) A amostra foi dividida em alíquotas de tamanho apropriado. Clique aqui para ver uma versão maior desta figura.
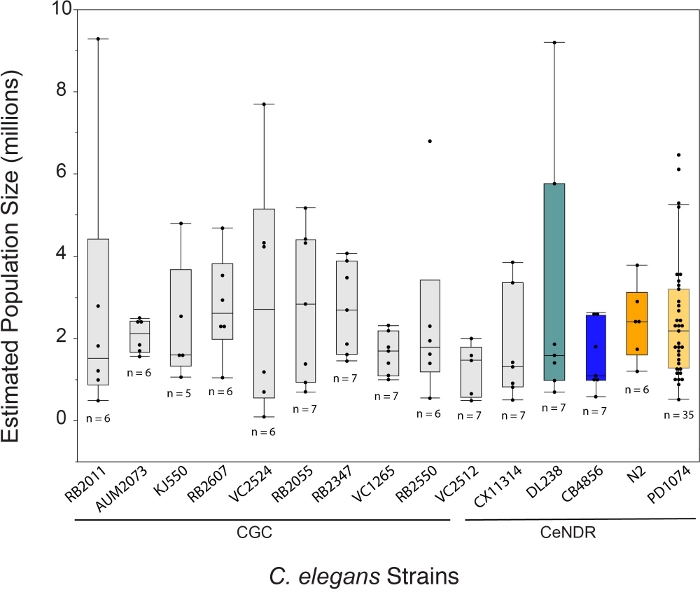
Figura 3: Método LSCP gerado em média uma população de 2,4 milhões de vermes em estágio misto. O LSCP produz tamanhos populacionais nos menores crescimentos populacionais em cerca de 94.500 e nos maiores crescimentos populacionais em torno de 9.290.000. O tamanho médio da população em todas as cepas foi de 2,4 milhões de vermes. Barras abaixo de C. elegans nomes de cepas indicam se uma cepa é um mutante CGC ou isolado natural CeNDR. O tamanho da amostra LSCP é exibido para cada cepa. Foram realizadas comparações para todos os pares que utilizam o Teste HSD de Tukey. Não foram observadas diferenças significativas entre os tamanhos populacionais estimados em cepas de C. elegans (F(14.108) = 0,7, p = 0,77). As barras coloridas indicam displays de cores padrão para a representação da tensão C. elegans. Clique aqui para ver uma versão maior desta figura.
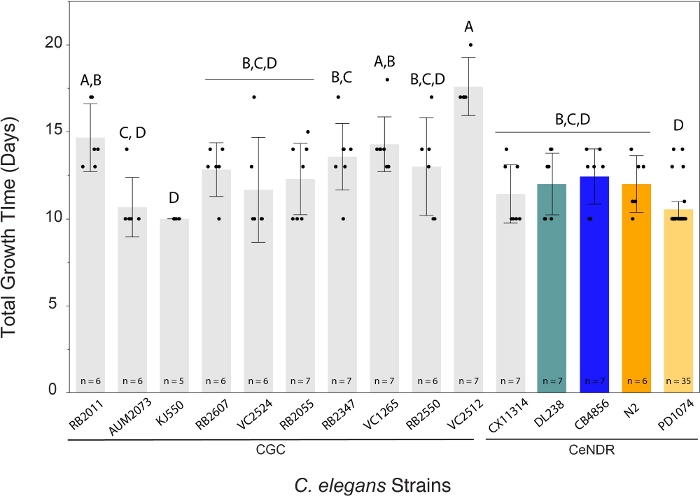
Figura 4: O método LSCP gerou grandes populações mistas de vermes em 10 a 20 dias. Um dado C. elegans LSCP cresceu até que a amostra estava cheia de vermes adultos, atingiu um grande tamanho populacional, e tinha o mínimo de grama bacteriana sobrando. Os LSCPs levaram entre 10 a 20 dias para crescer em uma população em estágio misto completo, dependendo da tensão. O tempo médio de crescimento em todas as cepas foi de 12,2 dias. O tamanho da amostra LSCP é exibido para cada cepa. Cada barra de erro foi construída utilizando-se 1 desvio padrão da média. Os níveis não conectados pela mesma letra são significativamente diferentes. Comparações para todos os pares usando o Teste HSD da Tukey. Uma diferença significativa foi encontrada na quantidade de tempo de crescimento no LSCP necessário em todas as cepas de C. elegans (F(14.108) = 8,8, p < 0,0001*). As barras coloridas indicam displays de cores padrão para a representação da tensão C. elegans. Clique aqui para ver uma versão maior desta figura.
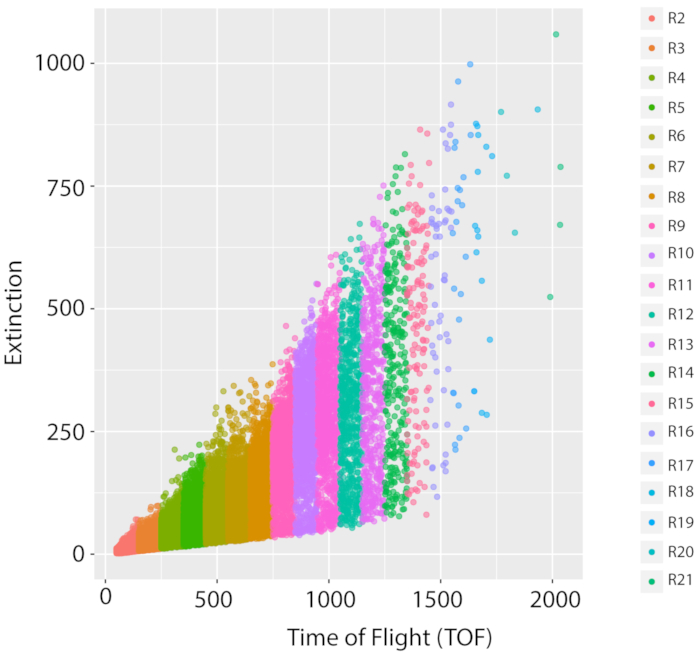
Figura 5: População mista e medição de crescimento da cepa de referência do tipo selvagem, PD1074. Uma distribuição LPFC representativa de um crescimento LSCP da cepa de referência do tipo selvagem, uma variante da cepa original de N2 Bristol, (PD1074) documenta a distribuição de tamanho e contagem de eventos de uma população em estágio misto. O eixo x exibe o comprimento (Time of Flight, TOF) dos worms classificados. O eixo y exibe a densidade óptica (extinção óptica, EXT) dos worms classificados. Cada ponto de dados é um worm que foi documentado na amostra. Cada região TOF utilizada para análise de imagens é exibida em uma cor diferente. Foram criadas vinte regiões TOF (R2 – R21) variando de um TOF de 50 a 2050. Os detalhes sobre cada região do TOF podem ser encontrados na Tabela Suplementar 1. Clique aqui para ver uma versão maior desta figura.
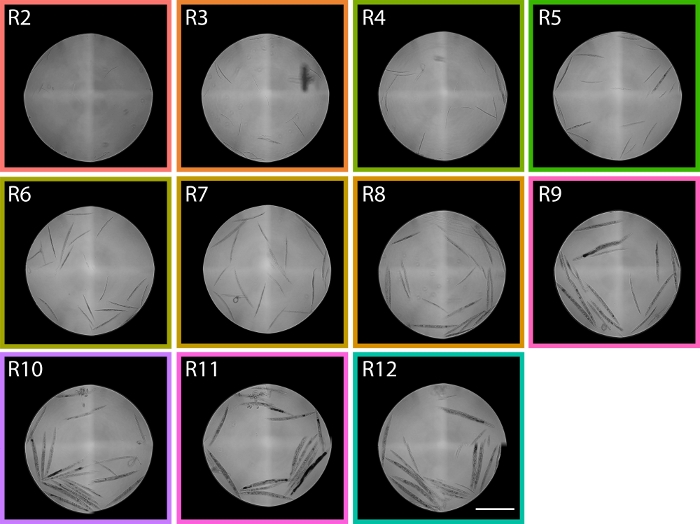
Figura 6: Imagens de vermes classificados de regiões TOF que variam de R2 – R12 mostram a distribuição PD1074 LPFC. Na região R2, vermes L1 podem ser identificados e na região R9 são predominantemente gravid adultos, abrangendo os dois extremos larvais de desenvolvimento que nos dão regiões aproximadas dentro da distribuição de citômetros de fluxo de onde são esperados estágios na distribuição. A barra de escala representa 1 mm. As imagens representativas foram tiradas da distribuição LPFC exibida na Figura 5, e as caixas coloridas correspondem às regiões da Figura 5. Clique aqui para ver uma versão maior desta figura.
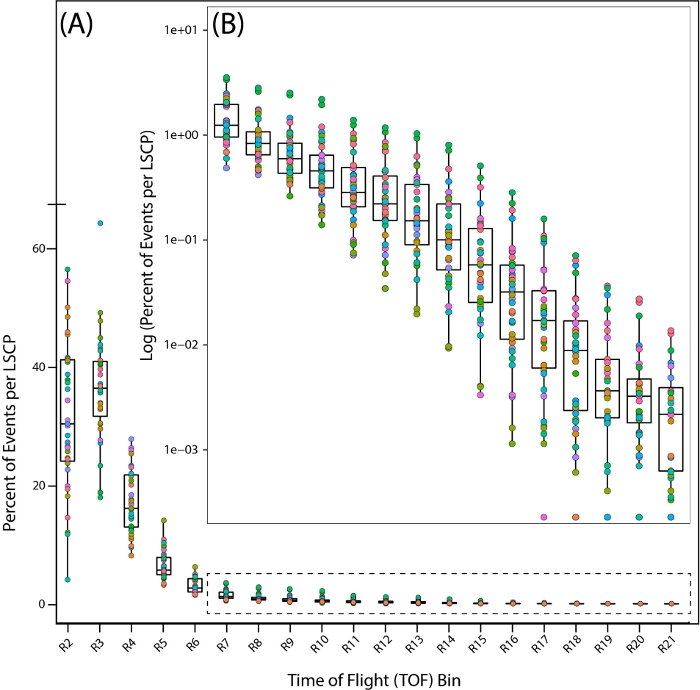
Figura 7: Distribuição populacional através do tempo de voo (TOF) regiões na cepa de referência do tipo selvagem, PD1074. Distribuição de vermes em toda a região da TOF mostrando as regiões onde os vermes foram encontrados. Cada LSCP PD1074 é representado como uma cor individual. (A) O eixo x mostra as vinte regiões TOF (R2 – R21) observadas e contadas para o LSCP, exibindo toda a distribuição de tamanho. O eixo y mostra a porcentagem de vermes de um determinado LSCP que tinha um tamanho corporal que caiu em uma determinada região TOF. (B) Como uma fração menor da população de vermes cai entre as regiões R7-R21, o registro do percentual de vermes que caíram dentro de cada região foi levado para exibir a distribuição populacional. O eixo x exibe as regiões R7-R21 TOF. O eixo y exibe o registro da porcentagem de worms de um determinado LSCP que tinha um tamanho corporal que caiu em uma determinada região TOF. Clique aqui para ver uma versão maior desta figura.
Figura suplementar 1: Temperatura média diária (°C) das condições de crescimento sob as quais o LSCP foi cultivado e manuseado. As temperaturas reportadas da sala de Temperatura Controlada (TC) foram documentadas e coletadas ao longo do período de seis meses de crescimento e coleta da amostra. A temperatura média diária é relatada aqui. Não foram observadas diferenças significativas entre a temperatura em que o LCSP cresceu durante a duração do projeto (F(5,24) = 2,59, p = 0,0524). Toda a diferença de temperatura não foi superior a 0,003 °C durante o período de seis meses de crescimento e geração da amostra. Clique aqui para baixar este número.
Tabela suplementar 1: As regiões fechadas tof costumavam classificar vermes em placas de 384 poços para imagem. Foram criadas regiões binadas para abranger um TOF de 100 em toda a distribuição TOF de 50 a 2050. Regiões fechadas podem ser alteradas e otimizadas para atender às suas necessidades. Cada região TOF utilizada para análise de imagens é exibida em uma cor diferente. Clique aqui para baixar esta tabela.
Tabela suplementar 2: modelo de placa de 384 poços de regiões TOF e replicação de layout. Cada amostra foi classificada em uma placa de 384 poços para imagem. Foram criadas quatro réplicas para cada região selecionada para classificação. Regiões fechadas podem ser alteradas e otimizadas para atender às suas necessidades. Consulte a Tabela Suplementar 1 para regiões fechadas específicas criadas e utilizadas neste protocolo. Cada região TOF utilizada para análise de imagens é exibida em uma cor diferente. Clique aqui para baixar esta tabela.
Tabela suplementar 3: C. as cepas de elegans utilizadas neste protocolo contêm uma mistura de cepas CGC e CeNDR. A cepa, o genótipo, a fonte de tensão e os detalhes estão descritos nesta tabela. Clique aqui para baixar esta tabela.
Discussão
Uma variedade de vasos pode ser usado como um LSCP. Neste protocolo, foi utilizada uma assadeira padrão de vidro. Os LSPCs em uso tinham dimensões externas de 35,56 x 20,32 cm, dimensões internas de 27,94 x 17,78 cm, e aproximadamente 4,45 cm de profundidade e vinham com uma tampa equipada. Assim, a quantidade de bactérias utilizadas aqui foi otimizada para um LSCP com as dimensões acima para produzir uma grande população de vermes em estágio misto. O volume e a concentração bacterianas podem ser ajustados para atender às necessidades experimentais.
A contaminação por, fungos ou outras fontes bacterianas pode ocorrer em qualquer etapa do método LSCP, por isso manuseie amostras com cuidado. Antes de iniciar qualquer etapa do protocolo, certifique-se de que o espaço de trabalho seja limpo com 70% de etanol e 10% de alvejante. Se disponível, trate as áreas usadas com luz UV por 30 minutos e ligue um filtro de ar HEPA 30 minutos antes de iniciar cada etapa.
Ao cultivar o LSCP em uma configuração controlada (ou seja,, em uma sala de tomografia situada a 20 °C), o usuário pode acompanhar mais facilmente o crescimento da amostra e documentar a contaminação potencial. Se a superfície do LSCP estiver contaminada, corte a contaminação quando possível e deixe que a amostra continue a crescer ou descarte a amostra se a contaminação não for possível de controlar. É imperativo abordar a contaminação rapidamente para reduzir o crescimento indesejado e garantir que não seja superando os vermes por recursos.
Este método destina-se àqueles que querem cultivar culturas de população mista em larga escala de C. elegans. Embora possa ser possível cultivar populações sincronizadas de vermes no LSCP como feito em placas de Petri disponíveis comercialmente e na cultura líquida, os autores não testaram essa opção. Além disso, se os usuários desejam cultivar mais de 2,4 milhões de worms em média em uma determinada amostra, um método diferente é recomendado4. O sucesso do crescimento depende da tensão que está sendo processada no gasoduto. Os autores foram capazes de cultivar com sucesso populações de aproximadamente 2,4 milhões de vermes em pelo menos cinco réplicas biológicas de 15 cepas de C. elegans, indicando que o método é robusto.
Antes de iniciar o experimento, observe que a idade e a saúde de um determinado verme podem influenciar a fecundidade e o tempo subsequente de crescimento populacional. Certifique-se de que os vermes sejam mantidos em condições saudáveis com o mínimo de estresse antes de serem usados neste gasoduto. Supõe-se que amostras de estoque foram criadas, congeladas e mantidas a -80 °C para reduzir a deriva genética ao longo do tempo.
Dependendo das necessidades de um determinado experimento, o número de adultos gravid iniciantes em um LSCP pode ser alterado. Alterar o número de adultos gravid iniciantes no LSCP mudará a taxa de crescimento e, portanto, tempo para colher. Cinco adultos gravid são usados para semear cada LSCP pelas seguintes razões: (1) Uma maneira simples, rápida e eficiente de semear muitas cepas de C. elegans em LSCPs de uma só vez foi necessária e (2) para reduzir as diferenças de idade entre os adultos gravid escolhidos que poderiam levar à heterogeneidade de crescimento.
Este método permite ao usuário colher grandes populações de vermes com todas as etapas do ciclo de vida presentes. Com os métodos atuais disponíveis, coletar amostras em larga escala de C. elegans requer sincronização alvejante para obter o número de vermes desejados para o trabalho a jusante. Dada essa abordagem, pode-se agora cultivar o maior número possível de vermes em fermentadores ou culturas líquidas em larga escala sem as dificuldades associadas à sincronização do alvejante e múltiplas etapas de manuseio. Nosso protocolo permite atingir as cepas de interesse de forma eficiente, usar o tempo mínimo de manuseio no crescimento da amostra em si e isolar estágios de vermes ou a população conforme necessário em dutos a jusante.
Um LPFC foi utilizado como uma ferramenta para documentar a distribuição e o tamanho da população em um determinado LSCP. O LPFC utilizado é um sistema de fluxo contínuo que analisa, classifica e distribui worms com base em seu tamanho (TOF) e densidade óptica. À medida que um determinado verme passa pela célula de fluxo, o detector de perda de luz axial captura a quantidade de luz de sinal bloqueada por um laser de estado sólido de 488 nm pelo tempo que leva um worm para passar, dando ao usuário o TOF e a densidade óptica do worm. A óptica e detectores de coleta de fluorescência também podem ser utilizados para maximizar a sensibilidade e a coleta de fluorescência em cada amostra. Os parâmetros de coleta LPFC variam de acordo com o instrumento. Os usuários podem empregar uma variedade de plataformas para capturar o tamanho do worm e não se limitam a usar este protocolo se um LPFC não estiver disponível.
Os autores estão usando amostras cultivadas no método descrito aqui para identificar metabólitos desconhecidos em várias cepas de C. elegans via Cromatografia Líquida – Espectrometria de Massa, Espectroscopia de NMR e sequenciamento de RNA. Os autores planejam continuar a usar este método para o crescimento de amostras neste pipeline com uma variedade de cepas C. elegans, pois novas cepas de interesse podem ser facilmente processadas usando este pipeline.
Divulgações
Os autores não têm nada a revelar.
Agradecimentos
Agradecemos aos membros do Laboratório Edison por discussões úteis e feedback sobre este manuscrito; em particular, B.M. Garcia. Algumas cepas foram fornecidas pelo CGC, que é financiado pelo NIH Office of Research Infrastructure Programs (P40 OD010440), e pelo CeNDR, que é financiado pela NSF Living Collections CSBR 1930382. Este trabalho foi apoiado por uma subvenção do NIH (U2CES030167).
Materiais
| Name | Company | Catalog Number | Comments |
| 10 mL Sterile Serological Pipettes | VWR | 89130-898 | |
| 10 ul pipette tips | VWR | 89079-438 | |
| 100 ul pipette tips | VWR | 89079-442 | |
| 1000 mL Graduated Cylinder | VWR | 10124-380 | |
| 1000 ul pipette tips | VWR | 89079-488 | |
| 15 mL conical tubes | VWR | 89039-668 | |
| 190 Proof Ethanol | VWR | 89125-166 | |
| 2 L Wide Neck Erlenmeyer Flask | VWR | 75804-654 | |
| 50 mL conical tubes | VWR | 75874-294 | |
| Agar | Sigma | 05040-100G | |
| Agarose | Sigma | A9539-500G | |
| BVC Control G Fluid Aspiration System | Vacuubrand | ||
| Calcium Chloride | Sigma | 449709-10G | |
| Cholesterol | Sigma | C3045-25G | |
| Clorox Bleach | VWR | 89414-502 | |
| Conviron Control Temperature Room | Conviron | https://www.conviron.com/environmental-rooms | |
| Corning Low Volume 384 Well Black with Clear Flat Bottom Polystyrene TC-Treated Microplate | VWR | 89089-866 | |
| Fisher Scientific Accuspin 3R | Fisher | ||
| Flat-Bottom 24-Well Plate | VWR | 29443-952 | |
| Honeywell True HEPA Purifier 465 sq ft. | Home Depot | 204390560 | |
| HT115 E. coli (DE3) | CGC | HT115(DE3) | https://cgc.umn.edu/strain/HT115(DE3) |
| Kimwipes | VWR | 470224-038 | |
| Large Scale Culture Plate (LSCP) | Pyrex | 1090948 | Pyrex 2-quart Glass Baking Dish with Red Lid |
| Magnesium Sulfate | Sigma | C86677-25G | |
| MgSO4 | VWR | 97062-998 | |
| Microscope Plain Slides | VWR | 16004-422 | |
| Millipore Filter | Millipore | 1.11727.2500 | |
| Molecular Devices ImageXpress | Molecular Devices | Model Number:IXMConfocal | https://www.moleculardevices.com/products/cellular-imaging-systems/high-content-imaging/imagexpress-micro-confocal#gref , Authors used MetaXpress Software Version 6.5.4.532 |
| Nystatin (10mg/mL) | Sigma | N6261-25MU | |
| Peptone | Sigma | P7750-100G | |
| Petri Dishes (6 cm) | VWR | 25384-092 | |
| Pipette Controller | VWR | 613-4180 | |
| Potassium Chloride | Fisher | P217-3 | |
| Potassium Phosphate Monobasic | VWR | 0781-500G | |
| Potasssium Hydroxide | Fisher | P250-500 | |
| Red Fluroscent Microspheres | Polysciences | 19507-5 | |
| Sodium Chloride | Sigma | 746398-500G | |
| Sodium Hydroxide | Fisher | 111357 | |
| Sodium Phosphate Dibasic Anhydrous | Fisher | BP332-500 | |
| Standard Gilson Pipette Set | Gilson | FA10002M, FA10004M, FA10006M | |
| Streptomycin (100mg/mL) | Sigma | S6501-25G | |
| Union Biometrica COPAS BioSorter | Union Biometrica | https://www.unionbio.com/biosorter/ , authors used: Flow Pilot software version 1.6.1.3. |
Referências
- Félix, M. A., Braendle, C. The natural history of Caenorhabditis elegans. Current Biology. 20 (22), 965-969 (2010).
- Corsi, A. K. A Transparent window into biology: A primer on Caenorhabditis elegans. WormBook. , 1-31 (2015).
- Brenner, S. The genetics of behaviour. British Medical Bulletin. 29 (3), 269-271 (1973).
- Stiernagle, T. Maintenance of C. elegans. WormBook: The Online Review of C. elegans Biology. , (2006).
- Xiong, H., Pears, C., Woollard, A. An enhanced C. elegans based platform for toxicity assessment. Scientific Reports. 7 (1), 9839 (2017).
- Loer, C. M., et al. Cuticle integrity and biogenic amine synthesis in Caenorhabditis elegans require the cofactor tetrahydrobiopterin (BH4). Genetics. 200 (1), 237-253 (2015).
- Li, Y., Paik, Y. K. A potential role for fatty acid biosynthesis genes during molting and cuticle formation in Caenorhabditis elegans. BMB Reports. 44 (4), 285-290 (2011).
- Meli, V. S., Osuna, B., Ruvkun, G., Frand, A. R. MLT-10 Defines a Family of DUF644 and Proline-rich Repeat Proteins Involved in the Molting Cycle of Caenorhabditis elegans. Molecular Biology of the Cell. 21 (10), 1648-1661 (2010).
- Fritz, J. A., Behm, C. A. CUTI-1: A novel tetraspan protein involved in C. elegans CUTicle formation and epithelial integrity. PloS One. 4 (4), 5117 (2009).
- Golden, J., Riddle, D. A pheromone influences larval development in the nematode Caenorhabditis elegans. Science. 218 (4572), 578-580 (1982).
- Jeong, P. Y., et al. Chemical structure and biological activity of the Caenorhabditis elegans dauer-inducing pheromone. Nature. 433 (7025), 541-545 (2005).
- Srinivasan, J., et al. A blend of small molecules regulates both mating and development in Caenorhabditis elegans. Nature. 454 (7208), 1115-1118 (2008).
- Kaplan, F., et al. Ascaroside Expression in Caenorhabditis elegans Is Strongly Dependent on Diet and Developmental Stage. PLoS One. 6 (3), 17804 (2011).
- Golden, J., Riddle, D. A pheromone influences larval development in the nematode Caenorhabditis elegans. Science. 218 (4572), 578-580 (1982).
- Çelen, &. #. 3. 0. 4. ;., Doh, J. H., Sabanayagam, C. R. Effects of liquid cultivation on gene expression and phenotype of C. elegans. BMC Genomics. 19 (1), 562 (2018).
- Andersen, E. C., Bloom, J. S., Gerke, J. P., Kruglyak, L. A Variant in the Neuropeptide Receptor npr-1 is a Major Determinant of Caenorhabditis elegans Growth and Physiology. PLoS Genetics. 10 (2), 1004156 (2014).
- Rosenblatt, M. A central limit theorem and a strong mixing condition. Proceedings of the National Academy of Sciences. 42 (1), 43-47 (1956).
- Boyd, W. A., Smith, M. V., Freedman, J. H. Caenorhabditis elegans as a model in developmental toxicology. Methods in Molecular Biology. 889, 15-24 (2012).
- Nika, L., Gibson, T., Konkus, R., Karp, X. Fluorescent Beads Are a Versatile Tool for Staging Caenorhabditis elegans in Different Life Histories. Genes, Genomes, Genetics. 6 (7), 1923-1933 (2016).
- Denver, D. R., Morris, K., Streelman, J. T., Kim, S. K., Lynch, M., Thomas, W. K. The transcriptional consequences of mutation and natural selection in Caenorhabditis elegans. Nature Genetics. 37 (5), 544-548 (2005).
- Massie, M. R., Lapoczka, E. M., Boggs, K. D., Stine, K. E., White, G. E. Exposure to the metabolic inhibitor sodium azide induces stress protein expression and thermotolerance in the nematode Caenorhabditis elegans. Cell Stress & Chaperones. 8 (1), 1-7 (2003).
- Kevin, S., Pulak, R., Strange, K. Techniques for Analysis, Sorting, and Dispensing of C. elegans on the COPAS Flow-Sorting System. C. elegans. Methods in Molecular Biology. 351, 275-286 (2006).
- Lee, D., et al. Selection and gene flow shape niche-associated variation in pheromone response. Nature Ecology & Evolution. 3 (10), 1455-1463 (2019).
- Cook, D. E., Zdraljevic, S., Roberts, J. P., Andersen, E. C. CeNDR, the Caenorhabditis elegans natural diversity resource. Nucleic Acids Research. 45, 650-657 (2016).
- Nika, L., Gibson, T., Konkus, R., Karp, X. Fluorescent Beads Are a Versatile Tool for Staging Caenorhabditis elegans in Different Life Histories. Genes, Genomes, Genetics. 6 (7), 1923-1933 (2016).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados