Method Article
체외(In Vitro ) 티타늄 실린더에 사용되는 Er, Cr : YSGG 및 다이오드 레이저의 효과 평가
요약
본 연구에서는 Er,Cr:YSGG 및 다이오드 레이저를 총 96개의 특수 설계된 티타늄 실린더의 평면에 별도로 적용했습니다. 다른 표면에 열전대를 놓고 온도를 측정했습니다. 프로파일로미터, SEM 및 AFM으로 분석된 표면 거칠기.
초록
임플란트 주위 질환은 치과 임플란트와 관련된 중요한 문제입니다. 본 연구의 목적은 비수술적 임플란트 주위 질환 치료를 위해 티타늄 실린더에 다이오드와 에르븀, 크롬 도핑된 이트륨-스칸듐-갈륨-가넷(Er,Cr:YSGG) 레이저를 적용할 때의 표면 거칠기와 온도 변화를 평가하는 것입니다. 대조군을 포함한 총 13개 그룹을 940nm 다이오드(0.8 W-1.3 W-1.8 W) 및 Er,Cr:YSGG(1.5 W-2.5 W-3.5 W) 레이저로 20s/W 및 40 s/W의 6가지 출력 모드로 구성하고, 각 그룹별로 8개의 티타늄 실린더를 처리했습니다. 이 과정에서 초기 및 최종 온도는 실린더의 정점 슬롯에 배치된 열전대를 사용하여 기록되었습니다. 적용 후 모든 디스크의 거칠기(Ra)를 프로파일로미터로 측정했습니다. 표면은 2차원 및 3차원 표면 검사를 위해 주사 전자 현미경(SEM)과 원자력 현미경(AFM)으로 스캔되었습니다. 조사 중 티타늄 실린더의 온도 변화를 평가한 결과, 다이오드 레이저를 40초 동안 조사한 실린더는 20초 동안 조사한 실린더보다 유의하게 높았습니다. Er, Cr : YSGG 처리 된 실린더에서 일부 샘플에서는 온도가 감소하고 일부 샘플에서는 최소한으로 증가했습니다. 프로파일로미터 값(Ra)은 모든 그룹의 거칠기 측면에서 통계적으로 유의하지 않았습니다. 그러나 SEM 이미지는 처리된 표면에서 녹고 미세 기공의 수가 증가하는 것을 보여주었습니다. 이 시험관 내 연구의 한계로 인해 Er, Cr: YSGG 및 다이오드의 적용은 특히 열 안전성 측면에서 임플란트 주위염 관리를 위한 안전한 접근 방식으로 간주될 수 있습니다. 표면 거칠기는 변하지 않았지만 이러한 레이저를 사용하면 Ti 실린더 지형에서 용융 변화와 미세 기공이 발생했습니다. 이러한 레이저 설정이 박테리아 감소 및 골유착에 어떤 영향을 미치는지 확인하려면 추가 연구가 필요합니다.
서문
치과 임플란트는 손실된 치아를 대체하기 위해 일반적으로 허용되는 치료 옵션입니다 1,2. 임플란트 주위 점막염 및 임플란트 주위 염은 임플란트 주위 질환으로 분류됩니다. 임플란트 주위 점막염은 연조직에 국한되어 있으며, 생리학적 뼈 재형성을 제외하고는 뼈 손실의 증거가 없습니다. 임플란트 주위염은 플라크와 관련이 있으며 치과 임플란트 주변 조직에 영향을 미치는 병리학적 상태입니다. 그것은 임플란트 주위 점막의 염증과 그에 따른 지지하는 뼈의 손실이 증가하는 것으로 구별됩니다3. 장애의 시작과 진행에 대한 주요 병인학적 요인은 임플란트 주위 플라크 생물막의 파괴입니다4. 임플란트 주위 질환에 대한 수많은 연구에 따르면 임플란트 주위 점막염(PIM)의 유병률은 9.7%에서 64.6%까지인 반면, 임플란트 주위염(P)의 유병률은 4.7%에서 45% 사이입니다5.
플라크 축적은 임플란트 주위염을 유발하는 주요 병인학적 요인이지만, 임플란트의 다양한 지형적 특성으로 인해 치료가 복잡합니다. 비수술적 임플란트 주위염 치료의 기본은 임플란트 표면의 괴사조직 제거와 부착된 생물막을 제거하여 박테리아 부하를 질병 유발 임계값 이하로 감소시키는 감염 관리입니다 6,7. 티타늄 계면과 뼈 결함 해부학의 복잡한 미시적 및 거시적 지형은 표면 오염 제거를 제한합니다. 다양한 기계적(큐렛, 초음파 장치, 공기-분말 마모, 티타늄 브러시), 화학적(구연산, 클로르헥시딘, 항균제) 및 물리적(레이저, 광역학 요법) 오염 제거 기술의 효능을 조합하여 평가했습니다8. 현재 연구에 따르면 임플란트 주위염에 대한 비수술적 중재 기법을 병용하는 것이 괴사조직 제거술만 사용하는 것보다 더 효과적이라고 한다9. 기계적 치료에 화학적 항균제 또는 국소적/전신 항생제를 통합하면 상당한 효능이 입증되었습니다. 그럼에도 불구하고 이러한 개입은 가능한 부작용을 초래할 수 있다10. 레이저 기술이 발전함에 따라 치과용 레이저는 임플란트 표면에 대한 항감염, 해독 및 사용자 친화적 효과로 인해 점점 더 인기를 얻고 있습니다10,11.
흡수 피크, 장치의 작동 모드 및 조직 특성은 레이저 조사 중 열 증가에 영향을 미칩니다. 중요한 전임상 조사에 따르면 50°C까지 1분 동안 온도를 높이면 혈관 손상이 발생하고, 60°C까지 올라가면 혈류가 중단되고 뼈 괴사가 발생하는 것으로 밝혀졌다12. 시험관 조사에 따르면 다이오드 레이저를 10초만 조사하면 임플란트 표면이 뼈 안전 임계값(10°C)보다 높은 온도에 도달할 수 있습니다. 뼈의 생존력은 단지 10°C의 온도 상승만으로도 손상될 수 있다13.
최근의 수많은 연구는 이 영역에서 레이저의 유익한 영향을 조사하는 데 집중되었습니다 14,15,16,17,18. 다양한 레이저 파장은 적절한 매개변수가 적용될 때 임플란트 표면에 상당한 항균 효과와 안전성을 보여줍니다. 강도, 빈도 및 파장을 포함한 여러 변수가 레이저 치료의 효능에 영향을 미칩니다. 여러 연구에서 CO2, Er:YAG, Er, Cr: YSGG 및 다양한 다이오드 레이저를 포함한 다양한 레이저 파장의 살균 효과를 입증했으며, 이를 통해 임플란트 주위염 치료에서 다양한 레이저의 유익한 효과를 확인할 수 있습니다. 아오키 외 19,20,21. 연구진의 검토를 통해 레이저 적용은 재생 요법을 포함한 비수술적 및 외과적 임플란트 주위 치료 모두에서 표면 세척을 촉진하고 주변 조직 세포를 활성화하여 치유를 촉진한다는 결론을 내렸습니다22.
다이오드 레이저는 임플란트의 표면 패턴에 영향을 주지 않고 임플란트 표면에 살균 효과를 발휘할 수 있습니다. 임플란트 주위염 치료에 관해서는 다이오드 레이저가 치주 조직의 치유를 촉진하기 때문에 갈 길이 될 수 있습니다 23,24,25.
에르븀, 크롬 도핑: 이트륨, 스칸듐, 갈륨, 석류석(Er,Cr:YSGG) 레이저는 생물막을 제거하고 임플란트 표면의 오염을 제거하는 데 효과적인 특성을 나타냅니다11. 강력한 살균 효과와 뼈 재생 특성은 수력 특성 덕분에 기계적 손상을 일으키지 않고 에르븀 레이저에 의해 입증되었습니다11, 14.
티타늄 임플란트에 대한 레이저 조사로 인한 변화에 관한 데이터는 부족합니다. 더욱이, 티타늄 표면의 조사에 대한 명확한 방법론은 아직 정의되지 않았으며, 이는 전력 및 적용 시간과 같은 레이저 매개변수를 포함합니다. 이전 연구에서는 Er, Cr : YSGG 레이저16 적용이 온도 변화에 영향을 미치지 않는 것으로 나타났지만 다이오드 레이저 연구는13을 초과하여 임계 값16,26을 초과하지 않았습니다. 티타늄 표면의 Ra 값에 대한 레이저 처리의 효과에 대한 다양한 결과는 문헌18,27에서 확인할 수 있습니다. 본 연구의 귀무가설은 Er, Cr:YSGG 레이저, 다이오드 레이저 간에 티타늄 표면의 온도 및 거칠기 변화 측면에서 차이가 없다는 것입니다. 본 연구는 다양한 시간 및 전력 설정에서 Er, Cr:YSGG 및 다이오드 레이저를 사용하여 티타늄 소재의 표면 거칠기 및 온도 변화를 모니터링하여 안전한 작동 매개변수를 결정하는 것을 목표로 했습니다. 온도 변화 평가는 열전대를 사용하여 수행하고, 프로파일 로미터를 사용하여 표면 거칠기를 평가하고, SEM 및 AFM 기술을 통해 표면 변화를 분석했습니다.
프로토콜
참고: 기존 임플란트와 동일한 소재로 제작되고 SLA 기술로 임플란트 표면을 복제하도록 설계된 티타늄 실린더는 높이가 10mm이고 직경이 5mm입니다. 깊이 7mm, 너비 3mm의 캐비티가 실린더 중앙에 위치합니다(그림 2). 3mm의 너비는 가장 깊은 지점에서 1mm로 줄어듭니다. 프로파일로미터로 표준 임플란트의 표면 거칠기를 측정하는 것은 불가능합니다. 임플란트 표면을 시뮬레이션하는 것과 동일한 재료를 사용하여 제조업체가 설계한 티타늄 실린더 상단의 5mm 직경의 평평한 표면에 적용된 레이저의 효과를 평가할 수 있었습니다. 또한 실린더 중심에서 온도 변화를 측정하기 위해 티타늄 실린더의 바닥 표면 중심에서 열전대 팁이 배치될 실린더 깊이를 향해 깊이 7mm, 너비 3mm의 홈이 만들어졌습니다. 이 홈을 사용하면 외부 표면에 의존하지 않고 실린더 내부에서 처리된 표면의 온도 변화를 평가할 수 있습니다. 3차원 영상은 원자력 현미경(Atomic Force Microscope, AFM)을 사용하여 특별히 제작된 티타늄 실린더의 평평한 표면을 분석하여 얻었습니다. 940nm 다이오드(0.8 W28, 1.3 W29, 1.8 W30) 및 2.780 nm Er,Cr:YSGG(1.5 W31, 2.5 W31, 3.5 W32) 레이저를 회사 권장 사항에 따라 세 가지 다른 와트수로 사용했으며, 각각 20초 및 40초 적용 시간으로 12개 그룹을 구성했습니다. 적용 후 거칠기 평가를 위해 제어 그룹이 추가되었습니다. 손가락 지지대가 있는 스탠드는 적용하는 동안 Ti 실린더를 안정적으로 유지하기 위해 3차원 프린터에서 인쇄되었습니다(재료 표).
1. 샘플 크기
- G*Power 프로그램의 검정력 해석을 사용하여 표본 크기를 계산합니다. 각 그룹에 대한 최소 샘플 수는 효과 크기 d: 0.6906, 표준 편차 16.8, 검정력: 0.80 및 α: 0.05로 온도 변화에 대한 n=8 샘플로 결정되었습니다.
참고: 이 연구에서는 300μm 직경의 팁(e3 팁)과 360° 발사 탄성 RFPT5-14 팁(580μm 직경 및 14mm 길이)의 940nm 다이오드 레이저가 장착된 Er,Cr:YSGG 레이저를 레이저 시스템으로 사용했습니다(그림 1).
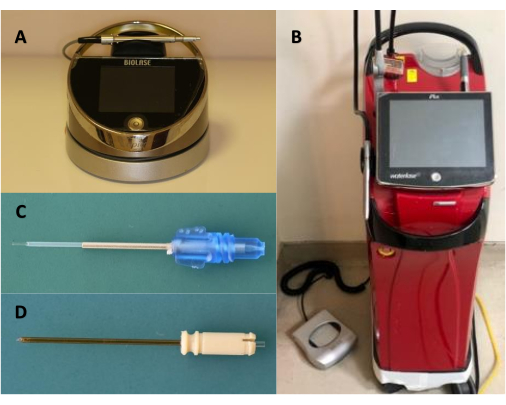
그림 1: 사용된 기기 및 장비. (A) 다이오드 레이저, (B) Er,Cr:YSGG 레이저, (C) E3 팁, (D) RPTF5-14 팁. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
2. 실무 그룹 결정
- 임플란트 주위 점막염에 주머니 내 적용을 위해 권장되는 Watt of lasers를 이상적인 사용 조건으로 사용하십시오. 또한 권장 와트에 비해 연구 그룹에 하나의 낮은 값과 하나의 높은 값을 포함합니다. 여기서 사용한 값은 Er, Cr:YSGG의 경우 1.5W, 3.5W, 다이오드 레이저의 경우 0.8W와 1.8W입니다.
- 작동 시간이 온도 변화에 미치는 영향을 평가하기 위해 적용 시간을 20초 및 40초로 결정합니다. 스터디 그룹은 표 1에 나와 있습니다.
| 그룹 이름 | 레이저 유형 | 샘플 수(n) | 와트 (W) | 시간 (초) |
| E1 | 어, 크롬: YSGG | 8 | 1.5 W | 20 |
| E2 | 8 | 2.5 W | 20 | |
| 3회 | 8 | 3.5 W | 20 | |
| 4회 | 8 | 1.5 W | 40 | |
| 5회 | 8 | 2.5 W | 40 | |
| 6회 | 8 | 3.5 W | 40 | |
| 디1 | 다이오드 | 8 | 0.8 W | 20 |
| D2 | 8 | 1.3 W | 20 | |
| 3일차 | 8 | 1.8 W | 20 | |
| 4일차 | 8 | 0.8 W | 40 | |
| 5일차 | 8 | 1.3 W | 40 | |
| 6일차 | 8 | 1.8 W | 40 | |
| C | 제어 | 8 |
표 1: 스터디 그룹 정보.
3. 실험 설정 준비
- Rhinoceros (3D 그래픽 및 디자인) 프로그램을 사용하여 직경 10mm, 두께 5mm의 캐비티가있는 3D로 실린더 스탠드를 설계하십시오.
- 앱을 엽니다. 지름 10mm의 원을 그립니다. 한 축에서 원을 50% 줄여 타원을 만듭니다. Extuder를 누르고 타원을 3차원으로 올립니다.
- 손가락을 지지하기 위해 다시 원을 그립니다. 압출기 키를 사용하여 3차원에서 두 번째 원을 올립니다. 높이를 첫 번째 원보다 작게 만듭니다.
- 부울 명령을 사용하여 타원형 도면에 10mm 구멍을 드릴합니다. 열전대 지원의 경우, 스윕 1 명령으로 L자형 선을 만들고 3차원을 작성합니다.
- 사각형을 그리고, 압출기 명령으로 3차원으로 확대한 후, 베이스를 만듭니다. 디자인을 인쇄한 후 Ti 실린더가 올 구멍 주위에 실리콘을 바르고 건조시킵니다. 이렇게 하면 레이저가 적용되는 동안 실린더가 제자리에 유지됩니다.
- 에어컨이 있는 밀폐된 방을 27°C의 온도로 가져오십시오. 실린더가 고정될 스탠드를 양면 테이프로 플라스틱 통 중앙에 고정합니다.
알림: Ti 실린더를 삽입하고 표면에 공기를 짜냅니다. - 온도계의 열전대를 스탠드의 슬롯에 있는 Ti 실린더의 속이 빈 부분에 놓습니다.
- 적용 시간을 추적하기 위해 크로노미터를 준비합니다. 3번째 관찰자가 각도를 기록하고 스톱워치로 시간을 추적합니다.
4. 실험 절차
- 레이저를 적용하는 동안 시술자의 안전을 위해 보호 안경을 착용하십시오. Er,Cr:YSGG 레이저용 RPTF5-14 팁을 삽입합니다. 다이오드 레이저용 팁 E3 삽입.
- Er,Cr:YSGG 레이저를 켭니다. Perio 폐쇄 모드를 선택합니다. 1.5W, 2.5W 및 3.5W 레이저를 각각 20초 및 40초 동안 적용합니다. 레이저가 적용된 96개의 Ti 실린더가 있습니다. Ti 실린더에 하나의 레이저 유형, 1와트, 1회만 조사합니다.
- 다이오드 레이저를 켭니다. Perio Pocket Mode를 선택합니다. 0.8W, 1.3W 및 1.8W 레이저를 각각 20초 및 40초 동안 적용합니다.
- 레이저가 시작될 때 3번째 관찰자가 타이머를 시작하도록 합니다. 시간이 다 되면 경고하십시오.
- 레이저 팁을 표면에 15° 각도로 적용하고 접촉하여 계획된 시간 동안 전체 표면을 지그재그로 적용합니다.
- 적용하는 동안 초기 및 최종 온도 값을 기록하십시오. 끝 온도 값에서 시작 온도 값을 뺍니다. 온도 변화를 계산합니다.
참고: 총 12개 그룹, 6개의 Er, Cr:YSGG 및 6개의 다이오드 레이저 그룹에 대한 온도 변화 값을 확인합니다. - 그룹 번호가 적힌 투명 백에 샘플을 보관하십시오.
5. 재료의 2차원 및 3차원 이미징
- 주사전자현미경(SEM) 및 원자력 현미경(AFM) 분석을 수행하여 Ti 실린더 표면의 형태 변화를 평가하고 시연합니다.
참고: FEI Quanta FEG 250 기기가 사용되었습니다. - SEM에 넣기 전에 샘플을 코팅하지 마십시오. 1 개의 제어 그룹, 6 개의 다이오드 레이저 그룹 및 6 개의 Er, Cr : YSGG 레이저 그룹을 포함하여 13 개의 그룹이 있습니다. 대조군의 경우 처리를 수행하지 않고 AFM 및 SEM으로만 표면 이미지를 촬영합니다.
- 13개의 연구 그룹 각각에서 하나의 실린더를 무작위로 선택합니다. SEM 장치에 삽입합니다. 샘플이 혼합되지 않도록 플랫폼과 샘플 코드의 위치를 기록해 둡니다.
- Ti 실린더를 평평한 표면이 위로 향하게 하여 SEM 장치에 놓습니다. 저진공 모드를 사용하여 분석을 수행합니다. 해석 중에 챔버 압력을 60Pa로 설정합니다.
- 장치가 완전히 준비되면 평평한 표면의 임의의 지점에서 250배, 1000배 및 5000배 배율로 이미지를 기록합니다. 모든 샘플에 대해 이 절차를 반복합니다.
알림: SEM 장치가 진공 청소를 마치면 이미지를 수집할 준비가 된 것입니다. - AFM 측정의 경우 각 연구 그룹에서 하나의 Ti 실린더를 무작위로 선택합니다. 태핑 모드에서 측정을 수행합니다.
- Ti 실린더를 AFM 기기에 놓습니다. 기기의 끝이 샘플 위에 오도록 상단 덮개를 놓습니다. 기기 창의 빨간색 표시등이 이미징할 표면에 있는지 확인합니다.
- 전압을 2로 설정합니다. Auto land 버튼을 사용하여 팁을 샘플에 더 가깝게 이동합니다. 스캔 시작 버튼을 눌러 스캔을 시작합니다.
- 각 샘플에 대해 5μm x 5μm 디지털 이미지를 가져와 느린 스캔 속도(1Hz)로 기록합니다. Ti 실린더의 평평한 표면에서 AFM 기기로 촬영한 이미지를 기록합니다. AFM 기기는 25μm2 면적을 시각화합니다.
6. 표면 거칠기 측정
참고: Surftest SJ 201, Mitutoyo, Tokyo, Japan, 장치가 여기에 사용되었습니다.
- 프로파일로미터의 해상도를 0.01mm로, 가로 길이를 3.0mm로, 다이아몬드 레코딩 핀 팁의 직경을 5μm로 설정합니다. 측정 속도를 0.5mm/s로 설정하여 Ra 값을 결정합니다.
- Ti 실린더를 홀더로 고정하고 프리셀을 사용하고 Ti 실린더를 측면에서 잡고 고정합니다. 프로파일로미터의 바늘을 Ti 표면과 접촉하게 놓습니다.
- 시작 버튼을 누릅니다. 찾은 Ra 값을 저장합니다. 각 실린더의 평평한 표면에서 다른 방향으로 5회 측정을 반복합니다(그림 2). 다양한 방향을 얻으려면 사전 판매를 통해 Ti 실린더를 자체 주위로 움직입니다. Ti 원통의 전체 길이에 대해 반복합니다.
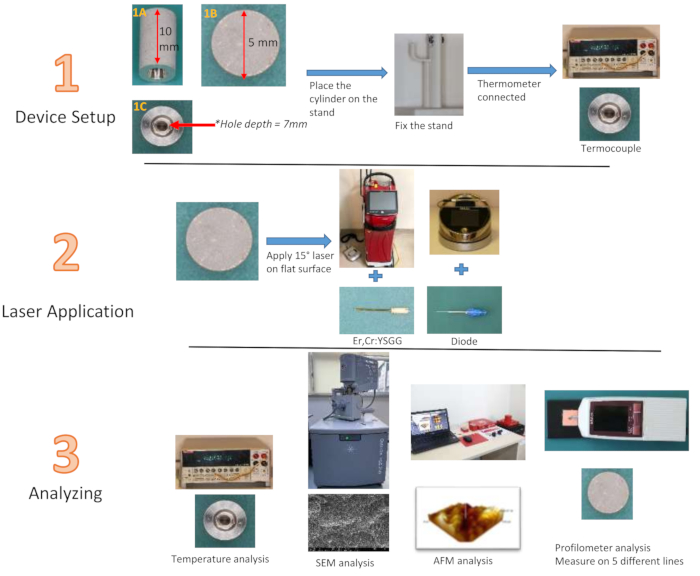
그림 2: 스터디 그룹의 순서도. (1A) Ti 실린더 측면 뷰, (1B) 상단 뷰, (1C) 하단 뷰 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
7. 통계 분석
- SPSS-Windows 통계 패키지 프로그램을 사용하여 통계 분석을 수행하고 Kruskal-Wallis 및 Mann-Whitney 테스트를 적용합니다. 통계적 신뢰 수준을 95%(α = 0.05)로 설정합니다.
결과
적용 시간 20초와 40초를 기준으로 평가한 결과, 통계적으로 유의미한 차이가 관찰되었습니다. 40초 레이저가 적용된 Ti 실린더 표면의 온도 변화는 20초 레이저가 적용된 온도보다 더 큰 것으로 관찰되었습니다(p=0.037; 그림 3).

그림 3: 모든 샘플의 시간에 따른 온도 변화. 상자에서 위아래로 이어지는 선은 데이터의 최소값과 최대값을 보여줍니다. 상자 안의 가로선은 데이터의 중앙값을 나타냅니다. 둥근 표시는 이상치입니다.
a=40대 그룹과 비교해 통계적으로 유의한 차이. (0,05<쪽)
이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
온도 변화는 레이저 유형(Er, Cr: YSGG 및 다이오드)에 따라 두 그룹으로 분류하여 분석했습니다. 다이오드 레이저를 사용한 Ti 실린더의 온도 변화는 Er,Cr:YSGG 레이저를 적용한 실린더의 온도 변화보다 큰 것으로 관찰되었습니다. 결과는 통계적으로 유의합니다(p=0.001, 그림 4 참조). 다이오드 레이저 적용에만 테스트된 Ti 실린더의 평가에서, 결과는 40초 다이오드 레이저 적용이 모든 와트 값에서 20초 적용에 비해 훨씬 더 높은 결과를 산출하는 것으로 나타났습니다(p < 0.001; 그림 4). 그림의 상자 안에 있는 빨간색 선은 중앙값을 나타냅니다. 상단과 하단의 막대는 최대 및 최소 온도 값을 나타냅니다.

그림 4: 모든 샘플에 대한 레이저 유형 및 시간에 따른 온도 변화. 상자에서 위아래로 이어지는 선은 데이터의 최소값과 최대값을 보여줍니다. 상자 안의 가로선은 데이터의 중앙값을 나타냅니다. 둥근 표시는 이상치입니다.
a=다이오드 그룹과 비교하여 통계적으로 유의미한 차이. (0,05<쪽)
b= 다이오드 레이저 40초와 비교하여 통계적으로 유의한 차이 (p<0,05)
이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
온도 변화에 대한 최신 통계 평가는 와트 값을 기반으로 수행되었습니다. Er,Cr:YSGG 레이저를 사용한 그룹에서 와트 값(p < 0.001) 및 와트 시간(p < 0.001) 매개변수만 조사할 때 상당한 차이가 관찰되었습니다. Er,Cr:YSGG 레이저의 적용에서 시간 자체는 온도 변화에 큰 영향을 미치지 않는 것으로 관찰되었습니다(p=0.959). 다이오드 레이저에 노출된 모든 Ti 실린더의 온도 변화를 평가한 결과, 와트, 시간 및 와트 시간 변수를 고려하여 통계적으로 유의미한 차이가 관찰되었습니다(p < 0.05). Ti 실린더 표면에 1.8W가 적용된 다이오드 레이저 그룹의 온도 범위는 0.8W가 적용된 다이오드 레이저 그룹의 온도 범위보다 현저히 컸습니다(p = 0.006; 그림 5).
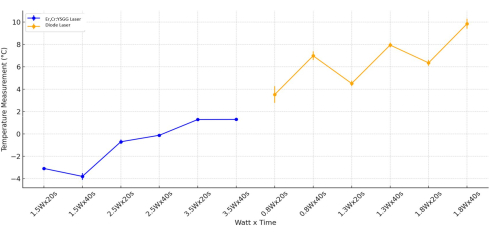
그림 5: 결합된 온도 분석. Er, Cr:YSGG 및 다이오드 레이저 유형에 대한 분석은 Watt 및 Time에 의해 수행되었습니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
이미징 분석
SEM 이미지에서는 모든 그룹에서 미크론 크기의 다공성 구조가 관찰되었으며, 이는 샌드블라스팅되고 산이 거칠어진 임플란트 표면의 예상되는 모양입니다. 5000배 배율에서 레이저 처리된 티타늄 표면은 대조군(빨간색 원)에 비해 미크론 크기의 기공이 눈에 띄게 확대된 것으로 나타났습니다. 250배 및 1000배 배율에서 Er, Cr:YSGG 및 다이오드 레이저로 40초 동안 처리된 티타늄 표면은 20초 동안 처리된 것보다 더 많은 용융을 보였습니다(그림 6). AFM 이미지에서 대조군의 표면 압흔 분포는 레이저 처리된 그룹보다 더 균일했습니다(그림 7, 그림 8). AFM 이미지는 티타늄 실린더의 평평한 표면에서 25μm2의 매우 작은 영역만 시각화했기 때문에 전체 표면에 대한 자세한 결과를 얻을 수 없었습니다.

그림 6: 모든 연구 그룹의 SEM 이미지. 6개의 다이오드 레이저 그룹은 D1-D6으로 표시되고 6개의 Er,Cr: YSGG 레이저 그룹은 E1-E6으로 표시됩니다. 이미지는 250배, 1000배, 5000배, 배율로 촬영됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 7: 대조군의 AFM 이미지. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 8: 모든 연구 그룹의 AFM 이미지. 6개의 다이오드 레이저 그룹은 D1-D6으로 표시되고 6개의 Er,Cr: YSGG 레이저 그룹은 E1-E6으로 표시됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
표면 거칠기 결과
거칠기 매개변수는 레이저 유형(p = 0.841), 와트(p = 0.900), 시간(p = 0.399) 변수와 레이저 유형, 와트 및 시간 변수를 함께 평가(p = 0.924; 그림 9).

그림 9: 레이저 유형, 와트 및 시간별 거칠기 분석. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
이러한 결과를 고려할 때 Er, Cr:YSGG 및 다이오드 레이저가 임플란트 주위 질환에서 티타늄 표면의 오염을 제거하는 데 안전하다는 결론을 내릴 수 있습니다. 온도 변화는 10°C 미만이었으며, 이는 매개변수가 안전 범위 내에 있음을 나타냅니다. 동시에 프로파일로미터 값은 크게 변하지 않았으며, 이는 표면 거칠기 측면에서 단점이 없음을 나타냅니다. 이미징 분석에서 얼굴 변화가 감지되었지만 거칠기 분석으로 뒷받침될 수 없었습니다. 연구 결과는 사용된 레이저 매개변수가 안전 범위 내에 있음을 뒷받침합니다.
a=다이오드 그룹과 비교하여 통계적으로 유의미한 차이. (0,05<쪽)
b= 다이오드 레이저 40초와 비교하여 통계적으로 유의한 차이 (p<0,05)
토론
임플란트 주위염 치료에서 임플란트 표면의 오염을 제거하는 최적의 방법에 대한 중요한 논의가 진행 중입니다. 이전 간행물에서는 국소 또는 전신 의약품의 활용, 레이저 적용, 기계 및/또는 화학적 세척, 임플란토플라스티(implantoplasty)를 제안했습니다. 우리의 연구 결과에 따르면 측정된 모든 온도는 10°C의 임계 안전 임계값13 미만으로 상승합니다. 그러나 본 연구는 in vitro 연구이며 항상 임상 조건을 재현할 수 없다는 점을 염두에 두고 Er,Cr:YSGG 레이저와 다이오드 레이저의 사용은 임플란트 지형에서 용융 변화와 미세 기공을 유발하는 반면 표면 거칠기는 변하지 않는 것으로 관찰되었습니다.
오염 제거를 위한 Ho:YAG 및 Nd:YAG33 레이저의 사용은 표면 효과로 인해 부적절한 것으로 보고되었습니다. 그러나, Er,Cr:YSGG 레이저(34)와 다이오드 레이저(18)가 이러한 목적에 효과적인 것으로 밝혀졌다. 다이오드 레이저는 TGF-β1 신호에 의해 자극된 HBD-2 발현을 통해 주변 조직의 치유를 향상시킵니다. 이 연구는 티타늄 표면에 Er,Cr:YSGG 레이저를 지그재그 동작으로 적용한 후 섬유아세포 생존력 및 조골세포 분화의 증가와 함께 표면 거칠기 및 P. gingivalis 집락화의 감소를 밝혔습니다35. 이 연구의 결과는 Er, Cr : YSGG 레이저가 최대 3.5W에서 최대 40 초의 에너지 설정에서 티타늄 표면에 열 손상을 일으키지 않음을 보여주었습니다. 이 발견은 Smeo et al.36에서 발표한 문헌 검토와 관련이 있으며, 이 문헌 검토에서는 에르븀 레이저가 올바른 레이저 매개변수와 함께 사용할 때 임계 온도 임계값을 초과하지 않고 항균 효과를 발휘할 수 있다고 결정했습니다.
이 조사에서 940nm 다이오드 레이저 매개변수는 0.8W, 1.3W 및 1.8W였으며, 여기에는 20초 및 40초의 서로 다른 전력 출력 및 조사 시간이 포함되었습니다13. 티타늄 표면에 다이오드 레이저의 사용을 평가하는 두 가지 다른 연구에서 20초37 및 40초38이 적용 시간으로 사용되었습니다. 유사하게, 티타늄 및 치아 표면에 적용된 Er,Cr:YSGG 레이저는 20초39 및 40초40의 적용 시간으로 사용되었습니다. 한 연구에서 다이오드 레이저는 18초 만에 임계 온도를 초과했습니다13. 다이오드 레이저 응용 분야에서는 펄프(임계 임계값 5.6°C)의 열 손상을 방지하기 위해 뿌리 표면에 장기간 노출되지 않는 것이 좋습니다(임계 임계값 5.6°C)28,41. 티타늄 표면의 온도 변화에 대한 다양한 레이저의 사용의 영향을 평가한 연구는 Er:YAG, CO2, Nd:YAG 및 다이오드 레이저가 물탱크에서 10°C의 임계 온도 변화를 초과하지 않는다고 보고했다(42). 마찬가지로, 이 연구에서 940nm 다이오드 레이저 그룹은 훨씬 더 빠른 온도 상승을 생성했습니다. 그러나 최종 온도 값은 임계 임계값 미만이었습니다. 940nm 다이오드 레이저의 응용 분야에서는 감소된 전력 출력을 선택하고 조사 시간을 최소화함으로써 온도 상승을 줄일 수 있습니다. 이러한 결과는 수냉식이 없을 때 증가된 전력/에너지 밀도 13,43,44와 상승된 온도 사이에 양의 관계가 있음을 나타내며, Er,Cr:YSGG 레이저 16,45와 같은 조사 중 수냉의 중요성을 강조합니다.
기계 및 3D 광학(접촉식 및 비접촉식) 형상 측정법은 치과 재료 나노 형상 및 임플란트 표면 거칠기의 정량적 측정을 위한 가장 인기 있는 체외 방법이며, SEM 이미지는 정성적 평가를 위한 황금 표준입니다31. 접촉식 프로파일로미터로 거칠기를 측정하면 표면이 손상되고 부정확한 측정이 발생할 수 있습니다46. SEM 이미징은 샘플의 정량적 및 정성적 분석을 용이하게 할 수 없었지만, AFM 이미지는 표면 거칠기 및 3D 깊이 측면에서 정량적 정보를 제공할 수 있었습니다47. 레이저 치료 후 임플란트 표면에서 형태학적 변화가 관찰되었으며, 이는 대조군에 비해 미세공의 직경이 증가하고, 형태가 용융되며, 움푹 들어간 미세공의 유병률이 증가하는 것을 특징으로 합니다. 이러한 실험 조건에서 SEM 분석 중 Ti 실린더의 표면은 표면 변화를 나타냈습니다. 더욱이, 이러한 변경은 레이저 유형, 사용된 전력 및 레이저 조사에 소요된 시간의 영향을 받았습니다. 저자들은 다이오드18 및 Er,Cr:YSGG21,48 레이저의 표면 손상 수준과 시간이 출력 증가와 상관관계가 있다는 결론에 동의했습니다. 추가 연구에서는 이러한 변형이 치료적 영향을 미치는지 조사해야 한다.
미세지형(microtopography)이라고도 하는 치과 임플란트 표면 거칠기는 골유착에 영향을 미치는 중요한 요소입니다. 최근 연구에서 티타늄 표면은 4가지 프로토콜로 처리되었습니다. 레이저 처리된 표면에 티타늄 표면 및 중간엽 줄기세포가 보존되었으며 줄기세포 접착 결과는 다른 기술(Ti-Ni 브러시, 공기 흐름 및 치과 버)보다 우수했습니다49. 조사된 Ti 실린더의 모든 Ra 값은 레이저 조사 중에 감소되었습니다. 그러나 방사선 조사 전과 후에 통계적으로 유의미한 차이는 나타나지 않았습니다. 다이오드 레이저 조사는 더 큰 출력 수준이 사용되었을 때 Ti 표면을 녹여 표면 거칠기를 줄였습니다. 이러한 결과는 Stübinger et al.50의 이전 연구와 일치하며, 810nm 다이오드 레이저를 사용하여 임플란트 표면의 오염을 제거했으며 표면에 큰 영향을 미치지 않았으며 Kim et al.51 및 Rezeka et al.17이 수행한 연구 결과와 모순되며, 2W 및 3W 전력으로 처리했을 때 940nm 파장을 사용하고 레이저 적용으로 표면 거칠기가 증가하는 것을 관찰했습니다.
이 연구는 세포 및 미생물 검사가 부족하여 제한적입니다. 현재 연구는 다이오드 및 Er,Cr:YSGG 레이저 조사에 따른 Ti 실린더의 지형 변화를 평가하는 것을 목표로 합니다. 그럼에도 불구하고 다양한 치료법의 생물학적 의미는 추가 시험관 내 및 생체 내 조사가 필요합니다. 또 다른 한계는 이 연구에서 수행된 표면 거칠기의 통계적 분석에는 프로파일로미터 데이터만 포함된다는 것입니다. AFM 접근법은 치과에서 자주 사용되는 두 가지 레이저 유형의 효능을 평가하는 데 효과적인 것으로 입증되었습니다.
결론
우리의 조사에서 온도 상승 중 어느 것도 생리학적 임계값인 10°C를 초과하지 않았습니다. 결과적으로, 통계적으로 유의미한 온도 차이는 임상적으로 무관한 것으로 간주되었습니다. 레이저 유형과 출력은 RA에 큰 영향을 미치지 않았습니다. 따라서 0.8W, 1.3W, 1.8W 다이오드 레이저와 1.5W, 2.5W, 3.5W의 Er,Cr:YSGG 레이저를 20초 및 40초 동안 조사하면 Ti 표면을 손상 없이 청소할 수 있습니다. 그럼에도 불구하고 이러한 결과는 시험관에서 수행되었으며 이 연구의 결과를 검증하기 위해서는 임상 시험이 필요할 것입니다. 본 연구에서는 임플란트 괴사조직 제거의 임상 시나리오를 시뮬레이션하는 다양한 기법을 조사했습니다.
공개
저자는 공개할 이해 상충이 없습니다.
감사의 말
연구에 사용된 티타늄 실린더는 Naxis Implant에서 생산했습니다.
자료
| Name | Company | Catalog Number | Comments |
| Atomic Force Microscopy | ezAFM | Compact AFM Model | |
| Diode | Biolase | Epic 10, 940 nm Wavelength | |
| E3 Tip | Fiber Diameter: 300 µm, Fiber Length: 9 mm | ||
| Er,Cr:YSGG Laser | Iplus | 2780 nm Wavelength | |
| Profilometer | Mitutoyo | Surftest SJ-201 Model | |
| RFPT-14 Tip | Outer Tip Diameter: 580 µm, Tip Length: 14 mm | ||
| Scanning Electron Microscope | FEI | Quanta FEG 250 Model | |
| Stand | Custom Design | Rhinoceros application, Flamix PLA filament, Bambulab X1C Device | |
| Thermometer | Keithley | 2000 Series Model, K tip termokulp | |
| Titanium Cylinder | Naxis | 10 mm height, 5 mm diameter, SLA Surface, Titanium |
참고문헌
- Guillaume, B. Dental implants: A review. Morphologie. 100 (331), 189-198 (2016).
- Henry, P. J. Tooth loss and implant replacement. Aust Dent J. 45 (3), 150-172 (2000).
- Berglundh, T., Armitage, G., Araujo, M. G., et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 89 (1), S313-S318 (2018).
- Herrera, D., Berglundh, T., Schwarz, F., et al. Prevention and treatment of peri-implant diseases—The EFP S3 level clinical practice guideline. J Clin Periodontol. 50 (S26), 4-76 (2023).
- Guarnieri, R., Reda, R., Di Nardo, D., Pagnoni, F., Zanza, A., Testarelli, L. Prevalence of Peri-Implant Mucositis, Peri-Implantitis and Associated Risk Indicators of Implants with and without Laser-Microgrooved Collar Surface: A Long-Term (≥20 Years) Retrospective Study. J Pers Med. 14 (4), (2024).
- Figuero, E., Graziani, F., Sanz, I., Herrera, D., Sanz, M. Management of peri‐implant mucositis and peri‐implantitis. Periodontology 2000. 66 (1), 255-273 (2014).
- Tomasi, C., Wennström, J. L. Full-mouth treatment vs. the conventional staged approach for periodontal infection control. Periodontology 2000. 51 (1), 45-62 (2009).
- Baima, G., Citterio, F., Romandini, M., et al. Surface decontamination protocols for surgical treatment of peri‐implantitis: A systematic review with meta‐analysis. Clin Oral Implants Res. 33 (11), 1069-1086 (2022).
- Subramani, K., Wismeijer, D. Decontamination of titanium implant surface and re-osseointegration to treat peri-implantitis: a literature review. Int J Oral Maxillofac Implants. , Accessed August 4, 2024 (2012).
- Świder, K., Dominiak, M., Grzech-Leśniak, K., Matys, J. Effect of different laser wavelengths on periodontopathogens in peri-implantitis: A review of in vivo studies. Microorganisms. 7 (7), 189(2019).
- Mizutani, K., Aoki, A., Coluzzi, D., Yukna, R., Wang, C. Y., Pavlic, V., Izumi, Y. Lasers in minimally invasive periodontal and peri‐implant therapy. Periodontology 2000. 71 (1), 185-212 (2016).
- Eriksson, R. A., Albrektsson, T. The effect of heat on bone regeneration: An experimental study in the rabbit using the bone growth chamber. J Oral Maxillofac Surg. 42 (11), 705-711 (1984).
- Geminiani, A., Caton, J. G., Romanos, G. E. Temperature change during non-contact diode laser irradiation of implant surfaces. Lasers Med Sci. 27 (2), 339-342 (2012).
- Alpaslan Yayli, N. Z., Talmac, A. C., Keskin Tunc, S., Akbal, D., Altindal, D., Ertugrul, A. S. Erbium, chromium-doped: yttrium, scandium, gallium, garnet and diode lasers in the treatment of peri‐implantitis: Clinical and biochemical outcomes in a randomized-controlled clinical trial. Lasers Med Sci. 37 (1), 665-674 (2022).
- Peters, N., Tawse-Smith, A., Leichter, J., Tompkins, G. Laser therapy: The future of peri-implantitis management. J Periodontol. 22 (1), 1(2012).
- Alhaidary, D., Franzen, R., Hilgers, R. D., Gutknecht, N. First investigation of dual-wavelength lasers (2780 nm Er,Cr:YSGG and 940 nm diode) on implants in a simulating peri-implantitis situation regarding temperature changes in an in vitro pocket model. Photobiomodul Photomed Laser Surg. 37 (8), 508-514 (2019).
- Rezeka, M. A., Metwally, N. A., Abd El Rehim, S. S., Khamis, M. M. Evaluation of the effect of diode laser application on the hydrophilicity, surface topography, and chemical composition of titanium dental implant surface. J Prosthodont. 2024, 1-8 (2025).
- Khalil, M. I., Sakr, H. Implant surface topography following different laser treatments: An in vitro study. Cureus. 15 (5), e38731(2023).
- Tosun, E., Tasar, F., Strauss, R., Kivanc, D. G., Ungor, C. Comparative evaluation of antimicrobial effects of Er:YAG, diode, and CO2 on titanium discs: An experimental study. J Oral Maxillofac Surg. 70 (5), 1064-1069 (2012).
- Stübinger, S., Homann, F., Etter, C., Miskiewicz, M., Wieland, M., Sader, R. Effect of Er:YAG, CO and diode laser irradiation on surface properties of zirconia endosseous dental implants. Lasers Surg Med. 40 (3), 223-228 (2008).
- Park, J., Heo, S., Koak, J., Kim, S. K., Han, C. H., Lee, J. H. Effects of laser irradiation on machined and anodized titanium disks. Int J Oral Maxillofac Implants. 27 (6), Accessed September 22, 2024 1215-1221 (2012).
- Aoki, A., Mizutani, K., Schwarz, F., et al. Periodontal and peri-implant wound healing following laser therapy. Periodontol 2000. 68 (1), 217-269 (2015).
- Roncati, M., Lucchese, A., Carinci, F. Non-surgical treatment of peri-implantitis with the adjunctive use of an 810-nm diode laser. J Indian Soc Periodontol. 17 (6), 812-817 (2013).
- Romanos, G. E., Gutknecht, N., Dieter, S., Schwarz, F., Crespi, R., Sculean, A. Laser wavelengths and oral implantology. Lasers Med Sci. 24 (6), 961-970 (2009).
- Hauser-Gerspach, I., Stübinger, S., Meyer, J. Bactericidal effects of different laser systems on bacteria adhered to dental implant surfaces: An in vitro study comparing zirconia with titanium. Clin Oral Implants Res. 21 (3), 277-283 (2010).
- Hafeez, M., Calce, L., Hong, H., Hou, W., Romanos, G. E. Thermal effects of diode laser-irradiation on titanium implants in different room temperatures in vitro. Photobiomodul Photomed Laser Surg. 40 (8), 554-558 (2022).
- Koopaie, M., Kia Darbandsari, A., Hakimiha, N., Kolahdooz, S. Er,Cr:YSGG laser surface treatment of gamma titanium aluminide: Scanning electron microscopy-energy-dispersive X-ray spectrometer analysis, wettability and Eikenella corrodens and Aggregatibacter actinomycetemcomitans bacteria count - in vitro study. Proc Inst Mech Eng H. 234 (8), 769-783 (2020).
- Kayar, N. A., Hatipoǧlu, M. Could we set a convenient irradiation time to reduce the possibility of thermal pulp damage during diode laser as an adjunct to periodontal treatment? An in vitro analysis. Photobiomodul Photomed Laser Surg. 39 (7), 480-485 (2021).
- Barrak, H., Mahdi, S. S., Alkurtas, S. A., Size, P. Clinical applications of a 940 nm diode laser for laser troughing versus conventional method: A preliminary study. Iraqi J Laser. 23 (2), (2024).
- Beer, F., Körpert, W., Passow, H., et al. Reduction of collateral thermal impact of diode laser irradiation on soft tissue due to modified application parameters. Lasers Med Sci. 27 (5), 917-921 (2012).
- Schwarz, F., Nuesry, E., Bieling, K., Herten, M., Becker, J. Influence of an erbium, chromium-doped yttrium, scandium, gallium, and garnet (Er,Cr:YSGG) laser on the reestablishment of the biocompatibility of contaminated titanium implant surfaces. J Periodontol. 77 (11), 1820-1827 (2006).
- Al-Omari, W. M., Palamara, J. E. The effect of Nd:YAG and Er,Cr:YSGG lasers on the microhardness of human dentin. Lasers Med Sci. 28 (1), 151-156 (2013).
- Kreisler, M., Götz, H., Duschner, H., d’Hoedt, B. Effect of Nd:YAG, Ho:YAG, Er:YAG, CO2, and GaAlAs laser irradiation on surface properties of endosseous dental implants. Int J Oral Maxillofac Implants. 17 (5), 202-209 (2002).
- Kottmann, L., Franzen, R., Conrads, G., Wolfart, S., Marotti, J. Effect of Er,Cr:YSGG laser with a side-firing tip on decontamination of titanium disc surface: An in vitro and in vivo study. Int J Implant Dent. 9 (1), 7(2023).
- Yao, W. L., Lin, J. C. Y., Salamanca, E., et al. Er,Cr:YSGG laser performance improves biological response on titanium surfaces. Materials. 13 (3), 756(2020).
- Smeo, K., Nasher, R., Gutknecht, N. Antibacterial effect of Er,Cr:YSGG laser in the treatment of peri-implantitis and their effect on implant surfaces: A literature review. Lasers Dent Sci. 2 (2), 63-71 (2018).
- Fletcher, P., Linden, E., Cobb, C., Zhao, D., Rubin, J., Planzos, P. Efficacy of removal of residual dental cement by laser, ultrasonic scalers, and titanium curette: An in vitro study. Compend Contin Educ Dent. , (2025).
- Lollobrigida, M., Fortunato, L., Serafini, G., et al. The prevention of implant surface alterations in the treatment of peri-implantitis: Comparison of three different mechanical and physical treatments. Int J Environ Res Public Health. 17 (8), 2624(2020).
- Arora, S., Lamba, A. K., Faraz, F., Tandon, S., Ahad, A. Evaluation of the effects of Er,Cr:YSGG laser, ultrasonic scaler and curette on root surface profile using surface analyser and scanning electron microscope: An in vitro study. J Lasers Med Sci. 7 (4), 243-249 (2016).
- Jin, S. H., Lee, E. M., Park, J. B., Kim, K. K., Ko, Y. Decontamination methods to restore the biocompatibility of contaminated titanium surfaces. J Periodontal Implant Sci. 49 (3), 193-204 (2019).
- Kayar, N. A., Hatipoǧlu, M. Can we determine an appropriate timing to avoid thermal pulp hazard during gingivectomy procedure? An in vitro study with diode laser. Photobiomodul Photomed Laser Surg. 39 (2), 94-99 (2021).
- Monzavi, A., Fekrazad, R., Chinipardaz, Z., Shahabi, S., Behruzi, R., Chiniforush, N. Effect of various laser wavelengths on temperature changes during peri-implantitis treatment: An in vitro study. Implant Dent. 27 (3), 311-316 (2018).
- Valente, N. A., Calascibetta, A., Patianna, G., Mang, T., Hatton, M., Andreana, S. Thermodynamic effects of 3 different diode lasers on an implant-bone interface: An ex-vivo study with review of the literature. J Oral Implantol. 43 (2), 94-99 (2017).
- Leja, C., Geminiani, A., Caton, J., Romanos, G. E. Thermodynamic effects of laser irradiation of implants placed in bone: An in vitro study. Lasers Med Sci. 28 (6), 1435-1440 (2013).
- Strever, J. M., Lee, J., Ealick, W., et al. Erbium, chromium:yttrium-scandium-gallium-garnet laser effectively ablates single-species biofilms on titanium disks without detectable surface damage. J Periodontol. 88 (5), 484-492 (2017).
- Bourauel, C., Fries, T., Drescher, D., Plietsch, R. Surface roughness of orthodontic wires via atomic force microscope, laser specular reflectance, and profilometry. Eur J Orthod. 20 (1), Accessed February 13, 2025 79-92 (1998).
- Choi, S., Kim, J. H., Kim, N. J., et al. Morphological investigation of various orthodontic lingual bracket slots using scanning electron microscopy and atomic force microscopy. Microsc Res Tech. 79 (12), 1193-1199 (2016).
- Huang, H. H., Chuang, Y. C., Chen, Z. H., Lee, T. L., Chen, C. C. Improving the initial biocompatibility of a titanium surface using an Er,Cr:YSGG laser-powered hydrokinetic system. Dent Mater. 23 (4), 410-414 (2007).
- Furtsev, T. V., Koshmanova, A. A., Zeer, G. M., et al. Laser cleaning improves stem cell adhesion on the dental implant surface during peri-implantitis treatment. Dent J. 11 (2), 30(2023).
- Stübinger, S., Homann, F., Etter, C., Miskiewicz, M., Wieland, M., Sader, R. Effect of Er:YAG, CO and diode laser irradiation on surface properties of zirconia endosseous dental implants. Lasers Surg Med. 40 (3), 223-228 (2008).
- Kim, H. K., Park, S. Y., Son, K., et al. Alterations in surface roughness and chemical characteristics of sandblasted and acid-etched titanium implants after irradiation with different diode lasers. Appl Sci. 10 (12), 4167(2020).
재인쇄 및 허가
JoVE'article의 텍스트 или 그림을 다시 사용하시려면 허가 살펴보기
허가 살펴보기더 많은 기사 탐색
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. 판권 소유