Method Article
骨組織工学における潜在的な使用のためのグラフェン - ハイドロキシアパタイトナノコンポジットの合成
要約
グラフェンナノリボンおよびハイドロキシアパタイトナノ粒子の新規ナノコンポジットを、溶液相合成を用いて調製した。これらのハイブリッドは、生理活性足場材に採用された場合、組織工学および骨再生における潜在的な用途を示すことができる。
要約
骨組織工学のための新規材料の開発は、ナノメディシンの最も重要な推力分野の1つです。いくつかのナノコンポジットが、細胞の接着、増殖、および骨形成を促進するためにハイドロキシアパタイトを用いて製造されている。この研究では、グラフェンナノリボン(GNR)とハイドロキシアパタイトのナノ粒子(nHAPs)を使用してハイブリッドナノコンポジットの開発に成功し、生理活性足場材に採用すると骨組織の再生を改善する可能性があります。これらのナノ構造体は、生体適合性であり得る。ここでは、新規材料の調製に2つのアプローチを用いた。1つのアプローチでは、nHAPが合成され、同時にGNRにコンジュゲートされ、GNR表面上にnHAPのナノハイブリッド(nHAP/GNRと表記される)をもたらす共官能化戦略が使用された。高分解能透過型電子顕微鏡(HRTEM)により、nHAP/GNR複合体は、GNR(最大長1.8μm)の細くて薄い構造と、針状のnHAP(長さ40~50nm)の離散パッチ(150~250nm)で構成されていることが確認されました。他のアプローチでは、市販のnHAPをGNRと共役させてGNR被覆nHAP(GNR/nHAPと表記される)を形成した(すなわち、nHAP/GNRナノハイブリッドに対して反対の向きを有する)。後者の方法を用いて形成されたナノハイブリッドは、表面にGNRのネットワークで覆われた直径50nm〜70nmの範囲のnHAPナノスフィアを示した。エネルギー分散スペクトル、元素マッピング、およびフーリエ変換赤外(FTIR)スペクトルは、両方のナノハイブリッドにおけるnHAPおよびGNRの良好な統合を確認した。熱重量分析(TGA)は、GNRの存在による高温での損失は、GNR/nHAPおよびnHAP/GNRについてそれぞれ0.5%および0.98%であることを示した。反対の向きのnHAP-GNRナノハイブリッドは、骨組織工学アプリケーションを改善するための細胞機能を潜在的に促進するために、生理活性足場に使用するための重要な材料を表す。
概要
グラフェンは、spハイブリダイズした炭素からなるシート状の二次元構造を有する。いくつかの他の同素体は、グラフェンの拡張されたハニカムネットワークに起因し得る(例えば、グラフェンシートの積層は、同じ材料を転がり落ちながら3Dグラファイトを形成し、1Dナノチューブの形成をもたらす)。同様に、0Dフラーレンはラッピング2のために形成される。グラフェンは、室温での両極性電界効果および量子ホール効果を含む魅力的な物理化学的および光電子的特性を有する3,4。単一分子吸着事象の検出および非常に高いキャリア移動度は、グラフェン5,6の魅力的な属性に加わる。また、幅が狭く平均自由行程が大きく、低抵抗率で電流密度が高く、電子移動度が高いグラフェンナノリボン(GNR)は、有望な相互接続材料7と考えられている。したがって、GNRは無数のデバイス、最近ではナノメディシン、特に組織工学と薬物送達における応用のために探求されています8。
様々な外傷性疾患の中で、骨損傷は、骨折、再生および新しい骨との置換を安定させ、感染に抵抗し、骨非結合体を再整列させることの困難さのために、最も困難なものの1つと考えられている9,10。外科的処置は、大腿骨軸骨折の唯一の代替手段のままである。中央アメリカとヨーロッパでは、毎年約5200万ドルが骨損傷の治療に費やされていることに注意する必要があります11。
骨組織工学用途のための生理活性足場は、骨自体のマイクロおよびナノ建築特性に似ているので、ナノハイドロキシアパタイト(nHAP)を組み込むことによってより効果的であり得る12。化学的にCa10(PO4)6(OH)2として表され、Ca/Pモル比が1.67であるHAPは、生物医学的用途、特に歯周欠損の治療、硬組織の置換、および整形外科手術のためのインプラントの製造に最も好ましい13,14。したがって、GNRで強化されたnHAPベースの生体材料の製造は、優れた生体適合性を有することができ、オッセオインテグレーションを促進し、骨伝導性であるそれらの能力のために有利であり得る15,16。このようなハイブリッド複合足場は、細胞接着、拡散、増殖、および分化などの生物学的特性を維持することができる17。ここでは、図1に示すようにnHAPおよびGNRの空間配置を合理的に改変することによって、骨組織工学のための2つの新しいナノコンポジットの作製を報告する。2つの異なるnHAP-GNRs配列の化学的および構造的特性をここで評価した。
プロトコル
1. 沈殿によるnHAPの合成
- 1 M Ca(NO3)2∙4H2Oおよび0.67 M(NH4)H2PO4を含む反応混合物50 mLを用いて手付かずのnHAPを合成し、続いてNH4OH(25%)を滴下してpHを1018付近に維持する。
- その後、超音波照射(UI)により反応混合物を30分間攪拌する(500W電力および20kHz超音波周波数)。
- 得られた溶液を、nHAPの白色沈殿物が落ち着くまで室温で120時間成熟させる。室温で5分間、1398 x g で遠心分離することによりnHAPを回収する。
- 沈殿物を脱イオン(DI)水3xで洗浄し、48時間凍結乾燥する。乾燥粉末を4°Cで保存する。
2. nHAP/GNRナノコンポジットの作製
注: 以下では、nHAP と GNR の 2 つの異なる空間配置を表す nHAP/GNR (つまり、GNR サーフェス上の nHAP) および GNR/nHAP (GNR コーティングされた nHAP) ナノコンポジットを製造するための 2 つのアプローチについて説明します (図 1)。
- nHAP/GNRの合成
- nHAP/GNRsナノコンポジットを調製するには、以下のように、nHAPを合成してGNRに同時に共役させることができる共官能化戦略を使用する。
- 1 M 硝酸カルシウム 4 水和物 [Ca(NO3)2·4H 2 O] および 0.67 M リン酸水素二アンモニウム [(NH 4)2 HPO4] の混合物に 5 mg の GNR (材料表) を 50 mL の最終容量19 に溶解する。
- この反応の間、25%のNH4OHを滴下して、pHを〜10に維持する。得られた混合物をUIで30分間攪拌する。
- 反応終了後、成熟するまで溶液を室温で120時間邪魔されずに放置する。
- GNRを被覆するnHAPのゼラチン状沈殿物の形成を観察し、続いてnHAP/GNRの白色沈殿物が沈降する。
- 沈殿物3xを室温で1398 x g で5分間遠心分離して洗浄し、続いてDI水に再分散させた。
- 回収した洗浄沈殿物を48時間凍結乾燥する。乾燥粉末を4°Cで保存する。
- 対照サンプルとして手付かずのnHAPおよびGNRを使用する。
- GNR/nHAPナノコンポジットの合成
- 市販のnHAPを5mg/mLの濃度で5mgのGNRで補充した50mLのDI水に懸濁する。
- 得られた混合物をUIによって30分間攪拌し、その後、混合物を室温で120時間邪魔されずに放置する。
- 成熟後、得られたGNR/nHAPの白色沈殿を、室温で1398 x g で5分間遠心分離することによって回収する。
- DI水を使用してサンプル3xを洗浄し、48時間凍結乾燥し、さらに使用するために乾燥粉末を4°Cで保存する。
3. nHAP、nHAP/GNR、および GNR/nHAP の特性評価
- 高分解能透過型電子顕微鏡(HRTEM)( 材料表を参照)を使用して、ナノコンポジット11の形態およびサイズを特徴付ける。
- エネルギー分散分光法(EDS)を用いてナノコンポジットの元素組成を解析し、走査型透過電子顕微鏡(STEM)を用いて元素マッピングを行う11。
- 500-4000cm-1の波数のきれいなサンプルに対してフーリエ変換赤外(FTIR)分光法を実行して、ナノコンポジット16中の化学基を分析する。
- 合成されたnHAPの粉末X線回折(XRD)分析は、1.5406ÅのX線波長、それぞれ40mAおよび40kVの電流および電圧設定、および20°~90°の範囲の2θを用いて行う。
- 窒素流下でサンプルを室温から1000°Cまで窒素流下で10°C/分の速度で加熱することにより、熱重量分析(TGA)を使用してナノコンポジット中のGNRの負荷率を評価します。
結果
HRTEM分析
GNRは、 図2で観察されたように、それぞれ細長い竹のような構造で、ある程度の距離で曲がっていました。最長GNRは1.841μmで、最小の曲がったGNRは497nmであった。ナノリボンは、しばしば、多くの場所でらせん状の配置を形成するためにねじれたことに起因し得る幅の目に見える変化を示した。GNRのこのような一方向アライメントは、磁気特性、導電率、または熱輸送などの魅力的な特徴を得るのに役立ち得る7。
室温で硝酸カルシウム四水和物およびリン酸水素二アンモニウムを用いて合成されたnHAPs(ステップ1)は、40nm〜50nmの範囲のサイズを有する棒状または針状であった(図3)。合成されたナノ材料は、凝集および結晶成長のために凝集塊中に見出された。一方、使用した市販のnHAPsは球状であった(図4)。これらのナノスフィアは直径50〜70nmであり、15〜20個の球の離散的なクラスターに存在していた。
nHAPは、共機能化戦略(ステップ2.1)においてGNR(nHAP/GNRとして表される)上に その場で 沈着した。得られたGNRとnHAPのナノコンポジットは、高度に多孔質の相互接続されたナノ構造からなっていた。パッチでGNR表面を覆う針状のnHAPの優位性(図5)は、nHAP核生成のためのナノ特徴足場として機能するGNRに起因する。nHAPパッチは、長さおよび幅が150nm〜250nmの間であることが見出された(図5A、B)。元素マッピングは、GNR上の中間結節パッチが、元素カルシウムおよびリンの存在のために実際にnHAPであることを確認した(図5C)。
他の方法(ステップ2.2)では、予め形成されたnHAPをGNRに共役させ、GNR被覆nHAPの形成をもたらした(GNR/nHAPとして表され、すなわち、nHAP/GNR複合体と比較して逆向きを有する)。この場合、GNRsは球状nHAPナノ粒子の表面に薄膜を形成した(図6)。
興味深いことに、図2Aで明らかなようにGNRの周囲で見られる曲がりや畳み込みは、図5と図6に見られるように、nHAPとの機械的相互作用と付着を著しく強化した可能性のある安定性の低い特性に主に起因しています。さらに、手付かずのGNRの表面積が大きいことは、より多くのnHAP負荷にも役立ちます。また、複合溶液を120時間エージングすると、アパタイトから高結晶性ハイドロキシアパタイトへの完全な変換がもたらされました(図3および図5)。GNR表面の酸素系官能基はCa2+と静電的に相互作用し、受容体部位として機能する。アパタイトナノ構造体は、さらに、これらのアンカーされた陽イオンとリン酸イオンとの間のin situ反応に起因して得ることができる(工程2.1)。GNR表面上の微細構造nHAPの配向は、グラフェンベースのテンプレート上の酸素基の量およびタイプ、前駆体の相対濃度(Ca2+およびHPO42-)、反応混合物のpH、および成熟時間を含むいくつかの要因によって制御される。反応条件の累積的な効果は、おそらく非共有結合性物理吸着のために、nHAPナノスフェアの表面上の透明なGNRの包み込みをもたらした。
エネルギー分散スペクトル(EDS)分析
ナノコンポジットの主要成分および元素組成を確認するために、エネルギー分散型スペクトル分析を行った。 図7Aでは、手付かずのGNRのEDSスペクトルはGNRに対応する炭素ピークを示したが、HRTEM分析中にサンプルのマウントに使用されたグリッドに帰属した銅を除いて他のピークは観察されなかった。 図7B は、HRTEM分析中にサンプルをマウントするために使用される炭素被覆銅グリッドに炭素および銅のピークが帰属される市販の予め形成されたnHAPナノスフェアのEDSスペクトルを示す。 図7Cでは、炭素含有量の明らかな増加はGNRに起因するが、カルシウムおよびリンに特異的な他のピークはGNR/nHAPナノコンポジット中のnHAPによるものであった。図 8 は、合成時のnHAP(ステップ1)(図8A)およびnHAP/GNR複合体(図8B)のEDSスペクトルを示す。nHAP/GNRスペクトルにおける炭素含有量の顕著な増加は、新たに合成されたnHAPの小さなパッチのみが観察されたGNRの大部分によるものである。
FTIR 分析
nHAPとGNRの結合は、FTIRスペクトルを通して確認された。図9は、nHAP、GNR、nHAP/GNR、およびGNR/nHAPのFTIRスペクトルを示しています。600cm-1の面外曲げピークのOHはGNR12のFTIRに見られる。nHAPにP-O伸縮に帰属される1030cm-1にピークが観察され、その化学組成を15で確認した。特に、nHAPの特徴的なP-O伸縮ピークはnHAP/GNRおよびGNR/nHAPにも見られ、両方の複合材料にnHAPが存在することを示している。複合材料にのみ見られる他の2つのピーク、1413および1447cm-1は、それぞれδCH2振動および炭酸基(CO32−)に帰属され、GNRおよびnHAP16の共役を確認する。
X線回折(XRD)分析
HAP(ステップ2.1)のXRDパターンを図10に示す。強いピークは、材料の良好な結晶性を示した。ピーク位置はICDD標準データ(PDF2カード:00-009-0432)のピーク位置とよく一致していた。これにより、nHAPの六方晶結晶構造(P63/m空間群)が確認でき、格子パラメータ値はa=b=0.940nm、c=0.615nmであった。(002)、(102)、(211)、(300)、(300)、(300)、(310)、(113)、(222)、(213)に対応する2θ値、32.9°、31.8°、32.9°、34.1°、33.9°、46.6°、および49.4°の2θ値における顕著で強いピークのいくつかは、それぞれ合成されたnHAP 16、20、21の純度を確認した。
熱重量分析(TGA)
コンジュゲート中の負荷率を推定するために熱重量分析(TGA)を採用した(図11)。TGA分析中に質量の3つの顕著な損失が明らかであった。100°Cまでの温度での最初の質量損失は、閉じ込められた物理的な水によるものです。100°Cから200°Cの間の第2の損失は、GNRの炭素煤への分解によるものである。その後の500°Cまでの質量の着実な減少は、nHAPの結晶化によるものであった。さらに加熱すると錯体の分解がもたらされた。GNRの存在による損失は、GNR/nHAPおよびnHAP/GNRにおいてそれぞれ0.5%〜0.98%であることが見出された。したがって、HAPが主要成分として発見され、GNRがGNR/nHAP内で表面指向であったという以前の分析とよく一致しています。一方、GNRはnHAP/GNRに豊富にあり、nHAPはGNRの長いストレッチに離散的なパッチを形成した。
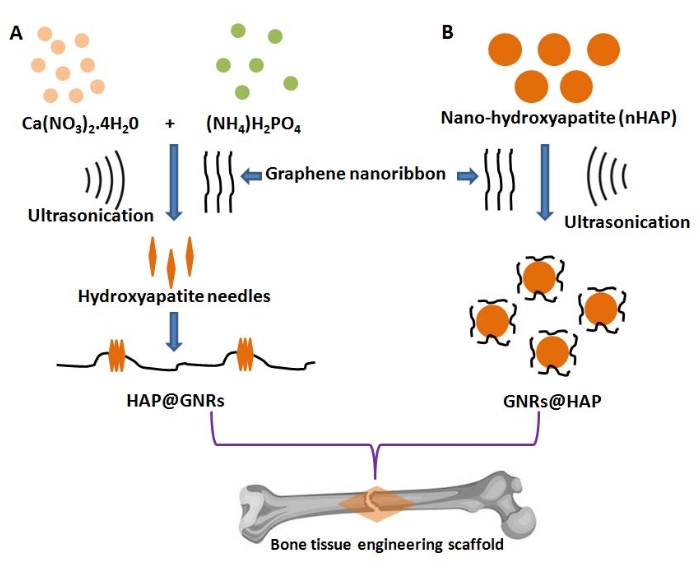
図1:逆配向グラフェンナノリボン-ハイドロキシアパタイトハイブリッド複合材料を合成するための模式図:(A)nHAP/GNRおよび(B)GNR/nHAPの図。この図の拡大版を表示するには、ここをクリックしてください。

図2:GNRの構造解析:(A)裸のGNRのHRTEM解析;(B)GNRの走査型透過電子モード(STEM)画像;(C)GNRの元素マッピング(赤、緑、黄、青の色はそれぞれ炭素、酸素、リン、カルシウムを表す)。この図の拡大版を表示するには、ここをクリックしてください。

図3:合成されたnHAPの構造解析: (A)nHAPのHRTEM解析;(B)100nmを表す差し込みスケールバーを有するnHAPの走査型透過電子モード(STEM)画像;(C)赤、緑、黄、青の色がそれぞれ炭素、酸素、リン、カルシウムを表すnHAPの元素マッピング。 この図の拡大版を表示するには、ここをクリックしてください。
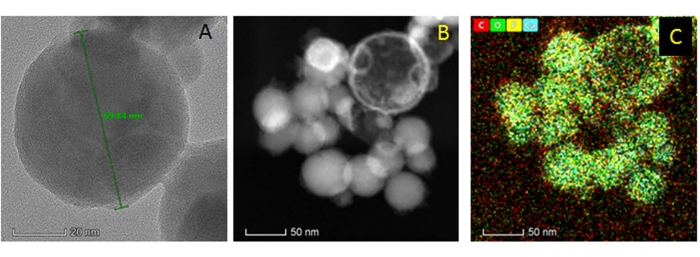
図4:市販の予め形成された nHAPの構造解析:(A)nHAPのHRTEM解析;(B)nHAPの走査型透過電子モード(STEM)画像;(C)赤、緑、黄、青の色がそれぞれ炭素、酸素、リン、カルシウムを表すnHAPの元素マッピング。 この図の拡大版を表示するには、ここをクリックしてください。

図5:共官能化戦略によって合成されたnHAP/GNRの構造解析:(A)nHAP/GNRのHRTEM解析;(B) nHAP/GNRの走査型透過電子モード(STEM)画像;(C)赤、緑、黄、青の色がそれぞれ炭素、酸素、リン、カルシウムを表すnHAP/GNRの元素マッピング。この図の拡大版を表示するには、ここをクリックしてください。

図6:GNR/nHAPの構造解析:(A)GNR/nHAPのHRTEM解析;(B)50nmを表すスケールバーがはめ込まれたGNR/nHAPの走査型透過電子モード(STEM)画像。(C)GNR/nHAPの元素マッピング(赤、緑、黄、青の色はそれぞれ炭素、酸素、リン、カルシウムを表す)。この図の拡大版を表示するには、ここをクリックしてください。

図7:GNR/nHAPナノコンポジットのEDS分析:(A)GNR、(B)市販の予め形成されたnHAPおよび(C)GNR/nHAPナノコンポジット。この図の拡大版を表示するには、ここをクリックしてください。
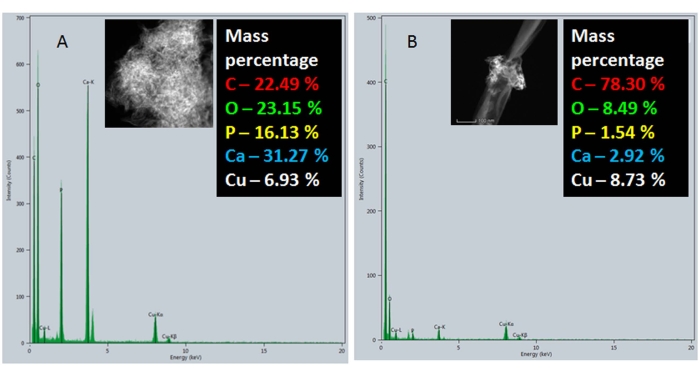
図8:nHAP/GNRナノコンポジットのEDS分析: (A)As-synthesized nHAPおよび(B)nHAP/GNR。 この図の拡大版を表示するには、ここをクリックしてください。

図 9: ナノコンポジットの FTIR 分析。 この図の拡大版を表示するには、ここをクリックしてください。

図 10: nHAP の X 線回折 (XRD) 分析。 この図の拡大版を表示するには、ここをクリックしてください。

図 11: ナノコンポジットの熱重量分析。 この図の拡大版を表示するには、ここをクリックしてください。
ディスカッション
様々な金属、ポリマー、セラミック、およびそれらの組み合わせが整形外科インプラントおよび固定アクセサリーとして研究されてきたが、HAPは骨自体との化学的類似性および結果として高い細胞適合性のために最も好ましい材料の1つであると考えられている20,21,22。この研究では、HAPの向きが変化し、骨形成の促進、骨形成、骨伝導性などのHAPのユニークな特性に大きな影響を与える可能性があります。さらに、HAPの配向を変えることは、体内の長骨がコラーゲンとのHAの異方性配向を有するのに対し、直方体骨はコラーゲンとのHAのランダムな配置を有するので、ナノコンポジットの機械的特性にさらに影響を与え、天然骨のそれをさらに模倣することができる。天然HAPはヒトの歯および骨の主要構成成分であるが、その物理的性質は、CaP相23の反応時間、pH、リン酸濃度、および化学的性質などの反応条件に大きく依存することに留意すべきである。したがって、この研究では、超音波照射(UI)下で10のpHでnHAPを合成するために湿式化学的方法を使用した。Barbosa et al. (2013)はまた、焼成なしの水性沈殿と併せてUIが、高い結晶性と特異性を有するnHAPを生成する単純で迅速で効率的な方法であることを報告した18。
人工的に製造されたHAP関連生体材料は、固有の脆性、低い破壊靭性、および摩耗22を含む貧弱な機械的特性を示すことが多いことに注意することは重要である22。したがって、nHAPは、(i)ナノ粒子に関連する表面官能化、(ii)複合体内の界面における静電相互作用、および(iii)足場24、25、26のマトリックスからのナノフィラーへの応力の伝達を容易にするために、ここでGNRで強化される。ここで続いた湿式化学合成は、主に小さな針状粒子において、より大きな粒子(〜40nm)に凝集した手付かずのnHAPをもたらした。この結果は、Barbosa et al. (2013)の報告とよく一致しており、UIは「ホットスポット」と呼ばれるバブル壁を近接して形成することによって核生成を誘発するのに重要な役割を果たしたと推測された18,27。
ホスト粒子とゲスト粒子の両方の粒径の減少は、一定の限界までしか流動性を高めることができないことに注意することは興味深いことである。その後、ホスト粒子の寸法のさらなる減少は、流動性28に悪影響を及ぼす凝集をもたらし得る。実質的に粒子を含まないソリューションで一次核生成を誘導することとは別に、UIは高い過飽和レベルを防ぎます。さらに、過飽和の確立と核生成および結晶化の開始との間の経過時間のUI媒介性の減少は、nHAPの形状進化およびGNR上の機能化のパターンにおいて鍵となり得る。nHAP/GNR構造は、空間的に集中した領域で発生する高エネルギーの攪拌に加えて、反応温度、気泡の崩壊に伴う圧力、衝撃波の累積的な影響に起因する可能性があります。同様に、UIの存在下で元のGNRとnHAPを同時に追加することによって合成されたGNR/nHAP構造は、その後の急速な局所冷却速度が過飽和を増強することに起因する可能性がある。圧力の局所的な増分はまた、結晶化の温度を低下させることができるが、活性化エネルギーによって作り出される障壁は、GNR18,27の表面官能化中のキャビテーションによるエネルギーの伝達によって有意に克服され得る。
1つの報告は、合成中のUIの過度の適用(〜30〜120分)が、nHAP結晶29の結晶性および/またはサイズを減少させることを示している。これは、我々の研究で観察された官能化の方向性をさらに決定するかもしれない。この研究においても、結果は、nHAPの合成中の比較的長い曝露時間(30分)のUIがGNRs上のnHAP沈着をもたらすことを示した。一方、予め形成されたnHAPとGNRを使用した30分間のUIは、球形のnHAP上にGNRの堆積をもたらした。したがって、この方法は、足場製造のためのGNR組み込み複合材料を得るためのnHAPの大規模生産に理想的である30,31。優れた機械的特性を有するこのような新規な逆向き複合材料は、骨組織工学にとって有意であり得る。特に、Fanら(2014)は、グラフェンを導入すると、元のグラフェンおよびnHAPと比較して、周囲の骨とのより高い骨統合性(すなわち、優れた生体適合性)を示すnHAPの硬度およびヤング率を有意に改善することができると報告した32。したがって、優れた機械的特性および生体適合性を有するGNRおよびnHAPからなるナノコンポジットは、多数の整形外科用途のための有望な生体材料であり得る33、34、35。
しかしながら、反対の向きを有するナノハイブリッドの製造における主要な課題は、ナノコンポジット36、37の所望の配向を得るために反応パラメータを厳密に従うべきであることである。さらに、共機能化戦略では、GNRに沈着した針状のnHAPの量が少なくなり、骨組織再生および機械的強度の可能性を低下させる可能性がある。両方の方法におけるnHAPの形状は異なり、これは骨形成の量に大きく影響し、したがって生物医学的用途に関連する様々な特性を引き起こす可能性がある。
結論として、ここでは、GNRとnHAPからなるナノコンポジットを、整形外科における潜在的な用途を有する可能性のある対照的な空間配置で合成した。結果は、nHAPの形態および官能化時間(すなわち、官能化が合成後に起こるか、またはnHAP合成と同時に起こるか)がナノコンポジット中のnHAPおよびGNRの配向を決定することを示した。合成中の共官能化はnHAP/GNRをもたらし、予め形成されたnHAPによる官能化はGNR/nHAPをもたらした。これらのナノコンポジットは、骨形成を促進する足場の開発に適用可能であり、したがって、さらなる研究を保証する再生ナノメディシンにおいて大きな可能性を秘めている。
開示事項
著者には利益相反はありません。
謝辞
Sougata Ghosh博士は、インド政府科学技術省(DST)、インド政府科学技術省、およびインドのジャワハルラール・ネルー先端科学研究センターが、ナノ科学技術のポスドク海外フェローシップ(Ref. JNC/AO/A.0610.1(4) 2019-2260 2019年8月19日付)の下で資金提供を受けたことを認めます。Sougata Ghosh博士は、タイのバンコクにあるカセサート大学のポスドクフェローシップと、Reinventing University Program(参考文献番号6501.0207/10870、2021年11月9日付)の下での資金提供を認めています。著者らは、特性評価実験の支援をしてくれたKostas Advanced Nano-Characterization Facility(KANCF)に感謝したい。KANCFは、ノースイースタン大学のコスタス研究所(KRI)内の共有の学際的な研究および教育施設です。
資料
| Name | Company | Catalog Number | Comments |
| Ammonium phosphate monobasic | Sigma-Aldrich | 216003-100G | Synthesis |
| Calcium nitrate tetrahydrate | Sigma-Aldrich | 237124 | Synthesis |
| Centrifuge | Hettich | EBA 200S | Recovery |
| Fourier transform infrared spectrometer | Brucker | Vertex 70 | Characterization |
| Graphene nanoribbon | Sigma-Aldrich | 922714 | Synthesis |
| High resolution transmission electron microscope | Thermo Fisher Scientific | Themis Titan 300 | Characterization |
| Magnetic stirrer | IKA | C-MAG HS7 S68 | Functionalization |
| Micropipettes | TreffLab | 06H35687 | Reagent preparation |
| pH meter | Eutech pH5+ | ECPH503PLUSK | Reagent preparation |
| Thermogravimetric analyzer | TA Instruments | SDT Q600 | Characterization |
| Ultrasonic bath | Bandelin | DT100 | Functionalization |
| Universal Oven | Memmert | UF55 | Functionalization |
| Weighing balance | Precisa | XB220A | Reagent preparation |
| X-ray diffractometer | Brucker | D8-Advanced | Characterization |
参考文献
- Novoselov, K. S., et al. Electric field effect in atomically thin carbon films. Science. 306 (5696), 666-669 (2004).
- Novoselov, K. S., et al. Unconventional quantum Hall effect and Berry's phase of 2π in bilayer graphene. Nature Physics. 2 (3), 177-180 (2006).
- Zhang, Y. B., Tan, Y. W., Stormer, H. L., Kim, P. Experimental observation of the quantum Hall effect and Berry's phase in graphene. Nature. 438 (7065), 201-204 (2005).
- Ozyilmaz, B., et al. Electronic transport and quantum hall effect in bipolar Graphene p−n−p junctions. Physical Review Letters. 99 (16-19), 166804 (2007).
- Morozov, S. V., et al. Giant intrinsic carrier mobilities in graphene and its bilayer. Physical Review Letters. 100 (1-11), 016602 (2008).
- Han, M., Ozyilmaz, B., Zhang, Y., Jarillo-Herero, P., Kim, P. Electronic transport measurements in graphene nanoribbons. Physica Status Solidi B: Basic Solid State Physics. 244 (11), 4134-4137 (2007).
- Talyzin, A. V., et al. Synthesis of graphene nanoribbons encapsulated in single-walled carbon nanotubes. Nano Letters. 11 (10), 4352-4356 (2011).
- Allen, M. J., Tung, V. C., Kaner, R. B. Honeycomb carbon: A review of graphene. Chemical Reviews. 110 (1), 132-145 (2010).
- Ghosh, S., Webster, T. J. Metallic nanoscaffolds as osteogenic promoters: Advances, challenges and scope. Metals. 11 (9), 1356 (2021).
- Ghosh, S., Webster, T. J. Mesoporous silica based nanostructures for bone tissue regeneration. Frontiers in Materials. 8, 213 (2021).
- Medeiros, J. S., et al. Nanohydroxyapatite/graphene nanoribbons nanocomposites induce in vitro osteogenesis and promote in vivo bone neoformation. ACS Biomaterials Science and Engineering. 4 (5), 1580-1590 (2018).
- Faniyi, I. O., et al. The comparative analyses of reduced graphene oxide (RGO) prepared via green, mild and chemical approaches. SN Applied Sciences. 1 (10), 1-7 (2019).
- Neelgund, G. M., Oki, A., Luo, Z. In situ deposition of hydroxyapatite on graphene nanosheets. Materials Research Bulletin. 48 (2), 175-179 (2013).
- Rajkumar, M., Sundaram, N. M., Rajendran, V. Preparation of size controlled, stoichiometric and bioresorbable hydroxyapatite nanorod by varying initial pH, Ca/P ratio and sintering temperature. Digest Journal of Nanomaterials and Biostructures. 6 (1), 169-179 (2011).
- Mondal, S., et al. Hydroxyapatite coated iron oxide nanoparticles: A promising nanomaterial for magnetic hyperthermia cancer treatment. Nanomaterials. 7 (12), 426 (2017).
- Oliveira, F. C., et al. High loads of nano-hydroxyapatite/graphene nanoribbon composites guided bone regeneration using an osteoporotic animal model. International Journal of Nanomedicine. 14, 865-874 (2019).
- Murugan, N., Sundaramurthy, A., Chen, S. -. M., Sundramoorthy, A. K. Graphene oxide/oxidized carbon nanofiber/mineralized hydroxyapatite based hybrid composite for biomedical applications. Materials Research Express. 4 (12), 124005 (2017).
- Barbosa, M. C., Messmer, N. R., Brazil, T. R., Marciano, F. R., Lobo, A. O. The effect of ultrasonic irradiation on the crystallinity of nano-hydroxyapatite produced via the wet chemical method. Materials Science and Engineering C. 33 (5), 2620-2625 (2013).
- Rodrigues, B. V. M., et al. Graphene oxide/multi-walled carbon nanotubes as nanofeatured scaffolds for the assisted deposition of nanohydroxyapatite: characterization and biological evaluation. International Journal of Nanomedicine. 11, 2569-2585 (2016).
- Sharma, M., Nagar, R., Meena, V. K., Singh, S. Electro-deposition of bactericidal and corrosion-resistant hydroxyapatite nanoslabs. RSC Advances. 9 (20), 11170-11178 (2019).
- Kamrujjaman, M., Khandaker, J. I., Haque, M. M., Rahman, M. O., Rahman, M. M. Study of the dependency of pH values on HAp synthesis. Journal of Nanomaterials & Molecular Nanotechnology. 7, 4 (2019).
- Baradaran, S., et al. Mechanical properties and biomedical applications of a nanotube hydroxyapatite-reduced graphene oxide composite. Carbon. 69, 32-45 (2014).
- Sassoni, E. Hydroxyapatite and other calcium phosphates for the conservation of cultural heritage: A review. Materials. 11 (4), 557 (2018).
- Tang, H., Ehlert, G. J., Lin, Y., Sodano, H. A. Highly efficient synthesis of graphene nanocomposites. Nano Letters. 12 (1), 84-90 (2012).
- Walker, L. S., Marotto, V. R., Rafiee, M. A., Koratkar, N., Corral, E. L. Toughening in graphene ceramic composites. ACS Nano. 5 (4), 3182-3190 (2011).
- Rafiee, M. A., et al. Enhanced mechanical properties of nanocomposites at low graphene content. ACS Nano. 3 (12), 3884-3890 (2009).
- Luque de Castro, M. D., Priego-Capote, F. Ultrasound-assisted crystallization (sonocrystallization). Ultrasonics Sonochemistry. 14 (6), 717-724 (2007).
- Azhari, A., Toyserkani, E. Additive manufacturing of graphene-hydroxyapatite nanocomposite structures. International Journal of Applied Ceramic Technology. 12 (1), 8-17 (2015).
- Li, H., Wang, J., Bao, Y., Guo, Z., Zhang, M. Rapid sonocrystallization in the salting-out process. Journal of Crystal Growth. 247 (1-2), 192-198 (2003).
- Zou, Z., Lin, K., Chen, L., Chang, J. Ultrafast synthesis and characterization of carbonated hydroxyapatite nanopowders via sonochemistry-assisted microwave process. Ultrasonics Sonochemistry. 19 (6), 1174-1179 (2012).
- Rouhani, P., Taghavinia, N., Rouhani, S. Rapid growth of hydroxyapatite nanoparticles using ultrasonic irradiation. Ultrasonics Sonochemistry. 17 (5), 853-856 (2010).
- Fan, Z., et al. One-pot synthesis of graphene/hydroxyapatite nanorod composite for tissue engineering. Carbon. 66, 407-416 (2014).
- Ghosh, S., Mostafavi, E., Thorat, N., Webster, T. J., Liu, H., Shokuhfar, T., Ghosh, S. Nanobiomaterials for three- dimensional bioprinting. Nanotechnology in Medicine and Biology. , 1-24 (2021).
- Ghosh, S., Sanghavi, S., Sancheti, P., Balakrishnan, P., Sreekala, P., Thomas, S. Metallic biomaterial for bone support and replacement. Fundamental Biomaterials: Metals. Vol 2. Woodhead Publishing Series in Biomaterials. , 139-165 (2018).
- Hazra, A., Basu, S. Graphene nanoribbon as potential on-chip interconnect material-A Review. C Journal of Carbon Research. 4 (3), 49 (2018).
- Zanin, H., et al. Fast preparation of nano-hydroxyapatite/superhydrophilic reduced graphene oxide composites for bioactive applications. Journal of Materials Chemistry B. 1 (38), 4947-4955 (2013).
- Lobo, A. O., et al. Fast preparation of hydroxyapatite/superhydrophilic vertically aligned multiwalled carbon nanotube composites for bioactive application. Langmuir. 26 (23), 18308-18314 (2010).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved