Method Article
臨床用陽電子放出断層レントゲン写真撮影 (ペット) ルコース合成プロトコルの自動化
* これらの著者は同等に貢献しました
要約
複数初期臨床研究臨床試験に関与している陽電子放出断層撮影 (PET) 画像処理サイトには、堅牢で汎用性の高い検査製造能力が必要があります。ルコース [18F] を使用して Clofarabine、カセット ベースの柔軟な radiosynthesizer を使用してルコース合成の自動化および臨床用合成を検証する方法を示す例として。
要約
新しい陽電子放出断層レントゲン写真撮影 (ペット) トレーサーの開発は、研究者や臨床医は、生物学的目標とプロセスのますます広い配列のイメージを有効にします。ただし、異なるトレーサーの増加数は radiopharmacies に彼らの生産のための課題を作成します。歴史的にそれは radiosynthesizer のカスタム構成とそれぞれの個々 のトレーサーの繰り返し生産のためホットセル捧げること実践してきましたが、このワークフローを変更する必要になっています。各トレーサー使い捨てカセット/キットに基づく最近の商業 radiosynthesizers は、カスタム トレース固有の変更の必要性を排除することによって機器の 1 つのセットを持つ複数のトレーサーの生産を簡略化します。さらに、これらの radiosynthesizers のいくつかはオペレーターが開発し、市販キットの購入に加えて、独自の統合のプロトコルの最適化を有効にします。このプロトコルでは、これらの radiosynthesizers のいずれかでの新しいペット トレーサーの手動合成の自動化方法の一般的な手順を説明して臨床グレードのトレーサーの生産のための検証します。たとえば、ELIXYS radiosynthesizer、[18F] を生成する、同じシステムで日常臨床プローブ製造と同様、両方のペット トレーサーの開発努力をサポートできる柔軟なカセット ベースの放射化学ツールを用いて Clofarabine ([18F] CFA)、ペット トレーサー体内デオキシシチジン キナーゼ (dCK) 酵素活性を測定します。手動合成を翻訳、直感的な化学シンセサイザー ソフトウェアでサポートされている「ユニットの操作」に変換されます基本的な放射化学プロセスに合成プロトコルを分割します。これらの操作、急速に変換できる自動合成プログラムにドラッグ アンド ドロップ インターフェイスを使用してそれらを組み立てることによって。基本的なテストの後、合成・精製の手順は、希望収量、純度を達成するために最適化を必要があります。所望の性能を達成すると、合成の検証は臨床使用のためラジオト レーサーの生産のための適合性を決定するため行われます。
概要
生物学的ターゲットの増加配列は動的にリビングで視覚化することで分子のイメージ投射様相ペットボトル科目ペットは、1のイメージングの前に主題に注入される特定ラジオト レーサー (陽電子放出核種で標識分子) を使用して、特定の生物学的、生化学的、および薬理学的プロセスの生体内での試金を提供します。これらのプロセスは基礎科学および臨床研究2,3,4の発見、開発、および患者のケア5,における薬の臨床使用での様々 な研究にペットの使用の増加6、多様なラジオト レーサー7,8の需要をリードしています。Radiochemist の被曝を避けるために、これらの短命のトレーサーの再現性のある生産を確保するためには、彼らは通常、「ホットセル」内部に動作自動化された radiosynthesizer を使用して製造されています。最近の radiosynthesizers は、またカセット9 を交換するだけで複数の種類のラジオト レーサーを準備するための柔軟性を提供しながら臨床グレードの製造を遵守するのタスクを簡素化するのに使い捨てカセット/キット アーキテクチャを使用します。.ただし、初期の臨床段階では通常自動 radiosynthesis; を実行する市販カセット/キットです。その結果、ペット医薬品製造施設の合理的なコストで、適切な期間内の cGMP グレード トレーサー生産機能を実装するシステムをカスタマイズする闘争します。したがって、開発とトレーサーの最適化を容易にする機能を備えたカセット/キット アーキテクチャを組み合わせる radiosynthesizers を開発されています。
ELIXYS フレックス/化学 (ELIXYS) は、幅広い試薬、溶媒と反応温度互換性10柔軟なカセット ベースの radiosynthesizer の例です。3 つの反作用の容器があり、ロボットのメカニズムを使用して、任意の特定合成プロトコル11で必要に応じて流体経路を動的に構成します。シンセサイザー ソフトウェア ドラッグ アンド ドロップトラップ同位体、同位体の溶出、試薬の追加、反応などの単位操作によって異なるトレーサーの合成プログラム (シーケンス) の作成が可能します。蒸発12。各ユニットの操作には、様々 な期間、温度、または不活性ガスの駆動圧 (圧力) などの演算子が利用できるプログラム可能なパラメーターがあります。各単位操作の性質を理解するには、手動合成単位操作のシーケンスに容易に翻訳することができ、13のプロトコルの最適化中に変更します。ELIXYS ピュア/フォーム モジュールと組み合わせて、統合システムは、自動浄化とペット トレーサーの定式化も実行できます。この radiosynthesizer を使用して、について報告した 24 の異なる18F 標識トレーサーの補欠分子族11,14,15,16, 自動合成として同様の生体分子の17、試薬およびシステムの構成ではなくを変更するだけで自動酵素 radiofluorination。[18F] の自動合成を示されている他のタウ蛋白のイメージングのための RO6958948 もつれ18、補欠分子族 [18F] の自動合成 F-Py-TFP ペプチド19 の後続の表示、[18F] の自動合成とホスホジエステラーゼ 10 a (PDE10A) のイメージングのための AM58020。また、いくつかのグループによるトレーサーの生産を含む 4-[18F]、臨床使用に適したフルオロ triphenylphosphonium ([18F] FBnTP) ミトコンドリア膜電位の21、[イメージング18前立腺特異膜抗原 (PSMA)22日、[18F] のイメージングのための F] DCFPyL タウ23のイメージングの THK 5351。
本稿で我々 は [18F] と私たちの経験を使用して手動 radiosynthetic プロシージャが素直かつ迅速に変換する方法 cGMP ガイドラインに従うルーチンの生産に適した自動合成を説明するために CFA。トレーサー [18F] CFA dCK 活動のイメージング用に設計されました。[18F] の手動 radiosynthesis CFA シュウらによって記述されていた2 つの反作用の容器、中間シリカ カートリッジ精製、最終的な HPLC 精製法として24ステップ (補足資料、詳細については、セクション 1を参照)。最近の in vitroおよび前臨床試験は、dCK、このトレーサーの例外的な特異性を示されている、最初の人間学が有利な体内25を示しています。[18F] の感度を確認する臨床試験をより広いスケールで直接的な利害関係がある CFA ペット dCK 活動の変動と長期的な興味このトレーサー26の臨床応用の可能性を。T 細胞の活性化を引き起こす、DNA 損傷を誘発するまたは dCK 依存型ヌクレオシド アナログ プロドラッグに依存の治療のための有用なバイオ マーカーがあります。特に、[18F] CFA Clofarabine による治療の潜在的な応答のための患者の層別化を有効にします。[18F]CFA は、研究と臨床試験に向かって前進して dCK 阻害剤の開発にも促進するかもしれない。このトレーサーは手動で合成されて伝統的に、のですべてのこれらの研究を進める [18F] の信頼性の高い、自動合成を必要とする CFA の臨床使用に適しています。
我々 は、[18F] の自動合成を報告した前臨床研究16, このプロトコルの CFA がビルドこれらの努力にさらに、このトレーサーの臨床の生産に必要な追加の変更について説明します完全に自動化された浄化と定式化、プロトコルの検証、および品質管理試験の統合を含みます。ここで説明する一般的な手順は、[18F] の自動および臨床的に適切な合成の開発に限定されない CFA 他の臨床使用に適した自動合成を開発する単純な方法で一般化することができますが、フッ素 18 ラベルの付いたラジオト レーサー。
プロトコル
1. 一般的な手順オートメーションおよび臨床製造用の Radiosynthesis プロトコルの検証のため
-
臨床の製造のための手動合成スキームの適格性を分析します。
- 任意の望ましくない残留化学物質による製品汚染のリスク分析を行います。
- クラス 1 溶剤ベンゼンなどを避け、適切な代替溶剤 (クラス 2 またはクラス 3) に置き換えてください。
- 潜在的な残留不純物として最終的な定式化を検出することは困難になる化学物質を避けます。
- 高純度グレード (必要な USP または Ph.Eur。 グレード) で市販されている、分析証明書を提供している唯一の化学物質を選択してください。
- 望ましくない化学物質や溶剤リスク分析によって検出され、1.1 節を繰り返してどれもが残っている場合は、合成方式を絞り込みます。
- 任意の望ましくない残留化学物質による製品汚染のリスク分析を行います。
-
統合のプロトコルを自動化します。
- 同じシンセサイザーを用いたトレーサー自動プロトコルはすでに作成およびオンライン リポジトリにアップロード、合成プログラムのコピーをダウンロードします。
- 自動合成プログラムが既に存在しない場合作成します。
- 紙とペンを使用して、分割の大まかな手順がマニュアルの合成 (例えば、乾燥/活性化 [18F] フッ化物、放射化学反応、浄化手順等の実行を容易にする暖房します。)。更に必要とされる個別の基本的なプロセスに大まかな手順を破壊します。たとえば、[18F] の合成スキームとして CFA は図 1に示すように、大まかな手順の同定は図 2 aに示すように、プロセスに内訳は図 2 bに示すように。
- 紙とペンを使用して、シンセサイザー ソフトウェアによって提供される個々 の単位操作に各プロセスをマップします。たとえば、[18F] の合成における基本的なプロセスのマッピング分析 CFA シンセサイザー ソフトウェア13における適切な単位操作には図 2に示すように。
- Radiosynthesizer のプログラミング インターフェイスを使用して、空白プログラムを作成し、メニューボタン (左上) をクリックして、シーケンスを選択する新しい、をクリックし、シーケンス内の各識別された単位操作を追加シーケンスボタン。1.2.2.2 の手順で識別される単位操作ごとに、フィルム ストリップ ビュー、クリックまたは単位操作の各パラメーターの目的の値を記入するタイプに使用可能な操作からユニットの操作をドラッグします。図 3インターフェイスの例を示すときすべての操作は、[18F] を合成する CFA が設定されてし、ユーザーが選択するパラメーター値を編集する最初の反応ユニット操作。[18F] の最終的な合成プログラム CFA、補足資料、テーブル S1とS2で説明。
- 合成プログラムを確認します。
- ドライランを実行します。セットアップおよび 2.1 から 2.3、期待される動作を確認するすべての試薬と放射性核種 (例えば、[18F] フッ化物) 以外の溶媒を使用しての手順と同様にプログラムを実行します。
- 必要に応じて、調整ユニットの操作のパラメーター値 (例えば、時間や試薬、所望のレベル等に溶剤を蒸発させる時間/温度を完全に転送する運転圧力)、プログラムの再テスト。パラメーター値を調整するには、まず、メイン メニュー (左上) からシーケンスを選択して、編集モードに戻るし、新しく作成されたプログラムを選択します。次に、フィルム ストリップ ビュー (画面の下部) に必要なユニットの操作をクリックして、目的のパラメーターに移動し、、選択または新しい値を入力します。
- プログラムを評価するため低活性 (< 370 MBq) テストを実行します。
- 収量、合成時間、反復性、および他の目的の測定可能な結果を改善するためにパラメーター値を調整することで自動合成を最適化します。
-
品質管理 (QC) のテスト手順を開発します。
- 最終製品の非放射性の参照および潜在的な化学的不純物のサンプルを使用して、分析のラジオ HPLC を開発および/またはラジオ薄層クロマトグラフィー (TLC のラジオ) 法種を十分に分離の定量化学純度、モル活動、放射化学純度、放射化学アイデンティティ。再現性、直線性分析方法を検証し、検出と定量限界を決定します。
- 同様に、開発し、揮発性の不純物 (例えば合成の際に使用される溶剤の残留量) を分析するガス ・ クロマトグラフィー法を検証します。
- 開発し、検出とその他の潜在的な不純物 (例えば、クリプタンド 222経由で標準色のスポット テスト) の定量化分析試金を検証します。
- 不稔性、pH、radionuclidic id、radionuclidic 純度、放射能濃度、製品ボリュームおよびエンドトキシン レベルの決定のための標準の手順を使用します。
-
合成検証を実行します。
- 合成と QC テスト手順の標準操作手順 (Sop) を確立し、材料を統合追跡装置現在良い準拠製造実習 (cGMP) 要件とします。
- Sop を次臨床の製造向けに同じ放射能レベルを介して3 つ独立して連続生産を実行する合成手順を検証します。合成パフォーマンスと品質管理テストの結果を文書化します。
- すべての連続した検証の実行は、QC の制限を事前設定を渡す必要があります。検証を実行が失敗した場合、エラーの根本的な原因を適切に対処した後全体の検証プロセスを繰り返します。
2 臨床使用のための例: 自動 [18F] CFA の合成
- Radiosynthesizer を準備します。
- Radiosynthesizer の電源を入れます。
- 不活性ガスの供給に十分な圧力となって、radiosynthesizer は、ガスの供給に接続されるように、必要なバルブが開いていることを確認します。
- 原子炉 #1 と #2 位置で新しい使い捨てカセットをインストールし、電磁攪拌棒を含む反応容器を挿入します。各カセット転送ディップ チューブはまっすぐに指摘したことを確認します。
- 試薬バイアルを準備し、図 4の図によるとカセットにそれらをインストールします。
- インストール [18O] 空カセット #1 のW1位 H2O 回復バイアル。
- 第四紀メチル (QMA) カートリッジをアクティブにする最初 12 mL の脱イオン水で続いて、それを 1 M KHCO3溶液 12 mL を渡します。Sep-pak シリカ カートリッジ、それを酢酸エチル 5 mL を渡すことによって条件します。
- カートリッジを接続し、図 5 aに示すように、すべてのカセット チューブ接続を行います。インテリアは、ロボットの動きを妨げるかもしれないどこでハングアップするカセット チューブ (未使用チューブなど) がないことを確認します。
- [18F] フッ化物のソース行をサイクロトロンからカセット 1 [18F] フッ化物の入力ラインに接続します。
- 廃棄物コンテナーが空を確認します。場所浄化/定式化サブシステムから廃棄物のコンテナー (すなわち、サンプル ループ 1 廃棄ライン、高速液体クロマトグラフィー サブシステム廃棄物ライン、およびシリンジ ポンプ廃棄ライン) へ廃棄物ライン。
- 高速液体クロマトグラフィーの入力ラインに接続します。場所 hplc 用移動相は 25 mM 酢酸アンモニウムと HPLC 移動相入力行江藤のコンテナーに"B"のコンテナーにライン「A」を入力します。
- 浄化/定式化サブシステムと HPLC カラムを平衡します。
- メイン メニュー (左上) から高速液体クロマトグラフィーを選択してソフトウェアで浄化/定式化モジュールの管理ページを開きます。既定では、[浄化] タブが既に選択されます。(このページを図 6に示します)。
- 5.0 mL/分で定義された溶媒組成に流量を設定し、浄化の列にインストールされているどの列の位置を選択します。イソクラティック モードで少なくとも 10 分のための高速液体クロマトグラフィー ポンプをオンにします。
- 製品ラインおよび携帯電話の段階では、1 分ごとにすべての分数コレクション ラインすすいでください。
- 各 HPLC サンプル ループおよび管の 10 ml の注射器を使用して移動相の HPLC サンプル ループ伝達すすいでください。
- 浄化/定式化サブシステム シリンジ ポンプ入力ラインに接続します。使用には、想定し, 浸出液行および再構成線 0.9% 生理食塩水の塩化ナトリウム (90 mg/mL) が集中しています。
- 首相の定式化サブシステム。
- 浄化/処方コントロール ページの定式化] タブに移動します。
- 濃縮塩化ナトリウム (90 mg/mL) をプライム プレスは、シリンジ ポンプを初期化する初期化を想定し, 浸出液] タブを選択します。5 mL を調剤します。
- 0.9% 生理食塩水を首相タブ調剤 5 mL の再構成を選択します。
- T 型接続の浄化/定式化サブシステムの前面から製品や最終製品のラインを接続します。ターンでは、最終滅菌製品バイアルに接続されている滅菌フィルター (0.22 μ m) に T 型接続の出力を接続します。最終製品のバイアルのヘッド スペースに滅菌フィルター通気針を挿入します。最終的なシステムのセットアップの写真を図 5Bに示します。
- コールド トラップにドライアイスとエタノールまたはメタノールを追加します。
- 合成プログラムを実行します。
- メイン メニュー ボタン (左上) からシーケンスを選択して、プログラムの一覧に移動します。[18F] CFA プログラムを選択し、実行ボタンを押してプログラムを開始します。
- 慎重に実行前のチェックリストの各項目を通過し、完成して、それらをチェックします。実行前チェックリスト画面の一部を図 7に示します。
- セットアップが完了を確認し続けるを押し、自動合成を開始するが発生します。
- 必要な場合、監視の合成を介して視覚的なフィードバック (原子炉カメラ)、センサーの読み値 (例えば、温度、圧力、真空、放射読書、等) および秒読みのタイマー リアルタイム。代表的なスクリーン ショットを図 8に示します。
- 浄化ユニット操作中に放射線検出器クロマト グラム上に表示する製品のピークが開始されると製品を選択します。この装置の操作中に代表的なスクリーン ショット (出力 UV 検出器及び放射線検出器のクロマト グラムを含む) は、図 9に示すように。
- 放射線検出器のクロマト グラム ピークは、ベースラインに戻ってきた、無駄に廃棄容器に高速液体クロマトグラフィー サブシステムのフロー パスを流用するを選択します。
- 設定し、定式化プログラムを実行
- プログラム (シーケンス画面) の一覧から、開く、 [18F] CFA 製剤プログラム。
- 定式化の単位操作のパラメーターを調整します。
- HPLC ポンプ流量と分数コレクションの期間に基づいて収集した製品分数 (V分数) の量を計算します。
- 10% 以下のエタノール濃度を希釈するために必要な追加の生理食塩水の量を計算して isotonicity を達成するために必要な追加のナトリウム塩化物 (90 mg/mL) の量を計算します。
- これらの値を使用してプログラムを変更します。塩化ナトリウム (90 mg/mL) のボリュームを想定し, 浸出液のステップの入力し、再構成手順の生理食塩水の量を入力します。(計算は補足資料、図 S2で説明します)。
- プログラムを保存します。
- プログラムを実行します。システムは塩化ナトリウムと食塩水配合 isotonicity を確保し滅菌製品バイアルに殺菌フィルターを介してそれを提供収集した精製した製品一部を希釈します。
- 収集を策定 [18F] 品質管理・出荷の CFA
- 熱い細胞から作り出された [18F] CFA 製品を削除します。
- 滅菌作業テクニックを使用して、品質管理テストを実行する 2 つのサンプル (300 μ L) を撤回します。
- 最初のサンプルを使用すると、任意の成長を観察することがなく流体チオグ リコール酸・ 14 d のトリプシン大豆スープを接種最終製剤の無菌テストします。
- 2 番目のサンプルを使用すると、手順 1.3 の開発手順に従って品質管理を実行できます。米国薬局方に従い UCLA アーマンソン医サイクロトロン施設設置手順は次のとおりです。
- 目視による外観を評価します。
- インジケーター紙で pH を評価します。
- キネティック発色性細菌エンドトキシン試験 (賭け) を用いたエンドトキシンのコンテンツを評価します。
- 放射性サンプルの非放射性参照化合物共溶出を確認して分析ラジオ高速液体クロマトグラフィーと放射化学アイデンティティを評価します。
- 目的の製品に対応する AUC を持つガンマ線検出器クロマト グラムの放射性不純物 (AUC) 曲線下面積を比較することによって分析ラジオ高速液体クロマトグラフィーと放射化学的純度を評価します。
- 不純物紫外線アクティブすべての UV 検出器クロマト グラムの AUC を決定して化学分析 HPLC 純度を評価します。
- UV 検出器クロマト グラムの目的の製品に対応する AUC を決定することで臼歯部の活動およびキャリア分析ラジオ高速液体クロマトグラフィーと質量を評価します。
- 2 つの異なる縦長」でその活動を測定し、減衰曲線を当てはめ、プローブの半減期を評価します。
- ガスクロマトグラフィーによる定式化の残留溶剤量を評価します。
- ガンマの分光器を用いた放射性核種エネルギーを評価します。
- TLC ベースのスポット テストを使用してクリプタンド 222 のコンテンツを評価します。
- すべてのテストを渡すと場合、は、臨床画像サイトへの出荷のプローブの定式化をリリースします。
- ポストを実行し、システムのシャット ダウン
- 高速液体クロマトグラフィー精製カラムおよびすべての 70% (v/v) 水エタノール製品コレクション用チューブすすいでください。これは、ステップ 2.1.12 のような純粋な/フォーム コントロールのページで行ってください。
- ソフトウェアの電源ボタンを介してradiosynthesizer をシャット ダウンします。ポップアップ ウィンドウは、システムの電源をオフすることができますが表示されます。
- 適切な遮断弁を閉じることによって圧縮空気と不活性ガスの供給をオフにします。
- (通常夜間) 崩壊ホットセルにおける残留放射能のための時間を許可します。
- きれいに、radiosynthesizer
- 削除し、すべてのカセット、カートリッジ、原子炉容器、合成の際に使用される試薬バイアルの処分します。
- コールド トラップの内容を空にします。
- 浄化サブシステム流体パスをクリーンアップします。
- 既存のクリーニング プログラムを開くか、1 つ浄化単位操作 (すなわちでクリーン] チェック ボックスがオン) モードを洗浄を含む新しいプログラムを作成します。補足資料図 S9例についてを参照してください。
- [パラメーターの構成] ページで、浄化と 70% を含むボトルに接続されている HPLC 移動相入力ラインに使用された列を選択水エタノール。2 mL/min の流速をプログラム、5 分の注入ループごとの洗浄期間と 30 の各製品と一部出力の洗浄期間 s の選択乾燥ラインプログラムの持続時間 30 秒。
- 大型廃棄物コンテナーにすべての分数のライン出力を配置します。
- プログラムを実行します。
- 終了後、廃棄容器を空にします。
- 定式化サブシステム流体パスをクリーンアップします。
- 既存のプログラムを開くか、クリーニング モード (すなわち、[クリーン] タブで選択されているクリーンチェック ボックス) と 1 つの定式化ユニットの操作を含む新しいプログラムを作成します。補足資料図 S10例についてを参照してください。
- リザーバーきれいな希釈 (浄化/定式化サブシステム フロント) 100 mL の EtOH で。
- (> 50 mL のエタノールを含む) 江藤貯水池の浄化/定式化サブシステム想定し, 浸出液入力行を配置します。
- 最終製品の出力ラインと共に廃棄物コンテナーのリンスと再構成の入力行を配置します。
- プログラムを実行します。
- 終了後、廃棄容器を空にします。
結果
[18F] の生産を自動化する方法 CFA が開発され、3 つの検証バッチを合成しました。合成・精製・定式化 [18F] の CFA で達成された 90 ± 5 分 (n = 3) 非減衰補正放射収量は 8.0 ± 1.4% (n = 3)。3.24 GBq、2.83 GBq 3.12 GBq、それぞれ 34.3 GBq、41.8 GBq 41.1 GBq から開始され、3 失点のアクティビティは待機。得られた [18F] CFA 製剤は、すべての品質管理試験 (表 1) を渡されます。自動化されたプロトコルは、臨床試験をサポートする臨床グレード [18F] CFA の生産のため現在使用されています。
| 品質管理データ | 検証 1 を実行 | 検証 2 を実行 | 検証 3 を実行 |
| ["Pass"の要件] | |||
| 外観 | 渡す | 渡す | 渡す |
| [クリア、無色、粒子状物質の無料] | |||
| EOS で放射能濃度 | 213 MBq/mL | 210 MBq/mL | 180 MBq/mL |
| [≤ 740 MBq/mL @ EOS] | |||
| pH | 6 | 5.8 | 6 |
| [5.0-8.0] | |||
| 半減期 | 115 分 | 108 分 | 112 分 |
| [105-115 分] | |||
| 放射化学的純度 | 99% | 99% | 99% |
| [> 95%] | |||
| 相対保持時間 (RRT) 放射化学アイデンティティ | 1.01 | 1.01 | 1.01 |
| [1.00 < RRT < 1.10] | |||
| 臼歯部の活動 | 314 GBq/µmol | > 370 GBq/µmol | > 370 GBq/µmol |
| [≥ 3.7 GBq/µmol] | |||
| 最終製品の総キャリアの固まり | 3.1 μ g | < 1 μ g | < 1 μ g |
| [≤ 50 μ g/用量] | |||
| 最終製品における不純物合計質量 | ND | ND | ND |
| [≤ 1 μ g/用量] | |||
| 最大許容注入量に基づいて総キャリア大量 ≤ 50 μ g/線量と不純物合計質量 ≤ 1 μ g/線量 | 全体のバッチ | 全体のバッチ | 全体のバッチ |
| ガスクロマトグラフィーによる残留エタノール コンテンツ | 8.90% | 9.50% | 9.60% |
| [≤ 10%] | |||
| ガスクロマトグラフィーによる残留の EtOAc コンテンツ | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ 5000 ppm] | |||
| ガスクロマトグラフィーによる残留 MeCN コンテンツ | < 1 ppm | < 1 ppm | < 1 ppm |
| [≤ 410 ppm] | |||
| カラー スポット試験による残留 K222 | 渡す | 渡す | 渡す |
| [< 50 μ g/mL] | |||
| フィルター膜の整合性テスト | 渡す | 渡す | 渡す |
| [バブル ポイント ≥ 50 psi] | |||
| エンドトキシン | 渡す | 渡す | 渡す |
| [≤ 175 EU/バッチ] | |||
| ガンマの分光学によって radionuclidic の純度 | 渡す | 渡す | 渡す |
| [> 99.5%] | |||
| 不妊 | 渡す | 渡す | 渡す |
| [USP < 71 > の要件を満たす] |
表 1: 品質管理 (QC) テスト データ集計検証の 3 つのバッチにします。EOB = 末衝突;EOS = 合成; 末ND = 検出されたではないです。

図 1: [18F] CFA radiosynthesis スキーム。MMT Monomethoxytrityl を =。この図の拡大版を表示するのにはここをクリックしてください。

図 2: 手動合成の単位操作の自動化シーケンスへの変換。(A) このパネル、大まかな手順の概要を説明 [18F] の手動合成 CFA。このパネル (B) では、各手順の実行に必要な基本的な手順を示しています。(C) Radiosynthesizer 固有ユニットの操作の基本的な手順を実行するために使用、カードとして表示されます。パラメーター値の独自のセットには各単位操作 (下線付きで示されている) ソフトウェアによって構成されています。表記"R1"と"R2"#1 と 2、反作用の容器をそれぞれ示します。試薬番号に対応する試薬は、図 4で示されます。単位操作のシリーズはシーケンスとして保存、自動合成を実行するソフトウェアによって実行されます。この図の拡大版を表示するのにはここをクリックしてください。

図 3: 合成プログラムを作成する radiosynthesizer (ELIXYS) のソフトウェア インターフェイスのスクリーン ショットします。単位操作は、ドラッグ アンド ドロップ インターフェイスを使用して写真の目的の順序で配置されます。このスクリーン ショットで反応ユニットの操作が選択されていると、編集可能なパラメーター値が画面のメイン部分に表示されます。この例では、アクティブな攪拌しながら 10 分間反応容器 120 ° C で (シール) #1 にすると、フッ素化反応は実施されます。反応時間が経過した後、容器が 35 ° C に冷却されます。他のユニットの操作をプログラムすることができますパラメーター値の詳細は、補足資料セクション 3のとおりです。この図の拡大版を表示するのにはここをクリックしてください。

図 4: 試薬の設定画面のスクリーン ショットします。[18F] CFA 合成シーケンスのすべての試薬は、コンポーネントの選択領域で強調表示されている使い捨てカセット #1 に読み込まれます。ここで説明 [18F] CFA の合成、溶離液1.0 mg の K2CO3 + K222 MeCN、前駆体の H2O/0.5 mL の 0.4 mL で 5.0 mg は MeCN、0.6 mL で CFA 前駆体の 6 mg、 HPLC 移動相は 85:15 v/v 25 mM アンモニウム酢酸: エタノール。この図の拡大版を表示するのにはここをクリックしてください。

図 5: Radiosynthesizer セットアップ [18F] の合成に CFA 。(A) これはカセット流体パス、カートリッジへの接続および転送する接続を示す模式図浄化/処方モジュールに radiosynthesis モジュールから最終的な粗製品。(両方のモジュールは、単一のコンピューターおよびソフトウェアのインタ フェースで制御される)(B) [18F] CFA 合成の準備の後、ホットセル内 radiosynthesizer の写真です。この図の拡大版を表示するのにはここをクリックしてください。

図 6: 浄化/定式化モジュールの制御インターフェースのスクリーン ショットします。この画面は合成のセットアップ中に高速液体クロマトグラフィーおよび定式化サブシステムを手動で制御するオペレーターによってアクセスされます。この図の拡大版を表示するのにはここをクリックしてください。

図 7: 実行前チェックリスト画面。演算子は、システムにインストールされているカセットのシリアル番号を入力し、システムを正しく構成し、合成のために準備を確保するために各項目をオフにチェックする必要があります。これらのセクションに加えて、オペレーターはまた求め名前と合成の説明 (セクション 1) を実行および多くすべて試薬使用されます (セクション 2) の番号しすべての炉ビデオ フィードが正しく機能していることを確認するように求めている (セクション 6)。この図の拡大版を表示するのにはここをクリックしてください。

図 8: [18F] CFA 合成シーケンスを実行中に radiosynthesizer ソフトウェアのスクリーン ショットします。ソフトウェアでは、フィルム ストリップ地区単位操作の順序が表示されます。完了した操作はグレーし白で強調表示されている、現在の操作が、灰色で強調表示されます、今後操作が暗い灰色で表示されます。画面の中央の領域は、どのサブコマンドを実行するを含む、アクティブな単位操作の状態だけでなく、システムの現在のステータス (炉動画のフィードとセンサー データ) を示しています。反応するとこの特定ユニットの操作は、フッ素化反応。Temp領域に現在の原子炉の温度は (プログラム) ターゲット温度の横に表示されます。この下に、活動領域は、反応ステップに関連付けられた 3 つのセンサーから放射線センサーの値を表示します。最後に、左側のビデオフィードは原子炉バイアルのライブビューが表示されます。この図の拡大版を表示するのにはここをクリックしてください。
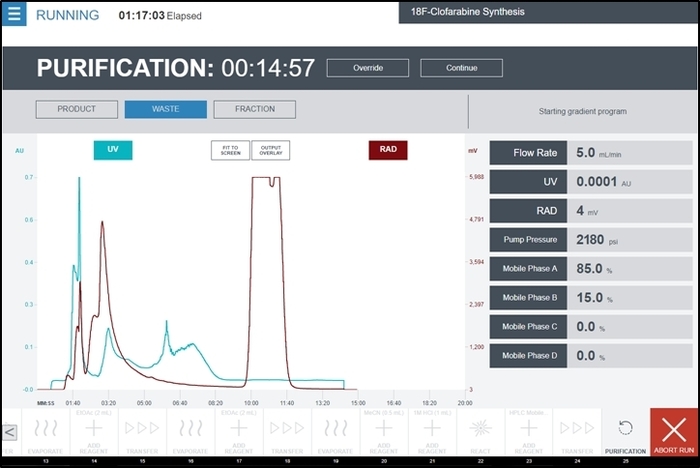
図 9: スクリーン ショット [18F] の合成の際に浄化ユニットの操作を実行している間 radiosynthesizer のユーザー インターフェイスの CFA。の UV 検出器及び放射線検出器浄化/定式化モジュールの出力がリアルタイムで中央のグラフに表示されます。検出器、高速液体クロマトグラフィー ポンプからのフィードバックは、画面の右側に表示されます。オペレーターは、ピークが表示を開始したとき、一時的に製品を選択して切り替え、廃棄物に戻す完全なピークを見た後で製品のピークを収集します。この図の拡大版を表示するのにはここをクリックしてください。
ディスカッション
このプロトコルは、臨床グレード トレーサー製剤の生産を達成するために手動統合のプロトコルを自動化しているときに撮影する必要があります基本的な手順を定義します。品質管理開発を含む全体の開発サイクルは、[18F] ラジオト レーサーによって例証される CFA (dCK 活動用)。臨床使用のためのトレーサーの適合性を確保するため自動合成の変更に特に注意を払いました。合成 [18F] フッ化物の活性化など、前駆体分子、中間カートリッジ精製、保護グループの削除とセミ分取 HPLC 精製、製剤の radiofluorination の基本的なプロセスが伴います注射。これらの基本的なプロセスは、 18F 標識ペット トレーサーの大半の合成のために十分な標準的なレパートリーを構成します。
合成を設計している間試薬とその品質保証の選択は臨床使用のため特に重要です。モックの合成 (溶媒のみ) を実行することによって適切なプログラミングと適切な接続を確保する放射能と、合成が実行されるときに予期しないエラーを排除することが不可欠です。その後合成の最適化 (溶剤、ボリューム、量、温度、反応時間、および精製条件) は、開発の特定のペット トレーサーによって異なります。これらの実験の中には、特定のフォーカスを輝いていた達成することができる最終製品の化学的・放射化学的純度、これらは臨床使用のための厳しい要件を満たす必要がある必要があります。下で十分な利回りの純粋な製品を確実に生成する合成が散発的に失敗するリスクより高い降伏プロセス通常優先されます。合成が適切に最適化されている最終工程 (規制要件) 臨床の適合性を確保するための検証テストを受ける必要があります。検証済みの合成法は、臨床用ペット トレーサーを生成する使用できます。検証された方法に従ってペット トレーサーを合成する場合標準の運用手順を徹底的に従う必要があります。コンプライアンス、ソフトウェアをプログラムして、演算子合成を開始する実行をクリックした後の重要なステップを介して実行前チェックリストの完了を確認しています。システムは、自動化された方法で合成を実行が、浄化手順手動介入が必要です。オペレーターはする必要があります、したがって、HPLC 精製段階では、ガスクロマト グラフ画面を注視、開始および停止製品の割合を収集するときリアルタイムで手動で入力します。
アンモニウム酢酸溶液とエタノールから成る注射溶媒系を用いた製品の混合物のセミ分取 HPLC 精製法を合理化し自動化、最適化の取り組み [18F] CFA 合成内;従来法浄化16後溶媒を交換するための追加の手順が必要。後続の定式化処理、したがって、フラクションのレベルを許可してどちらの希釈によって行うことができます、その isotonicity を確保するためのエタノールの量を減らすだけ必要です。定式化の手順を行った変数を考慮する定式化モジュール、精製した製品分数を経由する NaCl 水溶液の可変ボリュームの追加を許可する単一の定式化ユニットの操作から成る 2 番目のプログラムを使用して高速液体クロマトグラフィー精製後に得られるボリュームです。収集した製品の分数ボリュームだった代わりに定数であると設定されている場合、定式化ユニットの操作はメイン合成プログラムは、独立したプログラムの必要性を避けることで含めることが。手動での介入を避けるために代替的アプローチ、定式化モジュールのすべての機能を使用すること (例えば、希釈水で浄化されたトレーサー C18 固相抽出カートリッジでトラップをそれを洗浄、エタノールの固定量と溶出、最後に、一定量の生理食塩水で希釈し、)。
自動化と臨床使用のための統合のプロトコルの検証のためここで紹介しているテクニックは、かなり一般的にするものです。Radiosynthesizer (ELIXYS) の選択により、幅広い合成自動化および検証できます。これは複雑な 3 ポット合成含まれていますまたは揮発性溶剤の高温を含む合成。合成の最適化は、ソフトウェア プログラムのパラメーターを変更することによって実現できます。シンセサイザーには、TLC のラジオやラジオ HPLC 分析用試料の除去のための反作用の容器の配置などの変更の影響を監視する機能があります。ただし、システム変更することがなくシステム現在できません非常に低い試薬ボリューム (~ 5-20 μ L)、中間製品の蒸留、または [18F] の取扱いの取扱いのアルフ、 68Ga、または他の radiometals。自動化する手動の合成にこのような手順が含まれています、彼らは回避することはできません、自動化および別の radiosynthesizer プラットフォームで検証は適切かもしれません。
この作業は、[18F] の自動化生産のためのプロトコルの開発に焦点を当てたが CFA 臨床用、その他の多くのペットのトレーサーの合成自動化できる臨床の生産に適した方法で同じロジックとメソッド。次のメソッドは、ここで示した、我々 も 9 の自動合成を適応している (4-[18F] フッ素 - 3-[ヒドロキシメチル] ブチル) グアニン ([18F] FHBG) および臨床用検証します。ユーザーによって設定されたプロトコルにアップロードすることができますソフィー プローブのネットワーク、合成プログラムを共有するための web ポータルからダウンロードし、異なる radiopharmacy サイト27の間でドキュメントを関連付けられています。これはコミュニティの努力の重複を避けるためでき、pet を含む多施設臨床調査を促進します。
開示事項
カリフォルニア大学の理事ジェフリー ・ コリンズ ・ r ・ マイケル ・ ヴァン ・ ダムによって発明されたソフィーに技術供与しているが、ライセンスのトランザクションの一部としてソフィー持分を撮影します。さらに、r ・ マイケル ・ ヴァン ・ ダムは創始者とソフィーのコンサルタントです。この整理の言葉が検討されており、その利益相反ポリシーに従ってロサンゼルス カリフォルニア大学によって承認されました。エリック Schopf とクリストファー ・ ドレイクが従業員とソフィーの株主です。
謝辞
この作品は、国立癌研究所 (R44 CA216539) と分子イメージングのラルフと UCLA crump さん所のマージョリー crump さんによって行われた寄付から UCLA 財団が一部サポートされています。
資料
| Name | Company | Catalog Number | Comments |
| ELIXYS FLEX/CHEM | Sofie (Culver City, CA, USA) | 1010001 | Radiosynthesizer |
| Radiosynthesizer cassette | Sofie (Culver City, CA, USA) | 1861030400 | Cassette for ELIXYS FLEX/CHEM |
| ELIXYS PURE/FORM | Sofie (Culver City, CA, USA) | 1510001 | Radiosynthesizer purification module |
| [O-18]H2O | IBA RadioPharma Solutions (Reston, VA, USA) | IBA.SP.065 | >90% isotopic purity |
| [F-18]fluoride in [O-18]H2O | UCLA | N/A | Produced in a cyclotron (RDS-112; Siemens; Knoxville, TN, USA) by the (p,n) reaction of [O-18]H2O. Bombardment at 11 MeV using a 1 mL tantalum target with havar foil. |
| Deionized water | UCLA | N/A | Purified to 18 MΩ and passed through 0.1 µm filter |
| Acetonitrile (MeCN) | Sigma-Aldrich (St. Louis, MO, USA) | 271004 | Anhydrous, 99.8% |
| Ethanol (EtOH) | Decon Laboratories, Inc. (King of Prussia, PA, USA) | 2701 | Anhydrous, 200 proof |
| Sodium hydroxide (NaOH) solution | Merck (Burlington, MA, USA) | 1.09137.1000 | 1M solution |
| Hydrochloric acid (HCl) solution | Fisher Chemical (Hampton, NH, USA) | SA48-500 | 1M solution |
| Ethyl acetate (EtAc) | Fisher Chemical (Hampton, NH, USA) | E195SK-4 | HPLC grade |
| Sodium chloride (NaCl) | Fisher Chemical (Hampton, NH, USA) | S-640-500 | USP grade |
| Ammonium acetate | Fisher Chemical (Hampton, NH, USA) | A639-500 | HPLC grade |
| Potassium carbonate (K2CO3) | Fisher Chemical (Hampton, NH, USA) | P-208-500 | Certified ACS |
| CFA precursor | CalChem Synthesis (San Diego, CA, USA) | N/A | Custom synthesis |
| Cryptand 222 (K222; Kryptofix 2.2.2) | ABX Advanced Biochemical Compounds (Radeberg, Germany) | 800.1000 | >99% |
| Sodium chloride (NaCl) solution (saline) | Hospira (Lake Forest, IL, USA) | 0409-4888-02 | 0.9%, for injection, USP grade |
| Silica cartridge | Waters (Milford, MA, USA) | WAT051900 | Sep-pak Classic |
| Quaternary methylammonium (QMA) cartridge | Waters (Milford, MA, USA) | WAT023525 | Sep-pak Light Plus |
| Sterile syringe filter (0.22 µm) | Millipore Sigma (Burlington, MA, USA) | SLGSV255F | Millex-GV |
| Glass V-vial (5 mL) | Wheaton (Millville, NJ) | W986259NG | Used for reaction vessels |
| Septa | Wheaton (Millville, NJ) | 224100-072 | Used for reagent vials |
| Crimp cap | Wheaton (Millville, NJ) | 224177-01 | Used for reagent vials |
| Amber serum vial (2 mL) | Voigt (Lawrence, KS, USA) | 62413P-2 | Used for reagent vials |
| Magnetic stir bar | Fisher Scientific (Hampton, NH, USA) | 14-513-65 | Used for reaction vessels |
参考文献
- Phelps, M. E. Positron emission tomography provides molecular imaging of biological processes. Proceedings of the National Academy of Sciences. 97 (16), 9226-9233 (2000).
- Kitson, S., Cuccurullo, V., Ciarmiello, A., Salvo, D., Mansi, L. Clinical Applications of Positron Emission Tomography (PET) Imaging in Medicine: Oncology, Brain Diseases and Cardiology. Current Radiopharmaceuticalse. 2 (4), 224-253 (2009).
- Sengupta, D., Pratx, G. Imaging metabolic heterogeneity in cancer. Molecular Cancer. 15, 4(2016).
- Rabinovich, B. A., Radu, C. G. Imaging Adoptive Cell Transfer Based Cancer Immunotherapy. Current Pharmaceutical Biotechnology. 11 (6), 672-684 (2010).
- Matthews, P. M., Rabiner, E. A., Passchier, J., Gunn, R. N. Positron emission tomography molecular imaging for drug development. British Journal of Clinical Pharmacology. 73 (2), 175-186 (2012).
- Hargreaves, R. The Role of Molecular Imaging in Drug Discovery and Development. Clinical Pharmacology & Therapeutics. 83 (2), 349-353 (2008).
- Radiosynthesis Database of PET Probes (RaDaP). , Available from: http://www.nirs.qst.go.jp/research/division/mic/db2/ (2017).
- 18F-Database of Imaging Radiolabelled Compounds (DIRAC). , Centre National de la Recherche Scientifique. Available from: http://www.iphc.cnrs.fr/dirac/ (2013).
- Keng, P. Y., Esterby, M., van Dam, R. M. Emerging Technologies for Decentralized Production of PET Tracers. Positron Emission Tomography - Current Clinical and Research Aspects. Hsieh, C. -H. , InTechOpen. London, UK. 153-182 (2012).
- Lazari, M., Irribarren, J., Zhang, S., van Dam, R. M. Understanding temperatures and pressures during short radiochemical reactions. Applied Radiation and Isotopes. , 82-91 (2016).
- Lazari, M., et al. ELIXYS - a fully automated, three-reactor high-pressure radiosynthesizer for development and routine production of diverse PET tracers. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3 (1), 52(2013).
- Claggett, S. B., Quinn, K., Lazari, M., Esterby, J., Esterby, M., van Dam, R. M. A new paradigm for programming and controlling automated radiosynthesizer. Journal of Nuclear Medicine. 53 (suppl. 1), 1471-1471 (2012).
- Claggett, S. B., Quinn, K. M., Lazari, M., Moore, M. D., van Dam, R. M. Simplified programming and control of automated radiosynthesizers through unit operations. European Journal of Nuclear Medicine and Molecular Imaging (EJNMMI) Research. 3, 53(2013).
- Lazari, M., et al. Fully Automated Production of Diverse 18F-Labeled PET Tracers on the ELIXYS Multireactor Radiosynthesizer Without Hardware Modification. Journal of Nuclear Medicine Technology. 42 (3), 203-210 (2014).
- Lazari, M., et al. Fully-automated synthesis of 16β-18F-fluoro-5α-dihydrotestosterone (FDHT) on the ELIXYS radiosynthesizer. Applied Radiation and Isotopes. 103, 9-14 (2015).
- Collins, J., et al. Production of diverse PET probes with limited resources: 24 18F-labeled compounds prepared with a single radiosynthesizer. Proceedings of the National Academy of Sciences. 114 (43), 11309-11314 (2017).
- Drake, C., et al. Enzymatic Radiofluorination of Biomolecules: Development and Automation of Second Generation Prosthetic on ELIXYS Radiosynthesizer. Journal of Nuclear Medicine. 58 (supplement 1), 1(2017).
- Gobbi, L. C., et al. Identification of Three Novel Radiotracers for Imaging Aggregated Tau in Alzheimer's Disease with Positron Emission Tomography. Journal of Medicinal Chemistry. 60 (17), 7350-7370 (2017).
- Ippisch, R., Maraglia, B., Sutcliffe, J. Automated production of [18F]-F-Py-peptides. Journal of Nuclear Medicine. 57, 275(2016).
- Chen, H., et al. AMG 580: A Novel Small Molecule Phosphodiesterase 10A (PDE10A) Positron Emission Tomography Tracer. Journal of Pharmacology and Experimental Therapeutics. 352 (2), 327-337 (2015).
- Waldmann, C. M., et al. An Automated Multidose Synthesis of the Potentiometric PET Probe 4-[18F]Fluorobenzyl-Triphenylphosphonium ([18F]FBnTP). Molecular Imaging and Biology. 20 (2), 205-212 (2018).
- Ravert, H. T., et al. An improved synthesis of the radiolabeled prostate-specific membrane antigen inhibitor, [18F]DCFPyL. Journal of Labelled Compounds and Radiopharmaceuticals. 59 (11), 439-450 (2016).
- Betthauser, T. J., et al. Characterization of the radiosynthesis and purification of [18F]THK-5351, a PET ligand for neurofibrillary tau. Applied Radiation and Isotopes. 130, 230-237 (2017).
- Shu, C. J., et al. Novel PET probes specific for deoxycytidine kinase. Journal of Nuclear Medicine. 51 (7), 1092-1098 (2010).
- Kim, W., et al. [18F]CFA as a clinically translatable probe for PET imaging of deoxycytidine kinase activity. Proceedings of the National Academy of Sciences. 113 (15), 4027-4032 (2016).
- Barrio, M. J., et al. Human Biodistribution and Radiation Dosimetry of 18F-Clofarabine, a PET Probe Targeting the Deoxyribonucleoside Salvage Pathway. Journal of Nuclear Medicine. 58 (3), 374-378 (2017).
- SOFIE. Sofie Probe Network. , Available from: http://www.sofienetwork.com/ (2018).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved