Determinazione della densità di un solido e di un liquido
Panoramica
Fonte: Laboratorio del Dr. Michael Evans — Georgia Institute of Technology
Il rapporto tra la massa di una sostanza e il suo volume è noto come densità di massa o, semplicemente, densità della sostanza. La densità è espressa in unità di massa per volume, come g/mL o kg/m3. Poiché la densità di una sostanza non dipende dalla quantità di sostanza presente, la densità è una "proprietà intensiva".
Per misurare la densità di un campione di materiale, è necessario determinare sia la massa che il volume del campione. Sia per i solidi che per i liquidi, è possibile utilizzare una bilancia per misurare la massa; tuttavia, i metodi per determinare il volume sono diversi per solidi e liquidi. Poiché i liquidi possono fluire e assumere le forme dei loro contenitori, oggetti in vetro come un cilindro graduato o un pallone volumetrico possono essere utilizzati per misurare il volume di un liquido. Il volume di un solido di forma irregolare può essere misurato mediante immersione in un liquido - la differenza di volume causata dall'aggiunta del solido è uguale al volume del solido.
Questa dimostrazione illustra i metodi per misurare la densità di solidi e liquidi. Utilizzando un pallone volumetrico e una bilancia analitica, è possibile determinare la densità dell'etanolo. Utilizzando un cilindro graduato, una bilancia analitica e l'acqua come liquido spostato, è possibile determinare la densità del metallo zinco.
Principi
Per definizione, tutta la materia ha massa e occupa volume. La densità di una sostanza è il rapporto tra la sua massa e il suo volume. A temperatura e pressione costanti, la densità di una sostanza è costante.
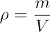
La densità è una proprietà intensiva di una sostanza che non dipende dalla quantità di sostanza presente. Pertanto, la densità può essere utilizzata per identificare una sostanza pura sconosciuta se è disponibile un elenco di densità di riferimento e lo sperimentatore può scegliere una quantità conveniente di sostanza con cui lavorare quando misura la densità.
Per misurare la densità di un campione di una sostanza, è necessario misurarne la massa e il volume. La massa viene tipicamente misurata utilizzando una bilancia analitica, uno strumento preciso che si basa sulla forza esercitata dal campione a causa della gravità. Il contenitore per contenere il campione (utilizzato anche per misurare il volume) viene pesato e tarato, quindi solo la massa del campione appare sul display della bilancia quando il campione viene aggiunto al contenitore.
Per i liquidi, questo contenitore è in genere un pallone volumetrico, che ha una marcatura che corrisponde a un volume specifico. Il contenitore viene riempito fino alla linea con il campione liquido e pesato nuovamente dopo che il matraccio vuoto è stato tarato. La densità misurata è il rapporto tra la massa misurata e il volume indicato sul matraccio.
La maggior parte delle sostanze solide sono di forma irregolare, il che complica la determinazione del volume. È impreciso, ad esempio, determinare il volume di una polvere misurandone le dimensioni. Invece di misurare direttamente le dimensioni o utilizzare vetreria come un pallone volumetrico, è necessario utilizzare un metodo di spostamento del liquido per misurare il volume di un solido di forma irregolare. Un cilindro graduato contenente un volume noto di liquido (in cui il solido è insolubile) viene tarato. Il solido viene aggiunto al cilindro e la massa totale viene pesata di nuovo per determinare la massa del solido. L'aggiunta del solido provoca uno spostamento verso l'alto del liquido, con conseguente nuova lettura del volume. Il volume del solido è uguale alla variazione di volume dovuta allo spostamento del liquido(cioè, la differenza di volume del liquido prima e dopo l'aggiunta del solido).
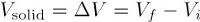
Per quanto riguarda i liquidi, la densità misurata di un campione solido è il rapporto tra la massa misurata e il volume misurato.
Procedura
1. Determinazione della densità dell'etanolo liquido
- Posizionare un matraccio volumetrico da 50 ml pulito e asciutto su una bilancia analitica.
- Premere il pulsante "Tare" o "Zero" sulla bilancia. La bilancia dovrebbe leggere 0,000 g.
- Utilizzare un imbuto buret per aggiungere 45 ml di etanolo liquido al pallone volumetrico.
- Utilizzare una pipetta Pasteur per aggiungere gli ultimi 5 ml di liquido, fino a quando il fondo del menisco del liquido tocca la marcatura sul pallone.
- Pesare nuovamente il pallone volumetrico e registrare la massa dell'etanolo.
- Per ottenere risultati ottimali, ripetere i passaggi da 1,1 a 1,5 due volte di più per ottenere due misurazioni di densità aggiuntive.
2. Determinazione della densità del metallo solido di zinco
- Aggiungere circa 40 ml di acqua a un cilindro graduato da 100 mL pulito e asciutto. Registrare il volume esatto dell'acqua.
- Posizionare il cilindro e l'acqua su una bilancia analitica. Premere il pulsante "Tare" o "Zero" sulla bilancia. La bilancia dovrebbe leggere 0,000 g.
- Aggiungere circa 10 pellet di zinco al cilindro graduato. Registrare il nuovo volume dell'acqua più pellet di zinco utilizzando il livello del liquido dopo l'aggiunta dello zinco (Figura 1).

Figura 1. Lo zinco aggiunto al cilindro a destra provoca lo spostamento del livello dell'acqua verso l'alto. - Pesare il cilindro, l'acqua e i pellet di zinco sulla bilancia. Registrare la massa dei pellet di zinco.
- Per ottenere risultati ottimali, ripetere i passaggi da 2,1 a 2,4 due volte di più per ottenere due misurazioni di densità aggiuntive.
Risultati
La tabella 1 elenca i risultati per la determinazione della densità dell'etanolo utilizzando un matraccio volumetrico da 50 ml. Le densità sono state calcolate dividendo la massa misurata per 50,0 ml. La densità media misurata era di 0,789 ± 0,001 g/ml. La tabella 2 elenca i risultati per la determinazione della densità di un campione di zinco metallico utilizzando un cilindro graduato da 100 ml e il metodo dello spostamento del liquido. Si noti che le densità misurate sono costanti (entro errore sperimentale) per entrambe le sostanze. La tabella 2, in particolare, dimostra che la densità è indipendente dalla quantità di sostanza studiata.
| Prova | Massa di etanolo (g) | Volume di etanolo (mL) | Densità (g/mL) |
| 1 | 39.448 | 50.0 | 0.789 |
| 2 | 39.392 | 50.0 | 0.788 |
| 3 | 39.489 | 50.0 | 0.790 |
Tabella 1. Risultati per la determinazione della densità dell'etanolo utilizzando un matraccio volumetrico da 50 ml.
| Prova | Massa di zinco (g) | Volume di zinco (mL) | Densità (g/mL) |
| 1 | 5.6133 | 0.9 | 6.2 |
| 2 | 7.6491 | 1.2 | 6.3 |
| 3 | 8.2164 | 1.3 | 6.3 |
Tabella 2. Risultati per la determinazione della densità di un campione di zinco metallico utilizzando un cilindro graduato da 100 ml e il metodo dello spostamento del liquido.
Applicazione e Riepilogo
La densità è una caratteristica proprietà intensiva di una sostanza. Pertanto, le misurazioni della densità possono essere utilizzate per identificare una sostanza pura sconosciuta se è disponibile un elenco di possibili densità di riferimento. Ad esempio, la densità può essere utilizzata per distinguere tra metalli simili nell'aspetto esteriore (Figura 2).
In contesti in cui è auspicabile una massa molto bassa o molto elevata, la densità è una proprietà critica del materiale. Gli ingegneri dei materiali considerano attentamente la densità dei materiali per la costruzione in questi contesti. Ad esempio, i corpi di alcuni computer portatili leggeri sono realizzati in alluminio, uno dei metalli meno densi. Le racchette da tennis leggere contengono titanio, un altro metallo a bassa densità.

Figura 2: Masse equivalenti di alluminio (Al) e zinco (Zn) metallico. Lo zinco metallico occupa un volume molto più piccolo a causa della sua maggiore densità.
Vai a...
Video da questa raccolta:

Now Playing
Determinazione della densità di un solido e di un liquido
General Chemistry
556.0K Visualizzazioni

Vetreria di laboratorio e relativi usi
General Chemistry
655.9K Visualizzazioni

Soluzioni e concentrazioni
General Chemistry
274.1K Visualizzazioni

Determinazione della composizione percentuale di massa in una soluzione acquosa
General Chemistry
383.4K Visualizzazioni

Determinazione della formula empirica (minima)
General Chemistry
181.8K Visualizzazioni

Determinazione delle regole di solubilità di composti ionici
General Chemistry
141.4K Visualizzazioni

Uso del pH-metro
General Chemistry
345.6K Visualizzazioni

Introduzione alla titolazione
General Chemistry
424.3K Visualizzazioni

Legge dei gas perfetti
General Chemistry
78.4K Visualizzazioni

Determinazione spettrofotometrica di una costante di equilibrio
General Chemistry
158.5K Visualizzazioni

Principio di Le Châtelier
General Chemistry
265.1K Visualizzazioni

Depressione del punto di congelamento per l'identificazione di un composto sconosciuto
General Chemistry
160.7K Visualizzazioni

Determinazione dell'equazione cinetica e dell'ordine di reazione
General Chemistry
196.1K Visualizzazioni

Utilizzo della calorimetria a scansione differenziale per misurare cambiamenti nell'entalpia
General Chemistry
44.5K Visualizzazioni

Complessi chimici di coordinazione
General Chemistry
91.4K Visualizzazioni