Method Article
כינונה מחדש של חלבון טראנסממברנלי, יון ערוץ מתח מגודרת, KvAP, לענק Unilamellar שלפוחית למיקרוסקופי וצמד תיקון ללימודים
In This Article
Summary
הכינון מחדש של החלבון הטרנסממברני, KvAP, לתוך שלפוחית unilamellar ענקית (GUVs) הוא הוכיח לשתי שיטות התייבשות-החזרת נוזלים - electroformation, ונפיחות בסיוע ג '. בשני השיטות, שלפוחית unilamellar קטנה המכילה החלבון הם התמזגו יחד כדי ליצור GUVs כי אז יכול להיות שנחקר על ידי מיקרוסקופ פלואורסצנטי ואלקטרופיזיולוגיה תיקון מהדק.
Abstract
הענק Unilamellar שלפוחית (GUVs) היא מערכת פופולרית biomimetic לחקר התופעות הקשורות קרום. עם זאת, נפוץ פרוטוקולים לגדול GUVs חייב להיות שונה כדי ליצור GUVs המכיל חלבונים הטרנסממברני פונקציונליים. מאמר זה מתאר שתי שיטות התייבשות-החזרת נוזלים - electroformation ונפיחות בסיוע ג '- כדי ליצור GUVs המכיל אשלגן ערוץ המתח מגודרת, KvAP. בשתי השיטות, פתרון של שלפוחית unilamellar קטנה המכיל חלבון מיובש באופן חלקי כדי ליצור ערימה של ממברנות, אשר לאחר מכן מותרת להתנפח בחיץ להחזרת נוזלים. לשיטת electroformation, הסרט מופקד על אלקטרודות פלטינה, כך ששדה AC יכול להיות מיושם בהחזרת נוזלי סרט. בניגוד לכך, שיטת הנפיחות בסיוע ג 'משתמשת במצע ג'ל agarose כדי לשפר את התייבשות סרט. שני שיטות יכולות לייצר GUVs ב( למשל, 100 מ"מ) ריכוזי מלח נמוכים (למשל, 5 מ"מ) ופיסיולוגיים. GUVs וכתוצאה מכך מאופיין באמצעות מיקרוסקופ פלואורסצנטי, והפונקציה של ערוצים מחדש נמדדה באמצעות תצורת תיקון מהדק מבפנים החוצה. בעוד נפיחות בנוכחות שדה חשמלי משתנה חשמלי (electroformation) נותנת תשואה גבוהה של GUVs ללא פגם, שיטת הנפיחות בסיוע ג 'מייצרת הפצת חלבון הומוגנית יותר ולא דורשת ציוד מיוחד.
Introduction
כאשר לומדים את העקרונות הפיסיקליים ששולטים במערכות חיים, גישות מלמטה למעלה תאפשר לשלוט בניסויי הרכב מערכת ופרמטרים נוספים שאינם מניפולציות בקלות במערכות מבוססות תאים 1. לתהליכים מבוססי קרום, Giant Unilamellar שלפוחית (GUVs, קוטר ~ 1-100 מיקרומטר) הוכיחו להיות מערכת biomimetic מאוד שימושית 2-7 כפי שהם מתאימים לבחינה מיקרוסקופית ומיקרומניפולציה 8-10. אמנם יש פרוטוקולים רבים ושונים כדי לייצר GUVs, רוב מתחלקים לשתי קטגוריות - תחליב המבוסס גישות 11,12 וטכניקות המבוססות על rehydrating סרט שומנים 13-16. בשיטות המבוססת על אמולסיה, העלונים הפנימיים וחיצוניים של קרומי הבוס הם התאספו ברצף מmonolayers שומנים בממשקים מים / שמן. גישה זו היא אידיאלית עבור מתמצת חלבונים מסיסים בבGUVs, וגיבוש GUVs עם הרכב שומנים עלון א-סימטרי. עם זאת, GUVs נוצר מתחליבים יכול לשמור עקבות של ממס שמשנות את התכונות מכאניות של הקרום 17, והגישה היא לא במיוחד מתאימה היטב לכינון מחדש חלבון טרנס-קרום.
שיטות להחזרת נוזלי סרט מסתמכות על העובדה שהייבוש (התייבשות) גורם תערובות שומנים רבות כדי ליצור ערימה רבת-שבשבת של ממברנות. אם זה ערימה ממוקמת אז במגע עם חיץ המימי, קרומים בערימה יעברו תזרים בנפרד ממס כביניהם ועל פני השטח של הערימה, קרומי אדם יכולים לנתק כדי ליצור GUVs 13,18 (כמו גם גן חיות אמיתית של אובייקטי lipidic אחרים). עם זאת, גם ליצירות חיץ ושומנים בדם אופטימליות, יש בשיטה זו קלסית "נפיחות ספונטנית" תשואה נמוכה יחסית של GUVs ללא פגם. שיטה נפוצה אחת כדי להגביר את התשואה של GUVs ללא פגם היא "electroformation221 ;, שבו שדה זרם חילופין (AC) מיושם בהחזרת נוזלי סרט. בעוד המנגנון נותר הבין היטב, "electroformation" יכול לתת תשואות בוס מרהיבות (> 90% בנסיבות חיוביות) למאגרי ריכוז נמוך מלח (<5 מ"מ) 14,19, ואפילו יכול לעבוד במאגרים פיסיולוגיים (~ 100 מ"מ) באמצעות תדירות גבוהה יותר (500 הרץ לעומת 10 הרץ) שדה AC ואלקטרודות פלטינה 15. גישה חלופית כדי להגביר את התשואה של GUVs ללא פגם היא "בסיוע ג 'נפיחות", שבו פתרון השומנים מופקד על מצע ג'ל פולימרים ולא פסיבי מצעים (למשל, זכוכית, PTFE) המשמשים ב" נפיחות ספונטנית קלסית ". כאשר סרט השומנים / ג'ל התוצאה הוא rehydrated, GUVs יכול במהירות ליצור אפילו למאגרים פיסיולוגיים 16,20.
כל השיטות הללו יכולים לייצר GUVs שומנים בדם היחיד שיכול לשמש כדי לחקור תופעות קרום הקשורים כגוןאינטראקציה בין חלבונים וקרומים מסיסים. עם זאת, כדי לשלב חלבון טרנס-קרום לGUVs, יש צורך בשינויים משמעותיים כדי להבטיח כי החלבון נשאר במצב תפקודי לאורך כל הליך הכינון מחדש. בעוד פתרונות של שומנים בממסים אורגניים (למשל, כלורופורם, cyclohexane) הם אידיאליים להפקת סרטי שומנים, חלבונים טרנס-קרום הם בדרך כלל יציבים רק כאשר תחום טרנס-הקרום הידרופובי שלהם מוטבע בbilayer שומנים בדם, או מוקף בmicelle חומרי ניקוי ( לדוגמא, במהלך טיהור חלבונים). לפיכך, החומר המוצא לכינון מחדש הוא בדרך כלל קרומי ילידים, חלבון מטוהר בתמיסת ניקוי, או שלפוחית המכיל חלבון unilamellar קטנה (proteo-רכבי שטח) ו / או שלפוחית רבת-שבשבת (proteo-MLVs) שהוקמו על ידי הסרת חומר ניקוי ב נוכחות של שומנים. רוב השיטות לשלב חלבונים בממברנה אלה לGUVs נחלקות לשלוש קטגוריות.
Insertio הישירn: החלבון חוצה הממברנה התלויה בחומר הניקוי מעורבב עם שומנים בדם בלבד, GUVs מראש יצר, בלשון המעטה חומר ניקוי solubilized, וחומרי הניקוי ולאחר מכן להסיר באמצעות biobeads 21. בעוד פשוט מבחינה מושגית, שיטה זו דורשת שליטה מדויקת של ריכוז חומר הניקוי, כגבוה מדי ריכוז חומר ניקוי יכול לפזר את GUVs בעוד נמוך מדי יכול לגרום לריכוז החלבון להתפתח או מצטבר.
בוס / Proteo-SUV Fusion: חלבון בproteo-רכבי שטח בשילוב עם, שומנים רק GUVs מראש יצר והיתוך הוא הקל עם פפטידים מיוחדים fusogenic 22 או חומר ניקוי 21. בדרך כלל היקף ההיתוך מוגבל מוביל לGUVs עם צפיפות חלבון נמוכה.
התייבשות / Rehydration: סרט המכיל שומני חלבון נוצר על ידי התייבשות חלקית של proteo-SUV (או proteo-MLV) פתרון וGUVs לאחר מכן גדל כמו לסרט שומנים טהור. האתגר הברור הוא להגן על החלבון במהלך dehydrati החלקיבשלב 23, אבל השיטה שמש בהצלחה כדי לשקם חלבונים טרנס-קרום כגון Bacteriorhodopsin, סידן-ATPase, integrin וVDAC לGUVs 7,23 - 25.
מאמר זה מתאר פרוטוקולי התייבשות / התייבשות לעשות GUVs המכיל את ערוץ המתח מגודרת אשלגן, KvAP, מpernix החיידקים הקדום, Aeropyrum היפר-thermophilic. יש KvAP רמה גבוהה של הומולוגיה לערוצי אשלגן תלויים מתח אוקריוטים 26 ומבנה הגבישי ידוע 27 , מה שהופך את מודל טוב ללימוד המנגנון של gating מתח. הייצור של proteo-רכבי השטח שתואר בפירוט בעבר ואינו חלק ממדריך זה 26,28,29. חשוב לציין, proteo-רכבי שטח KvAP לא צריך להיות מיוצרים עבור כל הכנת בוס, כפי שהם יכולים להיות מאוחסנים בaliquots הקטן (למשל, 10 μl) ב -80 מעלות צלזיוס למשך פרקי זמן ארוכים (> 1 שנה). Electroformationאו נפיחות בסיוע ג 'לאחר מכן ניתן להשתמש כדי לגדול GUVs מproteo-רכבי השטח KvAP (או proteo-MLVs).
השלבים העיקריים לפרוטוקול electroformation הם באיור 1. טיפות של תמיסה של רכבי שטח המכילים החלבון מופקדות על חוטי פלטינה (שמוצגים באיור 2). התייבשות חלקית של ההשעיה SUV מובילה להיווצרות של סרט חלבון שומנים באמצעות השילוב של רכבי שטח. במהלך התייבשות, שדה AC מוחל על אלקטרודות לסייע לשכבות השומנים לdelaminate ויוצר GUVs. שדה 10 הרץ עובד היטב בעת שימוש "דל מלח" (<5 מ"מ) חיץ להחזרת נוזלים 28 וGUVs להימשך מספר שעות כדי לגדול. בניגוד לכך, מאגרים פיסיולוגיים (המכילים ~ 100 מ"מ מלח) לעבוד היטב עם מתח נמוך יותר, 500 הרץ שדה AC אך דורש ממושך (~ 12 שעות) נפיחות תקופה של 15. שיטה זו מבוססת על פרוטוקול קודם, באמצעות איטו מחליק 24, אבל משתמשת בהמשך קאמרי מותאם אישיתaining שני חוטי פלטינה כפי שמוצג באיור 2 (ראה דיון לפרטים עיצוב והצעות לפשוטים יותר, מאולתר תאים).
איור 3 ממחיש את שיטת נפיחות בסיוע ג '. הפרוטוקול עובד היטב עם מאגרים עם ריכוזי מלח פיסיולוגיים, הוא מהיר, ומייצר GUVs עם הפצת חלבון הומוגני יותר. עם זאת, התשואה של GUVs המבודד, כנראה פגם-חופשי (כלומר, קרום הבוס הוא אחידה באורך-קשקשים אופטיים ואינו מצרף כל עצמים) הוא נמוך יותר, על אף שהוא מספק מספר מספיק לתיקון מהדק וניסויים מיקרו-מניפולציה . שיטה זו מבוססת על פרוטוקול שימוש בג'ל agarose לייצר GUVs שומנים בדם רק 16 ודורש ציוד ייחודי פחות מאשר שיטת electroformation.
האפיון של GUVs עם מיקרוסקופ פלואורסצנטי מתואר, כמו גם הליכים באמצעות הגדרת תיקון מהדק סטנדרטית ללמדוד את פעילות KvAP ב" מבפנים החוצה "נכרת תיקוני קרום.
GUVs המכיל חלבון גידול יכול להיות קשה יותר מGUVs שומנים בדם בלבד. בפרט, תשואת הבוס הסופית יכולה לסמוך ברגישות על איך בדיוק פתרון SUV מופקד ומיובש כדי ליצור ערימת הקרום. למישהו ללא כל ניסיון קודם עם GUVs, זה עשוי להיות מועיל לראשון לגדול GUVs שומנים בדם רק לאחר פרוטוקול קונבנציונלי 15,16 בי סרט הקרום נוצר על ידי הפקדת שומנים מממס אורגני. ברגע שהפרוטוקול הקונבנציונלי עובד היטב, בתצהיר SUV והתייבשות חלקית אז יכולים להיות שולטים באמצעות רכבי שטח שומנים בדם בלבד, שהם גם מאוד מועילים כאשר התאמת הפרוטוקול להרכב שומנים בדם חדש. כאשר GUVs לגדול באופן מהימן מרכבי שטח שומנים בדם בלבד, אז זה רק צעד קטן להפקת GUVs המכיל חלבון מproteo-רכבי שטח.
Protocol
1. פתרון הכנה
- להכין 5 מיליליטר של "חיץ SUV 'המכיל 5 מ"מ KCl, 1 מ"מ HEPES (pH 7.4) או טריס (pH 7.5), ו -2 trehalose מ"מ. סנן את החיץ עם מסנן מזרק 0.2 מיקרומטר ומתחלק ל1 aliquots מיליליטר אשר ניתן לאחסן ב -20 ° C.
הערה: פרטים נוספים לריאגנטים ומכשירים ניתנים ברשימת החומרים. - הכן 40 מיליליטר של 'צמיחת המאגר' המושל שימלא את הפנים הבוס בהחזרת נוזלי סרט. לצמיחה "נמוך מלח ', לשלב 5 מ"מ KCl, 1 מ"מ HEPES (pH 7.4) או 1 מ"מ טריס (pH 7.5), ו~ 400 מ"מ סוכרוז. לצמיחה "מלח פיסיולוגי", לשלב 100 מ"מ KCl, 5 מ"מ HEPES (pH 7.4) או 5 מ"מ טריס (pH 7.5), ו~ 200 מ"מ סוכרוז.
- הכן 40 מיליליטר של 'תצפית מאגר' לפתרון החיצוני בתא הניסוי על ידי שילוב של 100 מ"מ KCl, 5 מ"מ HEPES (pH 7.4) או 5 מ"מ טריס (pH 7.5), ו~ 200 מ"מ גלוקוז.
הערה: מאגרים אלה הם רק EXAmples. ראה דיון על מנת להתאים את המאגרים לניסויים אחרים. - מדוד את osmolarities של מאגרי הצמיחה והתבוננות עם osmometer. להוסיף גרגירים של סוכרוז או גלוקוז כדי להתאים אותם עד למרחק של 1%, כך שGUVs לא lyse או יקרוס כאשר הועבר מתא הצמיחה לתא התצפית.
הערה: בטווח ריכוז זה, הוספת 1 מ"מ של סוכרוז (13.7 מ"ג לכל 40 מיליליטר) או גלוקוז (7.2 מ"ג לכל 40 מיליליטר) מגביר osmolarity על ידי ~ mOsm 1. - סנן את מאגרי הצמיחה והתבוננות עם מסנן 0.2 מיקרומטר ולאחסן אותם על 4 מעלות צלזיוס לעכב התפתחות חיידקים.
- לפזר 50 מ"ג של בטא-קזאין ב 10 מיליליטר של 20 מ"מ טריס (pH 7.5) כדי ליצור חיץ פתרון 5 מ"ג / מיליליטר beta-קזאין צריך passivate את פני השטח של תאי ניסוי כך שGUVs לא מקל, להפיץ ופרץ. ברגע שבטא-קזאין הוא נמס לגמרי (עד כמה שעות ב 4 ° C), מסנן (0.2 מיקרומטר) אותו ל0.5 מיליליטר aliquots שיכול להיות קפוא הבזק ומאוחסןב -20 ° C לשימוש מאוחר יותר (aliquots מופשר מאוחסן על 4 מעלות צלזיוס בדרך כלל ניתן להשתמש עד שבוע 1).
2. הכנת SUV
- להכין ולהקפיא aliquots של proteo-רכבי שטח בעקבות הפרוטוקול מפורט שפורסם בעבר 28. השתמש KvAP שכותרתו fluorescently עם Alexa-488 maleimide, מחדש לתוך DPhPC רכבי השטח (10 מ"ג / מיליליטר) בחלבון ליחס שומנים של 1:10 (במסה).
הערה: Wild סוג KvAP מכיל ציסטאין אחד למונומר ממוקם בסמוך לתחנה הסופי C-התוך תאי (חומצת אמינו 247). - רכבי שטח פלורסנט, שומנים בדם בלבד:
הערה: ידית כלורופורם מתחת למכסת מנוע קטר כפפות nitrile ומשקפי מגן. הימנע משימוש בכל פלסטיק כלורופורם יכול לפזר אותם. ניתן לאחסן פתרונות כלורופורם בבקבוקוני זכוכית ענבר עם כובעי טפלון והועברו באמצעות מזרקים זכוכית. תשמור על עצמך כדי לשטוף את כל כלי הזכוכית לפחות 5 עד 10 פעמים עם כלורופורם לפני ואחרי pipetting שומנים.- הכן של 100 μl10 רכבי שטח מ"ג / מיליליטר DPhPC המכילים 0.5% mol של השומנים בדם אדום הניאון, טקסס האדומה-DHPE, על ידי ערבוב של פתרון DPhPC 100 μl (10 מ"ג / מיליליטר בכלורופורם) עם 8.2 μl של פתרון טקסס האדומה-DHPE (1 מ"ג / מיליליטר במתנול) בבקבוקון זכוכית 1.5 מיליליטר ענבר.
- ייבש את השומנים למטה תחת זרם של חנקן במנדף כימי תוך סיבוב הבקבוקון. כאשר הסרט נראה יבש, למקם את השומנים תחת ואקום במשך 3 שעות כדי להסיר כל ממס שיורי.
- הוספה של חיץ SUV 100 μl לשומנים, והמערבולת במרץ עד שלא שומנים נשאר תקועה על הקירות של הבקבוקון והפתרון הוא אחיד חלבי.
- Sonicate פתרון שומנים כדי ליצור רכבי שטח. להתאים את מיקום הבקבוקון עד אולטרסאונד גורם לתנועה ביותר וזרימה בתוך הבקבוקון, ולדאוג שלא לחמם את הפתרון שלא לצורך. המשך sonication עד הפתרון הופך שקוף, או במידת האפשר, (2-5 דקות לsonication קצה, ~ 20 דקות לsonication אמבטיה) שקופות.
- Aliquoרכבי שטח t (למשל, 10 או 20 μl μl) (-20 ° C) לשימוש מאוחר יותר והקפאה.
הערה: שומנים, במיוחד שומנים בלתי רוויים, יכול בקלות פירוט. פתרונות שומנים חנות ב 20 ° C (או 80 ° C) תחת ארגון ולהשתמש תוך 6 חודשים. ניתן לאתרם תוצרי פירוק שומנים בכרומטוגרפיה בשכבה דקה.
3. בוס צמיחה על ידי Electroformation
- להכין את חדר electroformation.
- אם התא לא נוקה, להסיר את החלונות, לסלק את כל איטום והשומן, לחלץ את החוטים, ולשטוף ולקרצף את החדר עם רקמות באמצעות מים ואתנול (≥70%) לסירוגין.
- לשפשף את החוטים גם, להטביע את החוטים וקאמריים באצטון, וsonicate במשך 5 דקות. נגב את הכל עם רקמה שוב באמצעות אצטון. שים את התא באתנול וsonicate במשך 5 דקות.
- להרכיב את התא על ידי החדרת החוטים דרך החורים, ולסובב ולנגב את החוטים כדי לוודא שהם arדואר נקי. שים את התא במים מזוקקים, sonicate במשך 5 דקות ולייבש את החדר עם זרם של חנקן או אוויר.
- הכן 30 μl של 3 מ"ג / מיליליטר ההשעיה SUV במאגר SUV. כדי ליצור GUVs המכיל חלבון, לשלב 8 μl של proteo-רכבי שטח (DPhPC 10 מ"ג / מיליליטר KvAP 1:10), 2 μl של רכבי שטח ניאון (10 מ"ג / מיליליטר DPhPC, 0.5 mol% TexasRed-DHPE) ו -20 μl של SUV חיץ בצינור 1.5 מיליליטר microcentrifuge לחלבון סופי לשומני יחס (מסה) של 1: 12.5 ו -0.1% mol TexasRed-DHPE. מערבבים את הפתרון במרץ.
- לחלופין, לתרגל את הפרוטוקול עם השומנים רק רכבי שטח, פשוט לשלב 10 μl של רכבי שטח ניאון (10 מ"ג / מיליליטר DPhPC ו 0.5 mol% TexasRed-DHPE) עם חיץ SUV 20 μl.
- להפקיד את SUV הפתרון.
- השתמש פיפטה 2 μl או מזרק זכוכית 5 μl להפקיד טיפות קטנות (<0.2 μl) של פתרון SUV בחוטים. כ נדרש 1 μl של פתרון כדי ליצור סדרה של טיפות לאורך1 סנטימטר של חוט. ודא הטיפות קטנות מספיק ומרווחים מספיק רחוק זה מזה, שהם לא נוגעים או פתיל.
- בואו רכבי השטח הופקד להתייבש במשך ~ 30 דקות באוויר פתוח. כאשר כל הטיפות התיישבו, לסובב את החוט כל כך פיקדונות השומנים קלים יותר להתבונן במיקרוסקופ.
הערה: אם רכבי השטח לא לייבש מספיק, הם יכולים פשוט לשטוף את החוטים כאשר מאגר הצמיחה נוסף, תוך ייבוש יותר מדי עלול לגרום נזק לחלבון. בגלל לחות באוויר משפיע על השיעור של ייבוש, זמן הייבוש ו / או לחות באוויר יכול להיות מותאם לתוצאות אופטימליות 30. סרט השומנים בחוטים צריך להיות גלוי תחת מיקרוסקופ.
- להרכיב את התא.
- לאטום את תחתית החדר: השתמש במזרק ללמרוח משחה ואקום לחלק התחתון של החדר סביב שלוש הבארות ולחץ coverslip x 22 מ"מ 40 מ"מ בעדינות נגדה לאטום את תחתית התא, כך שהוא שומר ללא פער. חותם את הצדדים של החדר (שבו יציאת חוטים) עםאיטום דבק. למרוח משחה ואקום על גבי התא מתאר שלוש בארות.
- לאט לאט להוסיף למאגר צמיחה עד כל טוב מלא לראש. הימנע מכל תנועה מהירה של הפתרון בבארות כמו זה יכול להתפשט סרט השומנים מהאלקטרודות.
- סגור את התא על ידי לחיצה על כיסוי השקופית העליונה בעדינות על הגריז, נזהר שלא לעקור את coverslip התחתון. השתמש במטלית כדי להסיר כל טיפות של חיץ בקצוות של להחליק את המכסה העליון.
הערה: זהו זמן טוב לבחון את התא מתחת למיקרוסקופ כדי לאשר שסרט השומנים נשאר בחוטים.
- חבר את מחולל אותות לחוטים באמצעות שני קליפים תנין. הגדר את התדירות (גל סינוס 10 Hz / 500 הרץ לחיץ מלח נמוך / גבוה) ולהשתמש במודד למדוד ולהתאים את המתח על פני החוטים 0.7 / 0.35 V שורש ממוצע ריבועים (VRMS) לחיץ מלח הנמוך / גבוה. מכסה את החדר עם רדיד אלומיניום כדי להגן על fluorophores מן האור. השאר tהוא GUVs לגדול במשך 2-3 שעות לחיץ מלח הנמוך, ו -12 שעות או O / N לחיץ מלח הגבוה.
- נתק את התא מגנרטור ולמקם אותו בזהירות על מיקרוסקופ הפוכה להעריך צמיחת בוס. השתמש ב, תנועות איטיות או יציבים זרימת נוזל בבארות עשויים בטרם עת לנתק GUVs מהחוטים.
הערה: GUVs על קצות החוט הוא בדרך כלל גלוי בניגוד שלב (40X אובייקטיבי מרחק עבודה ארוכה), ואילו ניתן לראות GUVs כל מקום במחצית התחתונה של החוטים עם epifluorescence. אם לא GUVs גלוי, נסה לסובב את החוטים להסתכל על פני השטח העליונים. ניתן לאחסן GUVs על 4 מעלות צלזיוס בתא צמיחה במשך כמה ימים.
4. צמיחת בוס על ידי נפיחות סייעו-ג'ל
- הכן 10 מיליליטר של פתרון agarose 1% על ידי ערבוב של agarose 100 מ"ג עם 10 מיליליטר של מים טהורים. מחממים אותו עד לנקודת רתיחה על ידי הצבתו במיקרוגל ב 480 W ל~ 20 שניות. מערבבים לוודא agarose הוא נמס לגמרי.
הערה: הפתרוןיכול להיות מאוחסן על 4 מעלות צלזיוס ומחוממת בעת צורך. - פלזמה נקייה (פלזמה אוויר) כיסוי שקופית 1 דקות, כך שפתרון agarose יתפשט יפה על זה. השתמש בכיסוי-שקופיות בתוך 15 דקות הבאות כאפקט של ניקוי פלזמה פג במהירות.
- החל 200 μl של פתרון agarose החם לכל 22 x 22 מ"מ 2 שקופיות כך הפתרון מרטיב את כל פני השטח. הטה את השקופית אנכית ולגעת בקצה התחתון לרקמות להסרת נוזל עודף ולהשאיר רק שכבה חלקה דקה של agarose בשקופית.
- מניחים את השקף על צלחת חמה או בתנור ב 60 ° C ולהשאיר אותה לייבוש לפחות 30 דקות. סרט agarose הוא בקושי נראה לעין בעין. לאחר השקופיות להתקרר לRT, להשתמש בם באופן מיידי, או לאחסן אותם לעד שבוע בכלי סגור על 4 מעלות צלזיוס.
- מניחים את coverslip מצופה agarose בצלחת פטרי 3.5 סנטימטר סטנדרטית.
- הכן את פתרון SUV כמו בסעיף 3.2 ולהחיל ~ 15 μl של פתרון SUV (3 מ"ג / מיליליטר שומנים בדם) ב~ 30 טיפות קטנות מאוד בעדינות על גבי משטח agarose. הקפד לא לעוות את שכבת agarose יותר מדי.
- מניחים את השקף תחת זרם עדין של חנקן כ 10-15 דקות ובצע את האידוי של החיץ על ידי העין כטיפי ייבוש.
- ברגע שהרכבים השטח התייבשו, להוסיף למאגר צמיחה כדי לכסות את פני השטח השקופיות. לשימוש קטן 3.5 סנטימטרים פטרי צלחת ~ 1 מיליליטר של חיץ.
- לאפשר לנפיחות כדי להמשיך ל~ 30 דקות, ולאחר מכן לבחון את הצמיחה של GUVs בתא באמצעות מיקרוסקופ הפוכה עם שלב בניגוד או ניגודיות דיפרנציאל התערבות (DIC).
הערה: תצפית epifluorescence קשה בשל הרקע החזק של fluorophores בג'ל והאוטומטית הקרינה של agarose.
5. קציר והתבוננות GUVs
- Passivate קאמרי תצפית (למשל, צלחת פטרי קטנה או coverslip זכוכית), כך שGUVs לא מקל, להפיץ ופרצו בתחתית התא. מכסה את צ'אםבער תחתון עם פתרון beta-קזאין, דגירה של 5 דקות, לשטוף את פתרון קזאין עם מים טהורים, יבש עם זרם של אוויר או חנקן, ולבסוף להוסיף למאגר תצפית (למשל, ~ 5 מ"מ עומק לצלחת פטרי קטן).
- לקצור את GUVs. חותך את הקצה של 100 טיפים פיפטה μl כך היא הפתיחה (~ 2 מ"מ קוטר) גדול יותר, ולשאוף לאט כמאמץ הגזירה של pipetting בקלות יכולה להרוס GUVs.
- לGUVs-נוצר אלקטרו, לפתוח את תא הצמיחה בעדינות על ידי הסרת coverslip העליון. הנח את קצה פיפטה ישירות מעל כל חוט ולשאוב ~ 50 μl תוך כדי התנועה את קצה פיפטה לאורך החוט כדי לנתק את GUVs.
הערה: זה עשוי לעזור כדי לסובב את החוט כדי לאסוף GUVs על "הצד השני" של החוט. - לGUVs "נפיחות בסיוע ג '", הקש ראשון בצד של צלחת פטרי כמה פעמים כדי לעזור GUVs להתנתק ממשטח coverslip. מקם את קצה פיפטה בדיוק מעל coverslip ולשאוב 50 μl תוך pulling הקצה אחורי על פני השטח. ישירות להעביר GUVs שנקטפו לחדר תצפית, או בחנות בצינור 1.5 מיליליטר microcentrifuge על 4 מעלות צלזיוס למשך שבוע עד 1.
- לGUVs-נוצר אלקטרו, לפתוח את תא הצמיחה בעדינות על ידי הסרת coverslip העליון. הנח את קצה פיפטה ישירות מעל כל חוט ולשאוב ~ 50 μl תוך כדי התנועה את קצה פיפטה לאורך החוט כדי לנתק את GUVs.
- מניחים את חדר התצפית במיקרוסקופ הפוכה, להוסיף GUVs לתא התצפית, ולחכות כמה דקות לGUVs להתיישב בתחתית התא.
- סקר קאמרי עם ניגוד שלב או DIC כדי לאתר במהירות ("פגם חופשי ')" מועמדי בוס "חלקים, כדוריים. לבחון כל "מועמד בוס" בepifluorescence שלא יכלול יפוזומים קטנים יותר המכילים מקוננים בתוך. לבסוף, ודא שעוצמת הקרינה שומנים היא אחידה ותואמת עם קרום אחד (כלומר, unilamellar).
הערה: בחלק מbilamellar (או רב-שבשבת) שלפוחית, הקרומים קרובים מדי זה לזה להיפתר כל כך שהם מופיעים unilamellar בניגוד שלב או תמונות DIC. עם זאת, ניתן להבחין אובייקטים אלה מunilame בפועלGUVs llar על ידי הקרינה השומנים שלהם, שהוא פי שניים (או יותר) בהיר יותר.
6. GUVs הידוק-תיקון
- הפוך טפטפות תיקון בקוטר טיפ 1-2 מיקרומטר מזכוכית נימי ורוסיליקט סטנדרטית באמצעות התכנית המומלצת לחולץ פיפטה.
הערה: טיפולים מיוחדים כגון ליטוש אש אינם נחוצים, וטפטפות יכולה לשמש במשך כמה ימים אחרי שהם כבר משכו אם הם נשמרים בקופסא סגורה. - Passivate התא על ידי דוגרים עם פתרון beta-קזאין (5 מ"ג / מיליליטר), כדי להבטיח שGUVs אינו דבק, להפיץ וקרע על משטחים קאמריים. לשטוף את קזאין לאחר 5 דקות.
- הכנס את האלקטרודה הקרקע, למלא את התא עם חיץ תצפית, להעביר 10 μl של ההשעיה הבוס כמתואר בשלב 5.2 ו -5.3, ולחכות כמה דקות לGUVs להתיישב בחלק התחתון.
- מלא פיפטה תיקון טרי עם פתרון (חיץ תצפית או פתרון iso-האוסמוטי אחר) ולעלות אותו על headstage מגבר תיקון מהדק.
- חיפוש דרך החדר לאיתור בוס "ללא פגם" כאמור בסעיף 5.4, ולבדוק שהוא מכיל חלבון פלואורסצנטי.
- החל לחץ חיובי קבוע (> 100 אבא, או בערך 1 סנטימטר H 2 O במד לחץ) כדי לשמור על פיפטה תיקון פנים נקיים, והכנס את פיפטה התיקון לתוך התא. להביא את פיפטה התיקון לשדה הראייה, יחול דופקי בדיקה למדידה / לפצות את מתח פיפטה קיזוז והתנגדות, ולבחון את פיפטה תחת תאורת ניאון כדי לאשר שהקצה הוא נקי.
- להביא את פיפטה התיקון כלפי הבוס, ובמידת צורך, בו זמנית להפחית את הלחץ החיובי כל כך את הזרימה החוצה מפיפטה את התיקון לא עושה הבוס "לברוח". כאשר פיפטה את התיקון היא קרובה לבוס, להחיל לחץ שלילי (עד 5 סנטימטרים H 2 O) כדי למשוך את הבוס נגד פיפטה את התיקון. לפקח על ההתנגדות כ"; לשון "של קרום הבוס נכנסה פיפטה את התיקון וצורות gigaseal.
- אם gigaseal לא יוצר, להסיר את פיפטה התיקון מהחדר ולחזור לשלב 6.4. אם תיקון הקרום יצר gigaseal, אבל הבוס נשאר מחובר לפיפטה, תחתוך את התיקון על-ידי התרחקות הבוס, מתפוצצים הבוס אל תחתית החדר, או בקצרה נע פיפטה מתוך פתרון.
- כאשר תיקון הקרום מבפנים החוצה כבר נכרת מן הבוס וgigaseal יציב, לכבות את דופקי הבדיקה וליישם פרוטוקול מתח כמו זה שמוצג באיור 13.
הערה: איור 13 להלן אמנת אלקטרו סטנדרטית לתיקון מבפנים החוצה שבזרם לתיקון-אלקטרודה הוא "חיובי", ו- V = V אמבטיה - פיפטה V. מחזיק את התיקון בפוטנציאל שלילי (לדוגמא, V = -100 mV) ל~ 30 מקומות שניות KvAP במצב המנוחה, ואילו צעדים (100 msec ל 5 שניות) לפוטנציאל חיובי יותר (לדוגמא, V = 100 mV) אז יכול לנהוג בה ל( מדינות) כלומר, פתוחות ניהול פעילה. - לאחר מדידות על תיקון קרום נסיים, לשבור את התיקון עם דופק zap או לחץ ובדוק שמתח היסט של האלקטרודה התיקון לא נסחף. הסר את פיפטה התיקון מהחדר, ולחזור לשלב 6.4.
תוצאות
הצמיחה של GUVs ניתן להעריך במהירות על ידי בחינה קאמרי הצמיחה מתחת למיקרוסקופ. לelectroformation, GUVs נוטה לגדול בצרורות לאורך חוטי הפלטינה, כפי שמוצג באיור 4. במהלך נפיחות בסיוע ג ', GUVs יופיע כמבנים כדוריים שבמהירות לגדול ופתיל יחד (איור 5).
GUVs ללא פגם מזוהה בקלות רבה יותר והעריך לאחר העברה לתא תצפית. יש צורך במדידות כיול להעריך איכות בוס בקפדנות, וכימות שיטתית כבר פורסמה בעבר 28. עם זאת, כמדריך אמפירי, צריך להיות מבודד GUVs "טוב" (כלומר, לא באשכול), יש לי קרום יחיד, חלק, כדורי חיצוני, אינם מכיל אובייקטים (כלומר, צינורות, שלפוחית מקוננת, וכו ') בפנים, ו יש לי הרמה "סטנדרטית" הקרינה שומנים (אובייקטים בהירים הם בדרך כלל דו או רב-שבשבת). איור 6 מציג תמונות דסק"ש וepifluorescence של בוס 'ללא פגם "לאחר העברה לפתרון גלוקוז iso-האוסמוטי. לעומת זאת בדסק"ש נובע מההבדל בצפיפות אופטית בין בוס סוכרוז מלא ופתרון האמבטיה גלוקוז מכיל. לעומת זאת השבירה של KvAP המכיל GUVs לעתים הוא פוחת לאורך זמן, למרות שKvAP עצמו לא צריך להיות חדיר לסוכרוז או גלוקוז. הקרינה החלבון אחידה בקרום הבוס מאשרת כי KvAP מאוגדת בבוס (כלומר, זה לא נשאר בסרט השומנים בדם) ולא יצר מיקרון בקנה מידה (או גדולים יותר) מצרפים.
איורים 7, 8 ו -9 תכנית תמונות confocal של שומנים בדם וחלבון מהקרינה GUVs המיוצר על ידי הפרוטוקול הנמוך-מלח electroformation, פרוטוקול electroformation מלח פיסיולוגי, ופרוטוקול נפיחות בסיוע ג '. השומנים הניאון (מגנטה) וחלבוןאותות (ירוקים) כבר טיפסו לאותה עוצמה ממוצעת, כך שיש לי GUVs עם מספר גבוה נמוך / חלבונים ליחידת שטח (צפיפות חלבון) מגנטה / צל ירוק בתמונות הכיסוי (עמודה ימנית), תוך GUVs עם צפיפות ממוצעת היא חלבון לבן. GUVs המבודד, ללא פגם זוהו והתפלגות גודל הבוס מוצגת באיור 10. בדרך כלל electroformation מייצר יותר GUVs ללא פגם מאשר נפיחות בסיוע ג ', אבל GUVs המיוצר על ידי electroformation קטן. איור 11 מציגה את התפלגות צפיפות חלבון מוסק מהקרינה של GUVs. Electroformation עם חיץ גבוה מלח מייצר GUVs שבו צפיפות החלבון משתנה מאוד מבוס לבוס. צפיפות החלבון של GUVs הפרט משתנה הרבה פחות לelectroformation עם חיץ מלח נמוך, בעוד שצפיפות החלבון של GUVs המיוצר על ידי נפיחות בסיוע ג 'להפליא אחידה.
טכניקת תיקון מהדק היא נרחב שימוששיטת ד ללימוד הפונקציה של תעלות יונים מתח מגודרת, כגון KvAP. בהקלטות "מבפנים החוצה", פיפטה נקייה זכוכית "תיקון" משמשת לבלו תיקון של קרום מבוס. האלקטרודה בתוך פיפטה את התיקון לאחר מכן נעשה שימוש כדי להחיל מתח, ולמדוד את התוצאה נוכחית זורם דרך תיקון הקרום. ההרכב של תיקון הקרום יכול להיות שונה מאוד משאר התא / הבוס 31, אבל התצורה "מבפנים החוצה" היא עדיין שימושית מאוד למדידת המוליכות היחידה הערוץ, הסלקטיביות יונית, וgating מתח תלוי. שלושת מאפיינים אלה הם דרך מצוינת כדי לקבוע, כי זרמים אינם בשל חפצים (למשל, בעיות gigaseal) או מזהמים (למשל, porins חיידקים מהטיהור), ויש ערוצי KvAP פונקציונליים בGUVs.
מוליכות ערוץ נמדדה ביותר בקלות בתיקונים רק עם אחד או שני ערוצים פעילים. בEXAmple מוצג באיור 12, לא פתחי ערוץ הם נצפו כאשר הקרום מוחזק ב -100 mV, ואילו ב+100 mV, פתחי ערוץ בודדים יכולים להיות ברורים נפתרו. ההיסטוגרמה הנוכחית מראה שתי פסגות המתאימות הסגור והמדינות פתוחות, ומתאימה אותם עם תפקיד כפול Gaussian תשואות נוכחי ערוץ יחיד של 10.9 ± 0.85 הרשות הפלסטינית, המקביל למוליכות של 109.2 ± 8.5 PS (ב100 מ"מ KCl). שים לב שמוליכות ערוץ אחד תלויה בפתרון (במיוחד ריכוז אשלגן) והרכב קרום 32,33.
כמו רבים K-ערוצים אחרים, תערוכת ערוצי KvAP בודדת "נוקשות" פרצי פתיחות וסגירות מהירות. כפי שהודגם בעבר, הסלקטיביות אשלגן יכולה להיבדק על ידי שימוש בפתרון שונה בפיפטה את התיקון (לדוגמא, פתרון פיפטה את התיקון 90 מ"מ NaCl, 10 מ"מ KCl) 28.
gating מתח תלוי לעתים קרובות זהtudied בתיקונים במספר רב של ערוצים, כדי להשיג ממוצע הרכב בקלות רבה יותר. אמנם אין מנגנון ברור לטובה (תחום תאיים על בוס פנים) הפיזיולוגי והפוך (תחום התוך תאי על הצד החיצוני הבוס) החדרת KvAP בGUVs, בתיקוני קרום "מבפנים החוצה" רוב הערוצים פונקציונליים יש לי " הכנסה פיזיולוגית "28. איור 13 מציגה את התגובה של תיקון קרום המכיל מרובה (> 10) ערוצים לשורה של צעדי depolarizing 5 שניות. בין כל שלב, התיקון שנערך ב -100 mV למשך 30 שניות כדי לאפשר ערוצים עם ההכנסה "הפיזיולוגית" כדי לחזור למצב המנוחה שלהם. כאשר הפוטנציאל הוא מספיק שלילי (לדוגמא, V <-60 mV) רוב הנוכחי נובע מדליפת gigaseal, והפתחים המזדמנים של אחד או שני ערוצים שעשויים להיות להם ההכנסה "ההפוכה". לצעדים לpote החיובי יותרntials, מספר גדל והולך של ערוצים שנצפה עד יש כל כך הרבה שכבר לא ניתן לפתור פתיחות וסגירות בודדות. לפיכך, ההסתברות הפתוחה של הערוץ היא בבירור מתח תלוי. קינטיקה של הפעלת KvAP ואיון שונה במידה ניכרת בין ממברנות שחורות שומנים (BLMs) 26 וGUVs, אבל זה עולה בקנה אחד עם דיווחים קודמים שgating הערוץ Kv יכול להיות רגיש להרכב הקרום והמדינה 34.

איור 1. הבוס Electroformation סכמטי:. טיפות המכילות רכבי שטח מופקדות על האלקטרודה התייבשות חלקית של הפתרון גורם לרכבי השטח לפתיל כדי ליצור ערימה של ממברנות. המאגר לאחר מכן הוסיף ושדה חשמלי AC מיושם. כמתנפח סרט, קרומים בודדים להתנתק מהערימה כדי ליצור GUVs. (נתון זה כבר mod ified מAimon et al. 28)

איור 2. בוס Electroformation קאמרי. קאמרי מחורץ מתוך PTFE-בלוק עם שלוש בארות (בקוטר 10 מ"מ, עומק 5 מ"מ). שני 0.5 מ"מ חוטי פלטינה קוטר מופרדים על ידי 3 מ"מ (מרחק מקצה לקצה) וממוקמים קרוב לחלק התחתון של החדר כדי להקל על הדמיה של החוטים. התלושים לכסות תחתון ועליונים מתקיימים במקום עם גריז ואקום, ודבק איטום מונע כל הדלפות מחורי החוט בצד. גנרטור AC מחובר עם קליפים תנין לחוטים. התא מבוסס על אחד שפותח על ידי ארנסטו Ambroggio ולואיס Bagatolli. (נתון זה שונה מאל Aimon et. 28)
"/>
איור 3. ג'ל סייע ספונטני נפיחות סכמטי: טיפות המכילות השעיה SUV מופקדות על ג'ל agarose כטיפה מייבשת, רכבי שטח הפתיל כדי ליצור סרט שומנים.. כאשר מאגר הצמיחה נוסף, הסרט והמסלקים וGUVs יוצר על פני השטח. GUVs לגדול לגודל של ~ 10 מיקרומטר על ידי נפיחות ופיוזינג עם GUVs השכן.

איור 4. תמונת נציג GUVs DPhPC מכיל KvAP גובר על חוט הפלטינה בחיץ מלח גבוה. GUVs דומה אשכולות ענבים לאורך החוט. תמונה בניגוד שלב באמצעות מטרת 40X LWD. אנא לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.

5. GUVs איור DPhPC מכיל KvAP נפיחות בagarose ג'ל. GUVs נראה כמו כדורים קלושים בקוטר של ~ 10 מיקרומטר. הכתמים הכהים / הבהירים הם אגרגטים agarose / שומנים בדם שממנה שלפוחית להתנפח. תמונה בניגוד שלב עם מטרת 40X LWD. אנא לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.

איור 6. תמונות של בוס ללא פגם. (ביצה-PC: הביצה-PA 9: 1 על ידי מסה) מכילות KvAP שכותרתו עם Alexa-488 שמאל: דסק"ש, מימין: Alexa-488 epifluorescence. עירור: 470/50 ננומטר, פליטה: 545/75 ננומטר. שים לב לקרינה אחידה מKvAP ללא אגרגטים גלויים. "Target =" 81fig6large.jpg _ blank "> לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.

איור 7. תמונות Confocal של שומנים בדם (מגנטה) וחלבון (ירוק) הקרינה מGUVs electroformed גדל בחיץ מלח נמוך חצים לבנים סימן (א) (סביר להניח) (ביצה-PC: 1 על ידי המונים: ביצה-PA 9). GUVs, תוך החץ האדום מסמן שלפוחית פוטנציאל דו-שבשבת עם הקרינה שומנים גבוהה יותר. שים לב כי עוצמת הקרינה היא בהירה במרכז התמונה בגלל השדה הגדול מאוד של נוף. (ב) זום מראה קבוצה קטנה של GUVs. שמאל (מגנטה): עירור TexasRed-DHPE: קו לייזר 543 ננומטר, פליטה: 605/70 ננומטר. מרכז (ירוק): KvAP שכותרתו עם עירור Alexa-488: קו לייזר 488 ננומטר, פליטה: 515/30 ננומטר. מימין: כיסוי.OAD / 52,281 52281fig7large.jpg "target =" / _ blank "> לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.
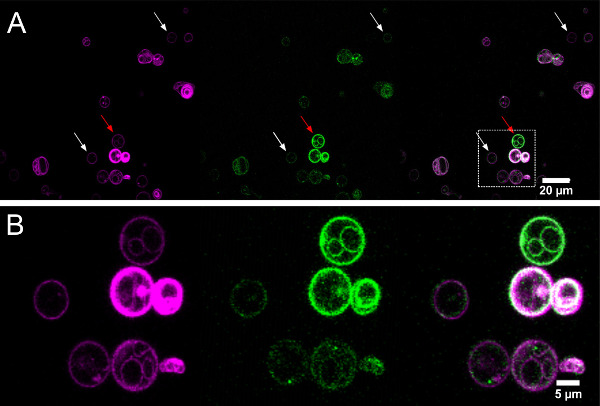
איור 8. תמונות Confocal של שומנים בדם (מגנטה) וחלבון (ירוק) הקרינה מGUVs electroformed גדל בריכוז מלח פיסיולוגי (ביצה-PC: ביצה-PA 9: 1 על ידי מסה). () GUVs (חצים לבנים להראות סביר unilamellar דוגמאות) הן בהשוואה יותר דלילות לפרוטוקול מלח הנמוך ויכולות להיות ריכוזים שונים מאוד חלבון (חץ אדום). (ב) זום מראה קבוצה קטנה של GUVs. שמאל (מגנטה): עירור TexasRed-DHPE: קו לייזר 543 ננומטר, פליטה: 605/70 ננומטר אמצע (ירוק): KvAP שכותרתו עם Alexa-488 עירור: קו לייזר 488 ננומטר, פליטה: 515/30 ננומטר. מימין:. Overlay אנא גללקק כאן כדי לצפות בגרסה גדולה יותר של דמות זו.

GUVs איור 9. תמונת Confocal של שומנים בדם (מגנטה) וקרינת חלבון (ירוק) של GUVs (DPhPC) שהוקם על ידי בסיוע ג 'נפיחות עם חיץ ריכוז מלח פיסיולוגי. להראות צפיפות חלבון הומוגני יותר מ GUVs electroformed מוכן עם חיץ פיסיולוגי. עזבתי (מגנטה): 0.1% BPTR-CER עירור: קו 543 nm לייזר, פליטה: 605/70 ננומטר. התיכון (ירוק): KvAP שכותרתו עם עירור Alexa-488: קו לייזר 488 ננומטר, פליטה: 515/30 ננומטר. מימין:. מיזוג של שני ערוצים אנא לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.
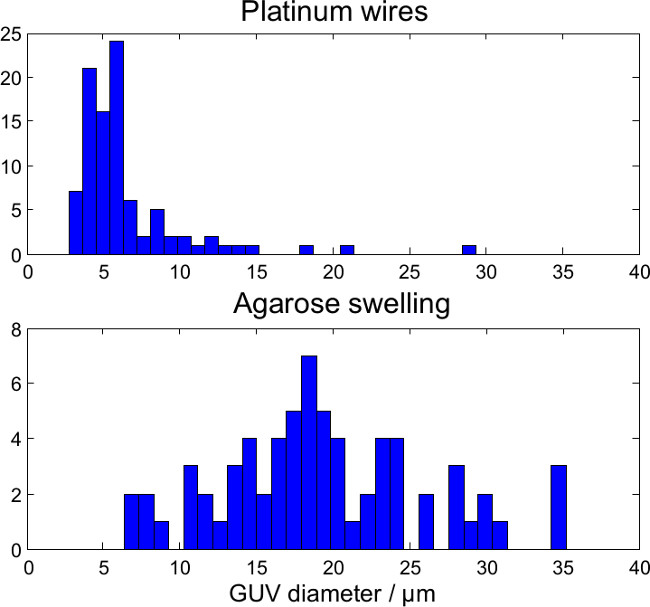
איור 10. הפצת גודל של proteo-GUVs ללא פגם (DPhPC) גדל בelectroformation במאגר מלח נמוך (למעלה, N = 94) או בסיוע ג 'נפיחות agarose (למטה, N = 68).

איור היסטוגרמות צפיפות חלבון 11. בוס: צפיפות החלבון (מספר החלבונים ליחידת שטח) של electroformed GUVs עם חיץ נמוך מלח (5 מ"מ KCl, DPhPC) משתנה פחות מאשר עם ריכוז מלח פיסיולוגי (100 מ"מ KCl, ביצה-PC: ביצה 9 -PA:. 1 על ידי מסה) צפיפות החלבון של GUVs (DPhPC) גדלה בסיוע ג 'נפיחות במאגר מלח פיסיולוגי מציגה את הווריאציה לפחות. צפיפות חלבון היא פרופורציונלית לעוצמת הקרינה KvAP-A488 לריכוזים אלה 28, ובכל היסטוגרמה עוצמות הקרינה מנורמלות על ידי הממוצע של ההתפלגות. (הפנל באמצע שונתהמAimon et al. 28)

12. פעילות ערוץ יחידה דמותו של בוס ממברנה תיקונים (אמנת מתח DPhPC 'מבפנים החוצה "). הבוס היה גדל ב100 מ"מ KCl, 5 מ"מ HEPES pH 7.4 בחוטי פלטינה. ערוצים יחידים פתוחים לאחר החלת 100 פוטנציאל mV על התיקון. בצד הימין של הבלעה היא היסטוגרמה המשמשת לחישוב מוליכות ערוץ אחד. הקו האדום הוא פונקצית גאוס כפולה עם מקסימום כושר ב4.70 ± 0.27 הרשות הפלסטינית ו15.62 ± 0.58 הרשות הפלסטינית, המקביל למוליכות של 109.2 ± 8.5 PS. העקבות היו מסוננת בשעה 10 kHz עם מסנן בסל 4 מוט ונרשמו ב -50 kHz.

איור-dependen מתח 13. ערוצי gating t בתיקון הממברנה מבוס נוצר על agarose בחיץ מלח גבוה (DPhPC, כנס מתח "מבפנים החוצה"). () תגובה הנוכחית קרום תיקון לצעד חולף במתח. פתרונות פיפטה ואמבטית שני הכילו 100 מ"מ KCl, והקרום נערך במשך 30 שניות ב -100 mV בין צעדי מתח רצופים. בבדיקה קרובה ניתן לראות כי העקבות מכילה ערוצים 1 או 2 שנראים לפתוח עם מתחים שליליים. הבלעה) מראה זום של הפתיחה מתעכבת והבלעה ב) הסגירה המאוחרת של הערוץ. זרמים סוננו במסנן בסל 4 מוט ב -10 kHz והקליטו על 51.3 kHz. הסמל האישי העקבות היו שנדגמו עד 513 הרץ. חולף הקיבול השלילי מנותק ב-150 הרשות הפלסטינית. נוכחי ממוצע (ב) (0.25 שניות t <5 שניות <) לעומת מתח צעד. זרמים במתח חיובי הם גדולים יותר, כי ההסתברות הפתוחה הערוץ היא מתח תלוי.Iles / ftp_upload / 52,281 52281fig13large.jpg "target =" / _ blank "> לחץ כאן כדי לצפות בגרסה גדולה יותר של דמות זו.
Discussion
מערכות מודל Biomimetic הן כלי חשוב ללימוד התכונות והאינטראקציות של חלבונים וקרומים. בהשוואה למערכות אחרות כמו מחדש BLMs או ממברנות שומנים בדם נתמכים, בוס מערכות מספר הזדמנויות הנוכחיות כוללים שליטה ניכרת של הרכב קרום, מתח וגיאומטריה, כמו גם להיות באמת ללא שמן בסיס. עם זאת, בשילוב חלבונים הטרנסממברני, כגון KvAP, לGUVs דורש התאמות משמעותיות של פרוטוקולים קונבנציונליים לGUVs שומנים בדם בלבד. פרוטוקול electroformation מוצג כאן התאפיין בעבר ומשמש ללימוד עקרונות biophysical של הפצת חלבון קרום ודינמיקה בקרומים מעוקלים 2,4,35. עבודה זו מדגימה פרוטוקול נפיחות בסיוע ג 'חדש, הוספה לקבוצה של שיטות לכינון מחדש של חלבונים בGUVs. שני פרוטוקולים יכולים לייצר GUVs ללא פגם המכיל צפיפות גבוהה של KvAP, ומדידות על תיקונים מבפנים החוצה לוודא שGUVs se להכיל, ערוצי מתח תלוי אשלגן סלקטיבי פונקציונליים.
יש שתי הגישות נקודות חוזק וחולשה שונות. כאשר ניתן להשתמש בתנאי מלח נמוכים, electroformation מציע פשרה טובה בין תשואת בוס וצפיפות חלבון אחידה. Electroformation עדיין נותן תשואות סבירות עם ריכוזי מלח פיסיולוגיים, אבל צפיפות החלבון יכולה להשתנות במידה רבה בין GUVs (ראה איורים 8 ו -11). וריאציות הצפיפות נראים צמודות לתקופה electroformation, כצמיחת חיץ דל מלח יכולה גם להיות וריאציות צפיפות משמעותיות אם הצמיחה ממשיכה הרבה יותר מ 2 שעות. בניגוד לכך, יש לי GUVs המיוצר על ידי נפיחות בסיוע ג 'חלבון צפיפות אחידה להפליא, אפילו עבור מאגרים פיסיולוגיים. עם זאת, חלק קטן של שלפוחית רבת-שבשבת גדול, והקרינה אוטומטית agarose מסבכת כימות של חלבון נמוך צפיפויות 16. שימוש באלכוהול פוליוויניל בPLAce של agarose דווח לשפר את תשואת הבוס בסיוע ג 'כאשר שומנים הופקדו מכלורופורם 20, אבל לא הצליחו לייצר GUVs באמצעות אלכוהול פוליוויניל עם פתרונות SUV. אם תשואה נמוכה יותר של GUVs ללא פגם מקובלת, יש נפיחות בסיוע ג 'יתרון ברור לניסויים הדורשים חלוקת חלבון אחידה.
Electroformation ונפיחות בסיוע ג 'יש גם דרישות ציוד שונות לגמרי. פרוטוקול הנפיחות בסיוע ג 'משתמש בציוד מיוחד קטן, פרט לשואב הפלזמה, שאינו חיוני כמו שיש הרבה שיטות חלופיות לייצור זכוכית נקייה, הידרופילי. בניגוד לכך, electroformation דורש קאמרי מותאם אישית עם אלקטרודות חוט. חוט פלטינה הוא יקר, אבל לפרוטוקול זה GUVs גדל יותר בקלות עם פלטינה מאשר חוטי טיטניום, וGUVs לא גדל על איטו מחליק בעת שימוש בריכוזי מלח פיסיולוגיים. הקוטר של אלקטרודות (0.5 מ"מ) הוא compromise בין פני האלקטרודה ומחיר. התא שמוצג באיור 2 מבוסס על עיצוב על ידי לואיס 15 Bagatolli וארנסטו Ambroggio, והיה במכונה מpolytetrafluoroethylene (PTFE) כדי לאפשר ניקוי עם רוב הממסים. עם זאת, כלוריד Polyacetal או פוליוויניל (PVC) צריך גם לעבוד היטב. היכולת להסיר את חוטי פלטינה לניקוי אגרסיווי היא חשובה, וכאשר לומדים את הפרוטוקול ראשון, כדאי להיות מסוגל להתבונן צמיחת בוס באתר דרך כיסוי השקופיות התחתונה מאוד. קטן יותר, נסגר בארות למנוע פתרון מהשכשוך קדימה ואחורה וגם לאפשר בדיקות של כמה קומפוזיציות שומנים במקביל. עם זאת, תא מותאם אישית מיוחד אינו הכרחי כאשר החלו לצאת. לדוגמא, ניתן מאולתרים תאים פשוטים, חד-היטב על ידי tacking שני חוטים עד לתחתית של צלחת פטרי קטנה, או באמצעות שעווה לכריכם בין שתי שקופיות זכוכית, או פשוט תוקע אותם דרך הכובע של בקבוקון קטן.
שני electroformation ופרוטוקולי נפיחות בסיוע ג 'צריך לייצר כמות מספקת של GUVs ללא פגם למייקרו-מניפולציה וניסויים תיקון מהדק. עם זאת, תשואת הבוס תלויה ברגישות על הקמת ערימת bilayer כאשר פתרון SUV הוא מיובש באופן חלקי. אם קשיים הם נתקלו בGUVs גדל (כלומר, לא או כמה GUVs גלוי בתא הצמיחה), זה יכול להיות מועיל מאוד לגדול GUVs שומנים בדם רק באמצעות פתרון שומנים / כלורופורם במקום של רכבי השטח 15,16 (ונמוך חיץ מלח). אם GUVs לא גדל גם מסרט שומנים / כלורופורם אז משהו בסיסי הוא (לדוגמא, פתרונות שגויים שומנים או מאגרים, שומן או לכלוך על אלקטרודות, מתח לא נכון או תדירות, וכו ') לא נכון. עם זאת, אם GUVs לגדול מסרטי שומנים / כלורופורם אבל לא סרטי SUV, אז הבעיה היא ככל הנראה עם ההתייבשות החלקית.
צעד ההתייבשות החלקית הואהדרך הקלה ביותר לשימוש מותאם שומנים רק רכבי שטח, כי אין סיכון של שומנים "denaturing" על ידי התייבשות מוגזמת. לelectroformation, זה יכול להיות מועיל לבחון את החוטים אחרי טיפות SUV כבר להתייבש כדי לבדוק שיש הקרינה שומנים בהירה בכל מקום שבו טיפה הופקדה. אם הקרינה השומנים נעלמה לאחר התא מלא בפתרון צמיחה, אז גם פתרון הצמיחה יש להוסיף בזהירות רבה יותר, או רכבי השטח צריך ליבש למשך זמן ארוך יותר כך הסרט מייחס בתקיפות רבה יותר לחוט. במהלך הצמיחה, לעשות לא חוטים ולא פתרון מהלך בטוח בתוך החדר (לדוגמא, כאשר לשים את התא במיקרוסקופ), כדי למנוע הפשטת GUVs את החוטים. כאשר GUVs לגדול היטב, הם בדרך כלל קל לראות בתמונות בניגוד שלב. עם זאת, GUVs הקטן יותר לעתים קרובות יותר ברור באמצעות הקרינה שומנים בדם, שהוא גם מועיל עבור לראות כיצד ערימת הקרום השתנתה במהלך הצמיחה. בדוק את כל פני השטח שלהחוטים (בתוך, מחוץ, עליון ותחתון) בכל הבארות, כמו גם את רצפת התא לפני השלכת הצמיחה, משום שתשואות יכולות להשתנות במידה ניכרת ממקום אחד למשנהו.
הטיפול והאחסון של GUVs השוואה פשוט לתאים, אך GUVs די רגיש ללחץ האוסמוטי, כוחות הגזירה והדבקה. תנועות חלקות, עדינות הן חשובות בעת קציר או העברת GUVs, וזה חשוב לpassivate משטחים כדי למנוע GUVs מדבקות ומתפוצץ. עם זאת, לניסויי מהדק תיקון התא יש לשטוף ביסודיות לאחר פסיבציה, כך שפתרון פסיבציה לא יכול לצפות את טפטפות והתיקון למנוע היווצרות gigaseal. לפסיבציה, טיפול beta-קזאין הוא פשוט ויעיל, ובהשוואה לאלבומין בסרום שור, שבו יש פונקצית תחבורת שומנים, beta-קזאין יש אינטראקציות מוגבלות יותר עם bilayers שומנים ויש להעדיף בעת עבודה עם GUVs 36. על ידי שינוי זמן הדגירה, זהGUVs כדי לקבל אפשרי לדבוק ללא מתפוצץ. עם זאת, GUVs לא ידבק לשקופית הכיסוי באותה עצמה שהתאים, וכך אכפת לי עדיין חייב להילקח במהלך כל הליך שיכולים לגרום לזרימה בתא (לדוגמא, זלוף חיץ, נע הקאמרית).
הקלטת תיקון מהדק היא שיטה קלסית ללימוד תעלות יונים מתח מגודרת כמו KvAP ופרוטוקול זה נגזר מטכניקות מקובלות לקבלת תיקונים "מבפנים החוצה" מהתאים חסיד. הגדרת תיקון מהדק סטנדרטית שבי פיפטה את התיקון יורדת באלכסון (למשל, 30-60 מעלות מאופקיות) לתוך צלחת פטרי קטנה צריכה לעבוד היטב. עם זאת, ניתן לקבל תמונות ברורות יותר של פיפטה את התיקון ואזור gigaseal באמצעות תא שבו כיסוי התלושים מהווים את החלק העליון ותחתון קאמריים (~ הפרדת 1 מ"מ), כך פיפטה את התיקון יכול להיכנס בצורה אופקית מהצד. בגלל לחצי פיפטה תיקון גדול אינם נחוצים, הלחץ יכול להיות במקום נוח גontrolled עם מזרק ומעקב עם כל מטר פשוט לחץ (למשל, מד לחץ מים מאולתר). זה יכול להיות מועיל לניסויי מהדק התיקון הראשונים תרגול עם GUVs שומנים בדם רק גדל באמצעות שומנים בדם / פתרון כלורופורם וחיץ דל מלח. בגלל התשואה של GUVs ללא פגם היא גבוהה מאוד, יהיה שפע של GUVs המושלם לעבוד עם גם אם רבים נהרסו במהלך הקציר וההעברה לתא הניסוי.
עם קצת תרגול, ניתן בקלות השיגו תיקוני קרום נכרת עם gigaseals היציב מDPhPC GUVs וKvAP-DPhPC GUVs. כדי להשיג שיעור הצלחה גבוה, זה עוזר כדי לבחור בזהירות סיבוב, אבל מעט-תנודות, GUVs ללא פגם ולבדוק שפיפטה את התיקון היא נקייה (מחפשים שומנים בקרינה) לפני שתנסה ליצור gigaseal. כאשר "לשון" קרום נכנסה פיפטה את התיקון, gigaseal בדרך כלל יוצר במהירות (<1 שניות) ללא כל צורך בשאיבה חזקה או ספציפיתמתח החזקת ג. בעוד חותם רע עשוי לשפר את הקרום זוחל יותר לתוך פיפטה את התיקון, לעתים קרובות את החותם נשאר עני בגלל הפנים פיפטה היה מזוהמים ויש צורך להתחיל מחדש עם טפטפת תיקון טרי ובוס. צורות DPhPC יציבה מאוד טלאי קרום (עשרות דקות) עם התנגדות חותם מצוינת גם במתח גבוה (למשל, ± 150 mV). SOPC: כולסטרול (3: 1 על ידי חפרפרת) יכול גם ליצור כתמים יציבים מאוד אבל יכול לדרוש יניקה גבוהה כדי לאטום, ואילו נראים כתמי הביצה-PC לשבור בקלות רבה יותר.
למפגשי תיקון מהדק יותר ייתכן שיהיה צורך להתאים את osmolarity של הפתרון קאמרי. אם osmolarity היא יותר מדי נמוכה ממאגר צמיחת בוס, GUVs להיות נפוח, מתוח וכדורי וזה לא יכול להיות אפשרי כדי לשאוב את קרום הבוס רחוק מספיק לתוך פיפטה התיקון ליצירת gigaseal. זה לעתים קרובות ניתן לתקן על ידי פשוט מחכה 10 או 20 דקות כאידוי מהתא מגביר את שלוחהosmolarity פתרון ernal עד GUVs להוציא את האוויר ומתחיל להשתנות. לעומת זאת, אם התא נותר פתוח במשך זמן רב מדי osmolarity של הפתרון החיצוני יכולה להגדיל עד GUVs להוציא את האוויר, tubulate והניצן. זה יכול להימנע על ידי חסימת אידוי מהתא (לדוגמא, עם שמן מינרלים) או מעת לעת הוספת מים מזוקקים כדי להחליף את המים שהתאדה.
בגלל ניתן לשלול חלבונים מתיקוני קרום נכרת 31, מספר הערוצים פעילים בתיקון נכרת לא פשוט קשור לצפיפות של חלבון בקרום הבוס. מדידות הקרינה מציעות הריכוז של KvAP בקרום התיקון הוא נמוך בהרבה מהבוס 28 וזה יכול להיות די קל להשיג תיקונים המכילים רק מספר קטן של ערוצים. עם זאת, אם תיקונים לכלול ערוצים רבים מדי להקלטת ערוץ אחד, צעדים ברורים של שימוש בטפטפות תיקון עם טיפים קטנים יותר ו / או הפחתת ד חלבון-לשומנים בדםensity בתמהיל SUV הם יעילים. בניגוד לכך, לביצוע מדידות הרכב על תיקונים המכילים ערוצים רבים, זה יכול להיות מועיל להתחיל עם צפיפות גבוהה יחסית של חלבון (לדוגמא, 1:10, חלבון לשומן לפי משקל), להשתמש בקרינת חלבון כדי לבחור GUVs עם צפיפות גבוהה של חלבון , להשתמש בטפטפות תיקון גדולה יותר (לדוגמא, 2 עד 3 מיקרון קוטר קצה) ולשאוב במהירות כדי לנסות ליצור את החותם במהירות. ברור, תצורת "כל התא" הסוג '(כלומר,' כל-הבוס ') תהיה אידיאלית כדי לאפיין את כל הערוצים בבוס, אך למרבה הצער "כל הבוס-" התצורה מציבה כמה בעיות טכניות 37.
הפתרונות, השומנים וריכוזי חלבון בהדרכה זה רק סיפקו כנקודת התחלה, וניתן לשנות כדי להתאים לצרכימים של ניסוי מסוים ביצוע מספר שיקולים.
כל הפתרונות צריכים לכלול חיץ pH כגון HEPESאו טריס כדי להבטיח חלבונים אינם חשופים לקיצוניות של pH. מאגר SUV צריך כנמוך ריכוז של מומסים כחלבון יסבול (לדוגמא, מלח 5 מ"מ או נמוך יותר), כריכוזיים מומס להגדיל במהלך שלב ההתייבשות החלקי וריכוזי מלח גבוהים יכולים לפגל חלבון או לגרום לסרט שומנים למהירות delaminate במהלך שלב החזרת הנוזלים. כמויות קטנות של סוכרים כגון trehalose (למשל, 1 מ"מ עד 5 מ"מ) הם חשבו על מנת להגן על החלבון במהלך התייבשות 23. בעוד trehalose היה מעורב בanhydrobiosis והוא האמין כדי להגן על קרום וחלבונים נגד dessication 38, סוכרוז או גלוקוז יכול לעבוד באותה מידה.
לחיץ הצמיחה, ריכוז מלח חשוב במיוחד כמו זה ישפיע על הפרמטרים לצמיחה אופטימלית בוס (למשל, מתח electroformation, תדירות ומשך זמן). בניגוד לכך, האילוץ העיקרי לחיץ התצפית הוא tכובע זה היה צריך להיות באותו osmolarity כחיץ הצמיחה. ההכללה של סוכרוז ו / או גלוקוז ב" חיץ הצמיחה "ו-" חיץ תצפית "יכולה להיות מועילה כדי להבטיח משקעי GUVs לחלק התחתון של חדר התצפית, בעוד הבדל במקדם שבירה בין בוס פנים וחוץ עוזר עם ניגודיות או שלב מיקרוסקופיה DIC. Electrophysiologists כולל לעתים קרובות יוני סידן או מגנזיום לפתרונות אמבטיה ו / או פיפטה תיקון כדי לשפר את היווצרות gigaseal עם קרום תא, אך אינם מופיעים אלה להיות חיוניים לGUVs. ואכן, יונים דו ערכיים, כגון מגנזיום וסידן יכולים לגרום להפרדת שלב שומנים ולהקל על הדבקה, כך שאם הבעיות האלה מתעוררות זה עשוי להיות מועיל להוסיף 1 mM EDTA.
ברור, משיכה העיקרית של מערכות מחדש בהשוואה לתאים היא היכולת לשלוט בהרכב שומנים בדם. DPhPC GUVs לגדול היטב ויוצר טלאי קרום נכרת יציבים, וגם הפרוטוקולים הללו עבדו EFfectively לתערובות המכילות שומנים phosphatidylcholine (PC), phosphatidylethanolamine (PE), phosphatidylglycerol (PG), חומצת phosphatidic, phosphatidylserine (PS) (PA) וכולסטרול. עם זאת, צמיחת הבוס היא רגישה לשני הרכב השומנים ואוגרת 15, וכן פרמטרים פרוטוקול (לדוגמא, כמות השומנים שהופקדו, מתח electroformation / תדר) ייתכן שיצטרכו להיות מותאמים לתערובות שומנים המכילות ריכוזים גבוהים של PE, הואשם שומנים (PG, הרשות הפלסטינית, PS), או כולסטרול. כאשר מתחיל, הביצה-PC, dOPC או DPhPC הוא בחירה ראשונה טובה, וזה גם מאוד מועיל לכלול שומנים ניאון להתבונן צמיחת בוס ולהבחין GUVs משלפוחית multilamellar עם שתיים או יותר bilayers. ניתן להכין תערובות שומנים על ידי שילוב של מתלי רכב שטח של פתרונות מניות, כשומנים לערבב במהלך שלב ההתייבשות החלקי (בתנאי הטמפרטורה גבוהה מכל טמפרטורת מעבר שלב בודדת). שימוש בריכוז גבוה יותר SUV (למשל,10 מ"ג / מיליליטר) פתרונות מניות מאפשר גמישות רבה, ואז יכולים להיות מדולל אלה עד 3 מ"ג / מיליליטר לפני התייבשות ההשעיה.
אם מנסה להתאים פרוטוקולים אלה לחלבונים טרנס-קרום אחרים, זה מאוד חשוב להיות מסוגל לצפות באופן ישיר ההתאגדות של חלבון לתוך פונקצית GUVs וחלבון מבחן. אמנם לא בעיה עם KvAP, תמיד יש את האפשרות כי במהלך התייבשות צעד חלבון טרנס-הקרום יישאר בערימת הקרום המובילה להיווצרות של GUVs שומנים בדם בלבד. תיוג ניאון של החלבון הוא מאוד נוח כפי שהוא מספק דרך מהירה וחד-משמעית להתבונן התאגדות חלבון לתוך GUVs וגם לבדוק לצבירה בתוך GUVs. זה גם מאוד חשוב לבדוק את תפקוד חלבון בGUVs כדי לוודא שהחלבון לא נפגע במהלך תהליך הכינון מחדש. לתעלות יונים כמו KvAP, מדידות תיקון מהדק יכולות להקים הנוכחות של ערוצים פונקציונליים בGUVs. עם זאת, ליגנד fluorescently שכותרתו, זיקה גבוהה (למשל, רעל, מצע או אנטי-גוף) יהיה גם מועיל מאוד לבדיקת מצבם של החלבונים בGUVs.
לסיכום, מאמר זה מדגים כיצד לייצר proteo-GUVs המכיל אשלגן ערוץ מתח מגודר KvAP ולאפיין אותם באמצעות מיקרוסקופ פלואורסצנטי ואלקטרופיזיולוגיה. אני מקווה שניתן להתאים שיטות אלה לכיתות חדשות של חלבונים בממברנה ולספק תשתית למערכות חוץ-גופית מורכבת יותר ללימוד ובניית חומר חי ממרכיבי היסוד שלה.
Disclosures
The authors have nothing to disclose.
Acknowledgements
We thank Susanne Fenz for discussing the possibility of reconstituting proteins by agarose swelling, Feng Ching Tsai for current measurements, and present and former members of the Bassereau group for support and assistance. The project was funded by the Agence Nationale de la Recherche (grant BLAN-0057-01), by the European Commission (NoE SoftComp), by the Université Pierre et Marie Curie (grant from the FED21, Dynamique des Systèmes Complexes). M.G. was supported by an Institut Curie International PhD Fellowship, S.A. by a fellowship from the Fondation pour la Recherche Médicale, G.E.S.T. by a Marie Curie Incoming International Fellowship from the European Commission and a grant from the Université Pierre et Marie Curie. The publication fees were covered by the Labex ‘CelTisPhyBio’ (ANR-11-LABX0038).
Materials
| Name | Company | Catalog Number | Comments |
| DPhPC (1,2-diphytanoyl-sn-glycero-3-phosphocholine) | Avanti Polar Lipids | 850356P | |
| Egg PC L-α-phosphatidylcholine (Egg, Chicken) | Avanti Polar Lipids | 840051P | |
| Egg PA L-α-phosphatidic acid (Egg, Chicken) | Avanti Polar Lipids | 840101P | |
| 18:1 (Δ9-cis) PC (DOPC) 1,2-dioleoyl-sn-glycero-3-phosphocholine | Avanti Polar Lipids | 850375P | |
| Cholesterol (ovine wool, >98%) | Avanti Polar Lipids | 700000P | |
| TRed-DHPE | Invirtogen | T-1395MP | labeled lipid |
| BPTR-Ceramide | Invirtogen | D-7540 | labeled lipid |
| Choloroform | VWR | 22711.290 | AnalaR Normapur |
| Acetone | VWR | 20066.296 | AnalaR Normapur |
| Ethanol | VWR | 20821.330 | AnalaR Normapur |
| Kimwipe | Kimtech | 7552 | |
| Hamilton syringes | Hamilton Bonaduz AG | diverse | |
| Amber vials and Teflon cups | Sigma | SU860083 and SU860076 | |
| Parafilm | VWR | 291-1214 | |
| Microcentrifuge tube | Eppendorf | diverse | |
| Agarose | Euromex | LM3 (1670-B, Tg 25.7C, Tm 64C) | |
| Sucrose | Sigma | 84097-1kg | |
| Glucose | Sigma | G8270-1kg | |
| Trehalose | Sigma | T9531-25G | |
| KCl | Sigma | P9333-1kg | |
| Hepes | Sigma | H3375-100G | |
| TRIS | Euromex | EU0011-A | |
| Osmometer | Wescor | Vapro | |
| pH meter | Schott instruments | Lab850 | |
| Sonicator | Elmasonic | S 180 H | |
| Syringe filter 0.2 µm | Sartorius steim | Minisart 16532 | |
| Function generator | TTi | TG315 | |
| Platinum wires | Goodfellow | LS413074 | 99.99+%, d = 0.5 mm |
| Polytetrafluoroethylene | Goodfellow | ||
| Dow Corning 'high vacuum grease' | VWR | 1597418 | |
| sealing paste | Vitrex medical A/S, Denmark | REF 140014 | Sigillum Wax |
| Cover slides 22 x 40 mm No1.5 | VWR | 631-0136 | |
| Cover slides 22 x 22 mm No1.5 | VWR | 631-0125 | |
| Plasma cleaner | Harrick | PDC-32G | airplasma, setting 'high' |
| Petri dishes | Falcon BD | REF 353001 | 3.5 cm x 1 cm |
| patch clamp amplifier | Axon instruments | Multiclamp700B | |
| DAQ Card | National Instruments | PCI-6221 | |
| Labview | National Instruments | version 8.6 | |
| Glass pipettes boro silicate OD 1 mm ID 0.58 mm | Harvard Apparatus | GC100-15 | |
| Electrode holder | Warner Instruments | Q45W-T10P | |
| Micromanipulator | Sutter | MP-285 | |
| Pipette puller | Sutter | P-2000 | |
| Camera | ProSilica | GC1380 | |
| Zeiss microscope | Zeiss | Axiovert 135 | |
| Objective | Zeiss | 40X long working distance, Phase contrast | |
| Objective | Zeiss | 100X Plan-Apochromat NA 1.3 | |
| Filterset GFP (for Alexa-488) | Horiba | XF100-3 | |
| Filterset Cy3 (for TexasRed) | Horiba | XF101-2 | |
| beta-casein | Sigma | C6905-1G | |
| Confocal microscope | Nikon Eclipse TE 2000-E | D-Eclipse C1 confocal head | |
| Objective | Nikon | Plan Fluor 100X NA 1.3 | |
| Matlab | Mathworks | for image processing and analysis of the current traces |
References
- Schwille, P. Bottom-Up Synthetic Biology: Engineering in a Tinkerer’s World. Science. 333 (6047), 1252-1254 (2011).
- Aimon, S., et al. Membrane Shape Modulates Transmembrane Protein Distribution. Developmental Cell. 28 (2), 212-218 (2014).
- Roux, A., et al. Membrane curvature controls dynamin polymerization. Proceedings of the National Academy of Sciences. 107 (9), 4141-4146 (2010).
- Domanov, Y. A., et al. Mobility in geometrically confined membranes. Proceedings of the National Academy of Sciences. 108 (31), 12605(2011).
- Sorre, B., et al. Curvature-driven lipid sorting needs proximity to a demixing point and is aided by proteins. Proceedings of the National Academy of Sciences. 106 (14), 5622-5626 (2009).
- Faris, M. D. E. A., et al. Membrane Tension Lowering Induced by Protein Activity. Physical Review Letters. 102 (3), 038102(2009).
- Streicher, P., et al. Integrin reconstituted in GUVs: A biomimetic system to study initial steps of cell spreading. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1788 (10), 2291-2300 (2009).
- Walde, P., Cosentino, K., Engel, H., Stano, P. Giant Vesicles: Preparations and Applications. ChemBioChem. 11 (7), 848-865 (2010).
- Liu, A. P., Fletcher, D. A. Biology under construction: in vitro reconstitution of cellular function. Nature Reviews Molecular Cell Biology. 10 (9), 644-650 (2009).
- Sens, P., Johannes, L., Bassereau, P. Biophysical approaches to protein-induced membrane deformations in trafficking. Current Opinion in Cell Biology. 20 (4), 476-482 (2008).
- Pautot, S., Frisken, B. J., Weitz, D. A. Production of Unilamellar Vesicles Using an Inverted Emulsion. Langmuir. 19 (7), 2870-2879 (2003).
- Stachowiak, J. C., et al. Unilamellar vesicle formation and encapsulation by microfluidic jetting. Proceedings of the National Academy of Sciences. 105 (12), 4697-4702 (2008).
- Reeves, J. P., Dowben, R. M. Formation and properties of thin-walled phospholipid vesicles. Journal of Cellular Physiology. 73 (1), 49-60 (1969).
- Angelova, M. I., Soléau, S., Méléard, P., Faucon, F., Bothorel, P. Preparation of giant vesicles by external AC electric fields. Kinetics and applications. Trends in Colloid and Interface Science VI. 89, 161-176 (1992).
- Bagatolli, L. A., Pott, T. Giant Unilamellar Vesicle Electroformation. Methods in Enzymology. 465, 161-176 (2009).
- Horger, K. S., Estes, D. J., Capone, R., Mayer, M. Films of Agarose Enable Rapid Formation of Giant Liposomes in. Solutions of Physiologic Ionic Strength. Journal of the American Chemical Society. 131 (5), 1810-1819 (2009).
- Campillo, C., et al. Unexpected Membrane Dynamics Unveiled by Membrane Nanotube Extrusion. Biophysical Journal. 104 (6), 1248-1256 (2013).
- Kwok, R., Evans, E. Thermoelasticity of large lecithin bilayer vesicles. Biophysical Journal. 35 (3), 637-652 (1981).
- Mathivet, L., Cribier, S., Devaux, P. F. Shape change and physical properties of giant phospholipid vesicles prepared in the presence of an AC electric field. Biophysical Journal. 70 (3), 1112-1121 (1996).
- Weinberger, A., et al. Gel-Assisted Formation of Giant Unilamellar Vesicles. Biophysical Journal. 105 (1), 154-164 (2013).
- Dezi, M., Di Cicco, A., Bassereau, P., Levy, D. Detergent-mediated incorporation of transmembrane proteins in giant unilamellar vesicles with controlled physiological contents. Proceedings of the National Academy of Sciences. 110 (18), 7276-7281 (2013).
- Kahya, N., Pecheur, E. I., de Boeij, W. P., Wiersma, D. A., Hoekstra, D. Reconstitution of membrane proteins into giant unilamellar vesicles via peptide-induced fusion. Biophysical Journal. 81 (3), 1464-1474 (2001).
- Doeven, M. K., et al. Distribution, lateral mobility and function of membrane proteins incorporated into giant unilamellar vesicles. Biophysical Journal. 88 (2), 1134-1142 (2005).
- Girard, P., Prost, J., Bassereau, P. Passive or Active Fluctuations in Membranes Containing Proteins. Physical Review Letters. 94 (8), 088102(2005).
- Betaneli, V., Petrov, E. P., Schwille, P. The Role of Lipids in VDAC Oligomerization. Biophysical Journal. 102 (3), 523-531 (2012).
- Ruta, V., Jiang, Y., Lee, A., Chen, J., MacKinnon, R. Functional analysis of an archaebacterial voltage-dependent K+ channel. Nature. 422 (6928), 180-185 (2003).
- Jiang, Y., et al. X-ray structure of a voltage-dependent K+ channel. Nature. 423 (6935), 33-41 (2003).
- Aimon, S., et al. Functional Reconstitution of a Voltage-Gated Potassium Channel in Giant Unilamellar Vesicles. PLoS ONE. 6 (10), e25529(2011).
- Lee, S., Zheng, H., Shi, L., Jiang, Q. -X. Reconstitution of a Kv Channel into Lipid Membranes for Structural and Functional Studies. Journal of Visualized Experiments. (77), (2013).
- Baykal-Caglar, E., Hassan-Zadeh, E., Saremi, B., Huang, J. Preparation of giant unilamellar vesicles from damp lipid film for better lipid compositional uniformity. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1818 (11), 2598-2604 (2012).
- Suchyna, T. M., Markin, V. S., Sachs, F. Biophysics and Structure of the Patch and the Gigaseal. Biophysical Journal. 97 (3), 738-747 (2009).
- Hille, B. Ion Channels of Excitable Membranes. , Sinauer Associates, Inc. (2001).
- Finol-Urdaneta, R. K., McArthur, J. R., Juranka, P. F., French, R. J., Morris, C. E. Modulation of KvAP unitary conductance and gating by 1-alkanols and other surface active agents. Biophysical journal. 98 (5), 762-772 (2010).
- Schmidt, D., MacKinnon, R. Voltage-dependent K+ channel gating and voltage sensor toxin sensitivity depend on the mechanical state of the lipid membrane. Proceedings of the National Academy of Sciences. 105 (49), 19276-19281 (2008).
- Quemeneur, F., et al. Shape matters in protein mobility within membranes. Proceedings of the National Academy of Sciences of the United States of America. , (2014).
- Parc, A. L., Leonil, J., Chanat, E. αS1-casein, which is essential for efficient ER-to-Golgi casein transport, is also present in a tightly membrane-associated form. BMC Cell Biology. 11 (1), 1-15 (2010).
- Garten, M., Toombes, G. E. S., Aimon, S., Bassereau, P. Studying Voltage Dependent Proteins with Giant Unilamellar Vesicles in a “Whole Cell” Configuration. Biophysical Journal. 104 (2), 466a(2013).
- Crowe, L. M., Reid, D. S., Crowe, J. H. Is trehalose special for preserving dry biomaterials. Biophysical Journal. 71 (4), 2087-2093 (1996).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved