Method Article
Application de Codé génétiquement fluorescent oxyde nitrique (NO •) Sondes, les geNOps, pour l'imagerie en temps réel de NO • Les signaux dans les cellules simples
Dans cet article
Résumé
This manuscript presents protocols for the application of novel genetically encoded nitric oxide (NO•) probes (geNOps) to monitor single cell NO• fluctuations in real-time using fluorescence microscopy. The Ca2+-triggered NO• formation on the level of individual endothelial cells was visualized by combining geNOps with a chemical Ca2+ sensor.
Résumé
L'oxyde nitrique (NO •) est un petit radical, qui médie plusieurs fonctions cellulaires importantes chez les mammifères, les bactéries et les plantes. Malgré l'existence d'un grand nombre de méthodes de détection de NO • in vivo et in vitro, la surveillance en temps réel de NO • au niveau d'une seule cellule est très difficile. Les effets physiologiques ou pathologiques de NO • est déterminée par la concentration réelle et de temps de séjour de ce radical. Par conséquent, des procédés qui permettent la détection de cellules isolées de NO • est hautement souhaitable. Récemment, nous avons élargi la palette de NO • indicateurs en introduisant unique à base de protéine fluorescente génétiquement codée oxyde nitrique (NO) • sondes (de geNOps) qui répondent directement aux cellulaires NO • fluctuations et, par conséquent, répond à ce besoin. Ici, nous démontrons l'utilisation de geNOps pour évaluer intracellulaires NO • signaux en réponse à deux chimique différente NO • molécules -liberating. Nos résultats also confirmer que fraîchement préparée de 3- (2-hydroxy-1-méthyl-2-nitrosohydrazino) -N-méthyl-1-propanamine (NOC-7) a un potentiel beaucoup plus élevé pour évoquer des changements dans les niveaux intracellulaires NO • par rapport à la inorganique NO • nitroprussiate donneur de sodium (SNP). En outre, deux couleurs imagerie des cellules vivantes en utilisant les geNOps verts (G-GENOP) et l'indicateur chimique Ca 2+ Fura-2 a été réalisée pour visualiser la réglementation stricte de Ca 2+ dépendante NO • formation dans les cellules endothéliales simples. Ces expériences représentatives démontrent que geNOps sont des outils appropriés pour enquêter sur la génération en temps réel et la dégradation des unicellulaires NO • signaux dans divers montages expérimentaux.
Introduction
Nous avons récemment développé une nouvelle classe de fluorescents NO • sondes codées génétiquement, appelé les geNOps 1. Ces capteurs sont constitués par un simple bâti, les bactéries dérivées, NO 2 • domaine de liaison, qui est conjugué à une protéine fluorescente distincte (FP) variante 3 (cyan, vert ou orange FP). NO • liaison au fer non hémique (II) Centre 4 dans les geNOps instantanément réduit l'intensité de fluorescence 1. Fait important, la fluorescence de geNOps récupère rapidement et complètement lorsque intracellulaires NO • Les niveaux diminuent 1. Par conséquent, geNOps permettent l'imagerie en temps réel de (sous-) cellulaires NO • fluctuations. Bien que NO • détection du mécanisme de geNOps restent peu claires à ce jour, ils se sont avérés être d'excellents NO • journalistes, et ont donc le pouvoir d'ouvrir une nouvelle ère de polychromie, quantitative NO • bioimaging avec de hautes résolutions spatiales et temporelles 1, 5. Autres disponibles fluorescents NO • sondes sont basées sur de petits composés chimiques, qui doivent être chargés dans les cellules, et sont modifiées de façon irréversible par NO • 6. Inconvénients supplémentaires de NO • petites fluorophores sensibles sont leur cytotoxicité potentiel et spécificité relativement faible ce qui rend difficile de les utiliser d'une manière fiable, analytique et concluante 7, 8, 9. Bien que l'utilisation efficace des sondes fluorescentes codées génétiquement nécessite des techniques de transfert de gènes efficaces, capteurs codés génétiquement à base de FP ont émergé comme des outils indispensables qui ont révolutionné notre compréhension du fonctionnement interne des cellules 10, 11. Avant le développement des geNOps simples à base de FP, un groupe Förster transfert d'énergie par résonance (FRET) à base • capteur de NO, appelé NOA-1 12, a été construit. Sato et al. conçu cette sonde sophistiquée qui se compose de deux sous - unités du NO • -sensible guanylate cyclase soluble (CGT), les deux capteurs à base de FRET de conjugués de rapports guanosine monophosphate cyclique (GMPc) niveaux 12. Comme cette sonde répond aux cGMP, il détecte indirectement intracellulaires NO • fluctuations 12. Bien que NOA-1 répond à NO • élévations dans la gamme de nano-molaire, cet outil n'a pas été utilisé fréquemment jusqu'à présent, probablement en raison des limitations concernant la disponibilité et la praticabilité de ce capteur bipartites encombrant.
Fonctions polyvalentes de NO •, ayant un impact fondamental des processus biologiques ont été bien caractérisés 13, 14. De nombreuses études ont montré que le NO • Concentration dans les cellules et sous - domaines qui détermine le destin des cellules dans la santé et les maladies 14, 15, 16. Dans les mammifères, NO • est principalement générée par voie enzymatique dans divers types de cellules par le bien caractérisé l'oxyde nitrique synthase (NOS) famille 17. Jusqu'à présent, trois isoformes de NOS ont été décrits 18, 19, 20; ce sont les Ca 2+ / calmoduline-dépendante NOS endothéliale (eNOS ou NOS-3) 18 et la NOS neuronale (nNOS ou NOS-1) 19 et le Ca 2+ / calmoduline-indépendante constitutivement active NOS inductible (iNOS ou nos- 2) 20. En outre, l'existence de mitochondrial NSA (mtNOS) a également été suggéré 21. Cependant, mtNOS est considéré comme une variante d'épissage de la nNOS, et est donc non classé séparément comme une isoforme 21. Une autre isoforme, à l' exception de ceux des cellules de mammifères, est le soi-disant NOS bactérienne (bNOS), trouve principalement dans les bactéries gram-positives 22. La production enzymatique de NO • est fortement contrôlée et dépend de la disponibilité de plusieurs cofacteurs tels que le nicotinamide adénine dinucléotide phosphate (NADPH), flavine adénine dinucléotide (FAD), la tétrahydrobioptérine (BH4), l' oxygène moléculaire et de la L-arginine 17. L'acide aminé L-arginine cationique est le substrat qui est converti en L-citrulline lors de la production NO • 17. En plus de la génération enzymatique hautement régulé de NO •, il a été postulé que le radical peut être réduit de façon non enzymatique à partir de pools de nitrite par les mitochondries dans des conditions hypoxiques 23. • Une fois que NO est produit à l' intérieur d' une cellule, il peut diffuser librement à travers les membranes biologiques 14,ref "> 15. Cependant, la demi-vie très courte de ce radical est principalement déterminée par les conditions environnementales et différentes voies et les réactions chimiques se dégradent efficacement NO • niveaux 24. Finalement, la formation, la diffusion et la dégradation de NO • dépend les paramètres environnementaux variés qui déterminent la concentration efficace de la molécule biologiquement active hautement 24.
La technologie geNOps permet la détection directe de (sous) NO cellulaire • fluctuation 1 et est donc adapté à réexaminer, et récemment découvrir les mécanismes responsables de l'accumulation et la décomposition des cellulaires NO • signaux. Ici, nous fournissons des protocoles simples et des résultats représentatifs pour l'utilisation de geNOps pour visualiser de manière exogène évoquée et NO • profils générés de manière endogène, au niveau des cellules individuelles. En outre, la technologie de geNOps peut être adapté pour applicature dans d'autres systèmes de modèles de cellules pour étudier les motifs complexes de NO • la formation, la diffusion et à la dégradation en réponse aux stimuli cellulaires et des contraintes diverses.
Protocole
1. Préparation de Tampons et solutions chimiques
- Préparer un tampon de stockage contenant 135 mM de NaCl, 5 mM de KCl, 2 mM de CaCl2, 1 mM de MgCl2, 10 mM HEPES, 2,6 mM NaHCO3, 0.44 mM de KH 2 PO 4, 0,34 mM de Na 2 HPO 4 mM , D - 10 glucose, 2 mM de l-glutamine, vitamines 1x MEM, 1x MEM acides aminés, 1% stylo streptocoque, et 1% amphotéricine B. Dissoudre tous les composants dans de l'eau distillée et agiter le tampon pendant 20 minutes en utilisant un agitateur magnétique à température ambiante. Ajuster le pH à 7,44 à l'aide de NaOH 1 M. Lors de l'addition goutte à goutte de NaOH, de mesurer le pH en utilisant un pH-mètre, tout en agitant en continu.
- Préparer un rapport Ca 2+ contenant un tampon physiologique qui se compose de 140 mM de NaCl, 5 mM de KCl, 2 mM de CaCl2, 1 mM de MgCl2, 10 mM de D-glucose et 10 mM de HEPES. Ajuster le pH à 7,4 en utilisant du NaOH comme décrit dans l'étape 1.1.
- Préparer un tampon exempt de Ca2 + qui se compose des mêmes ingrédientscomme indiqué dans l'étape 1.2. Utiliser EGTA 1 mM au lieu de 2 mM.
- Solubiliser Fura-2 heures dans du DMSO pour obtenir une solution mère 1 mM. Aliquoter la solution mère dans des flacons hermétiquement fermés et conserver à -20 ° C pendant jusqu'à un mois. En cas de gel, laisser la solution mère à équilibrer à la température ambiante pendant au moins 1 heure à l'abri de la lumière. Diluer la solution stock Fura-2 heures dans 1 tampon de stockage de ml (étape 1.1) pour obtenir une concentration finale de 3,3 uM.
- Préparer 1 ml d'une histamine solution mère 100 mM dans de l'eau distillée (pH 7,0). Diluer l'histamine solution mère 100 mM dans 100 ml Ca 2+ contenant un tampon physiologique à une concentration finale de 100 uM d' histamine.
- Solubiliser Nω-nitro-L-arginine (L-NNA) dans 100 ml de tampon physiologique contenant du calcium pour obtenir une concentration finale de 300 uM. Stocker les solutions à 37 ° C bain d'eau pendant au moins 1 heure jusqu'à ce que la L-NNA est complètement dissous.
- Solubiliser 10 mg CNP-7 wa distilléeter (pH 7,0) pour obtenir une solution mère à 10 mM. Aliquoter la solution mère dans de petites aliquotes dans des flacons hermétiquement fermés et stocker immédiatement à -70 ° C. Diluer la solution stock NOC-7 dans un tampon physiologique pour obtenir une concentration finale de 10 uM NOC-7.
NOTE: NOC-7 est un petit composé chimique qui libère spontanément NO avec une demi-vie courte. Toujours préparer les tampons de travail qui consiste NOC-7 juste avant chaque expérience. - Préparer une solution de nitroprussiate de sodium 1 mM (SNP) dans un tampon physiologique de calcium et de préparer une dilution de 10 pm.
NOTE: Toujours préparer de petites quantités (~ 10 ml) de solutions NO-donneurs en raison de la vitesse de dégradation rapide. - Préparer une solution tamponnée de phosphate (PBS) constitué de 137 mM de NaCl, 2,7 mM de KCl, 9,2 mM de Na 2 HPO 4 et 1,5 mM de KH 2 PO 4. Ajuster la valeur du pH à 7,44 avec du NaOH / HCl.
2. Préparation des cellules
NOTE: En oRDONNANCE pour obtenir une uniformité des performances de la mesure de l' oxyde nitrique (NO •) dans des cellules individuelles à l' aide geNOps, les cellules doivent être pré-incubées avec un fer (II) / vitamine C , contenant un tampon avant les expériences d'imagerie afin de rétablir Fe 2+ dans le NO • domaine liant le du NO • -probes. Dans le cas des cellules EA.hy926 et HEK293, incubation pendant 20 minutes avec le fer (II) solution de rappel conduit à l'activation complète des NO • capteurs.
- Graine de 5,5 x 10 5 EA.hy926 ou cellules HEK293 pour le lendemain ou 3,5 x 10 5 cellules pour le jour après jour suivant, le 30 mm couverture de microscope verres dans un puits d'une plaque à 6 puits. Incuber les cellules à 37 ° C dans un environnement humidifié à 5% de CO 2.
NOTE: Des informations détaillées concernant une infection adénovirale de cellules de mammifères et la construction de virus a été décrit par Zhang et al. 25. Cette étape ne concerne pas les cellules HEK 293 exprimant de manière stable G-GENOP. - Prenez le sérum de veau foetal (FCS) et l'aigle de milieu modifié de Dulbecco (DMEM) sans antibiotique et ajouter le type de virus adéno-associé 5 (AAV5) vecteur portant le gène codant pour G-GENOP (MOI: 500 pour les cellules EA.hy926 rendement presque 100 % de cellules positives; MOI: 1 est efficace pour les cellules HEK293).
NOTE: L'utilisation de vecteurs viraux adéno-associés est affecté au groupe de risque 2. niveau de biosécurité 2 de confinement est généralement requis pour le travail avec ce vecteur. Le cas échéant, l'infection par le virus peut également être effectuée dans du FCS contenant du milieu. Alternativement, les cellules peuvent être transfectées de manière transitoire en utilisant des supports à base de lipides-1. - Retirez le milieu de culture et laver les cellules avec pré-chauffé (37 ° C) PBS. Ajouter 1 ml de milieu DMEM / VAA5 dans chaque puits pendant 1 h. Cette étape ne concerne pas les cellules HEK 293 exprimant de manière stable G-GENOP.
- Ajouter 1 ml de 20% de FCS contenant du DMEM à chaque puits à une concentration finale de 10% de FCS. Ne pas retirer le support AAV5 contenant des cellules. gentlemanly SEESAW la plaque pour homogénéiser le milieu dans les puits. Incuber les cellules pendant 48 heures à 37 ° C dans un environnement humidifié à 5% de CO 2. Cette étape ne concerne pas les cellules HEK 293 exprimant de manière stable G-GENOP.
- Après 48 h, laver les cellules avec pré-chauffé PBS. ajouter ensuite 2 ml préchauffé tampon de stockage (section 1.1) à chaque puits et incuber les cellules à la salle RT pendant au moins 1 heure à l'abri de rayonnement lumineux.
- Remplacer le tampon de stockage avec 1 ml / puits de (II) une solution d'amplificateur de fer à la température ambiante (RT). Incuber les cellules pendant exactement 20 minutes dans l'obscurité.
NOTE: Ne pas dépasser ou de réduire le temps d'incubation optimal, car cela pourrait affecter la réactivité des NO • sondes. - Laver les cellules une fois avec du tampon de stockage et incuber chaque puits avec 2 ml de tampon de stockage pendant au moins 2 heures à température ambiante afin de permettre aux cellules d'atteindre l'équilibre.
- Remplacer le tampon de stockage avec 3,3 uM de Fura-2 heures dans un tampon de stockage de 1 ml pendant 45 minutes à la température ambiante, à l'abride la lumière.
- Laver les cellules deux fois avec du tampon de stockage et incuber encore une fois pendant au moins 30 minutes afin de permettre aux cellules d'atteindre l'équilibre.
3. Imagerie de cellules vivantes NO • et Ca 2+ signaux dans les cellules individuelles
- Fixer une lamelle de 30 mm revêtu de cellules EAhy.926 ou HEK293 (de l'étape 2.1) dans une chambre de perfusion en métal et placez-le sur le microscope. Connecter le tube d'arrivée aux réservoirs de tampon et l'efflux à une pompe à vide. Assurer un flux régulier et éviter la vidange de la lamelle.
- Démarrer la perfusion par gravité avec un tampon physiologique de calcium (étape 1.2), en utilisant un système de perfusion semi-automatique.
REMARQUE: Un tel système est constitué de réservoirs de tampon, les tubes respectifs, les vannes magnétiques qui sont commandés électroniquement et une pompe à vide (voir figure 1B). Le débit peut varier de 1 à 3 ml / min, dépendant de la hauteur des réservoirs de perfusion. Pour appli cohérentes de drogue locauxcation, le taux de tous les réservoirs utilisés de débit doit être à peu près égale. Ceci doit être testé avant des expériences d'imagerie. Considérez que les cellules endothéliales répondent à une augmentation de la contrainte de cisaillement qui peut être induite par une perfusion rigoureuse. - Mettre en marche le système d'imagerie et de permettre d'échauffement de tous les dispositifs pendant 30 min.
- Définir les paramètres d'imagerie utilisant des logiciels respectifs. Sélectionnez la longueur d'onde d'excitation de 340 nm et 380 nm pour fura-2 imagerie et 480 nm pour exciter G-GENOP. Pour minimiser la fluorescence blanchiment augmenter le binning de la caméra à 4 et à réduire l'intensité d'excitation et des temps d'exposition. Voir aussi les étapes 3,6-3,8.
REMARQUE: Les paramètres d'imagerie et les paramètres dépendent des appareils utilisés, fura-2 efficacité de chargement et de niveaux d'expression G-GENOP. - Sélectionnez la région d'imagerie en déplaçant le xyz table du microscope jusqu'à ce que plusieurs cellules fluorescentes sont dans le foyer. Ensuite, définir des régions d'intérêt (ROI) par l'intermédiaire de l'outil logiciel respectif. Dessinez régions couvrant plusieurs ensemble single cellules fluorescentes par champ d'imagerie manuellement. En outre, définir une région d'arrière-plan de taille similaire.
NOTE: Une fois que les images ont été acquises et stockées ROIs peut également être défini récemment après le processus d'imagerie pour l'analyse en outre l'utilisation des logiciels d'analyse d'imagerie respectifs (voir la liste des matériaux). - Début de la collecte des données sur un microscope à fluorescence inversé et avancé avec un étage d'échantillon motorisé, et une source de lumière monochromatique. exciter alternativement à 340 nm et 380 nm pour le Fura-2 heures et à 480 nm pour le G-GENOP, respectivement. Régler les temps d'exposition respectifs de telle sorte que pour tous les canaux, un signal de fluorescence clair est détectable au fil du temps. Voir aussi l'étape 3.4.
NOTE: Cela dépend de l'intensité de la lumière d'excitation et le binning de la caméra. Par exemple, utiliser 15% d'intensité de la lumière d'excitation, un binning de caméra de 4 et 150 ms pour 340 nm, 50 ms pour 380 nm, et 300 ms pour 480 nm. Voir aussi l'étape 3.4. - Recueillir la lumière émise à 510 nm pour fura-2 / h, 520 nm pour G-Genop en utilisant un dispositif (CCD) à couplage de charge avec l'ensemble de filtre approprié constitué de l'excitateur de 500 nm, un dichroïque 495 nm et un émetteur 510-520 nm. Enregistrez un total d'images toutes les 3 s.
- Enregistrer les premières minutes ( le cas échéant jusqu'à 3 min) dans un tampon physiologique Ca2 + (1,2) afin d' obtenir la ligne de base des signaux de fluorescence respectifs dans le temps.
- Une fois par fluorescence de base stable est observée, passer à 100 histamine uM ou ATP (1 uM ou 100 uM) contenant physiologique Ca 2+ tampon pour stimuler les cellules pendant 3 min.
NOTE: Les cellules EA.hy926 qui répondent aux agonistes montrent une forte augmentation du ratio fura-2 (fluorescence excitée à 340 nm divisée par la fluorescence excitée à 380 nm) et une nette diminution du signal de fluorescence G-GENOP. - Revenez à la mémoire tampon physiologique Ca 2+ sans histamine ou ATP et L-NNA pendant 5 min pour éliminer les composés à partir des cellules. Cette étape peut être prolongée jusqu'à ce que les fluoreschangements cence sont récupérés complètement.
- Administrer 10 uM NOC-7 dans un tampon physiologique Ca2 + pendant 2 minutes en utilisant le système de perfusion. Le donneur NO affecte fortement G-GENOP fluorescence qui diminue habituellement par> 20% en réponse à 10 uM NOC-7. Dans les cellules EA.hy926 l'effet NOC-7 est d'environ 3 fois plus forte par rapport à l'agoniste du G-GENOP fluorescence induite par trempe.
- Laver le NO • composé -releasing pendant environ 10 min avec Ca 2+ physiologique tampon et arrêter l' enregistrement une fois la fluorescence basale est récupéré.
Analyse 4. Données
- Exporter l'acquisition des données d'intensité de fluorescence moyenne des cellules individuelles au fil du temps, le logiciel d'analyse de données.
- Soustraire des valeurs de référence respectives, et calculer le rapport de 340 nm à 380 nm par des Fura-2 signaux respectifs de chaque cellule unique dans le temps.
- Soustraire les valeurs de fond du canal G-GENOP pour obtenir la fl réelleuorescence intensité de la NO sonde (F) au fil du temps en utilisant un logiciel de calcul.
- Prendre des valeurs de fluorescence de base en F 0 (F 0 est la fluorescence de la sonde de NO au cours du temps sans stimulation). Voir aussi l' étape 4.5 et la figure 1C.
- Calculer une fonction au fil du temps pour que les effets de fluorescence de blanchiment à l' aide de l'équation suivante: F = 0 F inital • exp (-K • Time) + F plateau. F inital: signal de fluorescence maximale une fois l' imagerie est commencé; K: constante de taux de fluorescence de blanchiment au fil du temps; F plateau: fluorescence minimale atteinte par la décoloration au fil du temps; Voir aussi les étapes 4.3- 4.4 et Figure 1C.
NOTE: Pour l'approximation, toutes les valeurs de fluorescence au cours du temps avant et après la stimulation des cellules peuvent être utilisés. De plus amples détails sont précisés par Bentley et al. 27. - Pour normaliser le signal G-GENOP au fil du temps, calculer 1-F / F0 (étapes 4,3-4,5). Voir la figure 1C et 1D.
Résultats
Visualisation des cellules uniques NO • Profils en réponse à transitoirement appliquée NO donateurs
Nous avons utilisé un clone de cellules HEK qui exprime de manière stable G-GENOP (figure 1A), afin de visualiser NO • signaux sur le niveau de la cellule unique en réponse à deux petits composés chimiques NO libérant différentes, CNP-7 et SNP. Les NO • donateurs ont été consécutivement appliqués et retirés à partir de cellules lors de l' imagerie à l' aide d' un système de perfusion par gravité qui a assuré flux continu (figure 1B). Toutes les cellules exprimant G-GENOP avec des intensités différentes ont montré une nette diminution de la fluorescence en réponse à la CNP-7 et SNP (figure 1C), indiquant rapide NO • accumulation dans les cellules lors de l'addition des NO • donateurs. Signaux de fluorescence normalisés (1-F / F 0) ont démontré que le NO • donateurs évoqués cellula homogèner NON • élévations qui a complètement récupéré après lavage des NO • composés -releasing (Figure 1D). Cependant, 10 uM de SNP induit seulement 50% du NO cellulaire • Signal (9,63 ± 1,05%, n = 3/38) qui a été atteint par 10 uM NOC-7 (18,10 ± 1,20%, n = 3/38, p < 0,0001). Afin d'atteindre l' égalité intracellulaires NO • niveaux avec le NO • donateurs, une concentration de 1 mM de SNP était nécessaire (Figures 1C, 1D).
Ensuite, nous avons testé la capacité fraîchement préparé par rapport a expiré NOC-7 pour élever intracellulaires NO • niveaux dans les cellules HEK. A cet effet, nous avons préparé quatre tampons expérimentaux contenant 5 uM NOC-7. Le NO • donneur a été soit ajouté fraîchement juste avant la mesure, ou maintenue dans les réservoirs pendant 1 h, 2 h et 3 h à la température ambiante avant la mesure. Les différents tampons ont été successivement appliqués à f éliminésROM , les cellules exprimant le G-GENOP en utilisant un système de perfusion (figure 2B). Cette approche a dévoilé la stabilité des aqueuses NOC-7 solutions qui, comme prévu, ont montré une diminution des capacités au fil du temps pour élever intracellulaires NO • niveaux (Figures 2A, 2C). Fait intéressant, NO • Les signaux récupérés nettement plus rapide lors de l'enlèvement des tampons expirés, par rapport à la intracellulaire NO • réponse qui a été évoquée par frais CNP-7 (figure 2C), l' adhérence indiquant peut - être des molécules intactes NO • -liberating à composants cellulaires .
Visualisation simultanée de Ca 2+ et NO • Les signaux dans les cellules endothéliales simples
Afin d'étudier Ca 2+ -triggered NO • formation dans les cellules endothéliales, l'endothéliales immortalisées cellules de remplacement couramment utilisé, la lignée cellulaire EA.hy926, était transiently transfectées avec G-GENOP et chargé avec Fura-2 / h (voir le protocole 2.8). La transfection a abouti à environ 10% des cellules endotheliales positives G GENOP (n = 6, la figure 3A), ce qui est suffisant pour enregistrer Ca2 + -evoked NON • la production au niveau des cellules endothéliales seules. Cependant, nous avons atteint près de 100% G-GENOP cellules EA.hy926 positives en utilisant un vecteur viral adéno-associé (n = 6; voir le protocole 2.2). Avant les mesures multi - canaux, les cellules ont été incubées pendant 20 min à température ambiante dans un tampon de stockage constitué par la L-NNA, un puissant inhibiteur irréversible NOS-26. Les cellules témoins ont été maintenus dans le même tampon de stockage sans L-NNA (voir Protocole 1.1) (figure 3B). Le traitement des cellules témoins avec l' histamine, un inositol 1,4,5-triphosphate puissant (IP 3) générant un agoniste, cytosolique instantanément élevée Ca2 + niveaux suivie d'une augmentation progressive du NO intracellulaire • jusqu'à ce que l'agoniste a été removed (figures 3C, 3D). Les cellules pré-traitées avec le NOS-inhibiteur montré cytosolique Ca 2+ signaux similaires, alors que le NO intracellulaire • niveau est resté à peu près inchangée en réponse à l' histamine (Figure 3E). EA.hy926 cellules exprimant G-GENOP ont également été traitées avec 1 uM et 100 uM de l'IP 3 générant agoniste ATP afin de tester si oui ou non geNOps conviennent de surveiller NO • signaux en réponse à la fois une faible physiologique et supra-physiologiques Les concentrations d'un agoniste (figure 3F). Dans la lignée cellulaire endothéliale 1 pM ATP évoqué un cytosolique clair NO • signal, qui était d' environ la moitié du signal obtenu par 100 pM ATP (Figure 3F).

Figure 1: profils de NO intracellulaires en réponse à différentes NO-liberati ng molécules. (A) images larges de cellules HEK de terrain exprimant de manière stable cytosolique G-GENOP. Barre d'échelle = 20 pm. (B) Représentation schématique d'un système de perfusion par gravité à base de semi-automatique pour l'application commandée et le retrait de la NOC-7 et le SNP. (C) représentatif (sur 3 expériences indépendantes) non normalisée d' intensité de fluorescence de cellules uniques traces en unités arbitraires en fonction du temps des cellules HEK exprimant de façon stable cytosolique G GENOP en réponse à 10 uM NOC-7, 10 uM de SNP, et 1 mM SNP. courbe gras noir représente la courbe moyenne de 26 traces unicellulaires (courbes gris clair). Courbe noire représente Parsemé F 0, qui a été utilisé pour la normalisation. (D) traces simples Normalisé et inversées (1-F / F 0, courbes gris clair), et courbe moyenne (courbe noire en gras) au fil du temps en réponse à 10 uM NOC-7, 10 uM SNP, et 1 mM SNP extrait de panneau C.es / ftp_upload / 55486 / 55486fig1large.jpg "target =" _ blank "> S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
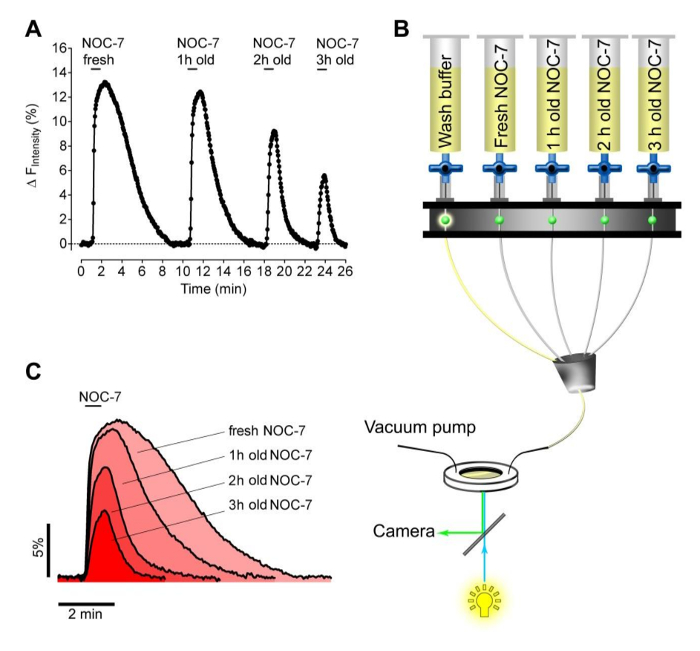
Figure 2: Essai de stabilité de la NOC-7 en utilisant des cellules HEK stable G-GENOP exprimant. (A) représentant NO • courbe de réponse de concentration dans le temps de manière stable G-GeNOps exprimant des cellules HEK lors de l' application de la NOC-7 solutions tampons fraîches et anciennes. Tous les tampons contenant de la CNP-7 ont été préparées d'abord avec une concentration finale de 5 uM en utilisant la même solution de stock (50 mM). Le temps écoulé des solutions respectives après la préparation jusqu'à ce que des quantités d'imagerie à 1 h, 2 h et 3 h comme indiqué. (B) Représentation schématique d'un système de perfusion de semi-automatique par gravité consécutivement ajouter et supprimer des solutions de la CNP-7 contenant lors de l' imagerie. (C) corrélations temporelles decellulaire NO • signaux en réponse fraîchement préparés et vieux CNP-7 tampons. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.

Figure 3: imagerie multicanal simultanée de NO • et Ca 2+ signaux dans les cellules EA.hy926 simples. (A) représentatifs grand champ images de fluorescence des cellules exprimant EAhy.926 G-GENOP (panneau de gauche) qui sont chargés avec fura-2 / h (moyenne et panneaux de droite). Barre d'échelle = 20 pm. (B) Représentation schématique du traitement des cellules avec 500 uM EAhy.926 Nω-nitro-L-arginine (L-NNA) pendant 20 minutes dans une plaque à six puits avant la mesure. (C) au cours du temps représentatif d'un enregistrement simultané de fura-2 (excitation: 340 nm / 380 nm emission: 510 nm) et des signaux G GENOP (excitation: 480 nm; émission: 520 nm) en réponse à 100 uM d'histamine. Comme indiqué histamine a été éliminé au bout de 3 min à l'aide d'un système de perfusion. (D) Les courbes représentent des enregistrements simultanés de cytosolique Ca 2+ (-2 fura signaux de rapport, F 340 / F 380 est gris ligne pleine) et NO • (courbe normalisée et inversée, 1-F / F 0 est une ligne solide vert) signaux au fil du temps d'une seule fura-2 / am chargé cellules endothéliales exprimant transitoirement G-GENOP. Les cellules ont été stimulées avec 100 uM d' histamine pendant 3 min dans un Ca2 + (2 mM CaCl2) contenant un tampon (n = 03/08). (E) représentant enregistré simultanément Ca 2+ (ligne solide gris) et NO • Les signaux (ligne verte solide) au fil du temps d'une cellule EA.hy926 qui a été prétraités avec 500 uM Nω-nitro-L-arginine (L-NNA) avant à la mesure (n = 03/12). Les cellules ont été traitées avec 100 uM d'histamine en présence de 2 mMCa 2+. (F) représentant les courbes moyennes cytosoliques NO • Les signaux en réponse à 1 uM d' ATP suivie d'une seconde stimulation des cellules avec 100 pM d' ATP. Les barres représentent les valeurs moyennes ± écart-type des signaux G GENOP maximaux en réponse à 1 uM d'ATP (barre blanche) et 100 uM d'ATP (barre verte) de 4 expériences indépendantes; p <0,001 par rapport à 1 pM d'ATP. P-valeur a été calculée en utilisant un test t non apparié. S'il vous plaît cliquer ici pour voir une version plus grande de cette figure.
Discussion
Depuis la découverte de NO • comme une molécule de signalisation importante dans la biologie 28, la mesure spécifique en temps réel du radical dans des cellules individuelles, des tissus et des animaux entiers avec une haute résolution d'une manière réaliste et fiable a été aspiré. Nous rapportons ici l'application de récemment mis au point génétiquement codés fluorescents NO • sondes (geNOps) qui permettent précisément l' imagerie des cellules vivantes de NO • signaux utilisant grand champ de microscopie par fluorescence 1.
Pour contourner les procédures de transfection élaborées et invasives clone de cellules HEK qui exprime de manière stable fluorescente verte G-GENOP a été utilisé pour quantifier une seule cellule générée de manière exogène NO • profils. Comme les cellules HEK normalement ne produisent pas de manière endogène • NO 29, ce type de cellule est apte à la génération d'une lignée de cellules de détection à base GENOP, ce qui pourrait être utile pour de nombreuses autres applications dans des conditions de co-cultureavec NO • produire des cellules primaires ou même chez les animaux 30 vivant. Toutefois, dans cette étude, nous démontrons la capacité de divers composés NO • -liberating, de différentes concentrations et stabilités, pour évoquer intracellulaires NO • signaux en utilisant le modèle de cellules HEK G-GENOP exprimant. Nos données ont révélé que le NO • donneur de concentration, la qualité et la méthode d'application éventuellement déterminer les motifs de NO intracellulaires • profils. Ces informations sont indispensables pour la pharmacocinétique in situ la caractérisation des différentes NO • donateurs, qui sont indicatifs de plusieurs maladies. Notamment, geNOps ont été montré pour répondre de manière stable à de multiples applications répétitives de NO • donneur de impulsions sur une très longue période 1. En conséquence, les expériences utilisant NO • -liberating composés présentés ici, permettent des conclusions semi-quantitatives sur les diverses amplitudes et la cinétique de NO cellulaire respective226; les signaux (figures 1 et 2).
Bien que le HEK exprimant de manière stable le clone cellulaire provient probablement d'une seule cellule, une grande hétérogénéité du G-geNOps les niveaux d'expression a été observée (figure 1). Ceci est une caractéristique commune des clones cellulaires stables comme la transcription du (génome intégré) gène d'intérêt est sous le contrôle de nombreux facteurs tels que divers stress environnementaux 31 qui influencent les taux de croissance des cellules 32 et l'état du cycle cellulaire 33. Les geNOps simples à base de FP sont des sondes non-ratiométrique et, par conséquent, le NO • perte induite par des augmentations d'intensité de fluorescence avec le niveau d'expression GENOP 1. En conséquence, la normalisation des signaux de geNOps est essentiel pour la quantification cellulaires NO • signaux particulièrement dans le cas d'une analyse comparative. Comme le montre notre étude récente, une stricte corrélation linéaire bntre l'intensité de fluorescence basale de geNOps et la force de l'extinction de la fluorescence induite par NO • sur une large gamme d'intensités de fluorescence a été trouvée 1. Ceci est une caractéristique importante de geNOps pour la quantification absolue des cellulaires NO • signaux. Comme le montre la figure 1, la normalisation des signaux G-geNOps en réponse à NDP-7 et SNP a révélé homogènes NO • signaux dans différentes cellules HEK de la même plaque, ce qui indique que les cellules HEK ne sont pas diversifiés quant à leur capacité à prendre et dégrader le radical NO • qui provient du NO • donneur. En revanche, à l'aide de geNOps dans les cellules HeLa ont démontré hétérogénéités claires de cellulaires NO • signaux entre différentes cellules en réponse à la CNP-7. Ces différences pointer spécifiques du type NO • métabolisme et décomposition des taux de cellules, ce qui pourrait avoir des implications multiples dans la physiologie cellulaire et la pathologie, et peut être découvert en utilisant la GENOPla technologie de l'art.
Néanmoins, deux caractéristiques importantes de geNOps doivent être soigneusement examiné pour l'utilisation correcte des capteurs et des interprétations de données: i) geNOps nécessitent suffisamment de fer (II) pour répondre pleinement aux NO • 1 et ii) en fonction de la variante FP, geNOps peut être sensible au pH 1. Nous décrivons ici un protocole qui a été jugé approprié pour la supplémentation en fer non toxique (II) de geNOps, qui sont exprimés dans les deux HEK, des cellules HeLa ou EA.hy926 (voir Protocole 2.6). Bien qu'il ait été démontré que le traitement des cellules avec du fer (II) / vitamine C n'a pas affecté la morphologie cellulaire, la viabilité cellulaire et l' activité métabolique des cellules 1, il peut être nécessaire d'optimiser cette étape importante pour d' autres types de cellules et tissus. Cependant, dans certaines conditions expérimentales, l'exigence de fer (II), le chargement peut limiter l'applicabilité de geNOps. Notamment, il a été démontré que l'ascorbate peut réduire le NO • 35 et ascorbate de fer (II) complexes sont capables de piéger NO • 36, 37. En outre, l' excès de fer (II) et l' ascorbate peuvent induire des réponses inflammatoires 39 et eNOS découpler 41. Ces effets doivent être pris en considération lors de l'utilisation de la technologie geNOps. Il a été démontré que , dans certaines conditions expérimentales, le pH intracellulaire est affecté de manière significative 34, qui a le potentiel d'influencer la fluorescence geNOps 1. Notamment, les variantes de cyan et geNOps verts sont relativement sensibles au pH montrant une diminution de la fluorescence lors de l' acidification 1. Par conséquent, des changements aigus de la (sous) pH cellulaire peuvent simuler de faux NO • signaux lorsque vous utilisez les geNOps sensibles au pH. Comme suggéré dans nos travaux précédents, l'utilisation parallèle de NO • geNOps insensibles (geNOps mut) en tant contro négativels est recommandé de disséquer réelle cellulaire NO • signal du pH change 1. En plus des changements de pH cellulaire peuvent être inspectés en utilisant des sondes de pH tels que Sypher 34.
En outre, nous avons visualisé enzymatique NO endogène • la formation en réponse à un agoniste physiologique Ca2 + dans la cellule mobilisant l' endothelial porteuse EA.hy926. La lignée cellulaire EA.hy926 est un système modèle fréquemment utilisé exprimant constamment eNOS 38. Utilisation de geNOps transitoirement exprimés dans les cellules EA.hy926, a confirmé que IP 3 médiée les signaux de Ca évoquent profonde NO • formation dans ce type de cellule, qui a été presque complètement bloquée par L-NNA. Afin de corréler temporellement Ca 2+ avec NO • Les signaux, les cellules G-GENOP exprimant ont été chargées avec la excitables-UV chimique Ca 2+ -Indicateur fura-2 / h. La séparation spectrale du Ca 2+ lié et non lié fura-2 Fluo rescence du signal G GENOP peut être facilement réalisé avec des jeux de filtres disponibles dans le commerce 40. Imagerie les deux sondes ont dévoilé que le Ca 2+ enzymatique -triggered NO • formation se produit beaucoup plus lent par rapport à la hausse du cytosolique Ca dans ce type de cellules endothéliales. Cinétiques similaires de unicellulaires NO • signaux dans les cellules endothéliales de l' artère pulmonaire bovine sur le traitement des cellules avec l'agoniste bradykinine IP 3, générant ainsi que les contraintes de cisaillement ont été rapportés en utilisant NOA-1, un capteur très NO • -sensible indirecte 12 . Par conséquent, ces données soulignent que le Ca2 + -evoked eNOS dérivé NON • la formation nécessite un certain temps de démarrage jusqu'à ce que l'activité enzymatique totale est atteinte. Bien que la cinétique cellulaire NON • la formation, la diffusion et la dégradation peuvent être extraites à partir d' autres données, par exemple sur la base des mesures de tensions de NO • induite par la relaxation des vaisseauxss = "xref"> 26, le grand avantage de NO fluorescentes • sondes est qu'ils convertissent directement cellulaires NO • fluctuations en signaux visibles en temps réel. Par conséquent, l'imagerie cellulaire NO • signaux avec geNOps fournit une résolution spatiale et temporelle, et offre des possibilités uniques en (re) enquêter sur le (sous) cellulaire NO • homéostasie. Par exemple, l' imagerie eNOS la navette 42 en combinaison avec la technologie de geNOps dans les cellules endothéliales unique peut être adapté pour établir une corrélation entre la formation de NO • la localisation subcellulaire et la translocation de l'enzyme NO • productrices ou d' autres protéines appropriées telles que la calmoduline et 43 cavéoline.
Nous décrivons ici l'application possible du G-GENOP exprimant des cellules HEK et EA.hy926 de visualiser de manière exogène et endogène généré cellulaires NO • signaux sur le niveau d'une seule cellule et en temps réel sur une large fluorescence de champ m classiqueicroscope. Nos données impliquent que geNOps sont appropriés pour suivre spécifiquement (sous-) cellulaires NO • Dynamique dans diverses conditions expérimentales en utilisant toutes sortes de types de cellules intéressantes.
Déclarations de divulgation
EE, MW, RM et WFG, les membres de l'Université médicale de Graz du personnel, ont déposé une demande au Royaume-Uni en matière de brevets (numéro de demande de brevet WO2015EP74877 20151027, numéro de priorité GB20140019073 20141027) qui décrivent les parties de la recherche dans ce manuscrit. Licences relatives à ce brevet sont fournies pour la prochaine génération d' imagerie par fluorescence (NGFI) GmbH ( http://www.ngfi.eu/ ), une société spin-off de l'Université médicale de Graz.
Remerciements
The authors acknowledge C.J. Edgell, Pathology Department, University of North Carolina at Chapel Hill, NC, USA for providing the EA.hy926 cells. Author E.E. is supported by Nikon Austria within the Nikon-Center of Excellence, Graz and is a fellow of the Ph.D. program in Molecular Medicine at the Medical University of Graz. The researchers are also supported by the Ph.D. program Metabolic and Cardiovascular Disease (DK-W1226) of the Medical University of Graz. This work was also funded by the FWF project P 28529-B27. Microscopic equipment is part of the Nikon-Center of Excellence, Graz that is supported by the Austrian infrastructure program 2013/2014, Nikon Austria Inc., and BioTechMed, Graz.
matériels
| Name | Company | Catalog Number | Comments |
| NaCl | Carl Roth, Karlsruhe, Germany | 3957.20 | sodium chloride |
| KCl | Carl Roth, Karlsruhe, Germany | 6781.1 | potassium chloride |
| CaCl2·2H2O | Carl Roth, Karlsruhe, Germany | T885.1 | calcium chloride dihydrate |
| MgCl2·6H2O | Carl Roth, Karlsruhe, Germany | 2189.2 | magnesium chloride hexahydrate |
| HEPES | Carl Roth, Karlsruhe, Germany | 9105.3 | 4-(2-Hydroxyethyl)-1-piperazineethanesulfonic acid |
| NaHCO3 | Carl Roth, Karlsruhe, Germany | 8551.1 | sodium hydrogencarbonate |
| KH2PO4 | Merck, Darmstadt, Germany | 104873 | potassium dihydrogen phosphate |
| Na2HPO4·2H2O | Carl Roth, Karlsruhe, Germany | 4984.1 | sodium hydrogenphosphate dihydrate |
| D(+)-Glucose monohydrate | Carl Roth, Karlsruhe, Germany | 6780.1 | >99.5%; for cell culture, endotoxin free |
| EGTA | Carl Roth, Karlsruhe, Germany | 3054.2 | ethylene glycol-bis(2-aminoethylether)-N,N,N′,N′-tetraacetic acid; calcium chelating agent |
| NaOH | Carl Roth, Karlsruhe, Germany | 6771.1 | sodium hydroxide |
| HCl | Carl Roth, Karlsruhe, Germany | 4625.1 | hydrochloric acid, fuming, 37% (~10 N) |
| DMSO | Carl Roth, Karlsruhe, Germany | 4720.1 | dimethyl sulfoxide; highly polar, aprotic organic solvent |
| L-Glutamic acid hydrochloride | Sigma Aldrich, Vienna, Austria | G2128 | (S)-2-Aminoglutaric acid |
| DMEM, low glucose | Sigma Aldrich, Vienna, Austria | D5523 | Dulbecco’s Modified Eagle’s Medium - low glucose; with 1,000 mg/L glucose and L-glutamine, without sodium bicarbonate, powder, suitable for cell culture |
| MEM Vitamin solution (100x) | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 11120037 | 100x the vitamins found in the standard Minimum Essential Medium (MEM) |
| MEM Amino acids solution (50x) | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 11130036 | 50x the essential amino acids (except L-glutamine) found in the standard Minimum Essential Medium (MEM) |
| Penicillin-Streptomycin (10,000 U/ml) | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 15140122.00 | antibiotics to prevent bacterial contamination of cell cultures |
| Amphotericin B | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 15290026.00 | Gibco Amphotericin B contains 250 µg of amphotericin B (Fungizone) and 205 µg of sodium deoxycholate; prevents the contamination of cell cultures by yeast and multicellular fungi |
| FCS | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 10270106 | Fetal Bovine Serum, qualified, E.U.-approved, South America origin |
| PBS, pH 7.4 | Gibco/Thermo Fisher Scientific, Waltham, MA, USA | 10010031.00 | phosphate-buffered saline |
| Fura-2 (AM) | Teflabs, Austin, TX, USA | 102 | fluorescent cytosolic calcium indicators |
| Histamine dihydrochlorid | Sigma Aldrich, Vienna, Austria | H7250 | 2-(4-Imidazolyl)ethylamine dihydrochloride; IP3-generating agonist |
| Nω-Nitro-L-arginine | Sigma Aldrich, Vienna, Austria | N5501 | N5-(Nitroamidino)-L-2,5-diaminopentanoic acid; L-NNA; inhibitor of nitric oxide synthase |
| NOC-7 | Calbiochem/Merck, Darmstadt, Germany | 487952 | 3-(2-Hydroxy-1-methyl-2-nitrosohydrazino)-N-methyl-1-propanamine; nitric oxide (NO) donor short half-life of NO release |
| Sodium nitroprusside dihydrate | Santa Cruz Biotechnology, Texas, USA | sc-203395A | sodium nitroferricyanide(III) dihydrate; nitric oxide releasing compound |
| 30 mm Cover slips | Karl Hecht, Sondheim v. d. Rhön, Germany | 41001130 | glass cover slips, HECHT "Assistent", size 1, round, 30 mm, (VE: 100 pcs.) |
| Iron(II) booster solution | Next generation fluorescent imaging (NGFI), Graz, Austria | n.a. | Iron(II) containing physiological buffer for non toxic iron(II) loading of cells; http://www.ngfi.eu/product/ironii-booster-solution/ |
| G-geNOp plasmid | Next generation fluorescent imaging (NGFI), Graz, Austria | n.a. | plasmid DNA encoding green NO sensitive probe (G-geNOp); http://www.ngfi.eu/product/g-genop/ |
| G-geNOp AAV5 | Next generation fluorescent imaging (NGFI), Graz, Austria | n.a. | adenovirus encoding green NO sensitive probe (G-geNOp); http://www.ngfi.eu/product-category/genops/viral-genops-vectors/g-genop-aav5/ |
| G-geNOp sensor cell line | Next generation fluorescent imaging (NGFI), Graz, Austria | n.a. | human embryonic kidney cell line (HEK293) stably expressing green NO sensitive probe (G-geNOp); http://www.ngfi.eu/product-category/genops/g-genop-sensor-cell-line/ |
| HEK293A cell line | Invitrogen/Thermo Fisher Scientific, Waltham, MA, USA | R70507 | subclone of human embryonic kidney cell line (HEK293) |
| EA.hy926 cell line | American Type Culture Collection (ATCC), Wesel, Germany | CRL-2922 | somatic cell hybrid clone of human umbilical vein cell line with a thioguanine-resistant clone of A549 |
| TILL iMIC | Till Photonics, Graefling, Germany | n.a. | digital microscope |
| Polychrome V monochromator | Till Photonics, Graefling, Germany | n.a. | ultra fast switching |
| AVT Stingray F145B | Allied Vision Technologies, Stadtroda, Germany | n.a. | Versatile CCD camera with Sony ICX285 EXview HAD sensor, IEEE 1394b |
| alpha Plan Fluar 40 | Zeiss, Göttingen, Germany | n.a. | 40X objective |
| dichroic filters | Chroma Technology Corp, Rockingham, Vermont, USA | n.a. | GFP emitter 514/3 nm (515dcxr) |
| ValveBank8 Controller | AutoMate Scientific, Inc., Berkeley, California, USA | 01-08 | programmable perfusion system control unit |
| BVC control | Vacuubrand, Wertheim, Germany | 727200 | Chemistry diaphragm pump ME 1C; vacuum pump for perfusion system |
| ImageJ software | NIH Image | Java image processing program inspired by NIH Image. http://imagej.net/Welcome |
Références
- Eroglu, E., et al. Development of novel FP-based probes for live-cell imaging of nitric oxide dynamics. Nat Commun. 7, 10623 (2016).
- Bush, M., et al. The structural basis for enhancer-dependent assembly and activation of the AAA transcriptional activator NorR. Mo. Microbiol. 95 (1), 17-30 (2015).
- Cranfill, P. J., et al. Quantitative assessment of fluorescent proteins. Nat. Methods. 13 (7), 557-562 (2016).
- D'Autréaux, B., Tucker, N., Spiro, S., Dixon, R., Poole, e. d. .. P. o. o. l. e. ,. R. .. K. .. ,. (. e. d. ). .. ,. Characterization of the Nitric Oxide-Reactive Transcriptional Activator NorR. Globins and Other Nitric Oxide-Reactive Proteins, Part B. 437, 235-251 (2008).
- Strack, R. Sensors and probes: Yes to genetically encoded NO• sensors. Nat Methods. 13 (4), 288 (2016).
- Auten, R. L. Response to 'The use of diaminofluorescein for nitric oxide detection: Conceptual and methodological distinction between NO and nitrosation. Free Radic. Biol. Med. 50 (12), 1812 (2011).
- Sivaraman, G., Anand, T., Chellappa, D. A Fluorescence Switch for the Detection of Nitric Oxide and Histidine and Its Application in Live Cell Imaging. ChemPlusChem. 79 (12), 1761-1766 (2014).
- Ye, X., Rubakhin, S. S., Sweedler, J. V. Detection of nitric oxide in single cells. Analyst. 133 (4), 423-433 (2008).
- Thyagarajan, B., Malli, R., Schmidt, K., Graier, W. F., Groschner, K. Nitric oxide inhibits capacitative Ca2+ entry by suppression of mitochondrial Ca2+ handling. Br J Pharmacol. 137 (6), 821-830 (2002).
- Germond, A., Fujita, H., Ichimura, T., Watanabe, T. M. Design and development of genetically encoded fluorescent sensors to monitor intracellular chemical and physical parameters. Biophy. Rev. 8, 121-138 (2016).
- Malli, R., Eroglu, E., Waldeck-Weiermair, M., Graier, W. F. Filling a GAP-An Optimized Probe for ER Ca2+ Imaging In Vivo. Cell Chem Biol. 23 (6), 641-643 (2016).
- Sato, M., Hida, N., Umezawa, Y. Imaging the nanomolar range of nitric oxide with an amplifier-coupled fluorescent indicator in living cells. Proc Natl Acad Sci USA. 102 (41), 14515-14520 (2005).
- Weidinger, A., Kozlov, A. V. Biological Activities of Reactive Oxygen and Nitrogen Species: Oxidative Stress versus Signal Transduction. Biomolecules. 5 (2), 472-484 (2015).
- Paolo, S. Nitric Oxide in Human Health and Disease. Encyclopedia of life sciences. , (2005).
- Pacher, P., Beckman, J. S., Liaudet, L. Nitric oxide and peroxynitrite in health and disease. Physiol Rev. 87 (1), 315-424 (2007).
- Bonafe, F., Guarnieri, C., Muscari, C. Nitric oxide regulates multiple functions and fate of adult progenitor and stem cells. J Physiol Biochem. 71 (1), 141-153 (2015).
- Forstermann, U., Sessa, W. C. Nitric oxide synthases: regulation and function. Eur. Heart J. 33 (7), 829-837 (2012).
- Dudzinski, D. M., Igarashi, J., Greif, D., Michel, T. The regulation and pharmacology of endothelial nitric oxide synthase. Annu Rev Pharmacol Toxicol. 46, 235-276 (2006).
- Zhou, L., Zhu, D. -. Y. Neuronal nitric oxide synthase: structure, subcellular localization, regulation, and clinical implications. Nitric Oxide. 20 (4), 223-230 (2009).
- Aktan, F. iNOS-mediated nitric oxide production and its regulation. Life Sci. 75 (6), 639-653 (2004).
- Ghafourifar, P., Cadenas, E. Mitochondrial nitric oxide synthase. Trends Pharmacol Sci. 26 (4), 190-195 (2005).
- Crane, B. R., Sudhamsu, J., Patel, B. A. Bacterial nitric oxide synthases. Annu Rev Biochem. 79, 445-470 (2010).
- Lundberg, J. O., Weitzberg, E., Gladwin, M. T. The nitrate-nitrite-nitric oxide pathway in physiology and therapeutics. Nat Rev Drug Discov. 7 (2), 156-167 (2008).
- Kelm, M. Nitric oxide metabolism and breakdown. Biochim Biophys Acta. 1411 (2-3), 273-289 (1999).
- Zhang, Y., et al. Estrogen-related receptors stimulate pyruvate dehydrogenase kinase isoform 4 gene expression. J Biol Chem. 281 (52), 39897-39906 (2006).
- Holzmann, S., Kukovetz, W. R., Windischhofer, W., Paschke, E., Graier, W. F. Pharmacologic differentiation between endothelium-dependent relaxations sensitive and resistant to nitro-L-arginine in coronary arteries. J Cardiovasc Pharmacol. 23 (5), 747-756 (1994).
- Bentley, M., et al. Vesicular calcium regulates coat retention, fusogenicity, and size of pre-Golgi intermediates. Mol Biol Cell. 21 (6), 1033-1046 (2010).
- Ignarro, L. J. Nitric oxide: a unique endogenous signaling molecule in vascular biology. Biosci Rep. 19 (2), 51-71 (1999).
- Upreti, M., Kumar, S., Rath, P. C. Replacement of 198MQMDII203 of mouse IRF-1 by 197IPVEVV202 of human IRF-1 abrogates induction of IFN-β, iNOS, and COX-2 gene expression by IRF-1. Biochem Biophys Res Com. 314 (3), 737-744 (2004).
- Lacin, E., Muller, A., Fernando, M., Kleinfeld, D., Slesinger, P. A. Construction of Cell-based Neurotransmitter Fluorescent Engineered Reporters (CNiFERs) for Optical Detection of Neurotransmitters In Vivo. J Vis Exp. (111), (2016).
- de Nadal, E., Ammerer, G., Posas, F. Controlling gene expression in response to stress. Na. Rev Genet. 12 (12), 833-845 (2011).
- Latchman, D. S. Transcriptional Gene Regulation in Eukaryotes. Encyclopedia of life sciences. , (2005).
- Bertoli, C., Skotheim, J. M., de Bruin, R. A. M. Control of cell cycle transcription during G1 and S phases. Nat Rev Mol Cell Biol. 14 (8), 518-528 (2013).
- Poburko, D., Santo-Domingo, J., Demaurex, N. Dynamic regulation of the mitochondrial proton gradient during cytosolic calcium elevations. J Biol Chem. 286 (13), 11672-11684 (2011).
- Suarez, S. A., et al. Nitric oxide is reduced to HNO by proton-coupled nucleophilic attack by ascorbate, tyrosine, and other alcohols. A new route to HNO in biological media. J Am Chem Soc. 137 (14), 4720-4727 (2015).
- Kuropteva, Z. V., Kudryavtsev, M. E. Ferrous-ascorbate complexes as carriers of nitric oxide. Gen Physiol Biophys. 16 (1), 91-96 (1997).
- Vanin, A. F., Huisman, A., Stroes, E. S., Ruijter-Heijstek, F. C., Rabelink, T. J., van Faassen, E. E. Antioxidant capacity of mononitrosyl-iron-dithiocarbamate complexes: implications for NO trapping. Free Radic Biol Med. 30 (8), 813-824 (2001).
- Lindberg, R. A., Dewhirst, M. W., Buckley, B. J., Hughes, C. S., Whorton, A. R. Ca2+-dependent nitric oxide release in endothelial but not R3230Ac rat mammary adenocarcinoma cells. Am J Physiol. 271 (1), 332-337 (1996).
- Campo, G. M., et al. The SOD mimic MnTM-2-PyP(5+) reduces hyaluronan degradation-induced inflammation in mouse articular chondrocytes stimulated with Fe (II) plus ascorbate. Int J Biochem Cell Biol. 45 (8), 1610-1619 (2013).
- Waldeck-Weiermair, M., et al. Spatiotemporal correlations between cytosolic and mitochondrial Ca2+ signals using a novel red-shifted mitochondrial targeted cameleon. PLOS ONE. 7 (9), 45917 (2012).
- Kuzkaya, N., Weissmann, N., Harrison, D. G., Dikalov, S. Interactions of peroxynitrite with uric acid in the presence of ascorbate and thiols: implications for uncoupling endothelial nitric oxide synthase. Biochem Pharmacol. 70 (3), 343-354 (2005).
- Liu, J., Hughes, T. E., Sessa, W. C. The first 35 amino acids and fatty acylation sites determine the molecular targeting of endothelial nitric oxide synthase into the Golgi region of cells: a green fluorescent protein study. J Cell Biol. 137 (7), 1525-1535 (1997).
- Feron, O. The Endothelial Nitric-oxide Synthase-Caveolin Regulatory Cycle. J Biol Chem. 273 (6), 3125-3128 (1998).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon