Method Article
La interfaz nerviosa periférica regenerativa del manguito muscular para la amplificación de señales nerviosas periféricas intactas
En este artículo
Resumen
Este manuscrito proporciona un método innovador para desarrollar una interfaz nerviosa periférica biológica denominada Interfaz nerviosa periférica regenerativa del manguito muscular (MC-RPNI). Esta construcción quirúrgica puede amplificar las señales eferentes motoras de su nervio periférico asociado para facilitar la detección precisa de la intención motora y el control potencial de los dispositivos de exoesqueleto.
Resumen
Los exoesqueletos robóticos han ganado elogios recientes dentro del campo de la medicina de rehabilitación como una modalidad prometedora para la restauración funcional para aquellos individuos con debilidad en las extremidades. Sin embargo, su uso se limita en gran medida a las instituciones de investigación, que con frecuencia operan como un medio de soporte estático de las extremidades, ya que los métodos de detección motora siguen siendo poco fiables. Las interfaces nerviosas periféricas han surgido como una solución potencial a esta deficiencia; Sin embargo, debido a sus amplitudes inherentemente pequeñas, estas señales pueden ser difíciles de diferenciar del ruido de fondo, lo que reduce su precisión general de detección del motor. Como las interfaces actuales dependen de materiales abióticos, la descomposición inherente del material puede ocurrir junto con la reacción del tejido de cuerpo extraño con el tiempo, lo que afecta aún más su precisión. La interfaz nerviosa periférica regenerativa del manguito muscular (MC-RPNI) fue diseñada para superar estas complicaciones observadas. Consiste en un segmento de injerto de músculo libre asegurado circunferencialmente a un nervio periférico intacto, la construcción se regenera y se reenerva por el nervio contenido con el tiempo. En ratas, esta construcción ha demostrado la capacidad de amplificar los potenciales de acción eferentes motores de un nervio periférico hasta 100 veces el valor normal a través de la generación de potenciales de acción muscular compuestos (CMAP). Esta amplificación de señal facilita la detección de alta precisión de la intención del motor, lo que potencialmente permite la utilización confiable de dispositivos de exoesqueleto.
Introducción
Solo en los Estados Unidos, aproximadamente 130 millones de personas se ven afectadas por trastornos neuromusculares y musculoesqueléticos, lo que resulta en más de $ 800 mil millones en impacto económico anual 1,2. Este grupo de trastornos es típicamente secundario a la patología dentro del sistema nervioso, en la unión neuromuscular o dentro del propio músculo3. A pesar de la variedad de orígenes patológicos, la mayoría comparte algún grado de debilidad de las extremidades 1,3. Desafortunadamente, esta debilidad es a menudo permanente dadas las limitaciones en la regeneración del tejido neural y muscular, especialmente en el contexto de un trauma severo 4,5,6.
Los algoritmos de tratamiento de la debilidad de las extremidades se han centrado clásicamente en medidas de rehabilitación y apoyo, a menudo confiando en aprovechar las capacidades de las extremidades intactas restantes (bastones, sillas de ruedas, etc.) 7. Sin embargo, esta estrategia se queda corta para aquellos cuya debilidad no se limita a una sola extremidad. Con las innovaciones recientes en tecnologías robóticas, se han desarrollado dispositivos avanzados de exoesqueleto que restauran la funcionalidad de las extremidades a las personas que viven con debilidad en las extremidades 8,9,10,11,12,13. Estos exoesqueletos robóticos a menudo son dispositivos portátiles alimentados que pueden ayudar con el inicio y la terminación del movimiento o el mantenimiento de la posición de las extremidades, proporcionando una cantidad variable de fuerza que se puede adaptar individualmente para el usuario 8,9,10,11,12,13 . Estos dispositivos se clasifican como pasivos o activos dependiendo de cómo proporcionan asistencia motora al usuario: los dispositivos activos contienen actuadores eléctricos que aumentan la potencia del usuario, mientras que los dispositivos pasivos almacenan energía de los movimientos del usuario para liberarla de nuevo al usuario cuando sea necesario14. Como los dispositivos activos tienen la capacidad de aumentar las capacidades de potencia de un usuario, estos dispositivos se utilizan con mucha más frecuencia en el contexto de debilidad de las extremidades[14].
Para determinar la intención motora en esta población, los exoesqueletos modernos comúnmente se basan en algoritmos de reconocimiento de patrones generados a partir de electromiografía (EMG) de los músculos distales de las extremidades 8,15,16,17 o electroencefalografía de superficie (sEEG) del cerebro18,19,20 . A pesar de la promesa de estas modalidades de detección, ambas opciones tienen limitaciones significativas que impiden la utilización generalizada de estos dispositivos. Como sEEG detecta señales de nivel de microvoltios transcranealmente18,19,20, las críticas se centran con frecuencia en la incapacidad de diferenciar estas señales del ruido de fondo 21. Cuando el ruido de fondo es similar a la señal de grabación deseada, esto produce bajas relaciones señal-ruido (SNR), lo que resulta en una detección y clasificación del motor inexacta22,23. La detección precisa de la señal se basa además en el contacto estable y de baja impedancia del cuero cabelludo21, que puede verse afectado significativamente por la presencia de cabello grueso / grueso, la actividad del usuario e incluso la sudoración22,24. En contraste, las señales EMG son varias magnitudes mayores en amplitud, lo que facilita una mayor precisión de detección de la señal del motor15,18,25. Sin embargo, esto tiene un costo, ya que los músculos cercanos pueden contaminar la señal, disminuyendo los grados de libertad capaces de ser controlados por el dispositivo 16,17,25 y la incapacidad de detectar el movimiento muscular profundo25,26,27,28. Lo más importante es que la EMG no puede ser utilizada como método de control cuando hay compromiso muscular significativo y ausencia completa de tejido29.
Para avanzar en el desarrollo de exoesqueletos robóticos, se requiere una detección consistente y precisa de la intención del motor del usuario previsto. Las interfaces que utilizan el sistema nervioso periférico han surgido como una técnica de interfaz prometedora, dado su acceso relativamente simple y selectividad funcional. Los métodos actuales de interfaz de nervios periféricos pueden ser invasivos o no invasivos y, por lo general, se incluyen en una de tres categorías: electrodos extraneurales 30,31,32,33, electrodos intrafasciculares 34,35,36 y electrodos penetrantes37,38,39,40 . Como las señales nerviosas periféricas generalmente están en el nivel de microvoltios, puede ser difícil diferenciar estas señales del ruido de fondo de amplitud similar41,42, lo que reduce las capacidades generales de precisión de detección motora de la interfaz. Estas bajas relaciones señal-ruido (SNR) a menudo empeoran con el tiempo debido al empeoramiento de la impedancia del electrodo 43 producida por la degradación del dispositivo39,43, o la reacción local de cuerpo extraño que produce tejido cicatricial alrededor del dispositivo y / o degeneración axonal local37,44. Aunque estas deficiencias generalmente se pueden resolver con la reoperación y la implantación de una nueva interfaz nerviosa periférica, esta no es una solución viable a largo plazo, ya que las reacciones asociadas a cuerpos extraños continuarían ocurriendo.
Para evitar estas reacciones tisulares locales generadas por la interacción de los nervios periféricos con las interfaces abióticas, es necesaria una interfaz que incorpore un componente biológico. Para abordar esta deficiencia, se desarrolló la Interfaz Nerviosa Periférica Regenerativa (RPNI) para integrar nervios periféricos transectados en los muñones de aquellos con amputaciones con dispositivos protésicos45,46,47,48. La fabricación del RPNI implica la implantación quirúrgica de un nervio periférico transeccionado en un segmento de injerto de músculo libre autólogo, con revascularización, regeneración y reinervación que ocurren con el tiempo. A través de la generación de potenciales de acción muscular compuestos a nivel de milivoltios (CMAP), el RPNI es capaz de amplificar la señal de nivel de microvoltios de su nervio contenido en varias magnitudes, facilitando la detección precisa de la intención motora45,48,49. Ha habido un desarrollo considerable de la RPNI en la última década, con un éxito notable en la amplificación y transmisión de señales nerviosas motoras eferentes tanto en ensayos con animales50,51 como en humanos47, facilitando el control de dispositivos protésicos de alta precisión con múltiples grados de libertad.
Los individuos con debilidad en las extremidades pero nervios periféricos intactos se beneficiarían de manera similar de la detección de alta precisión de la intención motora a través de interfaces nerviosas periféricas para controlar los dispositivos del exoesqueleto. Como el RPNI se desarrolló para la integración con nervios periféricos transeccionados, como en personas con amputaciones, fueron necesarias modificaciones quirúrgicas. A partir de la experiencia con el RPNI, se desarrolló la interfaz nerviosa periférica regenerativa del manguito muscular (MC-RPNI). Consiste en un segmento similar de injerto de músculo libre como en el RPNI, en su lugar se asegura circunferencialmente a un nervio periférico intacto (Figura 1). Con el tiempo, se regenera y se reinerva a través de la germinación axonal colateral, amplificando y traduciendo estas señales nerviosas motoras eferentes a señales EMG que son varios órdenes de magnitud más grandes52. Como el MC-RPNI es de origen biológico, evita la inevitable reacción de cuerpo extraño que ocurre con las interfaces nerviosas periféricas actualmente en uso52. Además, el MC-RPNI confiere la capacidad de controlar múltiples grados de libertad simultáneamente, ya que pueden colocarse en nervios distalmente diseccionados a músculos individuales sin una diafonía significativa, como se ha demostrado previamente en RPNIs49. Finalmente, el MC-RPNI puede operar independientemente de la función muscular distal, ya que se coloca en el nervio proximal. Dadas sus ventajas sobre las interfaces nerviosas periféricas actuales, el MC-RPNI es muy prometedor para proporcionar un método seguro, preciso y confiable de control del exoesqueleto.
Protocolo
Todos los procedimientos y experimentos con animales se llevaron a cabo con la aprobación del Comité Institucional de Cuidado y Uso de Animales (IACUC) de la Universidad de Michigan. Las ratas Fischer F344 y Lewis macho y hembra (~ 200-300 g) a los 3-6 meses de edad se utilizan con mayor frecuencia en experimentos, pero teóricamente se puede utilizar cualquier cepa. Si se utilizan ratas donantes en lugar de injertos musculares autólogos, las ratas donantes deben ser isogénicas a la cepa experimental. A las ratas se les permite el libre acceso a alimentos y agua tanto antes como después de la operación. Después de las evaluaciones terminales de punto final, la eutanasia se realiza bajo anestesia profunda con inyección intracardíaca de cloruro de potasio seguida de un método secundario de neumotórax bilateral.
1. Preparación experimental de la rata
- Anestesiar a la rata experimental utilizando una solución de isoflurano al 5% en oxígeno a 0,8-1,0 L/min en una cámara de inducción. Una vez que se logra la anestesia adecuada y se confirma con la ausencia de reflejo corneal, coloque a la rata en un cono nasal de rebreather con isoflurano bajado a 1.75% -2.25% para el mantenimiento de la anestesia.
- Inyecte una solución de 0.02-0.03 ml de carprofeno (50 mg/ml) en 0.2 ml de solución salina estéril con aguja de 27 g en el plano subcutáneo entre los omóplatos para analgesia peri y postoperatoria.
- Aplique ungüento estéril para los ojos en ambos ojos para prevenir las úlceras corneales mientras está anestesiado.
- Con una maquinilla de afeitar eléctrica, afeite la porción lateral de las extremidades inferiores bilaterales, que se extiende desde la articulación de la cadera, sobre el muslo y hasta la superficie dorsal de la pata.
- Esterilice el sitio quirúrgico limpiando primero con una almohadilla de preparación de alcohol, seguido de la aplicación de solución de povidona yodada, terminando con una limpieza final con una nueva almohadilla de preparación de alcohol para eliminar la solución residual de povidona yodada. Repita este proceso de limpieza alterno tres veces para mantener la esterilidad.
NOTA: Esto puede ser un irritante dermatológico; Asegúrese de que se elimine la mayor parte de la solución.
2. Preparación del injerto muscular
- Coloque a la rata en una almohadilla térmica debajo de un microscopio quirúrgico con una sonda de temperatura corporal intraoral de elección para el monitoreo de la temperatura corporal. Mantener el isoflurano al 1,75%-2,25% y el oxígeno a 0,8-1,0 L/min.
- Haga una incisión longitudinal a lo largo de la cara anterior de la extremidad posterior del donante deseado que se extiende desde justo por encima del tobillo hasta justo debajo de la rodilla con un bisturí # 15.
- Diseccionar a través del tejido subcutáneo subyacente usando tijeras de iris afiladas para exponer la musculatura subyacente y los tendones distales justo proximales a la articulación del tobillo. El tibial anterior (AT) es el más grande y anterior de los músculos; el músculo extensor largo de los dedos (EDL) se puede encontrar justo profundo y posterior a este músculo. Aísle el músculo EDL y su tendón distal de la musculatura circundante.
- Asegure el aislamiento del tendón correcto insertando ambos dientes de un fórceps o tijera de iris debajo del tendón distal justo proximal a la articulación del tobillo. Ejerza presión hacia arriba sobre el tendón abriendo los fórceps o las tijeras de iris. Este movimiento debe producir una extensión simultánea de todos los dedos de los pies simultáneamente. Si se produce dorsiflexión aislada del tobillo, eversión del tobillo o dorsiflexión de un solo dedo del pie, se ha aislado el tendón incorrecto.
- Realizar una tenotomía distal del músculo EDL a nivel del tobillo con tijeras de iris afiladas y diseccionar el músculo libre de tejidos circundantes trabajando proximalmente hacia su origen tendinoso.
- Una vez que se visualiza el tendón proximal, realice una tenotomía proximal utilizando tijeras de iris afiladas para liberar el injerto.
- Recorte ambos extremos tendinosos del injerto muscular y corte a la longitud deseada con tijeras de iris afiladas.
NOTA: Los injertos que miden 8-13 mm se han utilizado con éxito; sin embargo, la longitud más común utilizada es de 10 mm. - En un lado del injerto muscular, haga una incisión longitudinal a lo largo de toda la longitud recortada para facilitar la colocación del nervio dentro del injerto muscular y proporcionar contacto del nervio con el endomisio.
- Coloque el injerto muscular preparado en una gasa humedecida con solución salina para evitar la desecación del tejido.
- Cierre la piel que recubre el sitio donante con sutura crómica 4-0 de manera corriente.
3. Aislamiento y preparación del nervio peroneo común
- Marque la incisión quirúrgica, que se extenderá desde una línea ~ 5 mm desde la muesca ciática, extendiéndose hasta justo inferior a la articulación de la rodilla. Asegúrese de que esta marca sea inferior y esté en ángulo lejos del fémur que se puede palpar debajo.
- Incide a través de la piel y los tejidos subcutáneos a lo largo de la línea de incisión marcada con una cuchilla #15. Incide cuidadosamente a través de la fascia subyacente del bíceps femoral, teniendo cuidado de no extenderse a través de toda la profundidad del músculo ya que el nervio ciático se encuentra justo debajo.
- Utilizando tijeras pequeñas de punta roma o un hemostático, disecciona cuidadosamente a través del músculo bíceps femoral.
NOTA: El nervio ciático viaja en este espacio subyacente al bíceps, orientado aproximadamente en la misma dirección que la incisión marcada en la piel. Hay tres ramas notables del nervio ciático: sural (el más posterior y más pequeño de los nervios), tibial (típicamente más anterior, pero este nervio siempre se sumerge profundamente en la articulación de la rodilla) y peroneo común (típicamente ubicado entre tibial y sural, siempre viaja por encima de la articulación de la rodilla). - Identifique el nervio peroneo común (PC) y aíslelo cuidadosamente de los nervios circundantes con un par de microfórceps y microtijeras. Retire cualquier tejido conectivo circundante de los 2 cm medios del nervio. Tenga cuidado de no aplastar el nervio CP con fórceps en este proceso, ya que la lesión por aplastamiento puede alterar los resultados del punto final.
- Sobre la porción más central del nervio CP liberado, realice una ventana epineurial eliminando el 25% del epineuro a lo largo de la longitud del nervio que coincida con la longitud deseada del injerto muscular.
- Para realizar esto, sostenga el epineuro proximal con microfórceps, corte el epineuro inmediatamente subyacente con tijeras de microdisección y elimine ~ 25% del epineuro que viaja distalmente a lo largo del nervio. Tenga cuidado de eliminar este segmento en una sola pieza, ya que múltiples intentos pueden causar una eliminación epineurial irregular, lo que aumenta el riesgo de lesión nerviosa.
NOTA: El tejido nervioso subyacente al epineuro tendrá una textura pegajosa; Observar esta cualidad del nervio asegura que se haya eliminado el plano de tejido correcto.
4. Fabricación de construcción MC-RPNI
- Retire el injerto muscular de la gasa humedecida con solución salina y colóquelo debajo de la porción central del nervio PC donde se creó la ventana epineurial. Gire el nervio 180 ° para que la sección de la ventana epineurial entre en contacto con el músculo intacto y no subyaca a la línea de sutura eventual.
- Usando un 8-0 sutura de nylon, sutura el epineuro del nervio CP tanto proximal como distalmente al injerto muscular dentro del surco creado en el paso 2.8 utilizando suturas simples interrumpidas para asegurar el epineuro al endomisio.
NOTA: Coloque estos puntos, asegurándose de que el músculo esté en la longitud normal de reposo. Estirar o comprimir demasiado el músculo puede afectar las capacidades de regeneración y señalización más adelante. - Envuelva circunferencialmente los bordes del injerto muscular que rodea el nervio ahora asegurado y suture en su lugar utilizando un simple 8-0 interrumpido Puntadas de nylon (~4-6 dependiendo de la longitud).
- Una vez que se logra la hemostasia, cierre la fascia del bíceps femoral sobre la construcción con sutura crómica 5-0 en forma de carrera.
- Cierre la piel suprayacente de manera de correr con una sutura crómica 4-0.
- Limpie el área quirúrgica con una almohadilla de preparación de alcohol y aplique ungüento antibiótico.
- Terminar la anestesia inhalatoria y colocar a la rata en una jaula limpia aislada de los compañeros de jaula y permitir que se recupere con comida y agua ad lib.
- Una vez que la rata se haya recuperado adecuadamente, colóquela de nuevo con compañeros de jaula en una jaula limpia.
NOTA: Estas construcciones requieren una maduración de tres meses como mínimo para producir una amplificación adecuada de la señal nerviosa.
Resultados
La fabricación quirúrgica MC-RPNI se considera una falla perioperatoria si las ratas no sobreviven a la emergencia de la anestesia quirúrgica o desarrollan una infección dentro de una semana de la operación. Investigaciones anteriores han indicado que un período de maduración de 3 meses dará como resultado una amplificación de señal confiable a partir de estas construcciones42,45,48,49. En ese momento o posteriormente, puede ocurrir la exposición quirúrgica de los constructos y la evaluación. Si la fabricación de MC-RPNI fue exitosa, el músculo revascularizado debe ser fácilmente visible en el sitio de implantación original de MC-RPNI (Figura 2B). Los MC-RPNI exitosos también se contraerán después de la estimulación del nervio proximal (Video 1). A veces, pueden estar presentes cicatrices significativas e injertos musculares atróficos (Figura 2C), lo que indica una falla de revascularización / regeneración típicamente secundaria a un injerto demasiado grande, manejo inadecuado o lesión tisular perioperatoria. Estos injertos atróficos comúnmente tienen algún grado de contracción tras la estimulación del nervio proximal, pero producen una amplificación de señal más baja. En general, se considera una falla de fabricación si, tras la exposición, el MC-RPNI se encuentra desalojado del nervio o no tiene contracción tras la estimulación del nervio proximal.
El análisis histológico de estos constructos debe demostrar tejido nervioso y muscular viable sin fibrosis o cicatrización significativa (Figura 3). También se puede realizar inmunohistoquímica para confirmar la presencia de uniones neuromusculares inervadas con neurofilamento como marcador nervioso general en combinación con alfa-bungarotoxina como marcador de receptores de acetilcolina postsinápticos (Figura 4). Si el nervio objetivo implantado no logra inervar el componente muscular del MC-RPNI, la inmunotinción no demostraría ningún brote colateral del nervio motor que atraviese la construcción, ni ninguna unión neuromuscular inervada.
Las pruebas electrofisiológicas se pueden realizar en estos constructos en cualquier momento después de la maduración, con resultados publicados que demuestran señales estables específicamente en el MC-RPNI a los 3 meses52 y hasta 3 años en RPNI en sujetos humanos47. Los esquemas de pruebas electrofisiológicas pueden variar según el área de interés y el equipo disponible (Figura 5), pero las evaluaciones se realizan más comúnmente con la provisión de estimulación máxima al nervio proximal con un electrodo de gancho seguido de un registro de potenciales de acción muscular compuestos (CMAP) generados en el MC-RPNI (Tabla 1 ). Los electrodos de registro pueden variar según las preferencias del usuario, pero el parche / almohadilla epimisial, la sonda bipolar epimisial y los electrodos bipolares penetrantes se han utilizado experimentalmente con éxito. La amplitud media del nervio compuesto (CNAP) registrada en el nervio CP después de una estimulación nerviosa más proximal fue de 119,47 μV ± 14,87 μV. La amplitud media de la CMAP registrada en el MC-RPNI después de una estimulación nerviosa CP proximal similar fue de 3,28 mV ± 0,49 mV, lo que resultó en la amplificación de la señal nerviosa de 11-87x, con un factor de amplificación promedio general de 31,8 ± 7,70. Estas formas de onda CMAP generadas son similares en apariencia al músculo nativo, lo que respalda aún más que se han reinervado por su nervio contenido (Figura 6B).
Para garantizar que la fabricación de MC-RPNI no cause un impacto funcional negativo, se pueden realizar pruebas electrofisiológicas y de fuerza muscular en el músculo inervado distalmente. La mayoría de las pruebas se han realizado en el músculo EDL ipsilateral, ya que es fácilmente accesible para las pruebas y está inervado por el nervio peroneo común (la EDL contralateral se cosecha para la fabricación de MC-RPNI y, por lo tanto, no se evalúa). Los CMAP generados por el músculo EDL fisiológico después de la estimulación nerviosa CP proximal típicamente varían de 20-30 mV52. Al realizar esta prueba en ratas con MC-RPNI implantados, los CMAP EDL no son significativamente diferentes, con un promedio de 24.27 mV ± 1.34 mV. Además, al comparar las formas de onda CMAP generadas entre estos dos grupos, son notablemente similares (Figura 6C). Como medida adicional de la función muscular distalmente inervada, se puede realizar una prueba de fuerza muscular del músculo de interés (Tabla 2). Después de la estimulación nerviosa CP proximal, la fuerza tetánica máxima promedio de EDL generada en sujetos con MC-RPNI es de 2451 mN ± 115 mN, similar a la fuerza promedio de 2497 mN ± 122 mN obtenida del músculo EDL en sujetos control52.
El propósito general del MC-RPNI es amplificar la señal de nivel de microvoltios de su nervio contenido en varias magnitudes, aumentando la relación SNR y, por lo tanto, facilitando la detección precisa de la intención del motor. Se ha demostrado que esta amplificación ocurre de manera confiable en el rango de 10-20 veces 52, con experimentos más recientes que logran factores de amplificación de más de50 veces; Por lo tanto, si una construcción no proporciona un nivel similar de amplificación, se considera subóptima. Los resultados subóptimos generalmente se pueden atribuir a problemas a nivel del injerto muscular en el MC-RPNI, ya que la regeneración incompleta y, por lo tanto, la reinervación pueden resultar en una CMAP inferior a la estándar, lo que reduce las capacidades generales de amplificación del constructo. La forma de onda generada es típicamente atenuada, con una apariencia notablemente anormal. Si el injerto muscular falla por completo, la señal medida en el componente muscular puede ser inexistente (secundaria a tejido cicatricial significativo) o reflejar el CNAP generado en el nervio aguas arriba.
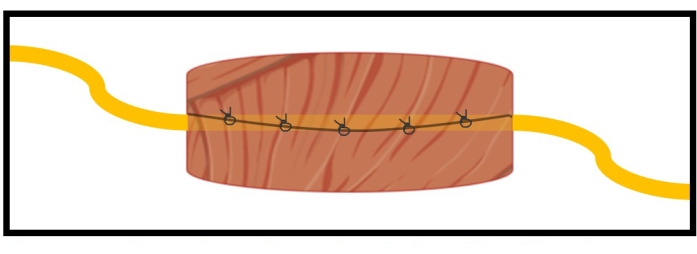
Figura 1: Esquema ilustrativo del MC-RPNI. El nervio periférico objetivo se puede ver en amarillo dentro del injerto muscular circundante. El MC-RPNI es capaz de amplificar sus potenciales de acción eferentes motores del nervio contenido a nivel de microvoltios a través de la generación de potenciales de acción muscular compuestos (CMAP) varias magnitudes mayores. Esto facilita la detección de la intención del motor que se diferencia fácilmente del ruido de fondo. Haga clic aquí para ver una versión más grande de esta figura.
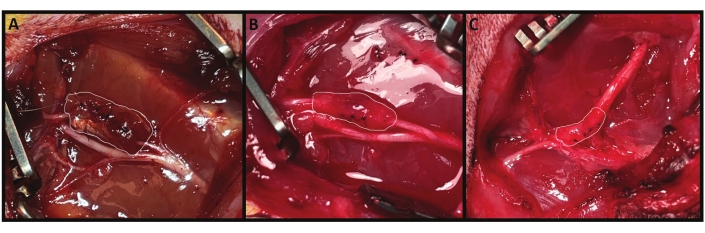
Figura 2: MC-RPNI in vivo. El MC-RPNI se fabrica utilizando un injerto muscular extensor autólogo de los dedos largos (EDL) extraído de la extremidad contralateral. Luego se asegura circunferencialmente al nervio peroneo común, con un ejemplo MC-RPNI delineado en blanco (A) en el momento de la fabricación inicial. Este mismo MC-RPNI se muestra nuevamente en (B) en el momento de la evaluación del punto final 3 meses después. El MC-RPNI tiene una coloración similar al músculo circundante y ha retenido una buena parte del volumen. Un ejemplo de un injerto de músculo atrófico se muestra en (C). El MC-RPNI tiene una apariencia similar a la cicatriz circundante y el tejido conectivo y ha perdido un volumen considerable. Haga clic aquí para ver una versión más grande de esta figura.
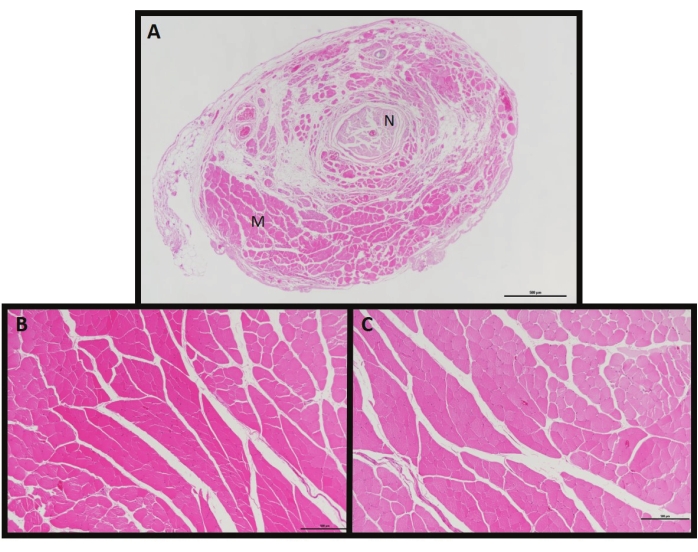
Figura 3: Histología MC-RPNI. (A) H&E de una sección transversal MC-RPNI con M indicando el componente muscular, y N, el nervio. (B) Sección transversal del músculo EDL inervado distalmente ipsilateral en una rata con un MC-RPNI. (C) Sección transversal del músculo EDL en una rata control sin un MC-RPNI. Haga clic aquí para ver una versión más grande de esta figura.

Figura 4: Inmunotinción del MC-RPNI. La imagen en la parte superior izquierda muestra una sección longitudinal de un espécimen MC-RPNI con núcleos anotados en azul (DAPI) y tejido nervioso en verde (neurofilamento). Un primer plano de otro MC-RPNI se muestra en la parte inferior derecha con múltiples uniones neuromusculares presentes (alfa-bungarotoxina en rojo para los receptores de acetilcolina). Haga clic aquí para ver una versión más grande de esta figura.
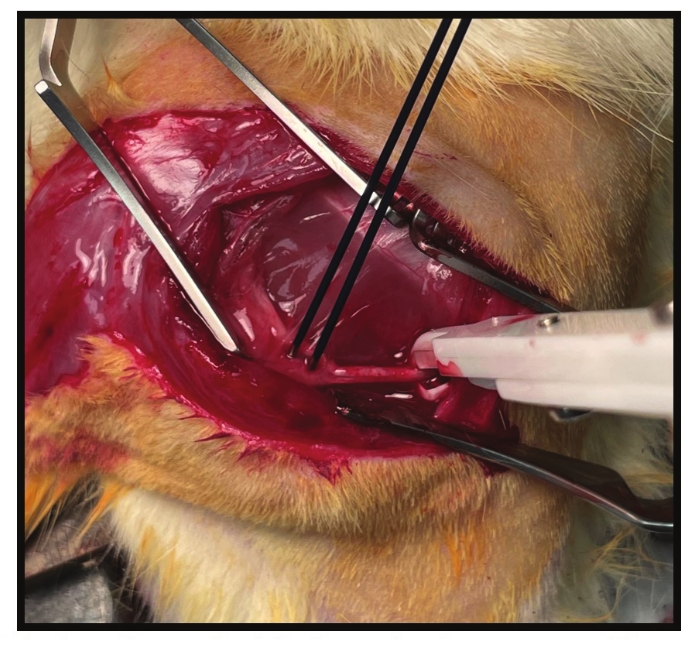
Figura 5: Configuración de la evaluación electrofisiológica del punto final. Las pruebas electrofisiológicas requieren al menos tres electrodos: (1) un electrodo de puesta a tierra - no se muestra; (2) un electrodo bipolar estimulante del nervio; y (3) un electrodo de registro bipolar. En esta configuración, se puede ver un electrodo de gancho estimulante bipolar en blanco a la derecha de la imagen colocada en el nervio peroneo común. El electrodo de la sonda bipolar de grabación se coloca en el MC-RPNI distal. Las señales se registran desde el MC-RPNI después de la estimulación del nervio proximal en el electrodo de gancho hasta que se alcanzan los CMAP máximos. Haga clic aquí para ver una versión más grande de esta figura.

Figura 6: Formas de onda electrofisiológicas estándar. Estos gráficos representan formas de onda típicas capturadas durante el análisis electrofisiológico de una rata con un MC-RPNI implantado después de la estimulación del nervio CP proximal. (A) En azul, se muestra un CNAP (*) registrado desde el nervio CP proximal hasta el MC-RPNI. El artefacto del sistema se indica con un (**). (B) El CMAP representativo registrado desde el MC-RPNI siguiendo el CNAP generado en (A). (C) La forma de onda CMAP resultante registrada del músculo EDL inervado distalmente ipsilateral. Haga clic aquí para ver una versión más grande de esta figura.
| ID de rata | Peso de la rata (g) | Amplitud nerviosa CNAP (μV) | Amplitud MC-RPNI CMAP (MV) | Factor de amplificación de la señal nerviosa | Latencia (ms) |
| 1 | 421 | 123.3 | 1.4 | 11.35 | 0.8 |
| 2 | 368 | 65.6 | 1.6 | 24.39 | 1.05 |
| 3 | 390 | 110.7 | 4.5 | 40.65 | 1.45 |
| 4 | 482 | 217.2 | 3.61 | 16.62 | 0.95 |
| 5 | 417 | 144.6 | 1.39 | 9.61 | 0.9 |
| 6 | 417 | 156.1 | 3.4 | 21.78 | 0.95 |
| 7 | 381 | 82 | 7.2 | 87.8 | 0.9 |
| 8 | 393 | 87.9 | 2.3 | 26.17 | 1.15 |
| 9 | 378 | 87.8 | 4.2 | 47.84 | 1 |
| 10 | 459 | n/d | 5.3 | n/d | 1.55 |
| 11 | 380 | n/d | 2.1 | n/d | 0.75 |
| 12 | 415 | n/d | 2.4 | n/d | 1 |
Tabla 1: Análisis electrofisiológico de punto final de MC-RPNIs. Una selección de resultados obtenidos de ratas sometidas a análisis de punto final a los 3 (Ratas 1-9) y 6 (Ratas 10-12) meses después de la fabricación. Después de la estimulación del nervio peroneo común (PC) proximal, se registraron potenciales de acción nerviosa compuestos (CNAP) en el nervio CP aguas abajo, y potenciales de acción muscular compuestos (CMAP) en el MC-RPNI aguas abajo. El factor de amplificación para cada prueba se puede ver en la columna de la derecha. Nota: para las ratas 10-12, el CNAP proximal al MC-RPNI no se pudo medir dadas las limitaciones anatómicas que resultaron de fabricar el MC-RPNI demasiado cerca del despegue del nervio CP del nervio ciático. La amplitud media del CNAP registrada fue de 119,47 μV ± 14,87 μV, mientras que la amplitud media del CMAP fue de 3,28 mV ± 0,49 mV, produciendo un factor de amplificación medio de 31,8 ± 7,70.
| ID de rata | Contracción máxima (mN) | V | Tetania máxima (mN) | V | Hz | Lo (mm) |
| 1 | 927.13 | 3 | 2668.29 | 3 | 80 | 30.64 |
| 2 | 768.22 | 3.5 | 2677.85 | 3.5 | 80 | 31.15 |
| 3 | 646.99 | 3 | 2164.84 | 3 | 80 | 28.36 |
| 4 | 863.62 | 3.5 | 3109.67 | 3.5 | 150 | 31.07 |
| 5 | 774.48 | 1.5 | 2723.24 | 2 | 80 | 28.83 |
| 6 | 558.19 | 4 | 1930.22 | 4 | 120 | 29.46 |
| 7 | 753.97 | 1 | 2605.64 | 1 | 100 | 31.13 |
| 8 | 768.38 | 2 | 2897.08 | 2 | 100 | 31.86 |
| 9 | 559.9 | 1.5 | 1984.17 | 1.5 | 100 | 31.11 |
| 10 | 600.6 | 5.5 | 2416.09 | 5.5 | 80 | 32.51 |
| 11 | 770.27 | 5.5 | 2496.89 | 5.5 | 80 | 31.89 |
| 12 | 672.22 | 2.5 | 1740.04 | 2.5 | 50 | 31.34 |
Tabla 2: Análisis de la fuerza muscular de ratas con MC-RPNIs implantados. Se realizaron pruebas de fuerza muscular en el músculo extensor largo ipsilateral (EDL) para determinar si el MC-RPNI tuvo algún impacto en la función muscular inervada distalmente. Después de la estimulación del nervio PC proximal, se registraron los trazados de fuerza y se calculó la fuerza activa relevante para la prueba de interés. Lo se definió como la longitud óptima de reposo muscular que producía la fuerza máxima. La fuerza de contracción máxima promedio registrada en ratas con MC-RPNI implantados fue de 722.0 mN ± 32.11 mN y la fuerza tetánica máxima promedio registrada fue de 2451 mN ± 115 mN, similar a los valores obtenidos de animales control (contracción máxima: 822.2 mN ± 41.11 mN; tetania máxima: 2497 mN ± 122 mN).
Video 1: Contracción de MC-RPNI después de la estimulación eléctrica del nervio proximal. Después de la estimulación eléctrica del nervio proximal proporcionada por el electrodo de gancho a la derecha, se puede ver una contracción muscular visible del MC-RPNI en el centro. Haga clic aquí para descargar este video.
Discusión
El MC-RPNI es una construcción novedosa que permite la amplificación de los potenciales de acción eferentes de un nervio motor periférico intacto para controlar con precisión un dispositivo de exoesqueleto. Específicamente, el MC-RPNI confiere un beneficio particular a aquellos individuos con debilidad en las extremidades causada por una enfermedad muscular significativa y / o ausencia de músculo donde las señales de EMG no se pueden registrar. Reducir la función muscular ya comprometida sería devastador en esta población; sin embargo, el MC-RPNI tiene la capacidad de proporcionar esta amplificación de la señal nerviosa sin detrimento del músculo inervado distalmente52 (Tabla 1 y Tabla 2). En aquellos individuos con enfermedad de la neurona motora inferior o de base muscular, los nervios sensoriales periféricos generalmente no se ven afectados por el proceso de la enfermedad53. A medida que se preserva la sensación, es imperativo mantener el nervio en continuidad y evitar lesiones, y el MC-RPNI parece evitar cualquier detrimento a los objetivos inervados distalmente en su conjunto según la histología (Figura 3), la inmunohistoquímica (Figura 4) y la evaluación de la función muscular (Tabla 2).
El MC-RPNI se basa en el concepto de germinación axonal colateral del nervio periférico contenido, concepto fácilmente demostrado tanto en investigaciones previas52 como en la técnica quirúrgica bien descrita de neurorrafia de extremo a lado54,55. Para garantizar una reinervación adecuada del injerto muscular durante la fabricación de MC-RPNI y evitar un impacto negativo en los objetivos inervados distalmente, es imperativo un manejo meticuloso del nervio. Durante la disección del nervio, el trauma se puede evitar mediante el manejo conciso del epineuro o del tejido conectivo solamente. Sin embargo, el potencial de lesión nerviosa en la fabricación de MC-RPNI es el más alto durante el paso de la ventana epineurial. Para evitar la transección aguda de las fibras nerviosas, se recomienda realizar este paso solo bajo un microscopio quirúrgico de alta potencia (al menos 5x) después de varias oportunidades de práctica en ratas no experimentales. Este paso puede tomar varios intentos para dominar, y no se recomienda realizar primero este paso en ratas destinadas al análisis experimental. Teóricamente, el neuroma en continuidad es una complicación que podría ocurrir después de la fabricación de MC-RPNI, especialmente en presencia de un traumatismo nervioso significativo. Sin embargo, esta complicación no se ha encontrado a lo largo de los muchos años de desarrollo.
La mayoría de los experimentos realizados con el MC-RPNI se han realizado en el nervio peroneo común dada su relativa facilidad de acceso, así como la evaluación de objetivos inervados distalmente. Teóricamente, cualquier nervio periférico con un componente motor podría ser sustituido. Los axones sensoriales puros podrían utilizarse ya que el tejido muscular tiene componentes sensoriales (fibras fusiformes, órganos tendinosos de Golgi, etc.), pero estos experimentos no se han realizado hasta ahora, y los resultados son difíciles de predecir. Para el componente de injerto muscular del MC-RPNI, los injertos varían de 20 a 150 mg dependiendo de la longitud del injerto y la edad de la rata, y cualquier injerto muscular de tamaño similar se puede utilizar con éxito. La regeneración del injerto muscular depende en parte de la capacidad de revascularizar, y los injertos grandes/gruesos tienen más probabilidades de sufrir necrosis y fibrosis, afectando la capacidad general de señalización56. La investigación realizada específicamente en RPNIs ha indicado una regeneración muscular exitosa y el mantenimiento de la amplificación de señales en injertos de hasta 300 mg56. Con respecto a la raza de ratas, Lewis y Fischer son recomendados ya que se sabe que la mayoría de las otras ratas utilizadas con fines experimentales se automutilan secundariamente a una lesión nerviosa57,58.
En general, las experiencias actuales con la fabricación de MC-RPNI han producido una tasa de fracaso del <5%. Las fallas de construcción más comunes observadas generalmente se atribuyen al segmento del injerto muscular, con lo cual en la exposición se observa que son atróficas o desalojadas del nervio. Los MC-RPNI desalojados generalmente resultan de una sutura inadecuada en el momento de la fabricación, lo que lleva a la "apertura" del injerto muscular envuelto circunferencialmente y la eventual extrusión parcial del nervio contenido. Sin embargo, estos MC-RPNI generalmente conservan cierto grado (aunque reducido) de capacidades de amplificación de señal, ya que una parte del injerto aún permanece asegurada al nervio. Los MC-RPNI atróficos son obvios en la exposición, ya que carecen de la apariencia típica del músculo esquelético, a menudo indistinguible del tejido cicatricial con coloración rosa claro a gris / blanco (Figura 2C). La atrofia del tejido muscular puede ser el resultado de muchos factores, incluyendo infección, demasiado grande / grueso de un injerto muscular, anemia aguda por pérdida de sangre, lesión muscular y / o nerviosa durante la fabricación, así como la falla de las suturas de sutura epineurial que causan pistones del injerto en el nervio, reduciendo la revascularización. En las pruebas electrofisiológicas, los MC-RPNI atróficos suelen producir poca o ninguna amplificación de señal; si se utilizan electrodos de alta sensibilidad, las grabaciones del CNAP del nervio subyacente se pueden registrar a través del músculo atrófico. Si se observa una atrofia significativa en múltiples sujetos experimentales, se debe volver al protocolo y determinar qué pasos requieren ajuste. Por supuesto, si no se registran señales al realizar evaluaciones, es importante solucionar problemas y no asumir que la construcción es un error. La solución de problemas de configuración del dispositivo es primordial, ya que la falta de señales puede ser secundaria a electrodos dañados (impedancia recomendada <16 Ω), configuración incorrecta del electrodo o incluso estimulación nerviosa proximal inadecuada (algunos nervios requieren estimulación eléctrica de 0.5-5 mA para comenzar a producir CMAP en el MC-RPNI aguas abajo).
Los métodos actuales de interfaz hombre-máquina para el uso del exoesqueleto en aquellos con debilidad en las extremidades generalmente se basan en grabaciones obtenidas de nervios periféricos o EMG del tejido muscular. Como se discutió anteriormente, el MC-RPNI confiere un beneficio significativo con respecto al control del exoesqueleto para aquellos individuos con tejido muscular severamente dañado o ausente donde los registros de EMG no son posibles29. El MC-RPNI también ofrece una ventaja sobre las opciones actuales de interfaz de nervios periféricos, incluidos los electrodos extraneurales 30,31,32,33, los electrodos intrafasciculares 34,35,36 y los electrodos penetrantes37,38,39,40 . Como las señales nerviosas inherentes están comúnmente en el nivel de microvoltios, el MC-RPNI tiene la capacidad de amplificar estas señales nerviosas más de 30 veces, lo que facilita la detección precisa de la intención del motor a partir del ruido de fondo y, por lo tanto, permite un control confiable del exoesqueleto. Con el uso crónico, los métodos actuales basados en electrodos finalmente luchan por superar las complicaciones inherentes a la longevidad del material in vivo y la reacción de cuerpos extraños, complicaciones que el MC-RPNI puede evitar dado su origen biológico. Con el tiempo, estas reacciones de cuerpos extraños resultan en daño tisular, formación de tejido cicatricial y eventual desmielinización axonal y degeneración. Los experimentos realizados hasta seis meses no han revelado ninguna evidencia de lesión neuronal, cicatriz o fibrosis/degeneración del tejido muscular inervado distalmente (Figura 3), y en combinación con la estabilidad del RPNI observada en sujetos humanos durante un período de observación de tres años47, es razonable concluir que los MC-RPNI podrían interactuar con éxito con los nervios periféricos en la escala de años a décadas.
El MC-RPNI está destinado a ser utilizado para el control del exoesqueleto en una variedad de patologías, incluidas las que surgen a nivel del sistema nervioso y del músculo mismo. Por ejemplo, las patologías basadas en los músculos pueden incluir afecciones que van desde traumatismos, distrofia muscular, miopatías inflamatorias y miastenia gravis. A pesar del profundo daño muscular y debilidad que puede resultar en estas condiciones 1,2,3, la mayoría tiene neuronas motoras inferiores funcionales que facilitarían la reinervación MC-RPNI y la detección de la intención motora. Para aquellas condiciones que resultan en una enfermedad muscular generalizada (distrofia muscular, etc.), es ciertamente posible que el componente del injerto muscular libre pueda verse afectado, limitando así el potencial de amplificación. Sin embargo, dado que la detección de incluso una sola unidad motora (10-400 μV)59 puede proporcionar la amplificación de las señales nerviosas periféricas, es razonable suponer que el MC-RPNI contendría suficientes unidades motoras dentro de su área más pequeña y definida para facilitar el control del exoesqueleto en esta población. Sin embargo, una limitación significativa del constructo es en aquellas patologías que resultan en una reducción significativa de las neuronas motoras superiores y / o inferiores, como en el accidente cerebrovascular, la lesión de la médula espinal, la atrofia muscular espinal (AME) y la esclerosis lateral amiotrófica (ELA). Sin una población adecuada de fibras nerviosas periféricas para reinervar el MC-RPNI, no puede regenerarse y proporcionar amplificación de señal, lo que lleva a la falla de la construcción. Se están realizando experimentos para determinar la población mínima de fibras nerviosas periféricas funcionales requeridas para la función adecuada de MC-RPNI.
El predecesor de MC-RPNI, el RPNI, ha demostrado un éxito inconmensurable con el control preciso de prótesis motorizadas en sujetos humanos a través de la amplificación y grabación de señales generadas a partir de nervios periféricos transectados. En particular, es capaz de hacerlo en la escala de meses a años sin reoperación o recalibración del dispositivo protésico. Quejas comunes con los métodos actuales de interfaz hombre-máquina para el centro de control del exoesqueleto sobre la contaminación de la señal de la diafonía y la necesidad de una recalibración frecuente en métodos dependientes de EMG26,27,28, y la inestabilidad de la interfaz nerviosa periférica con el tiempo que requiere cirugías secundarias37,39,44 . El MC-RPNI, sin embargo, es capaz de evitar estas complicaciones dada su composición biológica, así como las capacidades de colocación estratégica. Es imperativo establecer una comprensión profunda de esta construcción para allanar el camino para su uso en sujetos humanos y la eventual utilización generalizada de dispositivos de exoesqueleto precisos y confiables en aquellos que viven con debilidad en las extremidades.
Divulgaciones
Los autores no tienen revelaciones.
Agradecimientos
Los autores agradecen a Jana Moon por su gestión experta de laboratorio y asistencia técnica y a Charles Hwang por su experiencia en imágenes. Los experimentos en este documento fueron financiados en parte a través de subvenciones de la Fundación de Cirugía Plástica a SS (3135146.4), así como al Instituto Nacional de Salud Infantil y Desarrollo Humano bajo el número de adjudicación 1F32HD100286-01 a SS, y el Instituto Nacional de Artritis y Enfermedades Musculoesqueléticas y de la Piel de los Institutos Nacionales de Salud bajo el número de adjudicación P30 AR069620.
Materiales
| Name | Company | Catalog Number | Comments |
| #15 Scalpel | Aspen Surgical, Inc | Ref 371115 | Rib-Back Carbon Steel Surgical Blades (#15) |
| 2-N-thin film load cell (S100) | Strain Measurement Devices, Inc | SMD100-0002 | Measures force generated by the attached muscle |
| 4-0 Chromic Suture | Ethicon | SKU# 1654G | P-3 Reverse Cutting Needle |
| 5-0 Chromic Suture | Ethicon | SKU# 687G | P-3 Reverse Cutting Needle |
| 8-0 Monofilament Suture | AROSurgical | T06A08N14-13 | Black polyamide monofilament suture on a threaded tapered needle |
| Experimental Rats | Envigo | F344-NH-sd | Rats are Fischer F344 Strain |
| Fine Forceps - mirror finish | Fine Science Tools | 11413-11 | Fine tipped forceps with mirror finish ideal for handling delicate structures like nerves |
| Fluriso (Isofluorane) | VetOne | 13985-528-40 | Inhalational Anesthetic |
| Force Measurement Jig | Red Rock | n/a | Custom designed force measurement jig that allows for immobilization of hindlimb to allow for accurate muscle force recording |
| MATLAB software | Mathworks, Inc | PR-MATLAB-MU-MW-707-NNU | Calculates active force for each recorded force trace from passive and total force measurements |
| Nicolet Viasys EMG EP System | Nicolet | MFI-NCL-VIKING-SELECT-2CH-EMG | Portable EMG and nerve signal recording system capable of simultaneous 2 channel recordings from nerve and/or muscle |
| Oxygen | Cryogenic Gases | UN1072 | Standard medical grade oxygen canisters |
| Potassium Chloride | APP Pharmaceuticals | 63323-965-20 | Injectable form, 2 mEq/mL |
| Povidone Iodine USP | MediChoice | 65517-0009-1 | 10% Topical Solution, can use one bottle for multiple surgical preps |
| Puralube Vet Opthalmic Ointment | Dechra | 17033-211-38 | Corneal protective ointment for use during procedure |
| Rimadyl (Caprofen) | Zoetis, Inc. | NADA# 141-199 | Injectable form, 50 mg/mL |
| Stereo Microscope | Leica | Model M60 | User can adjust magnification to their preference |
| Surgical Instruments | Fine Science Tools | Various | User can choose instruments according to personal preference or from what is currently available in their lab |
| Triple Antibiotic Ointment | MediChoice | 39892-0830-2 | Ointment comes in sterile, disposable packets |
| Vannas Spring Scissors - 2mm cutting edge | Fine Science Tools | 15000-04 | Curved micro-dissection scissors used to perform the epineurial window |
| VaporStick 3 | Surgivet | V7015 | Anesthesia tower with space for isofluorane and oxygen canister |
| Webcol Alcohol Prep | Coviden | Ref 6818 | Alcohol prep wipes; use a new wipe for each prep |
Referencias
- Andersson, G. S. The burden of musculoskeletal diseases in the United States : prevalence, societal, and economic cost. American Academy of Orthopaedic Surgeons. , (1942).
- Yelin, E. H., Weinstein, S., King, T. The burden of musculoskeletal diseases in the United States. Seminars in Arthritis and Rheumatism. 46 (3), 259-260 (2016).
- McDonald, C. M. Clinical Approach to the Diagnostic Evaluation of Hereditary and Acquired Neuromuscular Diseases. Physical Medicine and Rehabilitation Clinics of North America. 23 (3), 495-563 (2021).
- Sass, F. A., et al. Immunology Guides Skeletal Muscle Regeneration. International Journal of Molecular Sciences. 19 (3), 835 (2018).
- Bruggeman, K. F., et al. Harnessing stem cells and biomaterials to promote neural repair. British Journal of Pharmacology. 176 (3), 355-368 (2019).
- Vijayavenkataraman, S. Nerve guide conduits for peripheral nerve injury repair: A review on design, materials and fabrication methods. Acta Biomaterialia. 106, 54-69 (2020).
- O'Dell, M. W., Lin, C. C., Harrison, V. Stroke rehabilitation: strategies to enhance motor recovery. Annual Review of Medicine. 60, 55-68 (2009).
- Ambrosini, E., et al. The combined action of a passive exoskeleton and an EMG-controlled neuroprosthesis for upper limb stroke rehabilitation: First results of the RETRAINER project. International Conference on Rehabilitation Robotics (ICORR). , 56-61 (2017).
- Veerbeek, J. M., et al. Effects of robot-assisted therapy for the upper limb after stroke. Neurorehabilitation & Neural Repair. 31 (2), 107-121 (2017).
- Heo, P., et al. Current hand exoskeleton technologies for rehabilitation and assistive engineering. Journal of Precision Engineering and Manufacturing. 13 (5), 807-824 (2012).
- Kwakkel, G., Kollen, B. J., Krebs, H. I. Effects of robot-assisted therapy on upper limb recovery after stroke: A systematic review. Neurorehabilitation & Neural Repair. 22 (2), 111-121 (2007).
- Brewer, B. R., McDowell, S. K., Worthen-Chaudhari, L. C. Poststroke Upper Extremity Rehabilitation: A Review of Robotic Systems and Clinical Results. Topics in Stroke Rehabilitation. 14 (6), 22-44 (2007).
- Kalita, B., Narayan, J., Dwivedy, S. K. Development of active lower limb robotic-based orthosis and exoskeleton devices: A systematic review. International Journal of Social Robotics. 13, 775-793 (2021).
- Bosch, T., et al. The effects of a passive exoskeleton on muscle activity, discomfort and endurance time in forward bending work. Applied Ergonomics. 54, 212-217 (2016).
- Secciani, N., et al. A novel application of a surface ElectroMyoGraphy-based control strategy for a hand exoskeleton system: A single-case study. International Journal of Advanced Robotic Systems. 16 (1), 1729881419828197 (2019).
- Bützer, T., et al. PEXO - A pediatric whole hand exoskeleton for grasping assistance in task-oriented training. IEEE 16th International Conference on Rehabilitation Robotics (ICORR). , 108-114 (2019).
- Meeker, C., et al. EMG pattern classification to control a hand orthosis for functional grasp assistance after stroke. IEEE International Conference on Rehabilitation Robotics (ICORR). , 1203-1210 (2017).
- Witkowski, M., et al. Enhancing brain-machine interface (BMI) control of a hand exoskeleton using electrooculography (EOG). Journal of NeuroEngineering and Rehabilitation. 11 (1), 165 (2014).
- Cantillo-Negrete, J., et al. Motor imagery-based brain-computer interface coupled to a robotic hand orthosis aimed for neurorehabilitation of stroke patients. Journal of Healthcare Engineering. 2018, 1624637 (2018).
- Bhagat, N. A., et al. Design and optimization of an EEG-based brain machine interface (BMI) to an upper-limb exoskeleton for stroke survivors. Frontiers in Neuroscience. 10, 122 (2016).
- Habibzadeh Tonekabony Shad, E., Molinas, M., Ytterdal, T. Impedance and noise of passive and active dry EEG electrodes: A review. IEEE Sensors Journal. 20 (24), 14565-14577 (2020).
- Tariq, M., Trivailo, P. M., Simic, M. EEG-based BCI control schemes for lower-limb assistive-robots. Frontiers in Human Neuroscience. 12, 312-312 (2018).
- Gwin, J. T., Ferris, D. High-density EEG and independent component analysis mixture models distinguish knee contractions from ankle contractions. Annual International Conference of the IEEE Engineering in Medicine and Biology Society. 2011, 4195-4198 (2011).
- Tariq, M., Trivailo, P. M., Simic, M. Classification of left and right foot kinaesthetic motor imagery using common spatial pattern. Biomedical Physics & Engineering Express. 6 (1), 015008 (2019).
- Ryser, F., et al. Fully embedded myoelectric control for a wearable robotic hand orthosis. iInternational Conference on Rehabilitation Robotics (ICORR). , 615-621 (2017).
- Reeves, J., Starbuck, C., Nester, C. EMG gait data from indwelling electrodes is attenuated over time and changes independent of any experimental effect. Journal of Electromyography and Kinesiology. 54, 102461 (2020).
- Huang, J., et al. Control of upper-limb power-assist exoskeleton using a human-robot interface based on motion intention recognition. IEEE Transactions on Automation Science and Engineering. 12 (4), 1257-1270 (2015).
- Rodrigues, C., et al. Comparison of intramuscular and surface electromyography recordings towards the control of wearable robots for incomplete spinal cord injury rehabilitation. 2020 8th IEEE RAS/EMBS International Conference for Biomedical Robotics and Biomechatronics (BioRob). , 564-569 (2020).
- Rasool, G., et al. Spatial analysis of multichannel surface EMG in hemiplegic stroke. IEEE Transactions on Neural Systems and Rehabilitation Engineering : A Publication of the IEEE Engineering in Medicine and Biology Society. 25 (10), 1802-1811 (2017).
- Stieglitz, T., et al. Non-invasive measurement of torque development in the rat foot: measurement setup and results from stimulation of the sciatic nerve with polyimide-based cuff electrodes. IEEE Transactions on Neural Systems and Rehabilitation Engineering. 11 (4), 427-437 (2003).
- Polasek, K. H., et al. Human nerve stimulation thresholds and selectivity using a multi-contact nerve cuff electrode. IEEE Transactions on Neural Systems and Rehabilitation Engineering. 15 (1), 76-82 (2007).
- Kenney, L., et al. An implantable two channel drop foot stimulator: initial clinical results. Artificial Organs. 26 (3), 267-270 (2002).
- Ortiz-Catalan, M., et al. Patterned stimulation of peripheral nerves produces natural sensations with regards to location but not quality. IEEE Transactions on Medical Robotics and Bionics. 1 (3), 199-203 (2019).
- Boretius, T., et al. A transverse intrafascicular multichannel electrode (TIME) to interface with the peripheral nerve. Biosensors and Bioelectronics. 26 (1), 62-69 (2010).
- Petrini, F. M., et al. Six-month assessment of a hand prosthesis with intraneural tactile feedback. Annals of Neurology. 8 (1), 137-154 (2019).
- Jung, R., et al. Bionic intrafascicular interfaces for recording and stimulating peripheral nerve fibers. Bioelectronics in Medicine. 1 (1), 55-69 (2017).
- Christensen, M. B., et al. The foreign body response to the Utah Slant Electrode Array in the cat sciatic nerve. Acta Biomaterialia. 10 (11), 4650-4660 (2014).
- Zollo, L., et al. Restoring tactile sensations via neural interfaces for real-time force-and-slippage closed-loop control of bionic hands. Science Robotics. 4 (27), (2019).
- George, J. A., et al. Long-term performance of Utah slanted electrode arrays and intramuscular electromyographic leads implanted chronically in human arm nerves and muscles. Journal of Neural Engineering. 17 (5), 056042 (2020).
- Wendelken, S., et al. Restoration of motor control and proprioceptive and cutaneous sensation in humans with prior upper-limb amputation via multiple Utah Slanted Electrode Arrays (USEAs) implanted in residual peripheral arm nerves. Journal of NeuroEngineering and Rehabilitation. 14 (1), 121 (2017).
- Yang, Z., et al. Noise characterization, modeling, and reduction for in vivo neural recording. Proceedings of the 23rd Annual Conference on Neural Information Processing Systems (NIPS 09). , 2160-2168 (2009).
- Ursu, D. C., et al. In vivo characterization of regenerative peripheral nerve interface function. Journal of Neural Engineering. 13 (2), 026012 (2016).
- Lotti, F., et al. Invasive intraneural interfaces: Foreign body reaction issues. Frontiers in Neuroscience. 11, 497-497 (2017).
- Stiller, A. M., et al. A meta-analysis of intracortical device stiffness and its correlation with histological outcomes. Micromachines. 9 (9), 443 (2018).
- Kung, T. A., et al. Regenerative peripheral nerve interface viability and signal transduction with an implanted electrode. Plastic and Reconstructive Surgery. 133 (6), 1380-1394 (2014).
- Kubiak, C. A., Kemp, S. W. P., Cederna, P. S. Regenerative peripheral nerve interface for management of postamputation neuroma. JAMA Surgery. 153 (7), 681-682 (2018).
- Vu, P. P., et al. A regenerative peripheral nerve interface allows real-time control of an artificial hand in upper limb amputees. Science Translational Medicine. 12 (533), (2020).
- Svientek, S. R., et al. Fabrication of the composite regenerative peripheral nerve interface (C-RPNI) in the adult rat. Journal of Visualized Experiments: JoVE. (156), e60841 (2020).
- Ursu, D., et al. Adjacent regenerative peripheral nerve interfaces produce phase-antagonist signals during voluntary walking in rats. Journal of NeuroEngineering and Rehabilitation. 14 (1), 33 (2017).
- Vu, P. P., et al. Closed-loop continuous hand control via chronic recording of regenerative peripheral nerve interfaces. IEEE Transactions on Neural Systems and Rehabilitation Engineering. 26 (2), 515-526 (2018).
- Urbanchek, M. G., et al. Development of a Regenerative Peripheral Nerve Interface for Control of a Neuroprosthetic Limb. BioMed Research International. 2016, 5726730 (2016).
- Kubiak, C. A., et al. Physiologic signaling and viability of the Muscle Cuff Regenerative Peripheral Nerve Interface (MC-RPNI) for intact peripheral nerves. Journal of Neural Engineering. 18 (4), (2021).
- Rocha, J. A., et al. Diagnostic investigation and multidisciplinary management in motor neuron disease. Journal of Neurology. 252 (12), 1435-1447 (2005).
- Haastert, K., et al. Nerve repair by end-to-side nerve coaptation: histologic and morphometric evaluation of axonal origin in a rat sciatic nerve model. Neurosurgery. 66 (3), 567-576 (2010).
- Hayashi, A., et al. Collateral sprouting occurs following end-to-side neurorrhaphy. Plastic and Reconstructive Surgery. 114 (1), 129-137 (2004).
- Hu, Y., et al. Regenerative peripheral nerve interface free muscle graft mass and function. Muscle & Nerve. 63 (3), 421-429 (2021).
- Carr, M. M., et al. Strain differences in autotomy in rats undergoing sciatic nerve transection or repair. Annals of Plastic Surgery. 28 (6), 538-544 (1992).
- Sporel-Özakat, R. E., et al. A simple method for reducing autotomy in rats after peripheral nerve lesions. Journal of Neuroscience Methods. 36 (2), 263-265 (1991).
- Lemon, R. N., Mantel, G. W. H., Rea, P. A. Recording and identification of single motor units in the free-to-move primate hand. Experimental Brain Research. 81 (1), (1990).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados