Method Article
Instrumentación de Ovejas fetal Cerca plazo para multivariados Grabaciones no anestesiados crónicas
En este artículo
Resumen
El modelo de oveja fetal no anestesiado instrumentado crónicamente se utiliza para estudiar el desarrollo del feto humano en la salud y la enfermedad, ya que permite la colocación quirúrgica y el mantenimiento de los catéteres y electrodos, muestreo de sangre repetitivo, la inyección de sustancias, registro de la actividad bioeléctrica, y de imágenes in vivo. Se describen los procedimientos necesarios para establecer este modelo.
Resumen
The chronically instrumented pregnant sheep has been used as a model of human fetal development and responses to pathophysiologic stimuli such as endotoxins, bacteria, umbilical cord occlusions, hypoxia and various pharmacological treatments. The life-saving clinical practices of glucocorticoid treatment in fetuses at risk of premature birth and the therapeutic hypothermia have been developed in this model. This is due to the unique amenability of the non-anesthetized fetal sheep to the surgical placement and maintenance of catheters and electrodes, allowing repetitive blood sampling, substance injection, recording of bioelectrical activity, application of electric stimulation and in vivo organ imaging. Here we describe the surgical instrumentation procedure required to achieve a stable chronically instrumented non-anesthetized fetal sheep model including characterization of the post-operative recovery from blood gas, metabolic and inflammation standpoints.
Introducción
Una variedad de modelos animales existe para el estudio de ambos embarazos normales y comprometidos, incluyendo roedores de laboratorio, primates no humanos y los rumiantes domésticos. 1,2,3,4,5 El ovejas gestantes instrumentado crónicamente ha sido ampliamente utilizado durante 50 años como un modelo de desarrollo fetal humano y las respuestas a los estímulos fisiopatológicos tales como lipopolisacárido (LPS). 10.06 Las lesiones después de la exposición LPS imitan exactamente lo que se ve en los recién nacidos prematuros con leucomalacia periventricular, que se debe a un perfil de maduración similar de ambas especies. 11, 12
Otras complicaciones del embarazo también se han estudiado con gran detalle, como el descubrimiento de que los glucocorticoides prenatales promueven el desarrollo pulmonar 13-15 y comprender el impacto de la restricción del crecimiento intrauterino (RCIU) en el feto 16,17.
El uso extensivo del modelo de oveja fetal se debe a la unique amenability de la oveja fetal no anestesiado a la colocación y el mantenimiento de catéteres y electrodos quirúrgica, lo que permite el muestreo de sangre repetitivo, registro de la actividad bioeléctrica, la aplicación de la estimulación eléctrica y en imágenes del cerebro vivo. 18 de telemetría también es posible, aunque se usa con menos frecuencia sin embargo, debido a la sofisticación más alta para establecer, así como el coste inicial y de mantenimiento. 19
Por otra parte, el modelo de oveja fetal es muy versátil ya que son posibles muchas variaciones de la instrumentación en función de las medidas de interés. Por ejemplo, es posible grabar más de días a semanas señales multivariados en tiempo real tales como los movimientos fetales de respiración, la actividad eléctrica cerebral, respuestas cardiovasculares, electrocardiograma, el flujo sanguíneo regional a una serie de órganos usando sondas de flujo o microesferas, etc. Gracias a esta versatilidad, se han llevado a cabo una amplia gama de estudios que incluye el desarrollo de la cardisistema medades 20,21, (HPA) del eje hipotálamo-pituitario-adrenal 22, el desarrollo del cerebro y el desarrollo de 23 estados del sueño, en particular, de 24 años, los efectos de la hipoxia / asfixia 25, la hipotermia terapéutica 26, inflamación 6-11, combinación de ambos de 27 años, los glucocorticoides 28,29, antidepresivos 30, displasia broncopulmonar (DBP) 31,32, la programación fetal 33,34,35,36,37,38,39 o el desarrollo de modalidades de monitoreo fetal novela antes y durante el parto, por nombrar sólo pocas áreas de investigación. 40,41,42,43
El objetivo general del método presentado es mostrar la aplicación básica de este modelo versátil. Permite establecer una amplia variedad de protocolos experimentales agudos y crónicos que estudian la fisiología y la fisiopatología fetal en el integrador, órgano, los niveles celular y molecular.
Protocolo
Cuidado de los animales a las directrices del Consejo Canadiense de los Animales y la aprobación por el Consejo de Montréal Universidad de los Animales (protocolo nº 10-Rech-1560). La información detallada sobre los materiales y métodos utilizados se proporciona en la Tabla 1.
1. Anestesia
- Insertar un catéter de un solo lumen en una vena yugular.
- Sedate la oveja usando acepromacina (Atravet 10 mg / mL) 2 mg por vía intravenosa aproximadamente 30 min antes de la inducción de la anestesia con el fin de reducir el estrés asociado con el procedimiento que a su vez reduce los niveles de cortisol.
- Administrar diazepam (Diazepam 5 mg / ml) 20 mg, ketamina (Ketalar 100 mg / mL) 4-5 mg / kg y propofol (Propofol 10 mg / ml) 0,5 a 1 mg / kg por vía intravenosa para inducir la anestesia general.
- Inserte un catéter de intercambio de la vía aérea en la tráquea utilizando un laringoscopio con un tipo de hoja de Wisconsin (extralargas 350 mm Zurdo hoja) para ayudar con la intubación. Deslizar el tubo endotraqueal de silicio (diámetro de 9 a 12 mm Interior) fuera del catéter de cambio y de las vías respiratorias dentro de la tráquea. Esta técnica facilita el proceso de intubación. Inflar el manguito del tubo endotraqueal con cuidado para evitar la ulceración inducida por la presión de la tráquea y fijar el tubo en la cabeza de la oveja.
- Conecte el tubo endotraqueal al circuito respiratorio de la máquina de anestesia y comenzar la ventilación mecánica inmediatamente. Ajustar la configuración de ventilador para mantener una P a CO 2 dentro de los límites normales de 35 a 45 mmHg.
- Insertar un catéter en la arteria auricular (22 a 20 G; 1 en [0,9 x 25 mm] a 1,16 en [1,1 x 30 mm]) y conectarse a la tubería no conforme para supervisar la presión sanguínea arterial directa.
- Utilice un monitor fisiológico multiparamétrico para registrar el electrocardiograma, presión arterial directa, la saturación de oxígeno (SpO 2), capnografía (PETCO2), y la temperatura cada 5 minutos. Transferir todas phdatos ysiologic a través de un cable serie a un equipo de recolección de datos fisiológicos central. Mantenga la temperatura normal del cuerpo utilizando una manta de agua circulante.
- Administrar una solución de poli-iónico equilibrada a 10 ml / kg para la primera hora de la anestesia general y luego reducir a 5 mL / kg / h.
- Administrar trimetoprim-sulfadoxina 5 mg / kg IV de la oveja justo antes de la incisión de la piel como la profilaxis antibiótica.
- Utilizar técnicas asépticas estándar con todas las manipulaciones quirúrgicas de la oveja y el feto.
- Barrera enfermera las ovejas en todo momento. Esto incluye también el personal no quirúrgicos. Esto minimizará el potencial enzoótica para, por ejemplo, Coxiella burnetii. Utilice guantes y máscaras (N-95 tipo) en todo momento.
2. Descripción del Procedimiento Quirúrgico
- Haga una 20 cm incisión a través de la pared abdominal inferior inmediatamente craneal a la ubre a través de la línea alba para minimizar el daño del músculo abdominal.
- Retract epiplón mayor craneal y los cuernos uterinos se palpan manualmente. Palpar cada cuerno del cuerpo del útero a la punta del cuerno notar el número de fetos y su tamaño. Si hay más de un feto, elegir el feto más grande mediante la evaluación manualmente el tamaño de la cabeza y la anchura entre las órbitas.
- Sostenga la cabeza del feto elegido firmemente a través del útero parcialmente exteriorizado. Realice una histerotomía 10 cm en la gran curvatura con tijeras Metzenbaum. Poner inmediatamente sobre la cabeza de un guante quirúrgico estéril sin látex lleno con solución salina estéril como si fuera una mano. Como alternativa, utilice los 4x4 humedecidas para mantener la cabeza del feto húmedo. Asegure el útero a la pared abdominal.
- Exteriorizar los derecho e izquierdo miembros torácicos y tire suavemente el feto fuera del útero hasta el proceso xifoides.
- Inserte catéteres de polivinilo en la vena braquial derecha y la izquierda y las arterias utilizando una técnica de corte hacia abajo estándar. Inserte another de polivinilo catéter en la cavidad amniótica por fijando su extremo con el esternón del feto.
- Utilice sólo catéteres estériles. Se recomienda la esterilización de gas en su instalación estándar. Adjuntar cada catéter a una aguja y la aguja a una doble llave de paso para permitir el muestreo de sangre posterior o monitorización de la presión.
- Sutura electrodos de acero inoxidable a la manubrio, apéndice xifoides y para cada punto del hombro para vigilar el electrocardiograma (ECG).
- Volver al feto en el útero. Todos los catéteres y electrodos de salida a través de una pequeña incisión en el flanco izquierdo.
- Cierre la incisión de laparotomía usando un cierre de tres capas. Suturar la pared abdominal con una sutura de monofilamento sintético absorbible USP 2 en una manera simple continua. Cierre el espacio subcutáneo con una sutura trenzada absorbible sintético USP 0 en una sencilla forma continua. Utilice grapas de acero inoxidable quirúrgicas para cerrar la incisión de la piel.
- Descripción detallada del procedimiento quirúrgico
- Retire la lana por el afeitado el proceso xifoides a la glándula mamaria y largo del pliegue del flanco en cada lado con una hoja # 40. Limpie el abdomen ventral a continuación a fondo con un gluconato de clorhexidina al 4% y un cepillo suave durante 3 min.
- Realizar un lavado estéril estándar con gluconato de clorhexidina al 4% a partir del centro del abdomen y progresando de manera centrífuga durante 3 min. Vierta solución salina estéril en el abdomen para quitar el jabón desinfectante. Para la etapa final de la preparación quirúrgica, realizar tres pasajes alternos de solución de gluconato de clorhexidina al 2% y alcohol isopropílico al 70%.
- Asegúrese de que la profundidad de la anestesia es la adecuada antes de la incisión. Hacer una incisión de laparotomía estándar desde el ombligo hasta justo craneal a la ubre a través de la línea alba para minimizar el daño del músculo abdominal.
- Inserte un largo fórceps de esponja en el abdomen a lo largo de la pared abdominal izquierda arribaal sitio de salida prevista para los catéteres en la región paracostal.
- Empuje la punta de la pinza contra la pared hasta que un asistente puede localizarlo y confirmar el lugar apropiado. Abra ligeramente (1 cm) las mandíbulas de las pinzas y dejar que el asistente crea un 2 cm incisión de espesor total.
- Exteriorizar las puntas de las pinzas a través de la incisión, abrirá de nuevo, y agarre suavemente los catéteres con las pinzas que finalmente se retiró del abdomen a través de la incisión abdominal ventral. Es de destacar que algunos grupos implantan los catéteres y luego exteriorizan ellos. Esto tiene el inconveniente de que la monitorización del ECG fetal intraoperatorio no es posible.
- Palpar el útero para determinar la posición y los números fetal. Determinar el mayor feto utilizando la distancia inter-aural. Incisión en la pared uterina en la gran curvatura sobre el dorso de la cabeza, evitando los cotiledones.
- Inserte una cánula de extremo romo a través de las membranas de la placenta para obtener un ammuestra gratis por hemorragia fluido niotic. Incisión en las membranas de la placenta con unas tijeras.
- Exteriorizar la media craneal del feto a través de esta incisión. Coloque un guante quirúrgico de látex no estéril lleno de solución salina estéril a 37 ° C sobre la cabeza del feto para ayudar a mantener la normotermia.
- Durante la retirada de la parte superior del cuerpo del feto desde el útero, tienen el asistente que mantenga arriba de la Babcock para evitar la pérdida de líquido amniótico. Entonces, de nuevo utilizando fórceps Babcock, sujetar las membranas fetales y pared uterina a la piel para evitar la contaminación abdominal con líquido amniótico.
- Expose sólo las partes del cuerpo fetal que necesitan ser instrumentado y mantener las partes restantes dentro del útero o cubiertos por paños estériles húmedas y calientes (37 ° C), respectivamente.
- Secuestrar a ambos miembros torácicos para facilitar la exposición a la arteria braquial y la vena bilateralmente. Una incisión a lo largo de la cara medial de ambos antebrachium y cuidadodiseccionar completamente alrededor de la arteria braquial y la vena.
- Inserte catéteres de polivinilo en el derecho y las arterias braquial izquierda y el brazo izquierdo de la vena utilizando una técnica de corte hacia abajo estándar.
- Libertad para los buques que se cateterizó del tejido adyacente más de 1 cm. Ligar la porción distal del vaso con un trenzado de sutura absorbible sintética de 2-0 USP. Preplace una ligadura en el aspecto proximal del vaso pero mantenerlo no condicionada.
- Con unas tijeras Castroviejo, cortar transversalmente el recipiente a aproximadamente el 30% de su diámetro. Detenga el flujo de sangre parcialmente tirando de la sutura proximal. Insertar el catéter en una dirección proximal.
- Inserte el catéter de polivinilo hasta 8 cm proximal o hasta que se detecta la resistencia y luego tire un poco hacia atrás. Temporalmente asegurar el aspecto proximal del catéter utilizando una pinza vascular. Coloque otra sutura alrededor tanto en el aspecto proximal y distal del catéter. Un asistente está continuamente aspirating y el lavado del catéter para asegurar la permeabilidad del catéter.
- Cierre la piel fetal utilizando una sutura sintética absorbible trenzada USP 2-0, con un patrón de sutura continua.
- Libertad para los buques que se cateterizó del tejido adyacente más de 1 cm. Ligar la porción distal del vaso con un trenzado de sutura absorbible sintética de 2-0 USP. Preplace una ligadura en el aspecto proximal del vaso pero mantenerlo no condicionada.
- A la derecha y el hombro izquierdo, manubrio y el proceso xifoides, fijar un electrodo de acero inoxidable aislado para facilitar el seguimiento del ECG fetal.
- Suturar la presión amniótico y el catéter de muestreo hasta el esternón. Este catéter está fenestrado en su extremidad.
- Asegure todos los catéteres en el dorso del feto usando un material trenzado sutura sintética absorbible USP 2-0.
- Antes de la sustitución del feto de nuevo en el útero, administrar clenbuterol 30 mg IV lentamente durante 15 min para evitar la hipotensión y para proporcionar relajación uterina.
- Suturar las membranas fetales usando USP 4-0 material de sutura absorbible sintética trenzada con un patrón continuo. Incorporar un solo catéter o electrodo a la vez en los closure para asegurar un cierre estanco. Utilice un patrón de doble capa de Cushing respetando principios Halsted para cerrar la capa muscular del útero mediante un trenzado de material de sutura absorbible sintética USP 0. Denunciar los nudos quirúrgicos con cuidado.
- El uso de un patrón de sutura en bolsa de tabaco, asegurar todos los catéteres y cables de ECG cuando se aproximan a la incisión paracostal izquierda.
- El uso de un monofilamento sintético material de sutura absorbible USP 2 asegurar la línea alba con un patrón continuo. Cierre los tejidos subcutáneos utilizando USP 2-0 trenzado material de sutura absorbible sintética con un patrón continuo. Asegure la capa de la piel con grapas quirúrgicas.
- Administrar 250 mg de ampicilina por vía intravenosa y de nuevo a través del catéter amniótico en la cavidad amniótica. Reemplazar los líquidos perdidos amniótico con solución salina tibia.
- Coloque todos los catéteres exteriorizados y electrodos de ECG en una bolsa de lugar para mantener la esterilidad. Coloque un jersey alrededor del torso de la oveja para asegurar toda la una catéteresd electrodos en el cuerpo de la oveja.
- Deje de anestesia general, y retirar la intubación la oveja vez reflejos laríngeos han vuelto a la normalidad.
- Volver a la oveja a una jaula metabólica una vez que ella es estable después de la anestesia general. La oveja residirá en la jaula metabólica durante la duración del experimento. La oveja debe ser capaz de pararse, acostarse y comer a voluntad mientras se controla el feto no anestesiados sin sedante a la madre.
- Para los siguientes tres días, administrar antibióticos de forma profiláctica a la oveja (Trimetoprim sulfadoxina 5 mg / kg) y el feto (250 mg de ampicilina por vía intravenosa y de nuevo a través del catéter amniótico).
- Evaluar el estado metabólico de tanto oveja y el feto mediante análisis de sangre de gas.
- Lave todos los catéteres con el volumen mínimo de solución salina heparinizada posible. Precaución - no exceda la dosis diaria de heparina y fluidos permisible para el feto. Es posible fluido sobrecargar el feto. Flush lentamente una vezun día ~ 5 ml de NaCl por línea después de la profilaxis antibiótica.
- Retire la lana por el afeitado el proceso xifoides a la glándula mamaria y largo del pliegue del flanco en cada lado con una hoja # 40. Limpie el abdomen ventral a continuación a fondo con un gluconato de clorhexidina al 4% y un cepillo suave durante 3 min.
- Grabación y análisis de datos
- Durante la cirugía, opcionalmente registrar las tasas de ECG y del corazón de la madre y del feto, así como la presión arterial de la madre y la presión de la vía aérea (Paw) de forma continua (Figura 1). Utilice la ventana Monitor de vida para adquirir todos los datos maternos excepto ECG. Alimente estos datos en convertidor analógico-digital, junto con las señales de ECG fetal y materna; pasar ECG materno y fetal por primera vez en 1,901 mil pre-amplificador. Grabar y visualizar todos los datos en el software del fabricante.
- Tomar una muestra arterial 1 ml al mismo tiempo de la oveja y el feto para el análisis de gases en sangre arterial, lactato, glucosa y basar el exceso de determinación (en el plasma) en el inicio de la cirugía fetal (inmediatamente después de insertar el primer catéter arterial) y después de cerrar el útero .
- Durante la recuperación postoperatoria, tomar un 3 ml de muestra de sangre fetal para medir la IL-6 y TNF-α inflammperfiles Atory. Centrifugar el plasma a 4 ° C (4 min, 4000 xg), se decanta y almacenar el plasma a -80 ° C para la prueba de ELISA subsiguiente.
Nota: A los efectos de los resultados representativos reportados, seis días después de la cirugía los animales fueron sacrificados mediante la inyección intravenosa de pentobarbital sódico 20 ml. El crecimiento fetal se evaluó por el cuerpo, el cerebro, el hígado y pesos maternas. La duración del período experimental, obviamente, varían en función del diseño elegido para la pregunta de investigación particular y puede alcanzar ~ 6 semanas.
- Análisis de citoquinas (paso opcional)
- Determinar las concentraciones de citoquinas (IL-6, TNF-alfa) en el plasma utilizando un sándwich ELISA específico ovina. Anticuerpos monoclonales anti-oveja Pre-capa de ratón (anticuerpo de captura IL-6) o anticuerpo monoclonal de ratón anti-bovina (TNF-α) a una concentración 4 g / ml en la placa de ELISA a 4 ° C para O / N, después 3 veces lavar con tampón de lavado (0,05% Tween 20 en PBS, PBST).
- Bloquear las placas durante 1 h con 1% de BSA en PBST. Lavar las placas con tampón de lavado 3 veces.
- Utilice proteínas recombinantes ovejas (IL-6, TNF-alfa) como estándar ELISA, se preparan unas diluciones seriadas van desde estándar de 1 de 2.000 ng / ml a nivel 7 de 31,25 pg / ml.
- Carga de 50 l de estándares de proteína diluidas en serie y muestras por pocillo e incubar durante 2 horas a RT, se lavan las placas 3 veces. Ejecutar todos los estándares y las muestras por duplicado.
- Aplicar 50 l de anticuerpos policlonales de conejo anti-oveja (anticuerpo de detección IL-6) o anticuerpo policlonal de conejo anti-bovina (TNF-a) a una dilución de 1: 250 en pocillos e incubar durante 30 min a TA. Lavar las placas con tampón de lavado 5 veces.
- Añadir 50 l de la cabra anti-IgG de conejo conjugado con HRP (dilución 1: 5000) durante 30 min.
- Incubar con 50 l de solución de sustrato TMB por pocillo.
- Detener la reacción desarrollo de color a tiempo deseado con 25 l de 2 N de ácido sulfúrico.
- Lea la plates en ELISA lector de placas a 450 nm, con una corrección de longitud de onda 570 nm.
Nota: En nuestros ensayos, la sensibilidad de IL-6 ELISA fue de 16 pg / ml, la sensibilidad de TNF-ELISA fue de 13,9 pg / ml, respectivamente. Para todos los ensayos, los intra-ensayo e inter-ensayo coeficientes de variación fue <5% y <10%, respectivamente.
- Análisis estadístico
Nota: Los métodos estadísticos exactos dependerán de la pregunta de investigación. Aquí mostramos los métodos utilizados para la prueba de diferencias significativas en los gases en sangre reportados en la Tabla 2.- Pon a prueba la distribución normal de datos mediante la prueba de Kolmogorov-Smirnov, seguido de pruebas paramétricas o no paramétricas con ajuste para comparaciones múltiples, según corresponda.
- Use K-means análisis de conglomerados para identificar los fetos en la cohorte que eran espontáneamente hipóxica y determinar los respectivos valores de pO 2 y O 2 Sab (considere pO2 <20 mmHg o O 2 sáb <55% como fetal hipoxia). 44-48 de
- Utilice el software estadístico como SPSS para el análisis.
- Los datos actuales como media ± SD con diferencias estadísticas en p <0,05 consideró significativo.
Resultados
38 ovejas con plazos de fecha embarazadas fueron instrumentados a 128 ± 2 días de gestación (DGA, ~ 0,88 gestación, plazo 145 DGA) con arterial, venosa y catéteres amniótico y el electrocardiograma (ECG) electrodos con una técnica estéril bajo anestesia general (tanto oveja y el feto ). En caso de embarazo gemelar feto grande fue elegido en base a la palpación y estimar el diámetro intertemporal; alternativamente, el feto a ser instrumentada puede ser seleccionado al azar para evitar cualquier sesgo potencial o ambos fetos puede ser instrumentado. La duración total del procedimiento fue de 124 ± 27 min. La porción de la parte superior del cuerpo del feto a ser instrumentado permaneció fuera del útero de 92 ± 19 min. La mayoría de las ovejas instrumentados eran animales F2. Su presa era F1 (Border Leicester * Romanov) y el padre era un carnero Hampshire; se cruzaron como sigue: Hampshire (50%) - Border Leicester (25%) - Romanov (25%) = HABLRV.
Materna Representante y fisiológica del fetocaracterísticas durante la cirugía y la instrumentación se muestran en la Figura 1 y se encontraban dentro de la norma fisiológica para la edad gestacional del feto y la conducta maternal durante la anestesia.
Maternas pesos promedio de 75 ± 11 kg y 21 de 38 gemelos realizados (es decir, a una velocidad de 1,6 ± 0,5). En el momento de la necropsia (134 ± 3 DGA), entre los fetos únicos instrumentados pesó 4.090 ± 800 g, mientras que el peso gemelos era más baja en 3.300 ± 740 g (p = 0,003). El peso de los gemelos no instrumentado en 3300 ± 670 g fue similar al peso de los gemelos instrumentados (p = 0,78). 18 de los fetos instrumentados eran mujeres y 20 eran hombres.
La dinámica de los gases en sangre arterial fetal, glucosa y ácido-base de estado durante la cirugía y la recuperación después de la operación se presentan en la Tabla 1. Se observó una recuperación gradual del estado ácido-base fetal y un deterioro moderado de la oxigenación con pocos cambios en glucose y electrolitos del día después de la operación 1 a 3. En particular, en el día después de la operación 3, 42% de los fetos resultaron ser espontánea hipóxica con arterial pO2 11 mmHg de y O 2 sáb del 28%. Del clúster normóxico pO fetal 2 tuvo su epicentro a 22 mmHg y O 2 sáb 56%. Fetos Gemelas no fueron más hipóxica de fetos únicos (p = 0,26).
Arterial Fetal IL-6 ELISA rindió valores por debajo del umbral de sensibilidad de 16 pg / ml durante todo el período de recuperación post-operatoria. Del mismo modo, los niveles de TNF-α también se mantuvo sin cambios y muy baja a 29 pg / ml con ~ 30% de los animales también muestran valores por debajo del umbral de sensibilidad de 13,9 pg / ml durante todo el período de recuperación post-operatoria.
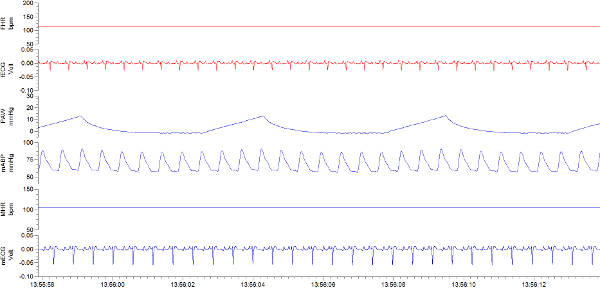
Figura 1. vigilancia materna y fetal intraoperatoria. FHR, i la frecuencia cardíaca fetaln latidos por minuto (lpm); fECG, electrocardiograma fetal (V); PAW, presión positiva de la vía aérea materna (mmHg); PAM, presión arterial materna (mmHg); MHR, la frecuencia cardíaca materna (bpm); mECG, ECG materno (V). El eje X es la escala de tiempo en el formato hh: mm:. Ss Por favor haga clic aquí para ver una versión más grande de esta figura.

Figura 2. espontánea hipoxia y el peso corporal fetal. No hay relación entre el peso corporal fetal y arterial PO 2 en el día después de la operación 3 se detectó (Spearman R = 0,326, p = 0,161). Haga clic aquí para ver una versión más grande de esta figura .
| Fuente ACE Luz | Schott-Fostec | A20500 | |
| Tijeras de disección | Ciencia Herramientas de Bellas | 14060-11 | |
| Tijeras de disección en ángulo | Ciencia Herramientas de Bellas | 15006-09 | |
| Mango de bisturí | Ciencia Herramientas de Bellas | 10003 - 12 | herramienta de disección alternativa |
| Hojas de bisturí curvas # 12 | Ciencia Herramientas de Bellas | 10012-00 | herramienta de disección alternativa |
| Tijeras de hueso | Ciencia Herramientas de Bellas | 16044 - 10 | |
| C & T de sutura atar fórceps | Ciencia Herramientas de Bellas | 00272-13 | |
| Pinzas Dumont SS - ángulo | Ciencia Herramientas de Bellas | 11203-25 | |
| Seda trenzada tamaño de sutura 6-0 | Teleflex Medical | 07 -30 de - 10 | |
| Cinta Médica | Transpore | 3M | |
| El clorhidrato de ketamina 100 mg / ml | Hospira | NDC 0409 - 2051 - 05 | Final no es de 80 mg / kg |
| Tranqui Ved Inyección (xilazina 100 mg / ml) | Vecdo | NDC 50989 - 234 - once | Final no es de 10 mg / kg |
| Naranja reactivo 14 | Sigma - Aldrich | R - 8254 | |
| Componentes de la solución de Ringer | Solución de gas se equilibra con 95% de O2 y 5% de CO2, pH final 7,4 | ||
| Cloruro de sodio | Sigma - Aldrich | S7653 | Concentración final: 118 mM |
| Cloruro de potasio | Fisher Scientific | P217 - 3 | Concentración final: 4,7 mM |
| El cloruro de calcio dihydrate | Fisher Scientific | C79 - 500 | Concentración final: 2,5 mM |
| Fosfato de potasio monobásico | Fisher Scientific | P -285 | Concentración final: 1,2 mM |
| Sulfato de magnesio | JT Baker | Ene-00 | Concentración final: 0,57 mM |
| 4- (2-hidroxietil) piperazina-1-etanosulfónico (HEPES) | Fisher Scientific | BP 310-500 | Concentración final: 5,95 g / L |
| Glucosa | Sigma - Aldrich | G8270 | Concentración final: 5,5 mM |
| LifeWindow | Digicare Tecnología Biomédica | ||
| CED bioamplificador y ADC unidades | Cambridge Electronic Design Limited, Unidad 4, Parque de las Ciencias, Milton Road, Cambridge CB4 0FE INGLATERRA. | BioAmp: 1902; ADC: Micro1401; Software de adquisición de datos: Punto 2, V7.13 | |
| Neurolog bioamplificador señal analógica | Digitimer Ltd 37 Hydeway Welwyn Garden City Hertfordshire, AL7 3BE, Inglaterra | NL108A | |
| ABL800Flex | Radiómetro Canadá; 200 Aberdeen Dr, London, ON N5V 4N2 | ||
| Eppendorf 5804R | Eppendorf Canadá; 2810 Argentia Road, # 2 Mississauga, Ontario, L5N 8l2 | ||
| Arrow yugular Cateterismo Set | Arrow International, Inc., 2400 Bernville Road, Reading, PA 19605 EE.UU. | ||
| Atravet | 10 mg / ml | ||
| Diazepam | 5 mg / ml | ||
| La ketamina | Ketalar | 100 mg / ml | |
| Propofol | 10 mg / ml | ||
| SurgiVeT | Tubos endotraqueales; Smiths Medical ASD, Inc. St. Paul, MN 55112, EE.UU. | ||
| Cocine Airway Cambio catéter con adaptadores RAPI-FIT | Cocine Critical Care 750, Bloomington IN 47402-0489 EE.UU. | ||
| Dispomed Ventilador | Dispomed Ltd., 745 Nazaire-Laurin, Joliette, Quebec J6E 0L6 | ||
| BD Insyte-W | Becton Dickinson, Infusión Terapia Systems Inc., 9450 S State St, Sandy Utah 84070 EE.UU. | 22-20 G; 1 en [0,9 x 25 mm] a 1,16 en [1,1 x 30 mm] | |
| Edwards Lifesciences Ref: PX272 kit de monitoreo de presión con TruWave Presión Desechables | |||
| LifeWindow LW6000 | Digicare Biomedical Tecnología 107 Commerce Road, Boynton Beach, FL 33426-9365 EE.UU. | ||
| Gaymar | |||
| Babcock | |||
| Catéteres de polivinilo | SCI (Scientific Commodities Inc.) | 2 metros | |
| 2-0 Vicryl | |||
| Tijeras Castroviejo | |||
| electrocardiograma (ECG) | LifYY, Metrofunk Kabel-Union, Berlín, Alemania | cuatro electrodos de cobre en la envoltura individual, de 2 metros | |
| 2-O Vicryl | |||
| 3-0 Vicryl | |||
| USP PDS II | |||
| Sulfadoxina Trimetoprima | |||
| Ampicilina | |||
| Llave de cierre | Argon Medical, Gato 041220001A | Doble Llave de paso de 4 vías con cierre luer macho | |
| Agujas | Tyco Healthcare 8881202389 | Agujas romas Monoject cubo de aluminio, 22Gx, 0.7mmx 38.1mm: para arterial fetal y catéteres venosos | |
| Agujas | Tyco Healthcare 8881202322 | Monoject cubo de aluminio agujas romas, 16GX, 1.6mmx38.1mm: para catéteres amniótico |
Tabla 1. Específica Reactivos / Equipo.

Por favor, haga clic en élvolver para ver una versión más grande de esta figura.
Tabla 2. Resumen general de la sangre fetal gases, metabolitos y electrolitos durante la cirugía y la recuperación post-operatoria. Fetal arterial pH de la sangre, pCO 2 (mmHg), pO2 (mmHg), la saturación de oxígeno (O 2 sáb%), glucosa (mg / dL), lactato (mmol / L) y el exceso de base (mmol / L) en varios puntos de tiempo de los periodos de instrumentación y recuperación: inicio de la cirugía fetal inmediatamente después de instalar el primer catéter arterial fetal (útero abierto), el fin de la cirugía fetal (útero día cerrado), después de la operación de 1 a 3. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
El anestésico y los procedimientos quirúrgicos se presentan que son necesarios para el establecimiento de un modelo animal para el estudio de la fisiología y la fisiopatología fetal: la oveja fetal no anestesiado instrumentado crónicamente.
Cuatro pasos críticos en el protocolo debe hacerse hincapié. En primer lugar, pasar los catéteres y electrodos a través del flanco materna: es importante que esto se hace a la vez para evitar cualquier lesión de órganos internos. En segundo lugar, fijar el sitio de operación uterotomy antes de exteriorizar el feto: esto es crucial para prevenir o minimizar la pérdida de líquido amniótico y la subsiguiente sutura de la membrana amniótica antes del cierre uterino. Cateterismo Tercero, arterial: las arterias ovejas fetales son alrededor de 1-2 mm de diámetro y por lo tanto, no es difícil de cateterizar por un cirujano experimentado; un equipo de dos cirujanos realiza mejor y más rápida en esta tarea, que ayuda a ahorrar tiempo para minimizar la longitud total del procedimiento. Cuarta cuidado seg,urante y organización de todos los catéteres y electrodos en la cavidad amniótica antes de devolver el feto en el amnios y el cierre del útero: esto ayuda a evitar el tirón accidental de los catéteres o desgarre de los electrodos de ECG debido a los movimientos maternos o fetales después de la cirugía.
En lugar del enfoque aquí presentado a cateterizar vasos braquial, carótida o vasos femorales también se puede utilizar. La elección depende del enfoque global de instrumentación que a su vez será dictada por el diseño del estudio. Recomendamos para minimizar el tiempo el feto pasa fuera del útero y reducir al mínimo el grado en que el feto debe permanecer fuera del útero para ser instrumentado. Estas consideraciones llevaron a la elección de los vasos instrumentados en el presente "enfoque mínima". Recomendamos cateterización arterias en ambos lados para permitir el control de la presión sanguínea intra-arterial y toma de muestras de sangre arterial sin interferencia mutua a lo largo de tque experimentar. Una ventaja añadida es la redundancia a prueba de fallos este enfoque presenta: en caso de una arteria no se bloquean durante el período experimental, el muestreo y control de la presión son posibles desde el mismo recipiente con el inconveniente de interrumpir la supervisión cuando se realiza el muestreo de sangre.
Hay tres limitaciones que impiden una adaptación más amplia de este modelo animal. Estas limitaciones pueden ser abordadas por algunas modificaciones sugeridas a continuación. En primer lugar, es el requisito de nivel de bioseguridad 2 encierros en algunas jurisdicciones. Esto es debido a un riesgo de infección por Coxiella burnetii de oveja embarazada en los seres humanos con un sistema inmunológico debilitado. 49,50 La vacunación está disponible para los animales y los seres humanos expuestos a disminuir este riesgo 51,52 y PCR pruebas se pueden hacer para garantizar que no animales positivos se entregan en el centro de investigación de la granja. Una solución puede ser combinar la vacunación de animales con la prueba de PCR múltiples en la granja de los hisopos vaginales realizados antes de la reproducción comience, antes de la entrega y de nuevo a partir del líquido amniótico durante la cirugía. Con estas precauciones, en algunas jurisdicciones el uso de ovejas en la investigación no se limita ya que es en otros. En segundo lugar, el coste por animal está en el intervalo de cuatro dígitos inferior, comparable a algunas cepas knockout murinos. Teniendo esto en cuenta, sin embargo, el aumento de la información de cada experimento ovejas fetal compara solamente a los primates no humanos en lo que respecta a la extensa cantidad de datos que se puede recoger, las preguntas que se le puede pedir y el potencial de la traducción a la causa humana a la sincronización del desarrollo de órganos en ovejas. En tercer lugar, está el tema de la cría y la disponibilidad de los animales durante ciertas épocas en sólo el año. Incluso con tratamiento hormonal, los resultados de la reproducción de ovejas, como la tasa de embarazo y la vitalidad de los corderos (fetos) son satisfactorios sólo unos meses alrededor temporadas de cría naturales. 53 Por lo tanto, el experimentoAl programación requiere una planificación cuidadosa con los años dividida en una de otoño y primavera temporadas. Una solución puede ser el establecimiento de septiembre a noviembre y una 'oveja' estaciones experimentales de abril a junio. Este problema también es una virtud, ya que permite tiempo para analizar los numerosos datos recogidos durante cada estación experimental.
Hay un número de factores que contribuyen a la importancia con respecto a los métodos existentes. Los datos morfométricos, cardiovasculares y de gases en sangre presentados estaban dentro del rango para las especies 54,55 y se parecen a los de la especie humana 56, una ventaja importante de este modelo animal. Una excepción es la tasa más alta de embarazos múltiples en comparación con el hermanamiento humana. 57 Sin embargo, esto también es una virtud del modelo, como el estudio de los efectos de hermanamiento sobre el desarrollo fetal es una tarea biomédica importante. 55,58,59 Niveles muy bajos de correos inflamación operatorio tal como se mide por la IL-6 y TNF-alfa ELISAscombinado con recuperación del estado ácido-base indican que la instrumentación quirúrgica fetal es bien tolerado y el período de recuperación después de la operación de 72 horas es suficiente para garantizar un estado básico estable de las ovejas del feto antes de comenzar un experimento. Alto porcentaje de espontánea hipoxia crónica moderada en ovejas fetales corto plazo los hace un modelo interesante para el estudio de los efectos crónicos de la hipoxia prenatal humano y la inflamación en el desarrollo fetal y perinatal, como por ejemplo, la restricción del crecimiento intrauterino, y los insultos perinatales, como la inflamación y asfixia aguda. 60,61,62 se utilizan varios modelos ovejas RCIU, algunos depender de la hipoxia espontánea, algunos inducir por embolización de la placenta, por ejemplo. 16,63-66 Por otro lado, la hipoxia severa antes del inicio de un experimento puede También ser un criterio de exclusión en los casos en que, por ejemplo, están a estudiar sistemas nerviosos cardiovasculares o centrales, como en este caso las respuestas de hipoxia crónica fetos unre conocido a diferir de aquellos que son de normoxia. 60 Otra aplicación importante es el estudio de impacto estrés materno prenatal sobre el desarrollo fetal y postnatal. 5,67 Por último, como puede verse en las numerosas publicaciones citadas con este modelo, la instrumentación fetal puede hacerse a través de una amplia gama de edades gestacionales en cualquier lugar de ~ 70-135 dGA correspondiente a mediados de la gestación - Estudios a corto plazo del desarrollo fetal. Con el avance de la edad gestacional, la instrumentación de la cada vez mayor complejidad son posibles, pero las consideraciones de la duración de la necesidad de instrumentación quirúrgica para ser sopesado frente a la necesidad de obtener un número de grabaciones multivariados del mismo feto.
Una serie de muy prometedoras aplicaciones futuras de la técnica presentada se deriva de la cada vez mayor número de reactivos de biología molecular ovejas específico y reciente secuenciación del genoma ovino. Estos desarrollos recientes han promovido aún más este Animal modelo sea un enfoque muy prometedor y de gran alcance para la comprensión del desarrollo del feto humano sano y patológico en diversas escalas de la organización, a partir de (epi) genoma a la fisiología integrativa. 68 69-74
Divulgaciones
No disclosures have been made.
Agradecimientos
authors gratefully acknowledge funding support from the Molly Towell Perinatal Research Foundation, Canadian Institutes of Health Research (CIHR), and Fonds de Recherche du Québec – Santé (FRQS) (to MGF) and CIHR-Quebec Training Network in Perinatal Research (QTNPR) (to LDD).
The authors wish to thank Esther Simard, Marco Bosa, Carl Bernard and Carmen Movila for technical assistance.
Materiales
| Name | Company | Catalog Number | Comments |
| ACE Light source | Schott-Fostec | A20500 | |
| Dissecting scissors | Fine Science Tools | 14060 - 11 | |
| Angled dissecting scissors | Fine Science Tools | 15006 - 09 | |
| Scalpel handle | Fine Science Tools | 10003 - 12 | alternating dissecting tool |
| Curved scalpel blades #12 | Fine Science Tools | 10012 - 00 | alternating dissecting tool |
| Bone scissors | Fine Science Tools | 16044 - 10 | |
| S & T suture tying forceps | Fine Science Tools | 00272 - 13 | |
| Dumont SS forceps - angled | Fine Science Tools | 11203 - 25 | |
| Braided silk suture size 6-0 | Teleflex Medical | 07 - 30 - 10 | |
| Medical Tape | transpore | 3M | |
| Ketamine hydrochloride 100 mg/ml | Hospira | NDC 0409 - 2051 - 05 | Final Does is 80 mg/kg |
| Tranqui Ved Injection (xylazine 100 mg/ml) | Vecdo | NDC 50989 - 234 - 11 | Final Does is 10 mg/kg |
| Reactive orange 14 | Sigma - Aldrich | R - 8254 | |
| Ringers Solution Components | Solution is gas equilibrated with 95% O2 and 5% Co2, final pH 7.4 | ||
| Sodium chloride | Sigma - Aldrich | S7653 | Final Concentration: 118 mM |
| Potassium chloride | Fisher Scientific | P217 - 3 | Final Concentration: 4.7 mM |
| Calcium chloride dihydrate | Fisher Scientific | C79 - 500 | Final Concentration: 2.5 mM |
| Potassium phosphate monobasic | Fisher Scientific | P -285 | Final Concentration: 1.2 mM |
| Magnesium sulfate | J.T. Baker | Jan-00 | Final Concentration: 0.57 mM |
| 4-(2-Hydroxyethyl)piperazine-1-ethanesulfonic acid (HEPES) | Fisher Scientific | BP 310 - 500 | Final Concentration: 5.95 g/L |
| Glucose | Sigma - Aldrich | G8270 | Final Concentration: 5.5 mM |
| LifeWindow | Digicare Biomedical Technology | ||
| CED bioamplifier and ADC units | Cambridge Electronic Design Limited, Unit 4, Science Park, Milton Road, Cambridge CB4 0FE ENGLAND. | Bioamp: 1902; ADC: micro1401; Data acquisition software: Spike 2, V7.13 | |
| Neurolog analog signal bioamplifier | Digitimer Ltd 37 Hydeway Welwyn Garden City Hertfordshire, AL7 3BE, England | NL108A | |
| ABL800Flex | Radiometer Canada; 200 Aberdeen Dr, London, ON N5V 4N2 | ||
| Eppendorf 5804R | Eppendorf Canada; 2810 Argentia Road, #2 Mississauga, Ontario, L5N 8L2 | ||
| Arrow Jugular Catheterization Set | Arrow International, Inc., 2400 Bernville Road, Reading, PA 19605 USA | ||
| Atravet | 10 mg/ml | ||
| Diazepam | 5 mg/ml | ||
| Ketamine | Ketalar | 100 mg/ml | |
| Propofol | 10 mg/ml | ||
| SurgiVeT | Endotracheal Tubes; Smiths Medical ASD, Inc. St. Paul, MN 55112, USA | ||
| Cook Airway Exchange Catheter with RAPI-FIT Adapters | Cook Critical Care 750, Bloomington IN 47402-0489 USA | ||
| Dispomed Ventilator | Dispomed Ltd., 745 Nazaire-Laurin, Joliette, Quebec J6E 0L6 | ||
| BD Insyte-W | Becton Dickinson, Infusion Therapy Systems Inc., 9450 S State St, Sandy Utah 84070 USA | 22 to 20 G; 1 in [0.9 x 25 mm] to 1.16 in [1.1 x 30 mm] | |
| Edwards Lifesciences Ref: PX272 Pressure monitoring kit with TruWave Disposable Pressure | |||
| LifeWindow LW6000 | Digicare Biomedical Technology 107 Commerce Road, Boynton Beach, FL 33426-9365 USA | ||
| Gaymar | |||
| Babcock | |||
| Polyvinyl catheters | SCI (Scientific Commodities Inc.) | 2 meters | |
| 2-0 Vicryl | |||
| Castroviejo scissors | |||
| electrocardiogram (ECG) | LIFYY, Metrofunk Kabel-Union, Berlin, Germany | four copper electrodes in single sheath, 2 meters | |
| 2-O Vicryl | |||
| 3-0 Vicryl | |||
| PDS II USP | |||
| Trimethoprim sulfadoxine | |||
| Ampicillin | |||
| Stopcock | Argon Medical, Cat 041220001A | Double 4-way Stopcock with male luer lock | |
| Needles | Tyco Healthcare 8881202389 | Monoject aluminum hub blunt needles, 22Gx, 0.7mmx 38.1mm: for fetal arterial and venous catheters | |
| Needles | Tyco Healthcare 8881202322 | Monoject aluminum hub blunt needles, 16Gx, 1.6mmx38.1mm: for amniotic catheters |
Referencias
- Barry, J. S., Anthony, R. V. The pregnant sheep as a model for human pregnancy. Theriogenology. 69, 55-67 (2008).
- Morrison, J. L. Sheep models of intrauterine growth restriction: fetal adaptations and consequences. Clin Exp Pharmacol Physiol. 35, 730-743 (2008).
- Rees, S., Inder, T. Fetal and neonatal origins of altered brain development. Early Hum Dev. 81, 753-761 (2005).
- Rees, S., Harding, R., Walker, D. The biological basis of injury and neuroprotection in the fetal and neonatal brain. Int J Dev Neurosci. 29, 551-563 (2011).
- Moisiadis, V. G., Matthews, S. G. Glucocorticoids and fetal programming part 1: Outcomes. Nat rev Endocrinol. 10, 391-402 (2014).
- Wang, X., Rousset, C. I., Hagberg, H., Mallard, C. Lipopolysaccharide-induced inflammation and perinatal brain injury. Semin Fetal Neonatal Med. 11, 343-353 (2006).
- Gotsch, F., et al. The fetal inflammatory response syndrome. Clin Exp Obstet Gynecol. 50, 652-683 (2007).
- Svedin, P., Kjellmer, I., Welin, A. K., Blad, S., Mallard, C. Maturational effects of lipopolysaccharide on white-matter injury in fetal sheep. J child neurol. 20, 960-964 (2005).
- Nitsos, I., et al. Chronic exposure to intra-amniotic lipopolysaccharide affects the ovine fetal brain. J Soc Gynecol Investig. 13, 239-247 (2006).
- Yan, E., Castillo-Melendez, M., Nicholls, T., Hirst, J., Walker, D. Cerebrovascular responses in the fetal sheep brain to low-dose endotoxin. Pedia res. 55, 855-863 (2004).
- Dean, J. M., et al. Delayed cortical impairment following lipopolysaccharide exposure in preterm fetal sheep. Ann Neurol. 70, 846-856 (2011).
- Dobbing, J., Sands, J. Comparative aspects of the brain growth spurt. Early Hum Dev. 3 (1), 79-83 (1979).
- Liggins, G. C. Premature parturition after infusion of corticotrophin or cortisol into foetal lambs. J Endocrinol. 42, 323-329 (1968).
- Liggins, G. C. Premature delivery of foetal lambs infused with glucocorticoids. J Endocrinol. 45, 515-523 (1969).
- Liggins, G. C., Fairclough, R. J., Grieves, S. A., Kendall, J. Z., Knox, B. S. The mechanism of initiation of parturition in the ewe. Recent Prog Horm Res. 29, 111-159 (1973).
- Morrison, J. L. Sheep models of intrauterine growth restriction: fetal adaptations and consequences. Clin Exp Pharmacol Physiol. 35, 730-743 (2008).
- Robinson, J. S., Hart, I. C., Kingston, E. J., Jones, C. T., Thorburn, G. D. Studies on the growth of the fetal sheep. The effects of reduction of placental size on hormone concentration in fetal plasma. J Dev Physiol. 2, 239-248 (1980).
- Carmel, E., et al. Fetal brain MRI - experiences in the ovine model of cerebral inflammatory response. Repro sci. 19 (3), 347A-348A (2012).
- Samson, N., Dumont, S., Specq, M. L., Praud, J. P. Radio telemetry devices to monitor breathing in non-sedated animals. Respir Physiol Neurobiol. 179, 111-118 (2011).
- Thakor, A. S., Giussani, D. A. Effects of acute acidemia on the fetal cardiovascular defense to acute hypoxemia. Am J Physiol Regul Integr Comp Physiol. 296, R90-R99 (2009).
- Green, L. R., Kawagoe, Y., Homan, J., White, S. E., Richardson, B. S. Adaptation of cardiovascular responses to repetitive umbilical cord occlusion in the late gestation ovine fetus. J Physiol. 535, 879-888 (2001).
- Unno, N., et al. Changes in adrenocorticotropin and cortisol responsiveness after repeated partial umbilical cord occlusions in the late gestation ovine fetus. Endocrinology. 138, 259-263 (1997).
- Muller, T., et al. Developmental changes in cerebral autoregulatory capacity in the fetal sheep parietal cortex. J Physiol. 539, 957-967 (2002).
- Keen, A. E., Frasch, M. G., Sheehan, M. A., Matushewski, B., Richardson, B. S. Maturational changes and effects of chronic hypoxemia on electrocortical activity in the ovine fetus. Brain Res. 1402, 38-45 (2011).
- Ross, M. G., et al. Correlation of arterial fetal base deficit and lactate changes with severity of variable heart rate decelerations in the near-term ovine fetus. Am J Obstet Gynecol. 208, e281-e286 (2013).
- Gunn, A. J., Gunn, T. R., de Haan, H. H., Williams, C. E., Gluckman, P. D. Dramatic neuronal rescue with prolonged selective head cooling after ischemia in fetal lambs. J Clin Invest. 99, 248-256 (1997).
- Xu, A., Piorkowska, K., Matushewski, B., Hammond, R., Richardson, B. S. Adaptive Brain Shut-Down Counteracts Neuroinflammation in the Near-Term Ovine Fetus. 20 (3), 222A (2013).
- Derks, J. B., et al. A comparative study of cardiovascular, endocrine and behavioural effects of betamethasone and dexamethasone administration to fetal sheep. J Physiol Lond. 499, 217-226 (1997).
- Lohle, M., et al. Betamethasone effects on fetal sheep cerebral blood flow are not dependent on maturation of cerebrovascular system and pituitary-adrenal axis. J Physiol. 564, 575-588 (2005).
- Morrison, J. L., et al. Maternal fluoxetine infusion does not alter fetal endocrine and biophysical circadian rhythms in pregnant sheep. J Soc Gynecol Investig. 12, 356-364 (2005).
- Allison, B. J., et al. Ventilation of the very immature lung in utero induces injury and BPD-like changes in lung structure in fetal sheep. Pediatr Res. 64, 387-392 (2008).
- Rozance, P. J., et al. Intrauterine growth restriction decreases pulmonary alveolar and vessel growth and causes pulmonary artery endothelial cell dysfunction in vitro in fetal sheep. Am J Physiol Lung Cell Mol Physiol. 301, L860-L871 (2011).
- Fowden, A. L., Giussani, D. A., Forhead, A. J. Endocrine and metabolic programming during intrauterine development. Early hum dev. 81, 723-734 (2005).
- Nathanielsz, P. W., Hanson, M. A. The fetal dilemma: spare the brain and spoil the liver. J Physiol. 548, 333 (2003).
- Manikkam, M., et al. Fetal programming: prenatal testosterone excess leads to fetal growth retardation and postnatal catch-up growth in sheep. Endocrinology. 145, 790-798 (2004).
- Savabieasfahani, M., et al. Fetal programming: testosterone exposure of the female sheep during midgestation disrupts the dynamics of its adult gonadotropin secretion during the periovulatory period. Biol Reprod. 72, 221-229 (2005).
- Bergen, N. H., et al. Fetal programming alters reactive oxygen species production in sheep cardiac mitochondria. Clin Sci (Lond). 116, 659-668 (2009).
- Cox, L. A., et al. A genome resource to address mechanisms of developmental programming: determination of the fetal sheep heart transcriptome. J Physiol. 590, 2873-2884 (2012).
- Mahoney, M. M., Padmanabhan, V. Developmental programming: impact of fetal exposure to endocrine-disrupting chemicals on gonadotropin-releasing hormone and estrogen receptor mRNA in sheep hypothalamus. Toxicol Appl Pharmacol. 247, 98-104 (2010).
- Blad, S., Welin, A. K., Kjellmer, I., Rosen, K. G., Mallard, C. ECG and Heart Rate Variability Changes in Preterm and Near-Term Fetal Lamb Following LPS Exposure. Reprod Sci. 15, 572-583 (2008).
- Frasch, M. G., et al. Heart rate variability analysis allows early asphyxia detection in ovine fetus. Reprod Sci. 16, 509-517 (2009).
- Frasch, M. G., Keen, A. E., Gagnon, R., Ross, M. G., Richardson, B. S. Monitoring fetal electrocortical activity during labour for predicting worsening acidemia: a prospective study in the ovine fetus near term. PLoS One. 6, e22100 (2011).
- Durosier, L. D., et al. Sampling rate of heart rate variability impacts the ability to detect acidemia in ovine fetuses near-term. Front pedia. 2, 38 (2014).
- Danielson, L., McMillen, I. C., Dyer, J. L., Morrison, J. L. Restriction of placental growth results in greater hypotensive response to alpha-adrenergic blockade in fetal sheep during late gestation. J Physiol. 563, 611-620 (2005).
- Edwards, L. J., Simonetta, G., Owens, J. A., Robinson, J. S., McMillen, I. C. Restriction of placental and fetal growth in sheep alters fetal blood pressure responses to angiotensin II and captopril. J Physiol. 515 (Pt 3), 897-904 (1999).
- Xu, A., et al. Adaptive brain shut-down counteracts neuroinflammation in the near-term ovine fetus. Front neurol. 5, 110 (2014).
- Xu, A., et al. The Ovine Fetal and Placental Inflammatory Response to Umbilical Cord Occlusions With Worsening Acidosis. Reprod Sci. 22 (11), (2015).
- Wang, X., Durosier, L. D., Ross, M. G., Richardson, B. S., Frasch, M. G. Online detection of fetal acidemia during labour by testing synchronization of EEG and heart rate: a prospective study in fetal sheep. PLoS One. 9, e108119 (2014).
- Reid, A., Malone, J. Q fever in Ireland A seroprevalence study of exposure to Coxiella burnettii among Department of Agriculture workers. Occ med. 54, 544-547 (2004).
- Roest, H. I., Bossers, A., van Zijderveld, F. G., Rebel, J. M. Clinical microbiology of Coxiella burnetii and relevant aspects for the diagnosis and control of the zoonotic disease Q fever. Vet quart. 33, 148-160 (2013).
- Neill, T. J., Sargeant, J. M., Poljak, Z. The effectiveness of Coxiella burnetii vaccines in occupationally exposed populations: a systematic review and meta-analysis. Zoonoses and public health. 61, 81-96 (2014).
- Roest, H. I., Bossers, A., Rebel, J. M. Q fever diagnosis and control in domestic ruminants. Dev biol. 135, 183-189 (2013).
- Frasch, M. G., et al. Fetal body weight and the development of the control of the cardiovascular system in fetal sheep. J physilo. 579, 893-907 (2007).
- Rurak, D., Bessette, N. W. Changes in fetal lamb arterial blood gas and acid-base status with advancing gestation. Am J Physiol Regul Integr Comp Physiol. 304, R908-R916 (2013).
- Frasch, M. G., et al. Fetal body weight and the development of the control of the cardiovascular system in fetal sheep. J physiol. 579, 893-907 (2007).
- Frasch, M. G., et al. Measures of acidosis with repetitive umbilical cord occlusions leading to fetal asphyxia in the near-term ovine fetus. Am J Obstet Gynecol. 200, 200.e1-207.e1 (2009).
- The ESHRE Capri Workshop Group. Multiple gestation pregnancy. Hum reprod. 15, 1856-1864 (2000).
- Frasch, M. G. Re The perinatal development of arterial pressure in sheep: effects of low birth weight due to twinning. Reproductive sciences (Thousand Oaks, Calif.). 15, 863-865 (2008).
- Hancock, S. N., Oliver, M. H., McLean, C., Jaquiery, A. L., Bloomfield, F. H. Size at birth and adult fat mass in twin sheep are determined in early gestation. J Physiol. 590, 1273-1285 (2012).
- Wassink, G., Bennet, L., Davidson, J. O., Westgate, J. A., Gunn, A. J. Pre-existing hypoxia is associated with greater EEG suppression and early onset of evolving seizure activity during brief repeated asphyxia in near-term fetal sheep. PLoS One. 8, e73895 (2013).
- Mathai, S., et al. Acute on chronic exposure to endotoxin in preterm fetal sheep. Am J Physiol Regul Integr Comp Physiol. 304, R189-R197 (2013).
- Heuij, L. G., et al. Synergistic white matter protection with acute-on-chronic endotoxin and subsequent asphyxia in preterm fetal sheep. J neuroinflam. 11, 89 (2014).
- Gagnon, R., Challis, J., Johnston, L., Fraher, L. Fetal endocrine responses to chronic placental embolization in the late-gestation ovine fetus. Am J Obstet Gynecol. 170, 929-938 (1994).
- Miller, S. L., Supramaniam, V. G., Jenkin, G., Walker, D. W., Wallace, E. M. Cardiovascular responses to maternal betamethasone administration in the intrauterine growth-restricted ovine fetus. Am J Obstet Gynecol. 201, 613.e1-613.e8 (2009).
- Regnault, T. R., et al. The relationship between transplacental O2 diffusion and placental expression of PlGF, VEGF and their receptors in a placental insufficiency model of fetal growth restriction. J Physiol. 550, 641-656 (2003).
- Wallace, J. M., Aitken, R. P., Cheyne, M. A. Nutrient partitioning and fetal growth in rapidly growing adolescent ewes. J reprod and fertil. 107, 183-190 (1996).
- Rakers, F., et al. Effects of early- and late-gestational maternal stress and synthetic glucocorticoid on development of the fetal hypothalamus-pituitary-adrenal axis in sheep. Stress. 16, 122-129 (2013).
- Jiang, Y., et al. The sheep genome illuminates biology of the rumen and lipid metabolism. Science. 344, 1168-1173 (2014).
- Begum, G., et al. Epigenetic changes in fetal hypothalamic energy regulating pathways are associated with maternal undernutrition and twinning. FASEB J. 26, 1694-1703 (2012).
- Byrne, K., et al. Genomic architecture of histone 3 lysine 27 trimethylation during late ovine skeletal muscle development. Anim Genet. 45, 427-438 (2014).
- Lie, S., et al. Impact of embryo number and maternal undernutrition around the time of conception on insulin signaling and gluconeogenic factors and microRNAs in the liver of fetal sheep. Am J physiol Endocrinol. 306, E1013-E1024 (2014).
- Nicholas, L. M., et al. Differential effects of maternal obesity and weight loss in the periconceptional period on the epigenetic regulation of hepatic insulin-signaling pathways in the offspring. FASEB J. 27, 3786-3796 (2013).
- Wang, K. C., et al. Low birth weight activates the renin-angiotensin system, but limits cardiac angiogenesis in early postnatal life. Physiol rep. 3, (2015).
- Zhang, S., et al. Periconceptional undernutrition in normal and overweight ewes leads to increased adrenal growth and epigenetic changes in adrenal IGF2/H19 gene in offspring. FASEB J. 24, 2772-2782 (2010).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoThis article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados