Method Article
Herstellung von Dünnschichtsilber/Silberchloridelektroden mit fein kontrollierten einlagigen Silberchlorid
In diesem Artikel
Zusammenfassung
Dieses Papier zielt darauf ab, eine Methode zur Bildung von glatten und gut kontrollierten Folien aus Silberchlorid (AgCl) mit einer bestimmten Abdeckung auf dünnen Silberelektroden zu präsentieren.
Zusammenfassung
Dieses Papier zielt darauf ab, ein Protokoll zur Bildung von glatten und gut kontrollierten Folien aus Silber/Silberchlorid (Ag/AgCl) mit designierter Abdeckung auf dünnschichtigen Silberelektroden zu präsentieren. Dünnschicht-Silberelektroden in den Größen 80 x 80 x m und 160 x 160 m wurden auf Quarzwafern mit einer Chrom/Gold-Schicht (Cr/Au) zur Haftung gesputtert. Nach Passivierung, Polieren und kathodischen Reinigungsprozessen wurden die Elektroden unter Berücksichtigung des Faraday-Gesetzes der Elektrolyse galvanisch oxidiert, um glatte Schichten von AgCl mit einem bestimmten Grad an Abdeckung auf der Silberelektrode zu bilden. Dieses Protokoll wird durch die Inspektion von Rasterelektronenmikroskop(SEM)-Bildern der Oberfläche der hergestellten Ag/AgCl Dünnschichtelektroden validiert, was die Funktionalität und Leistung des Protokolls unterstreicht. Auch suboptimal gefertigte Elektroden werden zum Vergleich gefertigt. Dieses Protokoll kann häufig verwendet werden, um Ag/AgCl-Elektroden mit spezifischen Impedanzanforderungen herzustellen (z. B. Sondierungselektroden für Impedanzsensorikanwendungen wie Impedanzdurchflusszytometrie und interdigitierte Elektrodenarrays).
Einleitung
Die Ag/AgCl-Elektrode ist eine der am häufigsten verwendeten Elektroden im Bereich der Elektrochemie. Es wird am häufigsten als Referenzelektrode in elektrochemischen Systemen aufgrund seiner einfachen Herstellung, ungiftige Eigenschaft und stabile Elektrodenpotenzial1,2,3,4,5,6.
Forscher haben versucht, den Mechanismus von Ag/AgCl-Elektroden zu verstehen. Die Schicht des Chloridsalzes auf der Elektrode ist ein grundlegendes Material in der charakteristischen Redoxreaktion der Ag/AgCl-Elektrode in einem elektrolythaltigen Chlorid. Für den Oxidationspfad kombiniert sich das Silber an den Unvollkommenheiten auf der Oberfläche der Elektrode mit den Chloridionen in der Lösung zu löslichen AgCl-Komplexen, in denen sie zu den Rändern der AgCl diffundieren, die sich auf der Oberfläche der Elektrode zur Ausfällung in Form von AgCl ablagern. Der Reduktionspfad beinhaltet die Bildung von löslichen AgCl-Komplexen mit dem AgCl auf der Elektrode. Die Komplexe diffundieren auf die Silberoberfläche und reduzieren zurück zu elementarem Silber7,8.
Die Morphologie der AgCl-Schicht ist ein entscheidender Einfluss auf die physikalische Eigenschaft von Ag/AgCl-Elektroden. Verschiedene Arbeiten zeigten, dass die große Oberfläche der Schlüssel zur Bildung von Referenz-Ag/AgCl-Elektroden mit hoch reproduzierbaren und stabilen Elektrodenpotentialen9,10,11,12ist. Daher haben Forscher Methoden zur Herstellung von Ag/AgCl-Elektroden mit einer großen Oberfläche untersucht. Brewer et al. entdeckten, dass die Verwendung von konstanter Spannung anstelle von konstantem Strom zur Herstellung von Ag/AgCl-Elektroden zu einer stark porösen AgCl-Struktur führen würde, wodurch die Oberfläche der AgCl-Schicht11vergrößert würde. Safari et al. nutzten den Massentransport-Beschränkungseffekt während der AgCl-Bildung auf der Oberfläche von Silberelektroden, um AgCl-Nanoblätter darüber zu bilden, wodurch die Oberfläche der AgCl-Schicht signifikant12erhöht wurde.
Es gibt einen steigenden Trend, AgCl Elektrode für Sensoranwendungen zu entwerfen. Eine geringe Kontaktimpedanz ist entscheidend für die Erfassung von Elektroden. Daher ist es wichtig zu verstehen, wie sich die Oberflächenbeschichtung von AgCl auf seine Impedanzeigenschaft auswirken würde. Unsere bisherigen Untersuchungen haben gezeigt, dass der Grad der AgCl-Abdeckung auf der Silberelektrode einen entscheidenden Einfluss auf die Impedanzcharakteristik der Elektroden-/Elektrolytschnittstelle13hat. Um jedoch die Kontaktimpedanz von Dünnschicht-Ag/AgCl-Elektroden richtig einschätzen zu können, muss die gebildete AgCl-Schicht glatt sein und eine gut kontrollierte Abdeckung haben. Daher ist eine Methode zum Erstellen glatter AgCl-Layer mit festgelegtem AgCl-Abdeckungsgrad erforderlich. Es wurden Arbeiten durchgeführt, um diesem Bedarf teilweise gerecht zu werden. Brewer et al. und Pargar et al. diskutierten, dass eine glatte AgCl mit einem sanften konstanten Strom erreicht werden kann, indem die AgCl-Schicht auf der Oberseite der Silberelektrode11,14hergestellt wird. Katan et al. bildeten eine einzige Schicht AgCl auf ihren Silberproben und beobachteten die Größe der einzelnen AgCl-Partikel8. Ihre Forschung fand heraus, dass die Dicke einer einzelnen Schicht von AgCl etwa 350 nm beträgt. Ziel dieser Arbeit ist es, ein Protokoll zu entwickeln, um feine und gut kontrollierte Filme von AgCl mit vorhergesagten Impedanzeigenschaften auf Silberelektroden zu bilden.
Protokoll
1. Herstellung einer Cr/Au-Haftschicht mittels Liftoff
- Spincoat HPR504 positiver Photowiderstand von 1,2 m Dicke auf einen Quarzwafer mit einer Streugeschwindigkeit von 1.000 U/min für 5 s und einer Spin-Geschwindigkeit von 4.000 U/min für 30 s.
- Softbake der Photoresist auf dem Quarz-Wafer bei 110 °C für 5 min auf einer heißen Platte.
- Setzen Sie den Wafer mit einem Maskenaligner so aus, dass Die Positionen für die Cr/Au-Abscheidung mit ultraviolettem (UV) Licht belichtet werden. Die Belichtungsleistungsdichte und -zeit beträgt 16 mW/cm2 bzw. 7,5 s (Belichtungsenergiedichte = 120 mJ/cm2).
- Entwickeln Sie den Wafer, indem Sie ihn in den positiven Widerstandsentwickler FHD-5 für 1 min. Spülen Sie den Wafer nach dem Entwicklungsprozess mit deionisiertem (DI) Wasser.
- Trocknen Sie den Wafer mit einem Stickstoff (N2) Geschütz. Den Wafer 5 min bei 120 °C in einen Ofen stellen.
- Mit Elektronenstrahlverdampfung (E-Strahl) eine 5 nm Cr-Schicht ablagern, gefolgt von einer 50 nm Au-Schicht auf dem Wafer. Die Abscheidungsraten betragen 1 s/s bzw. 2 °C.
- Legen Sie den e-strahl verdampften Wafer in einen Behälter. Gießen Sie reichlich Aceton in sich.
- Schließen Sie den Behälter mit einem Deckel. Legen Sie den Deckelbehälter 10 min in einen Ultraschallreiniger oder bis der Liftoff-Vorgang abgeschlossen ist.
- Spülen Sie den Wafer mit Isopropanol (IPA) gefolgt von DI-Wasser. Trocknen Sie es mit N2 Pistole und Ofen danach.
HINWEIS: Das Protokoll kann hier angehalten werden.
2. Herstellung von Dünnschicht Ag Elektroden auf der Haftschicht mittels Liftoff
- Spincoat AZ P4620 positiver Photowiderstand von 7 'm Dicke auf den Wafer mit einer Streugeschwindigkeit von 1.000 U/min für 5 s und einer Spin-Geschwindigkeit von 4.000 U/min für 30 s.
- Softbake der Photoresist auf dem Wafer bei 90 °C für 450 s auf einer kochplatte.
- Setzen Sie den Wafer mithilfe eines Maskenaligners so aus, dass Positionen für die Ag-Deposition mit UV belichtet werden. Die Belichtungsleistungsdichte und -zeit beträgt 16 mW/cm2 bzw. 45 s (Belichtungsenergiedichte = 720 mJ/cm2).
- Entwickeln Sie den Wafer, indem Sie ihn 2 min in FHD-5 tauchen. Spülen Sie den Wafer nach dem Entwicklungsprozess mit DI-Wasser ab.
- Trocknen Sie den Wafer mit einer N2 Pistole. Den Wafer 5 min bei 120 °C in einen Ofen stellen.
- Sputtern Sie eine 1'm Ag-Schicht auf dem Wafer. Die Sputterrate beträgt 86 nm/min.
- Legen Sie den gesputterten Wafer in einen Behälter. Gießen Sie reichlich Aceton in sich.
- Schließen Sie den Behälter mit einem Deckel. Legen Sie den Deckelbehälter 10 min in einen Ultraschallreiniger oder bis der Liftoff-Vorgang abgeschlossen ist.
- Spülen Sie den Wafer mit IPA gefolgt von DI-Wasser. Trocknen Sie es mit N2 Pistole und Ofen danach.
3. Passivierung des Wafers, um nur die Elektroden und Kontaktpads freizulegen
- Passivieren Sie die gesamte Waferoberfläche mit einer 2-m-Siliziumdioxidschicht (SiO2) unter Verwendung einer plasmaverstärkten chemischen Dampfabscheidung (PECVD).
- Passivieren Sie eine kleine Silizium-Dummy-Probe (ein Silizium-Wafer-Fragment) gleichzeitig den Wafer.
- Messen Sie die Dicke der Oxidschicht der Dummyprobe.
HINWEIS: Das Protokoll kann hier angehalten werden.
- Spincoat AZ 5214E Dual-Ton-Photoresist von 1,4 m Dicke auf den Wafer mit einer Streugeschwindigkeit von 1000 U/min für 5 s und einer Spin-Geschwindigkeit von 3000 U/min für 30 s.
- Softbake der Photoresist auf dem Wafer bei 90 °C für 150 s auf einer kochplatte.
- Setzen Sie den Wafer mithilfe eines Maskenaligners so aus, dass die Positionen für die Padöffnung mit UV belichtet werden. Die Belichtungsleistungsdichte und -zeit beträgt 16 mW/cm2 bzw. 2,25 s (Belichtungsenergiedichte = 36 mJ/cm2).
- Entwickeln Sie den Wafer, indem Sie ihn in FHD-5 für 75 s tauchen. Spülen Sie den Wafer nach dem Entwicklungsprozess mit DI-Wasser.
- Nach dem kurzen Trocknen des Wafers mit der Pistole N2 weiter trocken und hart im Ofen für 15 min bei 120 °C backen.
- Führen Sie das Descum von Photoresist auf dem Wafer für 1 min mit einem Plasma-Asher, um die vollständige Entfernung von unerwünschten Photoresist zu gewährleisten.
- Führen Sie eine reaktive Ionenätzung auf dem Wafer und der Dummy-Probe durch, um die Dünnschichtelektroden und Kontaktpads freizulegen.
- Nach einer kurzen Zeitoperation (z.B. 5-10 min) beenden Sie den Betrieb und nehmen Sie die Dummyprobe heraus.
- Messen Sie die Dicke der Oxidschicht auf der Oberseite der Dummy-Probe. Vergleichen Sie es mit dem Ergebnis in Schritt 3.1.2.
- Berechnen Sie die Rate der SiO2 Radierung der Maschine, um die Ätzdauer zu optimieren, um eine 10% Überätzung zu erreichen.
- Fahren Sie mit dem Ätzvorgang ohne die Dummy-Probe fort.
- Widerstehen Sie den geätzten Wafer 30 min durch Plasmaasche abstreifen, gefolgt von einem positiven Photoresist-Stripper MS2001-Bad bei 70 °C für 5 min.
- Spülen Sie den Wafer mit DI-Wasser. Trocknen Sie den Wafer mit N2 Pistole und Backofen.
HINWEIS: Das Protokoll kann hier angehalten werden.
4. Vorbereitung für die Herstellung von Dünnschicht-Ag/AgCl-Elektroden (Chip)
- Würfel schneiden den Wafer, um verschiedene Testchips zu erhalten.
- Polieren Sie die Elektrodenoberflächen auf den Spänen mit feinem Schleifpapier.
- Verkleben Sie die Kontaktpads auf dem Chip in weiteren Schritten an eine externe Leiterplatte für Schnittstellen.
- 3D-Druck einen Acrylhohl-Rechteckbehälter, um den Elektrolyten auf den Dünnschichtelektroden zu halten. Die Abmessungen des rechteckigen Behälters sollten die Platzierung eines Drahtes und einer Pipette in der Leere bequem ermöglichen.
- Mischen Sie eine kleine Menge Polydimethylsiloxan (PDMS) Prepolymer und sein Härtungsmittel gründlich. Das Verhältnis sollte 10:1 sein.
HINWEIS: Es ist sehr üblich, die PDMS-Mischung zu entgasen, um hochwertige PDMS-Geräte zu erhalten; in diesem Fall wird dies jedoch nicht benötigt, da das Gemisch nur als Klebstoff verwendet wird. - Legen Sie den Acrylbehälter auf den gewürfelten Chip so, dass sich alle Silberelektroden im Hohlraum des Behälters befinden.
- Verschmieren Sie mit einem Zahnstocher oder einer feinen Stange die ungehärtete PDMS-Mischung am äußeren Rand, wo sich der Behälter und der Chip berühren.
- Den Chip vorsichtig auf eine flache Kochplatte legen und das PDMS 2 h bei 80 °C aushärten oder bis der Behälter sicher auf dem Chip befestigt ist.
5. Vorbereitung für die Herstellung von Dünnschicht-Ag/AgCl-Elektroden (Reagenzien)
- Mit DI-Wasser und konzentrierter Salzsäure (HCl) erhalten Sie 0,01 M HCl-Lösung.
- Unter Verwendung von DI-Wasser und Kaliumchlorid (KCl) Pulver erhalten 3,5 M KCl-Lösung und 0,1 M KCl-Lösung.
HINWEIS: Das Protokoll kann hier angehalten werden.
6. Vorbereitung für die Herstellung von Dünnschicht-Ag/AgCl-Elektroden (Makroelektroden)
- Schneiden Sie einige silberdrähte.
- Polieren Sie die Oberfläche der Silberdrähte mit feinem Schleifpapier.
- Tauchen Sie 80% der Silberdrähte für 1 h in Haushaltsbleiche ein.
HINWEIS: Die Farbe des Drahtes ändert sich von silbrig zu dunkelviolett. Dies zeigt die Bildung von AgCl auf der Oberfläche des Silberdrahtes. - Spülen Sie den Ag/AgCl-Draht mit DI-Wasser.
- Erstellen Sie eine Ag/AgCl-Referenzelektrode mit einem der Ag/AgCl-Drähte, die sich auf Hassel et al. mit Modifikationen15beziehen.
HINWEIS: Bei den Modifikationen wird eine Pipette anstelle einer Glaskapillare verwendet, wobei 3,5 M KCl als Elektrolyt verwendet wird, wobei der Polymerblock und der vergoldete Verbinder abgetrennt und durch Parafilm ersetzt werden. - Bewahren Sie die Ag/AgCl-Elektroden auf, indem Sie sie in 3,5 M KCl-Lösung untertauchen. Stellen Sie sicher, dass das Silberteil nicht mit der Lösung in Berührung kommt.
- Schneiden Sie mehrere Teile von Ag/AgCl-Drähten und legen Sie sie in die in Schritt 5.2 genannten KCl-Lösungen.
HINWEIS: Das Protokoll kann hier angehalten werden.
- Schneiden Sie mehrere Teile von Ag/AgCl-Drähten und legen Sie sie in die in Schritt 5.2 genannten KCl-Lösungen.
7. Kathodische Reinigung der Mikro-Ag-Elektroden
HINWEIS: Alle folgenden Prozesse verwenden den elektrochemischen Analysator CHI660D und die zugehörige Software.
- Spülen Sie den Chip mit IPA gefolgt von DI-Wasser.
- 0,01 M HCl Lösung in den Acrylbehälter gießen.
- Die Pipettenaußenseite der Makro-Ag/AgCl-Referenzelektrode (in Schritt 6.5) und eine Makro-Ag/AgCl-Elektrode (in Schritt 6.3 hergestellt) mit Labor-Reinigungstüchern trocknen.
- Verbinden Sie den Chip und die Makroelektroden mit dem Analysator, so dass eine Dünnschicht-Ag-Elektrode auf dem Chip als Arbeitselektrode definiert ist, die Makro-Ag/AgCl-Referenzelektrode als Referenzelektrode und die blanke Makro-Ag/AgCl-Elektrode als Gegenelektrode definiert ist.
- Legen Sie die Makroelektroden in den Behälter. Verwenden Sie blu-tack als Deckel des Behälters, um die Makroelektroden zu verankern.
- Platzieren Sie das Setup in einem Faraday-Käfig.
- Klicken Sie in der CHI660D-Software auf die Registerkarte Setup in der oberen linken Ecke des Fensters. Klicken Sie dann auf Technik | Amperometrische i-t-Kurve | OK, um die kathodische Reinigung der Elektroden durchzuführen.
- Ändern Sie im Popup-Menü die Parameter für die kathodische Reinigung.
- Stellen Sie init E (V) auf -1.5ein.
- Legen Sie das Beispielintervall (Sek.) auf 0,1 (Standard)fest.
- Legen Sie die Laufzeit (Sek.) auf 900fest.
- Legen Sie die Ruhezeit (Sek.)auf 0 (Standard)fest.
- Legen Sie die Skalen während der Ausführung auf 1 (Standard)fest.
- Stellen Sie die Empfindlichkeit (A/V) entsprechend ein. Stellen Sie sie für eine 80 x 80 m Elektrode auf 1e-006ein.
- Drücken Sie OK. Starten Sie den Vorgang, indem Sie das Startsymbol unter der Menüleiste drücken.
- Lassen Sie das Experiment laufen und beenden.
- Öffnen Sie den Faraday Käfig.
- Entfernen Sie die Makroreferenz und die Gegenelektrode. Wischen Sie ihre Oberflächen trocken.
- Gießen Sie den verwendeten Elektrolyt in einen Abfallbehälter. Spülen Sie den Acrylbehälter mit DI-Wasser.
8. Herstellung von einlagigen AgCl auf der Oberseite der Dünnschicht Ag Elektroden
- 0,1 M KCl Lösung in den Acrylbehälter gießen.
- Verbinden Sie den Chip und die Makroelektroden mit dem Analysator, so dass die gereinigte Dünnschicht-Ag-Elektrode auf dem Chip als Arbeitselektrode definiert ist, die Makro-Ag/AgCl-Referenzelektrode als Referenzelektrode und die blanke Makro-Ag/AgCl-Elektrode als Gegenelektrode definiert ist.
- Legen Sie die Makroelektroden in den Behälter. Verwenden Sie blu-tack als Deckel des Behälters, um die Makroelektroden zu verankern.
- Platzieren Sie das Setup in einem Faraday-Käfig.
- Klicken Sie in der CHI660D-Software auf die Registerkarte Setup in der oberen linken Ecke des Fensters, und klicken Sie dann auf Technik | Chronopotentiometrie | OK, um galvananostatische Fertigung von einlagigen AgCl auf Silberelektroden durchzuführen.
- Ändern Sie im Popup-Menü die Parameter für einen solchen Prozess.
- Legen Sie den Kathodenstrom (A) auf 0 (Standard)fest.
- Stellen Sie den Annodischen Strom (A) so ein, dass die auf die Dünnschichtelektrode aufgebrachte Stromdichte 0,5 mA/cm2beträgt.
- Halten Sie das High- und Low E-Limit und die Haltezeit standardmäßig.
- Legen Sie die kathodische Zeit (Sek.) auf 10 (Standard)fest.
- Legen Sie die anodische Zeit (Sek.) entsprechend fest, um den erforderlichen Grad an AgCl-Abdeckung zu erreichen.
HINWEIS: In Bezug auf Das Faradays Law of Electrolysis beträgt die benötigte Zeit für eine 100%ige Abdeckung 262 s. Die benötigte Zeit variiert linear mit dem Deckungsprozentsatz. - Legen Sie die Anfangspolarität als anodischfest.
- Legen Sie den Datenspeicher Intvl (Sek.) auf 0.1 (Standard)fest.
- Legen Sie die Anzahl der Segmente als 1 (Standard)fest.
- Legen Sie die aktuelle Schaltpriorität als Zeitfest.
- Deaktivieren Sie die Hilfssignalaufzeichnung beim Sample-Intervall > = 0,0005s (Standard).
- Drücken Sie OK. Starten Sie den Vorgang, indem Sie das Startsymbol unter der Menüleiste drücken.
- Lassen Sie das Experiment laufen und beenden.
- Öffnen Sie den Faraday Käfig.
- Entfernen Sie die Makroreferenz und die Gegenelektrode. Wischen Sie ihre Oberflächen trocken.
- Submerse die Makroelektroden in 3,5 M KCl Lösung für die Lagerung.
- Gießen Sie den verwendeten Elektrolyt in einen Abfallbehälter. Spülen Sie den Behälter mit DI-Wasser.
- Bedecken Sie das Öffnen des Acrylbehälters mit Parafilm zur Weiterverarbeitung.
Ergebnisse
Abbildung 1 zeigt eine 80 x 80 m Ag/AgCl-Elektrode mit einer nach diesem Protokoll hergestellten AgCl-Abdeckung von 50 %. Nach Beobachtung summiert sich die Fläche des AgCl-Patches auf etwa 68 x 52 m, was etwa 55 % der AgCl-Abdeckung entspricht. Dies zeigt, dass das Protokoll die Menge der AgCl-Abdeckung auf den Dünnschicht-Ag-Elektroden fein steuern kann. Die hergestellte AgCl-Schicht ist ebenfalls sehr glatt, wie das Verklumpen benachbarter AgCl-Partikel zeigt. Darüber hinaus ist die Schicht von AgCl nur eine einzige Schicht, was durch das Fehlen von gestapelten AgCl-Partikeln und einem markanten Ag/AgCl-Schnittpunkt belegt wird. Abbildung 2 zeigt erfolgreichere Beispiele für Dünnschicht-Ag/AgCl-Elektroden, die mit diesem Protokoll hergestellt wurden, die 80 x 80 m Elektroden mit einer ausgewiesenen AgCl-Abdeckung von 70 % und 30 % sind, zusammen mit 160 x 160 -m-Elektroden mit einer ausgewiesenen AgCl-Abdeckung von 75 % und 90 %, was die Robustheit dieses Protokolls bestätigt.

Abbildung 1: Exemplar SEM-Bild der Dünnschicht-Ag/AgCl-Elektrode mit einer Dimension von 80 x 80 m und einer als AgCl bezeichneten AgCl-Abdeckung von 50 %. Die beobachtete AgCl-Abdeckung beträgt 55%, was die Wirksamkeit des Protokolls demonstriert. Diese Zahl wurde von Tjon et al.13geändert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Exemplar SEM-Bilder von Dünnschicht-Ag/AgCl-Elektroden mit verschiedenen Elektrodenbereichen und AgCl-Abdeckungen. (A) 80 x 80 m mit 70 % AgCl-Abdeckung. (B) 80 x 80 m mit 30 % AgCl-Abdeckung. (C) 160 x 160 m mit 75% AgCl-Abdeckung. (D) 160 x 160 m mit 90 % AgCl-Abdeckung. Diese Zahlen wurden von Tjon et al.13geändert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Abbildung 3 zeigt ein negatives Ergebnis, bei dem der Polierschritt weggelassen wird (d. h. Schritt 4.2). Abbildung 3A zeigt eine polierte Elektrodenoberfläche, während Abbildung 3B eine unpolierte Elektrodenoberfläche zeigt. Bei der ungeschliffenen Elektrode können an der Oberfläche fingerähnliche Strukturen beobachtet werden, die in Abbildung 4dargestellt sind, wo die polierte Elektrodenoberfläche glatt ist und durch den Polierprozess leichte Kratzspuren aufweisen. Abbildung 5 zeigt eine ungeschliffene 80-m-x-80-Mm-Ag/AgCl-Elektrode mit einer entworfenen AgCl-Abdeckung von 50 %. Nach Beobachtung ergibt sich nur eine Fläche der spärlich abgedeckten AgCl von etwa 40 x 40 m, was 25 % der scheinbaren Elektrodenoberfläche entspricht. Darüber hinaus scheint die gebildete AgCl für die unpolierte Elektrode bei Abbildung 1, in der das Protokoll ordnungsgemäß eingehalten wird, nach innen eingelassen zu sein, anstatt nach außen zu ragen.

Abbildung 3: SEM-Bilder für blanke Silberelektroden. (A) Polierte 160-m-x-160-m-Elektrode (B) Unpolierte 40-m-x-40-m-Elektrode. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 4: Zoomed SEM-Bild für ungeschliffene Silberelektroden. Fingerähnliche Strukturen können beobachtet werden. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: Suboptimale Fertigung von Dünnschicht-Ag/AgCl-Elektroden. Ohne Polieren ist der Erfassungsgrad des gebildeten AgCl auf der Oberfläche der Elektrode kleiner als der vorhergesagte Wert. Die entworfene AgCl-Abdeckung für diese 80 x 80 m dünne Silberelektrode beträgt 50 %, die tatsächliche Abdeckung jedoch nur 25 %. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
Die physikalischen Eigenschaften einer Ag/AgCl-Elektrode werden durch die Morphologie und die Struktur der auf der Elektrode abgelagerten AgCl gesteuert. In diesem Beitrag haben wir ein Protokoll zur präzisen Steuerung der Abdeckung einer einzelnen Schicht von AgCl auf der Oberfläche der Silberelektrode vorgestellt. Ein integraler Bestandteil des Protokolls ist eine modifizierte Form des Faraday-Gesetzes der Elektrolyse, das verwendet wird, um den Grad von AgCl auf den Dünnschicht-Silberelektroden zu steuern. Es kann wie:
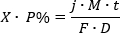
Wobei X die Dicke einer einzelnen AgCl-Schicht in cm ist (350 nm = 3,5 x 10-5 cm); P% ist der Prozentsatz der AgCl-Abdeckung auf der Oberfläche der Ag-Elektrode (100% = volle Abdeckung); j ist die angewendete Stromdichte in A/cm2 (0,5 mA/cm2), M ist das Molgewicht von AgCl (143,5 g/mol), t ist die Dauer der Eloxierung in s (262 s für 100% Abdeckung); F ist die Konstante des Faraday (96485 C/mol); D ist die Dichte von AgCl (5,56 g/cm3). Um den Erfolg des Protokolls sicherzustellen, müssen mehrere kritische Schritte im Protokoll beachtet werden. Schritt 4.2, bei dem es um das Polieren der Oberfläche der Dünnschicht-Silberelektrode geht, ist entscheidend, um die Oberfläche der Elektrode vor der galvanisch-bildung von AgCl auf der Elektrodenoberfläche zu definieren. Aus Abbildung 3 und Abbildung 4ist der Unterschied in der Oberflächenstruktur und Rauheit der durch Sputtern hergestellten Dünnschicht-Silberelektroden deutlich zu erkennen; Die ungeschliffene Silberoberfläche hat fingerartige Strukturen, während die polierte Silberoberfläche meist glatt ist und kleinere Kratzspuren durch Schleifpapierreiben verursacht. Dies schafft ein großes Problem, da die fingerartigen Strukturen effektiv die Oberfläche der Elektrode erhöhen. Dies macht die Bestimmung der Oberfläche der Elektrode und anschließend den Grad der AgCl-Abdeckung auf der Elektrode unmöglich. Die Seffect ist in Abbildung 1 und Abbildung 5gut dargestellt. Die protokollkonforme Ag/AgCl-Elektrode hat eine glatte, einschichtige AgCl-Schicht mit einer gut kontrollierten AgCl-Abdeckung, während die Elektrode ohne Beachtung des Polierschritts eine überschätzte Abdeckung von AgCl auf der Elektrode hat. Schritt 8.6.2, bei dem es um die Verwendung einer konstanten2 Stromdichte von 0,5 mA/cm2 zur Bildung der AgCl-Schicht auf der Dünnschicht-Ag-Elektrode geht, ist entscheidend, um eine glatte AgCl-Schicht mit einschichtigem Dicken zu erzeugen. Neu gebildete AgCl Ablagerungen an den Rändern der bestehenden AgCl auf der Oberfläche aufgrund seiner niedrigen Energie7,8. Dadurch können die AgCl-Partikel zunächst eine einzige Schicht bilden, bevor sie dicker werden. Wenn jedoch während der galvananostatischen Bildung der AgCl-Schicht eine hohe Stromdichte angewendet wird, könnte die neu gebildete AgCl genügend Energie haben, um sich direkt auf der Elektrode als entlang der vorhandenen AgCl-Kanten zu bilden, wodurch eine rauere AgCl-Oberfläche14entsteht. Dies macht den Grad der AgCl-Abdeckung auf der Elektrode nicht zu kontrollieren, da die AgCl-Formationsstellen unter solchen Bedingungen nicht vorhergesagt werden können. Dies macht auch die Bestimmung der AgCl-Oberfläche unmöglich, da ihre Rauheit die Oberfläche beeinflusst, was gezeigt hat, dass sie die Impedanzeigenschaften der Elektrode in unserer vorherigen Arbeitbeeinflusst 13.
Es gibt mehrere Möglichkeiten, um zu beheben, ob eine einzelne Ebene von AgCl richtig gebildet ist. Erstens, um zu überprüfen, ob der Polierschritt erfolgreich durchgeführt wird. Die Probe sollte nach dem Polierschritt unter einem SEM-Mikroskop ohne Goldbeschichtung beobachtet werden, um festzustellen, ob die Fingerstruktur durch eine glatte Oberfläche ersetzt wird. Wenn die Oberfläche der Elektrode vollständig mit AgCl bedeckt ist, führt eine weitere galvananostatische Oxidation zu einer plötzlichen Erhöhung des aufgebrachten Potentials auf das System, da die Verdickung der AgCl den ohmschen Widerstand der AgCl-Schicht erhöht. Damit kann ermittelt werden, ob die Oberfläche der Elektrode bereits vollständig mit AgCl bedeckt ist.
Es gibt eine wesentliche Einschränkung in Bezug auf die Verwendung dieser Methode, um Dünnschicht-Ag/AgCl-Elektroden mit guter Kontrolle der AgCl-Abdeckung herzustellen. Elektroden, die mit dieser Methode hergestellt werden, sind nicht überarbeitbar. Während des Prozesses der galvanisch-oxidation der Silberelektrode zur AgCl-Ablagerungsschicht werden die Stellen der Unvollkommenheit auf der Oberfläche der Elektrode in unvorhersehbarer Weise größer. Wenn die Elektrode reduziert wird, um AgCl wieder auf Ag zurückzusetzen, kann sie nicht garantieren, dass diese Stellen an der Elektrodenoberfläche wieder so gefüllt werden, wie sie war. Stattdessen wird die Oberfläche rauer. Wenn die Oberfläche nach einem Nacharbeiten mit Schleifpapier neu poliert wird, wird beim Polieren etwas Silber von der Oberfläche entfernt. Daher kann man dies nur für ein paar Mal tun, bevor die darunter liegende Goldschicht freigelegt wird.
Diese Methode konzentriert sich im Vergleich zu typischen Ag/AgCl-Elektrodenherstellungsverfahren auf eine feine Kontrolle der Abdeckung von AgCl auf der Oberfläche der Dünnschicht-Ag-Elektrode, während andere Methoden sich auf die Erstellung einer porösen Schicht von AgCl konzentrieren. Nach bestem Wissen des Autors ist dies das erste Mal, dass ein Protokoll entwickelt wird, um eine einzelne Schicht fein gesteuerter AgCl auf einer Silberelektrode herzustellen. Dies ist auf unterschiedliche Designziele zurückzuführen. Die meisten früheren Arbeiten zielten darauf ab, eine Referenz-Ag/AgCl-Elektrode mit hoher Elektrodenpotentialstabilität zu erreichen, während unser Protokoll darauf abzielt, die Sensor-Ag/AgCl-Elektrode mit geringer Kontaktimpedanz für Impedanz-Sensorsysteme wie Impedanz-Flow-Zytometer und interdigitierte Elektroden-Arrays zu entwerfen.
Zukünftige Experimente können einen ausgeklügelteren Polierschritt umfassen, z. B. mit einem Poliersystem, um eine noch glattere Oberfläche zu erzielen. Weitere Untersuchungen können auch durchgeführt werden, um den quantitativen Zusammenhang zwischen der Dicke der AgCl-Schicht und der Faraday-Gleichung der Elektrolyse zu bewerten.
Offenlegungen
Die Autoren haben nichts zu verraten.
Danksagungen
Diese Arbeit wurde durch ein Stipendium des RGC-NSFC Joint Fund unterstützt, der vom Research Grants Council of Hong Kong gesponsert wurde (Projekt Nr. N_HKUST615/14). Wir möchten Die Nanosystem Fabrication Facility (NFF) von HKUST für die Geräte-/Systemfertigung würdigen.
Materialien
| Name | Company | Catalog Number | Comments |
| AST Peva-600EI E-Beam Evaporation System | Advanced System Technology | For Cr/Au Deposition | |
| AZ 5214 E Photoresist | MicroChemicals | Photoresist for pad opening | |
| AZ P4620 Photoresist | AZ Electronic Materials | Photoresist for Ag liftoff | |
| Branson/IPC 3000 Plasma Asher | Branson/IPC | Ashing | |
| Branson 5510R-MT Ultrasonic Cleaner | Branson Ultrasonics | Liftoff | |
| CHI660D | CH Instruments, Inc | Electrochemical Analyser | |
| Denton Explorer 14 RF/DC Sputter | Denton Vacuum | For Ag Sputtering | |
| FHD-5 | Fujifilm | 800768 | Photoresist Development |
| HPR 504 Photoresist | OCG Microelectronic Materials NV | Photoresist for Cr/Au liftoff | |
| Hydrochloric acid fuming 37% | VMR | 20252.420 | Making diluted HCl for cathodic cleaning |
| J.A. Woollam M-2000VI Spectroscopic Elipsometer | J.A. Woollam | Measurement of silicon dioxide passivation layer thickness on dummy | |
| Multiplex CVD | Surface Technology Systems | Silicon dioxide passivation | |
| Oxford RIE Etcher | Oxford Instruments | For Pad opening | |
| Potassium Chloride | Sigma-Aldrich | 7447-40-7 | Making KCl solutions |
| SOLITEC 5110-C/PD Manual Single-Head Coater | Solitec Wafer Processing, Inc. | For spincoating of photoresist | |
| SUSS MA6 | SUSS MicroTec | Mask Aligner | |
| Sylgard 184 Silicone Elastomer Kit | Dow Corning | Adhesive for container on chip |
Referenzen
- Bakker, E., Telting-Diaz, M. Electrochemical sensors. Analytical Chemistry. 74 (12), 2781-2800 (2002).
- Jobst, G., et al. Thin-Film Microbiosensors for Glucose-Lactate Monitoring. Analytical Chemistry. 68 (18), 3173-3179 (1996).
- Matsumoto, T., Ohashi, A., Ito, N. Development of a micro-planar Ag/AgCl quasi-reference electrode with long-term stability for an amperometric glucose sensor. Analytica Chimica Acta. 462 (2), 253-259 (2002).
- Suzuki, H., Hirakawa, T., Sasaki, S., Karube, I. An integrated three-electrode system with a micromachined liquid-junction Ag/AgCl liquid-junction Ag/AgCl reference electrode. Analytica Chimica Acta. 387 (1), 103-112 (1999).
- Ives, D. J. G., Janz, G. J. . Reference Electrodes - theory and practice. , (1961).
- Huynh, T. M., Nguyen, T. S., Doan, T. C., Dang, C. M. Fabrication of thin film Ag/AgCl reference electrode by electron beam evaporation method for potential measurements. Advances in Natural Sciences: Nanoscience and Nanotechnology. 10 (1), 015006 (2019).
- Katan, T., Szpak, S., Bennion, D. N. Silver/silver chloride electrode: Reaction paths on discharge. Journal of The Electrochemical Society. 120 (7), 883-888 (1973).
- Katan, T., Szpak, S., Bennion, D. N. Silver/silver chloride electrodes: Surface morphology on charging and discharging. Journal of The Electrochemical Society. 121 (6), 757-764 (1974).
- Polk, B. J., Stelzenmuller, A., Mijares, G., MacCrehan, W., Gaitan, M. Ag/AgCl microelectrodes with improved stability for microfluidics. Sensors and Actuators B: Chemical. 114 (1), 239-247 (2006).
- Mechaour, S. S., Derardja, A., Oulmi, K., Deen, M. J. Effect of the wire diameter on the stability of micro-scale Ag/AgCl reference electrode. Journal of The Electrochemical Society. 164 (14), E560-E564 (2017).
- Brewer, P. J., Leese, R. J., Brown, R. J. C. An improved approach for fabricating Ag/AgCl reference electrodes. Electrochimica Acta. 71, 252-257 (2012).
- Safari, S., Selvaganapathy, P. R., Derardja, A., Deen, M. J. Electrochemical growth of high-aspect ratio nanostructured silver chloride on silver and its application to miniaturized reference electrodes. Nanotechnology. 22 (31), 315601 (2001).
- Tjon, K. C. E., Yuan, J. Impedance characterization of silver/silver chloride micro-electrodes for bio-sensing applications. Electrochimica Acta. 320, 134638 (2019).
- Pargar, F., Kolev, H., Koleva, D. A., van Breugel, K. Microstructure, surface chemistry and electrochemical response of Ag | AgCl sensors in alkaline media. Journal of Materials Science. 53 (10), 7527-7550 (2018).
- Hassel, A. W., Fushimi, K., Seo, M. An agar-based silver | silver chloride reference electrode for use in micro-electrochemistry. Electrochemistry communications. 1 (5), 180-183 (1999).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten