Method Article
Spore-Adsorption als ein Nonrecombinant Display-System für Enzyme und Antigene
In diesem Artikel
Zusammenfassung
Dieses Protokoll konzentriert sich auf die Verwendung von Bakteriensporen als "live" nanobiotechnologische Werkzeug zu adsorbieren, heterologe Moleküle mit verschiedenen biologischen Aktivitäten. Die Methoden zur Messung der Effizienz der Adsorption werden ebenfalls angezeigt.
Zusammenfassung
Die bakterielle Spore ist ein metabolisch ruhenden Zelle, durch eine Reihe von Schutzschichten, die rund um eine dehydrierte Zytoplasma gebildet. Diese eigenartige Struktur macht die Spore, extrem stabil und widerstandsfähig und hat vorgeschlagen, die Verwendung von der Spore als Plattform zur heterologen Moleküle anzuzeigen. So weit, eine Vielzahl von Antigenen und Enzyme angezeigt worden auf Sporen von Bacillus Subtilis und ein paar andere Arten zunächst durch einen rekombinanten Ansatz und dann durch eine einfache und effiziente Methode, nonrecombinant. Nonrecombinant Display-System basiert auf der direkten Adsorption von heterologen Moleküle auf der Oberfläche von Spore, den Bau von rekombinanten Stämme und die Freisetzung von gentechnisch veränderten Bakterien in der Umwelt zu vermeiden. Adsorbierten Moleküle sind stabilisiert und geschützt durch die Interaktion mit Sporen, die den raschen Abbau von Antigenen und den Verlust der Enzymaktivität bei ungünstigen Bedingungen begrenzt. Wenn, können für zusätzliche Reaktion runden Spore adsorbiert Enzyme leicht mit einer minimalen Reduktion der Aktivität gesammelt und wiederverwendet werden. In diesem Papier wird gezeigt, wie zu adsorbieren, Modell Moleküle an gereinigten Sporen von B. Subtilis, wie die Effizienz der Adsorption bewerten und sammeln von gebrauchten Sporen um sie für neue Reaktionen zu recyceln.
Einleitung
Display-Systeme sollen biologisch aktive Molekülen auf der Oberfläche von Mikroorganismen zu präsentieren und finden Anwendungen in den unterschiedlichsten Bereichen von Industrie, Medizin- und Umwelttechnik Biotechnologien. Neben Phagen1,2 und Zellen von verschiedenen gram-positive Art3,4,5,6,7, wurden ebenfalls Bakteriensporen als Display-Systeme von zwei Ansätze8,9vorgeschlagen.
Wegen seiner besonderen Struktur, nämlich eine dehydrierte Zytoplasma umgeben von einer Reihe von Schutzschichten10, bietet die Spore mehrere Vorteile gegenüber Phagen und zellbasierte Display Systeme8,9. Ein erste Vorteil ist die extreme Robustheit und Stabilität der Sporen zu Konditionen, die für alle anderen Zellen10,11schädlich wäre. Spore-Anzeige Antigene und Enzyme sind stabil, nach längerer Lagerung bei Raumtemperatur12 und vor Abbau bei niedrigem pH-Wert und hohen Temperaturen13 geschützt. Ein zweiter Vorteil der Sporen ist die Sicherheit vieler Spore-bildenden Arten. B. Coagulans, B. Subtilis, B. Clausiiund mehrere andere Arten werden weltweit als Probiotika verwendet und wurden auf dem Markt für den menschlichen oder tierischen Einsatz für Jahrzehnte14,15. Diese außergewöhnliche Sicherheitsbilanz ist eine offensichtliche allgemeine Voraussetzung für ein DGM-Anzeige-System und ist von besonderer Bedeutung, wenn das System für menschlichen oder tierischen Gebrauch16vorgesehen ist. Ein Drittel ist wichtiger Vorteil der eine Spore-basierte Display-System, dass es keinen Beschränkungen für die Größe des Moleküls, die ausgesetzt werden. In Phagen-basierten Systemen eine große heterologen Proteinen beeinträchtigen die Struktur der das Kapsid während in Zell-basierte Systeme, es kann Einfluss auf die Struktur der Membran oder Grenze/beeinträchtigen können die Membran Translokation Schritt17. Rund um die Spore Schutzschichten bestehen aus mehr als 70 verschiedene Proteine10 und sind flexibel genug, um große Fremdeiweiße ohne offensichtlich Konstruktionsfehler oder Funktionsbeeinträchtigung8akzeptieren. Darüber hinaus ist die Membran Translokation des heterologen Proteins mit beiden Spore-basierte Display-Systeme nicht erforderlich8,9. In der Tat heterologen Proteine entweder in der Mutterzelle Zytoplasma hergestellt und montiert auf der Spore, die im gleichen Zytoplasma bildet oder adsorbiert an der Reifen Spore8,9.
Spore-Anzeige wurde zunächst durch die Entwicklung einer genetischen Systems um die Spore Oberfläche18Ingenieur erhalten. Dieses genetische System beruhte auf i) den Bau einer gen-Fusion zwischen der gen-Codierung für eine Spore-Hüllprotein (verwendet als Träger) und für das Protein zu kodierenden gen angezeigt - die transkriptionelle und translationale Signale von der endogenen gen steuert den Ausdruck der Verschmelzung und Ii) Integration von Chimären gen auf dem Chromosom B. Subtilis , genetische Stabilität zu gewähren. Eine Vielzahl von Antigenen und Enzyme dieser rekombinanten Ansatz, mit verschiedenen Spore Oberflächenproteine als Träger und mit dem Ziel verschiedene Anwendungsmöglichkeiten, von Schleimhaut Impfstoff bis hin zu Biokatalysator, Biosensor, Bioremediation, angezeigt worden oder bioanalytische Tool8,13.
Vor kurzem wurde ein anderer Ansatz von Spore Display entwickelten19. Diese zweite System ist nonrecombinant und stützt sich auf die spontane und extrem engen Adsorption der Moleküle auf der Oberfläche Spore-9. Antigene19,20 und Enzyme13,21 effizient angezeigt worden und haben gezeigt, dass diese Methode ist wesentlich effizienter als die rekombinante. Dieser nonrecombinant Ansatz ermöglicht die Darstellung von Proteinen in gediegener Form20 und kann auch verwendet werden, mit autoklaviert, Tod Sporen19. Der molekulare Mechanismus der Adsorption ist noch nicht vollständig geklärt. Die negative Ladung und der Hydrophobie der Spore wurden als relevanten Eigenschaften für die Adsorption13,19,22vorgeschlagen. Vor kurzem hat sich gezeigt, dass ein Modell-Protein, das rote Autofluorescent Protein (mRFP) von den Korallen Discosoma, wenn um die Spore, adsorbiert durch die Lokalisierung in der inneren Schicht23Oberflächenschichten zu infiltrieren konnte. Wenn auch für andere Proteine nachgewiesen, erklären die internen Lokalisierung der heterologen Proteine ihre erhöhte Stabilität wenn Sporen23adsorbiert.
In einer aktuellen Studie zwei Enzyme katalysieren zwei aufeinander folgenden Schritten des Xylan-Abbau-Signalwegs waren unabhängig voneinander auf Sporen von B. Subtilis angezeigt und wenn gemeinsam inkubiert wurden beide Abbau Schritte21durchführen. Sporen gesammelt, nachdem die Reaktion waren noch aktiv und können weiterhin die Xylan-Abbau auf die Zugabe von frischem Substrat21. Selbst wenn ein Verlust von etwa 15 % des Endprodukts in der zweiten Reaktion21beobachtet wurde, ist die Wiederverwendbarkeit von adsorbierten Enzyme für einzelne, als auch Multi-Step Reaktionen ein weiterer wichtiger Vorteil der Spore-Display-System.
Pan Et Al.24 berichtete eine weitere Annäherung an heterologen Proteine auf der Oberfläche der Spore anzeigen: heterologe Proteine (ein Endoglucanase Protein und ein Beta-Galaktosidase man) in die Mutterzelle in Sporenbildung erzeugt wurden spontan eingehüllt in den bildenden Spore-Mantel, ohne die Notwendigkeit eines Trägers. Diese zusätzliche Spore-Display-System ist eine Kombination der beiden Ansätze bisher beschriebenen. Tatsächlich ist es rekombinante, da die heterologe Proteine entwickelt wurden, um in der Mutterzelle während der Sporenbildung, ausgedrückt werden, während deren Montage innerhalb der Mantel spontan war und daher nonrecombinant24. Jedoch bleibt die Effizienz der Anzeige dieses zusätzliche Ansatzes getestet und verglichen mit den anderen beiden Ansätzen mithilfe der gleichen heterologen Proteinen.
Dieses Protokoll schließt die Prozesse der Spore Produktion und Reinigung, die wurden ausführlich an anderer Stelle beschrieben24. Freuen Sie sich auf die Adsorption Reaktion, die Bewertung der Effizienz der Adsorption von Dot-Blot und Fluoreszenz-Mikroskopie und rundet das recycling von adsorbierten Enzyme für zusätzliche Reaktion.
Protokoll
1. Adsorption Reaktion
- Inkubieren Sie 2, 5 und 10 µg des mRFP mit 2 x 109 von B. Subtilis Wildtyp gereinigte Sporen in 200 µL Puffer, 50 mM Natriumcitrat, pH 4.0 (16,7 mM Natriumcitrat Dihydrat; 33,3 mM Zitronensäure) für 1 h bei 25 ° C auf einem schaukelnden Shaker (Abbildung 1) verbindlich .
- Zentrifugieren Sie die Bindung Mischungen (13.000 X g für 10 min) um Pellets (P2, P5 und P10) und Überstände (S2, S5 und S10) fraktionieren. Speichern Sie die Überstände für die indirekte Bewertung der Effizienz der Adsorption im Schritt 3.2 beschrieben.
- Waschen Sie die Pellets 2 X mit 200 µL Puffer und Aufschwemmen in 100 µL der Bindung zu puffern und nutzen es für die nächste Analyse zu binden.
Hinweis: Die verbindliche Reaktion tritt bevorzugt bei einem pH Wert niedriger als der isoelektrischen Punkt des Proteins; in der Regel 1,5 M Phosphat-gepufferte Kochsalzlösung (PBS), pH-Wert 4,0 oder 50 mM Natrium-Citrat, pH 4.0 verwendet.
2. direkte Aussage über die Effektivität der adsorption
-
Gewinnung von Oberflächenproteinen und western-Blot Analyse
- Nehmen Sie 50 µL des mRFP adsorbiert Sporen Wiederfreisetzung (P2, P5 und P10 Schritt 1.3) und fügen 50 µL 2 x Natrium-Dodecyl-Sulfat (SDS)-Dithiothreitol (DTT) (0,1 M Tris-HCl, pH 6,8; 2 % SDS; 0,1 M DVB-t) zur Oberfläche Spore Proteine lösen.
- Mithilfe der frei, gereinigte mRFP und Extrakte die gleichen Mengen von Sporen, die nicht an das Protein als positive und negative Kontrollen bzw. adsorbiert werden.
- Nach 45 min Inkubation bei 65 ° C, Zentrifugieren (13.000 X g für 10 min.) die Mischungen und analysieren 10 µL der extrahierten Proteine (überstand) durch western-Blot mit dem monoklonalen Anti-His Antikörper erkennen seine Tag an der N-terminalen des mRFP ( Abbildung 2A).
-
Fluoreszenz-Mikroskopie Beobachtungen
Hinweis: Durch Verwendung von fluoreszierenden heterologen Proteinen oder Durchführung einer Immunfluoreszenz-Analyse, ist es möglich zu lokalisieren und zu quantifizieren die adsorbierten Moleküle durch Fluoreszenz-Mikroskopie.- Nehmen Sie 5 µL der adsorbierten Sporen Wiederfreisetzung aus Schritt 1.3 und 95 µL 1 X PBS, pH 4.0 ~ 1 x 106 Sporen/µL zu erhalten.
- Platz 5 µL einer Aussetzung auf einen Objektträger, bedecken Sie es mit einem Deckgläschen vorher behandelt mit Poly-l-Lysin für 30 s, und unter dem Fluoreszenzmikroskop beobachten.
- Für jedes Feld speichern Sie die Phasenkontrast-Mikroskopie Bild und Fluoreszenz-Mikroskopie-Bild (Abbildung 2B).
Hinweis: Alternativ können fluoreszierende Sporen von Cytofluorimetry analysiert werden. Aufschwemmen insgesamt 106 Sporen adsorbiert oder mit dem heterologes Protein in 1 mL 1 X PBS, pH 4.0, nicht adsorbiert und analysieren die Suspension mit einem Durchflusszytometer (Abbildung 2C).
-
Datenanalyse mit ImageJ
- Die Fluoreszenz-Mikroskopie-Bilder mit ImageJ-Software (http://rsbweb.nih.gov/ij/) und sicherstellen, dass alle Bilder sind in der 8-Bit-Format zu öffnen (Bild | Typ | 8-Bit).
- Passen Sie den Kontrast, wenn nötig (Bild | Anpassen | Helligkeitskontrast) und stellen Sie sicher, dass die Skalierung des Bildes PIXEL (Bild | Skala).
- Wählen Sie im Menü Analyze Set Messungen. Stellen Sie sicher , Integrierte Dichteund Grau Mittelwert ausgewählthaben.
- Zeichnen Sie eine Linie um die Spore von Interesse mit der Zeichnung/Auswahl-Werkzeuge (z. B. Kreis, Polygon, oder Freiform) (Abbildung 3).
- Wählen Sie die Kennzahl aus Menü "Analyze" (oder drücken Sie Cmd + M). Ein Popup-Fenster mit einem Stack von Werten für diese erste Spore erscheint (Abbildung 3).
- Wiederholen Sie diese beiden Schritte für mindestens 50 andere Sporen in das Sichtfeld zu messenden gewählt.
- Wählen Sie mehrere Regionen ohne irgendwelche Sporen (die keine Fluoreszenz) und wiederholen Sie die Messung; Dies wird der Hintergrund sein.
Hinweis: Die Größe ist nicht wichtig. Diese entsprechenden Hintergrund-Fluoreszenz-Werte werden manuell Hintergrund subtrahieren verwendet werden. - Wählen Sie die Daten im Fenster Ergebnisse und kopieren Sie die Ergebnisse in ein Arbeitsblatt.
- Berechnen Sie den Mittelwert des Integrierten Dichte und Bereich der ausgewählten Sporen und der Hintergrund Fluoreszenz Werte und nutzen sie, um die korrigierte Summe pro Zelle Fluoreszenz (CTCF) mit der Formel erhalten: CTCF = mittlere integrierte Dichte - (mittlere Bereich x mittlere Hintergrundfluoreszenz).
Hinweis: Alternativ, wenn die Sporen gut getrennt erscheinen, ist es möglich, die Sporen über das Bildfeld, die mit der Funktion Analysieren Partikel, folgende ImageJ Anweisung zu analysieren. Um zu vermeiden, dass die Software eine bestimmte Fluoreszenz oder Spore Aggregate liest, muss die Dimension der Partikel im pixelˆ2 eingestellt werden = 50-200 (Abbildung 4).
3. indirekte Aussage über die Effektivität der adsorption
- Verdünnungsreihen für das gereinigte Protein vorzubereiten.
- Bereiten Sie eine erste 1,5 mL-Tube mit 250 µL des gereinigten mRFP auf eine Endkonzentration von 0,5 ng/µL, mit Bindung Puffer. Dieses Volumen ist ausreichend, um zwei Fahrspuren zu laden.
- Führen Sie sechs zweifache Verdünnungsreihen von jeweils 250 µL (Endvolumen) mit der Bindung Puffer.
- Bereiten Sie zweifache Verdünnungsreihen für den Überstand Proben mit dem ungebundenen mRFP Bruchteil der Adsorption Reaktion (S2, S5 und S10 aus Schritt 1.2).
- 100 µL jeder Überstand in ein 1,5 mL-Tube und fügen Sie 100 µL Bindung Puffer hinzu. Führen Sie sechs zweifache Verdünnungsreihen von jeweils 200 µL (Endvolumen) mit der Bindung Puffer.
- Schneiden Sie eine Nitrozellulose Membran (0,45 µm cutoff), 9 x 10 cm in der Größe, um den Bereich von 5 (Anzahl der Proben) x 6 (Anzahl der Verdünnungen) Punkte abdecken. Die Membran sollte nicht über den Rand der Dichtung der Dot-Blot Vorrichtung hinausgehen.
- Legen Sie die prewet Membran in der Dot-Blot-Vorrichtung. Entfernen Sie eventuelle Luftblasen eingeschlossen zwischen der Membran und der Dichtung. Decken Sie den unbenutzten Teil des Apparates mit Klebeband oder Paraffin Film zu verhindern, dass Luft durch diese Brunnen bewegt.
- Montieren Sie den Dot-Blot Apparat wie vom Hersteller beschrieben.
- Wenn ein Vakuum bei der Montage verwendet wird, rehydrieren Sie die Membran mit 100 µL 1 X PBS pro Bohrloch für die einheitliche Bindung des Antigens zu gewährleisten und verhindern, dass Halos oder eine schwache Erkennungssignal.
- Entfernen Sie vorsichtig den Puffer aus den Vertiefungen durch Vakuum. Sobald die Pufferlösung aus den Brunnen fließt, die Vakuumpumpe zu stoppen und trennen.
- Laden Sie den Standard in den meisten externen zweispurig und die Proben in der Mitte (Abbildung 5). Füllen Sie die entsprechenden Vertiefungen mit 100 µL jeder Verdünnung. Das gleiche Volumen für jede Vertiefung verwendet sollte eine homogene Filterung von allen Probe Brunnen sicherstellen.
- Schalten Sie die Vakuumpumpe für 2 min, Hör auf, und führen Sie das Beispiel, durch die Membran durch Schwerkraft zu filtern.
- Waschen Sie alle Brunnen mit 100 µL 1 x PBS und lassen Sie die Vakuumpumpe für weitere 5 Minuten nachlaufen der Wasch-Puffer vollständig aus dem Gerät abgelassen wurde.
- Lösen Sie mit dem Vakuum auf die Schrauben und öffnen Sie vorsichtig den Dot-Blot Apparat.
- Schalten Sie das Vakuum, nehmen Sie die Membran zu und nach ein western-Blot-Protokoll zu verarbeiten.
- Führen Sie eine densitometrische Analyse des Filters, mittels geeigneter Software, wie z. B. ImageJ.
- Messen Sie die integrierte Dichte jedes Punktes gliedern sie mit einem Kreis des gleichen Gebietes und verwenden den Befehl Analyze/messen .
- Machen Sie eine Hintergrundkorrektur des Bildes, Zeichnen eines Kreises in einen leeren Bereich und seine integrierte Dichte zu messen oder den Prozess/subtrahieren Hintergrund Befehl.
- Korrelieren Sie die integrierte Dichte der standard Punkte mit geladenen Eiweißmenge und erhalten Sie eine Kalibrierungslinie (R2 Werte für die Kalibrierung, die Kurven über 0,95 sein sollte).
- Verwenden Sie die Eichkurve, um die Konzentration des mRFP von jeder Probe Punkt zu extrapolieren.
- Berechnen Sie die Konzentration der mRFP bleiben in den ungebundenen Fraktionen.
Hinweis: Um die korrekte Schließung der Dot-Blot-Apparat und daher zum Thema der Membran ein gleichmäßiger Druck ziehen Sie die Schrauben durch die diagonal gekreuzten Schema und, öffnen Sie dann die Vakuumpumpe, um die Schrauben noch stärker.
4. spore Sammlung und Wiederverwendung
- Führen Sie für das recycling von adsorbierten Spore zwei Adsorption Reaktionen von 2.0 x 109 gereinigt Sporen mit 10 µg des gereinigten GH10-XA Xylanase oder 10 µg des gereinigten GH3-XT β-Enzym, wie beschrieben in Schritten 1.1-1.3(Abbildung 6).
- Sammeln Sie die Pellets mit dem Enzym adsorbiert Sporen, Aufschwemmen sie in 50 µL des Puffers für die enzymatische Reaktion-Assay (50 mM-Natrium-Phosphat-Puffer bei pH 6,5; 2,48689 g/L Na2HPO4, 4,88991 g/L NaH2PO4), optimale und mischen sie zusammen, um eine 100 µL Mischung von Sporen adsorbierenden GH10-XA oder GH3-XT zu erhalten.
- Das Substrat (5 mg/mL 4-O-methyl-d-glucuronod-xylan [MGX]) und lassen Sie die Enzymreaktionen statt 16 h bei 65 ° C.
- Zentrifugieren Sie das Reaktionsgemisch (für 15 min bei 13.000 X g) und speichern Sie den Überstand enthält das Enzym Reaktionsprodukt zu.
- Aufschwemmen Sie das Pellet in 100 µL der frischen 50 mM Natrium-Phosphat-Puffer bei pH 6,5 in der Gegenwart ein neues Substrat (MGX) (Abb. 6B).
Hinweis: Um mehr als ein Enzym adsorbieren, ist es möglich, beide zusammen adsorbieren oder eins nach dem anderen unabhängig. Die letztgenannte Möglichkeit erleichtert die Quantitative Analyse der Adsorption Effizienz und der Tätigkeit der jedes Enzym, so dass eine stöchiometrische Balance jedes Enzym benötigt für die Reaktionen.
Ergebnisse
Erfolgreiche Adsorption kann durch westliche Beflecken beurteilt werden. Auf die Reaktion die Mischung wird durch Zentrifugation fraktioniert und gewaschen, und der Pellet-Bruch (Abbildung 1) wird verwendet, um die Oberflächenproteine zu extrahieren. Der Extrakt ist von SDS Polyacrylamid Gelelektrophorese (PAGE), Electrotransferred ein Polyvinylidene Fluorid (PVDF) Membran, fraktioniert und gegen primäre und sekundäre Antikörper reagiert. Das Vorhandensein von Proteinen der erwarteten Größe, nur auf der Spur, geladen mit einem Auszug der adsorbierten Sporen, ist bezeichnend für eine erfolgreiche Adsorption Reaktion (Abb. 2A).
Die Effizienz der Adsorption Reaktion kann durch direkte und indirekte Methoden ausgewertet werden. Die direkte Auswertung der Adsorption Effizienz hängt von der heterologen Protein, das verwendet wurde und von Fluoreszenz-Mikroskopie (Abbildung 2B) und Cytofluorimetry (Abbildung 2C) auf den Pellet-Bruch durchgeführt werden kann nach der Fraktionierung der Adsorption Reaktion. Eine Quantifizierung der fluoreszierenden Signale auf Sporen kann durchgeführt werden, mithilfe der ImageJ-Software (Abbildung 3 und Abbildung 4). Eine indirekte Analyse der Effizienz Adsorption erfolgt durch eine Dot-Blot-Analyse (Abb. 5A) von der Überstand Fraktion mit dem ungebundenen Protein (Abbildung 1). Eine densitometrische Analyse des ungebundenen Proteins (Abb. 5B) können dann Wissenschaftler, indirekt die Menge des Proteins adsorbiert an Sporen zu berechnen.
Zwei aufeinander folgende Reaktionen können durch eine Mischung aus Sporen anzeigen entweder eines der beiden bestimmte Enzyme(Abbildung 6)katalysiert. Die adsorbierten Enzyme(s) können mit einem einfachen Zentrifugationsschritt, gewaschen und mit frischem Substrat für einen neuen Reaktionszyklus (Abb. 6B) inkubiert gesammelt werden.

Abbildung 1:allgemeine Systematik der Adsorption Experiment. Bitte klicken Sie hier für eine größere Version dieser Figur.
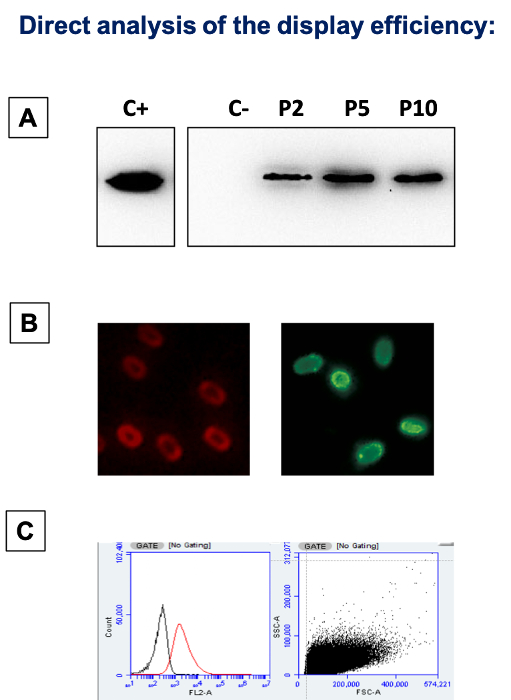
Abbildung 2 : Direkte Analyse der Effizienz des mRFP Displays. (A) Western-blot mit mRFP-spezifischen Antikörper. C + = frei gereinigtes mRFP; C - = ein Proteinextrakt aus Sporen nicht adsorbiert an das Protein; P2/P5/P10 = Proteine aus B. Subtilis Sporen adsorbiert mit 2, 5 und 10 mg des mRFP, bzw. extrahiert. (B) Immunfluoreszenz-Mikroskopie des adsorbierten Sporen. Immunoreactions wurden mit einem primären Antikörper erkennen die adsorbierten Protein und mit einem fluoreszierenden Sekundärantikörpers konjugiert mit Fluorescein erfolgt (FITC) durchgeführt. Die linke Tafel zeigt der rote intrinsische mRFP Fluoreszenz im Rechte Bereich zeigt die grüne Fluoreszenz der FITC-konjugierten Sekundärantikörper. (C) fließen durchflusszytometrischen Analyse der adsorbierten Sporen. Die Sporen mit mRFP-spezifische Antikörper und mit FITC-konjugierten Sekundärantikörper reagiert und dann analysiert wurden durch Cytofluorimetry. Die Analyse wurde auf die gesamte Spore Bevölkerung (10.000 Veranstaltungen, ungated) durchgeführt. Im linken Fenster werden nicht adsorbiert Sporen in schwarz, mRFP adsorbiert Sporen in rot angezeigt. Im Rechte Bereich zeigt den vorderen und seitlichen (FSC-SSC) Dot Streudiagramm. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 3: manuelle Quantifizierung der das Fluoreszenzsignal von ImageJ. Eine Fluoreszenz-Mikroskopbild von Sporen, adsorbiert mit rot fluoreszierende Protein-mRFP, mit ImageJ Software analysiert. Ein gelber Kreis wurde um eine Spore densitometrische Daten (vergrößertes Bild) gezogen. Das Popup-Fenster zeigt die Ergebnisse der densitometrische Analyse der ausgewählten Spore. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 4: gleichzeitige Quantifizierung der das Fluoreszenzsignal von ImageJ. (A) Popup-Fenster zu erhalten, bei der Auswahl der Partikel zu analysieren. Ein Intervall-Wert von 50-200 Pixel ^ 2 muss für Sporen23eingestellt werden. (B) Segmentierung des Bildes von Abbildung 3A nach der Anwendung Analysieren Partikel (links) und die relative densitometrische Analyseergebnisse (rechts). Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 5: Dot Blot und densitometrische Analyse. (A) Dot Blot mit Verdünnungsreihen des gereinigten mRFP im Duplikat (Std1 und Std2) und der Überstand (S10, S5 und S2) der Adsorption Reaktion mit 10, 5 und 2 µg des mRFP, bzw.23durchgeführt. (B) der Dot Blot-Panel A dient densitometrische Analysen. Die Kreise zeigen den Bereich verwendet, um die Dichte der Signale quantitate. Das Panel auf der rechten Seite berichtet ein Beispiel der Ergebnisse, die mit der densitometrische Analyse. Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 6: Umwandlung von Xylan durch wiederverwendbare Sporen. (A) allgemeine Schema der Xylan Abbau. (B) Sporen Anzeige der Xylanase oder die β-Enzym Enzyme, wenn miteinander vermischt katalysieren die zweistufige Abbau von Xylan. Nach der Reaktion wird die Probe durch Zentrifugation fraktioniert. Der Überstand enthält das Reaktionsprodukt, während das Pellet Spore-gebundenen Enzyme, die wiederverwendet werden können enthält, indem man frisches Substrat. Bitte klicken Sie hier für eine größere Version dieser Figur.
Diskussion
Dieses Spore-Adsorption-Protokoll ist sehr einfach und unkompliziert. Die Reaktion richtet sich streng nach den pH-Wert des Puffers Reaktion und die Effizienz der Adsorption ist optimal bei sauren pH-Werten (pH 5,0 oder niedriger). Im neutralen pH-Bedingungen die Effizienz der Adsorption ist gering, und bei alkalischen pH-Werten Adsorption kann nicht auftreten. Mit einem Volumen von 200 µL in 1,5 mL Röhrchen (oder ein ähnliches Verhältnis zu halten) auf einen rockigen Shaker optimalen Adsorption ergibt.
Adsorption ist sehr eng und Waschungen mit einem Puffer bei der gleichen pH des Puffers Reaktion verursachen kein Freigabe der adsorbierten Proteine. Waschungen mit alkalischen Puffer möglicherweise in einem minimal (in der Regel weniger als 15 %26) Version des adsorbierten Proteins.
Die indirekte Bewertung der Effizienz der Adsorption von Dot-Blot ist zuverlässig, wenn mehrere Verdünnungen des gereinigten und ungebundenen Proteins analysiert werden und die densitometrische Analyse wird ordnungsgemäß durchgeführt. Keine Hinweise auf Verschlechterung der heterologen Proteine wurde gemeldeten25. Die direkte Auswertung der Effizienz der Adsorption hängt stark von dem Protein, das adsorbiert wird. Wenn das Protein Autofluorescent oder Eindringmittel beschriftet, eine ImageJ-gestützte Analyse eine quantitative Bestimmung der Fluoreszenz und der Beträge der fluoreszierende Moleküle liefert präsentieren Sie auf der Spore. Wenn das Protein eine enzymatische Aktivität hat, könnte eine spezifische enzymatische Assays Aufschluss über die Mengen an Protein vorhanden auf die Sporen geben. Es ist jedoch bekannt, dass die enzymatische Aktivität im Zusammenhang mit Sporen durch ein Stabilisierungseffekt durch die Wechselwirkung mit der Spore13erhöht werden kann. Wenn die adsorbierten Protein nicht fluoreszierende ist und verfügt nicht über eine enzymatische Aktivität, kann die Effizienz der Adsorption von Dot Blot auf Sporen extrahiert unter drastischen Bedingungen ausgewertet werden.
Eine Sammlung von gebrauchten Sporen kann durch ein sehr einfaches Verfahren erfolgen. Ein Waschschritt mit der Reaktion Puffer möglicherweise wichtig, Nebenprodukte der Reaktion, zu entfernen, während die Zugabe von frischem Substrat wichtig, eine neue Reaktion21zu initiieren.
Offenlegungen
Die Autoren haben nichts preisgeben.
Danksagungen
Diese Arbeit wurde unterstützt durch "Finanziamento di Ricerca di Ateneo", L. Baccigalupi, Projekttitel "SP-LAY: bakterielle Sporen als live-Plattform für die Anzeige der Proteine".
Materialien
| Name | Company | Catalog Number | Comments |
| 0.1% Poly-L-lysine solution | Sigma | P8920 | |
| 0.45 µm Nitrocellulose Blotting Membrane | Sartorius | M_Blotting_Membranes | |
| 100× objective UPlanF1 | Olympus | microscope equipment | |
| Bacillus subtilis strain NCIB3610 | Bacillus Genetic Stock Center | 3A1 | |
| BD ACCURI C6 PLUS | BD | flow cytometer | |
| BX51 | Olympus | Fluorescent microscope | |
| Clarity | Biorad | 1705060 | |
| DP70 digital camera a | Olympus | microscope equipment | |
| Goat anti-Rabbit IgG (H+L) Cross-Adsorbed Secondary Antibody, FITC | Thermo fisher | F-2754 | |
| Goat Anti-Rabbit IgG H&L (HRP) | Abcam | ab6721 | |
| Monoclonal Anti-polyHistidine−Peroxidase antibody | Sigma | A7058-1VL | used to detect adsorbed proteins presenting a 6xhistidine-tag at C- or N- terminal |
| SecureSlip glass coverslip | Sigma | S1815-1PAK | |
| Superwhite Uncharged Microscope Slides | VWR | 75836-190 | |
| U-CA Magnification Changer | Olympus | microscope equipment |
Referenzen
- Felici, F., et al. Peptide and protein display on the surface of filamentous bacteriophage. Biotechnology Annual Review. 1, 149-183 (1995).
- Cortese, R., et al. Identification of biologically active peptides using random libraries displayed on phage. Current Opinion in Biotechnology. 6, 73-80 (1995).
- Sousa, C., Cebolla, A., de Lorenzo, V. Enhanced metalloadsorption of bacterial cells displaying poly-His peptides. Nature Biotechnology. 14, 1017-1020 (1996).
- Richins, R., Kaneva, I., Mulchandani, A., Chen, W. Biodegradation of organophosphorus pesticides by surface-expressed organophosphorus hydrolase. Nature Biotechnology. 15, 984-987 (1997).
- Wu, J. Y., et al. Expression of immunogenic epitopes of hepatitis B surface antigen with hybrid flagellin proteins by a vaccine strain of Salmonella. Proceedings of the National Academy of Sciences of the United States of America. 86, 4726-4730 (1989).
- Newton, S. M., Jacob, C. O., Stocker, B. A. Immune response to cholera toxin epitope inserted in Salmonella flagellin. Science. 244, 70-72 (1989).
- Fischetti, V. A., Medaglini, D., Pozzi, G. Gram-positive commensal bacteria for mucosal vaccine delivery. Current Opinion in Biotechnology. 7, 659-666 (1996).
- Isticato, R., Ricca, E. Spore surface display. Microbiology Spectrum. 2 (5), (2014).
- Ricca, E., et al. Mucosal vaccine delivery by non-recombinant spores of Bacillus subtilis. Microbial Cell Factories. 13, 115(2014).
- McKenney, P. T., Driks, A., Eichenberger, P. The Bacillus subtilis assembly and functions of the multilayered coat. Nature Reviews Microbiology. 11, 33-44 (2013).
- Knecht, L. D., Pasini, P., Daunert, S. Bacterial spores as platforms for bioanalytical and biomedical applications. Analytical and Bioanalytical Chemistry. 400, 977-989 (2011).
- Isticato, R., Cangiano, G., De Felice, M., Ricca, E. Display of molecules on the spore surface. Bacterial Spore Formers: Probiotics and Emerging Applications. Ricca, E., Henriques, A. O., Cutting, S. M. , Horizon Bionsciences. Norfolk, UK. 193-200 (2004).
- Sirec, T., et al. Adsorption of β-galactosidase of Alicyclobacillus acidocaldaricus wild type and mutant spores of Bacillus subtilis. Microbial Cell Factories. 11, 100(2012).
- Cutting, S. M. Bacillus probiotics. Food Microbiology. 28, 214-220 (2011).
- Baccigalupi, L., Ricca, E., Ghelardi, E. Non-LAB Probiotics: Spore Formers. Probiotics and Prebiotics: Current Research and Future Trends. Venema, K., Do Carmo, A. P. , Caister Academic Press. 93-103 (2014).
- Cutting, S. M., Hong, H. A., Baccigalupi, L., Ricca, E. Oral Vaccine Delivery by Recombinant Spore Probiotics. International Reviews of Immunology. 28, 487-505 (2009).
- Lee, S. Y., Choi, J. H., Xu, Z. Microbial cell-surface display. Trends in Biotechnology. 21, 45-52 (2003).
- Isticato, R., et al. Surface display of recombinant proteins on Bacillus subtilis spores. Journal of Bacteriology. 183, 6294-6301 (2001).
- Huang, J. M., et al. Mucosal delivery of antigens using adsorption to bacterial spores. Vaccine. 28, 1021-1030 (2010).
- Isticato, R., et al. Non-recombinant display of the B subunit of the heat labile toxin of Escherichia coli wild type and mutant spores of Bacillus subtilis. Microbial Cell Factories. 12, 98(2013).
- Mattossovich, R., et al. Conversion of xylan by recyclable spores of Bacillus subtilis thermophilic enzymes. Microbial Cell Factories. 16, 218(2017).
- Pesce, G., et al. Surface charge and hydrodynamic coefficient measurements of Bacillus subtilis by optical tweezers. Colloids and Surfaces B: Biointerfaces. 116, 568-575 (2014).
- Donadio, G., et al. Localization of a red fluorescence protein adsorbed on wild type and mutant spores of Bacillus subtilis. Microbial Cell Factories. 15, 153(2016).
- Pan, J. G., Choi, S. K., Jung, H. C., Kim, E. J. Display of native proteins on Bacillus subtilis spores. FEMS Microbiology Letters. 358, 209-217 (2014).
- Cutting, S., Vander Horn, P. B. Genetic analysis. Molecular Biological Methods for Bacillus. Harwood, C., Cutting, S. , John Wiley & Sons. Chichester, UK. (1990).
- Lanzilli, M., et al. Display of the peroxiredoxin Bcp1 of Sulfolobus solfataricus probiotic spores of Bacillus megaterium. New Biotechnology. 46, 38(2018).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten