Method Article
3D mitochondrialen Ultrastruktur von Drosophila indirekte Flüge Muskel von Serial-Abschnitt Elektron Tomographie aufgedeckt
In diesem Artikel
Zusammenfassung
In diesem Protokoll demonstrieren wir die Anwendung der seriell-Abschnitt Elektron Tomographie, mitochondriale Struktur in Drosophila indirekte Flüge Muskel aufzuklären.
Zusammenfassung
Mitochondrien sind zelluläre Kraftpakete, die produzieren ATP, Lipide und Metaboliten sowie Kalzium-Homöostase und Zelle Tod zu regulieren. Die einzigartige Cristae-reiche Doppelmembran Ultrastruktur von dieser Organellen ist elegant angeordnet, um mehrere Funktionen durchzuführen, durch die Partitionierung Biomoleküle. Mitochondrialen Ultrastruktur ist eng mit verschiedenen Funktionen; die feinen Details dieser Struktur-Funktions-Beziehungen sind jedoch erst am Anfang beschrieben werden. Hier zeigen wir die Anwendung der seriell-Abschnitt Elektron Tomographie, mitochondriale Struktur in Drosophila indirekte Flüge Muskel aufzuklären. Seriell-Abschnitt Elektron Tomographie kann Zellstruktur in drei Dimensionen zu studieren angepasst.
Einleitung
Elektronenmikroskopie ist ein wertvolles Instrument zur Untersuchung der strukturellen Kontext der subzellulären Baugruppen und Organellen, die zelluläre Prozesse ausführen. Methoden wurden entwickelt, um die Ultrastruktur von Geweben oder Zellen entweder durch chemische Fixierung mit Aldehyden zu erhalten oder durch hohen Druck Einfrieren (HPF) gefolgt von freeze Substitution (FS)1,2. Die eingebetteten Proben Blöcke können dann geschnitten, gebeizt und mit einem Transmissionselektronenmikroskop (TEM) beobachtet. Die HPF-Probe konnte auch unter Cryo-Zustand, z. B. durch Cryo-schneiden oder fokussierten Ionenstrahl (FIB) Fräsen und beobachtet von Cryo-EM3,4verarbeitet werden.
Obwohl dünn-Sektion EM morphologische aufschlussreiche Einblicke bietet, können die resultierenden 2D Bilder nur die Ultrastruktur der einen bestimmten Querschnitt zeigen. Wie die Ultrastruktur in ein 3D Volumen anordnet bleibt verdeckt. Um zellulären Ultrastruktur dreidimensional sichtbar zu machen, wurde eine Elektron Tomographie Methode entwickelt, wo Tilt Bilderserie erworben und zurück projiziert, um eine tomographische Rekonstruktion5 (Abbildung 1) zu generieren. Eine doppelte Tilt-Reihe kann gesammelt werden, durch die Probe 90° drehen und eine zweite Tilt-Serie zu erwerben. Dies minimiert fehlt-Wedge Artefakte, die ergeben sich aus der begrenzten Probenahme Winkel und Auflösung der Tomogramm verbessert.
Hier beschreiben wir die Anwendung der seriell-Abschnitt Elektron Tomographie studieren mitochondrialen Ultrastruktur von Drosophila indirekte Flüge Muskel (IFM)6,7,8,9 . Um 3D Rekonstruktionen für gesamte Mitochondrien (ca. 2,5 µm dicken) zu erhalten, wurden Serienschnitte von Drosophila IFM Gewebe Blöcke erhalten. Schichtbilder der einzelnen Abschnitte wurden einzeln mit automatischer Datenerfassungs-Software gesammelt. Tomographische Rekonstruktionen wurden generiert und serielle Schichtbilder schlossen mit dem IMOD Paket, einem rekonstruierten Volumen von eine gesamte Mitochondrium zu erhalten. Die verbundenen Schichtbilder wurden von 3D Software analysiert. Die Dichte der Mitochondrien Cristae wurden segmentiert, um einem Segmentierungsmodell zu generieren, die die Organisation in drei Dimensionen offenbart.
Protokoll
1. Abschnitt Drosophila Gewebe mit einer schwingenden Klinge-Mikrotom
- Drosophila auf Eis zu betäuben und jede einzelne Fliege in 1 mL 4 % niedrig schmelzende Agarose in Phosphatpuffer Tauchen. Lassen Sie Agarose, auf Eis erstarren. In der Regel wurden 4-6 fliegen verarbeitet.
- Verwenden Sie eine vibrierende Klinge Mikrotom zu Abschnitt Agarosegel eingebettete Drosophila in mit 100 µm dicke Scheiben und Tauchen in Fixativ Lösung mit 2,5 % Glutaraldehyd in 0,1 M Phosphatpuffer.
Hinweis: Vibratome-Schnitt wird bevorzugt, weil Gewebearchitektur mehr intakt im Vergleich zu anderen Methoden bleibt. Alternativ kann sezieren Pinzette zur IFM in die Fixativ Lösung mit 2,5 % Glutaraldehyd in 0,1 M Phosphatpuffer sezieren.
2. bereiten Sie EM Proben vom Hochdruck Einfrieren und Freeze Substitutionsmethode (HPF/FS)
- Phosphatpuffer, gefolgt von 2 Tropfen (~ 100 µL) der Phosphatpuffer mit 20 % BSA waschen Sie Gewebeschnitte in 3 Tropfen (~ 150 µL). Dann legen Sie Abschnitte in gold Träger für HPF mit Puffer und 20 % BSA gefüllt.
- Laden Sie die Probe mit Trägern in einem Hochdruck-Gefrierschrank entsprechend der Gebrauchsanweisung.
- Nach dem Einfrieren lassen Träger aus der Halterung unter flüssigem Stickstoff und übertragen auf einen Freeze-Ersatzgerät auf-140 ° c abgekühlt
- Führen Sie das Einfrieren-Substitution-Protokoll wie in Tabelle 1, mit dem FS cocktail mit 2 % Glutaraldehyd, 2 % Osmium ausgefällt und 0,1 % Uranyl Acetat in Aceton dargestellt.
- Vorsichtig entnehmen Sie die Proben aus den Trägern mit einer Nadel und Betten Sie der Proben im Harz bei Raumtemperatur ein. Polymerisieren Sie das Harz bei 65 ° C 16 h.
Hinweis: FS Protokolle sollten geändert werden, um andere Arten von Proben vorzubereiten. HPF/FS wird bevorzugt zur Erhaltung der Ultrastruktur und minimiert den Verlust von zellulären Inhalt.- Alternativ eine chemische Fixierung Protokoll anwenden. Exemplare über Nacht mit 2,5 % Glutaraldehyd befestigen, waschen mit Puffern und dann fixieren Sie mit 1 % Osmium ausgefällt für 2 h waschen und entwässern mit aufsteigenden Konzentrationen von Ethanol und dann infiltrieren und einbetten Exemplare in Spurrs Harz vor dadurch bei 65 ° C für 16 h.
3. bereiten Sie Serie Abschnitte der Exemplare für Elektronenstrahl-Tomographie
- Schneiden Sie die Probe-Blöcke, um den gewünschten Block Gesicht aussetzen, das Gewebe enthält.
- Vorbehandeln Goldpartikel (10 nm im Durchmesser) mit 1 % BSA für 30 min. Waschen und Aufhängen Goldpartikel in PBS-Puffer. Overlay-Goldpartikel auf Kupfer Slot Gitter beschichtet mit Carbon Folie Kugelmarker erstellen.
- Das Sichtfeld der Tomographie Erwerb unter TEM müssen ausreichend Kugelmarker (mindestens 5-10 Marker) einchecken.
- Geschnitten Sie Serienschnitte, 200-250 nm dicke, mit einem regungsloses.
- Sammeln Sie Serienschnitte auf Slot-Gitter mit einer perfekten Schleife für Dünnschliffe.
- Färben Sie die Abschnitte mit Reynold es Blei Citrat für 10 min.
- Eine zweite Schicht aus treuhändische Goldpartikel auf der Oberseite in den Abschnitten zu überlagern.
4. sammeln Sie Doppel-Kipp-Elektron Tomographie
- Laden Sie das Raster auf einer Doppel-Mittellinie Tomographie-Halter und stecken Sie in die Transmissions-Elektronenmikroskop in Betrieb bei 200 kV.
- Richten Sie das Mikroskop im Euzentrische Fokus.
- Richten Sie die automatische Datenerfassungs-Software. Einstellen und Ausrichten des Elektronenstrahls bei der Multi-Skalen-imaging-Einstellung. Sie finden Sie im Benutzerhandbuch für Betrieb Detail10 (Abbildung 2).
- Dunklen und hellen Referenzen Kamera in einem leeren Raum ohne Carbon Folie unter der Einstellung "Tomographie-Sammlung" zu erwerben.
- Einen Raster-Atlas bei geringer Vergrößerung zu sammeln. Mitochondrien auf Schnittserien als Ziele für Tomographie Sammlung auswählen.
- Erwerben Sie ein Tilt-Serie von-60 ° bis + 60 ° mit 2 ° c-Schritten auf Achse-A für jedes Ziel.
Hinweis: Der Neigungswinkel werden mechanisch durch die Gestaltung der Probenhalter eingeschränkt werden. Der Halter wird den Strahl im hohen Neigungswinkel blockieren. - Um die zweite Serie der Neigung zu sammeln, drehen Sie die Probenhalter 90°. Erwerben Sie einen neuen Atlas. Wählen Sie entsprechende Positionen und erwerben Sie die Tilt-Serie auf Achse-B für jedes Ziel zu.
Hinweis: Andere Softwarepakete, wie SerialEM und Xplore3D, stehen für die automatische Datenerfassung.
5. 3D Schichtbilder zu rekonstruieren und Segment Teilvolumina mit Software
- Schichtbilder Dual-Achse kippen Bilder mit IMOD Software11zu rekonstruieren.
- Sie finden Sie im Benutzerhandbuch zum Betrieb Detail.
- Richten Sie die individuelle Neigung-Serie durch die Position der gold Kugelmarker. Rekonstruieren Schichtbilder zurück Projektionsmethode oder durch die gleichzeitige Iterative Rekonstruktion Technik (SIRT) Methode für beide Achsen A und B-Achse bzw. (Abbildung 3).
- Kombinieren Sie Schichtbilder der Achse A und Achse-B, ein Doppel-Kipp-Tomogramm mit reduzierten fehlende Keil Artefakt zu generieren.
- Gemeinsam Doppel-Kipp Schichtbilder der Schnittserien Rekonstruktionen für gesamte Mitochondrium Volumen zu erhalten. Die Lücken zwischen den Schnittserien IMOD programmtechnisch zu modellieren.
- Trim verbundenen Schichtbilder und bin auf eine gewünschte Größe für die Volumen-Segmentierung.
- Analysieren Sie verbundene serielle Schichtbilder mit einer 3D-Software.
- Sie finden Sie im Benutzerhandbuch zum Betrieb Detail.
- Filtern Sie die Schichtbilder mit eine Gaußsche Filter (oder andere gewünschte Methode) verbessert den Kontrast der Funktionen und die Hintergrund dichten.
- Die Ultrastruktur der Mitochondrien zu segmentieren, entweder manuell oder automatisch.
- Anschauungsmodelle Segmentierung zur Inspektion in 3D ermöglichen.
- Filme mit verfügbaren Tools in 3D zu erzeugen.
Ergebnisse
Wir angewendet seriell-Abschnitt Elektron Tomographie Strukturmerkmale der Mitochondrien Cristae zu analysieren, die den energetischen Zustand und Alterung widerspiegelt. Wir zeigten, dass Mitochondrien von Drosophila IFM ein integriertes bilden Cristae und Matrix-Netzwerk in 3D (Abbildung 4)7. Darüber hinaus angesammelt mutierte fliegen mit mitochondrialen DNA Replikation defekt und eine beschleunigte Alterung Phänotyp Mitochondrien, die Unterabschnitte von Zwiebel-wie wirbelnde Kern (Abbildung 5)7enthalten.

Abbildung 1: Abbildung der Elektron Tomographie Rekonstruktion aus einer Reihe von Tilt. Im Experiment wird ein Elektronenstrahl ein 3D-Objekt durchlaufen, wenn das Objekt in unterschiedlichem Maße geneigt wird. Für jede Bedingung Tilt 2D Projektion erzeugt und mit einer Kamera erfasst. Die 2D Projektionen dürften dann wieder um das 3D-Objekt basierend auf der zentralen Scheibe Theorem zu rekonstruieren. In der Abbildung ist der gleiche Prozess für eine ursprüngliche 2D-Bild dargestellt, die in einer einzigen Dimension unter verschiedenen Neigungswinkel projiziert wird. Die 1D Projektionen werden verwendet, um das 2D-Bild zu rekonstruieren. Bitte klicken Sie hier für eine größere Version dieser Figur.
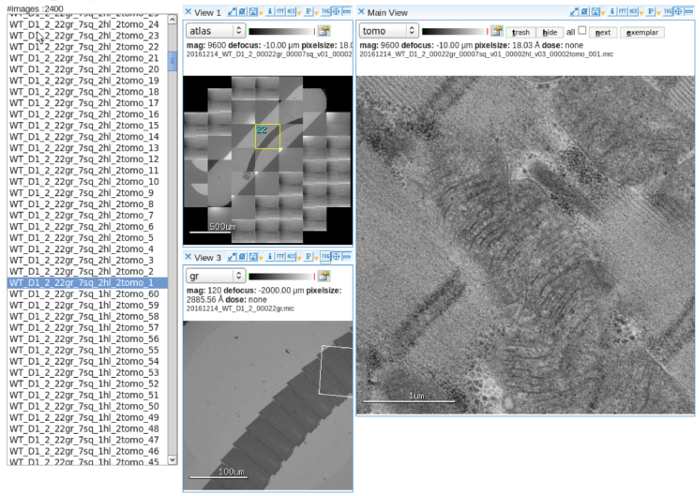
Abbildung 2: automatische Datenerfassung. Eine Bildanzeige Viewer Software zeigt des Atlas eine Slot-Raster mit Schnittserien kippen mehrskaligen Ausrichtung der Mitochondrien und erworbene Bilder. Maßstabsleiste = 500 µm (oben links), 100 µm (linken Bodenplatte), 1 µm (rechte Abbildung). Bitte klicken Sie hier für eine größere Version dieser Figur.

Abbildung 3: Serial-Abschnitt Elektron Tomographie von einem einzigen Mitochondrium in Drosophila indirekte Flüge Muskel. 2D Mikrographen (A) und (B) 3D Schichtbilder von Schnittserien deckt das gesamte Volumen der ein Mitochondrium. (C) verbundene seriell-Abschnitt Schichtbilder werden projiziert, erstellen Sie einen Längsschnitt mit der z-Achse vertikal dargestellt. Vor allem führte Gewebe schneiden zu Verlust von Material, so dass Lücken zwischen verknüpften Schichtbilder. Maßstabsleiste = 500 nm. Bitte klicken Sie hier für eine größere Version dieser Figur.
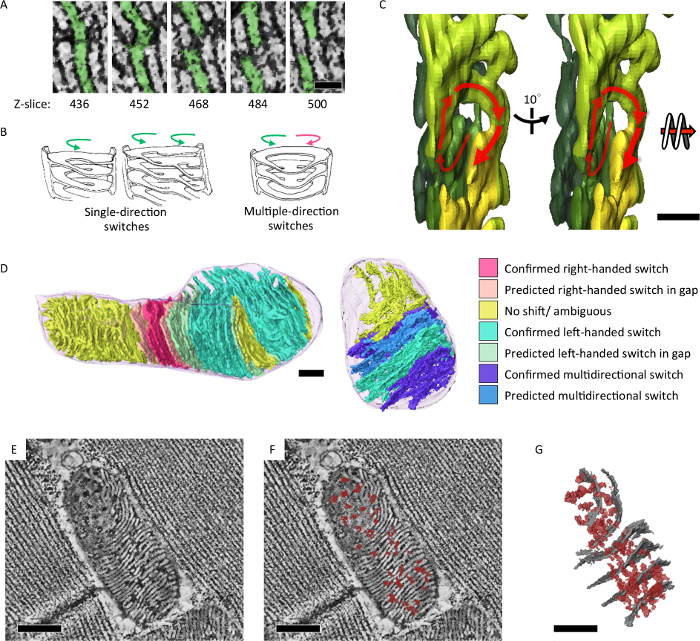
Abbildung 4: integrierte Intra-Mitochondrien Cristae und Matrix-Netzwerk in 3D gezeigt. (A) Scheiben der mitochondrialen Elektron tomographische Rekonstruktionen zeigen wechselt zwischen lamellaren Membranen durch die z-Achse. (B) Abbildungen von den beobachteten Cristae Muster direkt übergeben und/oder Linkshänder Spiralen wechseln. (C) tomographische Segmentierung zur Veranschaulichung einer linkshändigen Spirale in 3D (D) Cristae umschalten Muster analysiert und Farbe auf das Segmentierungsmodell (E, F) gerendert wurden. Tomographische Scheibe mit seitlichen Matrix Konfluenz (dunkle Rohdichten, rot markiert) über Cristae Membranen (weiße Dichte). (G) Segmentierung der Tomogramm in (E) mit seitlichen Matrix Konfluenz (in rot) Modell und repräsentative Cristae (in grau). Maßstabsleiste = 50 nm (A), 200 nm (C) und 300 nm (D, E, F, G). Die Figur wurde die Neuauflage von Jiang Et al. 7 Klicken Sie bitte hier, um eine größere Version dieser Figur.

Abbildung 5: Mitochondrien mit Zwiebel-wie wirbelnde Kernen angesammelt fliegen mit mitochondrialen DNA Replikation Fehler während des Alterns. Repräsentative tomographische Scheiben und die entsprechenden Segmentierung (richtigen Platten) zeigt eine Querschnittsansicht (oben) und einen Längsschnitt Ansicht (unten) aus einem wirbelnden Kern. Volumen-Segmentierung wird durch willkürliche Farbwiedergabe den wirbelnden Kern hervorheben. Maßstabsleiste: 200 nm. Die Figur wurde die Neuauflage von Jiang Et al. 7 Klicken Sie bitte hier, um eine größere Version dieser Figur.
| Schritt | Temp | Zeit | Lösung | |||
| 1 | -140 ° C bis-9 0 ° C | 30 min | Flüssiger Stickstoff | |||
| 2 | -90 ° C | 96 hr | FS-cocktail | |||
| 3 | -90 ° C bis-60 ° C | 6 h (5 ° C/h) | FS-cocktail | |||
| 4 | -60 ° C | 12 h | FS-cocktail | |||
| 5 | -60 ° C bis-25 ° C | 7 hr (5 ° C/h) | FS-cocktail | |||
| 6 | -25 ° C | 12 h | FS-cocktail | |||
| 7 | -25 ° C bis 0 ° C | 5 h (5 ° C/h) | FS-cocktail | |||
| 8 | 0 ° C | 1 hr x 3 Mal | Aceton | |||
| 9 | Raumtemp | Harz-infiltration | ||||
Tabelle 1: Freeze-Substitution-Protokoll.
Diskussion
In diesem Protokoll beschreiben wir einen optimierten Workflow für die Anwendung von seriell-Abschnitt Elektron Tomographie zur 3D mitochondrialen Ultrastruktur von Drosophila indirekte Flüge Muskel zu studieren. Erhaltung der Ultrastruktur in der Probe ist die größte technische Herausforderung für diese Art der Analyse. Um am besten die Ultrastruktur zwei methodische zu bewahren wurden Schritte enthalten. Erstens wurde Gewebe gesampelt, durch Schneiden mit vibrierender Klinge Mikrotom um die Gewebearchitektur so weit wie möglich zu halten. Zweitens wurde ein HPF/FS-Protokoll optimiert, um Organelle Ultrastruktur während der Vorbereitung des eingebetteten Proben Blöcke zu bewahren. Proben wurden unter hohem Druck, eingefroren, senkt den Gefrierpunkt des Wassers und reduziert die Bildung von Eiskristallen, die Ultrastruktur1beschädigen. Exemplare, die so dick wie 0,1 mm augenblicklich verglast sein kann, und dann einfrieren, Ersatz um Probe Blöcke für EM-Analyse zu generieren unterzogen. Die verbesserte Erhaltung der Ultrastruktur von HPF/FS wurde festgestellt, wenn im Vergleich zu chemischen Fixierung Methoden. Mit dieser Serie von Schritten für die Probenvorbereitung, wurde Erhaltung der mitochondrialen doppelte Membranen und Cristae Membranen erheblich verbessert.
Schnittserien der Probe zu erhalten, ist der schwierigste Schritt des Verfahrens. Da der Elektronenstrahl Durchdringungskraft begrenzt hat, die Dicke des Abschnitts beschränkt sich auf entweder 250 nm oder 500 nm mit einem TEM Betrieb bei 200 kV oder 300 kV, beziehungsweise. Da die Dicke der ein Mitochondrium möglicherweise mehr als 2 µm, Serienschnitte müssen volle Lautstärke Rekonstruktionen zu erhalten. Wiederherstellung einer ausreichenden Zahl von Schnittserien umfassen eine ganze Organelle ist jedoch eine technische Herausforderung. Das Block-Gesicht so flach wie möglich zwischen den Basen des Trapezes zu trimmen können eine Slot-Raster, um Platz für weitere Abschnitte und deckt damit größere Mengen. Darüber hinaus erhöht mit einer perfekten Schleife für Dünnschliffe die Erfolgsquote der Schnittserien an das Stromnetz zu übertragen.
Seriell-Abschnitt Elektron Tomographie kann mit Standardausrüstung EM Kern erreicht werden. Die Methode hat jedoch einige unvermeidlichen Einschränkungen, die durch technische Zwänge entstehen. Einer ist, dass Material unweigerlich verloren zwischen Serienschnitte, so dass Lücken in den verbundenen Wiederaufbau. Zweitens ist das fehlende Keil Artefakt, die aufgrund der begrenzten Neigungswinkel entsteht, die erreichbar sind. Diese Einschränkung tritt auf, weil der Probenhalter in eine volle Umdrehung eingeschaltet werden kann, ohne zu blockieren den Elektronenstrahl. Trotz dieser Einschränkungen bietet Serien-Abschnitt Elektron Tomographie ausreichenden Auflösung, Mobilfunk- und Organelle Ultrastruktur in 3D zu offenbaren.
Für die kleineren Maßstab Bildgebung ist Cryo-Elektron Tomographie eine neue Technologie, die verwendet werden, um die Struktur der makromolekularen komplexe und Baugruppen in Situ in nm oder Sub Ångström Auflösung in Kombination mit Sub-tomographische zu erhalten Umbau3. In dieser Anwendung sind die Zellen durch Schneiden oder Fräsen unter flüssigem Stickstoff fokussierten Ionenstrahl ausgedünnt. Die Schichtbilder werden unter Cryo-Bedingungen gesammelt wo sind molekulare Strukturen in der Nähe der nativen Zustand ohne chemische Fixierung, Austrocknung oder einbetten erhalten. Am anderen Ende der Skala um große Gewebe auf Kosten der Auflösung, analysieren ist Rasterelektronenmikroskopie serielle Block-Gesicht eine ansprechende Modalität, obwohl es ein spezifisches Instrument4erfordert.
Offenlegungen
Die Autoren erklären, dass sie keine finanziellen Interessenkonflikte.
Danksagungen
Die Untersuchungen wurden in der EM-Kern am Institut für Zell- und Organismische Biologie und die Cryo-EM Kern der Academia Sinica, Taipei, Taiwan durchgeführt. Die Arbeit wurde von der Academia Sinica und die meisten unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| vibrating blade microtome | Leica | VT1200S | Tissue sectioning |
| high-pressure freezer | Leica | EM HPM100 | Specimen preparation |
| freeze-substitution device | Leica | EM AFS2 | Specimen preparation |
| ultramicrotome | Leica | EM UC7 | Ultra-thin sectioning |
| dual-axis tomography holder | Fischione | Model 2040 | tomography collection |
| transmission electron microscope | FEI | Tecnai F20 | tomography collection |
| CCD | Gatan | UltraScan 1000 | tomography collection |
| Leginon | NRAMM/AMI | tomography collection | |
| IMOD | Boulder Laboratory for 3-D Electron Microscopy of Cells | Tomography reconstruction | |
| Avizo 3D | FEI | Tomography analysis |
Referenzen
- Dahl, R., Staehelin, L. A. High-pressure freezing for the preservation of biological structure: theory and practice. J Electron Microsc Tech. 13 (3), 165-174 (1989).
- Sabatini, D. D., Bensch, K., Barrnett, R. J. Cytochemistry and electron microscopy. The preservation of cellular ultrastructure and enzymatic activity by aldehyde fixation. J Cell Biol. 17, 19-58 (1963).
- Rigort, A., et al. Micromachining tools and correlative approaches for cellular cryo-electron tomography. J Struct Biol. 172 (2), 169-179 (2010).
- Denk, W., Horstmann, H. Serial block-face scanning electron microscopy to reconstruct three-dimensional tissue nanostructure. PLoS Biol. 2 (11), e329 (2004).
- Lucic, V., Forster, F., Baumeister, W. Structural studies by electron tomography: from cells to molecules. Annu Rev Biochem. 74, 833-865 (2005).
- Soto, G. E., et al. Serial section electron tomography: a method for three-dimensional reconstruction of large structures. Neuroimage. 1 (3), 230-243 (1994).
- Jiang, Y. F., et al. Electron tomographic analysis reveals ultrastructural features of mitochondrial cristae architecture which reflect energetic state and aging. SciRep. 7, 45474 (2017).
- Cogliati, S., Enriquez, J. A., Scorrano, L. Mitochondrial Cristae: Where Beauty Meets Functionality. TrendsBiochemSci. 41 (3), 261-273 (2016).
- Friedman, J. R., Nunnari, J. Mitochondrial form and function. Nature. 505 (7483), 335-343 (2014).
- Suloway, C., et al. Fully automated, sequential tilt-series acquisition with Leginon. J Struct Biol. 167 (1), 11-18 (2009).
- Mastronarde, D. N., Held, S. R. Automated tilt series alignment and tomographic reconstruction in IMOD. J Struct Biol. 197 (2), 102-113 (2017).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten