Method Article
Testproben zur Optimierung STORM Super Resolution Mikroskopie
In diesem Artikel
Zusammenfassung
Wir beschreiben die Herstellung von drei Prüfmustern und wie sie verwendet werden, um beurteilen zu optimieren und die Leistung der STORM-Mikroskope. Mit diesen Beispielen zeigen wir, wie Roh-Daten zu erfassen und verarbeiten sie zu Super-Resolution-Bilder in Zellen von ca. 30-50 nm Auflösung zu erwerben.
Zusammenfassung
STORM ist eine neu entwickelte Super-Resolution-Mikroskopie-Technik mit bis zu 10-mal höhere Auflösung als Standard-Fluoreszenzmikroskopie-Techniken. Jedoch, wie das Bild in eine ganz andere Weise als normal erworben, durch den Aufbau eines Bildes Molekül-für-Molekül, gibt es einige bedeutende Herausforderungen für die Nutzer in die versuchen, ihre Bildaufnahme zu optimieren. Um diesen Prozess zu unterstützen und gewinnen mehr Einblick, wie STORM arbeitet präsentieren wir die Herstellung von 3 Testproben und die Methodik der Erfassung und Verarbeitung von STORM Super-Resolution-Bilder mit typischen Auflösungen von 30-50 nm auf. Durch die Kombination der Testproben mit der Verwendung der frei verfügbaren Rainstorm Verarbeitungssoftware ist es möglich, eine große Menge an Informationen über Bildqualität und Auflösung zu erhalten. Mit Hilfe dieser Messdaten ist es dann möglich, die Bildgebungsverfahren von der Optik zu optimieren, die Vorbereitung, Farbstoff Wahl, Pufferbedingungen, und Bildaufnahme-Einstellungen probieren. Wir sind einelso zeigen Beispiele für einige häufige Probleme, die zu einer schlechten Bildqualität führen, wie laterale Drift, wo die Probe bewegt sich während der Bildaufnahme und Dichte bezogene Probleme, die in der "Fehllokalisation" Phänomen.
Einleitung
Vor kurzem wurde ein Bereich der optischen Mikroskopie Techniken entwickelt worden, die typischerweise als Super-Resolution-Mikroskopie oder Nanoskopie, die die Beugungsgrenze zu umgehen und erzeugen Bilder mit einer Auflösung von 100 nm oder besser 1,2 können bezeichnet. Seit der Ankündigung von Super-Resolution-Mikroskopie als die Nature Methods Verfahren des Jahres 2008 gab es eine große Entwicklung von Lokalisierungs-basierten Mikroskopen. Zum Beispiel gibt es Mehrfarbanwendungen 3-6, 7-12 3D-Implementierungen und Anwendungen auch mit lebenden Zellen 5,13-17. Darüber hinaus, da diese Systeme werden in die Hände von Zellbiologen kommerzialisiert und werden nun ihren Weg aus der Optik Laboratorien gibt es wahrscheinlich eine weitere Erhöhung ihrer Verwendung und Anwendung der biomedizinischen Fragen.
Ein Zweig dieser Familie ist die Lokalisierungsbasierte Methoden, die durch den Aufbau eines Bildes Molekül-für-Molekül zu arbeiten. Ichn Um dies zu tun, muss der Großteil der Fluoreszenzmoleküle in der Probe aus, so dass nur wenige räumlich getrennten Moleküle zu einem Zeitpunkt aktiv geschaltet sein. Diese Moleküle werden dann schnell ein-und ausgeschaltet, und viele Bilder aufgenommen werden, so dass ein beträchtlicher Teil der Bevölkerung ist abgebildet, um die darunterliegende Struktur mit Unter-Beugungs Präzision wiedergeben. Eine Reihe von Ansätzen veröffentlicht einschließlich GSDIM 18, 19 PALM, FPALM 20, 21 und STORM RESOLFT 22. Algorithmen, die die Position eines Einzelmoleküldetektion messen kann dann verwendet werden, um die tatsächliche Position des Moleküls mit Genauigkeiten besser als 20 nm unter Verwendung von Gauß-Fitting 23 zu lokalisieren, beispielsweise rapidSTORM 24,25 QuickPALM 26, 12 und palm3d Regensturm 27. Bei der Abbildung Zelle oder anderen biologischen Proben, die eine hohe Moleküldichte haben, ist es daher erforderlich, viele Tausende von Rahmen zu nehmendiese blinkt, räumlich getrennten, Signals, um Bild ein erheblicher Anteil der markierten Moleküle.
Stochastische optischen Rekonstruktion Mikroskopie (STORM) und der eng verwandten dSTORM und GSDIM Methoden-basierte Lokalisierungs Super-Resolution-Methoden, die gezeigt wurde, dass mit handelsüblichen organischen Farbstoffen 21 zu arbeiten. Sie haben sich seit gezeigt wurde für eine Reihe von verschiedenen Farbstoffen 28-30, die die Methodik insbesondere wegen der Spezifität und der relativen Bequemlichkeit der etablierten Immunmarkierung Ansätze zur Fluoreszenzmikroskopie durch attraktiv zu sein. Folglich gibt es einen einfachen Zugang zu einer Reihe von Farbstoff-Antikörper-und Farbstoff-Biomolekül-Konjugate, die das Potenzial in der Lokalisierung Basis-Superauflösende Bildgebung verwendet werden müssen. Während die allgemeinen Grundsätze des STORM und ähnliche Ansätze sind relativ einfach, und auf den ersten Blick die Hardware und die Probenvorbereitung scheinen relativ straightforward, gibt es eine Reihe von Schritten in dem Prozess, der entscheidend für die Erreichung hoher Qualität, artefaktfrei, Super-Resolution-Bilder sind.
Wie bei allen Mikroskopie-Techniken kann der Prozess des in 3 Hauptschritte betrachtet werden: erstens, Probenvorbereitung, zweite Bildaufnahme und, drittens, die Bildverarbeitung und / oder Bildanalyse und Interpretation. Die zusätzliche Auflösungsvermögen und Verfahren zur Erzeugung von Super-Resolution-Bildern mit einem Lokalisierungs-Ansatz führt einige neue Probleme und Überlegungen 31-33. Beginnend mit der Probenvorbereitung bei der Durchführung der Immunmarkierung, insbesondere indirekte Immunfluoreszenz, wo eine primäre und sekundäre Antikörperkombination verwendet wird, ist anzumerken, dass der fluoreszierende Farbstoff kann bis zu 20 nm von dem Molekül von Interesse sein werden. Im Fall von Mikrotubuli, führt dies zu Durchmessern von 35-50 nm im Vergleich mit einer erwarteten Mikrotubuli-Durchmesser von 25 nm 28,30. Auch sollte die Markierungsdichte meet die Nyquist-Kriterien, um eine hohe Bildqualität 14 zu erzeugen. Zum Beispiel für eine erwartete Bildauflösung von 20 nm entlang einer filamentösen Struktur sollte ein Farbstoffmolekül mindestens alle 10 nm 27 sein. Während viele Farbstoffe sind veröffentlicht worden, um für die Lokalisierung Basis nähert sich die Gesamtleistung des Farbstoffs ist eine Mischung aus mindestens vier wichtige Kriterien, nämlich detektierten Photonen pro Schaltereignis (die Helligkeit jedes Blinzeln - heller ist besser) arbeiten, das Gleichgewicht auf -off-Arbeitszyklus (das Kontrastverhältnis von Farbstoffen in der Aus-Zustand gegenüber - mehr ist im Allgemeinen besser ab), die Überlebensfraktion (eine geringe Bleichrate ist besser) und die Anzahl der Schaltzyklen (die Anzahl der Blinkzeichen pro Fluorophor - mehr ist besser für hohe Auflösung, obwohl ein Aufblinken pro Fluorophor kann ein Vorteil für die Molekül-Zwecke Zählen sein). Die Situation wird weiter durch die Tatsache, dass diese Eigenschaften für einen bestimmten Farbstoff kann in verschiedenen Pufferbedingungen variieren und kompliziertLaserleistung mit 28,29. Zudem sowie diese einzigartige STORM Erwägungen kann die Bildqualität durch die Optimierung der Probenvorbereitung in der gleichen Weise wie traditionelle Fluoreszenzmikroskopie-Techniken beispielsweise durch Minimierung von Eigenfluoreszenz durch Modifikation Fixierungsbedingungen und die Verwendung von Reagenzien Abschrecken verbessert werden. Auch ist die Minimierung nicht-spezifisch gebundenen Fluorophore wichtig, welche durch Einstellen Etikett Konzentrationen, Inkubationszeiten und Blockieren und Waschschritte durchgeführt werden können.
Der zweite Schritt der Bildaufnahme ist ebenfalls kritisch. Die optimalen Einstellungen des Mikroskops wird auf die Farbstoff, Pufferbedingungen Markierungsdichte und Probentyp, z. B. Monoschichten auf Glas, Zellen oder Gewebeproben ab. Die wichtigsten Überlegungen sind Kamera Belichtungszeit, Bildnummer, Beleuchtungswinkel (TIRF, Hilo, Epi) und Laserleistung. Das Ziel ist, so viele helle räumlich getrennten blinkt so schnell wie möglich zu sammeln. Wenn der Hintergrund is sehr hoch ist oder die blinkt nicht sehr hell, mit anderen Worten, das Signal-zu-Rauschverhältnis schlecht ist, wobei der Rekonstruktionsalgorithmus nicht in der Lage, die Positionen so genau zu lokalisieren. Sowie die Maximierung der Lokalisierungsgenauigkeit, also die Genauigkeit, mit jedem Molekül Position gemessen werden kann, hängt die Bildqualität auch bei einer hohen Anzahl von Lokalisierungen. Wenn eine unzureichende Anzahl der Moleküle von Interesse sind abgebildet, entweder aufgrund der schlechten Markierungseffizienz, übermäßiges Ausbleichen oder eine unzureichende Bildnummer, dann das resultierende Bild Super-Resolution wird punktiert und diskontinuierlich sein als Nyquist-Kriterien nicht eingehalten, 14,27 .
Und schließlich ist der dritte Schritt, Bildverarbeitung, besonders wichtig im Vergleich mit Standard-Fluoreszenzmikroskopie-Techniken. Es gibt eine Reihe von frei im Handel erhältlich und Algorithmen, die sowohl ein Vorteil, in Bezug auf Auswahl, und ein Nachteil ist, dass es verwirrend sein kann zu wissen, welche am besten geeignet ist, um zu verwenden. Wenn zum Beispiel die Rohdaten gut verteilte räumlich getrennte blinkt dann eine Einzelmolekül-Anpassungsalgorithmus sehr genau und effizient zu sein, beispielsweise durch die spärlich Anpassungsalgorithmen im Regensturm 27, rapidSTORM 24,25, palm3d 12 und 26 QuickPALM Software . Wenn die Rohdaten enthält eine Menge von überlappenden Signalen dann Algorithmen, die besser geeignet sein können, umfassen DAOSTORM 34, 35 und 3B deconSTORM 36. Darüber hinaus sind diese Algorithmen enthalten Schwellenwerte für verschiedene Kriterien wie Signal zählt, oder Photonen pro Blinken, sowie verschiedene Bilddarstellungsmöglichkeiten wie die Visualisierung mit geglätteter Gauß-Funktionen oder als Histogramme mit Pixelraster, wo der Super-Auflösungspixelgröße kann durch den Benutzer ausgewählt. Alle diese Optionen ändern das Aussehen des fertigen Bildes und haben Auswirkungen auf die Bildinterpretation und-analyse.
Daher präsentieren wir 3 Testproben, die den neuen Benutzer mit einem Ausgangspunkt für Dye-Lokalisierung Basis Super-Resolution-Experimente, die aus Gründen der Klarheit werden wir so STORM zu beziehen und erfahrene Anwender die Möglichkeit bieten wird, um weiter zu optimieren, ihre Experimente. Erstens ist es möglich, die Oberfläche des Glases mit einer fluoreszierenden Schicht von Dextran-Farbstoff-Konjugat. Dies bietet eine schnelle und einfache Möglichkeit, um festzustellen, dass das Mikroskop-, Farbstoff-und Puffer arbeiten daran, blinkt Fluoreszenzsignal erzeugen. Das Verfahren kann dann durch den Vergleich mittlere Lokalisierungsgenauigkeit und Anzahl von Regensturm Metriken erzeugt werden, um Pufferbedingungen zu optimieren, Bildaufnahme-Einstellungen und testen verschiedene Farbstoffe erweitert werden. Zweitens stellen wir ein einfaches Protokoll zur Herstellung von Aktin-Filamenten auf Glas, das leicht mit Phalloidin-Farbstoff-Konjugaten markiert werden können. Diese bieten ideale Strukturen, um Messungen der Auflösung in der Regel 27 und der Halbwertsbreite (FWHM) nehmender ein Faden wird als eine empirische Abschätzung der Resolution 37 gegeben. Es ist zu beachten, dass die Auflösung variiert zwischen den Proben und zwischen den Bildern innerhalb der gleichen Probe, weil Auflösung in der Lokalisierung Basis Super-Resolution-Mikroskopie ist eine Funktion der Fluorophor Helligkeit, Hintergrundgeräusche und Lokalisierung Dichte 27 und das sind nicht unbedingt konstant über der Probe werden. Aktin-Filamente werden verwendet, um mögliche Artefakte wie mislocalizations demonstrieren und treiben und wie sie mit Software-Funktionen innerhalb von Rainstorm identifiziert werden. Außerdem beschreiben wir die Verwendung von fluoreszierenden Bezugsmarkierungen sowohl richtige Maß und Drift. Und drittens die Färbung der Zellen mit dem epidermalen Wachstumsfaktor (EGF)-Farbstoff-Konjugate beschrieben. EGF ein nützlicher Indikator für die superauflösenden Bildern, weil ein Teil des Rezeptors auf der Zelloberfläche eine Endocytose durchläuft über Vesikel, die Unter-Beugungsstrukturen Größe von etwa 50-150 nm Durchmesser 27,38,39.
Protokoll
Hinweis: In diesem Protokoll werden Tipps und Anregungen folgende bestimmte Schritte gefunden. Die Bezeichnung "* 1" zeigt an, dass Note 1 ist relevant für diesen bestimmten Schritt, und so weiter.
1. Leuchtstoff-Beschichtung von Glas-Dextran
- Nach Zugabe von 200 ul 0,01% Poly-L-Lysin-Lösung in jede Vertiefung einer 8-Kammerdeckgläser und Inkubation für 10 min. Entfernen mit einer Pipette, um sicherzustellen, dass keine Restflüssigkeit ist.
- Rekonstituieren Dextran-Alexa 647 * 1 nach den Anweisungen des Herstellers, um eine 2 mg / ml Stammlösung erstellen. Daraus verdünnen 0,25 ul in 25 ul entionisiertem Wasser, um eine 20 ug / ml Lösung.
- Um eine hohe Dichte der Beschichtungs Dextran-Alexa 647-Lösung zu erstellen verdünnt 20 &mgr; l der 20 &mgr; g / ml Lösung in einer Gesamtmenge von 200 &mgr; l entionisiertem Wasser. Für eine mitteldichte Lösung zu verdünnen 2 ul in 200 ul de-ionisiertes Wasser (1:10.000 Verdünnung aus dem ursprünglichen Stammlösung). Für einen niedrigenDichte Lösung zu verdünnen 0,2 ul in 200 ul de-ionisiertes Wasser (1:100.000 Verdünnung aus dem ursprünglichen Stammlösung).
- In 200 ul der verdünnten Dextran-Alexa 647-Lösungen in jede Vertiefung und Inkubation für 10 min. Längere Inkubationszeiten können verwendet werden, was zu einer dichteren Beschichtung Dextran zurückzuführen sind. Ausziehen und mit H 2 O dreimal * 2
Anmerkung 1: Andere Dextran-Farbstoff-Konjugate können verwendet werden. Unkonjugierten Dextran kann auch Farbstoffe konjugiert werden, falls gewünscht Kombinationen sind nicht im Handel erhältlich.
Anmerkung 2: Die gleichen Dextran Kammern über einen Zeitraum von Wochen wieder abgebildet, obwohl die Gleichmäßigkeit der Fluoreszenz kann verringern. Lagerung bei 4 ° C in Abwesenheit eines Puffers wird empfohlen.
2. Leuchtstoff Aktin-Filamente auf Glas
- Nach Zugabe von 200 ul 0,01% Poly-L-Lysin-Lösung in jede Vertiefung und Inkubieren der Kammer für 10 min * 3. Rebewegen sich mit einer Pipette, um sicherzustellen, dass keine Flüssigkeit übrig ist.
- Hinzufügen von 90 &mgr; l Actin allgemeinen Puffer (gemäß den Anweisungen des Herstellers rekonstituiert) zu jeder Kammer. In 10 ul von 10 uM vorgeformte Aktin-Filament-Lösung und 1 ul Phalloidin-Alexa 647 (0,2 Einheiten, wenn in 1,5 ml Methanol als den Anweisungen des Herstellers) gelöst und vorsichtig pipettieren, auf und ab zu mischen. Inkubation: 30 min * 4.
Anmerkung 3: Eine Erhöhung des Volumens des Filaments Lösung innerhalb der Kammer zu weniger Filamente Bindung an die Poly-L-Lysin beschichteten Glas.
Anmerkung 4: Die Inkubationszeiten von bis zu 48 Stunden bei 4 ° C mit guten Ergebnissen getestet. Bildqualität verschlechtert Aktin-Filament einmal Kammer Schaltpuffer so ist es nicht empfehlenswert, die dieselbe Probe für mehr als einen Tag benutzen ausgesetzt.
3. Microsphere Leuchtstoffkügelchen als Bezugsmarken
- Verdünnen 1 ul TetraSpeck Perlen in 200 ul PBS und mischen.
- Fügen Sie die verdünnt Perlen in einem bildgebenden Kammer und warten Sie 15 min * 5. Entfernen Sie die Lösung und 3 x waschen mit PBS vor der Bildgebung.
Anmerkung 5 - die Verdünnung und Inkubationszeit kann angepasst werden, um unterschiedliche Dichten von Perlen zu erhalten. Dieses Protokoll führt in der Regel zwischen 3 bis 10 Perlen pro 20,5 x 20,5 um um Feld-of-view.
4. Epidermal Growth Factor Zellfärbung
- HeLa-Zellen in Kultur Abbildungskammern auf etwa 80% Konfluenz in Dulbecco modifiziertem Eagle Medium (DMEM) mit 10% fötalem Rinderserum (FBS) und 1% Penicillin-Streptomycin-Lösung ergänzt.
- Entfernen Sie das Kulturmedium und waschen mit PBS. Dann fügen Sie 500 ul von 4% Formaldehydlösung (4 ml 10% Formaldehydlösung, 1 ml 10X PBS, 5 ml Wasser) für 10 min. Entfernen Sie die Formaldehyd und 3 x waschen mit PBS. Nicht in die Zellen d bleibenry und verwenden Sie immer PBS gepufferten Lösungen zu hypotone Stress zu vermeiden.
ACHTUNG - Formaldehyd ist extrem giftig. Stellen Sie sicher, dass geeignete Schutzhandschuhe, Schutzbrille und Laborkittel getragen werden. Überprüfen Sie die lokalen Richtlinien für die Entsorgung von Formaldehyd.
- Rekonstituieren EGF-Alexa 647 nach Herstellerangaben um eine 50 ug / ml Stammlösung erstellen. In 2 ul dieser Stammlösung zu 200 ul 0,1% BSA-Lösung (in PBS). Entfernen Sie die PBS von den Zellen, fügen Sie den EGF-Lösung und Inkubation für 30 min.
- Entfernen Lösung und wäscht 3 mal mit PBS vor der Zugabe einer Blockierungslösung aus 0,1% BSA (in PBS) für 15 min. Entfernen Sie diese und waschen noch 3 mal mit PBS vor der Bildgebung.
5. Schalt Buffer Vorbereitung
- Bilden eine Enzymstammlösung (A) mit 10 &mgr; l Katalase (20 ug / ml), 20 ul 1 M Tris (2-carboxyelthyl) phosphin-Hydrochlorid (4 mM), 2,5 ml Glycerin (50%), 125 &mgr; l1 M KCl (25 mM), 100 ul 1 M pH 7,5 Tris-HCl (20 mM), 5 mg Glucoseoxidase (1 mg / ml) und oben bis zu 5 ml Volumen mit diH20. Dies ist ausreichend, um 100 x 50 ul-Aliquots, die bei -20 ° C gelagert und für bis zu 1 Jahr verwendet werden kann, zu machen.
- ) Machen Sie eine Glucose-Stammlösung (B) mit 4 g Glucose (100 mg / ml), 4 ml Glycerin (10%) und 36 ml diH20. Dies ist ausreichend, um 100 x 400 ul Aliquote, die gelagert werden können machen - 20 ° C und bis zu 1 Jahr verwendet.
- Machen Sie eine Reduktionsmittel-Vorratslösung (C) mit 113,6 mg MEA-HCl (1M) und 1 ml diH 2 0. Verwenden Sie frische oder machen 10 x 100 ul Aliquots, die bei -20 ° C gelagert und für bis zu 1 Monat verwendet werden können (nicht Aliquots einfrieren).
- Kurz vor der Bildgebung, mischen das Enzym (A), Glucose (B) und zusammen Reduktionsmittel (C) Stammlösungen im Verhältnis 50 ul, 400 ul, 100 ul und auf 1 ml mit PBS * 6. Dieser Puffer wird nun abfangen Sauerstoff und haben eine reduzierende Umgebung (100 mM MEA-HCl) * 7. * 8 8.5 (Einstellung ist normalerweise nicht notwendig) - Der endgültige pH-Wert sollte im Bereich von 6,0.
Anmerkung 6 - dieser Puffer zur Verwendung mit Carbocyanin-Farbstoffe, wie Cy5 und Alexa 647.
Anmerkung 7 - die endgültigen Enzymkonzentrationen sind 50 ug / ml (5 U / ml) Glucose-Oxidase und 1 ug / ml (40-60 Einheiten / ml) an Katalase. Die enzymatische Aktivität (Einheiten) wird von Lieferanten gegeben und können variieren. Die Berechnungen für Katalase annehmen, dass 1 ug / ml Endkonzentration nach dem Schritt 5.4 werden mit 50 Einheiten des Enzyms enthalten. Verschiedene Pufferzusammensetzungen einschließlich ähnlicher sauerstoffbindende Komponenten 21,30,40 gefunden werden. Für eine Zusammenfassung der Puffer-und Farbstoffkombinationen siehe Referenzen 28,29. Glycerin und TCEP sind für langfristige Lagerung bei -20 ° C erforderlich
Anmerkung 8 - wenn die Bildgebung Aktinfilamente hinzufügen 2 mM MgCl 2 und 0,2 mM ATP zur Stabilisierung ter Filamente.
6. Mikroskop Erwerb von STORM-Daten (mit Alexa 647-Farbstoff)
- Schalten Sie die STORM / PALM Mikroskop, vorzugsweise mindestens 3 Stunden vor der Belichtung, damit ein thermisches Gleichgewicht zu erreichen. Vor diesem Abbildungs eine erhöhte Chance Drift.
- Setzen Sie die Bildraum in den Mikroskoptisch Probenhalter. Sicherzustellen, dass die Probe fest an der Halterung und ist flach.
- Entfernen Sie die PBS von der Bildkammer und dann oben mit dem Schalt Puffer zu füllen. Ein Deckglas sorgfältig über die Oberseite der Kammer, um sicherzustellen, dass sich keine Blasen an alle und die gesamte Kammer bedeckt. Füllen Sie zusätzliche Puffer oder PBS, wenn irgendwelche Luftblasen zu sehen sind sonst Puffer Leistung sinken kann.
VORSICHT -, um die Chancen der lateralen und axialen Drift der Probe in Bezug auf die Objektivlinse zu minimieren, wird empfohlen, dass die Probe und der Puffer äquilibrieren gelassenauf Raumtemperatur für mindestens 15 min vor der Bilderzeugung.
- Suchen Sie eine Leuchtstoffstruktur von Interesse, die abgebildet werden. Wählen Sie den gewünschten Beleuchtungswinkel, in diesem Fall ein TIRF oder stark geneigten Winkel wird empfohlen, da dies verbessert das Signal-zu-Rausch-Verhältnis durch Minimieren out-of-focus-Licht, die besonders von Vorteil für die Zellproben ist. Werfen Sie einen Referenzbeugungsbegrenzten Bild der Struktur vor der STORM-Bildgebung.
- Erhöhung des Anregungslasers (mit einer geeigneten Anregungswellenlänge von ca. 640 nm) auf eine hohe Leistung, entsprechend etwa 2 kW / cm 2, während Bildgebung mit Kameraeinstellungen von 10 ms Belichtung und einer Zykluszeit von etwa 50 Hz (Frames pro Sekunde) . Sobald die Fluorophore sind in eine spärlich Blinkmuster (wahrscheinlich innerhalb von 10 Sekunden für die meisten Proben) umge sammeln 10.000 Frames * 9.
Hinweis 9 - 10000 Rahmen ist für die hier beschriebenen Probenaber es kann notwendig sein, um die Rahmennummer zu 50.000 oder mehr für andere Proben zu erhöhen.
7. Die Rekonstruktion superauflösende Bilder von Raw-Daten (mit Regensturm)
- Öffnen Sie die Datei rainSTORM.m aus MATLAB und führen (Abbildung 1A).
- In der Regensturm Fenster (Abbildung 1B) wählen Sie die Bilddatei mit der Schaltfläche Durchsuchen analysiert werden. Dies sollte ein. Tif-Datei (ImageJ kann verwendet werden, um andere Dateitypen in eine tif-Format zu konvertieren) sein. Ändern Sie die Pixelbreite, um die Rohdaten des Mikroskop-System verwendet, um die Daten zu erwerben * 10 entsprechen. Lassen Sie die anderen Werte auf die Standard.
Anmerkung 10 - Eine typische EMCCD Kamera hat eine Pixelgröße von 16 um so auf ein System mit einem 100-fach Objektiv die Bildpunktgröße auf dem Bild 160 nm sein. Kommerziellen Systemen die Pixelgröße in der Regel innerhalb der Software angezeigt. Pixelgrößen variieren zwischen 100 nm und 160 nm für die meisten Lokalisierungs Mikroskopen.
- Drücken Sie die Taste "Prozessbilder" und warten, bis ein vorläufiges Bild erscheint. Die Dauer der Behandlung wird von der Dateigröße, Computer-Spezifikation und der Anzahl der Kandidaten blinkt in den Rohdaten * 11 ab.
Anmerkung 11 - 10.000 Bildsequenzen von Aktin und EGF Daten dauerte 23 Sekunden und 25 Sekunden, um jeweils unter Verwendung eines PC mit einem Intel Xeon E5420 CPU. Mit dem gleichen Computer ohne Parallelverarbeitung Toolbox in MATLAB, oder mit einem Computer ohne Mehrkern-Verarbeitung, waren mal 66 sec und 81 sec auf.
- So generieren Sie einen aktualisierten Super-Resolution-Bild drücken Sie die Taste "Open-Bewerter" und ein zweites Fenster wird angezeigt (Abbildung 1C). Drücken Sie die "Kontrast anpassen"-Taste, um die Bildanzeige zu ändern wie gewünscht (1D). In einigen Fällen, wo das Bild sehr dunkel ist der Maximalwert verringert werden sollte.
- Verwenden Sie die Drehzahliewer Fenster (Abbildung 1C), nützliche Bildqualitätsmetriken zu generieren und zu verfeinern, die Super-Resolution-Bild weiter. Stellen Sie die ersten drei Qualitätskontrollparameter auf Werte von 4.000, 0,1 und 0,8 bis 2,0 bzw. * 12. Aktualisieren Sie die Zählungen pro Photon-Wert, der entweder auf einem Photonenkalibrierungsmessung oder mit Photon-Kurve von der Kamera-Hersteller für einen bestimmten EM-Gain-Einstellung angegeben Eichkurve Werte beruhen sollte. Dies ist entscheidend für den Erhalt genaue Präzision und Auflösung * 13 Messungen.
Anmerkung 12 - Signal Grafen lehnt blinkt basierend auf Helligkeit Kriterien. Je höher der Wert, desto heller die Blink sein muss, werden als Lokalisierungs im endgültigen Bild akzeptiert. Dies muss je nach den Photonenausgang des Farbstoffs und die Belichtungszeit und die Empfindlichkeit der Kamera verändert werden. Toleranz ablehnt blinkt, wenn eine signifikante quadratische Fehler zwischen dem Signal und der angepassten Gauß dh double Spitzen. PSF Sigma Bereich lehnt blinkt, wenn die Einbaubreite der PSF aus diesem Bereich liegt, kann also eine engere Bereich verwendet werden, um out-of-focus-Signale und großen aggregierten Blobs von konstanten Fluoreszenz abzulehnen. Mit einem breiteren Spektrum kann in Fehllokalisation Artefakte im endgültigen Bild erscheinen, führen. In der Praxis empfiehlt es sich, erste Qualitätskontrolle durchführen mit Hilfe der Lokalisierungsgenauigkeit Cutoff-Parameter.
Anmerkung 13 - für mehr Auflösung Metriken siehe Referenzen 23,27. In Kürze durch das Wissen, die Anzahl der Photonen, die von jedem hergestellt blinken ist es möglich, die Lokalisierungsgenauigkeit jedes Lokalisierungs berechnen und somit ableiten Gesamtmittel Präzision Schätzungen für das gesamte Bild. Mit einem Andor Ixon DU-897E mit einem Gain-Einstellung von 200 den Grafen pro Photon-Wert beträgt 9,04.
- Ändern Sie die Lokalisierungsgenauigkeit Cutoff (1C), um zwischen der Optimierung mittlere Lokalisierungs precis KompromissIonen gegen Lokalisierungsnummer in dem endgültigen Bild. Werte von 30-50 nm in Abhängigkeit von der Qualität der Daten und der Probe empfohlen. Beide die Histogramme und die info.txt Dateien können verwendet werden, um diese Entscheidung (1F und 1G) zu informieren.
- Die Rekonstruktion Skalierungsfaktor (Abbildung 1C) Standard ist 5, die Super-Resolution-Pixel des 32-nm-Annahme, dass die Pixelbreite in der Originalbilder ist 160 nm erzeugen wird. Wenn die RAW-Bilder haben eine Pixelgröße von 100 nm das wird super-aufgelöste Bilder mit Pixeln von 20 nm zu erzeugen. Erhöhen Sie den Skalierungsfaktor, der kleiner Super-Resolution-Pixel im fertigen Bild * 14 zu produzieren.
Anmerkung 14 - Auflösung der Lokalisationsmikroskopie, hängt von der für die Visualisierung (dh die Pixelgröße von einem einfachen Histogramm-Rekonstruktion) sowie die Lokalisierungsgenauigkeit erforderlich Glättung. In der Praxis sollte die Rekonstruktionspixelgröße in der Regel kleiner als die Lokalisierungs seinPräzision (siehe mittlere Präzisionsschätz Metrik in der Info-Text-Datei - Schritte 6.11 & 6.12). In diesem Fall ist der Auflösungsverlust durch Rekonstruktion Pixelgröße klein 23,27 sein. Beispielsweise können die Durchschnittsgenauigkeit Schätzungen in der Zeilen-und Spaltenrichtung von Fig. 4E sind 16,1 nm und 16,2 nm aufweist. Eine Pixelgröße von 16 nm wurde verwendet, um diese Daten (Rekonstruktion Skalierungsfaktor von 10 mit einem ursprünglichen Pixelbreite von 160 nm) sichtbar zu machen.
- Ändern Sie die Grenze Frame-Bereich (1C), um den Wiederaufbau, um Teilmengen der Rohdaten zu beschränken, zum Beispiel [2001-inf] würde die ersten 2000 Bilder von Rohdaten aus.
- Drücken Sie die Schaltfläche "Run Rezensent" (1C), um eine aktualisierte Super-Resolution-Bild (1E) zu erzeugen.
- Drücken Sie die 'Ansicht Histogramme "-Taste (Abbildung 1C), um die Bildqualitätsmetriken (1F) * 15 anzuzeigen.
Anmerkung 15 - Die Grafik oben rechts, welches die Anzahl der angenommenen Lokalisierungen gegen Kamerarahmennummer und der Thompson-Lokalisierung Precisions Histogramm in der rechten unteren Ecke (1F) kann verwendet werden, um die Option Lokalisierungsgenauigkeit Cutoff-Rezension zu informieren. Zum Beispiel würde unter Verwendung einer 50 nm-Sperr alle Lokalisationen mit schlechter Genauigkeit von in dem endgültigen Bild Superauflösungs aufnehmen lässt.
- Drücken Sie die Schaltfläche "Bild speichern" in der Gutachter (1C), um alle diese Daten * 16 speichern.
Anmerkung 16 - Zwischen 3 und 5-Dateien können je nach den gewählten (Bild Summe, STORMdataImage, STORMprocessed, Infos & hists) Optionen gespeichert werden, siehe Abb. 1G. Die STORM verarbeitete Bild mit modifizierten Kontrast und Farbkarten angezeigt. Die STORMdataImage ist ein Graustufenbild, bei dem der Grauwert jedes Pixels entspricht der tauber von Lokalisierungen, die in ihm identifiziert wurden.
- Nach Prüfung der Daten (zB Info.txt Datei und Histogramme) Rückkehr zum Schritt 7.6 und wiederholen Sie die nachfolgenden Schritte mit verschiedenen Rezensent Parameter, falls gewünscht. Mit 'Save Image "in Schritt 7.11 werden die zuvor gespeicherten Daten überschreiben.
8. Box-Tracking-und Drift-Korrektur (mit Regensturm)
- Folgen Sie den Schritten von 7,1 bis 7,9, um ein Bild in der üblichen Weise zu erzeugen.
- Drücken Sie die Taste 'Box-Tracking' in der Rezensent (1C), und klicken und ziehen Sie eine Box auf das Bezugsmarken oder die Struktur der Zinsen auf das Bild überprüft.
- Warten Sie, bis ein neues Bild erscheint, die die "Boxed Positionen" (siehe 6B, 6C und 6F für Beispiele) angezeigt wird. Speichern Sie dieses Bild, wenn gewünscht.
- Wenn das Objekt von Interesse ist ein Referenz-Markers dann Driftkorrektur kann durch Anklicken des 'Set Anchor "-Taste gefolgt von der" Sub durchgeführt werdenTrakt Drift "-Taste. Schließlich klicken Sie auf "Run Rezensent 'wieder eine neue STORM Bild, das jetzt werden alle Lokalisierungen nach den Bezugsmarken Positionen korrigiert generieren. Die Wulst Positionen werden von der endgültigen Bewertung Bild gelöscht.
- Wenn es andere Bezugsmarkierungen im endgültigen Bild Drift korrigiert, können diese durch Drücken von "Box-Tracking 'entfernt werden,' Löschen Boxed 'und dann so oft' Run-Bewerter", wie gewünscht.
Ergebnisse
Dextran
Eine erfolgreiche Beschichtung von Dextran sollte eine Leuchtstoffmonoschicht zu erzeugen. Bei der hohen Konzentration sollte diese relativ einheitliche angezeigt. Bei niedrigeren Konzentrationen wird es spärlicher (2A) angezeigt. Viele STORM / PALM Mikroskope haben die Möglichkeit, den Winkel der Beleuchtung von TIRF Epifluoreszenz zu ändern. Bei Verwendung eines Vollformat-Kamera-Ansicht, zum Beispiel bei 512 x 512 Pixel auf einem typischen EMCCD Kamera sollte eine gleichmäßige Ausleuchtung zu beachten. Wenn es irgendwelche Streifen oder out-of-focus-Regionen kann zeigen, dass die Probe sollte in den Probenhalter mit frischem Öl auf die Objektivlinse wieder eingesetzt werden. Alternativ kann es ein Problem mit dem Mikroskop zeigen.
Beim Erwerb von Super-Resolution-Rohdaten die Abbildungsleistung Laser sollte in etwa 2 kW / cm 2 erhöht werden. Es wird eine anfängliche Burst von Fluoreszenz, gefolgt von blinken als die Fluorophore in Antriebsvorübergehende Dunkelzuständen. Bei hohen Dichten Dextran blinkt die wahrscheinlich überlappen, insbesondere in der Nähe der Beginn der Bildaufnahme (Video 1). Bei mittleren und niedrigen Dichten sollten diese blinkt spärlich sein, dh räumlich getrennt und im Fokus mit keinem offensichtlichen Grund (siehe Rahmen 2.000, 5.000 und 8.000, 2A, Videos 2 und 3). Während dieser Phase der Bildaufnahme, bei konstanter Laserbeleuchtung, die Zahl der blinkt mit der Zeit ab (vgl. Rahmen 2000 mit Rahmen 8000 in der hohen Dichte Probe 2A). Der Hauptunterschied zwischen den verschiedenen Super-Resolution-Bilder der verschiedenen Dextran-Konzentrationen (hoch, mittel und niedrig) ist der Rückgang der Zahl der Lokalisierungen (2A und 2B). Mit anderen Worten, die Konzentration der fluoreszierenden Moleküle, die Anzahl der Blinksignale in den Ausgangsdaten und die Anzahl der Lokalisierungen eine proportionale Beziehung. Diese Beziehung,jedoch ist keine einfache lineare als bei sehr hohen Dichten Molekül sich die Software nicht, um erfolgreich zu lokalisieren Moleküle (vergleichen Sie die roten und blauen Linien, 2C). Der Grund dafür ist, dass bei der hohen Konzentration ist es nicht möglich, die Verarbeitungssoftware, die Positionen mit der Gaußschen Anpassungsalgorithmus, wo die blinkt nicht-sparse passen. Da die blinkt, verringern durch die Akquisitionsphase durch Photobleaching kann die Software mehr und mehr der blinkt passen, wie sie spärlich (2A und 2C) zu werden. Außerdem können auch einzelne Farbstoffmoleküle zu blinken, und daher mehr als einmal 28,41,42 lokalisiert werden.
Ein häufiges Problem bei der Abbildung einer dieser Proben, vor allem aber die Dextran eine hohe Dichte, kann die Anwesenheit von hellen, aber unkonzentriert Fluoreszenz Dunst, die schnell diffundierenden werden während der Akquisitionsphase STORM Bild angezeigt wird. Dies unterscheidet sich von den hohen Kontrast auf Fluorophoredie Oberfläche des Glases, die gesehen werden kann blinken (3A, Video 5). Diese freistehenden Fluoreszenzmoleküle können durch Erhöhung der Anzahl der Waschschritte mit PBS vor der Zugabe der Pufferschalt oder durch Zugabe von frischem Puffer in die Schaltkammer (3B, Video 6) verhindert oder beseitigt werden. Verarbeiten und Vergleichen der Daten von jeder Bildfolge führt zu sehr unterschiedlichen Superauflösungsbilder, die eine Abnahme bei der Anzahl der Lokalisation und der Präzision, mit der sie von der Software, die blinkt lokalisieren (Fig. 3C, 3D, 3E ausgerüstet sein und 3F).
Aktin-Filamente
Formten Aktinfilamente ersichtlich an der Oberfläche des Glases durch beugungsbegrenzte Abbildung (4A-4C) geklebt werden. Wenn die Anzahl der Filamente sehr niedrig wird, kann dann eine längere Inkubationszeit verwendet werden oder eine Abnahme des Volumens des AktinFilament-Lösung hilft auch. Auswahl einzelner relativ hellen Filamente (4D) und nicht verheddert Bereichen führt zu einer besseren Bildqualität. Während der Akquisitionsphase sollte hell Scharf blinkt entlang der Länge des Fadens (Video 7) gesehen werden. Sparse Blinken sollte während der Akquisitionsphase gesehen werden und dann anschließend in der verarbeiteten Daten sollte es eine dünne Endlosfaden (4E) sein, und die Lokalisierungen pro Frame sollte mit einem allmählichen Rückgang (4F), anders als in 3E.
Wenn das Blinken nicht-spärlich, oder wenn die Software nicht in der Lage, um die Moleküle zu lokalisieren, eine subtilere Artefakt, genannt Mislokalisation 32 führen kann. Dieser entsteht, wenn die Software-mittelt die Position von zwei überlappenden Moleküle und die Lokalisierung Position in der Mitte zwischen ihnen. Ein Hinweis, dass es keine wesentliche Anzahl von überlappe bliNKS und folglich mislocalizations, ist, dass die Durchschnittspräzisionsschätzungen in der gleichen Zeilen-und Spaltenrichtungen, also horizontal und vertikal sein, wo es mislocalizations würden diese entlang der Länge des Filaments aufgetreten sind, erzeugt eine größere als die normale Blink ( dh verteilt auf mehr Pixel), die haben damit weniger genau in eine der Richtungen lokalisiert worden wäre. Dies wird am einfachsten erkennen, wo es eine einzelne Aktin-Filament in dem Bildbereich und es horizontal oder vertikal liegt. In diesem Fall die STORM Mikroskop erreicht eine mittlere Genauigkeit von 16 nm in beiden Richtungen. Dies führt zu einem Genauigkeitsgrenze, ein Maß für die effektive Bildauflösung von etwa 34 nm auf. Diese Kennzahlen werden von Rainstorm 27, aber, wie wir haben eine fadenförmige Struktur mit gleichmäßigem Durchmesser, 7 nm mit der sehr kleinen Phalloidin Alexa-647-Label können wir ein Maß für die Halbwertsbreite, um die Auflösung des Bildes zu schätzen. Durch draFlügel eine Gerade durch den Glühfaden der Super-Resolution-Bild in ImageJ (4G), mit der Handlung Profilfunktion (4H) und anschließend Durchführen einer Gauss Passform (4I) die Halbwertsbreite als 43,2 nm berechnet. Beim Versuch, diese Messung empfehlen wir, dass die Pixelgröße sollten übereinstimmen oder etwas kleiner als der mittlere Präzision Schätzung für das Bild (siehe info.txt Datei 1G). In diesem Fall wurden 16 nm Pixel verwendet, um ein Bild zu rekonstruieren.
Zwei verwandte Probleme können mit Sturm, wo die blink Fluorophore werden nicht spärlich, dh einzelne Moleküle innerhalb von ca. 250 nm blinken gleichzeitig und damit die Signale überlappen auftreten. Die erste ist, dass je nach Algorithmus und den Qualitätskontrollkriterien verwendet es ist, blinkt die überhaupt nicht lokalisiert werden. Dies führt in Super-Resolution-Bilder mit wenigen oder keinen Lokalisierungen. Das zweite Problem dermislocalizations tritt auf, wenn die beiden blinkt ausreichend nahe beieinander, als eine einzige blink erscheinen aufgetreten. In diesem Fall ist die Position in dem endgültigen Bild stellt einen Mittelwert aus beiden. Für weitere Einzelheiten über diese siehe Referenz 32. In beiden Fällen kann dies mit sehr hoher Dichte Proben unzureichend Laserleistung oder mit Schaltpufferprobleme auftreten. Dieses Problem ist offensichtlich, wo eine Reihe von Aktin-Filamente Verzweigung und / oder einander kreuzen (Fig. 5A-D, Video 9). Durch Verarbeiten Teilmengen von Frames, und Vergleichen der ersten und letzten Rahmen 5000 können wir einen anderen resultierende Bild anzuzeigen. In der Super-Resolution-Bild mit den ersten 5.000 Frames (5C) können wir sehen, dass es viele Lokalisierungen in der Mitte des Bildes, aber wenn Sie die letzten 5000 Frames, nur sehr wenige davon sind offensichtlich, und wir mit links nur die Filamente, wenn auch geschuldet der geringen Anzahl von Lokalisierungen in der imag etwas diskontinuierlichene (Fig. 5D). Wird eine zu hohe Dichte Blinken vermutet Vergleich der Bilder mit der Lokalisierung pro Rahmen Daten deuten stark darauf hin, dass dieses Problem auftritt, während der erste Satz von Frames ist eine Durchschnittszahl von Lokalisierungen pro Rahmen von über 10 gegenüber der zuletzt eingestellten von Rahmen, wo es etwa 4 (Fig. 5E). Um die Wahrscheinlichkeit von auftretenden mislocalizations es ideal ist, so wenig Lokalisierungen pro Rahmen wie möglich zu haben, aber wenn es eine große Anzahl von Molekülen, die abgebildet werden, dh für eine hohe Dichte Probe erfordert dies minimiert, dass eine große Anzahl von Erfassungs Bilder, die zu einem anderen Problem in STORM Mikroskopie, die Drift genommen werden.
Lateral Drift - Aktin-Filamente und Passermarken
Drift auftritt, wenn die Probe bewegt sich in Bezug auf die Objektivlinse durch die Datenerfassungsphase. Das ist schwierig oder unmöglich zu sehen, During die Bildakquisitionsphase, insbesondere wenn es sich lateral anstatt axial, oder es sei denn, es wird speziell gemessen, wie es in der Regel weniger als 50 nm im Verlauf von mehreren Minuten für relativ stabile Mikroskopsysteme. Jedoch in rekonstruierten Bildern von bekannten Strukturen wie Aktinfilamente mit gut definierter Struktur, kann es in der Super-Auflösungsbilder erfasst werden. Das erste Anzeichen, daß seitliche Drift aufgetreten sein, dass die Struktur im Vergleich zu 67 nm größer ist als erwartet (6A, Video 8) beispielsweise mit einem relativ großen Halbwertsbreite im Vergleich zu den Daten von Präzisionsgrenze Regensturm, in diesem Fall 90 nm auf. Jedoch ist eine bessere Art und Weise, um eine Drift zu erfassen, indem die Lokalisierungen als eine Funktion der Zeit, das heißt zu sehen, ob die Lokalisierungen in den späteren Bildern im Vergleich zu denen in der frühen Frames verschoben. Dies ist in dem Fall von Aktin-Filamenten, die sehr klein und der einheitlichen Struktur sind, gesehen werden, wennmit einem Farbcode über die Box-Tracking-Funktion in Rainstorm (6B und 6C) angezeigt.
Drift ist ein gut bekanntes Problem, und es gibt eine Reihe von Strategien, die verwendet werden können, um es zu minimieren oder zu korrigieren, 19 nach dem Erwerb entweder mit Bezugsmarkierungen 21,43 oder Kreuzkorrelationen 44. Um Drift und richtig für sie zu messen, können fluoreszierende Kügelchen von 100 nm Durchmesser als Bezugsmarker (6D) verwendet werden. Weil sie klein und hell sind ihre Position genau zu messen mit Gauß-Anpassungsalgorithmen, wie beispielsweise Regen. In einem Beispiel, wo es relativ starken Drift von ca. 100 nm im Verlauf von 3 min 10 sec, während der Akquisitionsphase (6E), der gleichen Box-Tracking-Funktion können Farbcode verwendet, und bestätigen, dass Drift aufgetreten (6F werden ). Da alle vier Perlen in diesem Beispiel zeigen nahezu identische Drift es ist pÖGLICHE, einer von ihnen, in diesem Fall Wulst 2 auswählen, als Referenz zu verwenden und subtrahieren die Drift von den anderen Perlen (6G). Durch Zugabe von Bezugsmarkierungen auf einer biologischen Probe von Interesse ist, dann wird es möglich, zu messen und zu korrigieren jede Drift in dem die darunterliegende Struktur nicht bekannt ist oder viel mehr als eine Variable Aktin-Filament oder einem fluoreszierenden Kügelchen ist.
Epidermal Growth Factor
Schließlich kann EGF-gefärbten HeLa-Zellen verwendet, um ein realistisches Beispiel der Bildauflösung in den Zellen (7A, Video 10) zu geben. Diese Zellen sind relativ einfach, Bild wie sie den Hauptteil des EGF-Fluoreszenz in der Ebene des Fokus auf der Zelloberfläche in der Nähe des Deckglases haben. Die weniger hellen Bereich in der Mitte entspricht der Position des Kerns. TIRF-Beleuchtung können die Bildqualität durch die Beseitigung out-of-focus-Fluoreszenz, die aus Teilen der Zelle m verbessernembrane nicht in unmittelbarer Nähe zu dem Glas (etwa 150 nm Eindringen in Zellen). in Regionen von Interesse in der beugungsbegrenzten Bild vergrößert typischerweise undeutlich (Fig. 7B und 7C), aber in den Superauflösungsbilder sollte es eine Mischung sein, von Clustern und gelegentlichen isolierten einzelnen Pixel (7D-7F). Diese werden entweder isoliert EGF-Rezeptoren an der Zelloberfläche oder möglichst wenig unspezifische Bindung darstellen. Die Cluster werden ca. 100 nm im Durchmesser und sind wahrscheinlich auf die Bildung Pits und Vesikel, der Weg, über den EGF vorwiegend nach unten reguliert und endocytosiert entsprechen. Typische mittlere Präzision Schätzungen etwa 20 nm für diese Art der Probe mit einer Genauigkeitsgrenze von etwa 45 nm auf. Es sollte angemerkt werden, dass diese Präzisionsgrenze Maß der effektiven Auflösung nicht berücksichtigt Etikettengröße, oder einem Drift, die mit Bezugsmarker gemessen werden kann, aber immer noch noticeable von "Kometenschweife" auf den Clustern oder mit dem Box-Tracking-Funktion, wie in Abbildung 6 skizziert und in Protokollabschnitt 8 beschrieben.
| Komponente | Endgültige Konzentration |
| Katalase | 1 &mgr; g / ml (50 Einheiten) |
| Glucose | 40 mg / ml |
| Glucose-Oxidase | 50 &mgr; g / ml |
| Glyzerin | 12.50% |
| KCl | 1,25 mM |
| MEA-HCl | 100 mM |
| TCEP | 200 uM |
| Tris | 1 mM |
Tabelle 3. Schaltpuffer
| Typische Acquisition Einstellungen | Wert |
| Pixelgröße (nm) | 160 |
| Belichtungszeit (ms) | 10 |
| Verstärkung | 200 |
| Rahmengröße (Pixel) | 128 x 128 |
| Zykluszeit (fps) | 52,5 |
| Rahmennummer | 10.000 |
| 640 nm Laserleistungsdichte (kW / cm 2) | 2 |
Tabelle 4. Acquisition Einstellungen
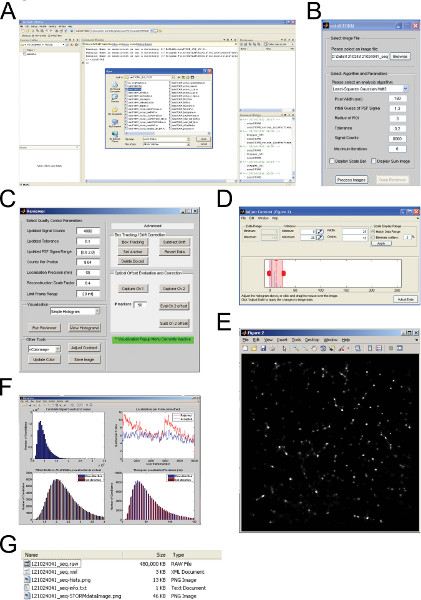
Fig. 1 ist. STORM Bildrekonstruktion Mit Regen. (A) Öffnungsregensturm aus MATLAB. (B) Rainstorm grafische Benutzerschnittstelle (GUI). (C) Rainstorm Bewertungs GUI. (D) Kontrast einstellen-Fenster. (E) STORM Bild nach Überprüfung und Kontrasteinstellung. (F) SeineHistogramme der Bildqualität Metriken. (G)-Dateien nach dem Drücken Spartaste im Bild Rezensent GUI erzeugt. Klicken Sie hier, um eine größere Abbildung anzuzeigen .

Abbildung 2. (A) Beugung begrenzt (DL)-Bilder zeigen unterschiedliche Konzentrationen von Dextran vor STORM Bildgebung. Super-Resolution-(SR) Bildrekonstruktionen haben eine Pixelgröße von 25 nm auf. 10.000 Bilder wurden mit einem 128 x 128 Pixel Bildgröße und einzelne Bilder aus dieser Sequenz dargestellt (2000, 5000, 8000) gesammelt. Mit einer Belichtungszeit 10 ms erfasst 52,5 Frames pro Sekunde. Bilder eine Pixelgröße von 160 nm auf. Zur Klarheit der Anzeige einer 0,1% Pixelsättigung Kontrastverstärkung wurde mit ImageJ aufgebracht. Die mittlere PräzisionSchätzungen sind 28 nm (hoch), 24 nm (mittel) und 16 nm (niedrig) für die verschiedenen Dextran Bilder. Die Lokalisierung Dichten 724 pro um 2 (hoch), 526 pro um 2 (mittel) und 13 pro ähm 2 (niedrig). (B) Graph, der ein Durchschnitt von drei 10.000 Framesequenzen von jeder Konzentration von Dextran. Fehlerbalken zeigen die Standardabweichung. (C) Graph, der die Anzahl der angenommenen Lokalisierungen pro Rahmen einer rollierenden Durchschnitt 100 Rahmen. Klicken Sie hier, um eine größere Abbildung anzuzeigen .

3. Poor Quality Dextran-Daten. (A) Beugung begrenzten Rahmen von einem 15.000 Rahmen STORM-Sequenz. Beachten Sie die diffuse Fluoreszenz Dunst über das Bild. Dies wird dadurch verursacht fluoropho res Diffusion durch das Medium. 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. (B) Das gleiche wie (A), nachdem der Puffer geändert worden war. Beachten Sie die verbesserten Kontrast als ungebundene Fluorophore wurden weggespült. (C) Hochauflösende Bildrekonstruktion entsprechend den in (A) gesammelten Daten. Identische Bildgröße, sondern mit Pixeln von 25 nm auf. Die mittlere Präzision schätzen 35 nm ist. (D) Hochauflösende Bildrekonstruktion entsprechend den in (B) gesammelten Daten. Identische Bildgröße, sondern mit Pixeln von 25 nm auf. Die mittlere Präzision schätzen 30 nm. (E) Graph, der die Anzahl der angenommenen Lokalisierungen pro Rahmen einer rollierenden Durchschnitt 100 Rahmen. Die rote Linie entspricht STORM-Sequenz (A & C), wo es einen hohen Hintergrund. Die blaue Linie zeigt die Daten entsprechend (B & D), wo der Hintergrund ist gering. (F) Grafik, die die Lokalisierung akzeptiert Nummer für die Bilder entsprechend hoch (C) und niedriger (D) Hintergrunddaten.href = "https://www-jove-com.remotexs.ntu.edu.sg/files/ftp_upload/50579/50579fig3large.jpg" target = "_blank"> Klicken Sie hier für eine größere Abbildung zu sehen.

4. Typische Actin Daten. (AC) Beugungsbegrenzte Bilder von Aktin-Filamenten vor der Zugabe des Puffers und Schalt STORM Bildgebung. Variable Längen der Filamente zu sehen. Sehr helle Fäden sind oft mehrere Fäden zusammen verheddert. Die Pixelgröße beträgt 160 nm. (D) eine beugungsbegrenzte Abbildung eines einzelnen Aktin-Filament. (E) Bild STORM (0,1% Kontrastverstärkung in ImageJ angewendet). Aus einer 10.000 Bildsequenz mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Die Pixelgröße von 16 nm auf. Die mittlere Präzision schätzen 16 nm ist. (F) Graph, der die Anzahl der angenommenen Lokalisations pro Bild, mit einem Rollgestell 100 Durchschnitt. (G) Eine in der Region des Aktin-Filament gezoomt von (E) vor der Erweiterung mit einer gelben Linie Profil über gezogen zu kontrastieren. (H) Ein Grundstück Profilansicht von der gelben Linie über das Aktin-Filament gezogen. In ImageJ erzeugt. (I) Ein Gauß-Fit der Handlung Profil mit dem Kurvenanpassungstool in ImageJ. Die Standardabweichung, d, wurde von 2,35 multipliziert, um eine Messung der Halbwertsbreite von 43,2 nm zu erhalten. Klicken Sie hier, um eine größere Abbildung anzuzeigen .
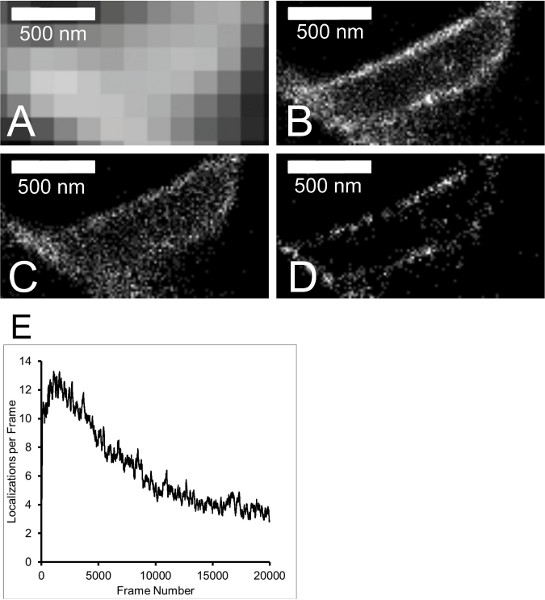
5. Mislocalized Aktin-Filamente. (A)-Beugung begrenzt Aktin-Filament. 160 nm Pixel. (B) STORM Bild der in (A) gezeigt Aktin-Filament. Aus einer 20.000 Bildsequenz mit einem 128 x 128 Pixel frame Größe, ein 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Die STORM Pixelgröße beträgt 16 nm auf. Alle 20.000 Frames verarbeitet. Die mittlere Präzision schätzen 17 nm ist. (C) als (B), sondern nur mit den ersten 5000 Frames der Framesequenz 20.000 verarbeitet. Die mittlere Präzision schätzen 18 nm ist. (D) Wie (B), aber nur mit den letzten 5000 Bilder der 20.000 Bildfolge verarbeitet. Die mittlere Präzision schätzen 17 nm ist. (E) Grafik der Lokalisierungen pro Rahmendaten von vollen 128 x 128 Pixel Bildansicht.

6. Lateral Drift. (A) STORM Bild einer Aktin-Filament aus einem 10.000 Bildsequenz rekonstruiert mit einem 64 x 64 Pixel Bildgröße, 10 ms Belichtungszeit und bei 64,6 Bildern pro Sekunde aufgenommen. Die STORM Pixelgröße beträgt 32 nm auf. Die mittlere Präzision schätzen ist32 nm auf. (B) A STORM Bild angezeigt mit der "Box-Tracking"-Funktion in Regen. Lokalisierungen sind mit einer Farbe entsprechend der Rahmennummer, wenn sie erworben wurden, angezeigt werden, zum Beispiel, sind Lokalisierungen von früh Aufnahmesequenz blau; Lokalisierungen von Ende in der Aufnahmesequenz sind rot. Die Vertriebenen Farben zeigen an, dass Drift ist aufgetreten. (C) Ein gezoomt in der Region von (A) angezeigt, mit dem Box-Tracking-Funktion in Regen. Die Vertriebenen Farben zeigen Drift ist aufgetreten. (D) eine beugungsbegrenzte Bild vier 100 nm fluoreszierenden Kügelchen, die als Bezugsmarkierungen verwendet werden können. Pixelgröße 160 nm. Zahlen 1-4 zeigen abgeschnitten und gezoomt Perlen einzeln. (E) Jede Leuchtstoffraupe entsprechend (D) in Rainstorm rekonstruiert aus einem 10.000 Bildsequenz mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Die STORM Pixelgröße beträgt 5 nm auf. Die mittlere Präzision schätzen ist 7 nm. (F) Perlen, die (D) und (E),angezeigt, mit der "Box-Tracking"-Funktion. Die Vertriebenen Farben zeigen Drift ist aufgetreten. (G) Mit Wulst Nummer 2 als Referenz, Perlen 1, 3 und 4 sind nach dem 'Subtrahieren Drift "-Funktion angezeigt wird, in Rainstorm verwendet. Vergleich mit (E) zeigt, dass die Seitendrift korrigiert. Die STORM Pixelgröße beträgt 5 nm auf. Klicken Sie hier, um eine größere Abbildung anzuzeigen .
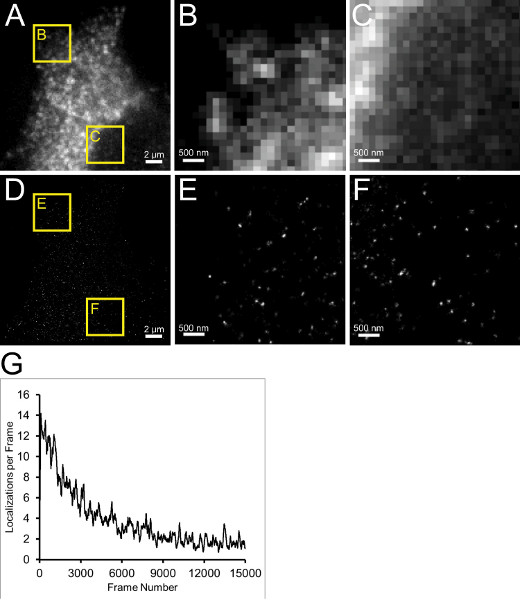
Abbildung 7. Typische EGF Daten. (A) beugungsbegrenzte Bild eines Teils einer HeLa-Zelle an der basalen Zelloberfläche fokussiert. Gelbe Felder zeigen in Regionen von Interesse in (B) gezeigt gezoomt & (C). (B) beugungsbegrenzten Bildes aus dem Bereich nahe dem Rand der Zelle (Feld B) vergrößert. (C) in die Beugung begrenzt Gezoomte Bild von Region unter den Zellkern (Feld C). (D) STORM Bild entsprechend (A). Aus einer 10.000 Bildsequenz mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Die STORM Pixelgröße beträgt 25 nm auf. Die mittlere Präzision schätzen 21 nm ist. (E) STORM Bild zu Feld E (D) entspricht. (F) STORM Bild zu Feld F (D) entspricht. (G) Lokalisierungen pro Rahmendaten von (D). Klicken Sie hier, um eine größere Abbildung anzuzeigen .
. 1-4 Videos Videos entsprechen 2A mit unterschiedlichen Konzentrationen Dextran Abbildung: 1 = hoch, 2 = mittel, 3 = gering, 4 = keine). 10.000 Bildsequenzen mit 128 x 128 Pixel Rahmengrößen mit einer Belichtungszeit 10 ms bei 52,5 Bildern pro Sekunde erfasst. Klicken Sie hier, um ein Video zu sehen ,load/50579/50579video2.mov "target =" _blank "> Video 2, Video 3 , Video 4
Videos 5-6. Videos entsprechen 3 A & B. Video 5 Abbildung ist Vorwäsche und Video 6 ist nach der Wäsche nach ungebundenen Fluorophore wurden entfernt. 15.000 Bildsequenzen mit einem 128 x 128 Pixel Bildgröße, eine 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Klicken Sie hier, um Video anzuzeigen 5 , 6 Video .
Video 7. Video zeigt das rohe Bildsequenz, die verarbeitet wurde, um die STORM Bild in 4E generieren. 10.000 Rahmen sequence mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Klicken Sie hier, um Video-7 sehen .
Video 8. Video zeigt das rohe Bildsequenz, die verarbeitet wurde, um die STORM Bild in 5B generieren. 20.000 Bildsequenz mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Klicken Sie hier, um Video-8 zu sehen .
Video 9. Video zeigt das rohe Bildsequenz, die verarbeitet wurde, um die STORM Bild in 6A generieren. 10.000 Bildsequenz mit einem 64 x 64 Pixel Bildgröße, 10 ms Belichtungszeit und bei 64,6 Bildern pro Sekunde aufgenommen. Klick hier, um Video 9 zu sehen.
Video 10. Video zeigt das rohe Bildsequenz, die verarbeitet wurde, um die STORM Bild in 7D generieren. 10.000 Bildsequenz mit einem 128 x 128 Pixel Bildgröße, 10 ms Belichtungszeit und bei 52,5 Bildern pro Sekunde erfasst. Klicken Sie hier, um Video anzusehen 10 .
Diskussion
Wir zeigen, mit einigen einfachen Testproben und der frei verfügbaren Software-Verarbeitung Rainstorm ist es möglich, STORM Super-Resolution Imaging optimieren. Diese Werkzeuge und Methoden wird nützliche Startpunkte für neue Benutzer und Möglichkeiten für erfahrene Benutzer das Vertrauen in ihre Mikroskope und ihre Verwendung von ihnen für die biologische und zelluläre Strukturen mit bisher unerreichter Genauigkeit untersuchen zu erhöhen. Durch Verwendung einer Kombination von Proben mit bekannter oder gut verstanden Strukturen und einem Algorithmus, der eine Anzahl von nützlichen Bildqualitätsmetriken, wie Mittelwert Präzisionsschätzungen Lokalisierungsnummer und Histogramme, ist es möglich, die Bildqualität zu verbessern und mehr Vertrauen haben, erzeugen kann, in der bildgebenden Verfahren STORM. Es gibt keine one-size fits all Ansatz zur Erfassung der Daten, da es eine Reihe von verschiedenen kommerziellen und selbst gebauten Mikroskop-Konfigurationen, die verwendet werden können. Darüber hinaus gibt es viele Probenvorbereitung und Bildaufnahmeschritte, die beeinflussen könnenReferenz das endgültige Bild daher mit Software-Tools und Testmuster ist entscheidend für das Verständnis und die Optimierung STORM Bildqualität.
Darüber hinaus können diese Protokolle nützliche und weniger zweideutig Möglichkeiten der Fehlerbehebung von Problemen, die auftreten können. Beispielsweise das Dextran Probe ist ein sehr nützlicher Weg, um zu ermitteln, ob es eine Fehljustierungen oder ungleichmäßige Beleuchtung der Probe. Wenn es Bedenken, dass die Schaltpuffer kann nicht arbeiten eine sehr einfache Sichtprüfung, um zu sehen, ob es eine "blinkende 'wird Ihnen helfen. Aktinfilamente sind eine nützliche Methode zur Messung der Auflösung mit FWHM Vergleiche sowie Hervorhebung Drift und Fehllokalisation Artefakte. Es sollte jedoch angemerkt, daß als Lokalisierung basierte Superauflösungsverfahren können Fluorophor Dichte empfindlich sein, ungeachtet der anderen Faktoren, wie Belichtungszeit, Bildrate, Laserleistung und der Art und Weise wird das Bild verarbeitet werden, ist es unmöglich, zuweisen Der Beschluss, eineninsbesondere Mikroskop und davon ausgehen, dass alle Bilder wird diese Auflösung haben. Was ist möglich, jedoch ist es, verschiedene Aspekte der Auflösung wie Mittelwert Lokalisierungsgenauigkeiten, Lokalisierung Zahl messen und Drift-27. Auch wenn Bezugsmarkierungen können nicht in jedem Versuch sie können eingearbeitet werden, zumindest, verwendet, um ein Mikroskop-System, seine Umwelt besser zu verstehen, zu charakterisieren und operativen Überlegungen wie, wie viel Zeit erforderlich ist, um das thermische Gleichgewicht erreicht nach dem Start werden. Sowie Korrektur von lateralen Drift können Bezugsmarkierungen verwendet werden, zu charakterisieren und zu korrigieren Axialdrift, obwohl dies erfordert die Verwendung einer astigmatischen Linse und einen Rückkopplungsmechanismus, um die Probenposition zu korrigieren, während die Bilder erworben 43. Handels Super-Resolution-Systeme gehören in der Regel eine Art von Stabilitätskontrolle oder Fokus-Lock-Mechanismus, der eine praktische Lösung für die Korrektur Fokusdrift sein können.
Es gibt eineWieder Alternativen zu unspezifisch Beschichten des Glases mit Dextran, wie die Verwendung von Farbstoffen, die direkt oder anderen konjugierten Moleküle, wie Sekundärantikörper. Eine Einschränkung dieser Ansätze ist, dass die Anzahl der Moleküle an der Glas gebunden ist nicht bekannt. Alternative filamentöse Strukturen, die verwendet wurden, schließen Mikrotubuli 28 und 21 DNA. Die Kombination von sehr geringer Größe und bequem im Handel erhältlichen Reagenzien machen jedoch Aktin eine attraktive Alternative, insbesondere der Abstand des divergierenden oder verzweigte Filamente können auch eine nützliche Messung der Systemleistung 27 sein.
Es gibt Raum für die weitere Entwicklung von Testproben, trotz der jüngsten Fortschritte in diesem Bereich 28,29,46,47. Insbesondere stellt Multi-Color-Imaging eine Reihe von Herausforderungen in allen drei Hauptaspekte der Bildgebung, Probenkennzeichnung, Bildaufnahme (Hardware) und Software (Bildverarbeitung und Ausrichtung). Es gibt ein seiteine Reihe von Publikationen die Lösung dieser Fragen 4-6 und es ist daher klar, dass geeignete Testproben und Methoden kritisch zu erzeugen und zuverlässig Interpretation dieser Bildtypen. In der Tat, vor kurzem wurde gezeigt, dass dSTORM könnte verwendet werden, um zwei Farbbilder zu nehmen, und zu beheben, die hochsymmetrische Natur der Kernporenkomplex und die Autoren vermuten, dass dies eine ideale Möglichkeit, um die Leistung der chromatischen Aberration 45 Korrekturen zu beurteilen. Ein weiterer interessanter Ansatz ist die Verwendung von DNA-Origami, ein nanoruler, die die Möglichkeit der Positionierung Fluorophore zu bestimmten Unter-Beugungs Abständen 46 schafft erstellen. Dies bietet eine Möglichkeit zur Beurteilung Auflösung und macht Abstandsmessungen. Jedoch ist das letztendliche Ziel, diese Superauflösungstechniken, um nicht-idealisierten Proben, wie Zellen, die komplexe dreidimensionale Strukturen anzuwenden. In diesem Fall wird eine Kombination aus gründlicheres Verständnis ter Technik kombiniert mit Software-Tools, die den Anwender bei der Erfassung von Daten, die Verarbeitung in geeigneter Weise, und Bereitstellung von Bild Metriken helfen, ist wahrscheinlich die letzte Antwort sein. 28,29,47,48
Offenlegungen
Wir haben nichts zu offenbaren.
Danksagungen
Wir erkennen an, Mittel aus dem chemischen und biologischen Messtechnik-Programm von National Measurement Büro in Großbritannien. Wir danken Sebastian van de Linde, Miklos Erdelyi und Eric Rees für technische Beratung und Anregungen. Wir danken Miklos Erdelyi, Eric und Max Rees Ryadnov für hilfreiche Kommentare und Diskussionen zu diesem Manuskript.
Materialien
| Name | Company | Catalog Number | Comments |
| Labtek Imaging chamberglass | Fisher | CBR-166-390E | Sample preparation |
| Inverted Microscope | Olympus | IX71 | * See below for alternatives |
| 100 X TIRF Objective Lens | Olympus | UAPON 100XOTIRF | * See below for alternatives |
| EMCCD Camera | Andor | iXon 897 | * See below for alternatives |
| 640 nm laser | Toptica | iBEAM-SMART-640-S | *150 mW - for imaging Alexa 647 or Cy5 dyes |
| LabVIEW | National Instruments | *Acquisition software (controlling hardware) | |
| PC | Dell | Windows XP (64 bit), Intel Xeon E5420 CPU, 16 GB RAM *Instrument control and image processing | |
| ImageJ | Image analysis and processing http://rsbweb.nih.gov/ij | ||
| rainSTORM | Laser Analytics Group (Cambridge) software | http://laser.cheng.cam.ac.uk/wiki/index.php/Resources | |
| MATLAB | Running rainSTORM | http://www.mathworks.co.uk/products/matlab/ | |
| *Example of self-built STORM/PALM microscopes | Also see reference 29 http://code.google.com/p/quickpalm/wiki/Tutorial_CustomMicroscope | ||
| *Commercial STORM/PALM super-resolution microscopes | Leica SR GSD, Nikon N-STORM, Vutara SR-200, Zeiss Elyra P.1, DeltaVision OMX Blaze (Monet Localization) Alternatives to self-built microscopes | ||
| Table 1. Materials & Equipment | |||
| [header] | |||
| PBS (10X) | Fisher | VX70013065 | 1; 2; 3; 4 |
| Poly-L-Lysine | Sigma | P4707 | 1.1; 2.1 |
| Dextran-Alexa fluor 647 | Invitrogen | D-22914 | 1.2 |
| General actin buffer | Cytoskeleton Inc | BSA01 | 2.2 |
| Preformed-actin filaments | Cytoskeleton Inc | AKF99 | 2.2 |
| Phallodin-Alexa fluor 647 | Invitrogen | A22287 | 2.2 |
| TetraSpeck Microspheres (0.1 micron) | Invitrogen | T-7279 | 3.1 |
| HeLa cells | ATCC | CCL-2 | 4.1 |
| DMEM | Fisher | VX31966021 | 4.1 |
| FBS | Fisher | VX10500064 | 4.1 |
| Pen/Step | Invitrogen | 15070063 | 4.1 |
| Plastic dishes | Invitrogen | 734-0006 | 4.1 |
| EGF - Alexa fluor 647 | Invitrogen | E35351 | 4.3 |
| BSA | Sigma | A7906 | 4.3, 4.4 |
| Formaldehyde - 10 % solution EM grade | Polysciences | 04018-1 | 4.2 |
| Catalase | Sigma | C100 | 5.1 |
| Glucose oxidase | Sigma | G2133 | 5.1 |
| KCl | Sigma | P9541 | 5.1 |
| TCEP | Sigma | C4706 | 5.1 |
| Tris | Sigma | 93352 | 5.1 |
| Glucose | Sigma | C7528 | 5.2 |
| MEA-HCl | Sigma | M6500 | 5.3 |
| Glycerin | Sigma | G2289 | 5.1; 5.2 |
| Table 2. Reagents | |||
Referenzen
- Galbraith, C., Galbraith, J. Super-resolution microscopy at a glance. Journal of Cell Science. 124, 1607-1611 (2011).
- Toomre, D., Bewersdorf, J. A New Wave of Cellular Imaging. Annual Review of Cell and Developmental Biology. 26, 285-314 (2010).
- Bates, M., Huang, B., Dempsey, G., Zhuang, X. Multicolor Super-Resolution Imaging with Photo-Switchable Fluorescent Probes. Science. 317, 1749-1753 (2007).
- Bates, M., Dempsey, G., Chen, K. H., Zhuang, X. Multicolor Super-Resolution Fluorescence Imaging via Multi-Parameter Fluorophore Detection. Chemphyschem : a European journal of chemical physics and physical chemistry. 13, 99-107 (2012).
- Testa, I., et al. Multicolor fluorescence nanoscopy in fixed and living cells by exciting conventional fluorophores with a single wavelength. Biophysical journal. 99, 2686-2694 (2010).
- Baddeley, D., et al. 4D Super-Resolution Microscopy with Conventional Fluorophores and Single Wavelength Excitation in Optically Thick Cells and Tissues. PLoS ONE. 6, (2011).
- Shtengel, G., et al. Interferometric fluorescent super-resolution microscopy resolves 3D cellular ultrastructure. Proceedings of the National Academy of Sciences of the United States of America. 106, 3125-3130 (2009).
- Huang, B., Jones, S., Brandenburg, B., Zhuang, X. Whole-cell 3D STORM reveals interactions between cellular structures with nanometer-scale resolution. Nature Methods. 5, 1047-1052 (2008).
- Huang, B., Wang, W., Bates, M., Zhuang, X. Three-Dimensional Super-Resolution Imaging by Stochastic Optical Reconstruction Microscopy. Science. 319, 810-813 (2008).
- Juette, M., et al. Three-dimensional sub-100 nm resolution fluorescence microscopy of thick samples. Nat Meth. 5, 527-529 (2008).
- Vaziri, A., Tang, J., Shroff, H., Shank, C. Multilayer three-dimensional super resolution imaging of thick biological samples. Proceedings of the National Academy of Sciences of the United States of America. 105, 20221-20226 (2008).
- York, A., Ghitani, A., Vaziri, A., Davidson, M., Shroff, H. Confined activation and subdiffractive localization enables whole-cell PALM with genetically expressed probes. Nature Methods. 8, 327-333 (2011).
- Jones, S., Shim, S. -H., He, J., Zhuang, X. Fast, three-dimensional super-resolution imaging of live cells. Nature Methods. 8, 499-505 (2011).
- Shroff, H., Galbraith, C., Galbraith, J., Betzig, E. Live-cell photoactivated localization microscopy of nanoscale adhesion dynamics. Nature Methods. 5, 417-423 (2008).
- Hess, S., et al. Dynamic clustered distribution of hemagglutinin resolved at 40 nm in living cell membranes discriminates between raft theories. Proceedings of the National Academy of Sciences. 104, 17370-17375 (2007).
- Wombacher, R., et al. Live-cell super-resolution imaging with trimethoprim conjugates. Nature Methods. 7, 717-719 (2010).
- Klein, T., et al. Live-cell dSTORM with SNAP-tag fusion proteins. Nature Methods. 8, 7-9 (2011).
- Folling, J., et al. Fluorescence nanoscopy by ground-state depletion and single-molecule return. Nature Methods. 5, 943-945 (2008).
- Betzig, E., et al. Imaging Intracellular Fluorescent Proteins at Nanometer Resolution. Science. 313, 1642-1645 (2006).
- Hess, S. T., Girirajan, T. P., Mason, M. D. Ultra-high resolution imaging by fluorescence photoactivation localization microscopy. Biophys J. 91, 4258-4272 (2006).
- Rust, M., Bates, M., Zhuang, X. Sub-diffraction-limit imaging by stochastic optical reconstruction microscopy (STORM). Nature Methods. 3, 793-796 (2006).
- Hofmann, M., Eggeling, C., Jakobs, S., Hell, S. W. Breaking the diffraction barrier in fluorescence microscopy at low light intensities by using reversibly photoswitchable proteins. Proc. Natl. Acad. Sci. U.S.A. 102, 17565-17569 (2005).
- Thompson, R. E., Larson, D. R., Webb, W. W. Precise nanometer localization analysis for individual fluorescent probes. Biophys J. 82, 2775-2783 (2002).
- Wolter, S., et al. Real-time computation of subdiffraction-resolution fluorescence images. Journal of Microscopy. 237, 12-22 (2010).
- Wolter, S., et al. rapidSTORM: accurate, fast open-source software for localization microscopy. Nat. Methods. 9, 1040-1041 (2012).
- Henriques, R., et al. QuickPALM: 3D real-time photoactivation nanoscopy image processing in ImageJ. Nature Methods. 7, 339-340 (2010).
- Rees, E., et al. Blind Assessment of Localisation Microscope Image Resolution. Journal of Optical Nanoscopy. 1, 12(2012).
- Dempsey, G., Vaughan, J., Chen, K., Bates, M., Zhuang, X. Evaluation of fluorophores for optimal performance in localization-based super-resolution imaging. Nat Meth. 8, 1027-1036 (2011).
- van de Linde, S., et al. Direct stochastic optical reconstruction microscopy with standard fluorescent probes. Nature. 6, 991-1009 (2011).
- Heilemann, M., et al. Subdiffraction-Resolution Fluorescence Imaging with Conventional Fluorescent Probes. Angewandte Chemie International Edition. 47, 6172-6176 (2008).
- Owen, D. M., Sauer, M., Gaus, K. Fluorescence localization microscopy: The transition from concept to biological research tool. Commun Integr Biol. 5, 345-349 (2012).
- van de Linde, S., Wolter, S., Heilemann, M., Sauer, M. The effect of photoswitching kinetics and labeling densities on super-resolution fluorescence imaging. Journal of biotechnology. 149, 260-266 (2010).
- Veatch, S., et al. Correlation Functions Quantify Super-Resolution Images and Estimate Apparent Clustering Due to Over-Counting. PLoS ONE. 7, e31457(2012).
- Holden, S., Uphoff, S., Kapanidis, A. DAOSTORM: an algorithm for high- density super-resolution microscopy. Nature. 8, 279-280 (2011).
- Cox, S., et al. Bayesian localization microscopy reveals nanoscale podosome dynamics. Nat Methods. 9, 195-200 (2012).
- Mukamel, E., Babcock, H., Zhuang, X. Statistical deconvolution for superresolution fluorescence microscopy. Biophysical Journal. 102, 2391-2400 (2012).
- Shim, S. H., et al. Super-resolution fluorescence imaging of organelles in live cells with photoswitchable membrane probes. Proc. Natl. Acad. Sci. U. S. A. 109, 13978-13983 (2012).
- Parkar, N. S., et al. Vesicle formation and endocytosis: function, machinery, mechanisms, and modeling. Antioxid Redox Signal. 11, 1301-1312 (2009).
- Clague, M. J., Urbe, S. The interface of receptor trafficking and signalling. J Cell Sci. 114, 3075-3081 (2001).
- van de Linde, S., Sauer, M., Heilemann, M. Subdiffraction-resolution fluorescence imaging of proteins in the mitochondrial inner membrane with photoswitchable fluorophores. Journal of Structural Biology. 164, 250-254 (2008).
- Heilemann, M., Margeat, E., Kasper, R., Sauer, M., Tinnefeld, P. Carbocyanine Dyes as Efficient Reversible Single-Molecule Optical Switch. Journal of the American Chemical Society. 127, 3801-3806 (2005).
- Heilemann, M., Mukherjee van S,, A,, Sauer, M. Super-Resolution Imaging with Small Organic Fluorophores. Angewandte Chemie International Edition. 48, 6903-6908 (2009).
- Lee, S. H., et al. Using fixed fiduciary markers for stage drift correction. Opt Express. 20, 12177-12183 (2012).
- Mlodzianoski, M., et al. Sample drift correction in 3D fluorescence photoactivation localization microscopy. Optics express. 19, 15009-15019 (2011).
- Löschberger, A., et al. Super-resolution imaging visualizes the eightfold symmetry of gp210 proteins around the nuclear pore complex and resolves the central channel with nanometer resolution. Journal of Cell Science. 125, 570-575 (2012).
- Steinhauer, C., Jungmann, R., Sobey, T. L., Simmel, F. C., Tinnefeld, P. DNA origami as a nanoscopic ruler for super-resolution microscopy. Angew Chem Int Ed Engl. 48, 8870-8873 (2009).
- Laevsky, G. S., O'Connell, C. B. Comparative and practical aspects of localization-based super-resolution imaging. Current protocols in cytometry. Chapter 2, Unit2 20(2013).
- Gould, T., Verkhusha, V., Hess, S. Imaging biological structures with fluorescence photoactivation localization microscopy. Nature. 4, 291-308 (2009).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten