Method Article
不同连接方式电针对大鼠心电图及神经放电的影响
摘要
到目前为止,在临床和基础研究中还没有统一的电针连接方法。我们提出了一个方案,试图比较不同连接方法对大鼠心电图 (ECG) 和神经放电的影响,以探索连接电针仪的最合适方式。
摘要
电针 (EA) 是针灸中最常用的方法之一,对疼痛、抑郁、感觉运动障碍和其他疾病有很好的效果。EA 的有效性受多种因素影响,例如穴位选择的准确性、EA 治疗的持续时间和疗程以及 EA 参数。然而,很少有人讨论穴位不同、距离不同的EA仪器的正负极是否对疗效有影响。在本实验中,我们观察了将 EA 仪器连接到不同位置和距离的穴位对大鼠心电图和模糊神经放电的影响,并初步解释了不同方式的 EA 连接形成的电场是否对身体功能有影响。本实验中 EA 的连接模式包括身体两侧相同穴位、身体同一侧相同经络或不同经络穴位、同一穴位区域两针。结果显示,当正负极与身体两侧的穴位相连时,心电图和迷走神经活动的记录受到干扰 (前后肢相同);当穴位连接在身体同一侧时,两针之间的距离越小,对心电图和迷走神经活动记录的影响越小,效果随电流的增加而增加;当穴位位于同一穴位区域时,如果两针没有形成短路,则不会干扰心电图和迷走神经活动的记录。
引言
电针 (EA) 是一种治疗疾病的针灸疗法,通过将仪器输出的脉冲电流施加到人体的经络穴位。EA具有刺激参数稳定可调、可量化、定时、省力等优点,在某些疾病的治疗和科学研究中具有特殊优势,如各种神经痛和针灸麻醉的治疗机制研究、针灸镇痛等1.
一些因素会影响 EA 的有效性,例如穴位准确性、治疗持续时间和 EA 参数,例如波形、脉冲强度和频率。临床常用的 EA 是双向 EA,它引起的组织损伤较小,对人体正常生理功能的干扰较小。它还可以预防和治愈疾病。人体组织是由水、无机盐和带电胶体组成的复杂电解质的导体2。当 EA 应用于人体时,电场中的带电粒子会移动并引起浓度和分布的变化,从而影响人体的功能。运动、浓度和颗粒分布的变化是 EA 疗法的基础1。
在过去十年中,针对多种疾病的 EA 研究数量有所增加 1,2,3。关于 EA 的正负极的连接,很少有研究来详细阐明这一点。在 EA 期间,EA 仪器上的正负极应连接到两根针灸针上,以起到电刺激的作用。目前常见的模式如下:身体两侧两针连接同一穴位,身体同一侧不同穴位连接1。然而,这些连接方法的有效性尚未得到证实。一些科学家估计,身体两侧的两根针无法连接到正负极;否则,电流会影响心脏功能,但身体同一侧的两个不同点可以连接到正负极3。一些研究人员认为,连接正负极的针灸针应该在单个穴位区域使用,在穴位内形成电刺激,促进经络感应2。
各个穴位的电针可以激活或抑制神经放电 4,5。许多研究解释了 Tsusanli (ST36) 中 EA 对迷走神经的刺激作用 6,7,8。然而,这些研究没有详细说明 EA 的连接,也没有解释不同 EA 连接模式的影响差异。鉴于这项研究的空白,本研究使用电生理技术来解释不同 EA 连接对心电图和神经活动的影响。结果为 EA 的正确连接提供了进一步的证据。
研究方案
本实验方案经北京中医药大学标准化实验动物伦理审查批准,并完全按照实验方案(伦理审查代码:BUCM-2023110901-4046)进行。
1. 动物和分组
- 动物
- 获得 48 只健康的雄性 SPF 大鼠(8 周龄),体重约为 200-240 克。
注意:对于这项研究,动物由 Vital River Company [许可证号:SYXK(北京)2020-0033] 提供。 - 将所有大鼠饲养在北京中医药大学动物实验中心。在实验过程中,确保大鼠可以自由获得食物和水。
- 根据 12 小时的昼夜节律变化维持饲喂环境,并将环境温度控制在 23 ± 2 °C。
- 将所有手术器械浸泡在 75% 酒精中并高压灭菌。用紫外线灯对动物处理室进行消毒。
- 在麻醉下进行所有动物手术。用 20% 腹膜内氨基甲酸乙酯注射液 (1 g/kg) 麻醉大鼠,并确保大鼠继续自主呼吸。
- 在手术过程中用恒温板将大鼠的体温维持在 37 °C。
- 在实验过程中,用红霉素软膏保持大鼠的眼睛湿润。
- 实验结束时在麻醉下斩首并杀死大鼠,并根据需要储存标本/样品。
- 获得 48 只健康的雄性 SPF 大鼠(8 周龄),体重约为 200-240 克。
- 组
- 根据连接模式随机分组大鼠。将 8 只大鼠随机分配到每组。
- 对照组(无针灸):正常喂养大鼠,无需任何治疗。
- A 组,左前肢组中的单个穴位:将正负 EA 电极分别连接到 Quchi 点和距 Quchi 点 3 毫米(见 图 1A)。将瞭指点 (LI11) 定位在肘关节的外侧前凹处,定位后将针头垂直插入 ~5 毫米的深度。
- B 组,左前肢组中的两个穴位:将正负 EA 电极分别连接到曲池 (LI11) 和外关 (TE5) 点(见 图 1B)。在桡缝和尺骨缝合线中,将外关 (TE5) 点定位在前臂下 1/6 折点外。将针插入 2 mm 的深度。
- C 组,左前肢和后肢组中的两个穴位:将正负 EA 电极连接到 Quchi (LI11) 和 Tsusanli (ST36)(见 图 1C)。将 Tsusanli (ST36) 点定位在腓骨头下方 5 毫米和膝盖后外侧,然后将针头垂直插入 ~1 厘米的深度。
- D 组,两个后肢的相同穴位:将正负 EA 电极与双侧 Tsusanli (ST36) 连接(见 图 1D)。
- E 组,两个前肢上的相同穴位:将正负 EA 电极连接到双侧 Quchi(见 图 1E)。
2. 心电图连接
- 彻底麻醉后将大鼠约束在仰卧位。
- 平行于大鼠右前肢手腕、右后肢和左后肢的皮肤插入 1/2 英寸针灸针,避开肌肉。
- 将针手柄连接到记录电极:右前肢上的正(白色)电极,左后肢上的负(红色)电极和大鼠右后肢的参比电极(黑色)(见 图 2)。
- 使用生理信号记录器实时记录大鼠的标准肢体导联 II 表面心电图(采样率:1 KHz,过滤范围:低切滤波器,200 Hz;高切滤波器,0.8 Hz)。
3. 分离迷走神经并记录迷走神经放电信号
- 麻醉大鼠仰卧固定后,沿喉部和胸骨之间的颈部中线做一个 2-4 cm 的切口。
- 找到右颈动脉鞘(包含颈动脉、迷走神经和交感神经链)后,将右侧迷走神经干切断约 1-2 厘米(见 图 3A)。
注意:交感神经位于颈动脉外侧,伴随着迷走神经。与迷走神经相比,颈交感神经较细。 - 用一对铜钩电极连接神经干,并将参比电极夹在切口上以消除干扰。在整个实验过程中使用盐水维持迷走神经活动(参见 图 3B)。
- 用矿物油覆盖伤口表面,以保持电极和肌肉之间的绝缘。
- 使用生理信号记录器实时记录大鼠的神经放电情况(采样率:5 KHz,过滤范围:低切滤波器,100 Hz;高切滤波器,1000 Hz)。
4. EA 干预
注意:大鼠心电图后针灸和迷走神经分泌物稳定。
- 将两个针手柄分别连接到 EA 仪器的针夹上。
- 将 EA 刺激设置为波宽为 0.3 ms 的双向方波。将刺激强度设置为 0.2 mA,频率设置为 10 Hz,刺激时间设置为 20 分钟。
- 实时观察 EA 不同连接模式下大鼠的心电图和神经放电的变化。使用生理信号记录器在没有任何刺激的情况下收集数据 30 秒,EA 前 30 秒和 EA 后 30 秒。
- 使用记录软件记录大鼠心率、心电图波形和迷走神经放电的变化。
5. 数据的统计分析
- 比较大鼠在不同 EA 连接模式 (EA 前后) 的心电图和神经放电的变化。
- 将所有实验数据表示为均值±标准误差。
- 当数据通过正态分布检验时,执行学生的 t 检验。执行配对样本 t 检验以比较 EA 前后的变化,并将 p < 0.05 视为统计显著性。
结果
不同 EA 连接模式对大鼠心电图的影响
在对照组中,记录正常大鼠的心电图(见 图 4A)。结果发现大鼠的基线条件存在显著差异。大鼠的心率范围为 258 至 473 bpm(见 补充表 1)。
在 A 组中,记录数据与 Control 组相似。EA 刺激后 A 组大鼠的心率和波形没有显着变化(见 图 4A)。与对照组和 A 组相比,B 组的心电图波形显示干预较少,该组的心率也可以实时记录。其他组的结果表明,心电图数据受到 EA 频率的干扰(见 图 4A),因此在 EA 干预期间无法实时记录心电图。因此,我们记录了 EA 干预前后 60 秒的数据。
C 组和 D 组的心率在 EA 关闭并在短时间内恢复到之前的水平后增加,波形不受影响(见 图 4A)。E 组中的连接模式对 ECG 数据的影响最大。即使是低电流 (0.1 mA) 也会对数据记录产生很大影响。通电 20 分钟后,与 EA 之前相比,心率显着增加 (p < 0.05)(见 图 4B),并且动物在接下来的 30 分钟内不同程度地恢复。此外,大鼠的心电图波形显示高 p 波现象和 ST 段升高(见 图 4C),表明心脏异常。这些变化一直持续到实验观察结束。
不同 EA 连接模式对大鼠迷走神经放电的影响
结果显示,迷走神经放电呈规则簇状,30 s 内簇数从 31-66 个不等(见 补充表 2),神经放电记录与心电图相同。除对照组和 A 组外,其他组的神经放电数据受 EA 频率的影响,在 EA 干预期间无法准确记录(见 图 5A)。因此,我们记录了 EA 干预前后 30 s 的放电幅度(峰值)变化,并计算了 30 s 内的丛生放电次数。在 B 组中,迷走神经放电受 EA 频率的轻微影响,放电干扰随着电流的增加而增加。然而,30 s 内的放电变化和放电幅度并不明显。C 组中连接电流引起的电场很大,但束放电次数和最大放电值仍然稳定。然后,在 D 组中,虽然 EA 干预后出院频率降低,但与 EA 前相比数据不显著 (p > 0.05);E 组的数据显示影响最大,其中 30 s 内的束放电次数显着减少 (p < 0.05)(见 图 5B)。相比之下,峰值放电值增加 (p < 0.05)(参见 图 5C, 补充表 3)。
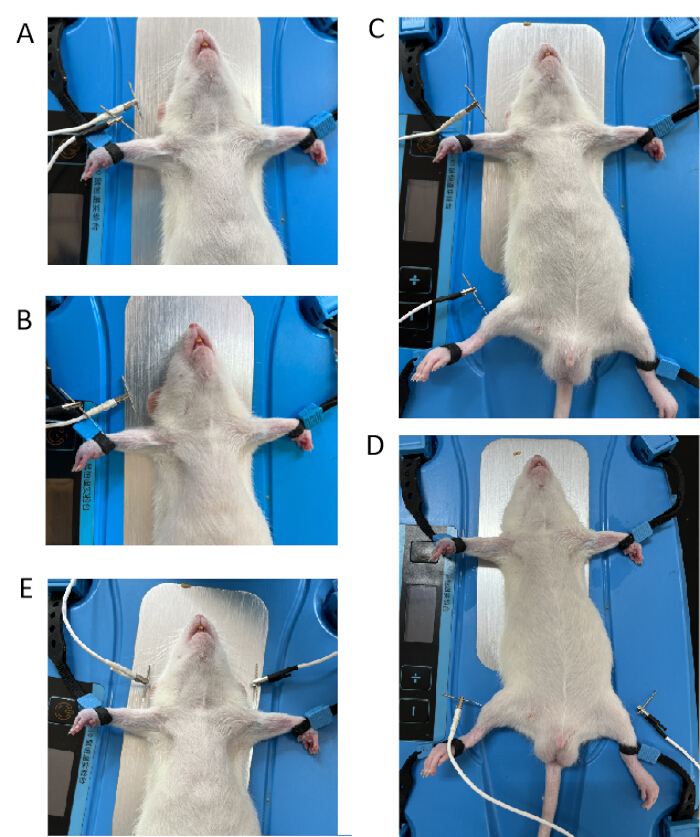
图 1:正负极 EA 电极的不同连接方式。 (A) 正负极 EA 电极连接到 Quchi 点,距离 Quchi 点 3 mm。(B) 正负 EA 电极连接到曲池 (LI11) 和外关 (TE5) 点。(C) 正负 EA 电极连接到 Quchi (LI11) 和 Tsusanli (ST36) 点。(D) 正负 EA 电极连接到双侧 Tsusanli (ST36) 点。(E) 正负 EA 电极连接到双侧 Quchi (LI11) 点。 请单击此处查看此图的较大版本。

图 2:ECG 观察的连接模式。 针柄连接到大鼠右前肢的正极(白色)电极和左后肢的负极(红色)电极,参比电极(黑色)连接到大鼠的右后肢。 请单击此处查看此图的较大版本。
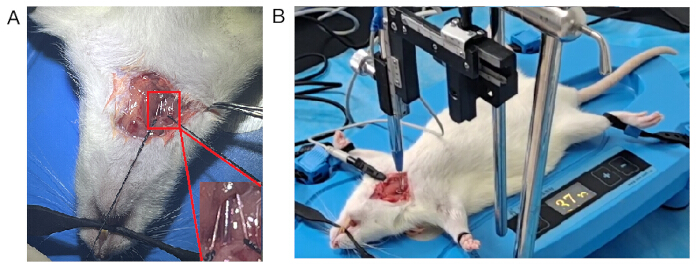
图 3:记录迷走神经活动的方法。 (A) 右侧迷走神经被分开。交感神经位于颈动脉外侧,与迷走神经相伴。左边是交感神经,右边是迷走神经。(B) 一对铜钩电极用于记录迷走神经活动,参比电极夹在切口上。 请单击此处查看此图的较大版本。
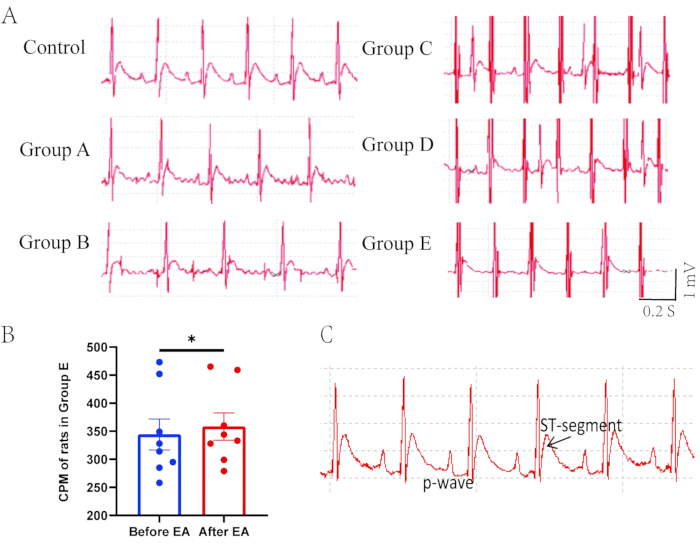
图 4:6 组心电图的记录数据。 (A) 实时记录不同 EA 连接模式的心电图。对照组大鼠心电图正常。A 组心电图与对照组相同。在 B 组中,连接 EA 后心电图受到轻微干扰。在 C、D 和 E 组中,心电图信号已被 EA 的频率完全掩盖。(B) 在 E 组中,与 EA 之前相比,EA 后的心率显着增加 (p < 0.05)。(C) E 组大鼠的心电图波形显示高 p 波现象和 ST 段升高。 请点击此处查看此图的较大版本。

图 5:不同 EA 连接模式对大鼠迷走神经放电的影响。 (A) 不同 EA 连接模式下迷走神经放电的实时记录数据。可以观察到迷走神经放电具有丛集放电的规律性。A 组迷走神经放电与对照组相似,而 B、C、D 和 E 组放电受到 EA 仪器频率的干扰。(B) E 组的数据显示影响最大,30 s 内丛集放电次数显着减少 (p < 0.05)。(C) 迷走神经分泌物在 30 s 内的峰值显著增加 (p < 0.05)。 请单击此处查看此图的较大版本。
补充表 1:不同组大鼠在 20 分钟 EA 会话前后 30 秒内的平均心率。*在 E 组中,平均心率与对照组相比显示出显着差异,而其他组则没有显着差异。 请点击此处下载此表格。
补充表 2:不同组大鼠在 20 分钟 EA 会话前后 30 秒内迷走神经簇放电的总数。*在 E 组中,大鼠的迷走神经丛集放电总数与对照组相比表现出显着差异,而其他组则没有显着差异。 请点击此处下载此表格。
补充表 3:不同组大鼠在 20 min EA 会话前后 30 s 内的迷走神经簇放电 (μV) 峰值。*在 E 组中,迷走神经簇放电的峰值与对照组相比显示出显着差异,而其他组则没有显着差异。 请点击此处下载此表格。
讨论
在这个实验中,我们观察了连接正负极的不同方式的影响,包括心率、迷走神经活动频率和放电振幅。结果表明,当正负极连接到身体的两个前肢时,它会影响生物电的发射。当正负极连接到身体的同一侧时,两针之间的距离越近,对生物电的影响就越小。电流越大,对生物电的影响就越大。所以,我们建议在同一穴位上连接模式,这样不会改变生物电。
通常,由于体电阻1,电场随着 EA 正负极之间距离的增加而增加。目前尚不清楚电场的影响是否会影响经络的运作和穴位的功能。为了证明这一点,需要一个更严格的实验设计。在 EA 刺激期间,来自电钻刺激信号的伪影和来自组织的电信号都被记录设备同时捕获。因此,录制的频率反映了这两个信号的合成,从而导致录制失真。因此,一些研究人员在电针治疗期间停止记录,这使他们无法在整个过程中观察到组织放电的变化9。在我们的实验中,即使在对侧相同点和同侧前后肢的连接模式下电流非常低,EA 的频率也会直接影响心电图记录和神经放电记录。在 EA10 的研究中,它被称为 EA 工件。一些研究表明了 EA 的伪影,因此修改了一些工具以消除 EA11 的伪影。在实验过程中,我们采取了许多措施来消除刺激伪影,例如连接地线和用锡箔包裹金属器件。我们发现 1 个穴位组 (A 组) 的心电图和神经放电在整个实验过程中不受影响。相比之下,在其他组中,EA 的刺激频率与测量数据叠加。这一发现为需要在 EA 干预期间记录数据的研究提供了一种简单有效的解决方案。
结果显示,心电图和迷走神经放电受连接前肢和后肢、后肢和双前肢的影响。但是,很难确定这种效果对身体是好是坏。一般认为,将前肢连接到双侧穴位产生的电流直接通过心脏。用这种方法长期治疗会对心脏1 有一定影响。这种效果也应根据身体的抵抗水平进一步评估,并使用疾病模型进一步证明。先前一项关于 EA 增强药物流产效果的研究12 发现,双侧穴位之间的连接不仅会加速水疱的排出,还会产生镇痛的效果,缩短月经时间。一侧合谷穴和三阴角之间的连接处效果减弱,不影响胎囊的排出率。然而,由于药物流产对人体具有破坏性,因此很难评估 EA 在这些连接模式下的效果。另一项研究13 比较了 EA 在贾吉穴的两种不同连接模式治疗腰椎间盘突出症的有效性。结果显示,Jiaji穴位 EA 的不同连接模式对腰椎间盘突出症有效,且跨脊髓对侧 Jiaji 点连接法的长期疗效优于同侧 Jiaji 点连接法。
本实验是基于健康大鼠的初步观察,在实验过程中发现大鼠之间存在很大差异。部分大鼠心率不规则,开始时心电图波形不稳定。在神经放电的观察中,发现一些大鼠开始时放电较弱。长期暴露在空气中后,神经很难保持稳定状态,大鼠呼吸时,电极接触肌肉,导致无法观察到的放电。我们使用的仪器的数据分析功能相对简单。未来需要更详细的实验设计和更先进的仪器来获得更客观的数据。
披露声明
作者没有什么可披露的。
致谢
本研究得到了国家中医高水平针灸管理重点学科(资助号 zyyzdxk-2023254)的支持。
材料
| Name | Company | Catalog Number | Comments |
| Accupuncture Needle | Hwato | N/A | |
| BL-420N physiological signal recorder | Techman | LAB-0017-0002-CDTM | |
| Electroacupucture instrument | HANS | 200A | |
| Erythromycin ointment | Shuangji | N/A | |
| Mineral oil | Solarbio | 8012-95-1 | |
| Thermostatic rat plate | Techman | JR-30 |
参考文献
- Liu, L., Dai, S. Clinical Electroacupuncture Therapy. , China Medical Science and Technology Press. Beijing. (2011).
- Han, J. Acupuncture: neuropeptide release produced by electrical stimulation of different frequencies. Trends Neurosci. 26 (1), 17-22 (2003).
- Yang, Z. Acupuncture and Moxibustion. , Shanghai Science and Technology Press. Shanghai. (1996).
- Zhang, Z., et al. Electroacupuncture regulates inflammatory cytokines by activating the vagus nerve to enhance antitumor immunity in mice with breast tumors. Life Sci. 272, 119259(2021).
- Liu, K., Jiang, J., Lu, S. Effect characteristics and mechanism of acupuncture in autonomic nerve regulation. Zhen Ci Yan Jiu. 46 (4), 335-341 (2021).
- Komegae, E. N., et al. Vagal afferent activation suppresses systemic inflammation via the splanchnic anti-inflammatory pathway. Brain Behav Immun. 73, 441(2008).
- Lu, M., et al. Electroacupuncture at ST36 modulates gastric motility via vagovagal and sympathetic reflexes in rats. World J Gastroenterol. 25 (19), 49-60 (2019).
- Jiang, H., et al. Electroacupuncture pretreatment at Zusanli (ST36) ameliorates hepatic ischemia/reperfusion injury in mice by reducing oxidative stress via activating vagus nerve-dependent Nrf2 pathway. J Inflamm Res. 16, 1595-1610 (2023).
- Ye, Z. A straightforward device for the removal of electroacupuncture artifacts. Journal of the First Affiliated Hospital of Shanghai. 6, 474-475 (1981).
- Huo, R., et al. Responses of primary afferent fibers to acupuncture-like peripheral stimulation at different frequencies: Characterization by single-unit recording in rats. Neurosci Bull. 36 (8), 907-918 (2020).
- Ye, X., et al. Effect of electroacupuncture at "Zusanli" (ST36) on vagal electrical activity in the rat. Acupuncture Research. 5, 290-293 (2006).
- Zhu, J., et al. Clinical observation of electroacupuncture enhancing drug abortion. Chinese Acupuncture and Moxibustion. 7, 389-391 (2000).
- Chen, J., Ni, M., Yin, J. Electroacupuncture treatments for gut motility disorders. Neurogastroenterol. 30 (7), e13393(2008).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。
我们使用 cookie 来增强您在我们网站上的体验。
继续使用我们的网站或单击“继续”,即表示您同意接受我们的 cookie。