Method Article
Kaynak Sınırlı Ayarlar için uygun bir HIV-1 İlaç Direnci İzleme Yöntemi
Bu Makalede
Özet
Antiretroviral tedavisi (ART) başarısız HIV-1 enfekte bireyler için ilaç direnci test gelecekteki tedaviler rehberlik ve tedavi sonuçlarını artırabilir. HIV yaygınlığının yüksek ama kaynak sınırlı ayarları optimize bireysel ve nüfus sağlık çıktıları sonuçta uygun fiyatlı ve erişilebilir ilaç direnci genotiplendirmesi ve yorumlama yöntemlerini gerektirir.
Özet
HIV-1 ilaç direnci ciddi antiretroviral tedavi (ART) etkinliğini ve etkisini uzlaşma potansiyeline sahiptir. Sahra-altı Afrika'da ART programları genişletmeye devam ederken, ART bireyler yakından ilaç direncinin ortaya çıkması için izlenmelidir. ART zaten dirençli viral suşlar izlemek için iletilen ilaç direnç sürveyansı da önemlidir. Genotiplendirme pahalı ve sofistike laboratuvar ve veri yönetimi altyapı gerektirir çünkü ne yazık ki, ilaç direnci testi, hala kaynak sınırlı ayarları kolayca erişilebilir değil. Bireyleri yönetmek ve bulaşan ilaç direncini değerlendirmek için bir açık erişim genotipik ilaç direnci izleme yöntemi tarif edilmektedir. Yöntem ilaç direnci desen yorumlanması ve bireysel hasta raporlarının nesil için ücretsiz açık kaynak yazılımı kullanır. Genotipleme protokol av plazma örnekleri için% 95'den daha büyük bir büyütme oranına sahiptiriral yük> 1000 HIV-1 RNA kopya / ml. Duyarlılığı viral yükleri <1.000 HIV-1 RNA kopya / ml için önemli ölçüde azaltır. Burada anlatılan yöntem olup, Birleşik Devletler Gıda ve İlaç İdaresi (FDA), Viroseq genotipleme yöntemi ile onaylı bir test HIV-1 ilaç direnci için bir yönteme göre doğrulanmıştır. Burada tarif edilen yöntemin sınırlamalar bu otomatik ve aynı panelinden alt tipleri A ve B, aynı zamanda ne kadar büyütülmüş, numune bir doğrulama panelinden dolaşan bir şekilde yeniden birleştirici CRF02_AG amplifiye etmek için başarısız olmadığı gerçeğini içerir.
Giriş
Güney Afrika'da HIV salgını, özellikle Güney Afrika 2, 3, antiretroviral tedavi (ART) bireylere eşlik eden bir üstel artış ile hızla 1 gelişen olmuştur. Insidansını 4 azaltılması ve kaynak sınırlı ayarları yaşam beklentisini (HBS) 5. artan büyük ölçekli tedavi programlarının epidemiyolojik etkisi üzerine delil olarak toplanmaya devam eder, ART kapsamını artırmak için çalışmalar hızlandırılacaktır. Test ve tedavi programları altında bir önleme aracı 6, 7 gibi tedavi kullanımına yönelik kılavuzların evrimi tedavi bireylerin mutlak sayısı daha da artacak demektir. Çok sayıda insanın ART bireylerin ortalama yaşam beklentisi, HIV enfekte olmayan nüfusun 8 o yaklaştıkça daha uzun süre için ART olacak. HIV ilaç direnci gelişimi ve iletim alwa varYS ART 9-12 başarılarına bir tehdit olarak kabul edilmiştir. Bu nedenle, daha fazla birey SANAT üzerine başlatılmaktadır daha fazla sıkı gözetim ve ilaç direncinin görüntülenmesi için bir ihtiyaç vardır.
Genotipik ilaç direnci (GRT) test gözetim için hem de ART alan bireylerde HIV-1 ilaç direncinin izlenmesi, hem gelişmiş ülkelerde başarılı bir şekilde kullanılmaktadır. Bu ayarları, GRT HIV-1 enfekte bireyler için bakım sürekliliği entegre edilmiştir. Çoğu uluslararası kurallar yetişkin ya da ART (birinci basamak ve ikinci basamak) 13-15 başarısız pediatrik hastalar için GRT tavsiye, pediatrik anneden çocuğa bulaşmasının (PMTCT) rejimleri önlenmesi maruz kalan hastalar ancak daha sonra 16 enfekte ile ayarları akut olarak enfekte olmuş bireylerin 13-15 arasında iletilen ilaç direnci yüksek seviyeleri. Ancak, maliyet, teknoloji ve altyapı gereksinimleri implemen sınırlıHBS ilaç direnci izleme benzer yaklaşımların tation.
Güney Afrika HIV tedavisi ve izlenmesi kurallar halen birinci basamak 17 rejimleri başarısız bireyler için ART rehberlik seçiminde GRT kullanımını tavsiye etmiyoruz. Bireyler öncelikle virolojik (HIV-1 RNA viral yük) parametreleri esas açılır. Ancak 2012 yılında, Güney Afrika, HIV Klinisyenler Derneği ilk Güney Afrikalı ARV ilaç direnci test yönergeleri 18 yayınladı. Bu kurallar ilk satır ve ikinci satır ART başarısız tüm yetişkinler için ve PMTCT 18 maruz enfekte bebekler ve çocuklar için GRT testini öneririz. Güney Afrika 19-29 iletilen ilaç direnci yüksek düzeyde için hiçbir geçerli kanıt yoktur Ancak, GRT akut enfekte bireyler için 18 tavsiye edilmez. Bu önerilerin bazıları ulusal tre içine zamanla entegre olacağı bekleniyorBölgedeki çeşitli ülkelerin nuları ailenizle konuşmak ve izleme kuralları. Zaten, 2013 Güney Afrika tedavi kılavuzlarında yetişkinler için ikinci bir hat arızası sırasında ve çocuklar 30 için birinci veya ikinci basamak PI-temelli rejim başarısızlık zamanında GRT önerisi şimdi var.
Güney Afrika'da tedavi kılavuzlarının içine GRT birleştiren potansiyel olarak maliyet-nötr olacağı gösterilmiştir. Gerçekten ikinci basamak tedavisi için açık olması gereken hastaları belirlemek için GRT kullanarak, görece daha pahalı ilk basamak ilaçlar daha vardır ikinci çizgi rejimi ilaçların maliyeti göz önüne alındığında programı herhangi bir ek maliyet neden olmayacaktır. Buna ek olarak, GRT da, başarısızlığın diğer nedenleri belirlemek tedavi seçenekleri korumak ve ortaya çıkan direnç desenleri 31 hakkında bilgi üretebilir. Bu nedenle, daha da bağlantısı, bakım An kalitesini artırmak için ilaç direnci izleme yöntemlerinin maliyetini azaltmak için gerekli oland sonuçları.
Burada, ters transkripsiyon polimeraz zincir reaksiyonu (PCR) ve sıralama (Tablo 1), hem de ilaç direnci yorumlanması için çoğunlukla açık kaynak yazılımlar için genel (açık kaynak) primerler kullanmak üzere tasarlanmış bir GRT yöntem mevcut. Klinik yönetimi için, protokol, ulusal tedavi kılavuzlarının yakın bağlılık ile laboratuvar ilaç direnci raporun uzman yorumuyla kapsamlı bir inceleme ve raporlama yöntemiyle tarafından iltifat. Protokol, dört farklı bileşenler ayrılır: 1) HIV ribonükleik asit (RNA) ekstraksiyon, 2) Ters transkripsiyon ve Polimeraz Zincir Reaksiyonu (PCR) amplifikasyonu, viral hedefler, 3) Sıralama ve kromatogramlar, hizalama analizi için 4) Biyoinformatik yöntemleri, curation ve dizi verilerinin yorumlanması.
Protokol
1.. Etilendiamintetraasetik asit (EDTA) Tam Kan işleme
Not: Kan, hemen toplanması en fazla 24 saat boyunca 4 ° C'de saklanabilir sonra işlenebilir.
- Bir biyogüvenlik kabini içinde çalışan, EDTA tam kan örneği oda sıcaklığına gelmesini bekleyin.
- Her numune için, numune kimlik (İD), depolama malzemesi (plazma), tarih ve yeterli cryovials etiket.
- 1,000 x g de 10 dakika süre ile numuneler santrifüjleyin. Santrifüj durdurmak için fren kullanmayın. Trombositler de dahil olmak üzere ve eritrositler, - çok ince bir tabaka - plazma, lökosit (buffy coat) Bu üç tabaka (üstten alta doğru) verecektir.
- Dikkatle her cryovial içine süpernatant (plazma) ve kısım 500 ml aspire. Hücre tabakası (buffy coat) bozacak veya herhangi hücreleri aktarmak için değil dikkat edin.
- RNA çıkarılması için ihtiyaç duyulana kadar -80 ° C'de saklayın, ya da hemen RNA ekstre geçin.
- Pozitif ve negatif kontroller de dahil olmak üzere plazma ekstre edilecek numunelerin kimlikleri ile ekstre çalışma hazırlayın.
- Her numune ayıklanmasını, örnek kimliği, çıkarma tarih ve "RNA" ile, 1.5 ml steril mikrosantrifüj tüpü etiket. Ayrıca, monte edilmiş kolonu ve toplama tüpü hem de ekstre çizelgedeki karşılık gelen sayılar ile çalışan liziz çözeltisi içeren bir 2 ml mikrosantrifüj tüpü etiket.
- Bio-güvenlik kabininde çalışan çalışma lizis çözeltisinin karşılık gelen 2 ml mikrosantrifüj tüpüne 200 ul örnek ekleyin.
- Vortex de ve oda sıcaklığında 10 dakika boyunca inkübe edilir.
- 10 dakika sonra, kısa bir süre için santrifüj tüpü.
- Tüplerin her biri mutlak etanol içinde 800 ml ilave edilir.
- Nabız vorteks ve kısaca santrifüj ile karıştırın.
- Ilgili sütun / toplama tüp montajı için bu çözüm 600 ul aktarın. 6,000 x santrifüj1 dakika boyunca g.
- Yeni bir toplama tüpüne sütun aktarın ve süzüntü içeren eski toplama tüpü atın. Iki kez daha yukarıda adım 2.8 (yukarıda) tekrarlayın.
- 1 dakika boyunca 6.000 xg'de her sütun ve santrifüj 500 ul yıkama tamponu AW1 ekleyin.
- Süzüntü ve tahsilat tüp atılır ve yeni bir toplama tüpüne sütun aktarın.
- Ekle 500 ul 3 dakika 20.000 xg tampon AW2 ve santrifüj oldu. Adımı 2.11 tekrarlayın.
- Ek bir 2 dakika için 20,000 xg'de yeni bir toplama tüpü içinde santrifüjleyin.
- 1.5 ml mikrosantrifüj tüp içinde süzüntü ve yer sütun atın.
- Sütunun tarafında sıvı dağıtmak olmayan sağlanması kolonun orta 60 ul Tampon AVE (RNaz içermeyen su) eklenir.
- 1 dakika boyunca oda sıcaklığında inkübe edin.
- 2 dakika boyunca 6.000 x g'de santrifüj.
- Sütunu atın ve 1.5 ml mikrosantrifüj tüpleri kapak.
- Numuneler artık rever için hazırızse transkripsiyon.
- Test kadar 6 saat boyunca 4 ° C 'de, hemen mağaza gerçekleştirilebilir ise. Test gecikebilir Ancak, eğer hemen ardından -80 ° C yerleştirin. NB: donma yok / 3 katından daha fazla örnekleri çözülme.
3. Ters Transkripsiyon için reaktif hazırlanması
- Başlamadan önce, pozitif ve negatif kontroller plazma, aşağıdakileri içeren işlemden geçirilen numune sayısı için gerekli reaktiflerin her hacimlerini hesaplar. Ayrıca reaktif denetimi ekleyin.
- Adım 3.1 'den hesaplanan miktarlar kullanılarak (yukarıda), kısa bir süre için darbe sonra girdaplanır, temiz, steril 200 ul PCR tüpü içinde deoksiribonükleotit trifosfat (dNTP)-primer karışımı hazırlayın. Her numune, ters primer RT21, 0.5 ul ve dNTP 0.5 ul sahip bakınız Tablo 2 gerekir.
- 200 | il PCR tüplerine dNTP-primer karışımı 1.0 ul alikosu.
- 1 μ ekleyerek ters transkriptaz hazırlayın (RT) enzim karışımı, 10x, ters transkripsiyon tamponu, 0.1 M DTT ve 1 ul vorteks ve kısaca santrifüj, ardından steril bir tüpe 25 mM MgCI2 2 ul, Tablo 3'e bakınız.
- 0.5 ul RNAseOUT ve Superscript III enzim karışımı boruya ters transkriptazın enzimlerin her biri ekleme daha sonra karıştırmak için hafifçe tüp dokunun.
- Soğuk bir blok üzerinde dNTP-primer karışımları ve enzim karışımı ile tüpleri tutmak ve RNA istasyonuna taşımak.
4. Ters transkripsiyon
- Kısa bir süre karıştırmak vorteks ardından dNTP-primer karışımı tüpüne RNA numunesinin 6 ul ekleyin.
- RNA'nın ilave edildikten sonra, dNTP / astar / RNA ve RT enzim karışımı soğuk bir blok ya da buz üzerinde tüpler karışımı hem de PCR odasına hareket eder.
- Kısaca (aşama 4,2) dNTP / astar / RNA karışımı tüpler santrifüj ve thermocyclerda içine koyun.
- RNA denatüre etmek için 5 dakika boyunca 65 ° C'de ısıtın.
- 4 ° C'ye hızla serin, 2 tutunmin.
- 4 ° C iken hala termalcycler Pause, tüpleri almak.
- Soğuk bir blok üzerine tüpler tutarken hızlı enzim karışımına 5 ul ekle.
- Tüp dokunarak hafifçe karıştırın ardından kısa bir süre tüpler santrifüj ve termalcycler dönmek.
- Ters transkripsiyon durdurmak için 5 dakika boyunca 85 ° C 'de denatürasyon, ardından enzim RNA nın ters transkripsiyonunu yapmak için 60 dakika boyunca 50 ° C'de tüpler tutun.
- 37 ° C'ye soğutun En kısa sürede sıcaklığı 37 ° C olur, duraklama ve PCR dışında tüp almak.
- Hızlı bir şekilde tüplere RNAse H 0.5 ul ekleyin ve PCR geri dönün.
- 20 dakika ve 4 ° C'de, daha sonra soğuk boyunca 37 ° C'de tutun
- Tamamlayıcı DNA (cDNA), hemen kullanılabilir veya gerekli olana kadar -20 ° C veya altında saklanabilir. Bununla birlikte, cDNA, uzun süreli depolama -80 ° C olmalıdır
5. PCR için reaktif hazırlanması
- BefoBaşlangıç re, işlenen numuneler ve kontrol sayısı için gerekli reaktiflerin her hacimlerini hesaplar. Üç kontrollerin (Pozitif, negatif ve Reaktif) ek olarak, aynı zamanda bir PCR denetimi (HIV DNA) ekleyebilirsiniz. Birinci ve ikinci tur PCR karışımları aynı zamanda hazırlanabilir ve gerekli olana kadar ikinci ana karışım -20 ° C'de saklanır. Karışımları ve yaklaşık 8 saat boyunca saklanabilir.
- Tablo 4 ve girdap gösterildiği gibi 18.4 ul su, 2.5 ul 10x tampon, 1.0 ul MgCl2, 0.5 ul dNTPs ve primerlerin her biri 0.25 ul ekleyin.
- Platin Taq polimeraz (5U/μl) 0.1 ul ekleyin ve hafifçe dokunarak tüpü karıştırın.
- 200 ul PCR tüplerine ana karışımı aliquot 23 ul.
- Soğuk bir blok veya PCR odaya buz hareket master miks tüpleri ile.
6. İçiçe PCR
- 1. tur PCR ustalar 23 ul cDNA 2 ul ekleyinr karıştırın.
- , Tüpler kapatın PCR in örnekleri koymak ve aşağıdaki PCR çevrim koşulları kullanılmaktadır: 2 dk için 2 dakika 30 saniye için 95 ° C 30 döngü, 20 saniye boyunca 58 ° C ve 72 ° C 94 ° C, Şekil 1 'de gösterildiği gibi, 10 dakika boyunca 72 ° C'de son bir uzantısı takip etmektedir.
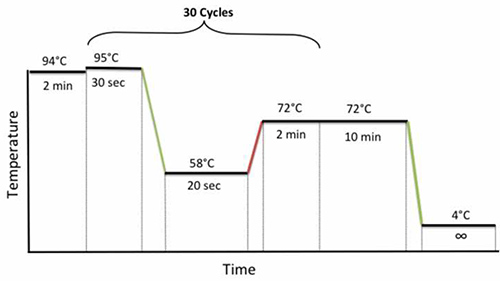
Şekil 1. İçiçe PCR döngü koşulları. resmi büyütmek için buraya tıklayın.
- 2. tur PCR aşamasında devam ya da daha sonraki bir aşamada gerekli kadar -20 ° C veya altında 1inci tur PCR ürünleri saklamak.
- 2. tur PCR için, 2. tur PCR master mix An 23 ul 1inci tur PCR ürünün 2 ul eklemekŞekil 1 aynı PCR programı kullanmak d.
7. Jel Elektroforez
- Jel hazırlanması
- 250 ml'lik bir cam şişeye agaroz tabletin bir 0.5 g eklenir ve şişeye 1x TBE tamponu, 50 ml.
- Kaynar mikrodalga ısı; tamamen erimiş kadar sık sık (yaklaşık her 30 saniye) girdap. Bir silikon kavrama veya silikon kullanın fırın sıcak şişeyi kavramak için eldiven. Agaroz çözüm bu süreci izlemek çok yakından çok kolay şişesinden kaynatın.
- Yaklaşık 10 dakika boyunca oda sıcaklığında soğutunuz.
- Uygun boyut tarağı içeren bir jel döküm tepsi içine agaroz dökün, jel yaklaşık 20-30 dk kullanıma hazırdır.
- Elektroforez odasında jel yerleştirin ve üretici tarafından tavsiye edildiği gibi çalıştırın.
- Jel elektroforez ve görselleştirme.
- 10 saniye için Vortex Roman Suyu kullanmadan önce.
- D 5 ul Roman Suyu 1 ul sulandırmakNA örnek ve karıştırın.
- Moleküler ağırlık belirteci 3 ul Roman Suyu 3 ul sulandırmak ve karıştırın.
- Bölme (yukarıda) 7.2.2 ve 7.2.3 gelen karışımları yükleyin ve PCR amplifikasyonu değerlendirmek için, 40 dakika için 100 V ve 400 mA'da jel üzerinde çalıştırıldı.
- Pozitif amplifikasyon 1315 bp fragmanının, Şekil 2 gibi, UV ışığı altında gözlemlenmiştir edilebilir.
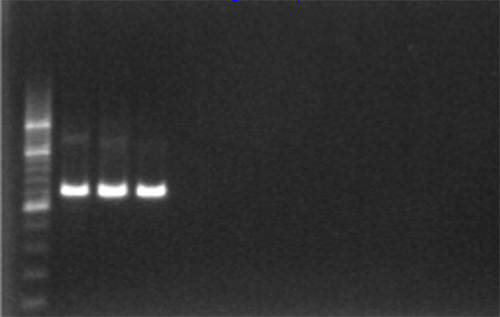
Şekil 2. % 1 agaroz jel elektroforezi ve 200 bp merdiven kullanılarak PCR amplifikasyonu jel onay. resmi büyütmek için buraya tıklayın.- Bu şekilde kirlenme olmadığını gösteren negatif ve belirteç kontrollerinde herhangi bir amplifikasyon olmalıdır.
8. PCR Product Temizleme
- Sıralama reaksiyonunun hazırlanmasında, pozitif ikinci tur PCR ürünleri PureLink PCR saflaştırma kiti kullanılarak temizlenir.
- PCR ürünü ve karışımı pipet ile 20 ul bağlama tamponu Yüksek Kesmesi (B3) çalışma 80 ul ekle.
- Bir toplama tüpü içinde bir döndürme kolonuna bağlanma tampon maddesi ile karıştırıldı örnek ekleyin.
- 1 dakika için 10,000 x g'de santrifüjleyin sütunu. Yeni bir toplama tüpüne sütunu aktarın.
- Etanol ile Yıkama Tamponu içinde 650 ul ile sütun yıkayın.
- 1 dakika için 10,000 x g'de santrifüjleyin sütunu. Yeni bir toplama tüpüne sütunu aktarın.
- Herhangi bir kalıntı yıkama tampon kaldırmak için 2-3 dakika boyunca maksimum hızda sütun santrifüj.
- Kit ile birlikte temiz bir 1.7 ml elüsyon tüpüne spin kolon yerleştirin.
- Sütunun merkezine elüsyon tamponu 40 ul ilave edin ve oda sıcaklığıdır de sütun inkübe1 dakika için e.
- 2 dakika (> 10.000 xg) için maksimum hızda sütun santrifüj.
- Elüsyon tüp dizileme için saflaştırılmış PCR ürünü hazır içerir. Sütunu atın.
- NanoDrop kullanılarak DNA konsantrasyonu ve kalitesi belirlenir.
- Hiçbir in-house dizme tesisleri varsa, saflaştırılmış PCR ürünleri bu aşamada ticari bir dizilim laboratuara gönderilebilir.
9. Dizileme reaksiyonları
- PCR ürünleri, büyük boya terminatörü kiti sürüm 3.1, ve her bir örnek için 4 primerleri (ileri ve iki iki ters) kullanılarak dizilir. Primer dizileri Tablo 2'de gösterilmiştir. Bu nedenle, sıralama çalıştırdıktan sonra, her bir numune bir kontige birleşmiş olmak dört sekansları olacaktır.
- Dört primerlerinin her biri için Tablo 5'de gösterildiği gibi sekanslama ayarlayın.
- Kullanmadan önce vorteks ile dizileme tampon ve primerler karıştırın.
- Mixbüyük boya sekanslama eklenmesinden önce, su, tampon ve primer. Vorteks ile karıştırın.
- Yavaşça tüp tersini veya hafifçe dokunarak büyük boya sıralama karışımını ekledikten sonra ana karışımı karıştırın.
- 96 oyuklu bir plaka içine optik ana karışımı kısım 9 ul.
- Şekil 3 aşağıda belirtildiği gibi plaka kurmak için 24 numune / plaka, çalıştırmak için.
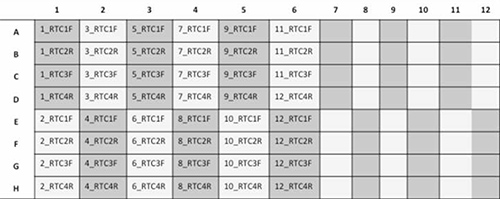
Şekil 3,. 12 hasta numuneleri 4 primerlerin her biri (RTC1F, RTC2R, RTC3F ve RTC4R) ile sıralı olması ile bir 96-plaka şeması gösterimi. resmi büyütmek için buraya tıklayın.
- DNA numunesi (~ 20-40 ng) 1.0 ul, bir ile plaka kapağın alüminyum kapak yapışkan ve yavaşça karıştırın.
- 1 dakika boyunca 3.000 x g'de santrifüj. Alüminyum kapağı çıkarın ve lastik sızdırmazlık mat ekleyin.
- PCR üzerine plakayı ve Şekil 4 'de gösterilen aşağıdaki döngü programı çalıştırmak.

Şekil 4. Sıralanması için PCR döngü koşulları. resmi büyütmek için buraya tıklayın.
- PCR tamamlandığında, hemen sıralama ürünü temizlemek.
10. Dizileme Temizleme
- Her dizileme reaksiyonu için, 50 ul mutlak etanol ve 5 ul 3 M sodyum asetat karıştırın.
- Bir çok kanallı pipet kullanarak, 55 eklemek ve# 956, her bir oyuğa, sodyum asetat / EtOH çözeltisi l.
- Her şey düzgün mühürlü sağlayarak, yapıştırıcı alüminyum kapağı ile kuyu Seal.
- 20 dakika boyunca 3.000 x g'de santrifüj.
- 20 dakika sonra kapağı çıkarın ve (bu pelet çıkarmak gibi süpernatant kurtulmak vurmayın!) Katlanmış bir laboratuvar doku üzerine, tek bir hareketle, plaka ters çevirin.
- 2 dakika boyunca 150 x g'de, aynı doku üzerinde baş aşağı plakaya santrifüjleyin.
- Hemen EtOH 150 ul soğuk% 70 ekleyin. Bu aşamada etanol ilave gecikme ETMEYİN.
- Aynı yapışkan alüminyum kapağı ve vorteks ile kapatılmalıdır.
- 5 dakika boyunca 3.000 x g'de santrifüj.
- 1 dakika boyunca 150 x g'de ters yeni katlanmış doku ve santrifüj üzerine Levha ters çevrilir.
- Santrifüj işleminden sonra, PCR ele koyun ve 2 dakika boyunca 50 ° C'de kurutun.
- Plakalar kuruduktan sonra, yapışkan folyo kapaklar ile mühür hazır wi devam etmek kadar -20 ˚ C'de folyo ve mağaza sarındizileme elektroforez inci.
- Sekansına hazır, 10 ml Hi-Di formamid temizlenmiş dizileme ürünleri çözülür zaman, denatüre ve elektroforez için yük.
11. Biyoinformatik
- Sıra Meclisi
- Program Geneious başlatın.
- Dizileri saklamak için çalışan bir klasör oluşturun.
- Ithalat aracını kullanarak çalışma klasörüne sıralama makine tarafından oluşturulan ABI dosyalarını içe. Geneious ithal her sekans için yüzde kalite puanı tahsis edecek.
- Üzerlerine çift tıklayarak kalite puanları>% 70 ile açık dizileri.
- Her dosya yeni bir pencerede açılacaktır. Yazılım, açık mavi çubuklar kullanarak sekans kalitesinin kromatogramın her bir nükleotid pozisyonundaki kalitesini gösterir. Bar yüksek, baz arama kalitesi daha iyi.
- İmleci kullanarak, kalitesiz genellikle uçlarını bırakarak sekansın orta bölümünü seçin.
- Kaliteli dizisi ile bölgeyi ayıklamak için extract düğmesine tıklayın.
- Her örnek için dört ekstre dizileri seçin ve bir referans dizisi karşı monte edin.
- Doğru okuma çerçevesi içinde olduğundan emin olmak için bir araya dizisini gözlemleyin. PQITLW: Doğru okuma çerçevesi içinde ise, Proteaz başlangıcı, aşağıdaki amino asitleri ile başlamalıdır. RT başlangıcı PISPIE ile başlayacak.
- 300. RT kodonuna PR başlangıcını kapsayan kontig bölgeyi ayıklayın. Bu işlem sırasında, ayrıca ekleme veya çıkarma ile kontrol edin.
- , Ekstre kontigin konsensüs dizisi boyunca bir git belirsizlikleri tanımlanması ve temel aramaların kalitesi (simetri, boy, arka plan ve kuşatıcı bölgelerin omuz) incelenmesi ile karışık bazlarla pozisyonlarını doğrulamak.
- Konsensüs dizisini seçip, dört primerleri konsensüs dizisinin ayrı bir dosya oluşturmak için ve labe ekstrakt düğmesiniBence bu uygun.
- Bilgisayar veya bir ağ klasörüne bir yedek depolama klasörüne diziyi aktarmak.
- Sıra Kalite Değerlendirmesi (HIVDB)
- De HIVDB programı kullanılarak analiz sekansı http://hivdb.stanford.edu .
- Özet veri silme ve eklemeler için kontrol edin ve sıra tüm 99 proteaz (PR) kodonlarını ve 1 300 RT kodonlarını kapsadığından emin.
- Böyle bir durdurma kodonu, çerçeve vardiya, belirsiz pozisyonları ve sıradışı artıkları hem PR ve RT bölgelerde, kalite güvence (QA) sorunları vurgulanan kontrol edin.
- Sıralama Kalite Kontrol
- Önceki dönemde yerel bir sekans veri tabanına karşı yeni dizisi vuruyoruz.
- Yeni dizi, veritabanındaki herhangi bir sekansına benzer bir>% 97 ise, protokol, tüm aşamaları dizi analizi ile başlayan ve geri ensur RNA ekstre edecek, gözden geçirilmelidire hiçbir karışıklık (örnek anahtarlama, mislabeling) veya kirlenme olduğunu.
- Herhangi bir sorun varsa tespit edilir, RNA ekstraksiyon aşamasından hem eski hem de yeni numunelerin analizi tekrarlayın.
- Dizileri hala>% 97 benzer ise, bireyler arasında herhangi bir epidemiyolojik bağlantı değerlendirmek için hastanın öyküsü gözden.
- Filogenetik Analizi
- Geneious içinde ClustalW programını kullanarak veritabanındaki tüm dizileri hizalayın.
- Elle hizadan dizileri, silme ve eklemeler için hizasını kontrol edin ve buna göre düzenleyin.
- Bir filogenetik PHYML kullanarak ağaç, ağaç Geneious inşaatçı ya Geneious diğer ağaç inşaatçılar Construct.
- Kısa dal uzunlukları ile örnekler için ağaç inceleyin.
- Olası kontaminasyon için kısa dal uzunlukları ile örnekleri inceleyin.
12. REGA DB Bilişim
- Sıra yükle
- RegaD giriş yapınBenzersiz bir kullanıcı adı ve şifreyi kullanarak B.
- Açılır menüden üzerine, Hasta kimliği altında, "ile başlar" seçeneğini seçin.
- Hasta kimliğini ekleyin ve kimin genotip yüklenecek olan kişiyi seçmek.
- Sol menüsünde "viral izolat" seçeneğini seçin.
- Viral izolata altında seçeneklerinden "add" seçeneğini seçin.
- Numune tarihi, Numune kimliği, Dizi kimliği ve Dizi tarihi girin.
- "Seçim dosyası" ve daha sonra yüklenecek dizisinin Fasta dosyasına gidin seçin.
- Yüklenmesine Fasta dosyayı seçtikten sonra, yükleme tıklayın.
- Yükledi dizisi dizisi belirler ve tarihlerin altında nükleotid kutusunda göründüğünde, pencerenin sağ alt kısmındaki ok düğmesini tıklatın.
- Düğmesine tıklayarak protein ve PR veya RT ya seçerek Halkla İlişkiler ve RT protein uyum için kontrol edin.
- Direnç butonuna tıklayarak ilaç direnci mutasyonu kontrol edin. Bu verirüç algoritmaları direnç profilleri: ANRS, Stanford HIVDB ve RegaDB.
- REGA kullanarak Rapor oluşturma
- Benzersiz kullanıcı adınızı ve şifrenizi kullanarak RegaDB oturum açın.
- Açılır menüden üzerine, Hasta kimliği altında, "ile başlar" seçeneğini seçin.
- Hasta kimliğini ekleyin ve kimin rapor oluşturulacak olan kişiyi seçmek.
- Sağa menüsünde, viral izolat seçin.
- Viral izolata altında seçeneklerinden "görünümünde" üzerine tıklayın.
- Eğer bir rapor oluşturmak istediğiniz viral izolat üzerine çift tıklayın.
- Viral izolat penceresinde, viral izolat rapor sekmesine tıklayın.
- Açılır menüden gelen genotip yorumlanması ve daha sonra kullanmak üzere seçin rapor şablonu için algoritmalar seçin.
- Algoritma ve şablonu seçildikten sonra, düğme "üretmek" üzerine tıklayın.
- Oluşturulan rtf belgesini indirin.
- Rtf yapmak açınBir word belgesi olarak dokümanla.
- Tedavi geçmiş grafiği yeniden boyutlandırma.
- Grafikte sonra, bölümü "Klinik grafik ve direnç yorumlama" ekleyin.
- Direnç masa ve klinik tablosunda verileri kullanarak, hastanın tedavi tarihi ile başlayan hastanın direnç profilinin bir açıklama eklemek, ve ilaçların hangi viral izolatın dirençli olduğunu. Ayrıca hastanın viral yük açıklamasını ve grafikten CD4 + hücre sayımı profilleri ekleyin.
- Bulaşıcı Hastalıklar inceleme için (ID) uzmanı ve gelecekteki hasta yönetimi önerileri raporu gönderin. Bu süreç aynı zamanda çok önemli bir kalite güvence aşamasıdır. Bir nihai rapor hastayı yönetmek klinisyen için tüm önerileri ile gönderilmeden önce tedavi öyküsü de genotip veya inconsistences herhangi bir hata, virolojik ve immünolojik profilleri tespit ve gözden geçirilebilir.
Sonuçlar
Doğrulanmış bir yöntem, daha önce bildirilen yöntem 20 bir modifikasyonu olmuştur. FDA tarafından onaylanmıştır Viroseq genotyping yöntemi, doğrulama referans yöntem olarak kullanılmıştır. AIDS Araştırma ve Viral Hepatit (ANRS) için Fransız Ulusal Ajanslar elde edilen yeterlilik test örneklerinin bir panel, iki yöntem arasındaki birincil karşılaştırma kullanılmıştır. Her iki yöntem başarılı bir şekilde genotipleme her iki yöntem ile amplifiye edilmiştir, numuneler için HIVDB program tarafından tüm klinik olarak önemli bir ilaç direnç-eşlikli mutasyonu tespit% 100 uyumlu idi. Tablo 6'da gösterildiği gibi, üç çift nükleotid dizileri% 99.5 özdeştir. Tahmin edilen amino asit sekansları,% 100 özdeştir. Beşte biri numune başarıyla Viroseq ile amplifiye edilememiştir. Viroseq ile amplifiye olmayan örneğe ek olarak, in-house yöntem gördü ikinci bir örnek amplifiye etmek için başarısızViroseq ile dolaşımlı rekombinant virüsü (CRF02_AG) için. Hem metodoloji ile güçlendirilmiş üç numune alt tip B (iki örnek) ve alt tip A (bir örnek) idi.

Şekil 5,. Dizisi kalite güvencesi parçası olarak yapılan bir HKY Komşu Katılma ağacın kullanımı. Çok kısa genetik mesafelerde dizisinin dört çift / kümeler vardır. RES655 ve RES655_1 arasındaki genetik mesafe (aynı numuneler farklı günlerde sıralı) 0.003 olduğunu. Genetik mesafe farklı epidemiyolojik bağlantısız bireylerden örnekler için (0.075) çok kısa olduğu gibi RES637_1/RES638 çifti ile potansiyel bir hatadır. RES638_1 kıyasla 0.075 bir mesafe ile ağacın başka RES637 vardır. CQ01/CQ02 küme önerdiği iki örnekpanelden aynı numunenin çoğaltır. Onlar REGA alt türlerinin aracı tarafından atanan alt türü teyit alt tip B referans dizisi ile birlikte küme. REGA subtiplemesi aracı sırasıyla A ve CRF02_AG olarak sınıflandırılmış ise CQ05 ve CQ04, sırasıyla alt tipler A ve G ile kümelenmiş. HIV alttiplendirmesinde ve rekombinasyon için başka bir araçtır http://www.datamonkey.org mevcuttur SCUEL vardır. resmi büyütmek için buraya tıklayın.
Beş numune bir panel içi yöntemin hassasiyetini değerlendirmek üzere kullanıldı. On adet aynı genotipi beş numunenin her biri için elde edilmiştir. 16 Kılcal 3130xl genetik analiz kullanılarak, 50 genotiplerinin 48, 24 çalışır üretilen ve aynı gün hazırlandı. Beş örnekleri için, tahmin edilen amino asit sekansları, tekrarlanmış arasında% 100 uyumlu idi. Nükleik asit sekansları, there>% 99 ikili benzerlik oldu.
Bu yöntemin kullanımının ilk iki yıl boyunca, altmış örnekleri dizilemesine RNA ekstre rasgele tekrarlandı. Dizisi kalite puanı ve tekrarlar arasındaki karışık üsleri sayısı arasında istatistiksel olarak anlamlı farklılık saptanmadı. Altmış çiftleri için nükleotid ve amino asit her ikisi de ikili karşılaştırmalar daha fazla% 99 aynıdır. Bu nedenle, tüm çiftleri için ilaç direnç mutasyonları% 100 uyumlu idi.
Maliyet azaltma
, Oda sıcaklığında, PCR ve dizileme için reaksiyon hacimleri üretilen dizilerin kalitesinden ödün vermeden, en az yarım, orijinal bir yöntem 20, 32 göre azaltılmıştır. Bu, RT ve PCR aşamaları için% 50 maliyetinde bir azalma sağladı.
Yeni yöntem, ilk dizisine altı dizileme primeri ile birlikte çalışmak için tasarlanmıştır proteaz geni ve ters transkriptaz geni 20, 32 ilk 300 kodonların 99 kodonları. Benzer yöntemler de altı ila sekiz primerler 33, 34 kullanır. Bazen seprately 35, 36, protaz ve RT genleri sequencing rağmen, son zamanlarda yayınlanan yöntemler, en az altı primerleri kullanılmıştır. Biz, 6-4 dizileme primerleri sayısını azaltmak için aranan, (Şekil 6)
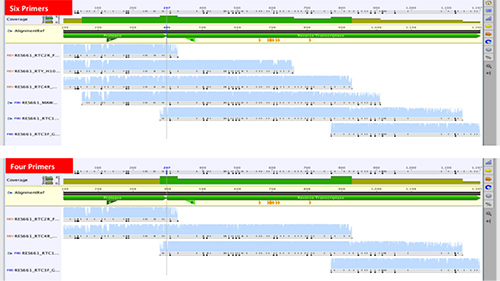
Şekil 6,. 99 HIV-1 proteaz kodonları ve ters transkriptaz geninin ilk 300 kodonları kapsayan 1197 bp pol dizisinin oluşturulması için altı dört vs dizileme primerleri Bitişik dizilerin karşılaştırılması.242/51242fig6highres.jpg "target =" _blank "> büyük resmi görebilmek için buraya tıklayın.
Altı primerlerinden meydana 17 numune, bir takım sekanslar, iki primer (MAW46 ve RTY) dışlanması sonra üretilen sekansları ile karşılaştırılmıştır. Alt tipler dizisi kalitesi skorlarında anlamlı farklılık saptanmadı 14 alt C, iki alt tip B, ve bir alt A. idi. Yine, nükleik asidin 17 çiftleri arasındaki ortalama ikili kimlik amino asit seviyesi üzerinde% 99 ve% 100 idi. Bu nedenle, 6-4 dizileme primerleri indirgeme neredeyse üçte bir oranında sıralama maliyetinde bir azalma ile sonuçlandı.
Bu protokolde kullanılan tek tescilli yazılım aracı dizisi montaj için Geneious oldu. Ilaç direnci yorumlama araçları, yanı sıra rapor araçları üreten tüm özgür, açık erişim araçları vardır. Bu özel yazılım kullanımı ile ilgili masrafları ortadan kaldırarak, daha fazla maliyetini düşürür. Bundan başka, collectivE müzakere bu protokol için reaktifler Life Technologies kolay erişim için bir kit içine paketlenmiş ve Satürn / Life Technologies yöntemi 37 genotiplenmesi olarak kullanılabilir izin. Ayrıca, Satürn üyeleri indirimli fiyata reaktifler erişebilirsiniz.
Klinik Ayarı
Açıklanan protokol KwaZulu-Natal kırsal toplumda izlenmesi ve ilaç direnci gözetimi uygulamaya konmuştur. 604 genotiplerinin toplam> 1000 RNA kopya / ml viral yükleri olan numuneler için,% 95 oranında bir amplifikasyon Aralık 2010 ve Mayıs 2013 arasında klinik örneklerden elde edildi. Bu klinik HIV ilaç direnci çalışma KwaZulu-Natal Üniversitesi (bkz. BF052/10) Biyomedikal Araştırma Etik Kurulu ve Sağlık KwaZulu-Natal Bölümü (bkz. HRKM 176/10) ve Sağlık Araştırma Komitesi tarafından onaylandı. Bireysel hasta raporları oluşturulmuş ve kliniklere geri gönderildihasta yönetimi için.
Yetmiş iki (72) genotipleri de, iletilen ilaç direnci çalışmanın bir gözetim parçası olarak oluşturulan bir büyük prospektif popülasyon tabanlı HIV sürveyans çalışma içinde yuvalanmış. Birincil numuneler EDTA mikrotüplerde toplanan iğne prick tam kan vardı. Genotiplemesi de 79% 19 oranında bir büyütme oranı vardı. Sürveyans çalışma örneklerinin genotip için etik onay KwaZulu-Natal Biyomedikal Araştırma Etik Komitesi Üniversitesi (bkz. BE066107) elde edilmiştir.
| Primer adı | Sekans | Uzunluk | Yön | HXB2 Pozisyon | |
| MAW-26 | TTGGAAATGTGGAAA GGAAGGAC | 23 | Ileri | 2028-2050 | 1. tur PCR |
| RT-21 | CTGTATTTCAGCTATC AAGTCCTTTGATGGG | 31 | Ters | 3539-3509 | 1. tur PCR |
| Pro-1 | TAGAGCCAACAGCCC CACCA | 20 | Ileri | 2147-2166 | 2. tur PCR |
| RT-20 | CTGCCAATTCTAATTC TGCTTC | 22 | Ters | 3462-3441 | 2. tur PCR |
| RTC1F | ACCTACACCTGTCAA CATAATTG | 23 | Ileri | 2486-2508 | Dizileme |
| RTC2R | TGTCAATGGCCATTG TTTAACCTTTGG | 27 | Ters | 2630-2604 | Dizileme |
| RTC3F | CACCAGGGATTAGAT ATCAATATAATGTGC | 30 | Ileri | 2956-2994 | Dizileme |
| RTC4R | CTAAATCAGATCCTAC ATACAAGTCATCC | 29 | Ters | 3129-3101 | Dizileme |
| RT-y | GTGTCTCATTGTTTAT ACTAGG | 22 | Ters | 2967-2946 | Dizileme |
| MAW-46 | TCCCTCAGATCACTC TTTGGCAACGAC | 27 | Ileri | 2251-2277 | Dizileme |
Tablo 1. Transkripsiyon, PCR ve tüm 99 HIV-1 Proteaz kodonları ve ters transkriptaz geninin ilk 300 kodonları kapsayan bir 1197 bp pol fragmanının üretiminde kullanılan özel sıralama primerleri ters.
| RT21 (5pmol/ml) | 0.5 | 0.2 |
| dNTP (10 mM) | 0.5 | 0.4 |
| Toplam | 1 |
Tablo 2. dNTP / Primer ters transkripsiyon reaksiyonu için karıştırın.
| Reaktif | Hacmi (mi) / reaksiyon | Konsantrasyon / reaksiyon |
| First Strand Tamponu (10x) | 1 | 1 |
| MgCl2 (25 mM) | 2 | 4 |
| DTT (0.1 M) | 1 | 0.008 |
| RNaseOUT (40 U / ml) | 0.5 | 16 |
| Üst Simge III Ters Transcriptase (200U/ml) | 0.5 | 8 |
| Toplam | 5 |
Tablo 3. Enzim ters transkripsiyon reaksiyonu için karıştırın.
| Reaktif | Hacmi (mi) / reaksiyon | Final Konsantrasyon / Reaksiyon |
| DEPC su tedavi | 18.4 | - |
| PCR Tamponu (10x) | 2.5 | 1 |
| 2, ki burada (50 mM) | 1 | 2 |
| dNTP karışımı (10 mM) | 0.5 | 0.2 |
| Ters primer (5 pmol / ml) | 0.25 | 0.05 |
| Ters primer (5 pmol / ml) | 0.25 | 0.05 |
| Platinum Taq Polimeraz (5 U / ml) | 0.1 | 0.02 |
| Ara toplam | 23 | - |
Tablo 4. Iç içe PCR Master mix.
| Reaktif | Hacmi (mi) / reaksiyon | Konsantrasyon / reaksiyon |
| DEPC su tedavi | 6.1 | |
| Dizi Tamponu (5x) | 2 | 1 |
| Primer (3.2 pmol / ml) | 0.5 | 0.16 |
| Big Dye Terminatör Sekanslama karışımı | 0.4 | - |
| Toplam | 9 |
Tablo 5. Dizileme reaksiyonlarının Master karışımı.
| Viroseq | Içi | % NA Benzerlik | |||||||
| Örnek kimlik | Tipi | Kalite puanı | PR Mutasyonlar | RT mutasyonlar | Tipi | Kalite puanı | PR mutasyonlar | RT Mutasyonlar | |
| CQ01 | B | 99.9 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | B | 99.2 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | 100 |
| CQ02 | B | 99.5 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | B | 99.5 | M46L, I54L, V82A, L90M | D67N, T69D, K70R, M184V, T215V, K219Q | 100 |
| CQ03 | NA | NA | NA | NA | NA | NA | |||
| CQ04 | CRF02_AG | 98.4 | I54V, V82F, I84V | M41L, L74I, L210W, T215Y, V108I, Y181C | NA | NA | NA | NA | NA |
| CQ05 | A | 99.7 | K103N | A | 93 | K103N | 100 | ||
Tablo 6. Karşılaştırmalı resulViroseq genotiplendirme yöntem ve ANRS tarafından sağlanan örneklerin bir panel kullanılarak in-house metodu arasında paralel analizi ts.
Tartışmalar
Birçok düşük maliyetli içi yöntemler 33, 34, 36 HIV ilaç direnci genotiplendirme daha uygun hale getirmek için denemek için çabalarında tarif edilmiştir. Kaynak sınırlı ayarları antiretroviral tedavinin bireyler için bakım süreklilik haline ilaç direnci test entegre etmek gerek hiç şüphe yoktur. Ancak, bildirilen yöntemler çoğu toplum düzeyinde ilaç direncinin gözetiminde ilaç direnci genotiplemede uygulama odaklanmak. Satürn / Life Technologies genotiplendirme yöntemi gözetim ve ilaç direncinin izlenmesi için tam entegre bir protokoldür. Bu yöntem, klinik yönetimi için raporlar ilaç direnci ve neslin yorumlanması için çoğunlukla açık kaynak ve açık erişim biyoinformatik kaynaklarını uygulanması uygun bir protokol olarak tasarlanmıştır.
Bu olmak için FDA onaylı Viroseq genotipleme yöntemi ile karşılaştırılarak gösterildibaşarılı bir şekilde çoğaltıldı laboratuvar Paneldeki çoğaltılan kütüphane numunelerinin% 100 ANRS test örneklerinin bir panel, ikinci ilaç direnci başkalaşımların teşhis doğru. Doğruluğu da alt C virüsleri, Güney Afrika'nın en baskın alt tipinin klinik örneklerinde değerlendirildi. Yöntem CRF02_AG yaygın olduğu dünyanın diğer bölgelerinde kullanılacak ise yöntem Ancak alt tip A ve B ile ilgili olarak alt C numuneleri üzerinde kadar doğru olduğu, yöntemi bu yana primerlerin modifikasyonu için bir ihtiyaç vardır CRF02_AG sahip olduğu gösterilmiş olan panel örneklerinden biri yükseltmek için başarısız oldu. Alt dağıtım 38 daha heterojen olduğu Alternatif M 33 virüs tüm grup duyarlı primerler bir dejenere dizi, 36 bölgelerde kullanılabilir.
Ters transkripsiyon ve PCR duyarlılığı, örneğin 500 ml olarak plazma daha yüksek miktarlar, RNA ekstre artırılabilir. Plazma Santrifüj edilebilirQIAamp viral RNA ekstraksiyonu, mini kiti ile tarif edildiği gibi protokol ile devam etmeden önce, viral parçacıklar konsantre 90 dakika boyunca 21,000 xg'de uged.
Gösterildiği gibi, yeni yöntem, bireysel hasta yönetimi için kapsamlı raporları üretir ek bir avantaja sahiptir. Bu raporlar RegaDB gelen genotip bir konsolidasyon, immünolojik ve virolojik izleme verilerinin yanı sıra, klinik ve tedavi öyküsü vardır. Bu aynı derecede ayrıntılı bir hastanın klinik geçmişi gözden yanı sıra tedavi önerileri takip direnç profilinin ayrıntılı laboratuar yorumuyla eşlik ediyor. Raporlarını incelemek ve hastalar için tedavi önerileri sağlamak için bir uzman hekimlerin kullanımı, hemşire gibi giderek değişen görev için DSÖ önerileri parçası olarak Güney Afrika'da ART sağlayan deneyimsiz klinisyenler için çok ihtiyaç duyulan mentorluk sağlar. Bu klinikraporlar ilaç direnci yönetiminde az veya hiç deneyimi olan klinisyenler için etkili öğretim yardımcıları olduğu gösterilmiştir. Hasta açısından bakıldığında, bizim yöntemimiz uzman HIV hizmetlerine erişmek için merkezi sitelere seyahat ihtiyacını azaltır.
Böylece, bir bütün olarak ele alındığında açıklanan protokol HIV ilaç direnci yönetimi HIV ile enfekte kişilerde başarısız ART için bakım süreklilik haline, uygun bir maliyetle entegre edilebildiği iyi bir platform sağlar. Üretilen veriler eden ilaç direnci gelişimi ve iletim değerlendirmek için epidemiyolojik amaçlar için kullanılabilir. Oluşturulan pol fragmanın büyüklüğü nüfus düzeyinde salgın daha iyi anlaşılmasını üretecek daha karmaşık filogenetik analiz için yeterince iyidir.
Açıklamalar
Sağlık Sistemleri Güçlendirilmesi ve HIV Tedavi Başarısızlığı (HIV-: Bu çalışma Wellcome Trust (082384/Z/07/Z), Avrupa Birliği (SANTE 2007 147-790), Hastalıkları ABD Merkezi tarafından desteklenmiştir CAPRISA (proje başlığı aracılığıyla kontrol TFC)), ve İsviçre Güney Afrika Ortak Araştırma Programı (SSJRP) başlıklı araştırma bursu "Swiss Prot / Güney Afrika: Protein Biyoinformatik Kaynak Geliştirme Önemlidir Sağlıkla ilgili Patojenler için". RL Wellcome Trust tarafından desteklenen (hibe sayısı 090.999 / Z / 09 / Z). Maliyeciler, çalışma tasarımı, veri toplama ve analizi, yayınlamak kararı, ya da yazının hazırlanmasında hiçbir rolü vardı. Yazarlar herhangi bir mali çıkarlarını beyan.
Teşekkürler
Yazarlar bu işi mümkün yapılan tüm meslektaşlarını, özellikle Maya Balamane, Elizabeth Johnston Beyaz, Sharon Sjoblom, Greg Ording Zakhona Gumede, Xolile Kineri, Phindile Mabaso, Lungisa Ndwandwe, James Garvey, Gavin Cobb, Senzo Maphanga, Terusha Chetty kabul etmek istiyorum , Kevi Naidoo, Andrew Skingsley, Katharine Stott ve Lungani Ndwandwe. Yazarlar ayrıca, Sağlık Bakanlığı ve Hlabisa HIV Tedavi ve Bakım Programı çalışmak Afrika Merkezi personelin tüm personele teşekkür etmek istiyorum.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Superscript III 1st strand Synthesis kit | Life Technologies | 18080051 | Reverse Transcription |
| SATURN/LiFE Technologies Custom Primers | Life Technologies | 4473517 | PCR |
| Platinum Taq | Life Technologies | 10966026 | PCR |
| PureLink QUICK PCR Purification Kit | Life Technologies | K310002 | PCR |
| Viroseq | ABBOTT | 4J94-20 | Reverse Transcription and PCR |
| Agarose Tablets (Dnase/Rnase free) | BIOLINE | BIO-41027 | PCR |
| TBE Buffer | MERCK | 1.06177.2500 | PCR |
| O'Range Ruler 200 bp DNA Ladder | Fermentas | FE SM0633 | PCR |
| Novel Juice | GeneDireX | LD001-1000 | PCR |
| MiniBis Bioimaging System | DNR Bioimaging Systems Ltd | Gel Documentation | |
| Power Pac 300 | BIORAD | Gel Electrophoresis | |
| Big Dye Terminator Kit version 3.1 | Life Technologies | 4337456 | Sequencing |
| Arrays | Life Technolgies | 4319899 | Sequencing |
| PoP | Life Technologies | 4363785 | Sequencing |
| 10x EDTA Buffer | Life Technologies | 402824 | Sequencing |
| Formamide | Life Technologies | 4311320 | Sequencing |
| 5x Sequencing Buffer | Life Tecgnologies | 4336697 | Sequencing |
| 3130 xl Genetic Analyzer | Life Technologies | Sequencing | |
| GeneAmp PCR System 9700 | Life Technologies | RT/PCR/Sequencing | |
| Centrifuge 5804 | EPPENDORF | Sample Processing | |
| Centrifuge 5415R | EPPENDORF | RNA Extraction | |
| Centrifuge 5415R | EPPENDORF | RT and PCR | |
| Centrifuge 5415D | EPPENDORF | PCR Product Clean up | |
| Centrifuge 5810 | EPPENDORF | Sequencing Clean up | |
| Picofuge | BIORAD | C1301-230V | RT and PCR |
| Vortex Genius 3 | IKA | RNA extraction and reagent preparation | |
| Vortex mixer | IKA | Sequencing Cleanup | |
| NanoDrop 2000 UV/VIS spectrophotometer | ThermoScientific | DNA quantification | |
| 3 M Sodium Acetate | MERCK | 567422 | Sequencing Clean up |
| Absolute Ethanol | MERCK | SAAR2233540LP | Sequencing Cleanup |
| 1.5 ml SARSTEDT Tubes | BIODEX | 72.692.005 | RNA Extraction |
| 2 ml SARSTEDT Tubes | BIODEX | 72.693.005 | RNA Extraction |
| 2 ml Collection tubes | SCIENTIFIC GROUP | MCT-200-NC/S | RNA Extraction |
| Optical MicroAmp 96-well reaction plates | Life Technologies | N8010560 | Sequencing |
| 200 µl 8 Strip StarPCR Tubes with attached flat caps | STAR Lab - supplied by CELTIC | A1402-3700 | RT and PCR |
| 200 µl PCR individual tubes | Scientific Group | CR/3745 | RT and PCR |
| Geneious | Biomatters | Sequence analysis | |
| Internet Access | Preferrably high speed | ||
| Web resources | |||
| hivdb.stanford.edu | Stanford University | Drug reistance analysis | |
| http://bioafrica.mrc.ac.za:8080/regadb-ui/RegaDB | SATuRN | database | |
| http://bioafrica.mrc.ac.za/tools/pppweb.html | SATuRN | Sequence quality tool | |
Referanslar
- Shao, Y., Williamson, C. The HIV-1 epidemic: low- to middle-income countries. Cold Spring Harbor Persp. Med. 2, (2012).
- Mutevedzi, P. C., et al. Scale-up of a decentralized HIV treatment programme in rural KwaZulu-Natal, South Africa: does rapid expansion affect patient outcomes. Bull. World Health Organ. 88, 593-600 (2010).
- Houlihan, C. F., et al. Cohort profile: Hlabisa HIV treatment and care programme. Int. J. Epidemiol. 40, 318-326 (2011).
- Tanser, F., Barnighausen, T., Grapsa, E., Zaidi, J., Newell, M. L. High coverage of ART associated with decline in risk of HIV acquisition in rural KwaZulu-Natal. South Africa. Science. 339, 966-971 (2013).
- Bor, J., Herbst, A. J., Newell, M. L., Barnighausen, T. Increases in adult life expectancy in rural South Africa: valuing the scale-up of HIV treatment. Science. 339, 961-965 (2013).
- Montaner, J. S., et al. The case for expanding access to highly active antiretroviral therapy to curb the growth of the HIV epidemic. Lancet. 368, 531-536 (2006).
- Granich, R. M., Gilks, C. F., Dye, C., De Cock, K. M., Williams, B. G. Universal voluntary HIV testing with immediate antiretroviral therapy as a strategy for elimination of HIV transmission: a mathematical model. Lancet. 373, 48-57 (2009).
- Johnson, L. F., et al. Life expectancies of South african adults starting antiretroviral treatment: collaborative analysis of cohort studies. PLoS Med. 10, (2013).
- Blower, S., Ma, L., Farmer, P., Koenig, S. Predicting the impact of antiretrovirals in resource-poor settings: preventing HIV infections whilst controlling drug resistance. Curr. Drug Targets. 3, 345-353 (2003).
- Geretti, A. M. Epidemiology of antiretroviral drug resistance in drug-naive persons. Curr. Opin. Infect. Dis. 20, 22-32 (2007).
- Larder, B. A., Darby, G., Richman, D. D. HIV with reduced sensitivity to zidovudine (AZT) isolated during prolonged therapy. Science. 243, 1731-1734 (1989).
- Erice, A., et al. Brief report: primary infection with zidovudine-resistant human immunodeficiency virus type 1. N. Engl. J. Med. 328, 1163-1165 (1993).
- Williams, I., et al. British HIV Association guidelines for the treatment of HIV-1-positive adults with antiretroviral therapy. HIV Med. 13 Suppl 2, 1-85 (2012).
- DHHS, . US Panel on Antiretroviral Guidelines for Adults and Adolescents. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. , (2012).
- Vandamme, A. M., et al. European recommendations for the clinical use of HIV drug resistance testing: 2011 update. AIDS Rev. 13, 77-108 (2011).
- DHHS, . US Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children. Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection. , (2012).
- . Department of Health. Clinical guidelines for the management of HIV & AIDS in adults and adolescents. , (2010).
- Conradie, F., et al. The 2012 southern African ARV drug resistance testing guidelines. S. Afr. J.HIV Med. 13, 162-167 (2012).
- Manasa, J., et al. Primary Drug Resistance in South Africa: Data from 10 Years of Surveys. AIDS Res. Hum. Retroviruses. 28, 558-565 (2012).
- Tshabalala, M., et al. Surveillance of transmitted antiretroviral drug resistance among HIV-1 infected women attending antenatal clinics in Chitungwiza, Zimbabwe. PLoS ONE. 6, (2011).
- Bartolo, I., et al. Antiretroviral drug resistance surveillance among treatment-naive human immunodeficiency virus type 1-infected individuals in Angola: evidence for low level of transmitted drug resistance. Antimicrob. Agents Chemother. 53, 3156-3158 (2009).
- Bartolo, I., et al. HIV-1 genetic diversity and transmitted drug resistance in health care settings in Maputo, Mozambique. J. Acquir. Immune Defic. Syndr. 51, 323-331 (2009).
- Hamers, R. L., et al. HIV-1 drug resistance in antiretroviral-naive individuals in sub-Saharan Africa after rollout of antiretroviral therapy: a multicentre observational study. Lancet Infect. Dis. 11, 750-759 (2011).
- Hamers, R. L., et al. HIV-1 Drug Resistance Mutations Are Present in Six Percent of Persons Initiating Antiretroviral Therapy in Lusaka, Zambia. J. Acquir. Immune Defic. Syndr. , (2010).
- Nwobegahay, J., Selabe, G., Ndjeka, N. O., Manhaeve, C., Bessong, P. O. Low prevalence of transmitted genetic drug resistance in a cohort of HIV infected naive patients entering antiretroviral treatment programs at two sites in northern South Africa. J. Med. Virol. 84, 1839-1843 (2012).
- Iweriebor, B. C., et al. Molecular epidemiology of HIV in two highly endemic areas of northeastern South Africa. Arch. Virol. 157, 455-465 (2012).
- Parboosing, R., Naidoo, A., Gordon, M., Taylor, M., Vella, V. Resistance to antiretroviral drugs in newly diagnosed, young treatment-naive HIV-positive pregnant women in the province of KwaZulu-Natal South Africa. J. Med. Virol. 83, 1508-1513 (2011).
- Nwobegahay, J. M., et al. Prevalence of antiretroviral drug resistance mutations and HIV-I subtypes among newly-diagnosed drug-naive persons visiting a voluntary testing and counselling centre in northeastern South Africa. J. Health Popul. Nutr. 29, 303-309 (2011).
- Nwobegahay, J., et al. Prevalence of drug-resistant mutations in newly diagnosed drug-naive HIV-1-infected individuals in a treatment site in the waterberg district, limpopo province). S. Afr. Med. J. 101 (2011), 335-337 (2011).
- Rosen, S., Long, L., Sanne, I., Stevens, W. S., Fox, M. P. The net cost of incorporating resistance testing into HIV/AIDS treatment in South Africa: a Markov model with primary data. J. Int. AIDS Soc. 14, 24 (2011).
- Dalai, S. C., et al. Evolution and molecular epidemiology of subtype C HIV-1 in Zimbabwe. AIDS. 23, 2523-2532 (2009).
- Chen, J. H., et al. In-house human immunodeficiency virus-1 genotype resistance testing to determine highly active antiretroviral therapy resistance mutations in Hong Kong. Hong Kong Med. 18, 20-24 (2012).
- Lee, C. K., et al. An in-house HIV genotyping assay for the detection of drug resistance mutations in Southeast Asian patients infected with HIV-1. J. Med. Virol. 84, 394-401 (2012).
- Aitken, S. C., et al. A Pragmatic Approach to HIV-1 Drug Resistance Determination in Resource-Limited Settings by Use of a Novel Genotyping Assay Targeting the Reverse Transcriptase-Encoding Region Only. J. Clin. Microbiol. 51, 1757-1761 (2013).
- Zhou, Z., et al. Optimization of a low cost and broadly sensitive genotyping assay for HIV-1 drug resistance surveillance and monitoring in resource-limited settings. PLoS One. 6, (2011).
- , Life Technologies. Life Technologies and SATuRN Collaborate to Increase Access to HIV Testing in Africa. , (2012).
- Lihana, R. W., Ssemwanga, D., Abimiku, A., Ndembi, N. Update on HIV-1 diversity in Africa: a decade in review. AIDS Rev. 14, 83-100 (2012).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır