Method Article
Экологически-контролируемое Microtensile Тестирование Механически адаптивных полимерных нанокомпозитов для
В этой статье
Резюме
Метод обсуждается в котором В естественных условиях Механические свойства раздражителей аспекты материалов как функцию времени. Образцы испытывают Экс естественных условиях Использование microtensile тестер с экологическим контролем для имитации физиологической среде. Эта работа способствует дальнейшему пониманию В естественных условиях Поведение нашем материале.
Аннотация
Implantable microdevices are gaining significant attention for several biomedical applications1-4. Such devices have been made from a range of materials, each offering its own advantages and shortcomings5,6. Most prominently, due to the microscale device dimensions, a high modulus is required to facilitate implantation into living tissue. Conversely, the stiffness of the device should match the surrounding tissue to minimize induced local strain7-9. Therefore, we recently developed a new class of bio-inspired materials to meet these requirements by responding to environmental stimuli with a change in mechanical properties10-14. Specifically, our poly(vinyl acetate)-based nanocomposite (PVAc-NC) displays a reduction in stiffness when exposed to water and elevated temperatures (e.g. body temperature). Unfortunately, few methods exist to quantify the stiffness of materials in vivo15, and mechanical testing outside of the physiological environment often requires large samples inappropriate for implantation. Further, stimuli-responsive materials may quickly recover their initial stiffness after explantation. Therefore, we have developed a method by which the mechanical properties of implanted microsamples can be measured ex vivo, with simulated physiological conditions maintained using moisture and temperature control13,16,17.
To this end, a custom microtensile tester was designed to accommodate microscale samples13,17 with widely-varying Young's moduli (range of 10 MPa to 5 GPa). As our interests are in the application of PVAc-NC as a biologically-adaptable neural probe substrate, a tool capable of mechanical characterization of samples at the microscale was necessary. This tool was adapted to provide humidity and temperature control, which minimized sample drying and cooling17. As a result, the mechanical characteristics of the explanted sample closely reflect those of the sample just prior to explantation.
The overall goal of this method is to quantitatively assess the in vivo mechanical properties, specifically the Young's modulus, of stimuli-responsive, mechanically-adaptive polymer-based materials. This is accomplished by first establishing the environmental conditions that will minimize a change in sample mechanical properties after explantation without contributing to a reduction in stiffness independent of that resulting from implantation. Samples are then prepared for implantation, handling, and testing (Figure 1A). Each sample is implanted into the cerebral cortex of rats, which is represented here as an explanted rat brain, for a specified duration (Figure 1B). At this point, the sample is explanted and immediately loaded into the microtensile tester, and then subjected to tensile testing (Figure 1C). Subsequent data analysis provides insight into the mechanical behavior of these innovative materials in the environment of the cerebral cortex.
протокол
1. Подготовка образцов
- Подготовьте ПВА-NC пленки толщиной в диапазоне 25-100 мкм, с использованием литья решения и технологии сжатия 10-12.
- Придерживаться пленки на кремниевой пластине при нагревании на горячей плите в течение двух минут при 70 ° С (выше температуры стеклования) содействовать тесный контакт между пленкой и подложкой. Этот шаг гарантирует, что полученные пленка остается плоским и фиксированных на кремниевой пластины, которая необходима для плоских процессов микрообработки.
- Pattern пленку в тестируемом образце геометрии лазерного микрообработке (VLS 3.50, VersaLASER). Установите CO 2 прямой записи параметров лазерного микрообработке до 1,0% мощность (0,5 Вт), 4,0% скорости (56 мм / с), и 1000 импульсов на дюйм 13,16.
- Образец образцы, которые будут использоваться для установления условий окружающей среды ("Установка образцов") в форме собачьей кости структуры с поперечными размерами площадки 1,5 х 1,5 мм 2, и боковой балкой тусклыйensions 300 х 3000 мкм 2, с толщиной соответствия, что пленки по всему (рис. 2).
- Образец образцов напр экспериментов естественных условиях («имплантат образец") в пучках 300 мкм и длиной 6 мм, с толщиной, соответствующих этому пленки.
- Осторожно освободить образцов из пластин с помощью лезвия бритвы и пинцет.
- Для обработки проб, подготовить специально обработанной Акриловые держатели, предназначенные для обслуживания, как часть рукоятки системы в microtensile тестера. Лазером маркировки показать осевой держатель и 1,5 мм от конца. Нанесите небольшое количество геля цианоакрилат клей на основе по осевой линии акриловый держатель и тщательно придерживаться 1,5 мм длины имплантата образца в держателе и перекрывают отмечены линии (фиг.3). Каждый имплантат выборка требует одного акрилового держателя. Быть осторожным, чтобы гарантировать, что клейкий гель остается только вдоль 1,5 мм длины ПВА-NC соблюдались акрилова держателя. В противном случае клей гель может повлиять на механические свойства образца.
- Удалить влагу из всех образцов, помещая их в эксикаторе в течение по крайней мере 24 часов.
- Измерение длины, ширины и толщины размеры образцов с помощью оптического микроскопа.
2. Установить условия окружающей среды
- Загрузите сухой установки образца в microtensile тестера (см. рисунок 4), первый зажим между мобильным захваты, затем между фиксированными захватами.
- Установить воздух щетка с заполненными водой резервуара в фиксированном положении, при этом сопло направлено на microtensile образца. Подключите аэрографа к воздушному компрессору с помощью пластиковых труб. С соплом аэрографа полностью закрыта, включите компрессор воздуха.
- Начать циклическую процедуру тестирования microtensile, чередуя деформацию растяжения (положительные деформации) и деформации сжатия (отрицательный штамм) применяется к TОн образца, оставаясь в пределах линейной упругой области напряженно-деформированного участка. Для ПВА-NC, приложенной деформации ограничено до менее чем 2%. В пользовательском тестер microtensile используемые в этих экспериментах, скорость деформации контролировали в то время как необходимое усилие для достижения этого штамма измерялась. Кроме того, различные настройки может включать в себя управление приложенной силы при измерении Полученный штамм.
- Постепенно увеличение потока из сопла щетка воздуха и контролировать наклон напряжение-деформация участка в зависимости от величины потока от щетки воздуха. Максимальный поток, который не вызывает значительного (> 10%), снижение модуля Юнга в течение 60 сек это уровень, который будет использоваться для экс виво экспериментов. На данный момент, влажности, которая не будет смачивать сухой образец (и тем самым способствовать снижению модуля Юнга), а также сведет к минимуму сушки образца после воздействия биологических жидкостей в естественных условиях были ЭСТАblished.
- Измерить температуру вблизи образца. Идеальная установка будет включать в себя термопары с цифровым отсчетом, и выполняться во время аэрограф работает. Установить интенсивность и расстояние до источника лучистой тепла, например, что температура держится до 37 ° С, в соответствии с физиологическими условиями.
3. Сравните экологический контроль с целью Номера для экологического контроля
- Погрузить образцы установки, по крайней мере 30 минут в фосфатном буферном растворе. По истечении этого времени, образец полностью насыщен и была снижена до минимума модуль Юнга при данной температуре.
- Быстро загрузить сэмпл в microtensile тестер и начать циклическое тестирование microtensile, с кистью воздух прочь, в то время как образец высохнет. От этого будет зависеть, как быстро высыхает образца под неконтролируемых условиях.
- Загрузите вторую PBS-насыщенных установки образца в microtensile тестер, и начать циклическое тестирование microtensileс кистью воздух далее. Это позволит определить, как быстро высыхает образца при контролируемых условиях окружающей среды.
4. Имплантация зонда и Эксплантация
- Установите имплантат образца фиксатора микроманипулятор и положение ортогонально кортикальной тканью.
- Перед введением, сохранить достаточно влажной ткани физиологическим раствором для обеспечения однородности ткани механики.
- Нижняя образца полимера в кору с помощью элементов управления микроманипулятор рукой. Оставьте образец в кортикальной тканью до времени имплантат цели, как правило, от 1 до 30 мин. Для предотвращения от высыхания тканей для моментов времени в течение 5 минут, слегка промокните ткань каждые 5 мин с использованием солевого пропитанной ватным тампоном.
- В то время как зонд имплантируется в коре головного мозга, готовят microtensile тестер для загрузки в настоящее время имплантированный образец путем установки приводного стержня с нулевым смещением положении 3,0 мм от стационарного зажима образца. Кроме того, установите сопло аэрографас параметром потока и излучающий источник тепла для соответствующей интенсивности определения на шаге 2.4.
- По окончании указанного времени имплантат, приподнять зонд из коры с помощью элементов управления микроманипулятор рукой. Сразу и осторожно удалить образец из микроманипулятор зажима и загрузить в microtensile тестер, как более подробно описано в шаге 5.2.
5. Microtensile Тестирование образцов имплантатов
- Чтобы сэкономить время после эксплантации, убедитесь, что microtensile тестер полностью готова принять имплантата образца до имплантации, как описано в шаге 4.4.
- Сразу после эксплантация, загрузка образца между двумя наборами microtensile зажимы тестера. Поскольку образец крепится к акриловым держателем призвана служить в качестве верхней половины один зажим, сборки поместить имплантат образец на мобильный захват, образец стороной вниз. Важно, чтобы гарантировать, что образец установлен таким образом, что штамм заявлIED только по длине зонда, чтобы избежать приложения крутящего момента образца во время испытания. Таким образом, образец должен быть установлен в центре каждого зажима и зажимы должны быть выровнены по отношению друг к другу.
- Регулировка положения образца таким образом, чтобы расстояние между зажимами составляет 3,0 мм, а конец зонда помещается в основной зажима. В этом 3.0 мм Расстояние между зажимами расстояние между метками для образца, и будет использоваться в дальнейших вычислениях для определения нагрузки на образец.
- Сразу после крепления образца между двумя зажимами, и в течение 2 мин эксплантация из нервной ткани, активируют двигателя в направлении растягивающей нагрузки на удлиненное образца с постоянной скоростью (10 мкм / сек использован здесь), одновременно измерения и записи удлинение образца (с использованием перемещение индикатора, Mitutoyu 543-561) и соответствующие силы (с помощью датчика, преобразователь Методы МБР-2.5), необходимых к деформации образца. Остановить microtensile испытание на механические разрушения образца, или когда конец диапазона шток привода будет достигнута. Экспорт собранных данных, а также выполнять анализ данных.
- Повторите microtensile тестирования для каждого образца и / или каждый набор условий (т.е. время вставки).
6. Анализ данных
- Преобразование исходных данных удлинение к инженерным штаммом применяется к имплантату образца путем деления расстояния удлинения начальной расчетной длины, как описано в формуле 1, где ε в приложенной деформации, т время, д является смещение измеряется микрометром индикатора и L 0 начальная длина калибровочного образца:
 (1)
(1) - Преобразование исходных данных усилие к инженерным напряжение на образце путем деления силы (в ньютонах), к TRAnsverse площадь поперечного сечения, как описано в уравнении 2:
 (2)
(2)
где σ является напряжение на образце, F сила измеряется датчиком (в ньютонах), ш 0 является исходной ширины образца и трет 0 является исходной толщины образца. - Участок напряжение (σ [т]) в зависимости от деформации (ε [т]) кривой для каждого образца с помощью компьютерной программы, такой как Microsoft Excel.
- Изолировать линейной упругой части сюжета и использовать программные инструменты кривой, чтобы найти лучший подходящую линию к этой части. Наклон наилучшего линия соответствует модуль Юнга образца. Выделенную часть участка должна включать не менее 10 напряженно-деформированного очка, и должны быть приняты от части участка, где склон является наибольшей.
- Для циклических испытаний, модуль Юнга должны быть определены для каждого цикла. Это может быть автоматизирован или выполняться вручную.
- Для циклических испытаний, участок модуль Юнга каждого цикла в зависимости от времени. Это указывает на то, каким образом измеренные модуля изменяется с течением времени, что свидетельствует о том, как быстро установки образца смачивающие или сушки.
- Для имплантат образцов, каждый образец и время имплантат соответствует одному циклу циклических испытаний. Измерение модуля Юнга по методике, описанной выше, для каждого имплантата образца.
- Сюжет модуля Юнга по сравнению с имплантатом времени. На данный момент, сравнения могут быть сделаны, чтобы настольная исследований и т.д.
Результаты
Механические свойства практически всех полимерных материалов, в том числе наши ПВА-NC, зависят от воздействия окружающей среды. В частности, они включают воздействием тепла и влаги. Когда материал является пластифицированный благодаря поглощению влаги или претерпевает фазовый переход, он отображает снижение модуля Юнга. При подготовке влажности и температуры контролируемой среды для исключая виво образец механической характеристикой, важно обеспечить, чтобы было минимальное изменение содержания влаги в образце при загрузке образца в microtensile тестер, а также во время механических испытаний. Это оценивается с помощью контрольных экспериментах установки образца для того, чтобы образец не зависит от влажности порожденных кистью воздух, а также не быстро высушить во внешней среде. 5 показан пример демонстрирует график механические свойства сухой установки образца в процессе CYCLческих испытаний на растяжение для соответствующей настройки кисти влаги воздуха. Любое изменение модуля Юнга в то время как щетка воздуха включена минимальна. Это важно, поскольку внешняя среда не должна способствовать уменьшению или увеличению жесткости. Когда поток воздуха от кисти установлена слишком высокой, модуль Юнга образца, существенно снизит в течение примерно 60 сек.
Контроль за механическую среду тестирования можно также обеспечить, чтобы материалы не преждевременно высохнуть. Например, использование нашей влаги контролируемой среде увеличивает время, требуемое для эксплантированы образец сушат и восстановить его предимплантационной механическими свойствами. Рисунок 6 демонстрирует сушки поведение двух контрольных образцах настройки пропитанный к насыщению затем подвергают циклической тестирование растяжении под как контролируемых, так и неконтролируемых условиях окружающей среды. В не-контролируемой среде, образцы восстановить модуль Юнгапревышающий 400 МПа в 150 сек в течение которого образец был загружен в microtensile тестера. Это увеличение модуля Юнга в 20-40 раз больше, чем насыщенного образца в результате быстрой сушки образца 13. Под экологического контроля, заметного увеличения Модуль Юнга не измеряется до 240 секунд после удаления из погружной ванне. Этот период времени является достаточным для обоих нагрузки образца и выполнять достаточно механического тестированием, для извлечения модуля Юнга.
Дизайн для имплантата образцы для тестирования бывших естественных условиях (рис. 3) включает в себя рассмотрение ряда факторов. Во-первых, образцы должны быть имплантированы в интересующую ткань, которая является кора головного мозга в данном исследовании. В результате, образец должен иметь иглу стиле геометрия, которая представлена узкой ПВА-NC луча. Кроме того, образец должен быть разработан с учетом силы, необходимой для рenetrate интересующей ткани без потери устойчивости. Коробление формулы Эйлера учитывает модуль Юнга материала, а также от длины, ширины и толщины пучка, чтобы обеспечить критическую силу, при которой балочного типа зонда, как ожидается, пряжка 17. В этом исследовании, размеры пучка были выбраны таким образом, что зонд будет проникать через нервную ткань без риска деформации. Учитывая предыдущие исследования, показывающие, усилием менее 15 мН, выбранной длины зонда 4,5 мм, чтобы позволить 3 мм луч испытания и длиной 1,5 мм для захвата, и известный толщина пленки превышает 75 мкм, можно подсчитать, что зонд шириной должна превышать 107 мкм. Чтобы обеспечить максимальную стабильность при помощи инструмента лазерной микрообработки, шириной 300 мкм был выбран для образцов. Дополнительным предметом озабоченности является обработка микрозонд образца во время введения в ткань и удаление из ткани. В качестве простого луч может быть поврежден во время обработки с приложением BEAм до более существенной структурой (т.е. акриловый держатель) позволяет безопасно передачи имплантации и механических испытаний. Наконец, эта сборка должна быть оптимизирована для обеспечения загрузки в динамометре как можно быстрее.
Представитель график, показывающий кривые напряжение-деформация для сухого образца и мокрого образца, который был имплантирован в коры головного мозга крыс в течение 30 мин показано на рисунке 7. Модуль Юнга, что соответствует наклону напряжение-деформация участка в линейной упругой области, очевидно, значительно больше для сухого образца, чем для имплантированного образца. Оба образца были напряженными, чтобы сломаться. Тем не менее, модуль Юнга является производным от линейной упругой части участка, собранные в начале испытания на растяжение, перед входом пластической деформации и разрушения образца, как показано на рисунке 8. Рисунок 9 показывает, что примерно через 5 мин после имплантации образец расиграет небольшие изменения в модуль Юнга, предполагая, что образец достигает насыщения и минимальной жесткости в течение этого периода времени.

Рисунок 1. Схематический обзор экспериментального метода, чтобы охарактеризовать в естественных условиях механических свойств раздражителей аспекты, механически адаптивный микрозонд нанокомпозитного полимера. (А) Во-первых, образец получали путем структурирования ПВА-NC пленка в пучок и монтажа на акриловые держателя. (B) Зонд затем имплантировали в кору головного мозга в течение определенного периода времени. (C) Наконец, образец эксплантированы и подвергали microtensile тестирование с использованием заказных microtensile тестера.

Рисунок 2. Лазерный микромеханический ПВА-NC установки образца для установления необходимых экологических условий для сохранения в естественных условиях механического поведения ПВА-NC Имплантат образцов после эксплантации.

Рисунок 3. Фотографии имплантат образец, состоящий из лазерного узором ПВА-NC балка крепится к акриловый держатель.

Рисунок 4. Блок-схема microtensile тестера. Образец зажимают между фиксированным зажимом и подвижного зажима, который присоединен к приводному стержню линейной пьезодвигателя. Скорость деформации линейного пьезодвигателя контролируется и напряжение измеряется с помощью перемещение индикатора. Нагрузка, необходимая напрягать меня образецasured от тензодатчика. Условий окружающей среды в непосредственной близости от образца контролируется щетка воздуха и тепла лампы.

Рисунок 5. Модуль Юнга (Е), как функцию времени, измеренный во время циклических испытаний на растяжение для определения правильной настройки щетка воздуха для регулирования влажности в испытательной среде. Заштрихованная область представляет время, в течение которого воздух щетка была включена. В аэрограф используют, модуль Юнга существенно не изменяется с течением времени, предполагая, что количество воды, поглощенной образцом установки с воздуха кисть не достаточно, чтобы внести свой вклад в снижение жесткости.

Рисунок 6. Модуль Юнга (E) в зависимости от времени для водо-насыщающейред образцов как влага контролируемых и не контролируемых условиях испытания на растяжение. восстановление начальной модуль Юнга гораздо медленнее в контролируемой среде.
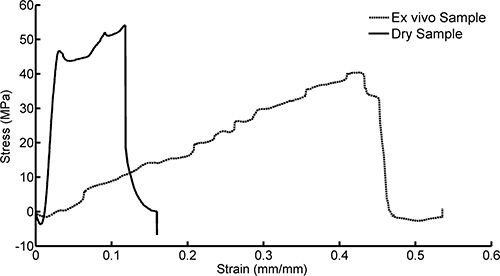
Рисунок 7. Пример напряженно-деформированного участков для ПВА-NC образцы, которые были сухими (не имплантированных) и влажный (экс естественных условиях, эксплантированы из ткани через 30 мин в естественных условиях).

Рисунок 8. Дополнительный комплект напряженно-деформированного участка, чтобы продемонстрировать, что линейная упругая часть сюжета изолирован от общего напряженно-деформированного участка (слева) и экстрагировали и подходят к линии (справа). Для этого конкретного измерения, Юнгамодуля составляет 16,8 МПа. Нажмите здесь, чтобы увеличить рисунок .
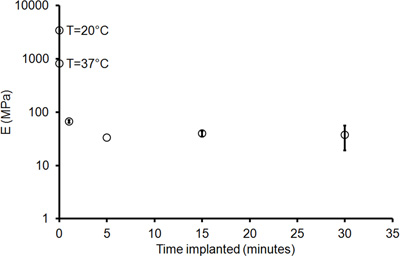
Рисунок 9. Модуль Юнга Е, в сравнении с имплантатом время для ПВА-NC образцы имплантирован в коре головного мозга. Столбики ошибок обозначают стандартную ошибку с п = 4, за исключением 5 мин имплантата, при п = 2.
Обсуждение
Продвижение имплантируемых биомедицинских микроэлектромеханических систем (BioMEMS) для взаимодействия с биологическими системами мотивирует развитие новых материалов с высокой заданными свойствами. Некоторые из этих материалов предназначены для демонстрируют изменение свойств материала в ответ на стимул найти в физиологической среде. Один недавно разработанные класс материалов реагирует на присутствие водородной связи образующие жидкости (например, воды) и при повышенных температурах, чтобы уменьшить модуль Юнга, мера жесткости материала, на три порядка 10,11,18. Эти материалы нанокомпозитных полимерных мягкой полимерной матрицы (то есть поли (винилацетата)) с целлюлозой нановолокон как нанонаполнителя фазу. Взаимодействие между целлюлозой нановолокон определяют механические свойства материала в целом, а также включены "вкл" при сухой и "выключено", когда влажный. Кроме того, вода пластифицируют полимер, паnocomposite, тем самым снижая температуру стеклования до температуры ниже температуры тела (37 ° С), что приводит к дальнейшему снижению модуля упругости. Одним из применений для этого класса материалов в качестве био-адаптивного субстрата для интракортикальных зондов для взаимодействия с отдельных нейронов 13,17. Однако преимущества механически адаптивный материал не ограничивается взаимодействие с нервной системы.
Представленные здесь метод, посредством которого механическое поведение ПВА-NC на основе микрозонды может быть оценена после имплантации в нервной ткани в течение заданного периода времени. Используя этот метод, экс естественных условиях механических данные могут быть собраны для сравнения с настольной исследований. Кроме того, в шкале времени изменения механические свойства могут быть оценены. Экологический контроль включен по тонкой настройке аэрографом и сияющей температурных режима обеспечивает механизм, посредством которого имплантированных образцов может быть проверена бывших естественных условиях с мини-Mal Изменение механических свойств в результате изменения в окружающей среде. Таким образом, в естественных условиях поведение материала можно сделать вывод, что обеспечивает превосходную информации по сравнению с настольной эксперименты с образцами полностью погружен в искусственную спинномозговую жидкость (ACSF). Сложный физиологический среда требует наличия таких методов, но экспериментальные методы оценки этого ограничены.
Есть несколько преимуществ для нашего метода для механической характеристике имплантированы, механически-адаптивных полимерных образцов нанокомпозита. Пользовательских тестер microtensile подходит для тестирования образцов с размерами, сравнимыми с типичным нейронных зонд (1,5-8 мм длиной, 50-500 мкм шириной, 15-100 мкм толщиной 3,19-21). Другие механические методы характеристику подходят как для больших, объемных образцов или наноразмерных образцов. Используя механический инструмент тестирования соответствующего масштаба удаляет неизвестные имущества масштабируемость. Кроме того, microtensile тестер имеет открытый доступ к тестируемого образца, что позволяет влажности и температуры среды тестирования. Кроме того, даже с контроля окружающей среды, необходимо, чтобы начать испытание на растяжение быстро после извлечения образца из нервной ткани. Ex сушки образец живом организме, и, следовательно, жесткости, было сведено к минимуму здесь использованием испытательного образца и конструкции microtensile тестер, которые способствуют быстрому (обычно в течение 120 секунд) загрузка и начало механических испытаний. Наконец, в этом microtensile тестер вмещает образцы, которые не имеют площадки на обоих концах, что облегчает использование зонда как образцы для механических испытаний, которые могут быть имплантированы в животных в идентичным образом, как для биологической оценки.
Удаление испытуемого образца из нервной ткани представляет новую среду, которая может привести к изменениям в поведении после механической эксплантации потому что стимулы аспекты поведения материала обратимой потенциально быстродействующие. При использовании этого экологически контролируемые испытания на растяжение метод оценки изменения механических свойств образцов после имплантации в мозг в течение заданного периода времени, потенциал ошибок относительно что фактический модуль Юнга в естественных условиях должны быть рассмотрены. Во-первых, путем тестирования образцов естественных бывший, они, по определению, удаляется из физиологической среде и подвергали альтернативный среды. Для образца с механические свойства в зависимости от условий окружающей среды, отбирают образец из окружающей среды изменит его механические свойства. Временная шкала, с которой это изменение происходит, зависит от свойствам материала, а также степень, до которой во внешнюю среду контролируется.
Такой подход к характеристике и количественной оценки стимулов проблематику механическое поведение лучше всего подходит для образцов с игольчатой геометрии, с длиной много большихт, чем ширина или толщина устройства. Кроме того, жесткость материала и конкретного двигателя и его максимальное усилие следует учитывать при выборе габаритов устройства. Учитывая набор размеров образца, более жесткий материал потребует большего выдвижной сила применить те же величины деформации в качестве материала с меньшим модулем упругости. Уменьшение ширины и / или толщины, или увеличение длины образца, позволит уменьшить усилие, необходимое для удлинения образца на заданную величину. Для пользовательские настройки тестирование растяжении, линейный пьезодвигателя имеет максимальную силу тяги N 6, который позволяет для образцов с модулем Юнга 5 ГПа и площадь поперечного сечения до 24000 мкм 2 напряженными 5%, не достигая максимального напряжение заставить электродвигателя. Датчик для измерения силы в microtensile тестер имеет разрешение менее 1 мН, так что наименьший модуль Юнга, которые могут быть измерены в образцах, используемых в нашем исследовании (ширина 300мкм, толщина 100 мкм) примерно 1 МПа. Этот нижний предел может быть дополнительно уменьшено с использованием образцов с большей площадью поперечного сечения, однако. Смещение индикатора имеет разрешение 0,5 мкм, что является достаточным для материалов с эластичными свойствами не более 0,2% деформации (при начальной длиной 3 мм), который является по порядку величины меньше, чем упругой области для ПВА- NC даже в сухом состоянии.
Один из недостатков этого метода бывших характеристика естественных условиях, что он не может быть эффективным для очень жесткие или хрупкие материалы. Практически говоря, в качестве образца должно быть быстро установлен в microtensile тестер, хрупкий материал находится под угрозой нарушения во время процедуры установки. Кроме того, пучкового типа образцов (с размерами, соответствующие этим наших экспериментов), один конец которого приклеен к акриловый держатель, а другой конец свободный не может быть использована для материалов, превышающей примерно 2,5 ГПа, в качестве силы, необходимой для страв пробе превышает силу зажима проведение образца в месте, в результате проскальзывание образца через зажимы и неточные результаты. Эта проблема была решена с использованием Догбон-образного образца с прокладками, на каждом конце. Это использование этого метода для измерения и анализа в естественных механических свойств микрозонды не ограничивается ПВА-NC класс материалов. Дополнительные возможности применения включают мониторинг скорости разложения биоразлагаемых материалов 22 и характеризующие механические свойства биологических тканей 23,24, а также характеристика микромасштабных структуры для небиологических приложений. Кроме того, дополнительные средства управления средой могут быть добавлены (например, рН, длина волны рассеянного света, электрическое поле, магнитное поле) для материалов, которые реагируют на различные стимулы 25,26. Одним из основных преимуществ этого способа является его универсальность и применимость к различным материилс и приложений.
Раскрытие информации
Нам нечего раскрывать.
Благодарности
Эта работа была поддержана Департаментом биомедицинской инженерии в Case Western Reserve University через обе лаборатории запуска средства (J. Capadona) и Medtronic стипендий (К. Поттер). Дополнительное финансирование на этом исследовании была частично поддержана грантом NSF ECS-0621984 (С. Zorman), Case Ассоциации выпускников (С. Zorman), Департамент по делам ветеранов через Премия заслуги обзора (B7122R), а также Advanced Платформа технический центр (C3819C).
Материалы
| Name | Company | Catalog Number | Comments |
| Silicon wafer | University Wafer | Mechanical grade | |
| Extruded acrylic sheet | Professional Plastics | SACR 062EF | Thickness 0.062" |
| Razor blade | McMaster-Carr | 3962A3 | |
| Tweezers | McMaster-Carr | 8384A47 | #5 tip |
| Super Glue Gel | Loctite | 130380 | |
| Air Brush | Snap-on Industrial | BF175TA | |
| Air Compressor | Paasche | B002YKN8YO | D500 |
| Thermocouple | Omega | HH12A | |
| Hot plate | Cimarec | SP131325Q | |
| CO2 direct-write laser | VersaLaser | 3.5 | |
| Dessicator | Fisher Scientific | 08-595 | |
| Lamp | custom-built | ||
| Microtensile tester | custom-built |
Ссылки
- Chen, P. J., Saati, S., Varma, R., Humayun, M. S., Tai, Y. C. Wireless intraocular pressure sensing using microfabricated minimally invasive flexible-coiled LC sensor implant. Journal of Microelectromechanical Systems. 19, 721-734 (2010).
- Ren, X., Zheng, N., Gao, Y., Chen, T., Lu, W. Biodegradable three-dimension micro-device delivering 5-fluorouracil in tumor bearing mice. Drug Delivery. 19, 36-44 (2012).
- Bai, Q. Single-unit neural recording with active microelectrode arrays. IEEE Transactions on Biomedical Engineering. 48, 911 (2001).
- Rousche, P. J., Pellinen, D. S., Pivin, D. P., Williams, J. C., Vetter, R. J., kirke, D. R. Flexible polyimide-based intracortical electrode arrays with bioactive capability. IEEE Transactions on Biomedical Engineering. 48, 361-371 (2001).
- Hassler, C., Boretius, T., Stieglitz, T. Polymers for neural implants. Journal of Polymer Science Part B: Polymer Physics. 49, 18-33 (2011).
- Mercanzini, A., Colin, P., Bensadoun, J. C., Bertsch, A., Renaud, P. In Vivo Electrical Impedance Spectroscopy of Tissue Reaction to Microelectrode Arrays. IEEE Transactions on Biomedical Engineering. 56, 1909-1918 (2009).
- Polikov, V. S., Tresco, P. A., Reichert, W. M. Response of brain tissue to chronically implanted neural electrodes. Journal of Neuroscience Methods. 148, 1-18 (2005).
- Subbaroyan, J., Kipke, D. Engineering in Medicine and Biology Society, 2006. , 3588-3591 (2006).
- Harris, J., Capadona, J., Miller, R., Healy, B., Shanmuganathan, K., Rowan, S., Weder, C., Tyler, D. Mechanically adaptive intracortical implants improve the proximity of neuronal cell bodies. Journal of Neural Engineering. 8, 066011 (2011).
- Capadona, J. R., Shanmuganathan, K., Tyler, D. J., Rowan, S. J., Weder, C. Stimuli-Responsive Polymer Nanocomposites Inspired by the Sea Cucumber Dermis. Science. 319, 1370-1374 (2008).
- Shanmuganathan, K., Capadona, J. R., Rowan, S. J., Weder, C. Stimuli-Responsive Mechanically Adaptive Polymer Nanocomposites. ACS Applied Materials & Interfaces. 2, 165-174 (2009).
- Shanmuganathan, K., Capadona, J. R., Rowan, S. J., Weder, C. Bio-inspired mechanically-adaptive nanocomposites derived from cotton cellulose whiskers. Journal of Materials Chemistry. 20, 180 (2010).
- Hess, A., Capadona, J., Shanmuganathan, K., Hsu, L., Rowan, S., Weder, C., Tyler, D., Zorman, C. Development of a stimuli-responsive polymer nanocomposite toward biologically optimized, MEMS-based neural probes. Journal of Micromechanics and Microengineering. 21, 054009 (2011).
- Capadona, J. R., Tyler, D. J., Zorman, C. A., Rowan, S. J., Weder, C. Mechanically adaptive nanocomposites for neural interfacing. Materials Research Society Bulletin. 37, 581-589 (2012).
- Ophir, J., Cespedes, I., Garra, B., Ponnekanti, H., Huang, Y. Elastography: ultrasonic imaging of tissue strain and elastic modulus in vivo. European journal of ultrasound. 3, 49-70 (1996).
- Hess, A., Shanmuganathan, K., Capadona, J., Hsu, L., Rowan, S., Weder, C., Tyler, D., Zorman, C. Micro Electro Mechanical Systems (MEMS). , 453-456 (2011).
- Harris, J. P., Hess, A. E., Rowan, S. J., Weder, C., Zorman, C. A., Tyler, D. J., Capadona, J. R. In vivo deployment of mechanically adaptive nanocomposites for intracortical microelectrodes. Journal of Neural Engineering. 8, 046010 (2011).
- Shanmuganathan, K. . Bio-inspired Stimuli-responsive Mechanically Dynamic Nanocomposites. , (2010).
- Rousche, P. J., Pellinen, D. S., Pivin, D. P., Williams, J. C., Vetter, R. J., Kipke, D. R. Flexible polyimide-based intracortical electrode arrays with bioactive capability. IEEE Transactions on Biomedical Engineering. 48, 361-371 (2001).
- Norlin, P., Kindlundh, M., Mouroux, A., Yoshida, K., Hofmann, U. G. A 32-site neural recording probe fabricated by DRIE of SOI substrates. Journal of Micromechanics and Microengineering. 12, 414 (2002).
- Ward, M. P., Rajdev, P., Ellison, C., Irazoqui, P. P. Toward a comparison of microelectrodes for acute and chronic recordings. Brain Research. 1282, 183-200 (2009).
- Lin, J. M., Chang, P. K. A Novel Remote Health Monitor with Replaceable Non-Fragile Bio-Probes on RFID Tag. Applied Mechanics and Materials. 145, 415-419 (2012).
- Kunzelman, K. S., Cochran, R. Stress/strain characteristics of porcine mitral valve tissue: parallel versus perpendicular collagen orientation. Journal of Cardiac Surgery. 7, 71-78 (1992).
- Snedeker, J., Niederer, P., Schmidlin, F., Farshad, M., Demetropoulos, C., Lee, J., Yang, K. Strain-rate dependent material properties of the porcine and human kidney capsule. Journal of Biomechanics. 38, 1011-1021 (2005).
- Ahn, S., Kasi, R. M., Kim, S. C., Sharma, N., Zhou, Y. Stimuli-responsive polymer gels. Soft Matter. 4, 1151-1157 (2008).
- Stuart, M. A. C., et al. Emerging applications of stimuli-responsive polymer materials. Nature Materials. 9, 101-113 (2010).
Перепечатки и разрешения
Запросить разрешение на использование текста или рисунков этого JoVE статьи
Запросить разрешениеСмотреть дополнительные статьи
This article has been published
Video Coming Soon
Авторские права © 2025 MyJoVE Corporation. Все права защищены