Necropsia diagnóstica e coleta de tecidos
Visão Geral
Fonte: Kay Stewart, RVT, RLATG, CMAR; Valerie A. Schroeder, RVT, RLATG. Universidade de Notre Dame, IN
Muitos experimentos em animais dependem de pontos de tempo finais de coleta de dados que são coletados a partir da colheita e teste de órgãos e tecidos. O uso de métodos adequados para a coleta de órgãos e tecidos pode impactar a qualidade das amostras e a análise dos dados coletados para o teste dos tecidos. O método de eutanásia do animal também pode impactar a qualidade das amostras. Este manuscrito vai delinear técnicas adequadas de necropsia para ratos.
Princípios
O método de eutanásia mais usado para camundongos e ratos é uma overdose de gás dióxido de carbono (CO2). De acordo com a American Veterinary Medical Association (AVMA), o uso de CO2 é aceitável com condições que minimizam a aversão e a angústia. 1 Os animais são deixados em sua gaiola de origem, que é colocada em uma câmara. O CO2 é introduzido gradualmente na câmara a uma taxa de deslocamento de 10% a 30% do volume da câmara/min, o que faz com que os animais percam a consciência antes da percepção da dor associada à ativação do nociceptor por ácido carbônico. O fluxo é então mantido na câmara uma vez que ocorreu parada respiratória para garantir que o animal esteja morto. Uma overdose de anestesia inalante também é aceitável, especialmente para projetos que requerem o uso de tecido pulmonar, pois o CO2 causa danos ao tecido pulmonar. A exsanguinação do animal também pode ser necessária para alguns experimentos para reduzir o volume de sangue nos tecidos.
O registro preciso de todos os achados é essencial durante uma necropsia. Deve-se iniciar um formulário que registra um histórico completo do animal, incluindo identificação animal, sexo, condições de moradia, data de nascimento, data de nascimento, número do estudo/número do protocolo e o nome do Pesquisador Principal. Um exame interno grosseiro é realizado à medida que as cavidades corporais são expostas para revelar os órgãos internos. Qualquer anormalidade óbvia deve ser notada. 2
A necropsia e a colheita de tecidos devem ser iniciadas imediatamente após a eutanásia do animal, pois o vazamento bacteriano do trato intestinal pode confundir alguns ensaios. Os órgãos internos devem ser observados a partir da cavidade abdominal e movendo-se para a cavidade torácica. Antes de remover qualquer amostra de tecido, é importante observar os órgãos in situ. 2 A colheita de órgãos e tecidos para exame histológico requer que os tecidos estejam devidamente preparados. As amostras de tecido para histologia devem ser de 0,5-1 cm de espessura para permitir a penetração suficiente da solução fixa. A fixação preserva tecidos biológicos que previnem a decomposição, a autolise e a putrefação. Também interrompe qualquer reação bioquímica em curso e pode aumentar a resistência mecânica ou estabilidade dos tecidos tratados. O objetivo amplo da fixação tecidual é preservar células e componentes teciduais para permitir a preparação de seções finas e manchadas. Salvo especificação em contrário, a fixação mais usada é a formalina com tamponador neutro de 10%. A formalina com 10% de buffer neutro está comercialmente disponível nos principais fornecedores. 3
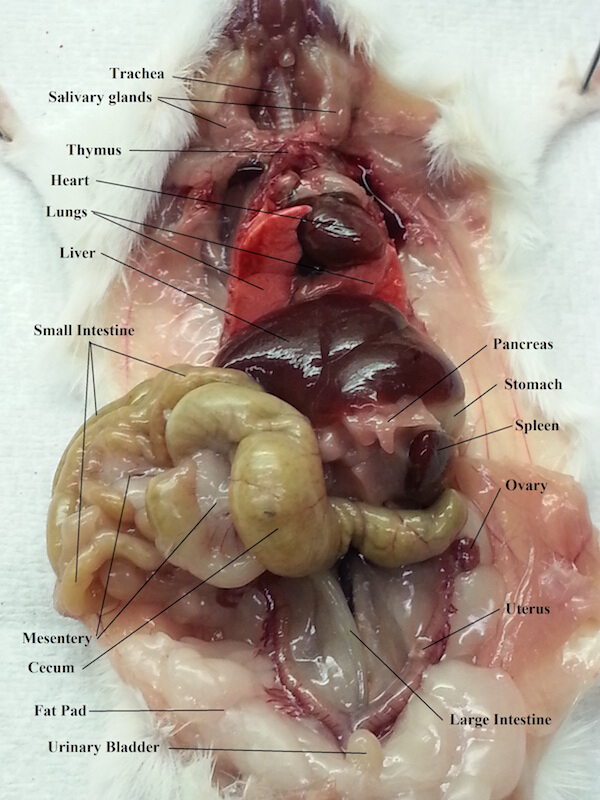
Figura 1. Órgãos abdominais e torácciis de uma ratazana fêmea.
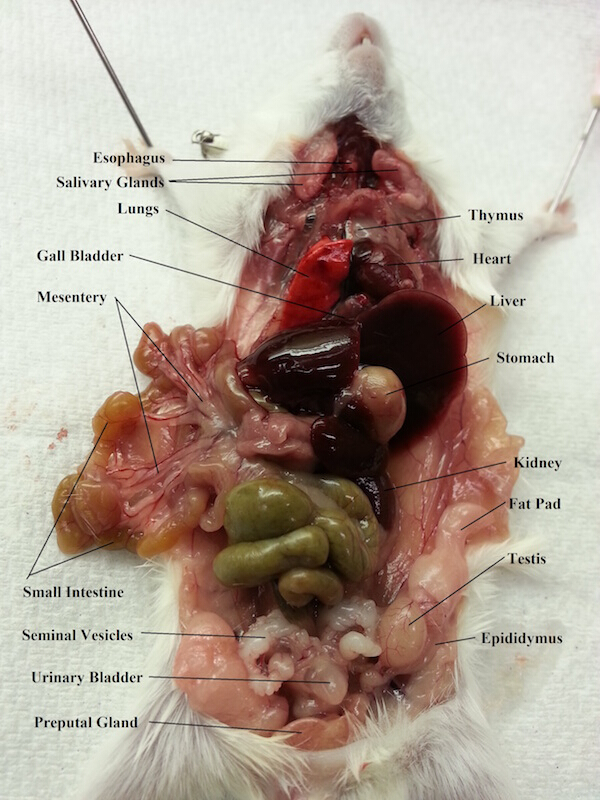
Figura 2. Órgãos abdominais e torácficos de um rato macho.
Procedimento
1. Exame externo
Um exame externo grosseiro do corpo, que inclui inspeção visual do corpo para lesões e massas, deve ser realizado como etapa inicial em uma necropsia. O casaco de cabelo deve ser examinado para áreas de queda de cabelo. Os dentes e unhas são avaliados para crescimento ou desgaste excessivos. Qualquer mancha da pele na boca, nares, olhos, aberturas anais e genitais deve ser notada. Testes de fita, raspagem de pele e exames de pele devem ser realizados para detectar parasitas externos (veja procedimentos abaixo).
- Teste de fita
- O equipamento necessário para um teste de fita inclui luvas, uma tira de fita celofane clara, um slide de microscópio de vidro e uma tesoura.
- Luvas são sempre usadas ao manusear a fita, pois o adesivo levantará óleos e células da pele dos dedos, obscurecendo achados ou causando confusão ao avaliar o slide.
- Corte um pedaço de fita ligeiramente mais estreito que a largura, e mais curto que o comprimento do slide do microscópio.
- Pressione cuidadosamente o lado pegajoso da fita para o ânus e área circundante, e remova-a rapidamente.
- Usando a extremidade oposta da fita, pressione-a entre as omoplatas e remova-a rapidamente.
- Aplique a fita no slide do microscópio.
- O teste de fita está pronto para exame microscópico. Os ovos parasitas são visíveis na ampliação 4X, mas devem ser examinados com ampliação de 10X para identificar adequadamente a espécie.
- É importante evitar tocar no lado adesivo da fita. A fita levantará detritos das mãos enluvadas e dificultará a leitura do slide.
- Raspagem de pele
- O teste de raspagem da pele é realizado em qualquer área de alopecia, lesões cutâneas ou excoração.
- O equipamento necessário para raspagem da pele é um escorregador de microscópio de vidro limpo, óleo mineral e uma espátula metálica ou lâmina de bisturi.
- Coloque algumas gotas de óleo mineral no deslizamento do microscópio.
- Belisque a pele em uma dobra na borda da lesão ou área de interesse.
- Coloque uma pequena quantidade de óleo mineral na pele.
- Coloque a borda da espátula ou lâmina de bisturi na pele e raspe contra a direção do crescimento capilar.
- Continue raspando até que uma pequena quantidade de vermelhidão seja visível na pele.
- Coloque o cabelo e o tecido raspados da superfície da pele no óleo na lâmina do microscópio. Se necessário, espalhe o material para que seja distribuído uniformemente no óleo.
- O slide está pronto para ser examinado sob o microscópio. Se desejar, uma mancha de cobertura pode ser aplicada à queda de óleo no slide. Examine o slide na ampliação 4X e 10X.
- Exame de pele
- O exame de pele é o último exame externo realizado; no entanto, é realmente feito após o exame interno ser concluído.
- O animal é colocado em uma placa de vidro ou plástico de Petri depois de todas as amostras internas de órgãos terem sido coletadas.
- O prato é colocado em uma geladeira por 15 minutos.
- Após 15 minutos, o prato é colocado sob um microscópio dissecando e a pele é examinada para parasitas externos. A maioria dos ácaros de pele se movem para as extremidades dos cabelos e são facilmente observados.
2. Exame interno bruto da cavidade abdominal
- Extirparecendo a pele
- Um pequeno corte é feito apenas antes da pelve em fêmeas e acima do prepuce em machos.
- O corte da pele é estendido ao queixo.
- Dissecção cega é usada para soltar a pele da fáscia e músculo.
- Os cortes transversais são feitos anteriores aos membros traseiros e posteriores aos membros da primeira. Deve-se tomar cuidado para não cortar os vasos sanguíneos na área axilar.
- Use dissecção contundente para expor a área cervical e o tórax. Devem ser exercidos cuidados extras para evitar a ruptura dos vasos jugular e carótida no pescoço.
- Glândulas mamárias
- Nas fêmeas, examine o tecido mamário para procurar massas, descoloração ou anormalidades.
- Lactante ou fêmeas grávidas terão aumento do volume de tecido mamário, e o leite pode estar presente.
- O tecido mamário é encontrado desde o topo do esterno no manúbrio até a abertura genital na superfície ventral, e estende-se lateralmente para cima ambos os lados quase tocando na superfície dorsal nos quadris e ombros.
- A excisão das glândulas mamárias requer agarrar a borda da glândula com fórceps do polegar e usar dissecção contundente para afrouxar os apegos à pele. Uma vez que a glândula tenha sido separada da pele, a tesoura de íris pode ser usada para cortar quaisquer anexos restantes antes de colocar a glândula em uma solução fixa.
- Glândulas subcutâneas
- As glândulas pré-putial são emparelhadas e localizadas apenas anteriores ao prepuce no rato macho. Eles parecem grandes e são uma cor cinza a amarelada com uma aparência espuma.
- As glândulas salivares submandibulares são emparelhadas, localizadas na mandíbula, e estendem-se ao longo do pescoço até o esterno de manúbrio. Eles têm uma cobertura dura e são firmemente aderidos aos músculos.
- A remoção dessas glândulas requer dissecção contundente e cuidados extras ao trabalhar na região cervical para evitar a ruptura dos vasos sanguíneos. Dissecção contundente é uma técnica em dissecção anatômica na qual os tecidos são separados e estruturas subjacentes expostas sem corte.
- Para dissecção contundente, a tesoura é usada para espalhar tecidos separados, em vez de cortá-los. As pontas fechadas são empurradas para o tecido e depois abertas para dividir tecido ao longo de planos naturais. Esse processo requer paciência e um toque delicado, pois o alongamento do tecido pode resultar em danos a órgãos e vasos sanguíneos adjacentes.
- As glândulas, uma vez liberadas dos músculos subjacentes, são levantadas e quaisquer anexos residuais são cortados.
- As glândulas requerem pelo menos um corte para permitir a penetração do fixador.
- A gordura subcutânea é avaliada para quantidade e deposição. Um animal obeso pode ter uma grande quantidade de gordura com a pele se sentindo espessa. Os animais que estão desidratados terão elasticidade reduzida da pele, e ele se sentirá mais fino.
- Músculo
- Observe os músculos abdominais, intercostais e expostos do pescoço e dos membros. Note qualquer espessamento anormal, massas ou descoloração.
- Se for necessário músculo para análise, selecione e corte a amostra antes de tomar qualquer órgão abdominal para reduzir a contaminação sanguínea.
- Abrindo a cavidade corporal
- Um pequeno corte transverso é feito no ponto mais caudal do músculo abdominal exposto.
- Levantando o músculo para longe dos órgãos, corte ao longo da linha alba até o xifoide.
- Corte os músculos abdominais da linha média lateralmente, logo acima dos membros traseiros de ambos os lados.
- Corte o músculo abdominal ao longo da curva das costelas em ambos os lados.
- Gordura abdominal
- Avalie a quantidade e o acúmulo de gordura corporal. Um animal saudável terá almofadas de gordura abdominal e alguma gordura ao longo da superfície dorsal na cavidade abdominal. Um animal excessivamente magro, ou um animal muito jovem, não terá quantidades consideráveis de gordura ao redor dos rins.
- Observe a cor da gordura corporal e note quaisquer anormalidades.
3. Órgãos abdominais
- Fígado
- Normalmente, a cor do fígado deve ser um vermelho escuro. As margens devem ser lisas e ter uma borda nítida. Um fígado anormal terá uma borda espessa e pode ter entalhes ou bordas escalopadas.
- Deve-se tomar cuidado ao manusear o fígado, pois é um tecido friável. Qualquer interrupção na integridade do órgão resultará em vazamento de sangue na cavidade corporal e ocultação dos órgãos.
- Reflita suavemente o fígado para longe do diafragma, e faça um corte nos vasos sanguíneos anteriores ao fígado.
- Reflita o fígado de volta em direção ao diafragma e segure o nódulo fibroso que conecta todos os lóbulos do fígado centralmente. Levante o fígado enquanto corta todos os acessórios ao trato intestinal e estômago.
- Remova o fígado em uma peça e borre o excesso de sangue da superfície do órgão. Pode ser colocado em um banho salino, ou enxaguado em soro fisiológico estéril, antes de cortar em seções mais finas para permitir a penetração de soluções fixas.
- Vesícula biliar
- A vesícula biliar é um pequeno saco transparente que muitas vezes aparece amarelo devido ao acúmulo de bile. Está presente em ratos, mas não em ratos.
- A vesícula biliar está localizada entre os lóbulos superiores do fígado ao longo da linha média. É geralmente conectado ao diafragma por um frênulo fino que pode ser acidentalmente rasgado, causando a ruptura da vesícula biliar.
- A vesícula biliar pode ser removida com o fígado e separada posteriormente para exame.
- Baço
- O baço é vermelho escuro e localizado ao longo da curvatura inferior do estômago. Deve ser regular em forma, com uma superfície ligeiramente fosca.
- É geralmente maior em machos do que em fêmeas. Animais com infecções parasitárias internas, infecções bacterianas ou doenças do sangue podem ter aumentado o baço.
- Como os filtros de baço danificaram os glóbulos vermelhos da circulação, ele é preenchido com sangue. Ao remover o baço, evite perfurar o órgão.
- Para removê-lo, o baço é levantado e os acessórios cortados entre o estômago e o baço.
- Trato intestinal
- As alterações pós-morte ocorrem rapidamente e incluem a poça de sangue nos tecidos, resultando no aparecimento de hematomas e no balonismo dos intestinos com gás frequentemente produzido pelo crescimento excessivo bacteriano. O trato intestinal é cuidadosamente examinado depois de ter sido removido do corpo.
- Estômago
- O estômago está localizado na extremidade distal do esôfago. Parece ser de dois tons, diferenciando as porções musculares e glandulares.
- O estômago deve ser avaliado para a presença de alimentos por sentir. Roedores geralmente comem constantemente devido a uma alta taxa metabólica. Deve-se notar um estômago vazio, pois pode ser indicativo de doença.
- Não corte o estômago, pois o conteúdo contaminará os órgãos da cavidade abdominal.
- Para remover o estômago do trato intestinal, o esôfago é cortado apenas antes do estômago. Se o estômago for colocado em um recipiente comum de fixação, um pedaço de sutura pode ser amarrado ao redor do esôfago para evitar derramamento de conteúdo estomacal antes do corte.
- Intestino delgado
- O intestino delgado é composto por três seções: o duodeno, o jejunum e o íleo. Não conterá pelotas fecais.
- O duodeno é uma seção mais curta do esfíncter estomacal posterior até o início do jejunum. O ducto biliar entra no intestino delgado no duodeno, e o tecido pancreático é mais firmemente ligado a esta porção do intestino delgado.
- O jejunum é a porção central do intestino delgado.
- As manchas de Peyer compostas de tecido linfoide em pequenas manchas ovais estão presentes na superfície não mesentérica do jejunum e do íleo no rato. 3 Estes fazem parte do sistema imunológico e podem ser úteis no diagnóstico de doenças imunológicas.
- O íleo é a porção distal do intestino delgado e é a parte mais longa, terminando no ceco.
- Ceco
- O ceco é uma cor esverdeada e muito macia.
- Está localizado na junção dos intestinos pequeno e grosso.
- A fermentação ocorre no ceco, então a punção do órgão resultará em um mau cheiro e contaminação dos órgãos com bactérias.
- Intestino grosso
- O intestino grosso começa no ceco e continua até o ânus. É facilmente identificável, pois pelotas fecais podem ser visualizadas dentro do lúmen do intestino.
- Não deve haver áreas de hemorragia ou descoloração imediatamente após a eutanásia.
- Mesenteria
- Os intestinos pequenos e grandes são ancorados ao corpo pela mesenteria, uma membrana contendo vasos sanguíneos, gordura e linfonodos.
- Deve ser examinado para nódulos linfáticos aumentados e quaisquer massas antes da remoção do trato intestinal.
- Pâncreas
- O pâncreas é um órgão difuso localizado abaixo do estômago e entre as primeiras dobras do duodeno. É um bronzeado claro para a cor cinza e composto de vários pequenos lóbulos com bordas irregulares.
- Pode não ser possível remover o pâncreas inteiro.
- Se o tecido pancreático for colhido, deve ser feito antes da remoção do trato intestinal.
- O tecido identificado como pancreático deve ser cuidadosamente provocado longe do tecido mesenérico ao seu redor.
- Removendo o trato intestinal
- O trato intestinal é removido como uma peça, começando pelo estômago e estendendo-se ao ânus.
- Um corte é feito através do intestino grosso, apenas anterior ao ânus. Todo o trato intestinal pode ser levantado e quaisquer ligações membranous cortadas. O trato intestinal pode então ser removido da mesenteria, cortado em seções e fixado.
- Ao colocar seções do intestino em frascos contendo outros órgãos, é imprescindível que as extremidades sejam amarradas para evitar a contaminação de tecidos com bactérias intestinais.
- O lúmen do trato intestinal pode ser exposto cortando seu comprimento usando uma tesoura pequena e fina. O interior pode ser enxaguado depois de expor o lúmen.
- Alguns estudos podem exigir que uma porção do intestino seja removida e lavada em vez de cortada. Ao fixar uma agulha cega em uma extremidade do tecido excisado, a solução salina ou fixativa pode ser forçada a entrar no intestino para lavar o conteúdo.
- Rim
- Os rins são órgãos emparelhados localizados contra os músculos das costas. O rim direito é maior que o esquerdo. Os rins em animais mais velhos podem estar cercados por depósitos de gordura, tornando-os difíceis de visualizar.
- É aproximadamente o tamanho e a cor de um feijão de rim escuro, e suas superfícies devem ser lisas.
- Imediatamente anterior ao rim está a glândula suprarrenal, aparecendo como um pequeno nódulo rosa-claro.
- Para remover o rim, isolá-lo usando um fórceps, e cortar entre o rim e o ureter.
- Os rins têm uma cápsula externa dura que pode ser descascada para melhor visualizar as superfícies. Corte um rim ao meio ao longo do eixo longo e o outro rim transversalmente. Note que qualquer grão dentro do rim pode indicar a presença de cristais ou depósitos minerais.
- Sistema reprodutivo feminino
- O útero é uma estrutura em forma de Y. O corpo do útero é curto com os chifres emparelhados à esquerda e à direita. Os chifres terminam nos tubos de falópio e nos ovários. Em uma fêmea não grávida, os chifres serão rosa pálido e fino. Em um animal grávida, os chifres aparecerão mais escuros e terão vasos sanguíneos pronunciados correndo ao lado dos chifres uterinos. À medida que a gestação prossegue, os chifres uterinos terão uma aparência de "corda de pérolas". Os embriões em desenvolvimento criarão uma área pálida dentro do chifre, e à medida que se desenvolvem, o útero se alongará e o tecido ficará mais fino, permitindo a visualização.
- Os ovários estarão localizados logo abaixo dos rins. Eles terão uma superfície áspera devido a diferentes estágios de maturação dos folículos. Ovários císticos terão vesículas cheias de fluidos. Este fluido pode variar de cor de palha a sanguineous.
- Para remover os ovários, corte os acessórios arteriais anteriormente e o tubo falópio posteriormente. Se desejar, os ovários podem ser retirados ligados ao útero.
- Para remover o útero, ele tem que ser suavemente agarrado e a tração aplicada para ser capaz de cortar abaixo do colo do útero. Após o corte, levante o corpo e os chifres do útero, quebrando qualquer apego na cavidade corporal.
- Sistema reprodutivo masculino
- As vesículas seminais são brancas, em forma de chifre, estruturas emparelhadas localizadas anteriormente à bexiga urinária e anexadas na linha média na próstata. O tamanho varia, mas eles podem ser tão grandes quanto o ceco.
- A próstata está localizada ao redor da bexiga urinária na base. Este tecido é geralmente um bronzeado leve. Em animais mais velhos, pode apresentar hiperplasia. Animais mais velhos geralmente terão mais gordura corporal que pode dificultar a visualização da próstata.
- Os testículos são emparelhados e localizados nos sacos escrotais. A superfície deve ser lisa com vascularização fina evidente na superfície. Camundongos e ratos não têm um anel inguinal ou esfíncter, o que permite que o animal retire os testículos na cavidade abdominal. Para visualizá-las, segure as almofadas de gordura abdominal localizadas no abdômen inferior e puxe-as anteriormente. Isso vai tirar os testículos do escroto para permitir o exame. O epidídicos está ao longo da margem inferior dos testis e tapers em direção ao topo. O vas deferens é anexado ao final do epidídis e leva de volta à próstata.
- A remoção dos testículos pode ser realizada cortando o acessório no escroto e cortando os vasos deferdes.
- Remover a próstata e vesículas seminais requer apreensão da base da bexiga urinária e do levantamento, enquanto corta os acessórios abaixo da próstata.
4. Cavidade torácica
- Pulmões
- Os pulmões são normalmente uma cor rosa brilhante, e esponjoso em textura com uma superfície lisa. No entanto, a eutanásia com CO2 pode causar hemorragias pulmonares, resultando em manchas vermelhas escuras que podem cobrir toda a superfície pulmonar.
- Coração
- O coração é vermelho escuro com quatro câmaras. Os ventrículos são musculosos e se sentem firmes ao toque. Os atrias são mais escuros de cor vermelha e sentam-se no topo dos ventrículos. Eles são muito menos musculosos e parecem flácidos.
- O saco pericárdico é uma membrana fina e translúcida ao redor do coração.
- Timo
- O timo está localizado anteriormente ao coração e se senta sobre a traqueia. Deve ser suave na textura.
- Em animais jovens, aparece bronzeado com uma textura gordurosa.
- Animais mais velhos terão infiltração de tecido adiposo no timo, ampliando-o e dando ao timo uma cor branca.
- Traqueia
- A traqueia se estende desde a epiglote até a bifurcação dos brônquios. É um tubo cartilaginoso e cristais que é flexível.
- Deve ser claro e não ter nenhum líquido fluido ou espumado no lúmen. A eutanásia com CO2 pode causar acúmulo de fluidos (soroanguinos e/ou espuma) nos pulmões e traqueia devido à hemorragia.
- Esôfago
- O esôfago se estende da cavidade oral até o estômago. É um tubo muito fino que fica diretamente atrás da traqueia e atrás do coração, e passa através do diafragma para o estômago.
- O esôfago é difícil de remover, pois é facilmente rasgado mesmo que o tecido seja elástico. A remoção do esôfago é mais facilmente feita dissecando-o longe da traqueia após a remoção do coração e pulmões.
- Remoção dos órgãos torácciis
- O coração e os pulmões são mais facilmente removidos juntos.
- Coloque os fórceps perpendiculares à traqueia e segure a traqueia firmemente, logo acima do timo.
- Usando a tesoura, faça um corte perpendicular à traqueia antes das fórceps. Este corte deve cortar a traqueia e o esôfago.
- Sem afrouxar o aperto na traqueia, levante a traqueia caudally, e corte qualquer apego dos pulmões à superfície espinhal na caixa torácica.
- O esôfago pode precisar ser cortado para ser capaz de levantar o coração e os pulmões livres da cavidade torácica.
- Depois que o coração é removido do corpo, ele pode ser lavado com soro fisiológico para remover sangue residual e coágulos, ou pode ser preenchido com fixação através da aorta.
- Uma vez que os pulmões são excisados, eles são inflados com fixação. Uma ligadura é colocada vagamente ao redor da traqueia. Uma agulha que é presa a uma seringa contendo o fixador de escolha é enfiada no lúmen da traqueia. A ligadura é apertada ao redor da agulha, e o fixador é injetado até que os pulmões sejam inflados. Após a remoção da agulha, a ligadura é apertada para evitar vazamentos.
- Cavidade oral
- Língua
- A língua dos roedores é lisa.
- Examine a superfície em busca de lesões, incluindo a parte inferior.
- A língua raramente é colhida, exceto para investigações especializadas, como estudos de câncer bucal.
- Para remover a língua, corte as superfícies buccal de cada lado da cavidade oral até a articulação temporal-mandibular.
- Desloque a mandíbula e reflita a maxila para revelar a epiglote e a base da língua.
- Usando fórceps para estender a língua, corte os acessórios abaixo caudalmente até a base da língua.
- Mantendo a tração, corte horizontalmente na base da língua para libertá-la da cavidade oral.
- Dente
- A dentração de ratos consiste em três molares e um incisivo em cada quadrante que é separado por um diástema desdentado. Eles são cobertos por esmalte apenas no lado labial; na superfície interior do dente é dentina.
- Os dentes de rato são normalmente uma cor amarelo/laranja. Esta cor é mais pronunciada no esmalte incisivo e é devido à presença de um pigmento contendo ferro. A cor começa em cerca de 21 dias após o nascimento e se aprofunda com a idade.
- Examine os dentes para crescimento excessivo ou má oclusão.
- Língua
5. Cabeça
- Olho
- Os olhos devem ser iguais em tamanho e claros de exudate. A conjuntiva deve ser suave.
- Para remover os olhos, aplique pressão sobre a pele ao redor do olho para trás e para baixo para projetar o olho da órbita. Usando um fórceps de ponta curva, isole o globo e corte os acessórios que o seguram na tomada.
- Ouvidos
- Observe as orelhas para identificação. Alguns investigadores pedem que as etiquetas de ouvido sejam incluídas com amostras de órgãos para confirmação da identidade animal.
- Os canais auditivos são examinados para qualquer lesão, massas ou exsudatos.
- Nariz
- O nariz é observado para fluido ou exsudato.
- As nares devem ser simétricas e claras.
Aplicação e Resumo
O passo final em muitos projetos de pesquisa é a necropsia dos animais experimentais. Uma observação detalhada das estruturas externas e internas seguidas da coleta de tecidos para análise suplementar fornece uma grande quantidade de dados de pesquisa. Técnicas adequadas para remoção e preservação de tecidos com as soluções fixativas adequadas são essenciais para a correta interpretação dos achados.
Referências
- Leary, S., Underwood, W., Anthony, R., Cartner, S., Corey, D., Grandin, T., et al. 2013. AVMA guidelines for the euthanasia of animals: 2013 edition.
- Parkinson, C.M., O'Brien, A., Albers, T.M., Simon, M.A., Clifford, C.B. and Pritchett-Corning, K.R. 2011. Diagnostic Necropsy and Selected Tissue and Sample Collection in Rats and Mice. 54. e2966. 1-7.
- Fiette, L. and Slaoui, M. 2011. Necropsy and Sampling Procedures in Rodents. Drug Safety Evaluation: Methods and Protocols, 39-67.
- Youngson, R.M. 2005. Collins dictionary of Medicine fourth edition.
Tags
Pular para...
Vídeos desta coleção:

Now Playing
Necropsia diagnóstica e coleta de tecidos
Lab Animal Research
58.3K Visualizações

Técnicas de manuseio e contenção de roedores
Lab Animal Research
175.2K Visualizações

Procedimentos de Cuidados Básicos
Lab Animal Research
28.1K Visualizações

Fundamentos da Reprodução e Desmame
Lab Animal Research
35.8K Visualizações

Identificação de roedores I
Lab Animal Research
54.9K Visualizações

Identificação de Roedores II
Lab Animal Research
25.7K Visualizações

Administração de Composto I
Lab Animal Research
101.0K Visualizações

Administração de Composto II
Lab Animal Research
35.1K Visualizações

Administração de Composto III
Lab Animal Research
31.6K Visualizações

Administração de Composto IV
Lab Animal Research
51.9K Visualizações

Retirada de Sangue I
Lab Animal Research
172.2K Visualizações

Retirada de Sangue II
Lab Animal Research
73.6K Visualizações

Indução e Manutenção da Anestesia
Lab Animal Research
50.8K Visualizações

Considerações para cirurgia de roedores
Lab Animal Research
22.5K Visualizações

Coleta de Tecido Estéril
Lab Animal Research
34.9K Visualizações
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados