Method Article
Produzione di proteine PRMT ricombinanti utilizzando il baculovirus Expression Vector System
In questo articolo
Riepilogo
Il baculovirus expression vector system (BEVS) è una solida piattaforma per lo screening dell'espressione e la produzione di proteina arginina metiltransferasi (PRMT) da utilizzare per studi biochimici, biofisici e strutturali. Quantità di milligrammo di materiale possono essere prodotte per la maggior parte dei PRMT e di altre proteine di interesse che richiedono una piattaforma di espressione eucariotica.
Abstract
Protein arginina metiltransferasi (PRMTs) metilati arginina residui su un'ampia varietà di proteine che svolgono un ruolo in numerosi processi cellulari. I PRMT possono essere mono- o dimetilati gruppi arginina guanidino simmetricamente o asimmetricamente. La queste proteine è un'area complessa e intensamente studiata che richiede quantità di milligrammo di proteine ricombinanti di alta qualità. Il sistema di vettori di espressione del baculovirus (BEVS) che utilizza il nucleopolidrovirus multiplo autographa californica (AcMNPV) e le cellule di insetti Spodoptera frugiperda 9 (Sf9) è stato utilizzato per lo screening dell'espressione e la produzione di molti PRMT, tra cui PRMT 1, 2 e da 4 a 9. Per schermare contemporaneamente l'espressione di più costrutti di queste proteine, inclusi domini e frammenti troncati, nonché le proteine a lunghezza intera, abbiamo applicato metodi scalabili utilizzando pipette multicanale regolabili e programmabili, combinate con piastre e blocchi a 24 e 96 pozzi. Nel complesso, queste regolazioni del metodo hanno permesso una generazione su larga scala di DNA bacmid, virus ricombinanti e screening dell'espressione proteica. L'utilizzo di vasi di coltura con un volume elevato di sospensioni cellulari Sf9 ha contribuito a superare i limiti di spazio nella pipeline di produzione per la produzione di proteine su larga scala mono lotti. Qui descriviamo protocolli dettagliati per l'espressione efficiente ed economica di PRMT funzionali per studi biochimici, biofisici e strutturali.
Introduzione
Proteina arginina metiltransferasi (PRMTs) metilati residui di arginina in modo monometile o simmetrico/asimmetrico dimetile. Le sequenze ripetitive RG/RGG/GRG sono altamente preferite dalla maggior parte dei PRMT e si trovano in un'ampia varietà di proteine1,2. Le proteine metilate dell'arginina come istoni o fattori di trascrizione e fattori di giunzione regolano la trascrizione, la giunzione e la struttura della cromatina3,4. La crescente conoscenza della diversa regolazione dell'utilizzo del substrato e del cofattore, del turnover e della cinetica dei PRMT, nonché della generazione di inibitori selettivi, ha fatto luce meccanicistica su questi enzimi e sui lorocomplessi 5,6. Tuttavia, non tutti i membri della famiglia PRMT sono studiati nella stessa misura; Ad esempio, PRMT9 è stato scoperto solo di recente come membro della famiglia PRMT1. Gli studi di struttura e funzione enzimatica per queste proteine richiedono quantità sufficienti, spesso milligrammi, di proteine ricombinanti per essere disponibili.
Il sistema di espressione procariotica Escherichia coli (E. coli)è di solito la prima scelta per lo screening dell'espressione utilizzando più costrutti per una data proteina7,8,9. Tuttavia, l'espressione basata su E. colinon sempre si traducono in quantità sufficienti di proteine PRMT nelle loro forme attive, come abbiamo notato in particolare per PRMT5 e PRMT7 (vedi sotto). Pertanto, i PRMT che non si esprimevano in E. coli o che dovevano essere prodotti dai meccanismi di espressione eucariotica sono stati sottoclorati in vettori appropriati per lo screening dell'espressione nel sistema vettoriale di espressione baculovirus alternativo (BEVS). Mentre I campioni espressi da E. coli di PRMT1, PRMT3 e PRMT8 sono stati ampiamente utilizzati per saggi in vitro e cristallografia, altri PRMT come PRMT5, che richiede il partner vincolante MEP50 del suo doppio dominio metiltransferasi, e PRMT come PRMT7 e 9, richiedono l'espressione delle cellule di insetti per ottenere quantità sufficienti di proteine attive. Nel complesso, i test standardizzati di media throughput metiltransferasi per PRMT4, 5, 6, 7 e 9 hanno utilizzato il BEVS nelle cellule degli insetti6. Il baculovirus expression vector system (BEVS) è una piattaforma versatile per produrre proteine ricombinanti che richiedono il meccanismo di espressione eucariotica che consente modifiche post-traslazionali essenziali per gli studi biochimici, biofisici e strutturali10,11,12. Diversi BEVS sono diventati disponibili in commercio dal primo uso segnalato di baculovirus nel 1983 per l'espressione proteica13. La maggior parte di questi protocolli utilizza diverse strategie per il trasferimento dell'espressione plasmide in cellule di insetti. Questi includono Bac-to-Bac, flashBAC, BaculoGOLD Bright, BacVector-3000, BacMagic, BacPAK, ecc. Il nostro protocollo si basa sul sistema più comunemente utilizzato in BEVS, il sistema Bac-to-Bac14, che è progettato per trasferire il gene / cDNA che codifica la proteina di interesse (POI, qui i PRMT) nel genoma del baculovirus mantenuto in un ceppo specializzato di E. coli tramite trasposizionesite-specific 15.
In breve, il vettore di trasferimento plasmide contenente il gene di interesse è stato trasformato in cellule competenti DH10Bac E. coli per generare DNA bacmidi virale ricombinante. Le cellule Sf9 aderenti sono state poi trasfette con DNA bacmid. Da quattro a cinque giorni dopo la trasfezione, i baculovirus ricombinanti iniziali secreti nel terreno di coltura cellulare sono stati recuperati ed etichettati come virus P1. Le scorte di baculovirus P1 sono state quindi utilizzate per l'amplificazione del virus (cioè la generazione di stock di baculovirus P2) e lo screening dell'espressione proteica. Sulla base dei risultati dello screening dell'espressione, i virus P2 per il miglior costrutto di espressione della proteina sono stati identificati e utilizzati per generare colture di sospensione di cellule di insetti infettate da baculovirus (SCBIIS) per la produzione di proteine su larga scala. Qui descriviamo i nostri protocolli dettagliati e descriviamo la logica alla base delle nostre scelte di recipienti reagenti e di coltura per supportare la nostra strategia di sviluppo di una metodologia più efficiente in termini di tempo, economica e scalabile per ottenere quantità sufficienti di proteine ricombinanti desiderate.
Protocollo
NOTA: la panoramica dei passaggi del protocollo BEVS è descritta nella figura 1.
1. Generazione di un DNA bacmid ricombinante
- Preparazione di piastre selettive agar LB per la trasformazione DH10Bac
- Preparare piastre di agar LB contenenti: 50 μg/mL di kanamicina, 7 μg/mL di gentamicina, 10 μg/mL tetraciclina, 200 μg/mL Bluo-gal e 40 μg/mL IPTG da selezionare per i trasformatori DH10Bac.
- Pesare 25 g di brodo LB premiscelato e 13 g di Bacto Agar e mettere in pallone da 2 L. Portare il volume a 1 L con acqua distillata e autoclave per 15-30 min a 121 °C.
- Impostare un bagno d'acqua a 50 °C e raffreddare la soluzione di agar autoclavato nel bagno d'acqua per 40-60 minuti fino a quando non viene raffreddato fino a 50-55 °C.
- Alla soluzione raffreddata aggiungere gentamicina ad una concentrazione finale di 7 μg/mL, kanamicina ad una concentrazione finale di 50 μg/mL, tetraciclina ad una concentrazione finale di 10 μg/mL, Bluo-gal ad una concentrazione finale di 200 μg/mL e IPTG ad una concentrazione finale di 40 μg/mL.
- Mescolare la soluzione di agar e aliquota 7-10 mL del mezzo a ciascuna piastra da 60 mm utilizzando una pipetta da 50 mL. Lasciare riposare le piastre a temperatura ambiente (2 ore) per indurirsi. Invertire, avvolgere e conservare a 4 °C. Le piastre contenenti antibiotici sono stabili fino a 4 settimane.
- Trasformazione del plasmide in cellule competenti DH10Bac E. coli
- Calcolare il volume richiesto di celle competenti.
- Scongelare le cellule competenti sul ghiaccio, spingi delicatamente verso il basso e rimospendi indietro toccando delicatamente.
- Utilizzare una pipetta a 12 canali per erogare 4 μL delle cellule in ogni pozzo della piastra PCR a 96 po' .
- Aggiungere ~ 0,3-0,5 μg di DNA plasmide ricombinante alle cellule competenti e mescolare delicatamente toccando. Incubare la miscela sul ghiaccio per 10-15 minuti.
- Shock termico la miscela in una macchina PCR a 42 °C per 45 s. Raffreddare sul ghiaccio per 2 minuti.
- Distribuire 0,5 mL di SOC medio ad ogni pozzo dei blocchi da 96 po '(pozzo profondo 96 2,4 mL).
- Utilizzare una pipetta a 12 canali per trasferire la sospensione batterica trasformata nel pozzo corrispondente del blocco e coprirla con un foglio di airpore.
- Posizionare il blocco in un'incubatrice di scuotimento a 37 °C con agitazione media (205 giri/min) per 4-5 ore.
- Distribuire uniformemente 30-50 μL della coltura sulla superficie della piastra di agar LB utilizzando perline di vetro sterili. Conservare il resto della coltura a 4 °C.
- Incubare le piastre a 37 °C fino a quando il colore delle colonie blu /bianche è percepibile (40-48 h). Scartare la coltura quando si ottengono abbastanza colonie bianche e grandi sul piatto.
- Per garantire che le colonie bianche contengano solo DNA bacmido ricombinante, ristriare una colonia bianca isolata su piastre di agar LB fresche contenenti antibiotici, bluo-gal e IPTG per verificare il fenotipo.
- Incubare per 48 ore a 37 °C.
- Scegli una colonia bianca verificata da una piastra ristriata per l'estrazione del DNA bacmidi ricombinante.
- Isolare il DNA bacmidi ricombinante
- Inoculare una singola colonia bianca isolata in 3 mL di mezzo LB integrata con 50 μg/mL di kanamicina, 7 μg/mL di gentamicina e 10 μg/mL tetraciclina in blocchi da 24 po'(24-ben blocchi di fondo rotondo) e coprire con un foglio di airpore.
- Crescere a 37 °C durante la notte con tremori a 250 giri/min.
- Centrifuga i blocchi da 24 pozzi a 2.100 x g per 10 minuti. Decantare il supernatante, invertire il blocco e toccare delicatamente su una carta velina assorbente. Aggiungere 250 μL della soluzione 1 (soluzione di resopensione cellulare) ad ogni pozzo.
- Sigillare i blocchi con cuscinetti a nastro o qualsiasi altra pellicola di tenuta e posizionarli su una piattaforma di scuotimento a 75 giri/min per 5-10 minuti. Controllare ogni bene per garantire una corretta lisi cellulare e, se necessario, rimescolare, utilizzando una punta da 1 mL.
- Aggiungere 250 μL della soluzione 2 (soluzione di lisi cellulare) ad ogni pozzo, sigillare i blocchi e posizionare su una piattaforma di scuotimento a 75 giri/min per 30 s (per evitare la contaminazione incrociata dei campioni, non invertire blocchi da 24 pozzetti) incubando a temperatura ambiente per 4 minuti.
- Aggiungere 250 μL di soluzione 3 (soluzione di neutralizzazione), sigillare i blocchi e posizionare sulla piattaforma di scuotimento a 75 giri/min per 30 s. Si formerà uno spesso precipitato bianco di proteine e DNA genomico E. coli. Posizionare il campione sul ghiaccio per 10-15 minuti.
- Centrifugare per 60 min a 2.100 x g a 4 °C per pelletare saldamente il materiale precipitato bianco. Durante la centrifugazione, etichettare un nuovo tubo di microcentrifugo e aggiungere 0,8 ml di isopropanolo assoluto.
- Trasferire delicatamente il supernatante sul tubo contenente isopropanolo, evitando qualsiasi materiale precipitato bianco. Mescolare invertendo delicatamente il tubo alcune volte e quindi mettere sul ghiaccio per 5-10 minuti. In questa fase, il campione può essere conservato a -20 °C durante la notte.
- Centrifugare il campione per 15 min a 14.000 x g a 4 °C. Rimuovere il supernatante e aggiungere 0,5 ml di 70% di etanolo a ciascun tubo. Invertire il tubo più volte per lavare il pellet. Centrifuga per 5 min a 14.000 x g a temperatura ambiente. (Facoltativo: lavaggio ripetuto)
- Portare i campioni all'interno della cappa di flusso laminare per garantire la sterilità della preparazione del plasmide e rimuovere il più possibile il supernatante.
NOTA: Il pellet può essere sganciato dal fondo del tubo, quindi guarda attentamente il pellet quando scarti il supernatante. - Asciugare all'aria il pellet all'interno della cappa di flusso laminare per 15-20 minuti e sciogliere il DNA in 50 μL di tampone di eluizione filtrato, 10 mM Tris-Cl, pH 8,5 (assicurarsi che i pellet non siano asciugati in modo troppo secco).
- Poiché il DNA bacmidi ricombinante è di dimensioni superiori a 135 kb, per evitare la tranciatura del DNA, sciogliere il pellet con una maschiatura delicata.
- Per verificare la presenza del gene di interesse nel DNA bacmid, impostare il mix di reazione PCR in una piastra PCR da 96 po '.
- Preparare la miscela PCR come segue: 1 μL di tampone, 0,2 μL (10 mM ciascuno) di dNTP, 0,1 μL di Taq DNA polimerasi, 0,1 μL (25 μM) di primer avanti e indietro (BACV2FWD: tattccggattattcataccg; BACV2REV: ctctacaaatgtggtatggc), 1 μL di DNA bacmide e 8 μL di acqua.
- Eseguire l'amplificazione dei geni bersaglio con denaturazione iniziale per 2 min a 95 °C, seguita da 25 cicli di 94 °C per 30 s, 55 °C per 30 s e 72 °C per 1 min/kb.
- Terminare la reazione dopo un'estensione finale per 7 min a 72 °C.
- Analizzare 10 μL del prodotto di amplificazione su un gel di agarosio 1% (w/v) contenente soluzione di colorazione dell'acido nucleico per elettroforesi.
- Conservare i DNA bacmidi verificati a 4 °C.
2. Generazione di scorte di baculovirus ricombinante
NOTA: Utilizzare cellule Sf9 in crescita esponenziale con una vitalità del 95% o superiore per qualsiasi fase del protocollo di espressione del baculovirus, inclusa la trasfezione cellulare per la generazione di baculovirus, l'amplificazione del volume del baculovirus, lo screening dell'espressione proteica e la produzione di proteine.
- Trasfezione di cellule Sf9 con DNA Bacmid e reagenti di trasfezione (T.R.) come JetPrime o X-tremeGENE 9.
NOTA: La colorazione Trypan Blue e un emocitometro possono essere utilizzati per determinare il numero di cellule vitali e la vitalità delle cellule%. Le cellule non vitali prendono la macchia e appaiono blu al microscopio mentre le cellule vitali rimangono non macchiate. Per calcolare la vitalità delle cellule % , si ottiene un conteggio totale delle celle (non macchiato e macchiato) e il numero di celle vitali viene diviso per il numero totale di celle e moltiplicato per 100.- Diluire le cellule Sf9 in crescita esponenziale a una densità cellulare finale di 4 x 105 cellule /mL in mezzi di insetti liberi dal siero e versare nel serbatoio del reagente sterile.
- Utilizzare una pipetta multicanale programmabile per seminare 0,5 mL delle celle Sf9 diluite in ogni pozzo di una piastra da 24 porri.
- Etichettare un pozzo della piastra come controllo (non trasfetto) e utilizzarlo come controllo per confrontare le cellule trasfette e non trasfette per valutare i potenziali segni di infezioni.
- Dopo aver seminato le cellule nelle piastre, scuotere delicatamente le piastre avanti e indietro più volte per garantire un monostrato uniforme di cellule. Non ruotare le piastre perché le cellule si raggruppano al centro del pozzo.
- Incubare le piastre a 27 °C per almeno 1 h per consentire l'attacco cellulare alle piastre di coltura.
- Mescolare bene il flaconcino reagente di trasfezione. Per ogni trasfezione, aggiungere 2 μL del reagente di trasfezione a 100 μL del buffer di trasfezione. Può essere utilizzato anche qualsiasi altro mezzo di insetto non soppresso. Depositare il reagente di trasfezione diluito in un serbatoio di reagente sterile e mescolare delicatamente per 10 s.
- Utilizzando una pipetta a 12 canali, trasferire 102 μL del reagente di trasfezione diluito in una piastra sterile a 96 microwell.
- Trasferire 10 μL di una soluzione da 0,2 μg/μL di DNA bacmidico ricombinante nel pozzo corrispondente di una piastra microwell da 96 pozzi e mescolare scuotendo delicatamente (toccando) la piastra dai lati.
- Incubare la miscela di trasfezione per 15-20 minuti per consentire una formazione complessa.
- Utilizzando una pipetta regolabile a 6 canali progettata per il trasferimento tra piastre da 96 a 24 poggia, aggiungere la miscela di trasfezione sulle celle dropwise nei pozzi corrispondenti delle piastre di trasfezione e incubare per 4-5 h a 27 °C.
- Scuotere delicatamente le piastre avanti e indietro più volte durante il tempo di incubazione per garantire la distribuzione uniforme della miscela di trasfezione sul monostrato cellulare.
- 4-5 ore dopo la trasfezione, aggiungere 1,5 mL di mezzo privo di siero di insetti integrato con il 10% (v/v) finale di siero bovino fetale inattivato dal calore e antibiotico-antimicotico all'1% (v/v) volume finale (100 unità/mL di penicillina, 100 μg/mL di streptomicina e 0,25 μg/mL di ampotericina B).
- Incubare le cellule in un incubatore di 27 °C per 72-96 ore. Scuotere delicatamente le piastre di trasfezione una volta al giorno quando possibile.
- Cercare i segni di infezione (SOI), evidenti nelle cellule trasfette a 72-96 ore dopo la trasfezione (Figura 2). Tieni presente che le cellule trasfette inizieranno a produrre il virus e infetteranno ulteriormente la coltura; quindi, cerca i segni dell'infezione.
NOTA: I segni di infezione sono cambiamenti strutturali nelle cellule degli insetti, come un aumento del 25-50% del diametro della cellula, nuclei cellulari ingranditi, forma uniformemente arrotondata, perdita di proliferazione e aderenza alla superficie del piatto di coltura, nonché una diminuzione della vitalità cellulare (Figura 2. Baculovirus Cellule Sf9 infette e non infette).
3. Screening dell'espressione proteica su piccola scala e amplificazione del virus
- Infezione delle cellule Sf9 con stock di baculovirus P1.
NOTA: 4-5 giorni dopo la trasfezione, i segni di infezione dovrebbero essere evidenti nelle cellule trasfette rispetto alle cellule di controllo (non trasfette) al microscopio invertito. I baculovirus ricombinanti iniziali secreti nel mezzo di coltura cellulare dovrebbero essere pronti per essere raccolti.- Seme 2 x 105 cellule Sf9 in crescita esponenziale in mezzi di insetti senza siero in ogni pozzo delle piastre a 24 po 'in un volume totale di 2 mL per l'infezione da virus P1 per amplificare il volume del virus (con conseguente generazione dei virus P2).
- Dopo aver pipettato le cellule nelle piastre, scuotere delicatamente le piastre, usando il movimento avanti e indietro per garantire un monostrato uniforme. Non ruotare le piastre perché le cellule si raggruppano al centro del pozzo.
- Incubare le piastre a 27 °C per almeno 1 h per consentire l'aderenza cellulare alla piastra.
- Erogare 4 mL di cellule Sf9 ad una densità di 3,5-4 x 106 in mezzo privo di siero di insetti in ogni pozzo di blocchi da 24 porci da infettare con virus P1 per lo screening dell'espressione proteica.
NOTA: Etichettare un pozzo delle piastre a 24 po 'e blocchi da 24 po 'come controllo e utilizzo come controllo non infetto per il confronto di cellule infette e non infette quando si cerca soi. - Utilizzare un multicanale elettronico programmabile per consentire la raccolta simultanea di virus P1 (fase 2.1.13), l'infezione delle cellule Sf9 appena sementi (fase 3.1.1) e l'infezione delle cellule di sospensione nei blocchi a 24 pozzi (fase 3.1.4) con 150 μL di virus P1.
- Spin down il resto delle scorte virali P1 raccolte per 15 min a 17.970 x g,trasferirle in tubi di microcentrifugo e conservarle al buio a 4 °C.
- Dondolare delicatamente le piastre a 24 pozzi (fase 3.1.1) su uno shaker alternativo per garantire una distribuzione uniforme dei virus P1 aggiunti sul monostrato cellulare; ripetere questo alcune volte durante il tempo di incubazione.
- Coprire i blocchi da 24 pozzi con la coltura di sospensione delle cellule Sf9 infette (fase 3.1.4) con un foglio di airpore.
- Incubare i blocchi di 24 pozzi a 27 °C, tremando a 245 giri/min per 72-96 ore.
- Cercare SOI entro 72-96 ore dopo il tempo di infezione nelle piastre a 24 po 'con virus P2 (passaggio 3.1.1) e nei blocchi da 24 po '(passaggio 3.1.4) con cellule infette per lo screening dell'espressione.
NOTA: 4-5 giorni dopo l'infezione delle cellule Sf9 con virus P1, soi dovrebbe essere evidente nelle cellule infette rispetto alle cellule di controllo non infette sotto un microscopio invertito. - Raccogliere virus P2 da piastre a 24 pozzi, centrifugare per 15 min a 17.970 x g,trasferirli in tubi di microcentrifugo e conservare al buio a 4 °C.
- A 72-96 ore dopo l'infezione, spruzzare sui blocchi da 24 po 'con etanolo al 70%, portare nella cappa di flusso laminare e controllare la densità e la vitalità delle cellule in alcuni pozzi mediante colorazione Trypan Blue.
- Procedere alla purificazione delle proteine se le cellule hanno segni di infezione e la vitalità è vicina al 70-75% come valutato dalla colorazione Trypan Blue.
- Pellettizzare le cellule centrifugando i blocchi di 24 pozzi a 525 x g a 4 °C per 15 minuti. Scartare il supernatante e sospendere completamente i pellet in 1 mL di tampone di lisi composto da 25 mM Tris pH 8.0, 300 mM NaCl, 0,6 % NP-40, 2 mM imidazolo, 5% glicerolo (v/v) e 1x cocktail inibitore della proteasi (cocktail inibitore della proteasi 100x comprende aprotinina 0,25 mg/mL, leupeptina 0,25 mg/mL, pepstatina A 0,25 mg/mL; E-64 0,25 mg/mL).
- Conservare la sospensione cellulare a -80 °C per la successiva purificazione delle prove (vedere 3.2.2).
- Purificazione proteica dalla sospensione cellulare congelata in blocchi di espressione di prova a 24 pozzi.
- Assemblaggio del blocco di associazione (Figura 3).
- Posizionare 3 strati sovrapposti di parafilm sulla parte superiore del blocco del pozzo profondo 96 (pozzo profondo 96 2,4 mL).
- Posizionare una piastra filtrante da 96 polietilene (micropiastra filtrante, 96 polietilene con membrana in polietilene ad altissimo peso molecolare da 25 μm) sulla parte superiore del blocco del pozzo profondo 96.
- Spingere verso il basso la piastra filtrante per fissare le punte nel parafilm per sigillare la piastra filtrante dal blocco profondo 96 punti.
- Trasferire 50 μL di liquame di resina Ni-NTA pre-equilibrato al 50% in ogni pozzo della piastra filtrante.
- Procedura di espressione di test
- Posizionare la sospensione cellulare congelata (fase 3.1.15) presente in blocchi di 24 pozzetti in un bagno d'acqua a RT per 5-10 minuti, quindi agitare a 450 giri/min per 20 minuti.
- Centrifuga i blocchi da 24 pozzi a 3.275 x g per 15 minuti.
- Utilizzando una pipetta multicanale, trasferire i lisati sgombrati in una piastra filtrante contenente 50 μL di liquame in resina Ni-NTA pre-equilibrato (passo 3.2.1.4) e sigillare la piastra filtrante con un tappetino a cappuccio da 96 po '(tappetino a cappuccio da 96 pozzoli, da utilizzare con pozzo quadrato, 2 mL).
NOTA: Utilizzare alcuni elastici per tenere insieme il blocco di legatura durante le fasi di incubazione e centrifugazione. - Posizionare il blocco di legame fissato per 45-60 minuti in un rotatore in una stanza fredda per incubare lisati sgombrato con resina Ni-NTA.
- Dopo l'incubazione, sollevare con cura la piastra filtrante e rimuovere lo strato di parafilm dalla superficie del blocco del pozzo profondo 96 (passaggio 3.2.1.1).
- Riposizionare la piastra filtrante sopra il blocco del pozzo profondo 96 e ruotare verso il basso il blocco di attacco fissato per 2 minuti a 235 x g.
- Legame di lavaggio Resina Ni-NTA 2x con 2 mL di tampone di lavaggio composto da 25 mM Tris pH 8.0, 300 mM NaCl, 5% glicerolo e 15 mM imidazolo.
- Spin giù il blocco con tampone di lavaggio ogni volta per 5 minuti a 235 x g per garantire la completa rimozione del liquido residuo.
- Trasferire la piastra filtrante sulla parte superiore della piastra PCR da 96 pozzi contenente 10 μL di colorante di carico 4x.
- Aggiungere 40 μL di tampone di eluizione (25 mM Tris pH 8.0, 300 mM NaCl, 5% glicerolo, 500 mM imidazolo) ad ogni pozzetti della piastra filtrante e incubare per 5 min.
- Spin giù il blocco per elutare le proteine nella piastra PCR da 96 punti a 235 x g per 10 minuti.
- Sigillare la piastra PCR da 96 pozzi con tap pad resistente alle alte temperature e riscaldare a 98 °C per 3 minuti.
- Caricare 15 μL di campioni di proteine eluitati nel tampone Laemmli standard sul gel SDS-PAGE al 4-20% accanto alla scala proteica ed eseguire il gel con tampone di corsa standard contenente SDS.
- Macchiare il gel con blu Coomassie e de-macchiare con acqua. Analizzare i risultati dell'espressione di test per identificare i migliori costrutti di espressione per la produzione su larga scala.
- Assemblaggio del blocco di associazione (Figura 3).
4. Preparazioni delle cellule di insetti infettate da baculovirus (SCBIIC) per la produzione di proteine
- 4 giorni prima del tempo di produzione programmato, dividere le cellule Sf9 in crescita esponenziale ad una densità cellulare finale di 2 x 106 cellule/mL in 125 mL / 250 mL / 500 mL Erlenmeyer vetro agitare le fiasche con deflettori in 50 mL / 100 mL / 200 mL di mezzo senza siero di insetti contenente 1% (v / v) antibiotico-antimicotico finale.
- Aggiungere 0,150 mL / 0,300 mL / 0,6 mL di virus P2 appropriati, incubare le cellule infette a 165 giri/min su uno shaker orbitale con un colpo di un pollice e ad una temperatura inferiore di 25 °C per rallentare la divisione cellulare.
- A 4 giorni dopo l'infezione, controllare le cellule al microscopio per soi e procedere alla produzione se la vitalità cellulare come verificato con la macchia Trypan Blue è vicina al 70-75%.
5. Preparazioni cellulari Sf9 per la produzione di proteine su larga scala
- 4 giorni prima del tempo di produzione programmato, calcolare il volume richiesto di cellule Sf9 per la produzione di proteine su larga scala.
- Seme 2 L di cellule Sf9 in crescita esponenziale in Mezzo senza siero di insetti ad una densità cellulare di 1 x 106 cellule / mL in 2,8 L Fernbach agitare i fiasche.
- Incubare i contenitori a 27 °C con set di scuotimento a 150 giri/min.
NOTA: Per prevenire la contaminazione batterica nella coltura cellulare sf9, utilizzare la gentamicina ad una concentrazione finale di 10 μg/mL o penicillina/streptomicina rispettivamente a 50 U/mL e 50 μg/mL.
6. Infezione delle cellule Sf9 con SCBIIS per la produzione di proteine su larga scala
- Dividi 2 L o 4 L di cellule Sf9 in crescita esponenziale in Insect Serum-Free Medium fino a una densità cellulare finale di 4 x 106 celle / ml in flaconi di frullato Di tonno da 2,5 L o bottiglie di reagente da 5 L.
- Aggiungere 10-12 mL/L della coltura di sospensione delle cellule di insetti infettate da baculovirus (SCBIIC).
- Incubare la coltura infetta delle cellule Sf9 su uno shaker con 145 giri/min alla temperatura inferiore di 25 °C (per rallentare la divisione cellulare) per 72-96 ore.
- A 72 ore dopo l'infezione, controllare le cellule al microscopio per la SOI e valutare la vitalità cellulare.
- Di solito, dopo circa 72 ore dopo l'infezione, la vitalità delle cellule Sf9 scende al 70%-75% (misurata usando la macchia Trypan Blue). Raccogliere le cellule Sf9 infette in una bottiglia di polipropilene da 1 L centrifugando a 900 x g per 15 min a 4 °C.
- Rimossare il pellet di cellule raccolto da 1 L della coltura cellulare di produzione con 20-25 ml di 1x PBS ruotando delicatamente e traslocando in tubi conici da 50 ml.
- Ruotare la sospensione cellulare a 900 x g per 15 minuti e scartare la soluzione PBS.
- Rimescolare il pellet di cellule lavate con 20-25 mL del tampone di sospensione (20 mM Tris-HCl pH 8.0, 500 mM NaCl, 5% glicerolo, 1x cocktail inibitore della proteasi) e congelamento flash in azoto liquido; conservare a -80 °C fino alla purificazione.
NOTA: Le procedure di purificazione per i PRMT sono state descritte in dettaglio nel documento pubblicato dall'SGC6.
Risultati
Una panoramica del protocollo BEVS è descritta nella figura 1. Più costrutti di espressione di PRMT, tra cui lunghezza intera, domini e frammenti troncati, sono stati generati presso il Structural Genomics Consortium (SGC, Toronto) secondo strategie internamente con il tentativo di aumentare il tasso di successo per identificare proteine solubili e stabili con un livello di espressionerelativamente alto 7,9. I lettori interessati sono incoraggiati a rivedere le definizioni e la metodologia dell'SGC di progettare un "frammento" come segmento della sequenza genica incorporata in un clone dell'espressione, "dominio" come dominio strutturale annotato da PFAM e "costrutto" come il frammento clonato in un vettore di espressione, tutti descritti in dettaglio in una precedente pubblicazione7. I costrutti di espressione dei PRMT presentati in questo protocollo sono per la produzione delle proteine con tag poliistidina clonate nel vettore pFBOH-MHL, che è una derivata del vettore pFastBac1. Nella figura 4,presentiamo l'analisi SDS-PAGE dei costrutti solubili con tag His di PRMT1, 2, 4-9 purificati da pellet raccolti dopo 4 mL di produzione in celle Sf9 (fase 3.1.4). PRMT1 e PRMT9 a lunghezza intera (FL) non sono presentati in questo gel, poiché FL PRMT1 è stato prodotto da E. colie FL PRMT9 prodotto da BEVS è stato purificato da Flag-tag6. I costrutti troncati di PRMT1, FL PRMT4 e tutti i costrutti PRMT8 mostrano una resa relativamente elevata, ma gli eluati proteici contengono frazioni di contaminanti co-purificati. Questi costrutti richiedono un'ulteriore ottimizzazione dei protocolli di purificazione. Sono quindi necessari ulteriori approcci per migliorare la purezza di queste proteine da produzioni scale-up, come una riduzione della quantità di perline di nichel nella fase dell'incubazione con un lisato chiarificato; un aumento delle concentrazioni di imidazolo nei tamponi di lavaggio; scissione della His-tag con proteasi TEV, seguita da applicazione su una resina ni-affinità; e, ulteriori passaggi di purificazione come l'esclusione delle dimensioni e la cromatografia a scambio ionico. I costrutti di PRMT2 mostrano una resa significativamente inferiore rispetto ad altre proteine e proteine PRMT2 a figura intera accompagnate da una forte banda di contaminanti. La produzione scale-up e due fasi di purificazione come IMAC e l'esclusione delle dimensioni hanno confermato un basso livello di espressione per questo costrutto insieme alla presenza persistente del contaminante co-purificante per la proteina FL. Proteine pure sono state ottenute per il complesso PRMT5 prodotto e purificato con il suo partner legante obbligato, MEP50. Il costrutto troncato di PRMT9 ha un livello di espressione inferiore di quasi due o tre volte, vicino a 1,5 mg/L, rispetto ad altri PRMT. Tuttavia, le scorte virali ricombinanti di questo costrutto sono state utilizzate per la produzione in scala, sono stati ottenuti cristalli diffrazione e la struttura è stata risolta per questa proteina insieme a PRMT4, 6 e 7(Figura 5).
Per le produzioni scale-up, i corrispondenti virus P2 sono stati utilizzati per infettare la coltura di sospensione delle cellule di insetti Sf9. Questo passaggio genera 50/100/200 mL di cellule infettate da baculovirus contenenti cellule infette e virus P3 nel supernatante. Per la produzione di proteine su larga scala, 2 L di cellule Sf9 sono state coltivate in ciascuno dei flaconi di frullato Fernbach da 2,8 L a 150 giri/min, 27 °C(figura 6). Il giorno della produzione, 2 L di cellule Sf9 (vitalità cellulare > 97%) in flaconi di frullato 2.5 L Tunair o 4 L in bottiglie di reagente da 5 L sono stati diluiti ad una densità cellulare di 4 x 106/ml. Queste cellule sono state infettate direttamente con 10-12 mL/L di coltura di sospensione di cellule di insetti infettate da baculovirus e incubate a una temperatura abbassata di 25 °C, a 145 giri/min. L'infezione del lotto di produzione direttamente con una coltura di sospensione di cellule di insetti infettate da baculovirus ha ridotto significativamente le fasi laboriose e dispendiose in termini di tempo nell'amplificazione del volume del virus, escludendo la gestione extra delle cellule infette, ed ha evitato la riduzione della degradazione del formicolio e del virus. La manutenzione della coltura cellulare SF9 e la produzione in scala sono state fatte nei recipienti di coltura ad alto volume di riempimento per adottare una produzione proteica su larga scala in un unico lotto(figura 6).
Prmt 4, 5 (in complesso con MEP50), 6, 7 e 9 proteine prodotte dalla piattaforma di produzione mediata da Baculovirus sono state utilizzate per la caratterizzazione cinetica e lo screening del composto inibitore presso l'SGC6. Le strutture cristalline sono state risolte e depositate nella Protein Data Bank (PDB) per le forme a tutta lunghezza o troncate delle proteine PRMT 4, 6, 7 e 9 con varie sonde chimiche e inibitori. I plasmidi di espressione per questi PRMT sono stati depositati nel repository plasmide Addgene (Addgene è un partner di distribuzione dell'SGC, https://www.addgene.org/) e sono disponibili per la comunità di ricerca(Figura 5).
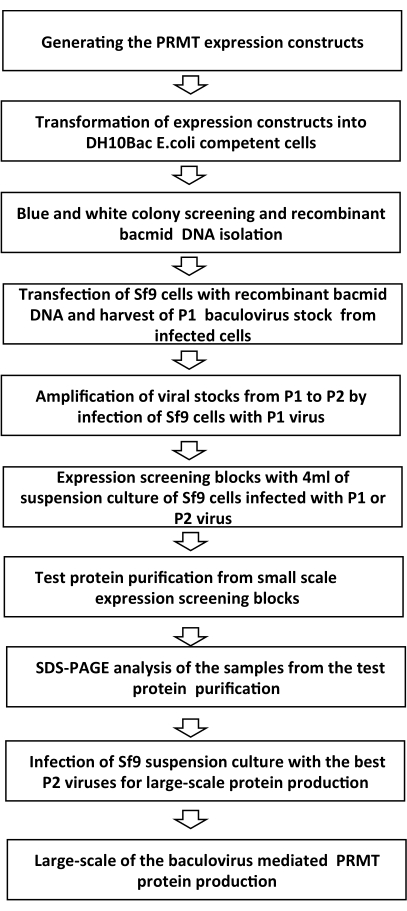
Figura 1: Panoramica schematica dei passaggi del processo di espressione del baculovirus Fare clic qui per visualizzare una versione più ampia di questa figura.

Figura 2: Baculovirus Cellule Sf9 infette e non infette. I segni di infezione sono cambiamenti strutturali nelle cellule degli insetti, come un aumento del 25-50% del diametro della cellula, nuclei cellulari ingrossati, forma uniformemente arrotondata, perdita di proliferazione e aderenza alla superficie del piatto di coltura, nonché una diminuzione della vitalità cellulare. Barra in scala bianca 200 μm. I segni di infezione presentati qui sono gli stessi per le cellule trasfette utilizzando sia reagenti di trasfezione, JetPrime e X-tremeGene 9. L'esempio specifico mostrato è per il reagente di trasfezione JetPrime. (A) Celle Sf9 non infette come controllo. (B) Cellule Sf9 infettate da Baculovirus. Clicca qui per visualizzare una versione più grande di questa figura.

Figura 3: Assemblaggio di piastre leganti per una rapida purificazione delle proteine di espressione di prova. Si prega di vedere il testo per i dettagli, passaggi 3.2.1-2 Fare clic qui per visualizzare una versione più grande di questa figura.
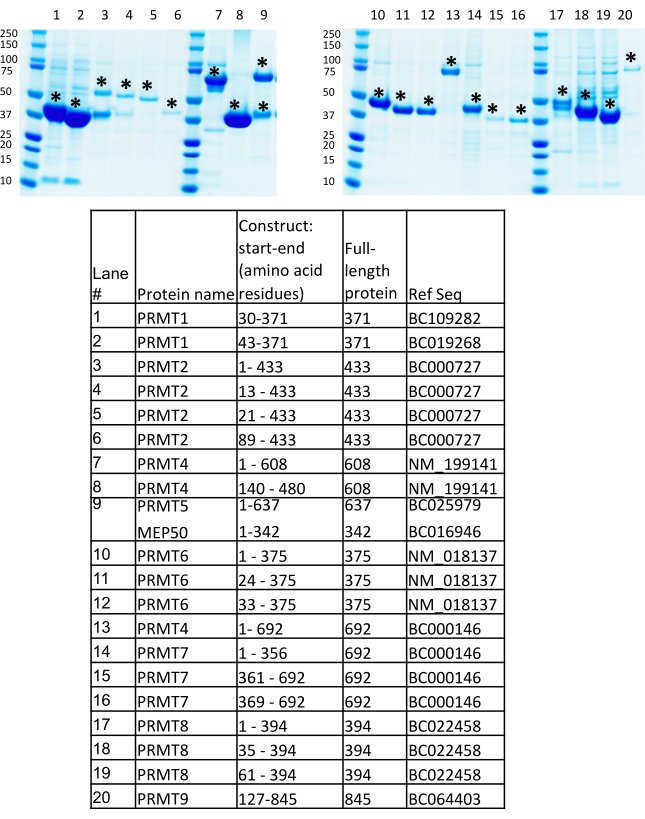
Figura 4 :Risultati dello screening dell'espressione proteica. Risultati dello screening dell'espressione proteica della produzione di proteine mediate da baculovirus in 4 mL di coltura di sospensione Sf9 infettati da corrispondenti virus ricombinanti P1 per diversi PRMT e il complesso PRMT5-MEP50. Clicca qui per visualizzare una versione più grande di questa figura.
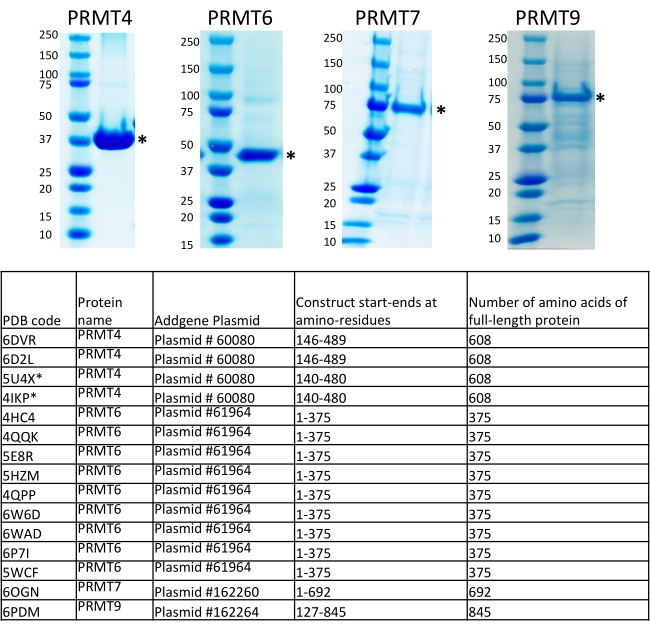
Figura 5: Riepilogo dei costrutti di espressione per PRMT4, 6, 7 e 9 utilizzati per gli studi sulla struttura cristallina presso il Structural Genomics Consortium di Toronto (SGC). Le strutture cristalline sono state risolte e depositate nella Protein Data Bank (PDB) per l'intera lunghezza o forme troncate di proteine PRMT 4, 6, 7 e 9 con varie sonde chimiche e inibitori. I plasmidi di espressione per questi PRMT sono stati depositati nel repository plasmide Addgene e sono disponibili per la comunità di ricerca (Addgene è un partner di distribuzione dell'SGC, https://www.addgene.org/). Clicca qui per visualizzare una versione più grande di questa figura.

Figura 6: Mantenimento delle cellule di insetti Sf9 e produzione di proteine nei diversi recipienti di coltura: (A) 2.8 L Fernbach flask per il mantenimento delle cellule e la produzione di proteine. L'uso del 72% fill-volume aumenta la velocità di produzione di 2,5 volte in una piattaforma di scuotimento. (B)Le fiasche di frullato Tunair (in questa immagine sono presentati solo 9 mastri su 10) e le bottiglie di reagente con un volume di riempimento dell'80% aumentano drasticamente la capacità produttiva della piattaforma di scuotimento. Clicca qui per visualizzare una versione più grande di questa figura.
Discussione
Uno dei vantaggi del BEVS nelle cellule di insetti si concentra sulla capacità dei macchinari di modifica post-traslazionale di consentire modifiche più complesse come fosforilazione, miristoilazione e glicosilazione. Insieme al ripiegamento altamente efficiente delle proteine dei mammiferi, queste modifiche facilitano elevate quantità di proteine modificate e piegate adatte a esperimenti a valle fisiologicamente rilevanti16.
Qui, abbiamo descritto protocolli dettagliati del BEVS che enfatizzano elementi critici per lo screening di espressioni di successo di costrutti multipli di proteine PRMT e produzione di proteine PRMT su larga scala nella piattaforma di espressione baculovirus: 1) L'uso di pipette multicanale regolari, regolabili e programmabili per trasferire i materiali biologici tra 24 e 96 - piastre e blocchi di coltura cellulare del pozzo nelle fasi della generazione di DNA bacmid e virus; una raccolta dei virus ricombinanti, l'amplificazione dei volumi virali dei virus ricombinanti e la preparazione dei blocchi di screening dell'espressione proteica. 2) Reagenti di trasfezione ad alte prestazioni ed economici per la generazione di virus ricombinanti. 3) Coltura di sospensione delle cellule di insetti infettate da baculovirus (SCBIIC) per la produzione di proteine su larga scala. 4) Utilizzo di fusti a frullato Ad alto volume 2.8 L Fernbach per mantenere la coltura di sospensione Sf9 e flaconi di frullato 2.5 L Tunair e bottiglie reagenti da 5 L per la produzione di proteine su larga scala.
Considerazioni speciali e motivazioni per le fasi di trasformazione e trasfezione.
Sebbene un protocollo commerciale raccomandi l'utilizzo di 100 μL di cellule competenti per unatrasformazione 14, l'efficienza di trasformazione delle cellule commerciali competenti DH10Bac E. coli è fino a 1 x 108 cfu / μg di DNA, quindi usiamo solo 4 μL. Questo è sufficiente per ogni trasformatore per ottenere colonie ricombinanti bianche isolate per l'isolamento del DNA bacmidi. Le cellule Sf9 aderenti nella piastra di trasfezione a 24 pompenti sono state sementi ad una densità cellulare di 2 x10 5 / mL in 0,5 mL di supporti per insetti senza siero. Questo volume è sufficiente per garantire una copertura uniforme della superficie di lavoro del pozzo. Allo stesso tempo, non diluizza troppo il mix di trasfezione, il che migliora l'efficienza di trasfezione. I reagenti di trasfezione non sono tossici per le cellule Sf9 e lo scambio di media non è necessario. Invece di un cambiamento dei supporti, altri 1,5 mL di supporti contenenti 10% (v/v) FBS vengono aggiunti nella piastra di trasfezione a 4-5 ore dopo il trasfezione per facilitare la crescita cellulare. L'efficienza di trasfezione di entrambi i reagenti di trasfezione è elevata. Tuttavia, con X-tremeGene 9, i segni di infezione nelle cellule trasfette (Figura 2) appaiono 10-12 ore prima rispetto al reagente JetPrime, quindi scegliamo tra questi reagenti a seconda del programma di lavoro dei passaggi successivi nei protocolli, che fornisce una certa flessibilità nel processo complessivo.
Lo screening dell'espressione del test proteico può essere impostato con virus P2 se la quantità dei virus ricombinanti iniziali, raccolti dalla piastra di trasfezione ed etichettati come P1, è un fattore limitante da utilizzare per lo screening dell'espressione proteica.
Considerazioni quando si sposta da volumi di cultura di piccole e grandi dimensioni.
Storicamente, si credeva che una crescita ottimale delle cellule richiedesse un elevato spazio aereo nella coltura delle sospensioni della manutenzione cellulare sf9 e delle produzioni in scala. Tuttavia, nel 2014, è stato riferito che l'alto spazio aereo nelle navi da coltura è meno critico di quanto si pensassein precedenza 17. Un contenitore di coltura impostato utilizzando una velocità di scuotimento opportunamente regolata al lancio orbitale della piattaforma di scuotimento fornirà un trasferimento di ossigeno sufficiente anche nella coltura di sospensioni ad alto volume di riempimento creando e mantenendo piccole bolle d'aria per un tempo più lungo. Con questo approccio, le cellule di insetti disponibili in commercio possono essere coltivate a una velocità di scuotimento più elevata entro un intervallo normale del tempo di raddoppio delle cellule senza sacrificare l'elevata vitalità cellulare.
Così, 6 anni fa, abbiamo iniziato ad aumentare il volume della coltura delle sospensioni in un pallone tremante durante il mantenimento delle cellule e abbiamo introdotto un diverso tipo di recipiente di coltura per la produzione di proteine regolando e monitorando le condizioni discuotimento (Figura 6). Per stabilire condizioni ottimali in questi vasi di coltura, abbiamo monitorato i parametri di coltura cellulare Sf9 come il tempo di raddoppio delle cellule insieme alla vitalità, alle dimensioni e alla forma delle cellule, allo stato di aggregazione e all'infettibilità delle cellule.
Ad esempio, per la manutenzione delle cellule Sf9, nei flaconi a scossa di Fernbach da 2,8 L, coltiamo 2 L invece di 0,8 L delle cellule di sospensione Sf9 che tremano a 150 giri/min a 27 °C e la vitalità cellulare la maggior parte delle volte è vicina al 99%, con cellule divisorie sane di forma uniforme. Per la produzione in scala, infettiamo 4 L di celle in bottiglie di reagente da 5 L che tremano ad alta velocità come 145 giri/min ad una temperatura ridotta di 25 °C. Gli incubatori più comunemente utilizzati con una piattaforma di scuotimento integrata possono contenere flaconi di scuotimento da 6 x 2,8 L o bottiglie di reagente da 6 x 5 L o flaconi di frullato Tunair da 10 x 2,5 L. Pertanto, la capacità dell'unica piattaforma di scuotimento, se riempiamo le fiasche di scuotimento Fernbach e le bottiglie di reagente a 1/3 rispetto al volume ad alto riempimento dei vasi è di 4,8 L contro 12 L usando flaconi di frullato Fernbach da 2,8 L e 10 L contro 24 L usando bottiglie di reagente da 5 L(Figura 6). La manutenzione della coltura delle celle a sospensione e la produzione in scala mobile nei vasi da coltura ad alto volume di riempimento ci hanno aiutato a superare i limiti dei volumi di produzione e ad adottare una piattaforma su larga scala. Pertanto, questo è molto utile per i laboratori senza accesso ai bioreattori e / o spazio limitato nelle pipeline di produzione.
Questo protocollo potrebbe essere prontamente adattato per la produzione e la purificazione di costrutti proteici con diversi tag di affinità utilizzando resine appropriate e modificando i tamponi di purificazione come descritto nel documento pubblicato dall'SGC6 per le proteine a figura intera contrassegnate con bandiera di PRMT4, 7, 9 e il complesso PRMT5-MEP50 e PRMT6 contrassegnato con isto. Sebbene descriviamo un protocollo BEVS per la famiglia di proteine PRMT, lo stesso approccio può essere applicato a qualsiasi altra famiglia proteica.
Divulgazioni
Gli autori non dichiarano alcun conflitto di interessi.
Riconoscimenti
Gli autori desiderano ringraziare Dalia Barsyte-Lovejoy per aver preso il tempo necessario per fornire preziosi feedback e commenti critici sul manoscritto e tutti i nostri colleghi SGC che hanno lavorato con la famiglia di proteine PRMT espressa dal Baculovirus Expression Vector System.
L'SGC è un ente di beneficenza registrato (numero 1097737) che riceve fondi da AbbVie, Bayer AG, Boehringer Ingelheim, Genentech, Genome Canada attraverso l'Ontario Genomics Institute [OGI-196], l'UE e l'EFPIA attraverso l'Impresa Comune Innovative Medicines Initiative 2 [sovvenzione EUbOPEN 875510], Janssen, Merck KGaA (alias EMD in Canada e negli Stati Uniti), Pfizer, Takeda e wellcome trust [106169/ZZ14/Z].
Materiali
| Name | Company | Catalog Number | Comments |
| 2.8L Nalgene Fernbach Culture Flask, Polycarbonate, | Nalgene | 29171-854 | For large scale maintenance of suspension culture of Sf9 cells |
| 24-Well Blocks RB | Qiagen | 19583 | For incubation of 4ml of suspension Sf9 cells for protein expression screening |
| 4-20 Criterion TGX Gel 26W 15 ul | Biorad | 5671095 | For SDS-PAGe analysis of the purified proteins |
| 50ml Reagent Reservoir | Celltreat Scientific Products | 229290 | Reservoir used for diluted transfection reagent and Sf9 cells suspension |
| 96-well cap mat, for use with square well, 2 mL | Greiner Bio-One | 381080 | Used to cover 96 well block |
| 96 well PCR plate | Eppendorf | 30129300 | |
| Bacto agar | BD | 214010 | For LB-agar selection paltes |
| Airpore Tape Sheets | Qiagen | 19571 | To cover 24 well blocks for protein expression screening |
| Allega X-15R Centrifuge | Beckman Coulter | 392932 | |
| Antibiotic Antimycotic (100x) | Gibco | 15240112 | |
| Bacmid DNA | in-house | non-catalog item | Bacmid DNA for baculovirus production |
| Bluo-Gal, 1g | Thermo Fisher | 15519028 | |
| Beckman JLA 8.1000 | |||
| Cell Culture Plates, 24-Well, with lid, flat bottom, sterile | Eppendorf | 30722116 | Tissue culture treated plate |
| Cell Resuspension Solution 0.5 L | Millipore Sigma | LSKCRS500 | For Bacmid DNA extraction |
| Cell Lysis Solution 0.5 L | Millipore Sigma | LSKCLS500 | For Bacmid DNA extraction |
| CELLSTAR Tissue Culture Plates, 96 well | Greiner Bio-One | 655180 | For transfection mix |
| ClipTip 1250, filter reload, sterile | ThermoFisher Scientific | 94420818 | Tips for programmable and adjustable multichannel pipette |
| dNTP Mix (25 mM each) | Thermo Fisher Scientific | R1121 | |
| E1-ClipTip Electronic Adjustable Tip Spacing Multichannel Equalizer Pipette, 15 to 1250 μL | ThermoFisher Scientific | 4672090BT | Programmable and adjustable multichannel pipette |
| E4 XLS adjustable spacer 6-channel pipette, 20-300 μL | Ranin | LTS EA6-300XLS | Ranin adjustable multichannel pipette |
| Filter microplate, 96-well, polypropylene, with 25 µm ultra high molecular weight polyethylene membrane | Agilent | 201005-100 | For protein purification in expression screening |
| Full-Baffle Flask Kit Tunair, 2.5L | IBI Scientific | SS-6003C | For large scale protein production in suspension culture of SF9 cells |
| Gentamicin 10x10ml | BioShop | 15750078 | |
| Heat Inactivated Fetal Bovine Serum | Wisent Biocenter | 080-450 | |
| I-Max Insect Media W/ L-Glutamine, 1 L | Wisent Biocenter | 301-045-LL | Serum free insect cells growth medium |
| InstantBlue, Ultrafast Protein Stain | Expedeon Protein Solutions | ISB1L-1L | For protein gel (SDS-PAGE) staining |
| Iptg, Ultra Pure, Dioxane Free, Min 99.5% | BioShop | IPT001.100 | |
| JetPRIME Transfection Reagent Provided with jetPRIME buffer | POLYPLUS TRANSFECTION Inc | 114-01 | For Sf9 cells transfection to generate baculovirus |
| Kanamycin Monosulfate | BioShop | KAN201.100 | |
| Lb Broth (Lennox), Powder Microbial Gro& | Sigma | L3022-1KG | |
| Masterblock 96 deep well 2.4mL | Greiner Bio-One | 780285-FD | Used in the transformation and expression screening procedures |
| Max Efficiency DH10Bac Competent Cells , 0.5ml | Thermo Fisher | 10361012 | Competent cells for bacmid DNA generation |
| mLINE 12-Channel Pipette, adjustable 30 - 300 uL | Sartorius | Sartorius 725240 | 12 channel pipette |
| Neutralization Solution, 0.5 L | Millipore Sigma | LSKNS0500 | For bacmid DNA extraction |
| New Brunswick Innova 44R, 120V, orbit 2.5 cm (1 in) | Eppendorf | M1282-0004 | Shaker incubator for incubaion of suspension of Sf9 cells |
| Ni-NTA Agarose | Qiagen | 30250 | For protein purification |
| Penicillin-Streptomycin (10,000 U/mL) | Gibco | LS15140122 | |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 500ml | Pyrex | 4444-500 | For suspension culture of Sf9 cells |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 125ml | Pyrex | 4444-125 | For suspension culture of Sf9 cells |
| PYREX Delong Shaker Erlenmeyer Flask with Baffles, Corning 250ml | Pyrex | 4444-250 | For suspension culture of Sf9 cells |
| RedSafe Nucleic Acid Staining Solution | Froggabio | 21141 | |
| RNase A, 0.9 mL | Millipore Sigma | LSKPMRN30 | For suspension buffer for bacmid DNA extraction |
| Roll & Grow Spherical Glass Plating Beads | MP Biomedicals | 115000550 | For spread of bacterial cells across the surface of an agar plate. |
| RT-LTS-A-300μL-768/8 (tips) | Ranin | 30389253 | Tips for ranin multichannel pipette |
| S.O.C. Medium | Thermo Fisher Scientific | 15544034 | |
| Serum, Cell Culture, Fetal Bovine Serum (Fbs), Hyclone, Characterized Canadian | cytivalifesciences | SH3039602 | Addition to the serum free medim for the transfected cells |
| Sf9 cells | Thermo Fisher | 12659017 | Insect cells |
| Sfx-Insect Cell Culture Media | Cytiva (Formerly GE Healthcare Life Sciences) | SH3027802 | Serum free insect cells growth medium |
| Tape Pad | Qiagen | 19570 | Tape Pad |
| Taq DNA Polymerase with ThermoPol Buffer - 2,000 units | New England Biolabs | M0267L | |
| Tetracycline Hcl | BioShop | TET701.10 | |
| Trypan Blue 0.4% Solution | Gibco | 15250061 | For assessment of cell viability |
| VITLAB Reagent Bottles, PP with Screw Caps, PP, BrandTech, 5L | VITLAB | V100889 | For large scale protein production in suspension culture of Sf9 cells |
| VWR Digital Mini Incubator | VWR | 10055-006 | Incubator for adherent Sf9 cells |
| VWR Incubating Microplate Shaker | VWR | 97043-606 | Incubator for suspension culture of Sf9 cells in 24 well blocks |
| VWR Petri Dishes | VWR | CA73370-037 | |
| X-tremeGene 9 DNA Transfection Reagent 1.0 M | Roche | 6365787001 | For Sf9 cells transfection to generate recombinant baculovirus |
Riferimenti
- Guccione, E., Richard, S. The regulation, functions and relevance of arginine methylation. Nature Reviews in Molecular Cell Biology. 20 (10), 642-657 (2019).
- Thandapani, P., O'Connor, T. R., Bailey, T. L., Richard, S. Defining the RGG/RG motif. Molecular Cell. 50 (5), 613-623 (2013).
- Lorton, B. M., Shechter, D. Cellular consequences of arginine methylation. Cell and Molecular Life Sciences. 76 (15), 2933-2956 (2019).
- Bedford, M. T., Clarke, S. G. Protein arginine methylation in mammals: Who, what, and why. Molecular Cell. 33 (1), 1-13 (2008).
- Frankel, A., Brown, J. I. Evaluation of kinetic data: What the numbers tell us about PRMTs. Biochimica Biophysica Acta Proteins Proteomics. 1867 (3), 306-316 (2018).
- Li, A. S. M., Li, F., Eram, M. S., Bolotokova, A., Dela Seña, C. C., Vedadi, M. Chemical probes for protein arginine methyltransferases. Methods. 175, 30-43 (2020).
- Savitsky, P., et al. High-throughput production of human proteins for crystallization: The SGC experience. Journal of Structural Biology. 172, 3-13 (2010).
- Gileadi, O., et al. Expressing the human proteome for affinity proteomics: Optimizing expression of soluble protein domains and in vivo biotinylation. New Biotechnology. 29 (5), 515-525 (2012).
- Graslund, S., et al. Protein production and purification. Nature Methods. 5, 135 (2008).
- Kost, T. A., Condreay, J. P., Jarvis, D. L. Baculovirus as versatile vectors for protein expression in insect and mammalian cells. Nature Biotechnology. 23, 567-575 (2005).
- Jarvis, D. L. Baculovirus-insect cell expression systems. Methods in Enzymology. 463, 191-222 (2009).
- Shrestha, B., et al. Baculovirus expression vector system: an emerging host for high-throughput eukaryotic protein expression. Methods in Molecular Biology. 439, 269-289 (2008).
- Smith, G. E., Summers, M. D., Fraser, M. J. Production of human beta interferon in insect cells infected with a baculovirus expression vector. Molecular Cell Biology. 3, 2156-2165 (1983).
- Invitrogen Life Technologies. . Invitrogen, Bac-to-Bac Baculovirus expression system. , (2010).
- Luckow, V. A., Lee, S. C., Barry, G. F., Olins, P. O. Efficient generation of infectious recombinant baculoviruses by site-specific transposon-mediated insertion of foreign genes into a baculovirus genome propagated in Escherichia coli. Journal of Virology. 67, 4566-4579 (1993).
- Irons, S. L., Chambers, A. C., Lissina, O., King, L. A., Possee, R. D. Protein Production Using the Baculovirus Expression System. Current Protocol in Protein Sciences. 91, 1-22 (2018).
- Rieffel, S., et al. Insect cell culture in reagent bottles. MethodsX. 1, 155-161 (2014).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon