Method Article
Utilizzo degli embrioni di pesce zebra Tg(Vtg1:mcherry) per testare gli effetti estrogenici dei composti interferenti endocrini
In questo articolo
Riepilogo
Presente qui è un protocollo dettagliato per l'uso di embrioni di pesce zebra Tg(vtg1: mCherry) per il rilevamento di effetti estrogenici. Il protocollo riguarda la propagazione del pesce e il trattamento degli embrioni e sottolinea il rilevamento, la documentazione e la valutazione dei segnali fluorescenti indotti da composti interferenti endocrini (EDC).
Abstract
Ci sono molti composti interferenti endocrini (EDC) nell'ambiente, soprattutto sostanze estrogeniche. L'individuazione di queste sostanze è difficile a causa della loro diversità chimica; pertanto, vengono utilizzati metodi sempre più di rilevamento degli effetti, come gli organismi biomonitor/bioindicatori sensibili all'effetto estrogenico. Questi organismi di biomonitoraggio includono diversi modelli di pesce. Questo protocollo riguarda l'uso del pesce zebra Tg(vtg1: mCherry) linea transgenica come organismo di biomonitoraggio, compresa la propagazione dei pesci e il trattamento degli embrioni, con particolare attenzione al rilevamento, alla documentazione e alla valutazione dei segnali fluorescenti indotti dall'EDC. L'obiettivo del lavoro è la dimostrazione dell'uso degli embrioni di linea transgenica Tg(vtg1: mCherry) per rilevare gli effetti estrogenici. Questo lavoro documenta l'uso di embrioni transgenici di pesce zebra Tg(vtg1: mCherry) per il rilevamento di effetti estrogenici testando due sostanze estrogeniche, . Il protocollo descritto è solo una base per la progettazione di saggi; il metodo di test può essere variato in base agli endpoint di test e ai campioni. Inoltre, può essere combinato con altri metodi di analisi, facilitando così l'uso futuro della linea transgenica.
Introduzione
C'è un numero significativo di composti interferenti endocrini (EDC) che sono tra le sostanze più pericolose nel nostro ambiente. Questi sono principalmente composti estrogenici che contaminano l'acqua dalle risorse naturali. La diversità chimica delle sostanze appartenenti al gruppo rende difficile la verifica della loro presenza, in quanto sono necessari diversi metodi analitici per la loro rilevazione. Sulla base della loro struttura chimica è molto difficile determinare se una sostanza è effettivamente in grado di agire come un estrogeno. Inoltre, queste sostanze non sono mai presenti in forma pura nell'ambiente, quindi i loro effetti possono essere influenzati da altri composti, troppo1. Questo problema può essere risolto con metodi di rilevamento degli effetti, come l'uso di organismi biomonitor/bioindicator che mostrano effetti estrogenici2,3,4,5.
Recentemente, una varietà di linea cellulare6 e sistemi di test a base di lievito2,3 sono stati sviluppati per rilevare gli effetti estrogenici. Tuttavia, questi sono generalmente solo in grado di rilevare il legame della sostanza al recettore estrogeno2,3. Inoltre, non sono in grado di modellare processi fisiologici complessi nell'organismo o di rilevare fasi ormone-sensibili delle fasi della vita; così, spesso portano a risultati falsi.
È noto che alcuni geni reagiscono in modo sensibile agli estrogeni negli organismi viventi7. La rilevazione di prodotti genici mediante metodi di biologia molecolare è possibile anche a livello di proteina o mRNA8,9, ma di solito comporta il sacrificio animale. Le leggi sulla protezione degli animali sono diventate più severe e vi è una crescente domanda di sistemi di prova alternativi che riducano al minimo il numero e la sofferenza degli animali utilizzati negli esperimenti o nella sostituzione del modello animale con un altro sistema modello10. Con la scoperta delle proteine fluorescenti e la creazione di linee di biomarcatori, le tecnologie transgeniche forniscono una buona alternativa11. Con queste linee, l'attivazione di un gene estrogeno-sensibile può essere testata in vivo.
Tra i vertebrati, il potenziale dei pesci nella valutazione del rischio ambientale è eccezionale. Offrono molti vantaggi rispetto ai modelli di mammiferi: essendo organismi acquatici, sono in grado di assorbire gli inquinanti attraverso tutto il loro corpo, produrre un gran numero di prole, e alcune delle loro specie sono caratterizzate da tempi di breve generazione. Il loro sistema endocrino e i processi fisiologici mostrano grandi somiglianze con altri vertebrati e anche con i mammiferi, compresi gli esseri umani12.
Diversi geni per il rilevamento degli effetti estrogenici nei pesci sono noti anche. I più importanti sono i recettori degli estrogeni aromatasi-b, choriogenin-H, e vitellogenina (vtg)7,13. Recentemente, sono state create diverse linee di biosensori che producono estrogeni anche da modelli di pesce utilizzati in laboratorio, come dal pesce zebra (Danio rerio)4,5,14,15,16,17. Il vantaggio principale del pesce zebra nella creazione di linee biosensori è il corpo trasparente degli embrioni e delle larve, perché il segnale fluorescente del reporter può quindi essere facilmente studiato in vivo senza sacrificare l'animale10. Oltre alla protezione degli animali, è anche una caratteristica preziosa in quanto consente di studiare la reazione dello stesso individuo in diversi momenti del trattamento18.
Questi esperimenti utilizzano una vitellogenina reporter transgenico zebrafish line15. Il costrutto transgene utilizzato per lo sviluppo di Tg(vtg1:mCherry) ha un lungo (3,4 kbp) promotore di vitellogenina-1 naturale. Il recettore degli estrogeni (ER) è una proteina potenziatore attivata dai ligando che è un rappresentante della superfamiglia di recettori steroide/nucleare. ER si lega a sequenze specifiche di DNA chiamate elementi di risposta degli estrogeni (ERE) con alta affinità e trasattiva l'espressione genica in risposta a estradiolo e altre sostanze estrogeniche, quindi più ERE nel promotore provoca una risposta più forte19. Ci sono 17 siti ERE nella regione promotrice del costrutto transgene Tg(vtg1:mCherry) e si prevede che imitano l'espressione del gene nativo vtg15. C'è un'espressione continua del segnale fluorescente nelle femmine sessualmente maturate. Tuttavia, nei maschi e nell'embrione l'espressione nel fegato è visibile solo dopo il trattamento con sostanze estrogeniche (Figura 1).
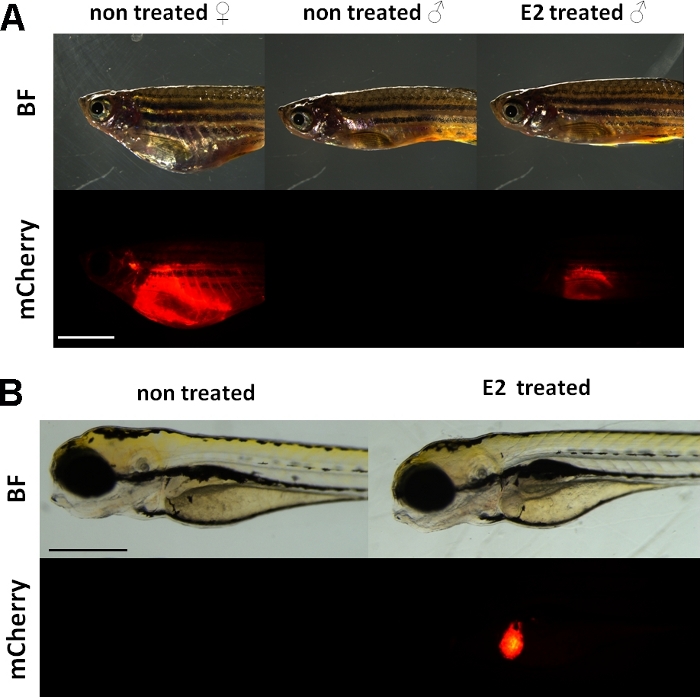
Figura 1: segnale fluorescente rosso nel fegato del pesce zebra adulto transgenico mcherry e 5 embrioni dpf, dopo l'induzione di 17-estradiolo (E2). Nella femmina e nel maschio trattata con E2 (tempo di esposizione E2:48 ore) la forte fluorescenza del fegato è visibile anche attraverso la pelle pigmentata. Nessun segnale fluorescente è visibile nel maschio non trattato (A). Dopo l'induzione di E2 (50 g/L tempo di esposizione: 0-120 hpf), si può osservare anche un segnale fluorescente rosso nel fegato di 5 embrioni dpf, che non è visibile negli embrioni di controllo (B). Mentre il segnale fluorescente è continuamente presente nelle femmine adulte, principalmente i maschi e gli embrioni della linea sono adatti per rilevare gli effetti estrogenici. (BF: campo luminoso, mCherry: visualizzazione filtro fluorescente rosso, singole immagini semplici, barra della scala A: 5mm, barra della scala B: 250 m) Fare clic qui per visualizzare una versione più grande di questa figura.
Simile alla vitellogena endogena, il reporter mCherry è espresso solo nel fegato. Poiché la vitellogenina viene prodotta solo in presenza di estrogeni, non c'è segnale fluorescente nei controlli. Poiché l'espressione è solo nel fegato, la valutazione dei risultati è molto più facile15.
La sensibilità e l'usabilità degli embrioni di questa linea sono state studiate su varie miscele composte estrogeniche e anche su campioni ambientali15,20e nella maggior parte dei casi sono state documentate relazioni dose-risposta (Figura 2). Tuttavia, nel caso di sostanze altamente tossiche, principalmente epatossiche (ad esempio, zearalenone), solo un segnale fluorescente molto debole può essere visibile nel fegato degli embrioni trattati e il segnale fluorescente massimo causato dall'interno di una gamma di concentrazione molto piccola, il che rende difficile stabilire relazioni effetto dose20.

Figura 2: Diagramma dose-risposta (A) e immagini fluorescenti (mCherry) del fegato (B) esposte a 17-ethynilestradiol (EE2), in 5 dpf vtg1:mCherry larve. I risultati sono espressi come densità integrata generata dalla forza del segnale e dalle dimensioni dell'area interessata (SEM, n - 60). 100% si riferisce al massimo osservato. L'intensità del segnale fluorescente è aumentata gradualmente con la concentrazione. Barra di scala 250 m. Fare clic qui per visualizzare una versione più grande di questa figura.
Ci sono diverse sostanze estrogeniche presenti nell'ambiente, ad esempio 17-estradiolo (concentrazione ambientale: 0,1–5,1 ng/L)21, 17-ethynylestradiol (concentrazione ambientale: 0,16–0,22 ,zearalenone (concentrazione ambientale: 0,095–0,22 g/L)23, bisfenolo-A (concentrazione ambientale: 0,45–17,2 mg/L)24. Durante il test di queste sostanze in forma puramente attiva con l'aiuto di embrioni transgenici mCherry, le concentrazioni di effetti più basse osservate (LOEC) per il rilevamento dei segni fluorescenti erano 100 ng/L per 17-estradiol, 1 ng/L per il trattamento 17-ethynilestradiol, 100 ng/L per zearalenone e 1 mg/L per il trattamento bisfenolo-A (96–120 hpf), che è molto vicino o all'interno della gamma di concentrazioni ambientali delle sostanze15. La linea transgenica Tg(vtg1:mCherry) può aiutare a rilevare l'estrogenità nei campioni di acque reflue dopo l'esposizione diretta. La linea è sensibile come il test estrogeno lievito comunemente usato, l'estrogeno lievito bioluminiscente (BLYES) assay15. Con l'aiuto di questa linea, gli effetti protettivi di beta-ciclodextrins contro la tossicità indotta da zearalenone sono stati confermati utilizzando miscele chimiche20.
In un recente rapporto, l'uso in vivo della linea transgenica è stato dimostrato con l'aiuto di due metaboliti estrogenici zearalenone (EA) ,25e zearalenolo . La linea di base del protocollo è appropriata per studiare gli effetti estrogenici di diversi composti o campioni ambientali sugli embrioni Tg(vtg1:mCherry).
Protocollo
Il Protocollo sugli animali è stato approvato ai sensi della legge ungherese sul benessere degli animali e tutti gli studi sono stati completati prima che gli individui trattati avrebbero raggiunto la fase di alimentazione libera.
1. Raccolta e trattamento dell'embrione
- Mantenere il tg(vtg1:mCherry) il pesce zebra a 25,5 x 0,5 gradi centigradi, pH 7 x 0,2, la conduttività tra 525 x 50 s/m, il livello di ossigeno 80% di saturazione e 14 h di luce e 10 h ciclo scuro.
- Riempire i serbatoi di accoppiamento con acqua di sistema e impostare il pesce per l'accoppiamento del pomeriggio prima della raccolta delle uova.
- Mettere il pesce maschio e femmina nel serbatoio e separarli con l'aiuto di un divisore.
- Rimuovere il divisore dai serbatoi mentre la luce si accende la mattina successiva. Controllare i serbatoi di accoppiamento per le uova ogni 15-20 min.
- Raccogliere tutti gli embrioni utilizzando un colino da tè o una rete fine densamente intrecciata e combinarli in un unico grande piatto Petri con tampone e3 (5 mM di cloruro di sodio, 0,17 mM di cloruro di potassio, cloruro di calcio di 0,33 mM, solfato di magnesio da 0,33 m) o acqua di sistema trasparente.
- Collocare gli embrioni nell'incubatrice impostata su 25,5 x 0,5 gradi centigradi.
- Dopo 1-1,5 h, rimuovere e scartare le uova non fecondate o dividere in modo inadeguato le uova con un tubo di trasferimento di plastica sotto un microscopio sezionato.
NOTA: Le uova non fecondate sono opache; uova fecondate sono trasparenti. Per iniziare il trattamento in una fase successiva dello sviluppo, prestare attenzione al normale sviluppo degli individui trattati. - Collocare gli embrioni selezionati nei vasi di trattamento (ad esempio, nei piatti Petri o nei piatti di coltura dei tessuti) che sono già stati etichettati e riempiti con diverse concentrazioni della sostanza di prova.
- Incubare gli embrioni a 25,5 x 0,5 gradi centigradi fino alla fine dell'esperimento.
NOTA: Gli embrioni possono reagire con significativa sensibilità individuale a vari composti estrogenici, quindi si consiglia di utilizzare almeno 15 embrioni in almeno tre trattamenti ripetuti al fine di valutare correttamente l'esperimento. Quando si seleziona il contenitore, tenere presente che lo sviluppo di un embrione richiede almeno 200 l d'acqua26. In questo esperimento gli embrioni sono stati incubati fino a 120 hpf a 25,5 x 0,5 gradi centigradi. - Aggiornare la soluzione di prova se è neccesary per mantenere la concentrazione di trattamento. Prestare attenzione quando si modifica la soluzione di prova per evitare di danneggiare gli embrioni.
NOTA: È anche possibile studiare la mortalità o i sintomi sublethal durante l'esperimento. Le concentrazioni utilizzate devono rimanere il più possibile stabili per ottenere risultati affidabili. Questo può essere facilmente raggiunto aggiornando le soluzioni di test. La frequenza di aggiornamento può variare a seconda della sostanza di prova. Pertanto, è consigliabile controllare la concentrazione della sostanza di prova mediante misurazioni analitiche per determinare la frequenza degli aggiornamenti della soluzione.
2. Preparazione delle larve per la fotografia
- Preparare in anticipo il 4% di metilcellulosa con MS-222 (tricaine-metano-sulfonato).
- Per farlo, aggiungere 4 mg/mL MS-222 a 100 mL di acqua a doppia distillazione ad una concentrazione finale di 0,168 mg/mL, e portare la soluzione a 4 gradi centigradi. Quindi aggiungere 4 g di metilcellulosa. Mescolare con un agitatore magnetico, quindi lasciarlo in 4 gradi centigradi.
- Il giorno successivo, mescolare di nuovo e la soluzione dovrebbe essere pronta per l'uso. Se la metilcellulosa non è completamente dissolta, rimettetela a 4 gradi centigradi e aspettate qualche ora in più.
- Mettere le larve di 5 giorni in un piatto Petri di 5 cm per gruppo di trattamento con una pipetta di pasteur.
- Rimuovere la soluzione di trattamento dalle larve con una pipetta di plastica, quindi riempire il piatto Petri con 2 mL di 0,02% MS-222 soluzione anestetica.
NOTA: L'anestesia è di solito efficace in meno di un minuto. Le larve sono acuite se non nuotano via in risposta al tatto. Un sovradosaggio di MS-222 può uccidere le larve. - Riempire ogni quadrato di un piatto Petri di 10 cm appositamente progettato con 4% di metilcellulosa con MS-222 (Figura 3).
NOTA: Incollare due aree quadrate da 1,5 x 1,5 cm nella parte inferiore del piatto Petri utilizzando fogli di plastica (altezza 1 mm, 5 mm di larghezza). Venti larve possono essere posizionate una accanto all'altra in un quadrato. Invece di un piatto Petri appositamente progettato, un altro contenitore a basso bordo può essere utilizzato per fissare la posizione degli embrioni.

Figura 3: Un piatto Petri di 10 cm con incollato 1,5 x 1,5 cm di larghezza, 1 mm di spessore quadrati di plastica per la preparazione delle larve per la preparazione delle larve per la fotografia. Fare clic qui per visualizzare una versione più grande di questa figura.
- Trasferire le larve anestesizzate in metilcellulosa con un po 'd'acqua in uno dei due quadrati. Dalla prima piazza trasferire le larve nel secondo quadrato.
NOTA: Con l'aiuto di questo trasferimento, il 4% di metilcellulosa utilizzato per la fotografia non verrà diluito e le larve non ruoteranno durante l'imaging. - Nel secondo quadrato, ruotare e orientare le larve sul loro lato sinistro e premere delicatamente verso il basso della cellulosa con una punta pipetta microloader tagliata fino a 2 cm.
NOTA: Non utilizzare altre punte pipette perché causano lesioni alle larve.
3. Microscopia
NOTA: La fotografia non uccide gli animali. Gli animali possono essere svegliati rimuovendoli dalla metilcellulosa e mettendoli in acqua di sistema fresco o in una soluzione di trattamento, in modo che lo stesso individuo possa essere esaminato più volte durante il trattamento.
- Per valutare il segnale del reporter espresso, immagini degli embrioni con la stessa vista e le stesse impostazioni.
NOTA: Vedere il passaggio 2.6 per un posizionamento ottimale degli embrioni. Le foto nel manoscritto sono state scattate nelle condizioni descritte. Campo luminoso: ingrandimento 60x, esposizione di 6 ms, Iris 100%, Guadagno:1.1, foto a fluorescenza: ingrandimento 60x, esposizione di 300 ms, Iris: 100%, Guadagno:1, filtro mCherry, fonte di luce fluorescente: lampadina ad alode in metallo di mercurio. Per scattare foto uno stereomicroscopio fluorescente, sono stati utilizzati una fotocamera dedicata e un software per il microscopio. - Posizionare il piatto Petri sullo stadio del microscopio.
- Concentrati sul fegato dell'embrione e cattura un'immagine di campo luminoso utilizzando il software associato.
- Passare il microscopio al filtro mCherry e scattare un'immagine fluorescente del fegato sotto la luce fluorescente utilizzando il software associato.
NOTA: Eseguire tutti i passaggi di fluorescenza al buio. Non modificare l'ingrandimento, la messa a fuoco o la posizione dell'embrione tra la cattura del campo luminoso e le immagini fluorescenti, in quanto ciò aiuterà nell'analisi delle immagini. - Ripetere i passaggi 3.3 e 3.4 fino a quando tutti gli embrioni dell'esperimento non sono stati immagine.
4. Determinazione della densità integrata
NOTA: Uno dei migliori indicatori per confrontare la potenza del segnale fluorescente è il valore di densità integrato (cioè il prodotto dell'area e il valore medio grigio). Uno dei modi più semplici per determinare la densità integrata consiste nell'utilizzare il programma ImageJ27. Il programma è disponibile su internet e può essere installato sul computer.
- Apri ImageJ quindi carica l'immagine fluorescente da analizzare trascinando e rigettando l'immagine o facendo clic su File. Aperto.
- Fare clic su Immagine Colore Dividi canali per dividere l'immagine realizzata dal filtro fluorescente in base alla tabella dei colori RGB.
- Lavorate con lo spettro dell'immagine del canale rosso, chiudete gli altri canali.
- Designare un'area ellittica di dimensioni simili nell'immagine in modo che i falsi segnali non interferiscano con la valutazione. Utilizzando gli strumenti Ovale, disegnare un'ellisse sopra l'area epatica evidenziata nel modo più accurato possibile.
- Se il segnale è debole utilizzare immagini microscopia leggera (cioè, la coppia di campo luminoso dell'immagine fluorescente) per determinare la posizione del fegato.
- Fare clic su Analizza Misurare per determinare la potenza del segnale e le dimensioni dell'area interessata. Il valore di densità integrato viene calcolato automaticamente dal software (colonna IntDen nel grafico).
- Continuare l'analisi ripetendo i passi da 4.1 a 4.6 fino all'analisi di tutte le immagini fluorescenti di tutti gli embrioni del gruppo di trattamento.
- Salvare i dati e quindi analizzare i valori di densità integrata.
NOTA: Selezionare sempre le stesse dimensioni dell'area nelle immagini durante l'analisi. Le dimensioni dell'area da analizzare dipendono dall'ingrandimento, dalla risoluzione dell'immagine, da altre impostazioni per le riprese, ecc. L'analisi può essere accelerata o resa più accurata utilizzando macro personali per l'analisi. Ad esempio, le macro possono essere utilizzate per garantire che l'area selezionata sia sempre la stessa nelle immagini esaminate. Descrizioni dettagliate per la creazione di macro che consentono la migliore analisi dell'immagine in base a particolari impostazioni di foto si trovano sul sito Web ImageJ.
Risultati
Nell'esperimento presentato in questo manoscritto, gli effetti di due sostanze estrogeniche sono stati testati a cinque concentrazioni a partire dalla fecondazione per 5 giorni sugli embrioni di pesce zebra Tg(vtg1:mCherry). Abbiamo studiato se i segnali fluorescenti apparissero nel fegato dei pesci alla fine del tempo di esposizione a causa delle sostanze e se ci fossero differenze nell'estrogenicità delle due sostanze. I risultati sono stati valutati sulla base delle immagini fluorescenti e dei valori di densità integrati. In generale, entrambe le sostanze hanno indotto l'espressione del transgene entro la fine del tempo di esposizione a quelle concentrazioni di prova a cui gli individui sono sopravvissuti. Nei casi di pesci di controllo non trattati, non era visibile alcun segnale fluorescente.
Nel caso di z-OL, alla più alta concentrazione di prova (8 M) tutti gli individui sono morti, quindi in questo caso il segnale fluorescente non poteva essere esaminato. A concentrazioni più basse (0,5 m–4 M), è stato osservato un forte segnale fluorescente nel fegato degli embrioni (Figura 4A). Non è stata osservata alcuna differenza significativa nell'intensità della fluorescenza e nelle dimensioni delle aree fluorescenti (p < 0,05). I valori di densità integrati di z-OL (Figura 4C) mostrano che la sostanza ha indotto l'aspetto di un segnale fluorescente. Non è stata riscontrata alcuna differenza significativa tra i valori di densità integrati e tra i trattamenti (p < 0,05). La densità media integrata variava tra 31,26 e 13,95 (0,5 m) e 34,25, 15,36 (4 m).
Non è stata documentata alcuna mortalità durante il trattamento con il campo di attività transgenica indotta dalla sostanza in tutte le concentrazioni di trattamento. L'intensità della fluorescenza e le dimensioni dell'area fluorescente aumentarono con l'aumentare della concentrazione, come si vede nelle immagini fluorescenti (Figura 4B). Confrontando visivamente le immagini fluorescenti di z- e z-oL, sia la potenza del segnale che la dimensione dell'area fluorescente erano visibilmente più deboli per il sistema di trattamento delle due sostanze. Studiando i valori integrati di . . ... . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . Tuttavia, nel caso di z-OL non c'è stata alcuna differenza significativa tra i valori di densità integrata delle singole concentrazioni (p < 0,05). La densità media integrata variava tra 15,86 x 4,08 (0,5 m) e 21,73 5,94 (8 m).

Figura 4: Presentazione dei valori di densità integrati derivati dall'intensità dei segnali fluorescenti nel fegato e dalle dimensioni dell'area interessata causata dal trattamento di zebre tra ziaralenolo di 5 giorni su embrioni di pesce transgenico Tg(vtg1:mCherry) di 5 giorni. Nell'esperimento, gli embrioni estrogeno-sensibili della linea del pesce zebra del biomarcatore (20 larve per gruppo in tre repliche in ogni concentrazione di trattamento) sono stati trattati con concentrazioni di 0,5 - M–8 di fecondazione in poi per 5 giorni. Le immagini dei fegati di pesce per i fegati di pesce per la zolle (A) e lo zolle (B) mostrano chiaramente che le sostanze hanno indotto la comparsa del segnale fluorescente. I dati di densità integrati sono presentati come media , deviazione standard (SD e barra di errore). I dati sono stati analizzati con il Grubbs iterativo per identificare gli outlier, che sono stati esclusi. I dati sono stati controllati per verificarne la normalità con il test di normalità Shapiro-Wilk ed è stato stabilito il rispetto dei requisiti dei metodi parametrici. Le analisi statistiche sono state eseguite utilizzando un ANOVA unidirezionale seguito da un test di Dunnett. Studiando i valori di densità integrati, non è stata riscontrata alcuna differenza significativa tra i trattamenti nei casi di z-OL (C) e di z-OL (D) (p < 0,05). Barra di scala 200 m. Fare clic qui per visualizzare una versione più grande di questa figura.
Esaminando i valori di densità integrati ottenuti dalle stesse concentrazioni di trattamento delle due sostanze (Figura 5), in ogni caso, la z-OL ha presentato medie di densità integrate più elevate rispetto a quella di z-OL, il che è coerente con le differenze tra i punti di forza del segnale osservati nelle immagini fluorescenti. Nei casi di tutte le concentrazioni di trattamento, sono state trovate differenze significative (0,5 M, p , 0,0011; 1 M, p , 0,0003; 2 M, p , 0,0329; e 4 M, p , 0,0325).

Figura 5: Confronto dei valori di densità integrati di zearalenolo e z. I dati di densità integrati sono presentati come media : deviazione standard SD - barra di errore. I dati sono stati analizzati con Grubbs iterativi per identificare gli outlier, che sono stati esclusi. I dati sono stati controllati per verificarne la normalità con il test di normalità Shapiro-Wilk ed è stato stabilito il rispetto dei requisiti dei metodi parametrici. Differenze significative sono state verificate con il test a t non accoppiato tra il test a t , e il test di z, per ogni concentrazione (0,5 M, p , 0,0011; 1 M, p , 0,0003; 2M, p - 0,0329; e 4 M, p , 0,0325). Fare clic qui per visualizzare una versione più grande di questa figura.
Discussione
L'uso di biomonitor/bioindicatori per effetti estrogenici si è diffuso in studi tossicologici. I modelli in vivo svolgono un ruolo eccezionale, perché a differenza dei test in vitro, non solo forniscono informazioni sulla risposta di una cellula o di un recettore, ma consentono anche lo studio di processi complessi nell'organismo. Diverse linee transgeniche per lo studio degli effetti estrogenici sono state prodotte da pesci zebra, uno dei quali Tg(vtg1:mCherry) è stato utilizzato per questi studi. Il metodo qui descritto illustra un protocollo per la sperimentazione di embrioni di questa linea al fine di rilevare l'attività degli estrogeni in vivo in principi attivi puri.
I maschi e gli embrioni della linea sono adatti anche per rilevare gli effetti estrogenici, ma gli embrioni hanno diversi vantaggi che promuovono la loro usabilità. In particolare, il corpo è trasparente, quindi il segnale fluorescente nel fegato può essere facilmente osservato. Il fegato di pesce zebra inizia a svilupparsi 6 ore dopo la fecondazione (6 hpf) e inizia a lavorare dopo 50 ore (50 hpf). In primo luogo, il lobo sinistro del fegato si forma, e a 96 ore (96 hpf) appare anche il lobo destro del fegato. La forma finale del fegato è sviluppata intorno al giorno 5 (120 hpf)28,29. Il fegato è in grado di produrre vitellogena endogena dall'età di 2-3 giorni di un embrione14, che coincide con la comparsa del segnale fluorescente nella linea Tg(vtg1:mCherry) 15. Pertanto, quando si progettano esperimenti, si dovrebbe tener conto del fatto che un segnale fluorescente può essere previsto solo nel fegato embrionale di quel momento. Il fegato degli embrioni di 5 giorni è già ben definito in un'area relativamente grande, dove il segnale fluorescente può essere facilmente rilevato sotto uno stereomicroscopio. Ciò rende possibile lo sviluppo di protocolli di prova che non sono soggetti alle leggi sulla protezione degli animali. La vitellogenina, e allo stesso modo la proteina fluorescente, sono prodotte dal lobo sinistro del fegato degli embrioni15. Pertanto, l'orientamento spaziale degli embrioni è importante per il rilevamento del segnale più forte quando si esamina il segnale fluorescente o si scattano fotografie. Questo è il motivo per cui gli embrioni sono stati posati a sinistra nel protocollo. Come si può vedere dai risultati rappresentativi, l'effetto estrogenico di un campione di prova è chiaramente indicato dal segnale fluorescente nel fegato, quindi i risultati possono essere valutati anche visivamente. Se la quantificazione dei risultati è necessaria, il valore di densità integrata definito dal programma ImageJ è appropriato. Tuttavia, per una corretta valutazione, è indispensabile che le immagini vengano scattate con le stesse impostazioni durante l'esperimento e che le dimensioni delle aree fluorescenti evidenziate siano le stesse in ogni immagine. Insieme al posizionamento preciso degli embrioni, questi sono i passi più critici del protocollo. È importante ricordare che nel caso degli embrioni l'espressione del transgene, analogamente alla produzione di vitellogena endogena, mostra una grande dispersione e differenze nella sensibilità individuale. In alcuni casi, ciò può causare grandi variazioni nei risultati, che dovrebbero essere prese in considerazione durante la progettazione degli esperimenti.
Un aspetto importante nel determinare le concentrazioni di trattamento è che le cellule degli embrioni, e quindi le cellule del fegato, possono essere danneggiate da alte concentrazioni di sostanze altamente tossiche, che possono portare a un calo dell'induzione della vitellogenina. Pertanto, le prove devono essere eseguite a concentrazioni inferiori a LC1015.
Confrontare la sensibilità delle linee di pesce estrogeno-sensibili tra loro è un compito difficile, perché le linee descritte finora sono state testate secondo diversi protocolli5,14,15,16. La linea testata in questo protocollo è in grado di rilevare le relazioni dose-effetto in casi di principi attivi puri, miscele e campioni ambientali, e i risultati ottenuti si sono correlati bene con i risultati con i test BLYES e le cellule HeLa15,20.
È stata dimostrata l'utilità degli embrioni della linea per testare gli agenti, tra cui zearalenone15. In questo lavoro, sono stati testati due metaboliti della tossina, z- e zearalenol. Secondo i dati della letteratura, la zolla è più tossica di30 z-OL e anche la sua estrogenità è più altadi 31. Questi risultati sono confermati dai nostri studi. Così, gli studi sugli embrioni della linea sono adatti anche per confrontare gli effetti estrogenici di altre sostanze estrogeniche.
La contaminazione da micotossina nella catena alimentare è un problema globale, quindi sono state migliorate diverse procedure per ridurre i livelli di micotossina nei mangimi animali e negli alimenti umani25,32. Una delle soluzioni più promettenti è la biodegradazione della micotossina da parte di microrganismi o dai loro enzimi. Può essere un metodo essenziale post-raccolta per diminuire o eliminare la decontaminazione della micotossina. La capacità degradante di EA di numerosi ceppi batterici è stata testata nella letteratura finora, tuttavia, recenti risultati di ricerca che dimostrano alta degradazione della tossina raramente specificano l'effetto negativo dei metaboliti33. Poiché gli embrioni di questa linea sono teoricamente adatti per testare gli effetti estrogenici di campioni con contenuto di materia organica15, può essere sviluppato un protocollo di trattamento che può aiutare a testare i prodotti di biodegradazione di EAA e la qualificazione dei ceppi degradanti.
Questo protocollo può essere modificato in molti modi in base agli endpoint di prova pianificati (ad esempio, insorgenza e lunghezza dell'esposizione) e ai campioni (ad esempio, miscele o campioni ambientali) che verranno testati e possono essere completati con altri metodi di prova (ad esempio, metodi molecolari). Pertanto, ci auguriamo che l'uso della linea Tg(vtg1:mCherry) diventerà un modello di test di estrogenità e per i metodi di test standard.
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è stato sostenuto dall'Ufficio nazionale per la ricerca, lo sviluppo e l'innovazione (NKFIH) del Fondo nazionale per la ricerca, lo sviluppo e l'innovazione (NKFIA); Accordo di sovvenzione: NVKP_16-1-2016-0003, EFOP-3.6.3-VEKOP-16-2017-00008 co-finanziato dall'Unione Europea, e il programma di eccellenza tematica NKFIH-831-10/2019 dell'Università Szent Istvàn, assegnato dal Ministero per l'Innovazione e la Tecnologia.
Materiali
| Name | Company | Catalog Number | Comments |
| 24 well tissue culture plate | Jet Biofil | TCP011024 | |
| Calcium-chloride (CaCl2) | Reanal Laborvegyszer Ltd. | 16383-0-27-39 | |
| GraphPad Prism 6.01 software | GraphPad Software Inc. | ||
| ImageJ software | National Institutes of Health, USA | Public access software, downloadable from: http://imagej.nih.gov/ | |
| Leica Application Suite X calibrated software | Leica Microsystems GmbH. | We used the softver described in the experiments, but any photographic software complies with the tests | |
| Leica M205 FA stereomicroscope, Leica DFC 7000T camera | Leica Microsystems GmbH. | We used the equipments described in the experiments, but any fluorescent stereomicroscope is suitable for the tests | |
| Magnesium-sulphate (MgSO4) | Reanal Laborvegyszer Ltd. | 20342-0-27-38 | |
| mCherry filter | Leica Microsystems GmbH. | ||
| Mehyl-cellulose | Sigma Aldrich Ltd. | 274429 | |
| Microloader pipette tip | Eppendorf GmbH. | 5242956003 | |
| Pasteur pipette | VWR International LLC. | 612-1684 | |
| Petri-dish | Jet Biofil | TCD000060 | |
| Potassium-chloride (KCl) | Reanal Laborvegyszer Ltd. | 18050-0-01-33 | |
| Sodium-chloride (NaCl) | Reanal Laborvegyszer Ltd. | 24640-0-01-38 | |
| Tricane-methanesulfonate (MS-222) | Sigma Aldrich Ltd. | E10521 |
Riferimenti
- Sumpter, J. P. Endocrine Disrupters in the Aquatic Environment : An Overview. Acta Hydrochimica et Hydrobiologica. 33 (1), 9-16 (2005).
- Routledge, E. J., Sumpter, J. P. Estrogenic activity of surfactants and some of their degradation products assessed using a recombinant yeast screen. Environmental Toxicology and Chemistry. 15 (3), 241-248 (1996).
- Sanseverino, J., et al. Use of Saccharomyces cerevisiae BLYES Expressing Bacterial Bioluminescence for Rapid, Sensitive Detection of Estrogenic Compounds. Applied and Environmental Microbiology. 71 (8), 4455-4460 (2008).
- Fetter, E., et al. Effect-directed analysis for estrogenic compounds in a fluvial sediment sample using transgenic cyp19a1b-GFP zebrafish embryos. Aquatic Toxicology. 154, 221-229 (2014).
- Gorelick, D. A., Halpern, M. E. Visualization of estrogen receptor transcriptional activation in zebrafish. Endocrinology. 152 (7), 2690-2703 (2011).
- Rider, C. V., Hartig, P. C., Cardon, M. C., Wilson, V. S. Development of a competitive binding assay system with recombinant estrogen receptors from multiple species. Toxicology Letters. 184 (2), 85-89 (2009).
- Gunnarsson, L., Kristiansson, E., Förlin, L., Nerman, O., Larsson, J. Sensitive and robust gene expression changes in fish exposed to estrogen - a microarray approach. BMC Genomics. 8 (149), 1-9 (2007).
- Vander Ven, L. T. M., et al. Vitellogenin expression in zebrafish Danio rerio evaluation by histochemistry, immunohistochemistry, and in situ mRNA hybridisation. Aquatic Toxicology. 65 (1), 1-11 (2003).
- Bakos, K., et al. Developmental toxicity and estrogenic potency of zearalenone in zebrafish (Danio rerio). Aquatic Toxicology. 136-137, 13-21 (2013).
- Strähle, U., et al. Zebrafish embryos as an alternative to animal experiments - A commentary on the definition of the onset of protected life stages in animal welfare regulations. Reproductive Toxicology. 33 (2), 128-132 (2012).
- Tsang, M. Zebrafish : A Tool for Chemical Screens. Birth Defects Research, Part C. 90 (3), 185-192 (2010).
- Hill, A. J., Teraoka, H., Heideman, W., Peterson, R. E. Zebrafish as a model vertebrate for investigating chemical toxicity. Toxicological Sciences. 86 (1), 6-19 (2005).
- Lee, C., Na, J. G., Lee, K., Park, K. Choriogenin mRNA induction in male medaka, Oryzias latipes as a biomarker of endocrine disruption. Aquatic Toxicology. 61 (3-4), 233-241 (2002).
- Chen, H., et al. Generation of a fluorescent transgenic zebrafish for detection of environmental estrogens. Aquatic Toxicology. 96 (1), 53-61 (2010).
- Bakos, K., et al. Estrogen sensitive liver transgenic zebrafish (Danio rerio) line (Tg(vtg1:mCherry)) suitable for the direct detection of estrogenicity in environmental samples. Aquatic Toxicology. 208, 157-167 (2019).
- Abdelmoneim, A., Clark, C., Mukai, M. Fluorescent reporter zebrafish line for estrogenic compound screening generated using a CRISPR/Cas9-mediated knock-in system. Toxicological Sciences. 173 (2), 336-346 (2019).
- Tong, S. K., et al. A cyp19a1b-GFP (aromatase B) transgenic zebrafish line that expresses GFP in radial glial cells. Genesis. 47 (2), 67-73 (2009).
- Segner, H. Zebrafish (Danio rerio) as a model organism for investigating endocrine disruption. Comparative Biochemistry and Physiology, Part C: Toxicology and Pharmacology. 149 (2), 187-195 (2009).
- Klinge, C. M. Estrogen receptor interaction with estrogen response elements. Nucleic Acids Res. 29 (14), 2905-2919 (2001).
- Faisal, Z., et al. Protective effects of beta-cyclodextrins vs. zearalenone-induced toxicity in HeLa cells and Tg(vtg1:mCherry) zebrafish embryos. Chemosphere. 240, 1-11 (2020).
- Kolpin, D. W., et al. Pharmaceuticals, hormones, and other organic wastewater contaminants in U.S. streams, 1999-2000: A national reconnaissance. Environmental Science and Technology. 36 (6), 1202-1211 (2002).
- Kuch, H. M., Ballschmiter, K. Determination of endocrine-disrupting phenolic compounds and estrogens in surface and drinking water by HRGC-(NCI)-MS in the picogram per liter range. Environmental Science and Technology. 35 (15), 3201-3206 (2001).
- Lundgren, M. S., Novak, P. J. Quantification of phytoestrogens in industrial waste streams. Environmental Toxicology and Chemistry. 28 (11), 2318-2323 (2009).
- Masoner, J. R., Kolpin, D. W., Furlong, E. T., Cozzarelli, I. M., Gray, J. L. Landfill leachate as a mirror of today’s disposable society: Pharmaceuticals and other contaminants of emerging concern in final leachate from landfills in the conterminous United States. Environmental Toxicology and Chemistry. 35 (4), 906-918 (2016).
- Panel on Additives and Products or Substances used in Animal Feed (FEEDA). EFSA Statement on the establishment of guidelines for the assessment of additives from the functional group ‘substances for reduction of the contamination of feed by mycotoxins' 1 EFSA. EFSA Journal. 8 (7), 1-8 (2010).
- Braunbeck, T., et al. Towards an alternative for the acute fish LC(50) test in chemical assessment: the fish embryo toxicity test goes multi-species - an update. Altex. 22 (50), 87-102 (2005).
- Schneider, C. A., Rasband, W. S., Eliceiri, K. W. NIH Image to ImageJ: 25 years of image analysis. Nature Methods. 9 (7), 671-675 (2012).
- Ober, E. A., Field, H. A., Stainier, D. Y. R. From endoderm formation to liver and pancreas development in zebrafish. Mechanisms of Development. 120 (1), 5-18 (2003).
- Tao, T., Peng, J. Liver development in zebrafish (Danio rerio). Journal of Genetics and Genomics. 36 (6), 325-334 (2009).
- Shier, W. T., Shier, A. C., Xie, W., Mirocha, C. J. Structure-activity relationships for human estrogenic activity in zearalenone mycotoxins. Toxicon. 39 (9), 1435-1438 (2001).
- Panel, E., Chain, F. Appropriateness to set a group health-based guidance value for zearalenone and its modified forms EFSA Panel on Contaminants in the Food Chain (CONTAM). EFSA Journal. 14, 4425 (2016).
- Binder, E. M. Managing the risk of mycotoxins in modern feed production. Animal Feed Science and Technology. 133 (1-2), 149-166 (2007).
- Risa, A., Krifaton, C., Kukolya, J., Kriszt, B., Cserháti, M., Táncsics, A. Aflatoxin B1 and Zearalenone-Detoxifying Profile of Rhodococcus Type Strains. Current Microbiology. 75 (7), 907-917 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon