Case Report
Technique hybride nouvelle et innovante pour la dissection aortique de type A
Dans cet article
Résumé
Le protocole décrit un remplacement aortique ascendant combiné à une couverture endovasculaire de l’ensemble de l’arc aortique avec une endoprothèse fenêtrée chez un patient présentant une dissection aortique aiguë de type A en l’absence de déchirure de l’arc aortique.
Résumé
La dissection aortique aiguë de type A à Stanford (TAAD) est une urgence chirurgicale caractérisée par un taux de mortalité élevé et de nombreuses complications. Dans le traitement du TAAD, le moment de l’intervention chirurgicale et le choix de l’intervention chirurgicale sont d’une importance capitale. La reconstruction totale ouverte de l’arc aortique reste l’étalon-or pour la chirurgie de l’arc aortique et est l’une des procédures les plus difficiles. Cependant, cette approche est invasive, relativement longue et associée à des saignements importants, ce qui nécessite des niveaux élevés de compétence de l’opérateur et comporte un risque de complications multiples, en particulier neurologiques. Ce rapport décrit une nouvelle procédure hybride appelée remplacement de l’aorte ascendante ouverte combinée à une endoprothèse fenêtrée de l’arc aortique total. Un cas a été sélectionné dans lequel la lésion n’impliquait pas l’arc aortique, du moins du côté de la plus grande courbure de l’arc. Un remplacement aortique ascendant a été effectué, suivi d’une intervention de l’arc avec des greffes de stent auto-modifiées pour préserver les branches natives de l’arc aortique. Cette approche permet une simplification rapide de la procédure, évite l’hypothermie profonde ou l’arrêt circulatoire associés à la chirurgie ouverte conventionnelle et atténue les complications neurologiques.
Introduction
La dissection aortique est une urgence cardiovasculaire rare associée à un taux de mortalité élevé ; cependant, son incidence a augmenté ces dernières années alors que l’âge d’apparition a diminué, en particulier pour la dissection aortique de type A de Stanford (TAAD)1,2. Le remplacement de l’aorte reste la procédure la plus couramment utilisée pour le TAAD3. De nombreuses complications postopératoires sont rencontrées et les taux de mortalité sont élevés en raison d’un traumatisme important et d’un arrêt circulatoire hypothermique prolongé 4,5.
Le développement de la réparation endovasculaire de l’aorte thoracique (TEVAR) a conduit à l’émergence de la chirurgie hybride 6,7,8, rendant la procédure peu invasive et moins complexe. Bien qu’il existe des indications strictes, la réduction des pertes sanguines, la réduction du temps opératoire et l’absence d’arrêt hypothermique profond atténuent le risque élevé de complications postopératoires.
La chirurgie hybride vise à raccourcir le temps de récupération fonctionnelle. La partie ascendante de l’aorte a été remplacée, que la racine soit gérée ou non. L’arcade a été fenestrée avec des greffes d’endoprothèse (SG), et une endoprothèse couvrait la partie descendante pour agrandir la lumière vraie. Cette technique hybride permet de réduire le temps opératoire, de diminuer les pertes sanguines, et le risque d’événements neurologiques postopératoires et de complications importantes est comparable ou inférieur à celui associé au remplacement ouvert. Les étapes chirurgicales sont simplifiées grâce à une gestion réduite des trois branches de l’arcade, par rapport aux autres chirurgies hybrides précédentes9. Des études antérieures ont démontré que la chirurgie hybride se caractérise par une réduction des traumatismes et une récupération accélérée. Il est reconnu que de nombreuses variations peuvent exister à presque toutes les étapes de la procédure10,11.
Cette étude présente une approche de la chirurgie hybride qui intègre TEVAR. Une identification précise et un alignement soigneux, en particulier des trois branches de la supra-arche, sont essentiels. Il s’agit d’un homme de 55 ans qui présentait une douleur thoracique intense. L’angiographie tomodensitométrique (TDM) a suggéré une TAAD sans rupture de l’arcade. Le patient a consenti à subir une chirurgie hybride, suivie d’un remplacement aortique ascendant et d’un arc total à l’aide d’une implantation de SG fenestrés auto-modifiés (figure 1), et a finalement reçu son congé de l’hôpital.
PRÉSENTATION DE CAS :
Un patient de 55 ans présentait une oppression thoracique et une douleur qui avait commencé il y a 11 heures sans aucun déclencheur apparent. Il souffrait d’hypertension depuis 3 ans, avec une pression artérielle maximale de 150/100 mmHg, et ne prenait aucun médicament pour contrôler sa tension artérielle. Il avait également des antécédents de goutte depuis 20 ans, sans antécédents d’hyperlipidémie, de diabète sucré, d’hépatite B ou de tuberculose. Il a nié avoir déjà subi une intervention chirurgicale, des transfusions sanguines, des allergies médicamenteuses ou alimentaires et n’a signalé aucun antécédent familial important. À l’admission, le patient était alerte et orienté et recevait de l’oxygène par une canule nasale. La surveillance cardiaque a révélé une fréquence cardiaque de 68 battements par minute, une saturation en oxygène de 100 %, une fréquence respiratoire de 16 respirations par minute et des pressions artérielles de 126/83 mmHg dans le membre supérieur gauche, de 139/79 mmHg dans le membre supérieur droit, de 135/80 mmHg dans le membre inférieur gauche et de 150/84 mmHg dans le membre inférieur droit. La température de la peau des membres supérieurs était fraîche, plus particulièrement du côté droit. Les deux pupilles étaient de taille égale, rondes et d’environ 3 mm de diamètre, et réagissaient à la lumière. Les bruits respiratoires des deux poumons étaient clairs à l’auscultation, sans râles secs ou humides. Les bruits cardiaques étaient normaux et aucun souffle pathologique n’a été entendu dans aucun des sites d’auscultation valvulaire. L’abdomen était mou, sans sensibilité ni douleur de rebond. Le foie et la rate n’étaient pas palpables sous la cage thoracique. Les membres présentaient une force musculaire normale et aucun œdème n’a été noté dans les membres inférieurs. Le pouls de la pédale dorsale était palpable et aucun signe pathologique n’a été détecté.
Diagnostic, évaluation et planification :
Après l’admission du patient, des tests et des investigations appropriés ont été effectués. L’échocardiographie cardiaque a révélé les diagnostics suivants : 1. hypertrophie ventriculaire gauche, 2. dilatation proximale de l’aorte ascendante. L’aorte s’est avérée anormale, et un examen TDM plus approfondi a confirmé le diagnostic de dissection aortique (type Stanford A) sans rupture de l’aorte ascendante ou de l’arcade. La dissection a impliqué l’artère mésentérique supérieure, les artères iliaques communes bilatérales et l’artère iliaque externe droite. L’artère rénale droite a été alimentée par la pseudocavité, et des épanchements pleuraux bilatéraux et une expansion insuffisante des lobes inférieurs des poumons ont été notés. Un traitement symptomatique, y compris le contrôle de la pression artérielle et de la fréquence cardiaque et l’analgésie, a été administré. Le diagnostic du patient a été confirmé, un examen de la tête et de l’abdomen a été effectué, les contre-indications à la chirurgie ont été exclues et la famille du patient a reçu des informations détaillées pour faciliter la préparation préopératoire.
Protocole
Le patient a obtenu son consentement éclairé écrit pour l’intervention, et il a donné son accord pour subir un remplacement de l’aorte ascendante avec les SG fenestrés. Cette étude a été menée conformément à toutes les directives institutionnelles, nationales et internationales en matière de bien-être humain12 et a reçu l’approbation du Comité d’éthique du Collège médical de Tongji de l’Université des sciences et de la technologie de Huazhong (document du Conseil d’examen institutionnel numéro TJ-IRB20220124). Le consentement éclairé écrit des patients a été obtenu pour la publication du manuscrit et de toutes les images qui l’accompagnent.
1. Évaluation préopératoire de la TDM
- La fenestration a été conçue en fonction des caractéristiques de la lésion, de la mesure précise avant l’opération, et de la configuration du SG (Figure 2).
- Les diamètres de l’aorte et des trois principales artères ramifiées ont été mesurés à l’aide d’images CTA, en utilisant soit le diamètre circulaire, soit le diamètre moyen elliptique des artères. Des mesures ont été prises à plusieurs points de repère anatomiques, avec une attention particulière à l’arc aortique et à ses branches, qui sont cruciales pour la planification de la chirurgie hybride pour le TAAD.
- Pour obtenir des mesures précises, une ligne médiane a d’abord été définie le long de l’aorte et de ses branches. Pour chaque artère, le diamètre a été mesuré au niveau du plan de section transversale perpendiculaire qui coupait la ligne médiane au site de mesure choisi afin d’éviter les artefacts ou les irrégularités de la paroi du vaisseau qui pourraient influencer la précision des mesures.
- L’aorte a été mesurée à des points clés, notamment l’aorte ascendante, l’arc aortique (distal à l’origine de l’artère brachiocéphale) et l’aorte thoracique descendante. De même, les diamètres des principales branches (brachiocéphale, carotide commune gauche et artère sous-clavière gauche) ont été mesurés à l’origine et aux points distaux le long de l’arcade, assurant la cohérence de la technique de mesure. Les mesures ont été obtenues à l’aide d’un outil logiciel calibré capable de générer des vues de coupe précises et de permettre une évaluation fiable du diamètre.
- L’angle de l’arc aortique est l’angle entre la ligne entre les extrémités proximale et distale de l’arc aortique et le plan horizontal. L’angle de l’arcade a été déterminé avec le patient en position couchée. Cet angle détermine l’angle de projection du bulbe lorsque l’arc aortique est déployé. Il est généralement oblique antérieur gauche de 30° à 60°, avec une moyenne de 45°.
2. Remplacement de l’aorte ascendante
- La greffe vasculaire artificielle (GAV) appropriée a été sélectionnée en fonction du diamètre naturel du vaisseau, tel que mesuré par TDM.
- L’état de la section du sinus aortique, de l’intima de la racine aortique, de l’ostium de l’artère coronaire et des structures des feuillets de la valve aortique a été évalué pour déterminer si le segment le plus proximal devait être traité.
- Dans ce cas, la valve aortique était impliquée dans la lésion, y compris l’implication de l’anneau aortique et la régurgitation de la valve. Après l’administration d’héparine pour obtenir une anticoagulation adéquate, la circulation extracorporelle (ECC) a été établie à travers les artères axillaires et fémorales et le patient n’a pas été soumis à un arrêt cardiaque hypothermique profond. ECC a été assisté afin d’effectuer l’intervention chirurgicale en toute sécurité.
- L’aorte ascendante a ensuite été excisée et un greffon artificiel sur mesure (30 mm), sélectionné sur la base des mesures CTA préopératoires, a été suturé en place pour remplacer le segment aortique malade. En même temps, la valve aortique a été remplacée par une prothèse valvulaire mécanique pour remédier au dysfonctionnement valvulaire et assurer la stabilité hémodynamique à long terme.
- Tout au long de la procédure, l’intégrité de l’ostium de l’artère coronaire a été préservée en évitant cette zone pour les opérations chirurgicales et les structures radiculaires de l’aorte ont été soigneusement inspectées pour assurer un bon alignement du greffon et de la valve. La procédure visait à obtenir un succès immédiat et à long terme dans la restauration de l’intégrité et de la fonction de l’aorte.
3. Fenestration SG
- Après la fin du remplacement de l’aorte ascendante, le thorax a été délibérément laissé ouvert pour faciliter l’évaluation ultérieure de l’anastomose distale. Afin d’assurer une identification précise du site anastomotique en vue d’une évaluation ultérieure, des pinces de Kelly ou des clips en titane ont été placés à l’emplacement de l’anastomose distale. Ces marqueurs servent de points de référence anatomiques clairs pour l’imagerie et les interventions chirurgicales ultérieures.
- Après la mise en place des marqueurs, une angiographie par soustraction numérique (DSA)13 a été réalisée pour évaluer l’intégrité et la perméabilité du segment aortique nouvellement construit (Figure 3). La technique d’imagerie DSA a été utilisée pour obtenir des images à haute résolution et en temps réel de l’anastomose distale, permettant une évaluation précise de la dynamique du flux sanguin et de l’absence de complications telles que sténose, fuite ou malposition. Le processus de soustraction numérique améliore la visibilité des structures vasculaires en éliminant les tissus d’arrière-plan et en mettant en évidence la lumière remplie de contraste.
- La position et la longueur des ouvertures SG ont été déterminées sur la base de l’imagerie peropératoire et des données CTA préopératoires. Dans ce cas, l’emplacement de la déchirure descendante était près de l’artère sous-clavière gauche.
- Pour éviter les endofuites et la gestion incomplète des lésions, une fenêtre in situ a été prévue pour l’artère sous-clavière gauche afin d’implanter le Viabahn, et une fenestration in vitro a été prévue pour les deux branches restantes de l’arcade.
- Tout d’abord, l’extrémité antérieure de l’endoprothèse a été recouverte et elle a dépassé l’anastomose aortique distale de 10 à 15 mm. La longueur de la fenêtre des SG a été définie par l’extrémité proximale de l’ostium du tronc brachiocéphale et l’extrémité distale de l’ostium de l’artère carotide commune gauche. La largeur de la fenêtre était principalement déterminée par le diamètre des récipients dans l’arc et leur position relative les uns par rapport aux autres.
- Pour positionner avec précision les fenêtres des SG avec les branches correspondantes de l’arc aortique, des sutures fixes en matériaux radio-opaques tels que du fil d’acier inoxydable ou de fines plaques métalliques ont été utilisées aux deux extrémités de la fenêtre SG. Ces matériaux sont choisis pour leur radio-opacité, qui permet une visualisation claire sous guidage fluoroscopique pendant la procédure.
- La suture a été réalisée avec un placement soigneux des sutures interrompues ou continues à travers les SG sur les bords de la fenêtre. Le fil ou la feuille métallique a été fixé à l’endoprothèse à ces endroits pour assurer un positionnement stable et un alignement précis de la fenêtre modifiée avec les vaisseaux de l’arche, en particulier au niveau du tronc brachiocéphale et de l’artère carotide commune gauche, afin de minimiser le risque de complications telles que la resténose ou le désalignement de la branche ostium.
- Si les branches étaient plus éloignées sur la proue, des fenêtres distinctes étaient utilisées pour chacune des trois branches, ce qui nécessitait des mesures précises à partir d’une image 3D.
4. Implantation des SG
- Des SG modifiés ont été implantés à travers l’artère fémorale (Figure 4).
- La poignée des SG a été tournée et le SG a été relâché avant de le dégainer lentement et d’ouvrir le support à la position de départ du revêtement du support. Le côté de la SG correspondant au point blanc sur la poignée est identifié comme étant le côté d’ouverture, et le marqueur de côté d’ouverture a été confirmé.
- Les positions antérieure et postérieure de la fenêtre ouvrante peuvent également être marquées à l’aide des segments SG correspondants. La position de l’arc aortique et de la branche à l’intérieur de l’arc a été déterminée à plusieurs reprises en marquant l’arc aortique et deux branches avec des marqueurs d’écran et des marqueurs correspondants sur l’os.
- Un fil-guide a été avancé à travers la gaine dans l’artère sous-clavière gauche, avec une fluoroscopie en temps réel guidant la procédure pour assurer un placement précis du cathéter sur le site correspondant aux SG précédemment déployés, après quoi un cathéter à ballonnet a été introduit à travers la gaine et avancé jusqu’à l’ostium de l’artère sous-clavière.
- La dilatation par ballonnet a été soigneusement réalisée sur le site des SG afin d’optimiser l’expansion de l’endoprothèse, d’améliorer l’apposition à la paroi aortique et de rétablir l’écoulement dans l’aorte disséquée. Le ballonnet a été gonflé graduellement et la pression a été soigneusement surveillée pour éviter d’endommager le vaisseau tout en assurant une expansion adéquate de l’endoprothèse. Après une dilatation réussie par ballonnet, une endoprothèse recouverte de Viabahn a été déployée sur le site afin de minimiser le risque d’endofuite et de sécuriser la position des SG.
- En fonction des besoins du patient, un deuxième stent a été implanté dans l’aorte descendante afin d’éliminer autant que possible la fausse lumière.
5. Positionnement du fil-guide
- Dans la procédure TEVAR pour TAAD, l’implantation de SG nécessite une manipulation méticuleuse du fil-guide pour assurer un déploiement précis de l’endoprothèse. Initialement, un fil-guide a été sélectionné et soigneusement façonné pour correspondre à l’anatomie de l’aorte. Pour soutenir le fil-guide de manière appropriée et prévenir toute complication lors de l’avancement, un AVG ramifié ou prétraité a été utilisé.
- Une fois le fil-guide bien en place, le SG a été avancé sur le fil-guide, assurant un déploiement fluide et contrôlé sur le site cible à l’aide d’un guidage fluoroscopique.
- Dans ce cas de chirurgie hybride pour TAAD, l’implantation du greffon de stent (SG) a été compliquée par une greffe aortique de remplacement courte (AVG) et la présence d’une valve aortique mécanique, qui a entravé le passage du fil-guide à travers la valve. Pour surmonter ce défi, un AVG ramifié ou prétraité a été utilisé, ce qui a permis de positionner le fil-guide au-dessus de la valve aortique, évitant ainsi l’interaction directe avec les composants mécaniques de la valve.
- L’AVG a été soigneusement avancé de manière à ce que le fil-guide dépasse du greffon, ancré à l’extérieur de la lumière de la valve aortique. Cela a fourni un chemin stable et sûr pour faire avancer le fil-guide à travers l’aorte tout en évitant tout dommage potentiel à la valve ou perturbation de sa fonction. La position du fil-guide a été soigneusement surveillée à l’aide de la fluoroscopie pour s’assurer qu’il est correctement placé au-dessus de la vanne.
- De plus, comme l’AVG de remplacement est court et que la valve aortique n’a pas été remplacée, le fil-guide a été prolongé dans le ventricule. L’embout a été prétraité pour s’assurer qu’il était incurvé, réduisant ainsi le risque de lésions cardiaques. Cependant, lorsque l’AVG de remplacement est de longueur idéale, la valve aortique n’affecte pas le fil-guide et elle a été placée directement dans le vaisseau.
6. DSA postopératoire
- Après l’intervention chirurgicale, une DSA a été réalisée pour évaluer le résultat de la réparation hybride chez le patient. L’ASD a fourni une imagerie à haute résolution, permettant une visualisation détaillée de l’ensemble de l’aorte, y compris les trois principales branches de l’arc aortique (tronc brachiocéphale, artère carotide commune gauche et artère sous-clavière gauche). C’était crucial pour s’assurer que l’arc aortique était bien perméable, sans signe de sténose ou de compromis dans le flux sanguin vers la tête, le cou et les membres supérieurs.
- De plus, DSA permet d’évaluer les SG nouvellement déployés, confirmant qu’ils ont été correctement positionnés, sans plis ni déplacements. La procédure a également été essentielle pour détecter toute complication potentielle, telle qu’une fuite interne, une migration de stent ou des endofuites, qui pourraient compromettre la réparation et nécessiter une intervention supplémentaire. Un flux sanguin régulier et non obstrué à travers l’arc aortique et dans les branches a été utilisé comme indicateur d’un résultat réussi, garantissant que la procédure hybride a effectivement rétabli une hémodynamique normale.
- Une fois que l’ASD a confirmé l’absence de fuite et la mise en place réussie de la greffe de stent, la poitrine a ensuite été fermée en couches. Cela implique la fermeture soigneuse du péricarde, suivie d’une réapproximation des muscles de la paroi thoracique, du fascia et de la peau, assurant une hémostase correcte et minimisant le risque de complications postopératoires telles que l’infection ou la déhiscence de la plaie.
Résultats
Les résultats représentatifs de ce cas démontrent le succès technique et la faisabilité de l’approche hybride du TAAD. L’opération a été réalisée dans un délai raisonnable de 6 h avec une perte de sang contrôlée de 500 ml, ce qui reflète la nature peu invasive de l’approche hybride par rapport à la chirurgie ouverte traditionnelle. Le rétablissement rapide du patient, qui se réveille seulement 3 heures après l’opération sans aucune anomalie sensorielle ou motrice, est un indicateur important de l’efficacité de la procédure dans le maintien de l’intégrité neuronale et vasculaire. L’absence de complications telles que des déficits neurologiques et le fait que le patient n’a pas eu besoin d’hypothermie profonde pendant l’intervention met en évidence la réduction du stress physiologique imposé par la technique hybride.
De plus, l’imagerie TDM postopératoire (Figure 5), qui n’a montré aucune fuite significative de contraste, aucun déplacement de l’endoprothèse et une circulation sanguine régulière dans les trois branches de l’arc aortique, confirme le succès technique de la mise en place de l’endoprothèse et confirme la perméabilité et la stabilité de la réparation. Ces résultats d’imagerie sont essentiels pour démontrer l’efficacité de la procédure hybride dans la réparation du TAAD et le rétablissement d’un flux sanguin normal vers la tête, le cou et les membres supérieurs. Le patient est sorti de l’hôpital le 11e jour postopératoire sans complications majeures, ce qui souligne encore l’issue favorable et le rétablissement rapide associés à cette approche.
Pour analyser le résultat, il est important d’évaluer à la fois les résultats postopératoires immédiats, tels qu’ils sont observés dans les données d’imagerie et de récupération, et le suivi à plus long terme pour évaluer la durabilité de la greffe de stent et la possibilité de complications tardives telles que des endofuites ou une resténose. De plus, la comparaison de cette approche hybride avec les techniques chirurgicales traditionnelles en termes de temps opératoire, de perte de sang et de taux de complications pourrait fournir des informations précieuses sur les avantages de la chirurgie hybride dans le TAAD.

Figure 1 : Schéma de principe de la technique hybride de remplacement aortique ascendant combiné à une greffe d’endoprothèse fenêtrée. Le site fenêtré a été aligné avec précision avec les branches de l’arc, permettant un flux sanguin régulier vers la tête, le cou et les membres supérieurs et l’élimination complète de la lésion aortique sans endofuite. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 2 : Images d’une TDM préopératoire. (A) Une image CTA tridimensionnelle du site de la lésion est visible, mais aucune déchirure n’est présente dans l’aorte. (B) L’image du plan transversal CTA montre les parties ascendante et descendante de l’aorte présentant une double lumière avec un lambeau intimal. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 3 : Images de l’ASD peropératoire. a est la déchirure de la dissection aortique. B est l’anastomose distale d’une greffe vasculaire artificielle. A est la longueur de la fenestration in vitro. B est la position de la fenestration de la combinaison. C est la longueur de la position de départ de la fenestration SG à partir de l’extrémité antérieure de la SG. Abréviations : BCT = tronc brachiocéphale ; LCCA = Artère carotide commune gauche ; LSA =Artère sous-clavière gauche Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 4 : Intervention chirurgicale. (A) Auto-modification des greffes d’endoprothèse à l’aide d’un stylo cautérisé ou d’un scalpel - Chirurgie fenêtrée. La longueur de la fenêtre est la longueur totale des saillies des branches et la largeur est le diamètre des branches. (B) Le processus d’implantation d’une endoprothèse (SG). (C) Aiguilles de flexion et de perçage réglables utilisées dans la technologie de fenestration in situ. Cet appareil peut ajuster de manière flexible l’angle et la position de l’extrémité avant. (D) Utilisez un ballonnet pour dilater le site de ponction afin de faciliter l’implantation du Viabahn après le passage de l’aiguille à travers l’endoprothèse couverte. Veuillez cliquer ici pour voir une version agrandie de cette figure.
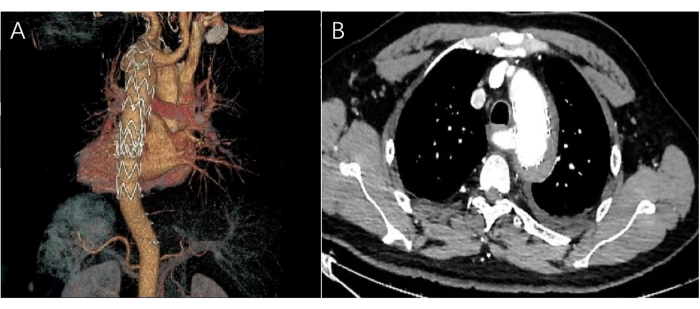
Figure 5 : Images d’une TDM postopératoire. (A) L’image tridimensionnelle postopératoire de la TDM montre que l’endoprothèse aortique se trouve dans l’arc aortique et que la déchirure de l’artère sous-clavière gauche est complètement fermée. (B) L’image horizontale de la TDM montre l’ombre de l’endoprothèse sans hématome ni fuite de contraste. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Discussion
Cette procédure est actuellement indiquée pour certains patients présentant des arcs aortiques de qualité, tels que ceux présentant 1) des déchirures de l’aorte descendante et/ou ascendante où l’arc aortique est suffisamment intact pour permettre l’utilisation d’une pince de blocage, sans déchirures du côté de la plus grande courbure et sans piégeage des branches supra-artérielles ; 2) même s’il y a des déchirures dans l’arcade, elles sont confinées au côté de la moindre courbure et la procédure TEVAR isolera les déchirures, minimisant ainsi le risque de fuite interne. Les étapes clés de la procédure de fenestration sont les suivantes : remplacement aortique ascendant, examen peropératoire de l’ASD, fenestration des SG, implantation de SG modifiés qui couvrent et prolongent l’anastomose de 10 à 15 mm, localisation et amarrage à la branche de l’arc et utilisation d’un fil-guide super rigide.
Cette procédure nécessite moins d’anastomoses, réduit le nombre d’étapes chirurgicales, est facile à réaliser et évite l’arrêt circulatoire par hypothermie profonde14. Dans TEVAR, le thorax n’est pas suturé et seule une membrane adhésive est utilisée, principalement pour éviter la réhéparinisation et la réadministration de protamine, ce qui augmente le risque de saignement thoracique et l’incapacité à détecter les saignements à temps. De plus, la membrane adhésive fournit un point d’appui si le stent a des difficultés à traverser l’anastomose distale. En cas de malposition, le problème peut être résolu rapidement, par exemple en créant un pontage ou en effectuant une ponction à l’aiguille de la membrane. En plus des complications chirurgicales habituelles, les complications neurologiques doivent être étroitement surveillées en postopératoire15,16. Le traitement de l’arcade peut affecter l’apport sanguin à la tête, au cou et aux membres supérieurs. En raison de ce risque, une DSA est réalisée au moins en postopératoire dans la salle d’opération pour évaluer l’apport sanguin aux branches de l’arcade. Les fonctions motrices et sensorielles du membre affecté doivent être évaluées dès que possible lorsque le patient est éveillé. La stabilité des SG peut être compromise après une chirurgie ouverte sur l’endoprothèse sus-jacente, et il existe un risque de migration des SG. Cette procédure hybride nécessite un haut niveau de compétence de la part du chirurgien cardiaque, qui doit non seulement maîtriser les techniques chirurgicales ouvertes, mais également avoir des compétences endovasculaires avancées.
En veillant à ce que la zone d’ancrage soit suffisamment longue, l’utilisation d’un stent de recouvrement peut minimiser le nombre d’étapes procédurales17. La conception de l’endoprothèse de recouvrement peut être adaptée aux caractéristiques de la lésion du patient18. Par exemple, si les trois branches de l’arc supra-aortique sont largement espacées, des fenêtres doubles ou triples peuvent être sélectionnées pour maintenir la stabilité de l’endoprothèse. Lorsque les branches supra-aortiques de l’arc sont touchées, comme dans le cas d’une artère infraclaviculaire coupée, la fenestration in vitro combinée à la fenestration in situ peut être utilisée pour implanter une endoprothèse dans le vaisseau, réduisant ainsi le risque d’endofuite. Cette approche peut aider à assurer la stabilité de l’endoprothèse, comme démontré dans ce cas.
La chirurgie hybride est faisable, mais de futures études prospectives sont nécessaires pour valider cette approche. La technique décrite, associée à des mesures CTA adéquates et à une localisation précise de la rupture, peut offrir une alternative précieuse à la fois à la chirurgie ouverte traditionnelle et aux procédures hybrides classiques. D’autres études sont nécessaires pour comparer les résultats à court et à long terme de cette procédure hybride avec ceux de la chirurgie ouverte et de la chirurgie hybride classique.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Les auteurs n’ont aucune reconnaissance.
matériels
| Name | Company | Catalog Number | Comments |
| Adjustable bend | Lifetech | 106938370117414.00 | The Lifetech Adjustable Bend is constructed from high-quality, biocompatible materials, ensuring both flexibility and durability. The outer layer is typically composed of a polyurethane or similar material that is resistant to kinking, while the inner components include a nickel-titanium alloy (nitinol), known for its superelastic properties, which allow the catheter to return to its original shape after bending to improve the navigability and adaptability of endovascular procedures in challenging vascular anatomies. |
| Artificial vascular graft | Terumo | 734006 | The artificial vascular graft used in this study is made from expanded polytetrafluoroethylene (ePTFE), a biocompatible synthetic material used in vascular surgeries. |
| Balloon catheter | Boston Scientific | H74939171060410 | The Boston Scientific B-Balloon Catheter is a highly advanced, precision-engineered device designed for use in percutaneous transluminal angioplasty (PTA) procedures, particularly in vascular interventions. Its key feature is the balloon catheter technology, which allows for the effective dilation of stenotic lesions in both peripheral and coronary arteries. |
| Guidewire | Cook Medical | G14544 | The Cook Guidewire is a high-performance medical device used to navigate and guide catheters, balloons, and other devices in interventional procedures. It is made from durable materials such as stainless steel and nickel-titanium alloy and is available in a range of sizes and designs tailored to specific clinical needs. The guidewire features a flexible, torqueable, and pushable structure that allows precise navigation through challenging anatomical pathways. |
| Mechanical valve | Medtronic | A7700 | The mechanical heart valve is a widely used prosthetic device designed for the replacement of damaged or diseased heart valves and is particularly suitable for younger patients who require a long-lasting solution for valve replacement, with a proven clinical track record of over 20 years of durability. |
| Pigtail catheter | Cook Medical | G11916 | The Cook Pigtail Catheter is constructed from radiopaque materials, allowing for clear visualization under fluoroscopy,and a versatile, reliable device that enhances the effectiveness of various diagnostic and therapeutic interventions. Its flexible, radiopaque design and pigtail shape provide stability and ease of navigation, making it a valuable tool for clinicians performing cardiac and vascular procedures. |
| Stent-graft | Lifetech | (01)06938370139126 | The Lifetech Stent-Graft is a highly effective and reliable solution for the endovascular treatment of a variety of vascular conditions, particularly aortic dissection.It has a discontinuous, non-radiopaque metal strip on the back.Its hybrid design, incorporating a self-expanding nitinol stent with a durable, biocompatible graft, provides both structural support and sealing, offering significant advantages over traditional open surgery in terms of patient recovery and procedural risk. |
| Stent-graft | Medtronic | VAMF3232C200TE | The Medtronic Stent-Graft represents a significant advancement in the field of endovascular surgery, offering a safe and effective alternative to open surgical repair for patients with complex vascular pathologies such as aortic dissection. The combination of a self-expanding nitinol stent with a durable, biocompatible graft provides optimal sealing and long-term durability. |
| Viabahn | Gore | VBHR080202W | The Gore Viabahn Stent-Graft is composed of a stainless steel or nitinol stent covered by a ePTFE (expanded polytetrafluoroethylene) graft.The Viabahn combines the mechanical support of a self-expanding stent with the sealing capabilities of a biocompatible graft, providing a durable, minimally invasive solution to treat complex vascular lesions. |
Références
- Zhu, Y., et al. Type A aortic dissection-experience over 5 decades: JACC historical breakthroughs in perspective. J Am Coll Cardiol. 76 (14), 1703-1713 (2020).
- Kallenbach, K., et al. Treatment of the aortic root in acute aortic dissection type A: insights from the German registry for acute aortic dissection type A. Eur J Cardiothorac Surg. , ezac261 (2022).
- Hagan, P. G., et al. The international registry of acute aortic dissection (IRAD): new insights into an old disease. JAMA. 283 (7), 897-903 (2000).
- Mousavizadeh, M., et al. Hypothermic circulatory arrest time affects neurological outcomes of frozen elephant trunk for acute type A aortic dissection: A systematic review and meta-analysis. J Card Surg. 36 (9), 3337-3351 (2021).
- Pupovac, S. S., et al. Moderate versus deep hypothermia in type A acute aortic dissection repair: Insights from the international registry of acute aortic dissection. Ann Thorac Surg. 112 (6), 1893-1899 (2021).
- National Society of Vascular Surgery, China. Chinese expert consensus on hybrid technique on treating thoracic aortic pathologies involving the aortic arch. Chinese Circ J. 35 (2), 124-130 (2020).
- National Committee of Experts on Cardiovascular Diseases. The Chinese expert consensus on hybridization techniques for treatment of aortic diseases involving the arch. Chinese J Circ. 35 (2), 124-130 (2020).
- Zhang, L., et al. Hybrid and frozen elephant trunk for total arch replacement in DeBakey type I dissection. J Thorac Cardiovasc Surg. 158 (5), 1285-1292 (2019).
- Liu, X., et al. Hybrid total arch replacement via ministernotomy for Stanford type A aortic dissection. Front Cardiovasc Med. 10, 1231905 (2023).
- Liu, Y., et al. Early outcomes of hybrid type II arch repair versus total arch replacement with frozen elephant trunk in acute DeBakey type I aortic dissection: a propensity score-matched analysis. Interact Cardiovasc Thorac Surg. 31 (4), 565-572 (2020).
- Liu, S., et al. Midterm outcomes of one-stage hybrid aortic arch repair for stanford type A aortic dissection: A single center's experience. Semin Thorac Cardiovasc Surg. 35 (2), 311-321 (2023).
- World Medical Association. World Medical Association Declaration of Helsinki: ethical principles for medical research involving human subjects. JAMA. 310 (20), 2191-2194 (2013).
- Dai, L., et al. Safety and effectiveness of the sutureless integrated stented graft prosthesis in an animal model. Heliyon. 10 (9), e30323 (2024).
- Sirota, D. A., et al. Hybrid technologies for reconstruction of proximal aortic dissection. Sovrem Tekhnologii Med. 15 (3), 42-51 (2023).
- Jensen, C. W., Chen, E. P. Management of brain malperfusion in acute type A aortic dissection. Asian Cardiovasc Thorac Ann. 30 (3), 364-370 (2022).
- Gaul, C., Dietrich, W., Erbguth, F. J. Neurological symptoms in aortic dissection: a challenge for neurologists. Cerebrovasc Dis. 26 (1), 1-8 (2008).
- Kuzniar, M. K., Wanhainen, A., Tegler, G., Mani, K. Endovascular treatment of chronic aortic dissection with fenestrated and branched stent grafts. J Vasc Surg. 73 (5), 1573-1582 (2021).
- Tenorio, E. R., et al. Fenestrated and branched aortic research Consortium investigators. Outcomes of endovascular repair of chronic postdissection compared with degenerative thoracoabdominal aortic aneurysms using fenestrated-branched stent grafts. J Vasc Surg. 72 (3), 822-836.e9 (2020).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon