Method Article
Utilisation d’un dispositif de résistance à commande numérique induite par le pied pour l’évaluation de l’imagerie par résonance magnétique fonctionnelle chez les patients atteints de parésie du pied
Dans cet article
Résumé
La réadaptation assurée des patients victimes d’un AVC chronique est généralement limitée dans le temps. L’étude basée sur l’imagerie de l’activité cérébrale à partir de tâches motrices liées à la marche peut conduire à l’établissement de biomarqueurs pour mesurer l’amélioration des résultats et justifier l’extension d’un traitement adapté. Un nouveau dispositif de mouvement du pied à résistance variable, compatible avec la résonance magnétique, ainsi qu’un protocole d’utilisation lors de l’imagerie par résonance magnétique fonctionnelle sont présentés.
Résumé
Les déficits neurologiques d’un AVC peuvent entraîner des handicaps moteurs à long terme, y compris ceux qui affectent la marche. Cependant, la réadaptation extensive après un AVC est généralement limitée dans le temps. L’établissement de biomarqueurs prédictifs pour identifier les patients qui pourraient bénéficier de manière significative d’une thérapie physique supplémentaire et démontrer une amélioration est important pour améliorer la qualité de vie des patients. La détection d’un remodelage neuroplastique de la région affectée et de changements dans les schémas d’activité excités lors de l’exécution de tâches motrices appropriées pourraient avoir des implications précieuses pour la récupération chronique d’un AVC. Ce protocole décrit l’utilisation d’un dispositif robotique (MR_COFID) induit par le pied compatible avec la résonance magnétique à commande numérique pour présenter une tâche motrice personnalisée impliquant un suivi de trajectoire à des sujets touchés par un AVC et ayant une déficience de la marche pendant l’imagerie par résonance magnétique fonctionnelle (IRMf). Dans la tâche, la flexion du pied est effectuée contre des forces résistives bidirectionnelles, qui sont ajustées à la force du sujet dans les directions de la dorsiflexion et de la flexion plantaire, tout en suivant un métronome visuel. L’IRMf utilise de manière non invasive la désoxyhémoglobine endogène comme agent de contraste pour détecter les changements dépendants du niveau d’oxygénation du sang (BOLD) entre les périodes actives et de repos pendant les tests. Des tests périodiques répétés peuvent détecter des changements liés à la thérapie dans les schémas d’excitation pendant l’exécution de la tâche. L’utilisation de cette technique fournit des données pour identifier et mesurer des biomarqueurs qui peuvent indiquer la probabilité qu’une personne bénéficie d’une réadaptation au-delà de ce qui est actuellement fourni aux patients victimes d’un AVC.
Introduction
L’utilisation de paramètres quantitatifs dérivés de l’imagerie cérébrale fonctionnelle et structurelle peut être plus utile et efficace pour suivre les progrès et prédire les résultats du traitement de l’AVC que l’évaluation des scores cliniques, et ces paramètres quantitatifs pourraient être utiles pour concevoir et améliorer des plans de traitement individualisés 1,2. Il reste difficile de développer des stratégies efficaces et personnalisées qui relient l’entraînement moteur à une réorganisation mesurable de l’activité neuronale et/ou à des améliorations de la fonction motrice. Dans des travaux antérieurs, des connaissances ont été développées sur la façon dont les méthodes de neuroimagerie fonctionnelle et la cartographie cérébrale chez les patients touchés par un AVC chronique peuvent montrer de tels changements 3,4,5,6,7,8. L’examen de la fonction cérébrale en relation avec la performance de la prise en main (qui est la clé de l’autonomie et de la qualité de vie du patient) a conduit à l’attente que cette technique pourrait également être appliquée au contrôle des mouvements du pied liés à la marche grâce à l’évaluation des modèles topographiques correspondants de l’activité neuronale et de la récupération de la fonction. Il a été postulé que l’incorporation de cartes fonctionnelles des lésions basées sur l’IRM pourrait aider à caractériser les déficits neurologiques plus précisément que les évaluations cliniques9 et que l’utilisation de dispositifs robotiques est plus efficace pour la récupération cérébrale que les paradigmes conventionnels10. Les cartes fonctionnelles peuvent donner un aperçu des parties d’un système qui fonctionnent, fournissant ainsi des informations qui ne sont pas évidentes à partir des observations cliniques11. Le succès de la réadaptation du mouvement et de la force du pied avec l’IRM pour les patients victimes d’un AVC facilitera l’élaboration de stratégies de traitement personnalisées basées sur les paramètres de l’IRM pour une population plus large atteinte d’autres affections neurologiques.
Dans le travail présenté ici, l’utilisation du dispositif robotique induit par le pied compatible avec l’IRM (MR_COFID ou dispositif du pied) pendant l’IRMf est décrite pour examiner les effets de l’entraînement des habiletés motrices post-AVC sur la fonction cérébrale. La motivation pour le développement de ce dispositif de pied à résistance contrôlée était le besoin critique non satisfait de rééducation du mouvement du pied chez les patients victimes d’un AVC. La construction d’un système adapté à la fois à la formation à domicile et au bureau et au suivi des réponses aux activités de formation basé sur la RM crée une approche unifiée qui répond aux limites antérieures en termes de formation et d’évaluation.
Le MR_COFID (figure 1A) est une adaptation du dispositif robotique manuel (MR_CHIRODv2)8,12 compatible avec la résonance magnétique, qui utilisait un actionneur à fluide électro-rhéologique (ERF) pour fournir une force résistive contrôlée dynamiquement en réponse à la saisie et à la compression par un sujet de son mécanisme de poignée. L’actionneur ERF (Figure 1B) est un piston bidirectionnel rempli de fluide dans lequel l’ERF d’un côté du piston est forcé par le mouvement du piston à s’écouler entre une paire d’électrodes dans un canal, qui renvoie le fluide de l’autre côté du piston. Lorsqu’une haute tension (HV) est appliquée aux électrodes, les particules de l’huile de silicone non conductrice s’alignent et se lient mécaniquement les unes aux autres, augmentant ainsi la viscosité du fluide et la résistance au mouvement de l’appareil. Dans le dispositif de poignée, l’actionneur est directement couplé aux poignées de préhension, à un capteur de charge pour mesurer la force appliquée et à un codeur optique pour mesurer le déplacement de la poignée. Le nouveau dispositif de pied transforme l’action linéaire du dispositif de préhension en déplacement angulaire du pied en dorsiflexion et en flexion plantaire à l’aide d’un mécanisme de curseur de manivelle (Figure 1C). La force de résistance de l’actionneur ERF est convertie presque proportionnellement au couple de résistance autour de l’articulation de la cheville. Le mouvement de manivelle de la pédale est symétrique par rapport au vecteur perpendiculaire à l’axe de l’actionneur principal, tirant ainsi parti de l’approximation selon laquelle l’angle de manivelle et son sinus sont presque égaux pour les petits angles. Comme seules les forces résistives peuvent être exercées par l’ERF, le système est intrinsèquement sûr ; L’actionneur ne peut pas pousser ou tirer activement le pied, et la force tombe à zéro lorsque le sujet s’arrête de bouger. La flexion plantaire maximale du dispositif du pied est de 35° et la dorsiflexion maximale est de 18°. Ces valeurs se situent dans l’amplitude de mouvement du pied dans des conditions normales de marche et de non-port de poids13,14, sont presque les mêmes que les valeurs utilisées dans d’autres recherches15, et ont été constatées lors d’essais préliminaires qu’elles atteignaient ou dépassaient l’amplitude de mouvement des sujets de course du côté affecté par la blessure et permettaient de maximiser les forces résistives disponibles via le mécanisme de transmission linéaire-angulaire. Le dispositif de préhension original et le mécanisme de mouvement supplémentaire du pied ont été fabriqués à partir de matériaux non ferreux (plastique, aluminium, laiton) pour la sécurité MR.
L’actionneur ERF utilise des champs électriques variables, plutôt que magnétiques, pour modifier la viscosité du fluide et n’est donc pas affecté par les champs magnétiques du scanner IRM. L’actionneur ERF est enfermé dans une coque cylindrique en cuivre qui est reliée au conducteur de blindage du câble coaxial HV ; ce câble est, à son tour, mis à la terre sur le panneau de pénétration de la cage de Faraday du scanner IRM. Cela empêche le bruit radiofréquence potentiel de la tension variable appliquée à l’actionneur d’affecter le scanner et empêche les champs magnétiques variables du scanner d’induire des courants dans les câbles, ce qui pourrait modifier la viscosité de l’ERF. Le câble HT continue à l’extérieur du panneau de pénétration jusqu’à l’amplificateur HT. Des connecteurs coaxiaux MHV (miniature haute tension) sont utilisés, qui offrent une sécurité supplémentaire lors du transport de tensions allant jusqu’à 4 kV (Figure 2).
Les câbles séparés du codeur optique et du capteur de pesage ont des blindages qui sont également mis à la terre sur le panneau de pénétration, empêchant ainsi leurs signaux (en particulier les signaux numériques provenant des canaux du codeur) d’affecter soit le scanner, soit la sortie du capteur de charge à petite tension. Les câbles blindés et mis à la terre à l’extérieur du panneau de pénétration transportent les signaux vers le module d’acquisition de données (DAQ). La sortie de la cellule de charge, qui utilise un pont de Wheatstone compensé en température, est amplifiée par un amplificateur d’instrumentation fixé aux bornes d’entrée analogiques de l’DAQ, fournissant un facteur d’amplification de 1 000x.
Le module DAQ exécute le micrologiciel à l’aide du langage de script Lua (Supplemental Coding File 1). Le script chargé sur le module DAQ s’exécute à une fréquence de boucle de 500 Hz, et le module lit le signal de l’encodeur et de la cellule de charge amplifiée, convertit les lectures du capteur en valeurs de longueur et de force, et les stocke dans des registres de mémoire pour l’accès et l’enregistrement par une interface utilisateur m-file (UI ; Graphique 3) sur l’ordinateur portable hôte (Fichier de codage supplémentaire 2). L’ordinateur portable hôte envoie les valeurs de force cible pour la dorsiflexion et la flexion plantaire, les paramètres du contrôleur en boucle fermée et les commandes de réinitialisation de l’encodeur à des registres de mémoire supplémentaires sur le module DAQ si nécessaire. Le script DAQ exécute une boucle de contrôle qui détecte la direction du mouvement de la pédale afin de déterminer la force à exercer : dorsiflexion ou flexion plantaire. Il calcule ensuite une tension de sortie proportionnelle à la différence entre les valeurs de force mesurée et la valeur cible, délimitée par 0 V et 4 V, qui est la plage d’entrée admissible de l’amplificateur HT. L’ERF réagit à l’amplitude du champ électrique appliqué ; l’inversion de la tension ne réduit pas la viscosité en dessous de celle du fluide non alimenté (sans champ électrique), de sorte que la sortie DAQ est limitée à un minimum de 0 V. L’acquisition de données quantifie (résolution de 12 bits) et échantillonne (500 Hz) les tensions analogiques, ce qui permet d’obtenir une sortie en escalier vers l’amplificateur HT qui peut provoquer des composants haute fréquence dans la sortie HT en raison des changements rapides à chaque étape. L’amplificateur HV a des bandes passantes de signal petites et grandes de 35 kHz et 8 kHz, respectivement, donc pour réduire la possibilité que du bruit RF détectable par le scanner soit généré, la sortie DAQ utilise un filtre RC de premier ordre avec une fréquence de -3 dB à environ 900 Hz, de sorte que les fréquences plus élevées sont presque éliminées. De plus, le dispositif à pied est positionné à l’extérieur de l’alésage du scanner près du pied du lit, minimisant ainsi toute interaction entre les capteurs de l’appareil, l’actionneur et le scanner. L’amplificateur, avec un gain de 1 000 V/V et une sortie de crête de 4 kV, génère des champs à travers l’écart ERF jusqu’à 4 kV/mm ; bien que la tension de claquage du fluide ERF ne soit pas signalée par le fournisseur, la viscosité et d’autres paramètres sont décrits jusqu’à ce niveau. Le cylindre ERF peut exercer une force d’un peu plus de 200 N lorsqu’il est complètement sous tension et qu’il est déplacé à la vitesse cible. La longueur du bras de moment où la bielle rejoint la pédale est de 56 mm, ce qui permet d’obtenir un couple maximal d’environ 11,2 Nm. C’est plus que suffisant pour les sujets atteints de parésie du pied ; Cependant, il peut être maîtrisé par des sujets forts et en bonne santé. Les composants matériels sont répertoriés dans la table des matériaux.
L’utilisation du dispositif du pied s’appuie sur les paradigmes d’entraînement et de test développés avec les dispositifs de préhension antérieurs 3,4,5,6,7,8,16 et d’autres travaux 11,17,18. Au moment de la publication, ce dispositif a été utilisé avec des sujets victimes d’AVC chronique présentant des déficits liés au pied pour étudier les changements neuroplastiques induits par la thérapie via l’imagerie par résonance magnétique et les évaluations quantitatives de la performance.
Comme décrit dans le protocole ci-dessous, les sujets subissant un balayage sont allongés sur le dos sur le lit du scanner, et leur tête est immobilisée dans la bobine de tête du scanner et positionnée à l’isocentre du scanner. Le dispositif de pied est positionné et verrouillé en place de sorte que la jambe du sujet testé soit droite et que son pied soit attaché à la pédale correspondante de l’appareil. De cette manière, la flexion de la cheville ne provoque pas de poussée ou de traction contre l’appareil, ce qui pourrait déplacer la position de la tête à l’intérieur de la bobine. Un cadre miroir est positionné devant les yeux du sujet, lui permettant de voir un écran de projection qui affiche des instructions et des repères visuels pour la tâche motrice.
Au cours de la tâche, le sujet voit soit un signe « + » pendant les périodes de repos, soit un métronome visuel pendant les tests, dans lequel un cercle se déplace de haut en bas sur l’écran (cible), et un autre cercle est affiché qui se déplace sous le contrôle de la position de la pédale de l’appareil (curseur ; Figure 4). On demande aux sujets de suivre de près le mouvement de la cible. La vitesse cible est déterminée de manière à ce que la force de réaction visqueuse non alimentée de l’appareil (les forces visqueuses augmentent avec l’augmentation de la vitesse) soit suffisamment faible pour que n’importe quel sujet puisse la surmonter, avec des forces accrues appliquées sous contrôle informatique.
La robotique est facile à déployer, applicable à diverses déficiences motrices, a une grande fiabilité de mesure et a la capacité de fournir un entraînement de haute intensité10. Ce dispositif basé sur ERF fournit une force de résistance contrôlée numériquement au sujet, et cet appareil est sécurisé par MR lorsqu’il est couplé à des composants non ferreux/non magnétiques, ainsi que compatible MR en raison de l’utilisation d’une électronique mise à la terre et blindée12. Il présente des avantages par rapport aux appareils connexes en ce sens qu’il est portable et relativement simple à utiliser, ce qui signifie qu’il peut être utilisé à la fois dans des environnements cliniques et à domicile, où une thérapie régulière peut être effectuée sans les coûts liés aux déplacements ou à l’établissement clinique. Le dispositif peut produire une résistance contrôlée par ordinateur et variant dans le temps en flexion plantaire et en dorsiflexion pour faciliter la création de routines de réadaptation spécifiques au patient et, ainsi, comble une lacune dans le domaine des dispositifs de réadaptation disponibles dans le commerce.
D’autres dispositifs de recherche existent mais n’étaient pas adaptés à la recherche actuelle pour diverses raisons. Certains appareils sont statiques, mesurant les forces appliquées de manière isométrique19 plutôt que sur l’amplitude de mouvement du sujet (RoM). Les appareils à base d’élastique appliquent une force croissante avec un déplacement croissant, plutôt qu’une résistance constante sur le RoM, et doivent être ajustés manuellement pour modifier les niveaux de force 20,21,22. L’utilisation de poids fixes et de charges gravitationnelles15,23 ne permet pas le contrôle informatisé des charges ou de différentes charges pour la flexion plantaire et la dorsiflexion. Les dispositifs pneumatiques24, 25, 26 permettent des variations de force entre les essais et une force constante sur l’ensemble de la RoM ; cependant, les vannes devraient être placées à une distance du scanner, de sorte que, généralement, ce dispositif ne serait pas en mesure de basculer rapidement entre les forces de flexion plantaire et de dorsiflexion lors du changement de direction du pied et n’aurait pas les capacités de réponse en fréquence des actionneurs ERF. Les moteurs électromagnétiques peuvent être utilisés27 dans l’environnement du scanner, mais uniquement en étendant le mécanisme suffisamment loin pour maintenir la sécurité et la compatibilité IRM, ce qui limite la portabilité et augmente le risque d’accident si l’un des composants du moteur est amené trop près de l’alésage. L’hydraulique28 peut être bidirectionnelle à différents niveaux de force, mais présente des défis similaires à l’utilisation de moteurs électromagnétiques en ce sens que le compresseur/pilote (généralement non compatible MR) doit être éloigné de l’alésage, limitant ainsi la portabilité et la réponse en fréquence. L’hydraulique a été combinée avec les systèmes ERF29 afin que le système puisse rétroentraîner l’effecteur final (pied ou dispositif de préhension) et fournir une résistance isométrique ; cependant, cette capacité n’était pas nécessaire pour la présente recherche et a été ajoutée au prix de l’utilisation de moteurs hydrauliques non compatibles avec l’IRM.
L’appareil pour le pied offre une combinaison de caractéristiques qui permettent ce qui suit : des exercices thérapeutiques précis et cohérents de contrôle du pied pendant de longues périodes ; la mesure de la capacité de performance motrice actuelle du sujet et l’ajustement de la difficulté de la tâche au fur et à mesure de la réadaptation ; contrôle en temps réel et réglage indépendant de la force appliquée en flexion plantaire et en dorsiflexion ; télécommande et réglage de la force de résistance sans interruption pour le réglage manuel ; et la sécurité et la compatibilité MR.
Protocole
Toutes les expériences ont été approuvées par l’Institutional Review Board du Massachusetts General Hospital et réalisées comme approuvé au Centre Athinoula A. Martinos pour l’imagerie biomédicale. Le consentement de la personne concernée pour l’utilisation et le partage de données anonymisées a été obtenu.
REMARQUE : Dans la présente étude, les critères d’inclusion étaient les suivants : (1) hémiparésie droite ou gauche avec mouvement résiduel de la jambe à la suite d’un AVC ischémique/ACM survenu ≥6 mois plus tôt ; (2) un score de30 sur 4-5 (le sujet se déplace avec un assistant pour naviguer dans les escaliers/surfaces inégales ou sans l’aide d’un assistant) ; (3) un score de 5 à 14 (léger/modéré) sur l’échelle NIHSS (National Institutes of Health Stroke Scale)31 ; (4) la capacité de rester debout pendant 5 minutes et de marcher 10 m ; (5) Âgés de 18 à 80 ans. À la suite des premiers essais, un critère supplémentaire a été inclus, qui consistait à vérifier que les sujets pouvaient déplacer la pédale sur au moins 5° de mouvement avec le pied parétique. Des données ont été recueillies sur les données démographiques, les facteurs de risque d’AVC, la durée de la physiothérapie ou de l’ergothérapie, la durée du séjour à l’hôpital pendant la phase aiguë, l’utilisation de médicaments, les infections intercurrentes et les complications.
1. Sélection et préparation des sujets
- Lors du recrutement, rencontrez les sujets potentiels, et testez leur capacité à déplacer les pédales de l’appareil avec leur pied parétique.
- Vérifiez l’ajustement du pied de chaque sujet dans les pédales de l’appareil. Pour les sujets ayant des pieds plus petits, testez l’ajustement de leurs pieds lorsqu’ils portent des baskets ou des chaussures similaires sans danger pour l’IRM.
- Les sujets qui ne peuvent pas exercer une force suffisante pour déplacer la pédale sur une amplitude de mouvement d’au moins 5° avec l’appareil sans tension doivent être exclus de l’étude.
- Avant l’arrivée, demandez aux sujets d’apporter les chaussures testées si cela est jugé nécessaire lors du précontrôle. Enregistrez les informations sur le sujet et obtenez le consentement éclairé conformément au protocole institutionnel.
- Chaque jour de test, dépister les sujets pour les contre-indications telles que spécifiées dans la politique de l’établissement de RM. Obtenez des renonciations signées dans le cas de sujets ayant des tatouages présentant un potentiel d’irritation et/ou de sensations de brûlure et toute autre renonciation spécifique à l’établissement.
- Demandez au sujet de mettre une blouse ou un pantalon approuvé par l’établissement et d’attendre d’être appelé dans la salle de scanner. Rangez les effets personnels du sujet conformément à la politique de l’établissement. S’il est jugé nécessaire, demandez au sujet de mettre les chaussures.
2. Configuration du dispositif de pied à résistance contrôlée
REMARQUE : Il est recommandé de terminer les étapes 2.1 à 2.3 avant l’arrivée du sujet.
- Installation dans la salle d’assistance IRM
- Placez l’amplificateur HT avec le module DAQ attaché sur le sol, à proximité du panneau de pénétration. Branchez le cordon d’alimentation CA dans la prise murale, branchez le câble coaxial HT dans les bornes de l’amplificateur HT et dans la fiche coaxiale MHV sur le panneau de pénétration, et branchez le câble du capteur dans la fiche correspondante sur le panneau de pénétration. Allumez l’interrupteur d’alimentation principal de l’amplificateur HV.
- Branchez la prise USB B du câble USB dans le module DAQ et la prise USB A du câble dans le câble du répéteur USB. Étendez le câble du répéteur USB de la salle de support IRM à la salle de contrôle IRM, et fixez le câble au sol à l’aide de ruban adhésif si nécessaire pour éviter que le personnel ou le sujet ne se déplace dans l’établissement.
- Activez le projecteur de salle de scanner.
- Installation dans la salle de contrôle IRM
- Placez l’ordinateur portable hôte du dispositif à pied à côté de l’interface du scanner IRM, branchez l’alimentation électrique et allumez l’ordinateur portable. Démarrez l’application MATLAB et chargez le programme d’interface utilisateur (UI).
- Branchez le câble USB de la boîte de boutons/signal de déclenchement du scanner IRM, le câble du projecteur de la salle de scanner et le câble du répéteur USB sur l’ordinateur portable.
- Si ce n’est pas déjà fait, ajustez les paramètres de l’écran de l’ordinateur portable de sorte que la fenêtre principale soit prolongée sur l’écran du projecteur à droite de la fenêtre principale de l’ordinateur portable. Déplacez le pointeur de la souris sur le côté droit de la fenêtre principale de l’ordinateur portable et vérifiez qu’il se déplace dans le champ de vision de l’écran du projecteur. Replacez le pointeur de la souris sur la fenêtre principale.
REMARQUE : Les formats du signal de déclenchement et du câble du projecteur peuvent différer d’un équipement à l’autre. Des adaptateurs vidéo ou des unités similaires peuvent être nécessaires.
- Installation dans la salle des scanners
- Vérifiez que la table du scanner est complètement à l’extérieur de l’alésage du scanner et qu’elle est complètement abaissée.
- Montez une bobine de tête dans la fente correspondante sur la table du scanner. Retirez la partie supérieure de la bobine et placez-la sur le côté. Couvrez les coussins de la table du scanner et la partie inférieure de la bobine de tête avec un drap de lit d’hôpital.
- Montez l’écran du projecteur dans l’alésage à l’extrémité opposée de la table du scanner.
- Insérez deux paires de vis de montage en laiton dans les fentes de montage de la bobine vers l’extrémité du pied de la table du scanner et placez le dispositif au pied entre les paires de vis. Fixez sans serrer les supports de fixation en plastique aux vis et aux trous d’alignement de la plaque de base du dispositif à pied (Figure 1A).
- Fixez le capteur et les câbles HT aux fiches du panneau de pénétration. Assurez-vous que les câbles ne sont pas enroulés autour de la table ou qu’ils ne risquent pas de se pincer ou de s’emmêler lorsque la table est déplacée dans l’alésage du scanner. Assurez-vous que le capteur et les câbles HV sont rallongés sans boucles entre le dispositif de pied et le panneau de pénétration.
- Démarrez le programme d’interface utilisateur dans la salle de contrôle (exécutez le script m-file) et vérifiez que les communications ont été établies entre l’ordinateur portable hôte et le module DAQ en observant le message de confirmation dans l’interface utilisateur (Figure 3).
- Acceptez les proportions de niveau de force par défaut dans la boîte de dialogue initiale de l’interface utilisateur en cliquant sur le bouton OK . Attendez que les boîtes de dialogue de confirmation s’affichent et se ferment d’elles-mêmes, ainsi que la fenêtre graphique initiale en direct de la force et du déplacement apparaissent.
- S’assurer que, pendant qu’un membre du personnel déplace la pédale de l’appareil dans son amplitude de mouvement et qu’un autre membre du personnel observe les traces de force et de déplacement, la trace de déplacement se déplace de -35° à +18° et vers l’arrière et que la trace de force montre des forces positives pour les mouvements dans le sens de la dorsiflexion, des forces négatives pour les mouvements dans le sens de la flexion plantaire, et revient à zéro au repos. Cela confirme le fonctionnement des capteurs, du module DAQ, de l’amplificateur HT et de l’actionneur ERF (Figure 3A).
- Si les signaux semblent normaux, cliquez sur Continuer dans la fenêtre du graphique en direct, puis sur le bouton Arrêter dans la boîte de dialogue de confirmation. Si ce n’est pas le cas, vérifiez les connexions des câbles et des connexions d’alimentation, puis refaites les étapes de configuration si nécessaire.
- Alignement du sujet et du dispositif du pied
- Escortez le sujet de la salle d’attente à la salle des scanners. Effectuer un dépistage des métaux conformément à la politique de l’établissement pour vérifier la présence d’objets ou d’implants non signalés. Fournissez au sujet des bouchons d’oreille de protection.
- Demandez au sujet de s’asseoir sur la table, puis de s’allonger sur le dos, la tête nichée dans la partie inférieure de la bobine de tête. Fournir de l’aide au besoin. Placez un rembourrage entre la tête du sujet et les parois de la bobine de tête pour vous assurer que le mouvement de la tête est empêché pendant l’imagerie.
- Demandez au sujet de redresser ses jambes. Déplacez l’appareil à pied vers ou loin du sujet jusqu’à ce que ses talons (ou les talons de ses chaussures) reposent sur les repose-pieds de l’appareil pour les pieds. Ajustez davantage pour aligner le pivot principal des pédales avec les chevilles du sujet.
- Fixez le dispositif de pied en place à l’aide des supports de retenue en plastique et des écrous à oreilles en plastique.
- Demandez au sujet de retirer le pied non testé de sa pédale et de le reposer légèrement à proximité du dispositif de pied. Soutenez la jambe non testée avec des oreillers si nécessaire. Fixez le pied testé dans la pédale de son dispositif à l’aide de sangles de retenue auto-agrippantes, en vous assurant que la plante du pied du sujet (ou l’avant de la chaussure du sujet) est en contact avec la pédale.
REMARQUE : Dans la présente étude, avec les sujets non témoins (AVC), le pied affecté par l’AVC a été testé en premier. Une fois l’essai du pied affecté terminé, ce pied a été retiré de la pédale, et le pied non affecté a été monté dans la pédale correspondante en utilisant le même processus qu’à l’étape 2.4.5. - Fournissez un dispositif d’alarme à mesure que l’ampoule est à pression, demandez-lui d’appuyer sur l’ampoule pour la tester et rappelez-lui qu’à tout moment, il peut appuyer sur l’ampoule pour communiquer avec les techniciens.
- Soulevez la table MR à pleine hauteur pour que le sujet puisse voir l’écran de projection à travers l’ensemble miroir.
- Installez la partie supérieure de la bobine de tête et montez l’ensemble de miroir de visualisation sur la bobine de tête. Vérifiez que le sujet peut voir clairement l’écran du projecteur dans le miroir.
3. Test de force du sujet
- Redémarrez l’interface utilisateur. Acceptez les proportions de niveau de force par défaut, ou ajustez-les si le protocole d’étude l’exige, puis cliquez sur le bouton OK comme ci-dessus. Lorsque les traces de force/déplacement sont apparues, demandez au sujet de déplacer le pied testé aussi loin que possible dans le sens de la dorsiflexion et de revenir à la flexion plantaire complète trois fois. Vérifiez que les traces de déplacement et de force semblent normales comme ci-dessus. Cela permet d’établir l’amplitude de mouvement pour l’essai, qui peut être inférieure à celle de l’amplitude totale du dispositif de pied (figure 3A).
- Si les résultats sont acceptables, cliquez sur Continuer dans la fenêtre du graphique en direct et sur Oui - Continuer dans la boîte de dialogue de confirmation ; cliquez sur Non-Réessayer si le sujet n’a pas suivi correctement les instructions de flexion ; ou cliquez sur Aller à l’arrêt s’il y a d’autres problèmes, et dépannez si nécessaire.
- Lorsque la boîte de dialogue de confirmation de la date et de l’heure s’affiche, cliquez sur Oui - Continuer dans la boîte de dialogue, ou cliquez sur d’autres options si vous souhaitez un autre nom de fichier ou un arrêt.
- Demandez au sujet de déplacer son pied testé en flexion plantaire complète, puis cliquez sur OK dans la boîte de dialogue de confirmation. Une fenêtre d’instruction/métronome apparaîtra (étiquetée sur la Figure 3). À l’aide de la souris, faites glisser cette fenêtre dans le champ de vision de l’écran de projection, puis cliquez sur OK pour confirmer que cette opération est terminée.
- Vérifiez que les instructions relatives au sujet sont affichées sur le projecteur. Vérifiez que le pied du sujet reste en flexion plantaire complète, et cliquez sur OK dans la boîte de dialogue correspondante. Le graphique de l’interface utilisateur passe à l’affichage du dynamomètre avec des indications des points de consigne de la force de résistance.
- Le métronome visuel décrit ci-dessus apparaît sur l’écran de projection avec un cercle cible solide se déplaçant vers le haut ou vers le bas sur l’écran à une vitesse constante et un curseur circulaire ouvert contrôlé par la position de la pédale de l’appareil. Demandez au sujet de bouger son pied pour que le curseur suive de près le mouvement de la cible. Si le sujet peut se déplacer avec succès dans toute son amplitude de mouvement tout en suivant la cible, cliquez sur (Fd, Fp) + 10 sur le graphique en direct pour augmenter les points de consigne de force pour la dorsiflexion et la flexion plantaire (Figure 3B).
- Observez si le sujet continue de suivre le mouvement du métronome avec précision.
- Si c’est le cas, cliquez à nouveau sur (Fd, Fp) + 10 pour augmenter les deux points de consigne de force. Si la dorsiflexion ne peut pas être terminée mais que la flexion plantaire continue de suivre le mouvement cible, cliquez une fois sur (Fd, Fp) - 10 et cliquez deux fois sur Fp + 10 pour réduire la force de résistance à la dorsiflexion d’un pas et augmenter la résistance plantaire d’un pas.
- Si la force de dorsiflexion a été réglée mais que le sujet ne peut plus suivre le métronome en flexion plantaire, cliquez une fois sur Fp - 10 , puis cliquez sur Continuer dans la fenêtre du graphique en direct. Les niveaux de force actuels sont utilisés par le programme UI comme points de référence pour les forces proportionnellement réduites appliquées pendant la phase de test.
- Si le point de consigne de la force de flexion plantaire a atteint le réglage maximum de l’appareil pour le pied, appuyez sur Continuer dans le graphique en direct et continuez.
REMARQUE : L’étape 3.7.3 se produit généralement pour les sujets témoins ayant une force de jambe normale et pour le membre non affecté chez les sujets victimes d’un AVC, car ils dépassent les capacités de l’appareil, qui est conçu pour se concentrer sur la force du membre affecté. - Notez les points de consigne de force (indiqués à droite du tracé de force) pour référence future. Cliquez sur Oui - Continuer pour continuer, Non - Tester à nouveau pour répéter, ou Arrêter s’il y a d’autres problèmes. Demandez au sujet de déplacer le pied testé jusqu’à ce qu’il se déplace complètement plantaire, puis de se détendre.
- Passez en revue l’utilisation de la poire à pression, la séquence de balayage et la tâche avec le sujet, et répondez à toutes les questions que le sujet pourrait avoir avant le début des balayages.
- Demandez au sujet de fermer les yeux pendant cette étape. Utilisez la ligne laser de marquage du scanner pour localiser la bobine de tête/la position de la tête du sujet. Déplacez la table pour centrer la tête du sujet dans l’alésage du scanner. Demandez au personnel de quitter la salle des scanners et de fermer la porte.
4. Exécution de la session d’IRM et de la tâche du dispositif au pied
- Effectuez l’enregistrement du sujet spécifique à l’installation et chargez le protocole de balayage. Informez le sujet que la séquence de balayage anatomique commencera et qu’il peut se détendre pendant cette partie du protocole, et demandez-lui de presser le bulbe pour vérifier sa compréhension. Lancez le balayage anatomique et attendez la fin.
- Comme indiqué par la fenêtre de dialogue fournie par l’interface utilisateur, informez le sujet que la partie IRMf et dispositif plantaire de l’étude commencera, et dites-lui qu’il doit s’assurer que son pied testé est en flexion plantaire complète, qu’il doit ramener son pied en flexion plantaire complète lorsqu’une croix de fixation apparaît à l’écran, et qu’ils doivent suivre le métronome visuel lorsqu’il apparaît. Cliquez sur OK dans la boîte de dialogue d’instructions.
- Suivez les instructions qui demandent à l’opérateur de préparer l’ordinateur de contrôle du scanner pour lancer la partie IRMf du protocole. Cliquez sur OK dans la fenêtre de dialogue d’instructions et lancez la séquence IRMf. Le programme d’interface utilisateur envoie automatiquement les paramètres de force souhaités au module DAQ.
REMARQUE : Dans la présente étude, la tâche de métronome visuel a été effectuée trois fois pour les membres affectés et non affectés par l’AVC à des niveaux de force de 60 %, 40 % et 20 % des niveaux maximaux définis à l’étape 3.7. Les niveaux de force sont mis à jour automatiquement à chaque répétition de l’essai. - Le sujet voit ses instructions affichées sur l’écran du projecteur. Un signe « + » (croix de fixation) apparaît, au cours duquel, comme indiqué précédemment, le sujet se repose.
- La cible du métronome visuel s’affiche avec le cercle plein se déplaçant de haut en bas à vitesse constante. Comme indiqué précédemment, le sujet déplace son pied testé en dorsiflexion et en flexion plantaire pour que le curseur circulaire ouvert suive la cible.
REMARQUE : Dans l’étude actuelle, les phases de repos (croix de fixation) et active (métronome) étaient de longueur égale, et le cycle a été répété sept fois. Au cours de la phase de métronome, il y avait deux cycles de dorsiflexion et de flexion plantaire à travers l’amplitude de mouvement. Ces paramètres peuvent être ajustés dans le script de l’interface utilisateur pour d’autres études. Chaque phase d’IRMf/métronome a duré environ 5 min 40 s. - Répétez les étapes 4.4 et 4.5 pour un total de sept cycles, après quoi la croix de fixation s’affiche et le sujet se repose.
- Répétez les étapes 4.2 à 4.6 pour un total de trois cycles.
- Entrez dans la salle d’IRM et basculez le pied monté dans le dispositif de pied conformément à l’étape 2.4.5. Répétez la section 3 du protocole pour le deuxième pied.
- Répétez la section 4 du protocole, en contournant les étapes 4.1 et 4.8 (enregistrement, balayage anatomique, changement de pied).
- Informez le sujet que la partie DTI de l’examen commencera et qu’il peut se détendre pendant cette phase de l’étude, et demandez-lui d’appuyer sur l’ampoule pour confirmer sa compréhension. Lancez l’analyse DTI et attendez la fin de l’analyse.
5. Opérations post-test
- Déplacez la table et le sujet hors de l’alésage du scanner et abaissez la table. Retirez l’ensemble du miroir, la section supérieure de la bobine de tête et le rembourrage autour de la tête du sujet. La protection auditive peut être jetée à ce moment-là.
- Aidez le sujet à s’asseoir et à se déplacer vers le vestiaire si nécessaire. Le sujet peut maintenant reprendre ses vêtements habituels.
- Parlez au sujet, répondez à toutes les questions post-test qu’il pourrait avoir, organisez la planification des rendez-vous futurs et remplissez les formulaires de paiement de l’allocation avant le départ du sujet.
- Démontez et emballez le matériel, puis démontez le dispositif de cheville de la table du scanner. Détachez les câbles HT et du capteur du panneau de pénétration. Détachez la boîte de boutons et les câbles du moniteur de l’ordinateur portable hôte. Rangez l’appareil de cheville et le matériel de support dans des étuis de transport.
- Effectuer un nettoyage spécifique à l’installation de la table du scanner et des surfaces de travail et de l’équipement pertinents.
- Extrayez les données des dossiers temporaires du système de numérisation pour une analyse hors ligne. Effectuez les procédures de déconnexion.
Résultats
Les résultats décrits ici concernent la compatibilité IRM du dispositif de pied, une analyse des résultats de balayage fonctionnel typiques et des notes sur le dispositif de pied.
La sécurité de l’appareil pour le pied a été évaluée par le personnel du Centre Athinoula A. Martinos et testée pour sa compatibilité IRM dans un scanner IRM 3 T. Pour les essais fantômes à l’aide d’une bouteille contenant une solution de 1,24 g de NiSO4·6H2O et 2,62 g de NaCl pour 1 000 g de H2O, le dispositif à pied a été fixé à la table du scanner à ~85 cm de l’extrémité de l’alésage, près de la ligne de 500 mt, à peu près dans la position nécessaire pour que le pivot de la pédale soit aligné avec l’articulation de la cheville d’un sujet, les jambes étendues. Les images des tests fantômes ont été capturées à l’aide des mêmes séquences de balayage que celles utilisées pour l’imagerie IRMf du sujet (avec auto-étalonnage généralisé, acquisition partiellement parallèle [GRAPPA] utilisée pour une résolution spatiale accrue et une sensibilité BOLD [dépendante du niveau d’oxygénation du sang]). Ces tests ont été effectués à la fois avec l’appareil en place mais inactif et avec l’appareil actif, l’un des auteurs déplaçant les pédales pour simuler l’activité du sujet et l’excitation de l’amplificateur HT sous le contrôle du module DAQ. Dix images ont été sélectionnées à partir des balayages dans chaque condition.
Les régions d’intérêt (ROI) dessinées au bord et au centre de l’image (Figure 5) ont été utilisées pour calculer le bruit de fond et le signal, respectivement ; Les moyennes du signal à chaque endroit étaient stables d’une période à l’autre, puisqu’elles s’écartaient de <0,2 % de la moyenne centrale sur les 10 acquisitions dans chaque condition. Il n’y avait pas de différence statistique (P = 0,1215, test t à deux échantillons, 10 répétitions/condition) dans le rapport entre le signal central et le signal de fond pour le test fantôme avec le dispositif de pied inactif (30,24 ± 2,31, sans dimension ; Graphique 5Aa) et l’essai fantôme avec le dispositif de pied actif (27,94 ± 3,76 ; Figure 5Ab). Cela suggère que ni l’activité HV ni les signaux du capteur n’ont eu d’effet sur les images IRM.
Les images acquises avec six volontaires qui se sont allongés dans le scanner et ont effectué la tâche de la même manière que les sujets ont montré que le dispositif au pied n’affectait pas le rapport signal/bruit (SNR) ou la qualité de l’image (Figure 5Ba, Bb, sans et avec le dispositif actif, respectivement).
Des activations typiques dans la M1 et la SMA (zone motrice supplémentaire) pour un sujet témoin ont été superposées aux images de l’atlas pour montrer la valeur statistique t liée à l’activité du mouvement par rapport à l’état de repos avec le dispositif de cheville passif (Figure 5Bd) et actif (Figure 5Be). Les différences de forme et de valeurs t ont été affectées par les différences dans la force appliquée pendant l’activité de mouvement et la variation de l’activité normale du cerveau à différents points de temps. Le suivi de ces images au fil du temps, pendant et après l’entraînement fournit des données permettant d’identifier les changements dans le cerveau affecté par l’AVC.
Les capteurs de force et de déplacement n’étaient pas non plus sensibles à l’électricité statique ou aux champs magnétiques variables dans le temps du scanner. Les enregistrements ont été collectés avec le dispositif de pied en place sur la table d’IRM à la fois avec la séquence d’IRMf active et avec le dispositif de pied dans un environnement de laboratoire non IRM, et ces enregistrements étaient indiscernables (valeurs de codeur stables dans les deux cas, ≤1 bit de bruit dans les enregistrements de force).
Conception du dispositif de pied à résistance contrôlée
Ledispositif de poignée MR_CHIROD v2 3,4,5,6,7,8 fournit le mécanisme de base du dispositif de pied, qui convertit la réponse linéaire de la poignée du dispositif de poignée en mouvement angulaire de la pédale autour de l’articulation de la cheville du sujet via un mécanisme à manivelle. Le dispositif de pied peut être monté sur les rails de montage hélicoïdal du lit d’IRM pour fournir une plate-forme solide qui est réglable en position pour s’adapter à la taille du sujet. Les pédales sont munies de sangles de retenue pour maintenir le pied en place lors de la flexion et de la dorsiflexion plantaires. Les entretoises ou les chaussures décalent le pied du sujet par rapport à la surface de base de la pédale et du dispositif de retenue du talon pour s’assurer que le centre de rotation de la cheville est aligné avec l’axe de la pédale. Cela minimise le mouvement axial de la jambe, empêchant ainsi la traduction du mouvement vers la tête du sujet pendant le balayage et l’apparition d’une excitation cérébrale non liée au mouvement du pied. Les pédales couplées gauche et droite permettent l’utilisation de l’appareil avec des patients touchés par un accident vasculaire cérébral de part et d’autre du cerveau. Pendant les tests, le genou du côté non testé est plié et soutenu par des coussinets pour éloigner le pied non testé de la pédale inutilisée. L’ancien dispositif de poignée et les nouveaux composants du MR_COFID (dispositif au pied) sont assemblés à partir de métaux non ferreux et de composants en plastique, et les appareils utilisent une électronique blindée. L’appareil a été évalué pour la sécurité de l’IRM au Centre Athinoula A. Martinos et testé pour sa compatibilité IRM, sans qu’aucun problème n’ait été observé sur l’imagerie fantôme. Les capteurs de force et de déplacement n’étaient pas sensibles à l’électricité statique ou aux champs magnétiques variables dans le temps du scanner.

Figure 1 : Dispositif MR-COFID. (A) 1 : Cylindre à fluide électro-rhéologique (ERF), cage de Faraday ; 2 : encodeur optique ; 3 : cellule de charge ; 4 : pédale et pivot ; 5 : Supports de retenue. (B) Détails du cylindre ERF : 1 : piston et arbre ; 2 : Fluide ER sous pression ; 3 : Écart de champ HV ; 4 : Retour de liquide RE. Le débit et les pressions s’inversent pour la course de retour. (C) Rotation de la pédale autour de l’axe de la cheville ; liaison de transmission pour la transformation de la force linéaire ERF en couple angulaire de la cheville. Veuillez cliquer ici pour voir une version agrandie de cette figure.
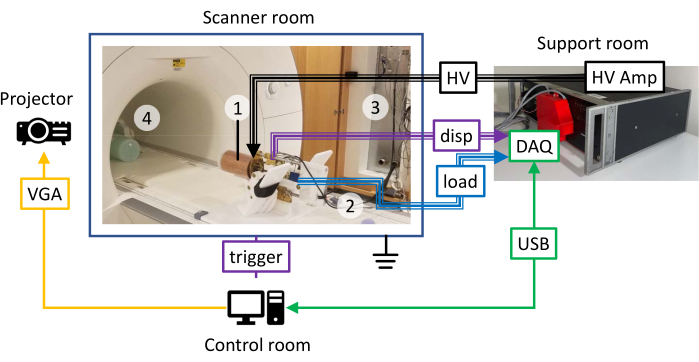
Figure 2 : Schéma de la configuration du dispositif de pied dans le scanner, le contrôle et les salles d’assistance. (1) Cage de Faraday autour du cylindre ERF, (2) câbles blindés pour l’alimentation HT, et (3) câbles d’encodeur et de cellule de charge avec blindages mis à la terre sur le panneau de pénétration du scanner IRM. (4) Fantôme cylindrique dans la bobine de tête au niveau de l’isocentre du scanner. Veuillez cliquer ici pour voir une version agrandie de cette figure.
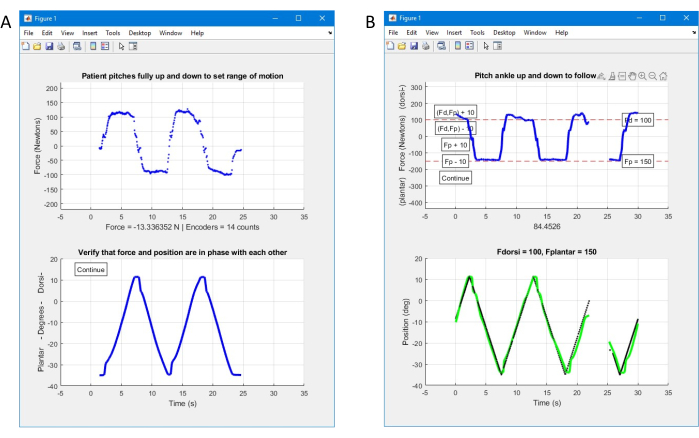
Figure 3 : Interface opérateur. (A) Interface initiale permettant de vérifier le fonctionnement de l’appareil et de mesurer l’amplitude de mouvement du sujet. (B) Deuxième interface pour établir le niveau de force du sujet en dorsiflexion et en flexion plantaire. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 4 : Instructions de fixation, croix de fixation et métronome visuel présentés au sujet. (A) Instructions affichées pendant l’essai d’amplitude de mouvement. (B) Instructions avant chaque phase de test pendant l’IRMf. (C) Croix de fixation affichée pendant les phases de repos. (D) Métronome visuel : un cercle fermé (cible) se déplace de haut en bas dans un cadre ovale tandis que le sujet contrôle un cercle ouvert (curseur) par flexion du pied pour suivre la cible. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 5 : Imagerie fantôme et du sujet. (A) Résultats d’imagerie fantôme (a) sans et (b) avec le dispositif de pied actif et avec l’analyse des ROI à l’intérieur du fantôme et à la périphérie du balayage. (B) Le fonctionnement du robot au pied n’affecte pas les images ou les activations humaines EPI. (a) Contrôle sans le robot au pied dans la salle du scanner. (b) Pas continu avec le robot à pied dans la salle de scanner. (c) Image en (b) moins l’image en (a). Activations, y compris en M1 et SMA (flèches) (d) avec le dispositif de cheville inactif et (e) énergisé à 60 % de la force maximale du sujet. Les valeurs statistiques t sont affichées (barre de couleur), indiquant une excitation statistiquement significative du cerveau pendant le mouvement par rapport à l’excitation au repos, superposées aux images de l’atlas. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Fichier de codage supplémentaire 1 : Pied pour Jove.lua - Micrologiciel de script Lua téléchargé sur le module DAQ. Veuillez cliquer ici pour télécharger ce fichier.
Fichier de codage supplémentaire 2 : FootDevice_forJove.m - Script de fichier m pour l’interface opérateur et les affichages pour les sujets. Le fichier de fonction auxiliaire est fourni dans le Fichier de codage supplémentaire 3. Veuillez cliquer ici pour télécharger ce fichier.
Fichier de codage supplémentaire 3 : ShutdownLabJackIfAbort.m - fonction auxiliaire m-file utilisée Veuillez cliquer ici pour télécharger ce fichier.
Discussion
Étapes critiques
Le pré-test de la capacité d’un sujet à générer au moins un mouvement minimal de la pédale avec son pied parétique est crucial. Un score FAC de 4 ou 5 et la capacité de se tenir debout pendant une période minimale reflètent la capacité combinée d’un sujet entre ses membres non affectés et parétiques, et ne reflètent pas la capacité de bouger le pied parétique seul. Dans la présente étude, l’un des objectifs principaux était de stimuler les changements neuroplastiques dans la région de la blessure par le biais d’une thérapie intensive impliquant le pied affecté, ainsi que l’examen de l’excitation dans le cerveau. Les sujets qui ne peuvent pas générer au moins le niveau de force requis et bouger la pédale seront incapables de suivre le métronome visuel ou de participer au paradigme d’entraînement associé – une séance de thérapie gamifiée dans laquelle un avatar vidéo se déplace dans une grotte ondulante tout en évitant les collisions avec les parois.
À l’étape 2.4 du protocole, le pied du sujet est fixé à la pédale et le dispositif à pied est positionné après que la tête du sujet a déjà été stabilisée à l’intérieur de la bobine de tête. Il est important de prévoir un rembourrage décalé sous la semelle et derrière le talon du pied et/ou de la chaussure afin que l’axe de mouvement de la cheville du sujet soit aligné avec le pivot principal du dispositif pour le pied. Si cela n’a pas été réalisé avec une précision raisonnable, lorsque le sujet fléchit son pied de haut en bas, sa jambe tendue sera poussée et tirée, ce qui transmettra à la tête du sujet, provoquant potentiellement un mouvement de la tête et produisant des artefacts de mouvement dans les scans IRMf.
Limitations
Comme mentionné ci-dessus, l’une des limites de cette itération de l’appareil est qu’il existe une exigence minimale de force de résistance, ce qui empêche les sujets présentant un certain niveau de parésie sévère d’utiliser l’appareil avec le seul membre affecté. Les études et les thérapies qui n’ont pas la restriction d’un seul membre peuvent utiliser les deux pédales simultanément, de sorte que l’aide peut être fournie par le membre non affecté. La tentative d’exercer un effort avec le membre affecté combinée au mouvement physique rendu possible par le membre assistant peut avoir des avantages, mais cet effet dépassait le cadre de l’étude dans le cadre de laquelle le dispositif de protection du pied a été initialement développé. Cette limitation pourrait être résolue dans une version ultérieure du dispositif, soit en remplaçant l’ERF actuel par un autre ayant une viscosité non alimentée plus faible, soit en redessinant le piston et le cylindre ERF. Cela augmenterait la plage de force dynamique et permettrait aux sujets plus gravement handicapés de participer à des études et de bénéficier d’une thérapie avec les successeurs de l’appareil.
Bien que le dispositif à pied n’ait été utilisé que pour générer une résistance à force constante pour un mouvement donné dans l’étude actuelle, il ne s’agit pas d’une limitation du dispositif. L’interface utilisateur peut être reprogrammée pour présenter des tâches de suivi de cible plus complexes qu’un simple métronome visuel, et/ou la force de résistance peut être modifiée de manière continue ou inattendue, ce qui signifie que le sujet devrait s’ajuster pour suivre la trajectoire. Le jeu d’entraînement mentionné ci-dessus fait un usage limité de chemins plus complexes (sous des forces uniformes) et permet à l’utilisateur de choisir entre les branches montantes et descendantes à différents moments pour aider à maintenir l’intérêt pendant les sessions d’entraînement prolongées. Des recherches futures pourraient établir que des stimuli plus complexes peuvent engendrer un remodelage neuronal et une récupération de fonction plus rapides.
Importance
Divers facteurs peuvent entraîner des handicaps à la cheville et affecter négativement la vie quotidienne, notamment l’obésité, l’activité physique excessive ou limitée, le vieillissement, les pathologies congénitales, les blessures, etc. Parmi eux, les handicaps neurologiques causés par des accidents vasculaires cérébraux ou des blessures à la colonne vertébrale ont la réadaptation la plus longue et la plus difficile. Les protocoles de rééducation conventionnels nécessitent un programme d’exercices intensifs utilisant des bandes de résistance, des rouleaux en mousse et des planches de rotation. Ces appareils simples ne peuvent pas fournir les informations quantitatives nécessaires au suivi du processus de réadaptation et à la personnalisation de la thérapie. De plus, ils ne peuvent pas administrer un traitement à forte dose et à haute intensité de manière constante. De nombreux robots de rééducation du mouvement du pied ont été développés pour surmonter ces limitations avec différentes architectures et caractéristiques de conception, notamment des orthèses actives, des exosquelettes et des robots basés sur des plates-formes32.
Parmi les appareils de mouvement du pied compatibles avec l’IRM, peu sont orientés vers la réadaptation. Certains appareils fournissent des stimuli de faible force et de haute fréquence sur une petite surface de la plante du pied pour susciter une activation cérébrale plutôt que pour soutenir une réadaptation fonctionnelle réaliste33,34. D’autres se concentrent sur la mesure de la cinématique ou de la force sans fournir une résistance suffisante ou prédéfinie 19,35,36,37,38,39. Quelques systèmes de rééducation compatibles avec l’IRM pour fournir une résistance liée à la marche sont soit pneumatiques25,40, soit utilisent des bandes élastiques21. Le dispositif de pied actuel utilise un type d’actionnement réglable dynamiquement à l’aide de fluides électrorhéologiques, qui peuvent modifier leur viscosité en réponse aux champs électriques appliqués. Comme le montre le dispositif de poignée précurseur, par rapport aux autres technologies d’actionnement, les ERF permettent une résistance rapide, précise et forte combinée dans un design compact et portable 41,42,43.
La réadaptation traditionnelle dépend généralement d’une pratique répétitive axée sur les tâches à l’intensité et à la durée nécessaires pour atteindre un plateau dans la capacité réacquise. Ainsi, la capacité d’un patient à obtenir un résultat positif en matière de rétablissement dépend soit de la motivation intrinsèque initiale du patient, soit des capacités motivationnelles extrinsèques/intrinsèques d’un thérapeute compétent. Le suivi clinique post-AVC est laborieux et imprécis. La couverture d’assurance pour la physiothérapie est limitée à 150 jours consécutifs pour un premier AVC44, et les patients qui ne répondent pas bien aux traitements précoces ne devraient généralement pas s’améliorer45. L’expérience de l’entraînement surveillé par imagerie et dispensé par robot à l’aide du dispositif de préhension suggère que la fenêtre de physiothérapie pour les patients victimes d’un AVC peut ne jamais se fermer 3,5,6,8,46. Les mesures dérivées de l’imagerie peuvent être meilleures que les évaluations cliniques en tant que prédicteurs du succès thérapeutique potentiel et peuvent fournir des informations pour guider une planification thérapeutique améliorée et individualisée. Les données obtenues suggèrent que les améliorations motrices acquises par l’entraînement persistent à long terme3. Cette ligne de travail a le potentiel d’apporter un changement de paradigme dans les soins de santé de l’AVC et de renouveler l’espoir pour les patients victimes d’AVC chronique.
Comme la neuroplasticité a été détectée à partir des prédicteurs de résultats basés sur les résultats avec le dispositif robotique de préhension 3,8,46,47,48, le développement d’un dispositif robotique induit par le pied (MR_COFID) compatible avec l’IRM a été proposé. Après la préhension, l’utilisation du pied est une cible critique pour la rééducation, car le dysfonctionnement du pied induit par un accident vasculaire cérébral provoque des trébuchements et des chutes49. Les résultats attendus de ce travail pourraient améliorer les résultats de l’AVC chronique, réduire les coûts grâce à une réadaptation accélérée et à un allègement du fardeau des soins après la réadaptation, et améliorer la qualité de vie des patients. Il deviendra de plus en plus important d’explorer le potentiel d’offrir une formation en réadaptation évolutive et efficace grâce à des approches innovantes, compte tenu de la réduction prévisible des budgets de santé et d’événements imprévus tels que la pandémie actuelle.
Déclarations de divulgation
Aucun des auteurs n’a de conflit d’intérêts à divulguer.
Remerciements
Ce travail a été soutenu par une subvention du National Institute of Neurological Disorders and Stroke (numéro de subvention 1R01NS105875-01A1) des National Institutes of Health à A. Aria Tzika. Ce travail a été effectué au Centre Athinoula A. Martinos d’imagerie biomédicale. Nous tenons à remercier le directeur, le Dr Bruce R. Rosen, M.D., Ph.D., et les membres du personnel du Centre Martinos, ainsi que le Dr Michael Moskowitz, M.D., pour leurs conseils et leur soutien. Enfin, nous remercions Virtumed, LLC pour la fabrication de l’appareil.
matériels
| Name | Company | Catalog Number | Comments |
| 3T MRI scanner | Siemens Medical Solutions USA, Inc., Malvern, PA | Magnetom Skyra | https://www.siemens-healthineers.com/en-us/magnetic-resonance-imaging/3t-mri-scanner/magnetom-skyra |
| Data acquisition unit (DAQ) | LabJack Corp., Lakewood, CO | T4 | https://labjack.com/news/labjack-t4 |
| High voltage amplifier | Trek, Inc., Lockport, NY | Model 609C-6 | https://www.manualsdir.com/manuals/268654/trek-609e-6-high-voltage-power-amplifier.html?page=2&original=1 |
| Matlab | The Mathworks, Ltd., Natick, MA | n/a | https://www.mathworks.com/ |
| USB repeater cable | Tripp Lite, Chicago, IL | U026-10M | https://assets.tripplite.com/product-pdfs/en/u02610m.pdf |
Références
- Stinear, C. M., Ward, N. S. How useful is imaging in predicting outcomes in stroke rehabilitation. International Journal of Stroke. 8 (1), 33-37 (2013).
- Heiss, W. D. Contribution of neuro-imaging for prediction of functional recovery after ischemic stroke. Cerebrovascular Diseases. 44 (5-6), 266-276 (2017).
- Astrakas, L. G., et al. Improving motor function after chronic stroke by interactive gaming with a redesigned MR-compatible hand training device. Experimental and Therapeutic. 21 (3), 245(2021).
- Astrakas, L. G., Li, S., Elbach, S., Tzika, A. A. The severity of sensorimotor tracts degeneration may predict motor performance in chronic stroke patients, while brain structural network dysfunction may not. Frontiers in Neurology. 13, 813763(2022).
- Astrakas, L. G., et al. Peak activation shifts in the sensorimotor cortex of chronic stroke patients following robot-assisted rehabilitation therapy. The Open Neuroimaging Journal. 14 (1), 8-15 (2021).
- Mintzopoulos, D., et al. Connectivity alterations assessed by combining fMRI and MR-compatible hand robots in chronic stroke. NeuroImage. 47, T90-T97 (2009).
- Mintzopoulos, D., et al. fMRI of rehabilitation in chronic stroke using MR-compatible robots. Proceedings of the International Society for Magnetic Resonance in Medicine. 16, 3285(2008).
- Mintzopoulos, D., et al. Functional MRI of rehabilitation in chronic stroke patients using novel MR-compatible hand robots. The Open Neuroimaging Journal. 2 (1), 94-101 (2008).
- Crafton, K. R., Mark, A. N., Cramer, S. C. Improved understanding of cortical injury by incorporating measures of functional anatomy. Brain. 126 (7), 1650-1659 (2003).
- Huang, V. S., Krakauer, J. W. Robotic neurorehabilitation: A computational motor learning perspective. Journal of Neuroengineering and Rehabilitation. 6 (1), 5(2009).
- Carey, L. M., Seitz, R. J. Functional neuroimaging in stroke recovery and neurorehabilitation: Conceptual issues and perspectives. International Journal of Stroke. 2 (4), 245-264 (2007).
- Khanicheh, A., Mintzopoulos, D., Weinberg, B., Tzika, A. A., Mavroidis, C. MR_CHIROD v.2: Magnetic resonance compatible smart hand rehabilitation device for brain imaging. IEEE Transactions on Neural Systems and Rehabilitation Engineering. 16 (1), 91-98 (2008).
- Baggett, B. D., Young, G. Ankle joint dorsiflexion. Establishment of a normal range. Journal of the American Podiatric Medical Association. 83 (5), 251-254 (1993).
- de Asla, R. J., Wan, L., Rubash, H. E., Li, G. Six DOF in vivo kinematics of the ankle joint complex: Application of a combined dual-orthogonal fluoroscopic and magnetic resonance imaging technique. Journal of Orthopaedic Research. 24 (5), 1019-1027 (2006).
- Hosseini Ghomi, R., Bredella, M. A., Thomas, B. J., Miller, K. K., Torriani, M. Modular MR-compatible lower leg exercise device for whole-body scanners. Skeletal Radiology. 40 (10), 1349-1354 (2011).
- Ottensmeyer, M. P., Li, S., De Novi, G., Tzika, A. A. Functional MRI in conjunction with a novel MRI-compatible hand-induced robotic device to evaluate rehabilitation of individuals recovering from hand grip deficits. Journal of Visualized Experiments. (153), e59420(2019).
- Carey, J. R., et al. fMRI analysis of ankle movement tracking training in subject with stroke. Experimental Brain Research. 154 (3), 281-290 (2004).
- Dong, Y., Dobkin, B. H., Cen, S. Y., Wu, A. D., Winstein, C. J. Motor cortex activation during treatment may predict therapeutic gains in paretic hand function after stroke. Stroke. 37 (6), 1552-1555 (2006).
- Newton, J. M., et al. Reliable assessment of lower limb motor representations with fMRI: Use of a novel MR compatible device for real-time monitoring of ankle, knee and hip torques. NeuroImage. 43 (1), 136-146 (2008).
- Francescato, M. P., Cettolo, V. Two-pedal ergometer for in vivo MRS studies of human calf muscles. Magnetic Resonance in Medicine. 46 (5), 1000-1005 (2001).
- Doolittle, J. D., et al. Evaluating a novel MR-compatible foot pedal device for unipedal and bipedal motion: Test-retest reliability of evoked brain activity. Human Brain Mapping. 42 (1), 128-138 (2021).
- Naimon, N. D., et al. A low-cost Mr compatible ergometer to assess post-exercise phosphocreatine recovery kinetics. Journal of Magnetism and Magnetic Materials. 30 (3), 281-289 (2017).
- Raymer, G. H., Allman, B. L., Rice, C. L., Marsh, G. D., Thompson, R. T. Characteristics of a MR-compatible ankle exercise ergometer for a 3.0 T head-only MR scanner. Medical Engineering & Physics. 28 (5), 489-494 (2006).
- Meyerspeer, M., Krssak, M., Kemp, G. J., Roden, M., Moser, E. Dynamic interleaved 1H/31P STEAM MRS at 3 Tesla using a pneumatic force-controlled plantar flexion exercise rig. Journal of Magnetism and Magnetic Materials. 18 (5), 257-262 (2005).
- Hollnagel, C., et al. Brain activity during stepping: A novel MRI-compatible device. Journal of Neuroscience Methods. 201 (1), 124-130 (2011).
- Quistorff, B., Nielsen, S., Thomsen, C., Jensen, K. E., Henriksen, O. A simple calf muscle ergometer for use in a standard whole-body MR scanner. Magnetic Resonance in Medicine. 13 (3), 444-449 (1990).
- Ryschon, T. W., et al. A multimode dynamometer for in vivo MRS studies of human skeletal muscle. Journal of Applied Physiology. 79 (6), 2139-2147 (1995).
- Sinha, S., Shin, D. D., Hodgson, J. A., Kinugasa, R., Edgerton, V. R. Computer-controlled, MR-compatible foot-pedal device to study dynamics of the muscle tendon complex under isometric, concentric, and eccentric contractions. Journal of Magnetic Resonance Imaging. 36 (2), 498-504 (2012).
- Unluhisarcikli, O., et al. A robotic hand rehabilitation system with interactive gaming using novel electro-rheological fluid based actuators. Proceedings of 2010 IEEE International Conference on Robotics and Automation. IEEE. , 1846-1851 (2010).
- Mehrholz, J., Wagner, K., Rutte, K., Meiner, D., Pohl, M. Predictive validity and responsiveness of the Functional Ambulation Category in hemiparetic patients after stroke. Archives of Physical Medicine and Rehabilitation. 88 (10), 1314-1319 (2007).
- Lyden, P., et al. Underlying structure of the National Institutes of Health Stroke Scale: Results of a factor analysis. Stroke. 30 (11), 2347-2354 (1999).
- Alvarez-Perez, M. G., Garcia-Murillo, M. A., Cervantes-Sanchez, J. J. Robot-assisted ankle rehabilitation: a review. Disability and Rehabilitation: Assistive Technology. 15 (4), 394-408 (2020).
- Hao, Y., et al. Novel MRI-compatible tactile stimulator for cortical mapping of foot sole pressure stimuli with fMRI. Magnetic Resonance in Medicine. 69 (4), 1194-1199 (2013).
- Gallasch, E., et al. Contact force- and amplitude-controllable vibrating probe for somatosensory mapping of plantar afferences with fMRI. Journal of Magnetic Resonance Imaging. 24 (5), 1177-1182 (2006).
- Noble, J. W., Eng, J. J., Boyd, L. A. Bilateral motor tasks involve more brain regions and higher neural activation than unilateral tasks: An fMRI study. Experimental Brain Research. 232 (9), 2785-2795 (2014).
- Martinez, M., et al. MRI-compatible device for examining brain activation related to stepping. IEEE Transactions on Medical Imaging. 33 (5), 1044-1053 (2014).
- Trinastic, J. P., et al. An fMRI study of the differences in brain activity during active ankle dorsiflexion and plantarflexion. Brain Imaging and Behavior. 4 (2), 121-131 (2010).
- de Lima-Pardini, A. C., et al. An fMRI-compatible force measurement system for the evaluation of the neural correlates of step initiation. Scientific Reports. 7 (1), 43088(2017).
- Promjunyakul, N. O., Schmit, B. D., Schindler-Ivens, S. M. A novel fMRI paradigm suggests that pedaling-related brain activation is altered after stroke. Frontiers in Human Neuroscience. 9, 324(2015).
- Zhang, T., et al. An MRI-compatible foot-sole stimulation system enabling characterization of the brain response to walking-related tactile stimuli. Frontiers in Neuroscience. 13, 1075(2019).
- Khanicheh, A., et al. MR compatible ERF-based robotic device for hand rehabilitation after stroke. Proceedings of the International Society for Magnetic Resonance in Medicine. 13, 1110(2005).
- Khanicheh, A., Mintzopoulos, D., Weinberg, B., Tzika, A. A., Mavroidis, C. MR_CHIROD v.2: A fMRI compatible mechatronic hand rehabilitation device. Proceedings of the 2007 IEEE 10th International Conference on Rehabilitation Robotics. , 883-889 (2007).
- Mintzopoulos, D., et al. On-line brain mapping using fMRI and a magnetic resonance compatible hand-induced robotic device (MR_CHIROD). Proceedings of the International Society for Magnetic Resonance in Medicine. 15, 3330(2007).
- Inpatient Rehabilitation Care. Medicare. , Available from: https://www.medicare.gov/coverage/inpatient-rehabilitation-care (2023).
- Benjamin, E. J., et al. Heart disease and stroke statistics-2017 update: A report from the American Heart Association. Circulation. 135 (10), e146(2017).
- Astrakas, L. G., Naqvi, S. H., Kateb, B., Tzika, A. A. Functional MRI using robotic MRI compatible devices for monitoring rehabilitation from chronic stroke in the molecular medicine era (Review). International Journal of Molecular Medicine. 29 (6), 963-973 (2012).
- Lazaridou, A., et al. Diffusion tensor and volumetric magnetic resonance imaging using an MR-compatible hand-induced robotic device suggests training-induced neuroplasticity in patients with chronic stroke. International Journal of Molecular Medicine. 32 (5), 995-1000 (2013).
- Lazaridou, A., et al. fMRI as a molecular imaging procedure for the functional reorganization of motor systems in chronic stroke. Molecular Medicine Reports. 8 (3), 775-779 (2013).
- Hyndman, D., Ashburn, A., Stack, E. Fall events among people with stroke living in the community: circumstances of falls and characteristics of fallers. Archives of Physical Medicine and Rehabilitation. 83 (2), 165-170 (2002).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon