Method Article
Visualisation de la résistance bactérienne à l’aide de sondes antibiotiques fluorescentes
Dans cet article
Résumé
Les antibiotiques étiquetés fluorescents sont des outils puissants qui peuvent être utilisés pour étudier de multiples aspects de la résistance aux antimicrobiens. Cet article décrit la préparation des antibiotiques fluorescents marqués et leur application à l’étude de la résistance aux antibiotiques chez les bactéries. Les sondes peuvent être utilisées pour étudier les mécanismes de résistance bactérienne (p. ex., efflux) par spectrophotométrie, cytométrie du débit et microscopie.
Résumé
Les antibiotiques fluorescents sont des outils de recherche polyvalents qui sont facilement utilisés pour l’étude de la résistance aux antimicrobiens, en raison de leur avantage significatif par rapport à d’autres méthodes. Pour préparer ces sondes, les dérivés de l’azide des antibiotiques sont synthétisés, puis couplés avec des alkyne-fluorophores utilisant le cycloaddition dipolar azide-alkyne par la chimie de clic. Après la purification, l’activité antibiotique de l’antibiotique fluorescent est testée par l’évaluation de la concentration inhibitrice minimale. Afin d’étudier l’accumulation bactérienne, la spectrophotométrie ou la cytométrie du débit peuvent être utilisées, permettant une analyse beaucoup plus simple que les méthodes reposant sur des dérivés antibiotiques radioactifs. En outre, la microscopie confocale peut être utilisée pour examiner la localisation au sein des bactéries, offrant des informations précieuses sur le mode d’action et les changements qui se produisent chez les espèces résistantes. L’utilisation de sondes antibiotiques fluorescentes dans l’étude de la résistance aux antimicrobiens est une méthode puissante avec beaucoup de potentiel d’expansion future.
Introduction
La résistance aux antimicrobiens (RMA) est une crise croissante qui constitue une menace majeure pour la santé humaine dans le monde entier. La résistance à la plupart des antibiotiques a été rapportée, et des infections causées par des bactéries résistantes à tous les médicaments cliniquement disponibles sont en train d’émerger. Afin de lutter contre la montée de l’AMR, nous devons mieux comprendre ce phénomène aux multiples facettes et les mécanismes sous-jacents et les interactions entre les antibiotiques et les bactéries. Un aspect qui a été historiquement mal compris est la perméation des antibiotiques dans les bactéries, avec les phénomènes d’accumulation et d’efflux. Ces connaissances sont cruciales dans la conception de nouveaux médicaments et la compréhension des mécanismes de résistance. Par conséquent, cela joue un rôle essentiel dans la recherche sur la RMA.
Il y a deux approches principales qui peuvent être prises afin de mesurer la concentration d’antibiotiques : mesurer le médicament directement ou marquer avec un moiety conçu pour faciliter la quantification. Bien que le marquage de l’antibiotique améliore la détection, cela peut perturber l’activité biologique du médicament, comme l’activité antimicrobienne et la perméabilité. Ce n’est pas un problème pour les méthodes non étiquetées; cependant, la détection peut être difficile. Au cours des dernières années, les progrès technologiques ont conduit à un boom de la recherche utilisant la spectrométrie de masse (MS) pour mesurer directement la concentration d’antibiotiques dans les bactéries1,2,3,4,5,6,7. Ces études ont montré qu’il est possible d’étudier l’accumulation intracellulaire dans une variété de bactéries, avec des bactéries gram-négatives les plus largement étudiées. Quantification de la perméabilité des molécules a ensuite été liée à l’activité et utilisée pour informer le développement de médicaments2,3,4, bien que la prudence doit être prise lors de la confondement direct de l’accumulation et l’activité cible5. Avant le développement de la SP, les seuls antibiotiques dont la concentration pouvait être directement mesurée étaient ceux qui possédaient une fluorescence intrinsèque, comme la tétracycline et les quinolones8,9,10,11. Bien qu’évidemment de portée limitée, l’accumulation et l’efflux ont été examinés et quantifiés, illustrant l’utilité de la quantification basée sur la fluorescence.
Les antibiotiques marqués ont été utilisés pendant de nombreuses décennies pour étudier les distributions, les modes d’action et la résistance, avec des étiquettes radioactives et fluorescentes étant communs. Les sondes radiomarquées ont l’avantage d’être presque identiques au composé parent, d’où l’activité biologique est peu susceptible d’être significativement différente. Des isotopes tels que 3H, 14C et 15N ont été fréquemment utilisés en raison de l’importance de ces éléments dans les antibiotiques, et une variété d’échafaudages antibiotiques ont été examinés1,10,12,13. Bien que la détection des radiosons soit simple, il existe un certain nombre de problèmes logistiques (p. ex., sécurité, demi-vie des isotopes) qui ont limité l’utilisation de cette approche. Une autre stratégie est les antibiotiques fluorescents. Ces sondes peuvent être utilisées pour examiner la distribution et les modes d’action et la résistance du médicament parent, en utilisant une technologie plus simple que la SP et sans les problèmes logistiques de rayonnement8. Le principal inconvénient de cette approche est que les antibiotiques sont généralement des molécules relativement petites, d’où l’introduction d’une moiety fluorescente pose un changement chimique important. Cette altération peut avoir un impact sur les propriétés physiochimiques et l’activité antibactérienne. Par conséquent, il faut prendre soin d’évaluer ces facteurs afin de générer des résultats représentatifs de l’antibiotique parent.
Dans ce travail, une méthode est décrite pour synthétiser, évaluer et utiliser des antibiotiques fluorescents, comme dans nos publications précédentes14,15,16. Grâce à des travaux antérieurs, un certain nombre d’antibiotiques fluorescents ont été préparés et utilisés à diverses fins (voir Stone et al.,8). Afin de minimiser la probabilité d’impact sur l’activité biologique, de très petits fluorophores sont utilisés dans ce travail: nitrobenzoxadiazole (NBD, vert) et 7-(dimethylamino)-2-oxo-2H-chromen-4-yl (DMACA, bleu). En outre, l’évaluation de l’activité antibactérienne à l’aide de la concentration minimale d’inhibition de dilution de microbroth (MIC) est décrite, de sorte que l’effet des modifications sur l’activité peut être mesuré. Ces sondes étiquetées fluorescentes peuvent être utilisées dans les essais spectrophotométriques, la cytométrie du débit et la microscopie. La gamme d’applications possibles est l’endroit où se trouve l’avantage des antibiotiques fluorescents. L’accumulation cellulaire peut être quantifiée, catégorisée et visualisée, ce qui n’est pas possible en utilisant la SP seule. On espère que les connaissances acquises grâce à l’utilisation d’antibiotiques fluorescents nous aideront à mieux comprendre la résistance et la lutte contre la RMA.
Protocole
1. Synthèse des alkyne-fluorophores
- Synthèse de NBD-alkyne (7-nitro-N -(prop-2-yn-1-yl)benzo[c][1,2,5]oxadiazol-4-amine)
- Dissoudre 1 031 mg de 4-chloro-7-nitro-benzofuran (5.181 mmol) dans 60 mL de tétrahydrofuran (THF). Ajouter 1 857 mg de CsCO3 (5,696 mmol), puis 0,39 ml de propargylamine (6,1 mmol). Chauffer la réaction à 50 oC pendant 2 h, qui passera du brun au vert, puis refroidir à la température ambiante (RT).
- Filtrer la réaction à l’aide d’une aide au filtrage (voir Tableau des matériaux)et laver à l’acétate d’éthyle (EA). Concentrez le filtrate sous pression réduite, puis dissoudrez les résidus dans 150 ml d’EA et passez à un entonnoir séparant de 500 ml.
- Laver la solution EA avec 100 ml d’eau et de saumure respectivement. Ensuite, combinez les phases aqueuses et lavez 2x avec 100 ml d’EA.
- Séchez les phases organiques combinées sur le sulfate de magnésium anhydre, puis filtrez et concentrez-vous sous pression réduite.
- Purifiez le produit brut par chromatographie flash sur gel de silice (20 à 30 % d’EA dans l’éther de pétrole [PE]), vérifiant la pureté par spectrométrie de masse de chromatographie liquide (LCMS, [M-H]- 219,1) et/ou la spectroscopie magnétique nucléaire (NMR), les changements chimiques comme suit :
1 Fois H NMR (CD3OD, 600 MHz) 8,54 (d, J 8,7 Hz, 1H), 6,35 (d, J - 8,4 Hz, 1H), 4,31 (dd, J -5,7 Hz, J -2,5 Hz, 2H), 2,43 (t, J - 2,5 Hz, 1H); 13 (en) C NMR (CD3OD, 150 MHz) 144,3, 143,7, 142,2, 135,8, 125,7, 100,0, 76,5, 74,2, 33,4.
REMARQUE : Lors de la purification par chromatographie de gel de silice, préparez la colonne en utilisant le moins de polar des solvants énumérés. Le composé brut peut être chargé comme solution concentrée ou adsorbed sur la silice si la solubilité ne le permet pas. Une fois que le composé a été ajouté au sommet de la silice, passer par 1 -2 volumes de colonne du même solvant utilisé pour mouiller la silice. Ensuite, commencez par le rapport solvant répertorié, en cours d’exécution à travers au moins 1 volume de colonne de chaque solvant, et en veillant à ne pas faire de grands sauts dans la composition du solvant. Recueillir des fractions, et vérifier la pureté / identité par LCMS ou TLC (chromatographie couche mince). Mélanger les fractions pures et concentrer sous pression réduite par évaporation rotative.
- Synthèse de DMACA-alkyne (2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl)-N-(prop-2-yn-1-yl)acetamide).
- Dissoudre 5,02 g de phénol 3-(dimethylamino) (36,6 mmol) dans 30 ml d’éthanol, puis ajouter 6,7 mL de diéthyle 1,3-acétoonedicarboxylate (36 mmol). Ajouter 10,5 g de ZnCl2 (77,2 mmol), puis refluxer la solution rouge pendant 42 h. Ajouter 9,20 g supplémentaires de ZnCl2 (67,6 mmol), puis reflux pendant 8 h.
- Refroidir la réaction et se concentrer sous pression réduite. Disperser le solide rouge résultant dans 200 mL d’EA, filtrer, puis transférer dans un entonnoir séparant de 500 ml.
- Laver l’EA avec 200 ml chacun d’eau et de saumure, puis sécher sur du sulfate de magnésium anhydre. Filtrer la phase organique séchée et se concentrer sous pression réduite.
- Purifiez le solide rouge (éthyle 2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl)acetate) par chromatographie flash sur gel de silice (0-100% EA en PE), vérifiant la pureté par LCMS ([M-H]- 275,1) et/ ou NMR, change chimique comme suit:
1 Fois H RMN (CDCl3, 600 MHz) 7,30 (d, J 8,9 Hz, 1H), 6,52 (dd, J - 8,9 Hz, J -2,6 Hz, 1H), 6,40 (d, J - 2,6 Hz, 1H), 5,87 (m, 1H), 2,96 (m, 8H), 2,25 (d, J 1,2 Hz, 3H). - Dissoudre 488 mg d’éthyle 2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl)acétate (1,18 mmol) dans 10 ml de THF, puis ajouter une solution de 157 mg de LiOH H2O (3,74 mmol) dans 15 ml d’eau. Remuer la réaction à RT pendant 3 h, puis passer à un entonnoir de séparation et diluer avec un supplément de 50 ml d’eau.
- Laver le mélange de réaction 2x avec 50 ml d’éther diététhyle (Et2O), puis laver la phase organique combinée 2x avec 25 ml d’eau. Prenez n’importe quel précipité jaune avec la couche organique. Concentrez la phase organique sous pression réduite à l’aide d’un évaporateur rotatif.
- Acidifier la phase aqueuse au pH 2 avec hCl concentré, et laisser refroidir jusqu’à 4 oC pendant la nuit. Filtrer la phase aqueuse acidifiée et ajouter le solide jaune à la phase organique concentrée.
REMARQUE: L’acide acétique 2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl) peut être utilisé sans autre purification, mais cela peut être vérifié par LCMS ([M-H]- 247.1) et /ou RmN, changements chimiques comme suit:
1 Fois H RMN (CDCl3, 600 MHz) 7,41 (d, J - 9,0 Hz, 1H), 6,62 (dd, J - 9,2 Hz, J -2,8 Hz, 1H), 6,52 (d, J - 2,8 Hz, 1H), 5,98 (d, J - 0,9 Hz, 1H), 3,05 (s, 6H), 2,35 (d, J 0,9 Hz, 2H); 13 (en) C RmN (CDCl3, 150 MHz) 162,2, 155,7, 152,9, 152,8, 125,3, 109,7, 109,3, 109,1, 108,8, 98,3, 40,2, 18,5. - Dissoudre 466 mg d’acide acétique de 2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl) (1,89 mmol) dans 7 mL d’azotesec,N-dimethylformamide (DMF) et placer sous une atmosphère d’azote.
- Dissoudre 0,33 ml de propargylamine (5,1 mmol) dans 7 ml de DMF sec sous azote. Ajouter 1,30 ml de di-isopropylethyl amine (DIPEA, 7,50 mmol) à la solution de colorant, puis 535 mg d’O-(1H-6-chlorobenzotriazole-1-yl)-1,1,3,3-tetramethyluronium hexafluororophosphate (HCTU, 1,29 m). Remuer la solution de colorant activé pendant 15 min à RT, puis ajouter la solution amine dropwise, et laisser remuer toute la nuit.
- Le lendemain, diluer la réaction avec 35 ml d’eau puis se concentrer sous pression réduite.
- Partitionner le solide orange qui en résulte entre l’EA et la saumure (100 ml chacun) dans un entonnoir séparant de 250 ml. Séparez les couches (exécutez les deux couches en flacons différents) et lavez la phase aqueuse avec 100 ml d’EA.
- Concentrez les phases organiques combinées sous pression réduite, puis redissolvez le solide orange en 3 ml d’acétonitrile 1:1 (ACN)/eau (v/v). Purififier le produit brut en injectant sur un système de chromatographie liquide à pression moyenne (MPLC) de phase inverse équipé d’une colonne de cartouche SC18 (solvant A : eau, solvant B : ACN).
- Vérifier les fractions de pureté par LCMS ([M-H]- 284,1, changements chimiques RMN donnés ci-dessous), puis combiner et lyophiliser les fractions appropriées pour donner 2-(7-(dimethylamino)-2-oxo-2H-chromen-4-yl)-N-(prop-2-yn-1-yl)acetamide, NMR shifts chemical as suit:
1 Fois H RMN (600 MHz, DMSO-d6) 8,65 (t, J 5,4 Hz, 1H), 7,52 (d, J - 9,0Hz, 1H), 6,72 (dd, J ' 9.1, 2.6 Hz, 1H), 6.55 (d, J '2.6 Hz, 1H), 6.00 (s, 1H), 3.88-3.87 (m, 2H), 3.62 (s, 2H), 3.13 (t, J '2.5 Hz, 1H), 3.01 (sH, 6); 13 (en) C NMR (125 MHz, DMSO-d6) 167,7, 160,7, 155,4, 152,9, 151,0, 126,0, 109,4, 109,1, 108,1, 97,5, 80,9, 73,3, 39,7, 38,4, 28,2.
2. Synthèse des antibiotiques fluorescents
- Préparer un dérivé de l’azide d’un antibiotique tel que décrit précédemment14,15,16.
REMARQUE : La procédure est spécifique à chaque antibiotique et exige un examen attentif de la relation d’activité de structure (SAR) de la molécule parente pour s’assurer que l’antibiotique fonctionnalisé conserve l’activité comparable au parent. (p. ex., ciprofloxacine16, linezolid14, et trimethoprim15). Voir Figure 1 pour des exemples d’antibiotiques fluorescents publiés, et le schéma de synthèse générale. - Cliquez sur la procédure de réaction A
REMARQUE : Pour la plupart des antibiotiques, suivez la procédure détaillée ici pour le huisgen catalysé au cuivre [2-3] cycloaddition de l’azide (étape 2.1) et de l’alkyne fluorescente (préparée à l’étape 1).- Placer l’azide-antibiotique dans un flacon de fond rond et ajouter tert-butanol (tBuOH) et de l’eau (1:1 v/v, 25 mL chacun par azide mmol).
- Ajouter le fluorophore-alkyne préparé à l’étape 1.1 (3 eq.) et chauffer la réaction à 50 oC. Ajouter ensuite le sulfate de cuivre (100 mm d’eau, 0,6 eq.) à la réaction, suivi de l’acide ascorbique (500 mm dans l’eau, 2,4 eq.).
- Remuer la réaction à 50 oC pendant 1 h, ou jusqu’à ce que l’analyse par LCMS sur indication de l’achèvement de la réaction (consommation complète d’azide de départ).
- Refroidir la réaction et purifier le cas échéant pour l’échafaudage d’antibiotiques et procéder à la purification soit par l’étape 2.3 ou 2.4.
REMARQUE : Plusieurs méthodes de purification différentes sont possibles, selon la polarité et la stabilité de l’échafaudage.
- Cliquez sur la procédure de réaction B
REMARQUE : Suivez cette procédure pour les antibiotiques à base de peptides, pour fournir des conditions de réaction plus fortes (travail non publié, Phetsang, 2019).- Placer l’azide-antibiotique peptide dans un flacon de fond rond et ajouter suffisamment de DMF (750 ml/mmol azide) pour se dissoudre.
- Ajouter le fluorophore-alkyne préparé à l’étape 1 (5 eq.) et chauffer la réaction à 50 oC pendant 1 h.
- Ajouter le cuivre (I) l’iodure (20 eq.), puis le DIPEA (120 eq.), puis l’acide acétique (240 eq.).
- Remuer la réaction à 50 oC pendant 1 h, ou jusqu’à ce que l’analyse par LCMS indique l’achèvement de la réaction (c.-à-d., la consommation complète d’azide de départ). Refroidir la réaction et procéder à la purification par la méthode 1 (voir l’étape 2.3).
- Méthode de purification 1 (utilisée pour la ciprofloxacine, le trimethoprim et la linézolid)
- Injectez la réaction de clic refroidie directement sur une colonne de cartouche SPLC C18.
- Incorporez une longue phase de lavage (environ 10 min) au début de la course (100% solvant A), puis exécutez un gradient jusqu’à 100% solvant B, suivi d’un retour au solvant A.
REMARQUE : Le solvant A peut être choisi à partir de l’eau, 0,05 à 0,1 % d’acide formique (FA) dans l’eau, 0,05 à 0,1 % d’acide trifluroacétique (AGT) dans l’eau, selon la solubilité, la stabilité et la meilleure résolution des pics. Le solvant B peut être choisi à partir de l’acétonitrile (ACN), de 0,05 à 0,1 % fa dans ACN, de 0,05 à 0,1 % dans aCN, pour correspondre au solvant A. Si l’élution s’avère difficile, le méthanol peut être utilisé à la place d’ACN. - Recueillir et combiner les fractions appropriées, comme indiqué par LCMS et la couleur (masse correcte vu, pic singulier), puis lyophiliser pour donner l’antibiotique fluorescent (semi)pur.
- Purifier davantage le produit si nécessaire. Évaluer la pureté par RMN et/ou LCMS et la chromatographie liquide à haute pression (HPLC), à l’aide d’une colonne et d’une méthode appropriées pour l’échafaudage.
- Méthode de purification 2
REMARQUE : Si la solubilité le permet, la prépurification peut être effectuée par l’accumulation aqueuse (utilisée pour les macrolides, œuvre inédite, Pierre 2019).- Diluer la réaction de clic refroidie avec de l’eau et Et2O (1:1 v/v, environ 10 fois dilution du volume de réaction initial), en transférant à un entonnoir de séparation de taille appropriée.
- Séparez les couches et lavez la phase aqueuse deux fois avec Et2O.
- Laver les phases organiques combinées 2x avec de l’eau (volume égal avec phase organique), puis sécher sur Na2SO4.
- Filtrer la phase organique séchée et se concentrer sous pression réduite.
- Purifie le produit brut par MPLC et/ou HPLC tel que décrit à l’étape 2.4.4.
REMARQUE : Consultez la figure 2 pour trouver des exemples de traces de lCMS de réaction par clic incomplètes, complètes et épurées. Les rendements purifiés typiques pour les réactions de clic d’antibiotique-fluorophore vont de 30 à 80%.
CAUTION : La plupart des produits chimiques utilisés dans ces synthèses possèdent des risques spécifiques pour la sécurité. La prudence doit être prise en tout temps, y compris l’utilisation d’équipement de protection individuelle. Et2O, tBuOH, FA, acide acétique, PE, EA, THF, ACN, DMF, EtOH, DIPEA, propargylamine, et HCTU sont tous inflammables; éviter tout contact avec la chaleur ou les sources d’étincelles. THF, propargylamine, DIPEA, tBuOH, FA, DMF, et PE sont tous toxiques; éviter l’exposition. Propargylamine, CsCO3, ZnCl2, LiOH-H2O, DIPEA, CuI, FA, acide acétique et HCl sont tous corrosifs; éviter tout contact et être conscient du contact de surface. ZnCl2, CuSO4, CuI, et PE présentent des risques environnementaux; être conscient des conditions d’élimination. THF peut former des peroxydes explosifs; prendre soin des conditions de stockage. Les azides organiques sont explosifs; prendre soin en particulier de la production à grande échelle.
3. Évaluation de l’activité antimicrobienne
REMARQUE : Tous les travaux impliquant des bactéries doivent être effectués dans des conditions stériles afin d’éviter la contamination de l’assay ou du laboratoire. Tous les supports doivent être autoclaved avant utilisation, et les plastiques et les équipements tels que les pipettes doivent être maintenus stériles. Il est recommandé de faire le travail dans une hotte de biocontenu (type 2).
- Streak stocks de glycérol de souches bactériennes appropriées pour l’échafaudage antibiotique sur l’agar bouillon lysogénie (LB, préparé selon les instructions du fabricant), et de croître pendant la nuit à 37 oC.
REMARQUE : Le choix des bactéries pour tester l’activité antibactérienne doit être fait en fonction de l’échafaudage antibiotique utilisé. Une gamme représentative de bactéries de 5 à 10 devrait être choisie parmi les espèces qui sont connues pour être sensibles à l’antibiotique, en tenant compte des capacités logistiques du laboratoire. Si possible, des bactéries résistantes devraient également être testées. Le protocole ci-dessous fonctionnera sur la plupart des bactéries, mais vérifiez si des conditions spéciales sont nécessaires (par exemple, CO2, médias spéciaux) et apporter des modifications au besoin. Les bactéries testées avec succès à l’aide de ces conditions comprennent Staphylococci, Streptococci, Bacilli, E. coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, et Enterococcus faecium. - Choisissez une seule colonie dans l’assiette, et la culture pendant la nuit dans 5 ml de cation ajustée Mueller-Hinton Broth (CAMHB, préparé selon les instructions du fabricant) à 37 oC.
- Diluer les cultures de nuit 40 fois en CAMHB et atteindre une phase médiane, la densité optique à 600 nm (OD600) de 0,4 à 0,8, volume 5 mL).
- Préparer les solutions de stock de chaque antibiotique fluorescent à 1,28 mg/mL dans de l’eau stérile, et pipette 10 l d’antibiotique à la première colonne d’une plaque de puits 96.
- Ajouter 90 L de CAMHB à la première colonne et 50 l à tous les autres puits. Ensuite, effectuez une dilution série2 sur la plaque.
- Mélanger soigneusement, puis diluer les cultures de phase de mi-log à 106 unités de formation de colonies (CFU)/mL et ajouter 50 L à tous les puits, pour fournir une concentration finale de 5 x 105 CFU/mL.
volume de culture (mL) (volume média en mL)/(OD600 x 1000)
p. ex., pour une culture OD600 -0,5 dans un volume média désiré de 12 ml, ajouter (12/(0,5 x 1 000) - 0,024 ml de culture à 12 ml de support - Couvrir les assiettes avec des couvercles et couver à 37 oC pendant 18 à 24 h sans trembler.
- Inspectez visuellement les plaques, le MIC étant le puits de concentration le plus bas sans croissance visible.
REMARQUE : Consultez le tableau 1 pour quelques exemples d’antibiotiques fluorescents actifs et inactifs.
4. Analyse de l’accumulation de sondes par spectrophotométrie et cytométrie de flux
REMARQUE : Ces temps de centrifugation ont été optimisés pour E. coli,de sorte que de légères modifications peuvent être nécessaires pour d’autres espèces. Des données représentatives pour l’accumulation de sonde sont rapportées pour la sonde de ciprofloxacine étiquetée NBD.
- Streak stocks de glycérol des souches bactériennes sur lb-agar et se développer pendant la nuit à 37 oC.
- Choisissez une seule colonie dans l’assiette et la culture pendant la nuit en LB à 37 oC.
- Diluer les cultures du jour au lendemain 50 fois dans les médias et passer à la phase médiane du journal (OD600 à 0,4 à 0,8).
- Centrifugeles les cultures à 1 470 x g pendant 25 min et décant les médias.
- Resuspendre la bactérie dans 1 ml de saline tamponnée par phosphate (PBS), puis centrifugeuse à 1 470 x g pendant 15 min.
- Décant les médias et de suspendre les granulés lavés dans PBS à un OD final600 2.
- Si désiré, ajouter 10,1 l de cyanure de carbonyle 3-chlorophenylhydrazone (CCCP, 10 mM en PBS) à 1 ml de bactéries (concentration finale de 100 m) et incuber à 37 oC pendant 10 min.
REMARQUE : LE CCCP est un inhibiteur de la pompe à efflux. L’ajout du PCPC permettra d’examiner l’impact de l’efflux. - Centrifuger les cultures à 18 000 x g pendant 4 min à 20 oC et décanter les médias.
- Ajouter 1 ml de solution antibiotique fluorescente (10 à 100 M en PBS) à la pastille, et couver à 37 oC pendant 30 min.
- Centrifuger les cultures à 18 000 x g pendant 7 min à 4 oC et décanter les médias.
- Resuspendre les bactéries dans 1 ml de PBS froid, et répéter l’étape 4.9.
- Répétez l’étape 4.10 un total de 4x.
- Si désiré, lysez les bactéries en ajoutant 180 l de tampon de lyse (20 mM Tris-HCl, pH 8,0 et 2 mM de sodium EDTA), puis 70 l de lysozyme (72 mg/mL en H2O).
- Incuber à 37 oC pendant 30 min, puis congeler-dégeler 3x (78 oC pendant 5 min, puis 34 oC pendant 15 min).
- Sonicate les échantillons pendant 20 min, puis chauffer à 65 oC pendant 30 min.
- Centrifuger les échantillons lysés (18 000 x g, 8 min), puis filtrer à travers une membrane de filtre de 10 kDa.
- Laver le filtre du 4x avec 100 l’eau.
- Transférer le lysate dans une plaque de puits noire à fond plat de 96 et mesurer l’intensité de la fluorescence sur un lecteur de plaque avec des longueurs d’onde d’excitation et d’émission appropriées pour le fluorophore (c.-à-d., DMACA : 400 nm,400 nm, 490 nm; NBD:ex 475 nm,em 545 nm).
REMARQUE : Voir La figure 3 pour des exemples d’analyses spectrophotométriques de bactéries utilisant l’antibiotique fluorescent de ciprofloxacine étiqueté NBD. - Pour l’analyse par cytométrie de flux, les mêmes conditions de croissance et de coloration peuvent être utilisées (étapes 4.1-4.17), avec des changements uniquement dans la préparation finale.
- Porter le volume total à 1 ml de PBS.
- Lisez des échantillons sur un cytomètre de débit à un débit d’environ 60 l/min, à l’aide d’amplification logarithmique pour l’acquisition de données (excitation F1 488 nm; émission de 525/20 nm).
- Enregistrez un total de 10 000 événements, puis analysez les données à l’aide d’un logiciel approprié.
- Tracer l’intensité de fluorescence de F1 par rapport au nombre d’événements compte, en estimant l’intensité médiane de fluorescence des pics d’histogramme après que la bactérie a été souillée.
REMARQUE : Voir La figure 4 pour des exemples d’analyses de cytométrie du débit de bactéries utilisant l’antibiotique ciprofloxacine étiqueté nbD.
5. Préparation à l’analyse microscopique
- Cultivez des sous-cultures à600 OD 0,4, comme pour l’évaluation du MIC, puis divisez-les en 1 ml d’aliquots et centrifugeuse à 18 000 x g pendant 3 à 5 min.
- Décantez et jetez les supports, puis suspendez à nouveau les granulés bactériens dans 500 l de HBSS.
- Centrifugeuse à 18 000 x g pendant 3 min, puis décantez et jetez les supports.
- Préparer des solutions de sondes antibiotiques dans HBSS à des concentrations de 1 à 100 M.
- Resuspendre les bactéries lavées dans 500 l de la solution de la sonde, et couver à 37 oC pendant 30 min.
- Répétez l’étape 5.3. Pour une expérience d’étiquetage multiple, resuspendre la pastille en 500 l d’un colorant d’acide nucléique orthogonally coloré. Pour le vert, utilisez Syto9 (5 M dans HBSS); pour le bleu, utilisez Hoechst 33342 (20 g/mL en HBSS). Incuber à RT pendant 15 à 30 min.
- Répétez l’étape 5.3, puis resuspend dans 500 'L de FM4-64FX (5 'g/mL dans HBSS) et incuber à RT pendant 5 min.
- Répétez l’étape 5.3, puis resuspend ezez dans 500 L de HBSS, et répétez l’étape 5.3 une fois de plus.
- Répétez l’étape 5.8, puis suspendez finalement les bactéries lavées et teints dans 15 'L du milieu de montage (voir tableau des matériaux).
- Pipette support de montage sur une lame de microscope et le dessus avec un glissement de couverture haute performance, puis sceller les bords avec du vernis à ongles clair.
REMARQUE : Voir Figure 5 pour des exemples d’images de microscopie confocales prises avec des antibiotiques à la ciprofloxacine et au triméthoprim étiquetés NBD, et figure 6 pour l’antibiotique à l’oxazolidinone (linezolid) étiqueté DMACA.
Résultats
Figure 1 Illustre la réaction de chimie de clic de clé (A) pour la préparation des antibiotiques fluorescents, et avec (B) des exemples de structures de nos antibiotiques fluorescents édités basés sur la ciprofloxacine (cipro), le trimethoprim (TMP), et le linezolid. Ces sondes ont toutes été synthétisées à partir des antibiotiques correspondants via un intermédiaire azide. Ils ont ensuite été couplés aux fluorophores NBD et DMACA, chacun fonctionnalisé avec un alkyne.
La figure 2 montre par exemple des traces de LCMS d’une réaction de clic ciprofloxacine-N3 et NBD-alkyne, où l’azide a eluté à 3,2 min et le produit à 3,8 min. La comparaison 1 et 2 montre comment la progression de la réaction au clic pourrait être suivie par la disparition du pic d’azide (par détecteur UV ou MS). Spectra 3 démontre l’impact de la purification, avec des pics erronés disparaissant des traces de SP et uv. La pureté et le progrès de réaction pourraient être quantifiés par l’intégration du pic du produit et de tout pic d’impureté.
La figure 3 démontre les résultats typiques de l’évaluation de l’accumulation intracellulaire par spectroscopie de fluorescence en présence et absence d’efflux. Dans cette expérience, E. coli a été traité avec TMP-NBD avec ou sans l’ajout de CCCP, qui s’effondre la force motrice de proton (PMF). La fluorescence intracellulaire des bactéries était significativement plus élevée lorsqu’elle était prétraitée avec CCCP, ce qui indique que l’efflux a réduit l’accumulation de ces bactéries. Cette expérience a été répétée à l’aide de bactéries déficientes en tolC, affichant la capacité de cet essais pour examiner l’impact des composants individuels de pompe d’efflux. Dans ce cas,bien qu’il y ait eu une augmentation de la fluorescence intracellulaire comparée aux bactéries sauvages de type, l’accumulation de CCCP a toujours augmenté. Ces résultats indiquent que tolC prend part à l’efflux TMP, mais n’est pas la seule pompe PMF-drive impliqués.
La figure 4 montre le résultat de la même expérience que la figure 2, mais avec l’accumulation mesurée par cytométrie de débit au lieu de la spectroscopie. Les mêmes tendances de données ont été observées, démontrant que l’une ou l’autre technique peut être employée pour étudier le phénomène de l’accumulation intracellulaire négociée d’efflux.
La figure 5 montre des images de microscopie confocale représentatives de sondes fluorescentes gram-positives (S. aureus) et gram-négatives (E. coli) étiquetées avec TMP-NBD (1) et cipro-NBD ( 2à 3) sondes fluorescentes, respectivement. Dans les deux cas, le colorant à membrane rouge FM4-64FX a été ajouté afin de comparer la co-localisation. Pour TMP-NBD, le colorant bleu acide nucléique Hoechst-33342 a également été utilisé. En superposant ces images, la localisation de l’antibiotique dans les bactéries a été visualisée. La comparaison des panneaux 2 et 3 montre comment l’impact de l’efflux a été examiné, avec l’inhibiteur de l’efflux CCCP utilisé dans 2, résultant en accumulation intracellulaire. Dans le panneau 3, aucun CCCP n’a été ajouté. Par conséquent, l’efflux est actif et aucune accumulation de sonde n’a été vue.
La figure 6 montre des images de microscopie confocale représentatives de bactéries Gram-positives (S. aureus) étiquetées avec la sonde l’oxazolidinone Lz-NBD étiquetée DMACA. Le colorant à membrane rouge FM4-64FX a été ajouté afin de comparer la co-localisation, et le colorant d’acide nucléique vert Hoechst-33342 a également été utilisé. En superposant ces images, la localisation de l’antibiotique dans les bactéries a été visualisée, montrant la localisation interne distincte de la membrane et de l’acide nucléique.
Le tableau 1 montre les valeurs du MIC pour trois séries d’antibiotiques fluorescents, la ciprofloxacine, le trimethoprim (TMP) et le linézolid (Lz), avec des données présentées pour les dérivés parent antibiotiques, NBD et DMACA de chacun. Des espèces représentatives pour chaque antibiotique ont été choisies, y compris gram-positive et gram-négative. Pour la série de ciprofloxacine, les deux sondes fluorescentes ont perdu l’activité antibiotique par rapport au médicament parent, mais ont conservé une certaine activité contre toutes les espèces. De même, les sondes linezolid ont perdu une certaine activité, mais sont restées un antibiotique modéré à faible. Les sondes TMP ont perdu presque toute activité contre les bactéries de type sauvage, mais étaient actives contre e. coli déficient e. coli, ce qui indique que la perte d’activité antibactérienne était due à un manque d’accumulation.

Figure 1 : Synthèse et structures de sondes dérivées d’antibiotiques. (A) Le schéma général de réaction pour la synthèse des sondes antibiotiques fluorescentes des azide-antibiotiques et des alkyne-fluorophores. (B) Les structures de nos sondes publiées basées sur la ciprofloxacine, le trimethoprim et le linezolid. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.

Figure 2 : Mesure de la pureté des sondes dérivées d’antibiotiques par LCMS. Les traces analytiques de LCMS de (1) incomplète, (2) complète, et (3) HPLC purifiéci ciprofloxacin-N3 - NBD-alkyne clic réactions démontrant la disparition du matériel de départ à l’achèvement de la réaction, et divers pics sur la purification. Une trace UV-Vis (absorption à 250 nm), trace B et MS (mode positif et négatif). Veuillez cliquer ici pour voir une version plus grande de ce chiffre.

Figure 3 : Mesure de lecteur de plaque de l’accumulation de sonde dérivée d’antibiotiques. Mesure spectroscopique de fluorescence de l’accumulation cellulaire de TMP-NBD (50 M) en nature sauvage (1, ATCC 25922) ettolC (2, ATCC 25922) E. coli incubé (A) avec et (B) sans ajout de CCCP (100 M). L’importance statistique (p '0,01; 'p '0,001) est indiquée entre l’absence ou la présence de CCCP et entre le type sauvage et letype de tolCE. coli. Les données rapportées sont la moyenne de SD pour trois expériences. Ce chiffre est adapté de notre publication précédente15, et illustre l’utilisation de la spectroscopie pour élucider le rôle de l’efflux sur l’accumulation intracellulaire. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.

Figure 4 : Mesure de cytométrie de flux de l’accumulation de sonde dérivée d’antibiotiques. Mesure de cytométrie de flux de l’accumulation cellulaire utilisant TMP-NBD dans le type sauvage (1, ATCC 25922) et letolC (2, ATCC 25922) E. coli incubé avec et sans ajout de CCCP (100 M). L’activité médiane de fluorescence est montrée à partir de 10 000 événements bactériens, l’importance statistique (md, p 0,001; - p , p - 0,0001) est indiquée entre l’absence et la présence de CCCP et entre le type sauvage et le type detolCE. coli. Les données rapportées sont la moyenne de SD pour trois expériences. Ce chiffre est adapté de notre publication précédente15, et illustre l’utilisation de la cytométrie de flux pour élucider le rôle de l’efflux sur l’accumulation intracellulaire. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.

Figure 5 : visualisation par microscopie confocale de la localisation de la sonde NBD. Images de microscopie confocales de 1) S. aureus en direct étiqueté avec Hoechst-33342 (bleu, acide nucléique), TMP-NBD (vert), FM4-64FX (rouge, membrane), et superposé; 2) E. coli vivant traité avec CCCP (inhibiteur d’efflux) étiqueté avec cipro-NBD (vert), FM4-64FX (rouge, membrane), et superposé; 3) E. coli vivant étiqueté avec cipro-NBD (vert), FM4-64FX (rouge, membrane), et superposé. Ce chiffre est adapté de nos publications précédentes15,16, et illustre l’utilisation de la microscopie pour examiner la localisation des sondes, y compris l’impact de l’efflux. Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
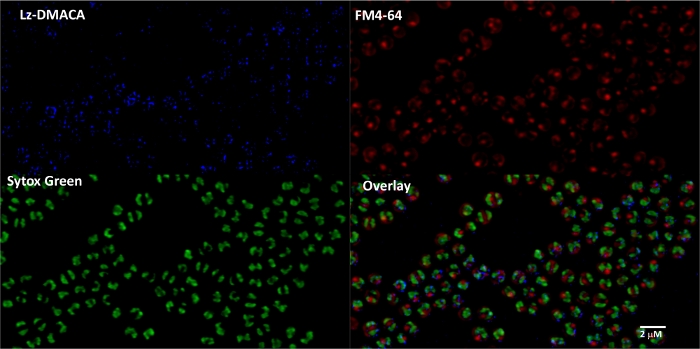
Figure 6 : visualisation par microscopie confocale de la localisation de la sonde DMACA. Images de microscopie confocales de S. aureus en direct étiquetéavec la sonde d’oxazolidinone Lz-DMACA (bleu), Sytox vert (vert, acide nucléique), et FM4-64FX (rouge, membrane). Veuillez cliquer ici pour voir une version plus grande de ce chiffre.
| MIC (g/mL) | |||||||||||
| Espèces | Souche | Cipro | Cipro-NBD (en) | Cipro-DMACA | Tmp | TMP-NBD (en) | TMP-DMACA (en) | Linezolid (Lz) | Lz-NBD | Lz-DMACA | |
| Staphylococcus aureus | ATCC 25923 | 0.125 - 0.5 | 32 à 64 ans | 16 | 1 | 16 | À l’autoricien | ||||
| ATCC 43300 | 1 | 16 | À l’autoricien | ||||||||
| Streptococcus pneumoniae | ATCC 700677 | 1 | 4 | 64 | |||||||
| Enterococcus faecium | ATCC 35667 | 1 - 8 | 32 | 32 à 64 ans | |||||||
| ATCC 51559 | 2 | 16 | 32 | ||||||||
| Klebsiella pneumoniae | ATCC 13883 | 0.015 - 0.06 | 8 - 16 | 8 - 32 | |||||||
| Pseudomonas aeruginosa | ATCC 27853 | 0.25 - 1 | 32 à 64 ans | 32 à 64 ans | |||||||
| Escherichia coli | ATCC 25922 | 0,004 euros | 8 | 2 | 0.5 | À l’autoricien | À l’autoricien | ||||
| Mutant 'tolC' | 0.125 | 0.25 | 2 | ||||||||
Tableau 1. Activités antibiotiques des sondes antibiotiques fluorescentes basées sur la ciprofloxacine, le trimethoprim, et le linezolid contre les souches bactériennes médicalement pertinentes appropriées, telles que mesurées par des essais mic de microdilution de bouillon. Dans la plupart des cas, les sondes ont perdu une certaine activité par rapport au médicament parent, mais ont conservé une certaine puissance antibiotique mesurable (suffisante pour être utile dans d’autres études).
Discussion
La création d’une sonde antibiotique fluorescente réussie doit commencer par une planification et un examen minutieux de la R-S du médicament parent. Si le R Sa n’est pas connu ou complètement exploré, plusieurs options pourraient devoir être testées pour trouver un site qui peut être modifié sélectivement sans abolir l’activité biologique. Une fois qu’un site/s a été identifié, l’installation d’un moiety de lien est souvent essentielle afin de fournir l’espacement stéril issu entre le site biologique d’action et le fluorophore inactif. Il faut prendre soin que la réaction utilisée pour attacher le lien à l’antibiotique laisse un groupe fonctionnel bio-stable, en évitant, par exemple, les esters qui sont sensibles au clivage par les esterases in vivo. Selon le profil pharmacodynamique et pharmacocinétique de l’antibiotique, un simple lien alkyl peut être utilisé, ou bien une option moins lipophile comme un lien de polyéthylène glycol (PEG) devrait être considéré. Avec le lien attaché, l’activité antibactérienne devrait être évaluée pour s’assurer que les MIC contre les bactéries pertinentes sont semblables au composé parent.
Dans ce travail, nous recommandons l’utilisation de Huigsen azide-alkyne [3-2] cycloaddition dipolar (cliquez sur la chimie, voir Figure 1) pour liguer le fluorophore à l’antibiotique, pour un certain nombre de raisons. Les réactions de clic sont très sélectives, ce qui signifie que la protection des groupes réactifs sur l’antibiotique n’est pas nécessaire, et en outre, la réaction laisse une téazole stable et biocompatible moiety. Le composant d’azide est introduit à la partie antibiotique dans nos procédures, car ceci est généralement plus facilement accompli avec une série de types structurels que l’introduction d’un alkyne. Les synthèses de deux fluorophores dérivés de l’alkyne sont décrites ici, bien que d’autres pourraient être explorées si désiré. NBD et DMACA ont été choisis en raison de leur petite taille, minimisant la possibilité d’interférer avec la pénétration cellulaire et l’interaction cible. La réaction de clic elle-même est effectuée à l’aide d’une catalyse en cuivre, où soit Cu2 (CuSO 4, avec un agent de réduction de l’acide ascorbique) ou Cu(CuI) peut être utilisé comme réactif de départ. Après la purification (Figure 2), les MIC doivent ensuite être testés comme avec l’azide. Même avec un examen attentif du choix du fluorophore et du site d’attachement, il est possible que l’activité antibiotique pauvre sera observée. Cela ne signifie toutefois pas qu’une sonde inactive est sans utilisation. Comme le montrent les sondes TMP, les composés ayant une faible activité antibactérienne peuvent encore se lier à la même cible que le médicament parent. Cela peut permettre des études sur le mode d’action et l’examen de phénomènes conduisant à la résistance, tels que l’efflux.
Comme indiqué dans la section des protocoles, il est possible d’analyser l’étiquetage bactérien par les antibiotiques fluorescents à l’aide d’un simple essai de spectrophotométrie (figure 3) ou de cytométrie du débit (figure 4). Les deux méthodes sont capables de quantifier l’accumulation cellulaire, et en lysant les cellules et en examinant la localisation de fluorescence dans le lysate, il est possible d’évaluer l’accumulation intracellulaire. Dans ce protocole, l’utilisation du lysozyme pour la lyse cellulaire est décrite, car il s’agit d’une technique rapide et universelle. D’autres conditions de lyse, telles que le traitement de nuit avec la glycine-HCl7,ont également été utilisées avec succès. En utilisant cette technique, il est possible d’étudier l’impact de l’efflux sur l’accumulation cellulaire d’antibiotiques, qui est un mécanisme majeur de résistance. Si l’efflux est effectivement présent dans les bactéries, un manque d’accumulation intracellulaire sera observé, bien que cela puisse être sauvé à l’aide d’un inhibiteur de l’efflux comme CCCP.
La microscopie peut également être effectuée pour inspecter visuellement la localisation des sondes dans différentes bactéries, recueillir des informations sur le mode d’action, et potentiellement aussi la résistance (voir la figure 5 pour des exemples représentatifs). Afin de voir la localisation dans les bactéries, un microscope confocal à haute résolution est nécessaire, équipé de capacités telles que SIM (microscopie d’éclairage structurée), SR-SIM (superrésolution-SIM), Airyscan, ou STED (épuisement des émissions stimulées). En outre, des bordereaux de couverture haute performance devraient être utilisés et des analyses post-imagerie effectuées sur un logiciel approprié (p. ex. FIJI, Zen ou Imaris). La localisation des sondes est comparée aux colorants qui tachent des architectures spécifiques, telles que Hoechst-33342 (bleu, acide nucléique), Syto-9 (vert, acide nucléique), et FM4-64FX (rouge, membrane). Le choix des colorants doit être fait pour correspondre à l’antibiotique fluorescent, de sorte que chaque couleur utilisée a un chevauchement spectral minimal. Afin d’obtenir les meilleures images possibles, une optimisation peut être nécessaire. Par exemple, si les bactéries sont trop encombrées sur la glissière, ne prenez qu’une partie de la pastille en suspension, puis diluez-vous avec un milieu de montage plus important. En revanche, si les bactéries sont trop clairsemées sur la diapositive, il suffit de commencer avec plus de bactéries. Dans ce protocole, l’utilisation d’un gel thermoréversible compatible avec les cellules vivantes (p. ex. Cygel) est recommandée pour l’imagerie cellulaire vivante, car elle immobilise les bactéries (y compris les bactéries motiles), mais d’autres supports de montage ou agarose ont également été utilisés avec succès.
Dans l’ensemble, malgré les défis qui peuvent être rencontrés dans la préparation d’un dérivé bioactif antibiotique fluorescent, la simplicité de leur utilisation et leur polyvalence font de ces sondes des outils attrayants pour la recherche en RMA. Les travaux futurs utilisant des antibiotiques fluorescents ont le potentiel de fournir un aperçu des mécanismes de résistance aux antibiotiques, d’améliorer notre compréhension du fonctionnement actuel des antibiotiques et d’aider au développement de meilleurs médicaments.
Déclarations de divulgation
Les auteurs n’ont rien à déclarer.
Remerciements
MRLS est soutenu par un Australian Postgraduate Award (APA) et un Institute for Molecular Biosciences Research Advancement Award. Wanida Phetsang a reçu l’appui de la Bourse internationale de l’UQI et du Prix d’études supérieures de l’IMB (IMBPA). MAC est un chercheur de principe NHMRC (APP1059354) et détient également une nomination de chercheur scientifique fractionnelle à l’Université du Queensland, avec son temps restant en tant que PDG d’Inflazome Ltd, une société développant des médicaments pour répondre aux besoins cliniques non satisfaits dans les maladies inflammatoires. MATB est soutenu en partie par Wellcome Trust Strategic Grant WT1104797/Z/14/Z et NHMRC Development grant APP1113719. La microscopie a été réalisée à l’Australian Cancer Research Foundation (ACRF)/Institute for Molecular Bioscience Cancer Biology Imaging Facility, qui a été créé avec le soutien de l’ACRF.
matériels
| Name | Company | Catalog Number | Comments |
| 3-(dimethylamino)phenol | Alfa-Aesar | B23067 | |
| 4-chloro-7-nitro-benzofuran | Sigma-Aldrich | 163260-5G | |
| Amicon Ultra-0.5 centrifugal filter unit with Ultracel- 10 membrane | Merck | UFC501096 | |
| Atlantis Prep T3 OBD (100 A, 5 uM, 10x250 mm) | Waters | 186008205 | |
| Atlantis T3 column (100 A, 5 uM, 2.1 × 50 mm) | Waters | 186003734 | |
| Bruker Avance 600 MHz spectrometer | Bruker | ||
| Buchi Reveleris C18 12g Cartridge | Buchi | BUC145152103 | |
| CCCP | Sigma-Aldrich | C2759 | |
| Celite 545 | Sigma-Aldrich | 22140-5KG-F | |
| Cygel | ABCAM | Ab109204 | |
| Elyra PS,1 SIM/STORM confocal microscope | Zeiss | ||
| FM4-64FX, fixable analog of FM™ 4-64 membrane stain | Life Technologies Australia Pt | F34653 | |
| Gallios flow cytometer | Beckman Coulter | ||
| Gamma 2-16 LSCplus lyophilise | CHRIST | ||
| Gilson HPLC 2020 | Gilson | ||
| Hanks' Balanced Salt solution, Modified, with sodium bicarbonate, without phenol red, calcium chloride and magnesium sulfate, liquid, sterile-filtered, suitable for cell culture | Sigma-Aldrich | H6648-500ML | |
| Hettich Zentrifugen Rotofix 32 | Hettich | ||
| High performance #1.5 cover slips (18 x 18 mm) | Schott/Zeiss | 474030-9000-000 | |
| Hoechst 33342, Trihydrochloride, Trihydrate - Fluo | Life Technologies Australia Pt | H21492 | |
| LB | AMRESCO | J106 | |
| Leica STED 3X Super Resolution Microscope with White Light Laser excitation | Leica | ||
| Lysozyme from chicken egg white lyophilized powder | Sigma-Aldrich | L6876 | |
| Mueller Hinton II Broth Cation adjusted | Becton Dickinson | 212322 | |
| Propargylamine | Sigma-Aldrich | P50900-5G | |
| Reveleris GRACE MPLC | Buchi | ||
| Shimadzu LCMS-2020 | Shimadzu | ||
| Sigma 1-15 Microcentrifuge | Sigma-Aldrich | ||
| Silica gel 60 (0.040-0.063 mm) for column chromatography (230-400 mesh ASTM) | Merck | 1093859025 | |
| SYTO 9 Green Fluorescent Nucleic Acid Stain | Life Technologies Australia Pt | S34854 | |
| TECAN Infinite M1000 PRO | TECAN |
Références
- Cai, H., Rose, K., Liang, L. H., Dunham, S., Stover, C. Development of a liquid chromatography/mass spectrometry-based drug accumulation assay in Pseudomonas aeruginosa. Analytical Biochemistry. 385 (2), 321-325 (2009).
- Bhat, J., Narayan, A., Venkatraman, J., Chatterji, M. LC-MS based assay to measure intracellular compound levels in Mycobacterium smegmatis: Linking compound levels to cellular potency. Journal of Microbiological Methods. 94 (2), 152-158 (2013).
- Davis, T. D., Gerry, C. J., Tan, D. S. General Platform for Systematic Quantitative Evaluation of Small-Molecule Permeability in Bacteria. ACS Chemical Biology. 9 (11), 2535-2544 (2014).
- Richter, M. F., et al. Predictive compound accumulation rules yield a broad-spectrum antibiotic. Nature. 545, 299(2017).
- Iyer, R., et al. Evaluating LC-MS/MS To Measure Accumulation of Compounds within Bacteria. ACS Infectious Diseases. 4 (9), 1336-1345 (2018).
- Prochnow, H., et al. Subcellular Quantification of Uptake in Gram-Negative Bacteria. Analytical Chemistry. 91 (3), 1863-1872 (2019).
- Dumont, E., et al. Antibiotics and efflux: combined spectrofluorimetry and mass spectrometry to evaluate the involvement of concentration and efflux activity in antibiotic intracellular accumulation. Journal of Antimicrobial Chemotherapy. 74 (1), 58-65 (2019).
- Stone, M. R. L., Butler, M. S., Phetsang, W., Cooper, M. A., Blaskovich, M. A. T. Fluorescent Antibiotics: New Research Tools to Fight Antibiotic Resistance. Trends in Biotechnology. 36 (5), 523-536 (2018).
- Piddock, L. J. V., Johnson, M. M. Accumulation of 10 fluoroquinolones by wild-type or efflux mutant Streptococcus pneumoniae. Antimicrobial Agents and Chemotherapy. 46 (3), 813-820 (2002).
- Mortimer, P. G. S., Piddock, L. J. V. A comparison of methods used for measuring the accumulation of quinolones by enterobacteriaceae, pseudomonas aeruginosa and staphylococcus aureus. Journal of Antimicrobial Chemotherapy. 28 (5), 639-653 (1991).
- Li, X. Z., Nikaido, H., Poole, K. Role of MexA-MexB-OprM in antibiotic efflux in Pseudomonas aeruginosa. Antimicrobial Agents and Chemotherapy. 39 (9), 1948-1953 (1995).
- Vince, R., Weiss, D., Pestka, S. Binding of N-substituted erythromycylamines to ribosomes. Antimicrobial Agents and Chemotherapy. 9 (1), 131-136 (1976).
- Vazquez, D. Antibiotics affecting chloramphenicol uptake by bacteria Their effect on amino acid incorporation in a cell-free system. Biochimica et Biophysica Acta (BBA) - Nucleic Acids and Protein Synthesis. 114 (2), 289-295 (1966).
- Phetsang, W., et al. An azido-oxazolidinone antibiotic for live bacterial cell imaging and generation of antibiotic variants. Bioorganic and Medicinal Chemistry. 22 (16), 4490-4498 (2014).
- Phetsang, W., et al. Fluorescent trimethoprim conjugate probes to assess drug accumulation in wild type and mutant Escherichia coli. ACS Infectious Diseases. 2 (10), 688-701 (2016).
- Stone, M. R. L., et al. Fluoroquinolone-derived fluorescent probes for studies of bacterial penetration and efflux. MedChemComm. 10 (6), 901-906 (2019).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon