Method Article
Untersuchung der Tensideffekte auf die Hydratkristallisation an Öl-Wasser-Schnittstellen mit einem kostengünstigen integrierten modularen Peltier-Gerät
In diesem Artikel
Zusammenfassung
Wir präsentieren ein Protokoll, um die Bildung von Hydraten in Gegenwart von nichtionischen Tensiden auf der Schnittstelle eines Wassertropfens in Cyclopentan untergetaucht zu studieren. Das Protokoll besteht aus dem Aufbau eines kostengünstigen, programmierbaren Temperaturreglers. Die Temperaturregelung wird mit Visualisierungstechniken und internen Druckmessungen kombiniert.
Zusammenfassung
Wir führen einen Ansatz ein, um die Bildung und das Wachstum von Hydraten unter dem Einfluss nichtionischer Tenside zu untersuchen. Das experimentelle System umfasst einen Temperaturregler, Visualisierungstechniken und Innendruckmessungen. Das Temperaturregelungssystem enthält einen kostengünstigen, programmierbaren Temperaturregler aus Festkörper-Peltier-Komponenten. Zusammen mit dem Temperaturregelungssystem haben wir Visualisierungstechniken und interne Druckmessungen integriert, um die Hydratbildung und -hemmung in Gegenwart nichtionischer Tenside zu untersuchen. Wir untersuchten die hydrathemmende Fähigkeit von nichtionischen Tensiden (Sorbitanmonolaurat, Sorbitanmonooleat, PEG-PPG-PEG und Polyoxyethylenesorbitan-Tristearat) bei niedrigen (d. h. 0,1 CMC), mittleren (d. h. CMC) und hohen (d. h. 10 CMC) Konzentrationen. Es entstanden zwei Arten von Kristallen: planar und konisch. Planare Kristalle wurden in klarem Wasser und niedrigen Tensidkonzentrationen gebildet. Konische Kristalle wurden in hohen Tensidkonzentrationen gebildet. Die Ergebnisse der Studie zeigen, dass konische Kristalle am effektivsten in Bezug auf die Hydrathemmung sind. Da konische Kristalle nicht über eine bestimmte Größe hinaus wachsen können, ist die Feuchtigkeitswachstumsrate als konischer Kristall langsamer als die Feuchtigkeitswachstumsrate als planarer Kristall. Daher sind Tenside, die Hydrate zwingen, konische Kristalle zu bilden, die effizientesten. Das Ziel des Protokolls ist es, eine detaillierte Beschreibung eines experimentellen Systems zu liefern, das in der Lage ist, den Cyclopentan-Hydratkristallisationsprozess auf der Oberfläche eines Wassertröpfchens in Gegenwart von Tensidmolekülen zu untersuchen.
Einleitung
Der Anreiz, den Mechanismus der Hydratkristallisation und -hemmung zu verstehen, ergibt sich aus der Tatsache, dass Hydrate natürlicherweise in Ölpipelines vorkommen und zu Schwierigkeiten bei der Durchflusssicherung führen können. So war beispielsweise die Ölpest1 im Golf von Mexiko im Jahr 2010 das Ergebnis einer Ansammlung von Hydraten in einem Unterwasser-Ölrohrsystem, die eine Kontamination der Umwelt verursachte. Daher ist das Verständnis der Hydratbildung und -hemmung von entscheidender Bedeutung, um zukünftige Umweltkatastrophen zu verhindern. Ein großer Teil der treibenden Kraft für die Untersuchung der Hydratkristallisation in den letzten Jahren ist die Bemühungen der Ölindustrie, die Agglomeration von Hydratstopfen und die anschließende Verstopfung des Flusses zu verhindern. Die erste Studie, die bestellte, dass Hydrate für verstopfte Strömungslinien verantwortlich waren, wurde von Hammerschmidt 19342durchgeführt. Bis heute ist es den Ölproduzenten sehr wichtig, die Hydratbildung für die Durchflusssicherung zu verstehen und zu hemmen3.
Eine Möglichkeit, die Hydratbildung zu verhindern, besteht darin, Tiefe Wasserleitungen zu isolieren, damit sich kein Eis bildet. Allerdings ist es teuer, die Pipelines angemessen zu isolieren, und die zusätzlichen Kosten können in der Größenordnung von 1 Million USD/km3liegen. Thermodynamische Inhibitoren, wie Methanol, können in Wellheads injiziert werden, um die Bildung von Hydraten zu verhindern. Allerdings sind große volumetrische Verhältnisse von Wasser zu Alkohol, so groß wie 1:1, erforderlich, um die Bildung von Hydraten angemessen zu verhindern4. Kürzlich wurden die weltweiten Kosten für die Verwendung von Methanol zur Hydratprävention mit 220 Millionen US-Dollar pro Jahr ausgewiesen. Dies ist keine nachhaltige Menge an Alkoholkonsum5. Darüber hinaus ist die Verwendung von Methanol problematisch, weil es umweltgefährdend ist und nicht für den Großtransport verwendet werden kann5. Alternativ können kinetische Inhibitoren, wie Tenside, das Hydratwachstum bei kleinen Mengen und Temperaturen von bis zu 20 °C6unterdrücken. Daher kann die Anwesenheit von Tensid die große Menge an Alkohol reduzieren, die für die Hydratprävention benötigt wird.
Tenside gelten als gute Inhibitoren für die Hydratkristallisation aus zwei Hauptgründen:
1) Sie können die Hydratbildung durch Veränderungen der Oberflächeneigenschaften hemmen; und 2) Sie helfen zunächst bei der Bildung von Hydratzellen, verhindern aber weiteres Wachstum und Agglomeration des Kristalls in der Pipeline7. Obwohl tenfactants sich als effiziente Inhibitoren erwiesen haben, fehlen noch immer viele Informationen über den Kristallisationsprozess in Gegenwart von Tensiden. Während einige Studien gezeigt haben, dass die Verwendung von Tensiden die anfängliche Hydratkristallisationszeit bei bestimmten Unterkühlungen verlängern kann, haben andere Studien Ausnahmen bei niedrigen Tensidkonzentrationen gefunden. Bei niedrigen Tensidkonzentrationen neigen die Wassertröpfchen dazu, sich zusammenzuschließen und den Prozess der Hydratbildung zu beschleunigen8. Der Hemmungsprozess wurde durch Tensidmoleküle erklärt, die das planare Hydratwachstum unterbrechen und das Hydrat zur hohlkonischen Kristallbildung zwingen. Die konischen Kristalle bilden eine mechanische Barriere für Kristallwachstum9und hemmen so das Wachstum.
In dieser Studie haben wir ein kostengünstiges, integriertes modulares Peltier-Gerät (IMPd) zusammen mit einer Hydrat-Visualisierungszelle entwickelt und implementiert und diese verwendet, um die Bildung von Cyclopentanhydrat in Gegenwart von nichtionischen Tensiden zu untersuchen. Der Grund für die Verwendung von Cyclopentan anstelle von gasarmen Gasen (z. B. CH4 und CO2), die normalerweise Hydrate in Tiefseespeichern bilden, ist, dass diese Gase höhere Drücke und niedrigere Temperaturen benötigen, um stabile Hydrate zu bilden. Da Cyclopentan Hydrate bei Umgebungsdruck und Temperaturen bis zu 7,5 °C bildet, wird es häufig als Modellmaterial für die Hydratbildung10verwendet.
Das integrierte modulare Peltier-Gerät (IMPd) besteht aus einem Open-Source-Mikrocontroller, Peltier-Platte, CPU-Kühler (Kühlkörper) und wasserdichtem digitalen Temperatursensor. Das Gerät kann eine maximale Temperaturdifferenz von 68 °C liefern. Die minimale Temperaturauflösung beträgt 1/16 °C. Das gesamte System, einschließlich der elektrischen Schaltung und Hardware, kann für weniger als 200 US-Dollar gebaut werden. Der Temperatursensor meldet sich an den Mikrocontroller, der Ausgangssignale an den Transistor sendet. Der Transistor leitet dann Strom von der Gleichstromquelle durch das Peltier-Element. Der Kühlkörper hilft, das Peltier-Element zu kühlen, indem er die Wärme, die von der heißen Seite des Peltiers kommt, in die Umgebungsluft konvektiert. Die montierten Hardwarekomponenten des IMPd-Systems sind in Abbildung 1a,bdargestellt. Abbildung 1c zeigt den Schaltplan mit allen Komponenten der Regelschleife (proportional-integral-derivative [PID]-Controller) und den Pin-Outs. Der Ausgangsstrom des Mikrocontrollers war mit dem Gate-Widerstand R1 auf einen maximalen Strom von 23 mA (I = 5 V/220 W) begrenzt. Der Pull-Down-Widerstand R2 in Abbildung 1c ermöglicht die Ableitung und das Ausschalten des Systems. Zur Optimierung des PID-Controllers werden Ziegler-Nichols-basierte Methoden in Kombination mit einem iterativen Verfahren verwendet11. Die Software für die integrierte Entwicklungsumgebung (IDE) des Mikrocontrollers wird verwendet, um Befehle zur Temperaturregulierung zu überwachen und an den Mikrocontroller zu senden.
Zusammen mit dem IMPd haben wir einen neuartigen Ansatz mit Visualisierungstechniken und internen Druckmessungen angewendet. Die Hydrat-Visualisierungszelle, die auf der OBERSEITE des IMPd platziert ist, besteht aus einer Messingzelle, die mit zwei doppelt schwenkten Beobachtungsfenstern ausgestattet ist. Die Fenster ermöglichen eine Videoaufzeichnung des Hydratbildungsprozesses auf dem Wassertröpfchen in Cyclopentan. Die komplementäre Metalloxid-Halbleiterkamera (CMOS) wird außerhalb des Fensters platziert und der Druckwandler wird an die Wassereinspritzleitung angeschlossen, um die internen Druckmessungen des Tropfens zu erhalten. Eine digitale Messumformer-Anwendung wird verwendet, um die Messwerte aus dem Druckaufnehmer zu erhalten. Ein Kamerabetrachter wird verwendet, um die Videos und Bilder von der CMOS-Kamera zu erfassen. Die Software steuert die Belichtungs- und Snapshot-Frequenz. Bildverarbeitungssoftwareprogramme werden verwendet, um das Wachstum des Hydrats zu verfolgen. Abbildung 2a zeigt eine schematische Beschreibung der Hydrat-Visualisierungszelle und Abbildung 2b zeigt eine Übersicht über das gesamte experimentelle System. Das Samenhydrat (Abbildung 2a) ist für eine konsistente Keimbildung und Verfolgung der Hydratwachstumsrate erforderlich. Das Samenhydrat ist ein kleines Volumen (z. B. 50–100 l) reines Wasser, das sich auf dem Boden der Hydratzelle ablagert. Wenn die Temperatur abnimmt, bildet der Tropfen Eis, das sich dann mit steigender Temperatur in Hydrat umdreht. Das kleine Stück des Samenhydrats kontaktiert dann das Wassertröpfchen. Dieser Prozess steuert die Initiierung des Hydrats im untergetauchten Wassertropfen. Kieselsäure-Desiccant wird in den Spalt zwischen den beiden Glasggeraden(Abbildung 2c) eingefügt, die als Sichtfenster dienen. Die Kieselsäure-Enttrocknung hilft, die Menge an Frost und Beschlagen auf den Fenstern zu reduzieren. Anti-Nebel wird auch auf das äußere Fenster angewendet, um Beschlagen zu reduzieren. Die Aufnahmen werden mit einer CMOS-Kamera und einem 28-90-mm-Objektiv aufgenommen. Zur Beleuchtung wird eine 150 W Glasfaser-Gänsehalslampe verwendet. Eine Acrylabdeckung wird auf die Messingzelle gelegt, um die Verdunstung von Cyclopentan zu begrenzen. Die Sanitärinstallation besteht aus einer Kombination aus flexiblen Polytetrafluorethylen-Schläuchen (PTFE) und starren Messingschläuchen. Eine Spritzenpumpe mit einer 1 ml Glasspritze und einer 19 G Nadel steuern den Wasserfluss und die Tensidlösung. Ein Druckwandler überwacht die Druckänderungen im Inneren des Wassertensidlösungströpfchens. 19 G PTFE-Schläuche verbinden die Spritze mit dem T-Fitting und 1/16 in.(1.588 mm) Messingschlauch verbindet den Messumformer und Messinghaken mit dem T-Fitting(Abbildung 2d). Ein etwa 5 cm langer Messinghaken mit einer 180°-Biegung erzeugt das Wasser-/Tensidlösungströpf. Die Biegung stellt sicher, dass das von der Spritze erzeugte Tröpfchen während des gesamten Experiments auf dem Rohr sitzt. Eine 1/16-in.-Edelstahl-T-Fitting in Verbindung mit PTFE-Zerkleinerungs-Ferrules und PTFE-Gewindeband versiegeln die Armaturen.
Mit diesem Gerät untersuchten wir vier verschiedene nichtionische Tenside mit verschiedenen hydrophil-lipophilen Gleichgewichten (HLB), die in der Ölindustrie häufig verwendet werden: Sorbitanmonolaurat, Sorbitanmonooleat, PEG-PPG-PEG und Polyoxyethylenesorbitan Tristearat.
Protokoll
1. Hydratbildung auf Wassertröpfchen in Cyclopentan
HINWEIS: Das unten beschriebene experimentelle Verfahren dient der Untersuchung der Hydratbildung an einem Wassertröpfchen in Cyclopentan unter Verwendung der in der Einleitung beschriebenen IMPd- und Hydrat-Visualisierungszelle.
- Befestigen Sie eine 19 G Nadel an der 1 ml Glasspritze (Abbildung 2b, C).
- Spülen Sie die 1 ml Glasspritze und 19 G Nadel 3x mit DI-Wasser.
- Füllen Sie die Spritze mit DI-Wasser.
- Füllen Sie die Hydrat-Visualisierungszelle (Abbildung 2b, E) mit 25 ml Cyclopentan.
- Legen Sie mit der Spritze ein Tröpfchen DI-Wasser (d. h. 50 x 100 L) an der Unterseite der Hydrat-Visualisierungszelle ein. Dieses Wassertröpfchen ist das Samenhydrat.
HINWEIS: Der Tropfen sollte am unteren Rand der Hydrat-Visualisierungszelle platziert werden. Der Zweck des Samenhydrats ist es, die Bildung des Hydrats zu initiieren und eine konsistente Keimbildung und Verfolgung der Wachstumsrate zu bilden. - Platzieren Sie den Temperatursensor in der Visualisierungszelle des Hydrats in der Nähe des unteren Bodens der Zelle.
- Setzen Sie die Acrylabdeckung auf die Hydrat-Visualisierungszelle, um eine Verdunstung des Cyclopentans zu verhindern. Verwenden Sie Schrauben, um die Abdeckung an Ort und Stelle zu halten.
- Passen Sie die Lichter und die Kamera so an, dass sie sich fokussieren. Passen Sie den Fokus auf das Samenhydrat an.
- Stellen Sie die Temperatur der Peltierplatte in der Temperaturregelung auf -5 °C ein.
- Überprüfen Sie die vom Temperatursensor abgelesenen Temperaturwerte.
- Sobald die Temperatur -5 °C erreicht ist, stellen Sie sicher, dass sich das Tröpfchen am Boden (Samenhydrat) in Eis verwandelt.
- Stellen Sie die Temperatur der Peltierplatte in 0,5 °C-Schritten auf 2 °C ein.
- Wenn die Temperatur 2 °C erreicht, füllen Sie die Sanitärinstallation mit Wasser mit der Spritze, und senken Sie den Messinghaken in das Cyclopentan, um 5 min auszuhalten.
HINWEIS: Diese Temperatur stellt sicher, dass das feste Eis in Hydrat umgewandelt wird, da das System über dem Schmelzpunkt des Eises liegt, aber unter dem von Cyclopentanhydraten11. - Starten Sie die Aufnahme mit der Kamera.
- Drücken Sie die Startmessung auf der Druckwandlersoftware, um die digitalen Messumformeraufzeichnungen zu starten.
- Schließen Sie die Spritze an die Spritzenpumpe an.
- Stellen Sie die Spritzenpumpe so ein, dass sie ein Volumen von 2 l einspritzt und aktiviert. Die Spritze wird das Wasser in das Cyclopentanbad tauchen, um das untergetauchte Tröpfchen zu bilden.
- Verwenden Sie eine Nadelspitze, um ein kleines Stück des Samenhydrats zu entfernen.
- Bringen Sie die Nadelspitze mit dem Stück Samenhydrat (Abbildung 3a) in kurzen Kontakt mit dem Wassertröpfchen (Abbildung 3b), um die Bildung des Hydrats auf dem Wassertröpfchen zu initiieren.
- Drücken Sie Aufzeichnung auf der Kameraaufnahmesoftware. Zeichnen Sie Bilder des Kristallisationsprozesses der Tröpfchenhälfte von der Kamera bei 1 Hz auf.
2. Hydratbildung auf Wassertensidtröpfchen in Cyclopentan
HINWEIS: Hydratkristallisationsexperimente mit Tensidlösungen werden auf die gleiche Weise wie reines Wasser durchgeführt. Bei der Verwendung einer Tensidlösung zur Untersuchung der Tensidwirkung auf die Hydratkristallisation ist es jedoch notwendig, die kritische Micelle-Konzentration (CMC) jedes Tensids zu finden. Die CMC kann entweder in der Literatur9 oder mit der unten beschriebenen Methode gefunden werden.
- Bereiten Sie 50 ml Standardlösungen aus Sorbitanmonolaurat, PEG-PPG-PEG und Polyoxyethylenesorbitan-Tristearat vor, indem Sie eine gemessene Masse jedes Tensids in entionisiertes Wasser auflösen, um eine Reihe von 12 Lösungen jedes Tensids vorzubereiten, die jeweils eine unterschiedliche Konzentration von 10-4 g/100 ml –1 g/100 ml darstellen.
- Bereiten Sie Lösungen von Sorbitanmonooleat in Cyclopentan in verschiedenen Konzentrationen vor.
HINWEIS: Cyclopentan wird aufgrund der hohen Hydrophobizität und geringen Löslichkeit von Sorbitanmonooleat in Wasser verwendet. Die gleichen Konzentrationen werden auch für Sorbitanmonooleat verwendet. - Messen Sie die Oberflächenspannung jeder Tensidlösung mit der Stalagmommetrie-Methode.
- Platzieren Sie die Spritzenpumpe und die Spritze vertikal, wie in Abbildung 4 dargestellt, um fallende Tropfen zu zählen.
- Programmieren Sie die Pumpe, um 1 ml Lösung mit einer Rate von 0,5 ml/min zu vertreiben und die Tropfen in die Luft freizusetzen.
- Erhalten Sie das Abwurfvolumen (V) als Durchschnitt, indem Sie 1 ml durch die Anzahl der beobachteten Tropfen dividiert.
- Testen Sie jede Lösung mindestens 3x.
- Berechnen Sie die Grenzflächenspannung mit
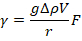
wobei g die Beschleunigung aufgrund der Schwerkraft ist,ist p die Dichteänderung an der Schnittstelle (d.h. die Dichtedifferenz zwischen Tensidlösung und Luft), V ist das Tröpfchenvolumen, F ist eine empirische Korrektur, die durch12
HINWEIS: Alternativ finden sich Oberflächenspannungen einiger Tensidlösungen in der Literatur9. - Zeichnen Sie die Oberflächenspannung als Funktion der Konzentration. Die Oberflächenspannung nimmt mit zunehmender Tensidkonzentration ab, bis sie abflacht und konstant wird.
- Finden Sie den CMC für jedes Tensid (d. h. die Konzentration, bei der die Oberflächenspannung abflacht) und verwenden Sie es in den Experimenten.
HINWEIS: Eine Erhöhung der Tensidkonzentration ändert die Oberflächenspannung nicht.
- Wiederholen Sie das experimentelle Verfahren in Abschnitt 1, aber anstelle von Wasser verwenden Tensidlösung in verschiedenen Konzentrationen im Vergleich zum CMC (d. h. 0,1x CMC, 1x CMC und 10x CMC).
3. Bildverarbeitung und Grenzflächenspannungsmessungen
HINWEIS: Die Verfolgung des konischen und planaren Hydratwachstums wird mit visuellen Analysemethoden durchgeführt. Die verwendeten Softwareprogramme sind in der Tabelle der Materialienbeschrieben. Ein Beispiel für die Konturerkennung und Färbung finden Sie in Abbildung 5. Da die Kamera nur die 2D-Projektion des kugelförmigen Tröpfchens erfasst, muss eine 3D-Rekonstruktion erstellt werden.
- Verfolgung des Hydratwachstums
- Öffnen Sie das erste Bild der Bildsequenz mit Bildverarbeitungssoftware.
- Verwenden Sie das Längenwerkzeug in der Software, um die Länge des Messingrohrs im Bild zu messen.
- Stellen Sie die Skala des Messingrohres im Bild basierend auf dem bekannten Durchmesser von 1/16 zoll (1.588 mm) ein.
- Wählen Sie aus jeder Sequenz 10 Gleichzugewiesene aus. Die Snapshots sollten den gesamten Prozess erfassen, vom Punkt der Keimbildung bis zur vollständigen Tröpfchenkonvertierung.
- Wiederholen Sie die Skalierungseinstellung (Schritte 3.1.1-3.1.3) für die 10 ausgewählten Snapshots.
- Verwenden Sie die Software, um die Kontur des Tropfens in jedem Frame manuell zu erkennen. Markieren Sie die Kontur rot(Abbildung 5b).
- Verwenden Sie die Software, um die Kontur des Hydrats in jedem Rahmen manuell zu erkennen. Färben Sie den gesamten Bereich des gesamten Bereichs des Hydrats in Schwarz(Abbildung 5b).
- Verwenden Sie mathematische Modellierungssoftware, um eine 3D-Rekonstruktion des Tropfens als Korrektur der Oberfläche zu bilden.
HINWEIS: Alle Einzelheiten über die Konstruktion der 3D-Oberfläche sind in Dann et al.13beschrieben.
- Scheinbare durchschnittliche Grenzflächenspannungsmessungen
HINWEIS: Die scheinbare durchschnittliche Grenzflächenspannung wird anhand der internen Druckdaten berechnet, die vom Druckaufnehmer erfasst werden.- Verwenden Sie die aufgezeichneten Daten desPDruckwandlers .
- Verwenden Sie für jeden Datenpunkt die Young-Laplace-Beziehung14, um die scheinbare durchschnittliche Grenzflächenspannung zu bestimmen (y),

wobei R11 und R22 die Tröpfchenradien der Krümmung sind undP die Druckänderung innerhalb des Tröpfchens relativ zu t = 0 ist.
ANMERKUNG: In der Anfangsphase nach der Tröpfchenbildung sind die beiden Radien ungefähr gleich, daher können R11 und R22 in der Young-Laplace-Gleichung durch den Radius des vorgegebenen 2-L-Tropfens von R = 782 mersetzt werden.
Ergebnisse
Mit diesem experimentellen System kann man die Hydratbildung an der Öl-Wasser-Schnittstelle untersuchen und die mit dem Kristallisationsprozess verbundene Grenzflächenspannung messen. Abbildung 6 zeigt eine repräsentative Reihe von Ergebnissen, die sowohl die Kristallbildung als auch die Grenzflächenspannung umfassen. Im planaren Schalenwachstum (Abbildung 6a) wuchs der Kristall von den beiden Polen in Richtung Äquator. Aus diesem Grund wuchs im planaren Kristall die Hydratschale ständig. In reinem Wasser und niedrigen Tensidkonzentrationen bildete das Hydrat eine planare Muschelmorphologie, wie in Abbildung 6azu sehen ist. Die in Abbildung 6b dargestellte Veränderung des Drucks und der scheinbare durchschnittliche Grenzflächenstress im Laufe der Zeit zeigten eine allmähliche Abnahme des scheinbaren durchschnittlichen Grenzflächenstresses, während das Hydratwachstum für die planare Muschelmorphologie fortschritt. Da das Hydrat wuchs und die Oberfläche bedeckte, gab es weniger verfügbare Fläche für die Tensidmoleküle, daher nahm die gleiche Anzahl von Tensidmolekülen eine kleinere Oberfläche ein, was zu einer verringerten scheinbaren durchschnittlichen Grenzflächenspannung führte. Die konische Morphologie (Abbildung 6c) wurde in hohen Tensidkonzentrationen beobachtet. Hier wuchs das Hydrat als konischer Kristall. Als der konische Kristall groß genug wurde, löste sich ein Teil des Kegels von der Tröpfchenoberfläche. Dieses Wachstumsmuster geschah immer wieder oszillativ. Der Kristall begann zu wachsen, bis er eine kritische Größe erreichte, dann brach er und der Prozess begann von neuem. Offensichtliche durchschnittliche Grenzflächenspannungsmessungen (Abbildung 6d) zeigten eine anfängliche Abnahme der Grenzflächenspannung, als der konische Kristall zu wachsen begann. In den Anfangsstadien des Wachstumsprozesses gab es eine Verringerung der verfügbaren Oberfläche für die Tensidmoleküle. Der konische Kristall wuchs und erreichte irgendwann seine kritische Größe. Weiteres Wachstum des Kristalls führte zu einer Ablösung von der Tropfenoberfläche. Der Kegelbruch von der Oberfläche führte zu einem plötzlichen Anstieg der verfügbaren Oberfläche für Tensidmoleküle und zu einer Zunahme der Grenzflächenspannung. Ein Kristall begann dann wieder zu wachsen, was zu einem oszillierenden Verhalten der scheinbaren durchschnittlichen Grenzflächenspannung führte. Dieses Oszillationsverhalten ist in Abbildung 6d zusehen.
Durch die Verfolgung des Hydratwachstums können wir Informationen über die Fähigkeit des Tensids erhalten, die Hydratbildung zu hemmen. Die kollektiven Wachstumsraten aller Tensidlösungen bei niedrigen (d. h. 0,1 CMC), mittleren (d. h. CMC) und hohen (d. h. 10 CMC) Konzentrationen sind in Abbildung 7dargestellt. Da die Standardabweichung zwischen den drei unabhängigen Messungen jeder Tensidkonzentration <5% betrug, werden keine Fehlerbalken dargestellt. Im Allgemeinen hemmte Tensidlösung das Hydratwachstum im Vergleich zu reinem Wasser. Das Tensid, das am wirksamsten bei der Hemmung der Hydratbildung war Polyoxyethylenesorbitan-Tristearat bei hoher Konzentration (d.h. 10 CMC). Die mit diesem Tensid gebildeten Hydrate hatten eine Wachstumsrate, die fast 3x langsamer war als die Hydrate, die mit dem nächstbesten Tensid gebildet wurden (d. h. Sorbitanmonolaurat bei 10 CMC). Wir fanden auch heraus, dass die effizienteste Kristallbildung in Bezug auf die Hydrathemmung der konische Kristall war. Wir fanden auch heraus, dass konische Kristalle am effektivsten für die Hydrathemmung waren. Da ein konischer Kristall nicht über eine bestimmte Größe hinauswachsen kann, wächst das Hydrat langsamer als ein planarer Kristall. Daher waren Tenside, die das Hydrat zwingen, konische Kristalle zu bilden, die effizientesten.

Abbildung 1: Hardwaremontage des Integrierten Modularen Peltier-Geräts (IMPd). (a) Montiertes Temperaturregelungssystem, das die Anordnung von A) dem Netzteil, B) Peltier auf Kühlkörper, C) Temperaturfühler und D) Mikrocontroller anzeigt. (b) Schematische Beschreibung der verschiedenen Komponenten des IMPd-Systems. (c) Schaltplan mit allen Komponenten der Regelschleife und den angezeigten Pinouts. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 2: Hydrat-Visualisierungszelle. (a) Schematische Beschreibung der Hydrat-Visualisierungszelle. (b) Montagehardware und Gerätelayout: A) Stromversorgung, B) Pumpe, C) Spritze, D) Kühlkörper, E) Messing-Visualisierungszelle, F) Kameralinse, G) Messumformer, H) Mikrocontroller, I) Beleuchtung. (c) Messing-Visualisierungszelle mit Abdeckung und Kieselsäure-Desiccant. (d) Klempnerweg von der Spritzenpumpe zum Messumformer und Messinghaken über PTFE-Schläuche und T-Fitting. Nachdruck (angepasst) mit Genehmigung von Dann et al.13. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 3: Keimbildung durch Samenhydrat. (a) Das Samenhydrat wurde mit der Spitze einer Nadel vom Boden der Hydrat-Visualisierungszelle entnommen. (b) Das Samenhydrat wird mit dem Wassertröpfchen in Kontakt gebracht, um den Hydratkristallisationsprozess einzuleiten. Nachdruck (angepasst) mit Genehmigung von Dann et al.13. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 4: Versuchsaufbau für die Tropfenzählung für Oberflächenspannungsmessungen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 5: Beispiel für die Oberflächenanalyse. (a) Rohes Bild des Hydrats auf dem Tropfen. (b) Die Tropfenkontur ist rot, der Hydratbereich schwarz markiert. Die Längenskala wird aus der Messung des bekannten Durchmessers des Messingrohres am unteren Bildrand bestimmt. Nachdruck (angepasst) mit Genehmigung von Dann et al.13. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
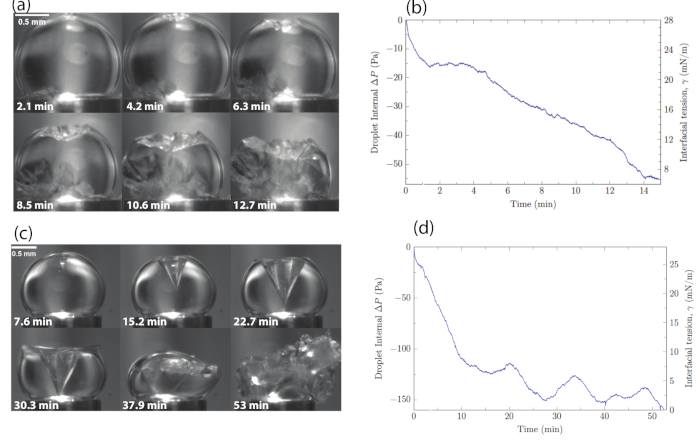
Abbildung 6: Zeitraffer und scheinbare durchschnittliche Grenzflächenspannungsmessungen für die verschiedenen Kristalltypen. (a) Zeitraffer des planaren Wachstums bei geringer Tensidkonzentration. (b) Druckdifferenz innerhalb des Vom Druckaufnehmer gelesenen Tropfens. Die scheinbaren durchschnittlichen Grenzflächenspannungswerte wurden mit der Young-Laplace-Gleichung ausgewertet, wie in Dann et al.13beschrieben. (c) Zeitraffer des konischen Hydratwachstums bei hoher Tensidkonzentration. (d) Die Druckänderung innerhalb des Tröpfchens relativ zu t = 0 und die entsprechenden scheinbaren durchschnittlichen Grenzflächenspannungswerte in Abhängigkeit von der Zeit während des Hydratwachstumsprozesses des konischen Hydrats. Nachdruck (angepasst) mit Genehmigung von Dann et al.13. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
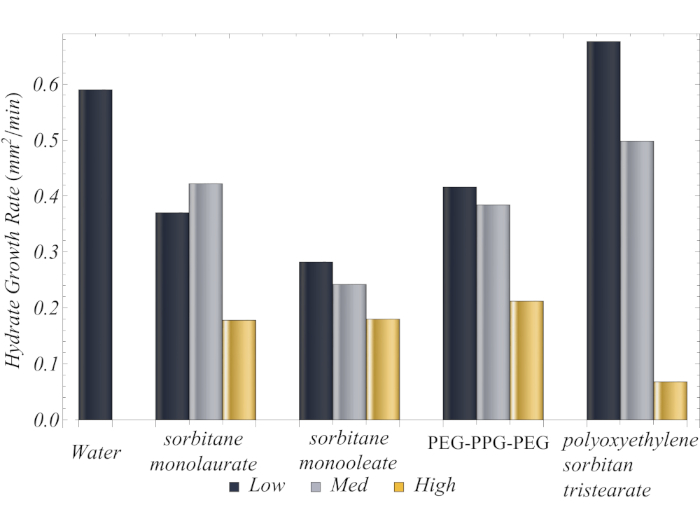
Abbildung 7: Hydratwachstumsrate für alle Tensidlösungen bei niedrigen (0,1 CMC), mittleren (CMC) und hohen (10 CMC) Konzentrationen. Nachdruck (angepasst) mit Genehmigung von Dann et al.13. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Diskussion
In diesem Artikel beschreiben wir eine experimentelle Technik zur Untersuchung der Hydratkristallisation an der Öl-Wasser-Schnittstelle in Gegenwart von nichtionischen Tensiden. Das Gerät besteht aus einem Temperaturregelungssystem und einer Visualisierungszelle, die eine Messingkammer mit Fenstern, CMOS-Kamera und Druckwandler umfasst. Das Temperaturregelungssystem besteht aus einem Mikrocontroller, einer leistungsstarken Peltierplatte, einem 120 mm CPU-Kühler als Kühlkörper und einem wasserdichten digitalen Temperatursensor. Eine Hydrat-Visualisierung Messingzelle wurde mit einer Kamera an einem Fenster befestigt und einem Drucksensor in der Lage, den Druck in einem Tropfen zu messen entwickelt. Die Tenside, die mit dem Gerät getestet wurden, waren Sorbitanmonolaurat, Sorbitanmonooleat, PEG-PPG-PEG und Polyoxyethylenesorbitan-Tristearat, die häufig in der Ölindustrie verwendet werden. Das Gerät ermöglicht die Messung der Wachstumsrate der Hydratkristalle sowie der inneren Druckänderungen innerhalb der Tropfen, während sie hydratkristallisiert werden. Aus den Druckänderungen kann man die scheinbare durchschnittliche Grenzflächenspannung extrahieren, die die Form des Hydratkristalls anzeigen kann.
Diese Methode kombiniert Visualisierungstechniken und interne Druckmessungen, um eine scheinbare durchschnittliche Grenzflächenspannung zu erzeugen. Dies führt zur Kombination der Form des Hydratkristalls mit dem Gedränge des Tensids an der Schnittstelle.
Die entscheidenden Schritte des Protokolls sind: (1) Die Abdeckung auf die Zelle nach dem Füllen mit Cyclopentan (25 ml), (2) Einsetzen eines Wassertröpfchens an den Boden der Zelle mit einer Spritze als Samenhydrat, (3) Senkung der Zelltemperatur auf -5 °C und Sicherstellen, dass sich das Samenhydrat zu Eis dreht, (4) Erhöhung der Temperatur auf 2 °C in 0,5 °C-Schritten, (5) Füllung der Sanitärlösung mit Wasser/Tensidlösung und Senken des Messinghakens in das Cyclopentan, um 5 min zu gleichsetzen, wenn die Temperatur in der Zelle erreicht 2 °C, (6) Start der Kamera- und Druckwandleraufnahmen, (7) Erzeugung des Wasser-/Tensidtröpfs aus dem Messingrohr mit der Spritzenpumpe und (8) Abkratzen einer kleinen Menge des zuvor auf dem Boden der Zelle gebildeten Hydrats und bringt es in kurzen Kontakt mit dem Tröpfchen, das den Hydratbildungsprozess initiiert.
Die vorgestellten Apparate und experimentellen Techniken können verwendet werden, um die Bildung von Kristallen an flüssigen Schnittstellen und die Wirkung von Tensiden auf die Kristallarten und die Hemmung des Kristallisationsprozesses zu untersuchen.
Offenlegungen
Die Autoren haben nichts zu verraten.
Danksagungen
Die Autoren danken der American Chemical Society - Petroleum Research Fund (ACS - PFR), Fördernummer: PRF 57216-UNI9, für die finanzielle Unterstützung.
Materialien
| Name | Company | Catalog Number | Comments |
| 1/16 in. Swagelok 316 stainless steel T-fitting | Swagelok | ||
| 19 gauge PTFE tubing | Scientific Commodities, Inc. | ||
| 19-gauge needle (model: 1001 LTSN SYR) | |||
| 1-Wire DS18B20 - waterproof digital temperature sensor | |||
| Anti fog | RainX | ||
| Arduino Leonardo open-source microcontroller | |||
| Brass tubing 1/16 in. | K&S Precision Metals | ||
| Chemyx Fusion 100 Infusion Pump | Chemyx | ||
| cMOS camera acA640-750um | Basler | ||
| Cyclopentane 98% extra pure | ACROS organics | AC111481000 | |
| Fiber optic goose-neck lamp 150W | AmScope | ||
| Fotodiox macro extension tubes, 35 mm | |||
| Hamilton glass syringe 1 mL | Hamilton | ||
| ImageJ software | |||
| Kipon EOS to C-mount adapter | Kipon | ||
| Lens 28-90 mm | Canon | ||
| Mathematica software | Mathematica | ||
| OMEGA PX409-10WGUSBH pressure transducer | OMEGA | ||
| Peltier plate TEC1-12715 | Amazon | ||
| Pluronic L31 (PEG-PPG-PEG) | Sigma Aldrich | 9003-11-6 | |
| Pylon Viewer v5.0.0.6150 | Basler | ||
| Span 20 (Sorbitan laurate, Sorbitan monolaurate) | Sigma Aldrich | 1338-39-2 | |
| Span 80 (Sorbitan Monooteate) | Sigma Aldrich | 1338-43-8 | |
| Thermaltake NiC C4 120mm CPU cooler | Thermaltake | ||
| Tween 65 (Polyoxyethylenesorbitan Tristearate) | Sigma Aldrich | 9005-71-4 | |
| variable Tooluxe DC power supply |
Referenzen
- Graham, B., et al. Deep water: The Gulf Oil disaster and the future of offshore drilling. Report to the President. , (2011).
- Hammerschmidt, E. Formation of gas hydrates in natural gas transmission lines. Industrial & Engineering Chemistry. 26, 851-855 (1934).
- Sloan, E. D. A changing hydrate paradigm-from apprehension to avoidance to risk management. Fluid Phase Equilibria. 228-229, 67-74 (2005).
- Xiaokai, L., Latifa, N., Abbas, F. Anti-agglomeration in cyclopentane hydrates from bio- and co-surfactants. Energy & Fuels. 24, 4937-4943 (2010).
- Sloan, E. D. Fundamental principles and applications of natural gas hydrates. Nature. 426, 353-363 (2003).
- Sloan, E. D., Koh, C. Clathrate Hydrates of Natural Gases. , CRC Press. Boca Raton, FL. (2007).
- Lee, J. D., Englezos, P. Unusual kinetic inhibitor effects on gas hydrate formation. Chemical Engineering Science. 61, 1368-1376 (2006).
- Daimaru, T., Yamasaki, A., Yanagisawa, Y. Effect of surfactant carbon chain length on hydrate formation kinetics. Journal of Petroleum Science and Engineering. 56, 89-96 (2007).
- Karanjkar, P. U., Lee, J. W., Morris, J. F. Surfactant effects on hydrate crystallization at the water-oil interface: hollow-conical crystals. Crystal Growth & Design. 12, 3817-3824 (2012).
- Leopercio, B. C., de Souza Mendes, P. R., Fuller, G. G. Growth kinetics and mechanics of hydrate films by interfacial rheology. Langmuir. 32, 4203-4209 (2016).
- Karanjkar, P. U., Lee, J. W., Morris, J. F. Calorimetric investigation of cyclopentane hydrate formation in an emulsion. Chemical Engineering Science. 68, 481-491 (2012).
- Mori, Y. H. Harkins-brown correction factor for drop formation. AIChE Journal. 36, 1272-1274 (1990).
- Dann, K., Rosenfeld, L. Surfactant effect on hydrate crystallization at oil-water interface. Langmuir. 34 (21), 6085-6094 (2018).
- Ibach, H. Physics of Surfaces and Interfaces. , Springer Science & Business Media. Berlin, Germany. (2006).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten